Терапевтическое средство против астмы.
Формула / Реферат
1. Применение селенорганических соединений общей формулы (1) и/или (1') или их фармацевтически приемлемых солей
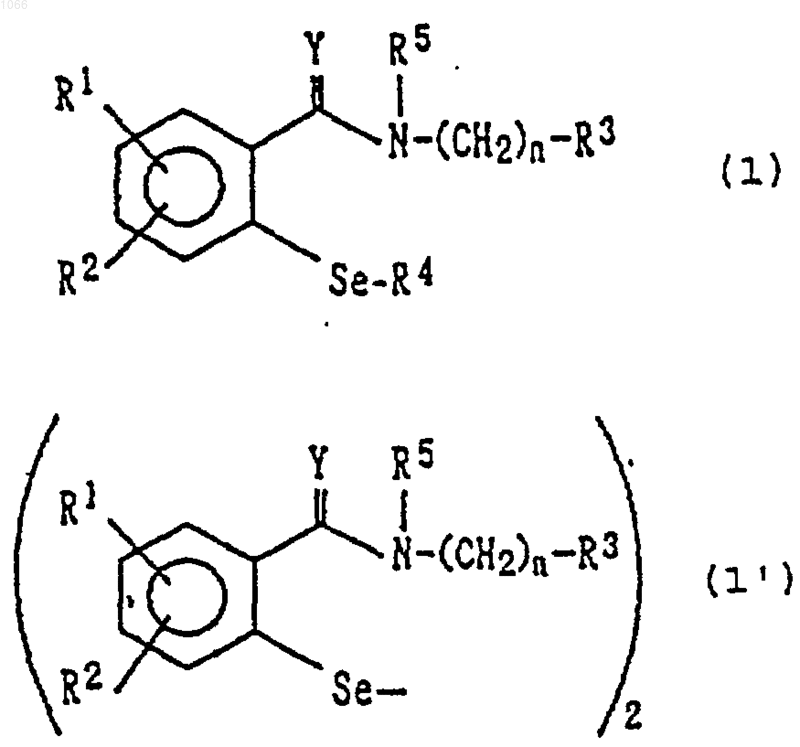
причем в формулах (1) и (1'):
R1 и R2 представляют собой независимо друг от друга атом водорода, атом галогена, группу трифторметила, нитрогруппу, группу C1-C6-алкила или группу C1-C6-алкоксила, причем R1 и R2 могут совместно образовывать поперечные связи с образованием метилендиоксигруппы;
R3 является группой арила, ароматической гетероциклической группой, содержащей 5-7 циклов группой циклоалкила или содержащей 5-7 циклов группой циклоалкенила, причем группа арила, ароматическая гетероциклическая группа, группа циклоалкила и/или группа циклоалкенила может быть замещена;
R4 представляет собой атом водорода, гидроксильную группу, группу S-глютатиона, группу-S-a-аминокислоты или группу аралкила (арилалкила), которая может быть замещена в ее арилостатке.
R5 является атомом водорода или группой C1-C6-алкила, или при этом R4 и R5 могут быть соединены друг с другом с образованием единственной связи;
Y представляет собой атом кислорода или атом серы,
n является целым числом между 0 и 5 включительно,
и атом селена может быть окислен,
в качестве терапевтического средства для лечения астмы.
2. Применение 2-фенил-1,2-бензоизоселеназол-3(2Н)-она или его фармацевтически приемлемой соли в качестве терапевтического средства для лечения астмы.
3. Применение по п.1 для лечения бронхиальной астмы.
4. Применение по п.2 для лечения бронхиальной астмы.
5. Применение по п.1 для подавления поздних астматических реакций.
6. Применение по п.2 для подавления поздних астматических реакций.
Текст
1 Настоящее изобретение относится к терапевтическому средству против астмы, которое эффективно подавляет астматические реакции, в частности поздние астматические реакции при бронхиальной астме. Общеизвестно, что бронхиальная астма считается заболеванием, которое вызывается сокращением мягких мышц в дыхательных путях вследствие анафилаксии типа 1. Однако последние открытия в этой области исследований показали, что часть астматического патогенеза обусловливается тем, что образуется противопоставленное ограничение дыхания, воспаление дыхательных путей, гиперсекреция слизи и новообразования структуры дыхательных путей вследствие хронического воспаления. Поэтому фармакологическая терапия должна соответственно учитывать этот патогенез. Имеющиеся в распоряжении в настоящее время медикаменты против астмы являются снижающими средствами для противопоставленного ограничения дыхания, как, например,бета-агонисты, и контрольными средствами,как, например, стероидные средства для ингаляции, для предотвращения симптомов посредством подавления воспалений дыхательных путей. Бета-агонист действует быстро в отношении сужения бронха и связанных с этим сопроводительных симптомов, как, например, кашель,сдавление грудной клетки и задыхание. Ингалируемый кортикостероид необходимо применять длительно и ежедневно для обеспечения надежного контроля при хронической астме. Однако, бета-агонист имеет некоторые отрицательные побочные действия, как, например,стимуляция сердечных сосудов, сокращение мышц и гипокалиэмия, и раздражения. Кроме того, ингалируемый кортикостероид усиливает кандидиазис (ротоглоточный кандидиазис),дисфонию и случайный кашель за счет раздражения верхних дыхательных путей, так что риск системных эффектов средства для ингаляции меньше риска системных кортикостероидов. Длительное применение орально или парентерально вводимых кортикостероидов может вызвать серьезные побочные действия, как например, остеопороз, высокое давление крови, диабет, заболевания гипофиза, серую катаракту,полноту, мышечную слабость и истончение кожи, которое вызывает кожное заболевание (cutaneous striae) и легкую чувствительность к надавливанию. Контрольные средства принимались длительное время и поэтому необходимо предотвращать или снижать системные побочные эффекты таких средств. Исходя из концепции, что контрольные средства имеют минимальные побочные эффекты за исключением главных, расширяющих бронхи и тормозящих воспаления эффектов,были разработаны антиаллергические средства,как, например, антагонисты рецептора гистамина, антагонисты рецептора лейкотриена, антаго 001066 2 нисты ингибиторов/рецептора синтетазы тромбоксана. Однако нет достаточных данных относительно их клинических преимуществ при продолжительном лечении астмы и поэтому ожидается разработка более эффективных тормозящих воспаление средств и дальнейшие клинические испытания. Считается, что возникающие поздние астматические реакции после возбуждения иммунной системы сопровождаются воспалением дыхательных путей. Наблюдались два вида астматических реакций непосредственно после антигенного раздражения и по прошествии нескольких часов. Более ранняя реакция называется непосредственным астматическим раздражением (IAR), а следующий за ним феномен - поздним астматическим раздражением (LAR). Непосредственное астматическое раздражение объяснялось ограничением дыхательных путей,которое вызывается острым сужением бронх,вызываемым выбросом аллергенов, в то время как позднее астматическое раздражение объяснялось воспалением дыхательных путей. Воспаление дыхательных путей, которое обычно характеризуется экстенсивной инфильтрацией косинофилей, клеток и одноклеточных клеток,вызывает набухание стенок дыхательных путей с легким мышечным сокращением или без него. Такие патологические изменения связываются не только с поздним астматическим изменением, но и с гиперактивностью дыхательных путей и обострением астмы (Метцгер В.Д., Ханнигнейк Г. В. и Ричардсон Х.Б. "Поздние астматические реакции, исследование механизма и значение", Clin. Rev. Allergy 3:145, 1985). Механизм таких патологических явлений еще не исследован полностью. В соответствии с этим является желательным разработка средства для лечения бронхиальной астмы, которое обладает отличной эффективностью аналогично адреналкортекальным гормонам, которое одновременно подавляет как непосредственные астматические реакции, так и поздние астматические реакции и является безопасным. Известно, что 2-фенил-1,2-бензоизоселеназол-3(2 Н)-он, который обычно называют также эбселеном и который представляет собой типичное применяемое в настоящем изобретении соединение, обладающее значительно ингибирующим липоксигеназу действием (Петер Куль и др., Простагландины, 31 (1986), 10291048). Однако никогда не сообщалось, что эбселен эффективен при лечении астмы. В указанных выше условиях изобретатели провели обстоятельные исследования и установили, что соединения, которые характеризуются приведенной ниже формулой (1) и/или (1'), обладают высокой эффективностью в отношении подавления астматических реакций, в частности, относительно поздних астматических реакций при бронхиальной астме. 3 В соответствии с этим, настоящее изобретение предлагает терапевтическое средство для лечения астмы, которое в качестве активнодействующего вещества содержит соединение приведенной ниже формулы (1) и/или (1') или его фармацевтически приемлемую соль.R1-R2 - независимо друг от друга атом водорода, атом галогена, группа трифторметила,нитрогруппа, группа C1-C6-алкила или группаC1-C6-алкоксила, причем R1 и R2 могут совместно образовывать поперечные связи с образованием метилендиоксигруппы.R3 является группой арила, ароматической гетероциклической группой, содержащей 5-7 циклов циклоалкилгруппы или содержащей 5-7 циклов циклоалкенилгруппы, причем группа арила, ароматическая гетероциклическая группа, группа циклоалкила и/или группа циклоалкенила может быть замещена,R4 представляет собой атом водорода, гидроксильную группу, группу S-глютатиона,группу -Sаминокислоты или группу аралкила(арилалкила), которая может быть замещена в ее арилостатке,R5 является атомом водорода или группойC1-C6-алкила, причем R4 и R5 могут быть соединены друг с другом с образованием единственной связи,Y представляет собой атом кислорода или атом серы иn является целым числом между 0 и 5 включительно, причем атом селена может быть окислен. Фиг. 1 показывает активное действие подавляющего эффекта эбселена при астматических реакциях у морских свинок, которые больны индуцированной антигенами астмой. В настоящем изобретении средства для лечения астмы охватывают также такие активные вещества, которые применяются для лечения астмы с ожиданием улучшения астматических условий и для профилактического лечения. Соединения, используемые в качестве активных веществ в средствах для лечения астмы,представлены указанными выше формулами (1) и (1'). Примеры для приведенной для R1 группыC1-C6-алкила содержат группу метила, группу этила, группу пропила, группу изопропила,группу n-бутила, группу изобутила, вторичную группу бутила и группу пентила. Примеры 4 группы C1-C6-алкоксила охватывают группу метоксила, группу этоксила и группу пропоксила. Примеры для приведенной для R3 группы арила охватывают группу фенила; примеры группы циклоалкила охватывают группу циклопентила, группу циклогексила и группу циклогептила; примеры группы циклоалкенила охватывают группу 1-циклопентенила, группу 1 циклогексенила и группу 1-циклогептенила и примеры ароматических гетероциклических групп охватывают 5- или 6-и членные ароматические группы гетероциклов, как например,группу пиридила, группу пиримидила, группу имидазолила, группу оксазолила, группу изоксазолила, группу тиазолила и группу фурила,причем эти группы могут быть замещены. Примеры заменителей охватывают группу C1-C6 алкила, группу C1-C6-алкоксила, галогенную группу, группу карбоксила и группу гидроксила. Число заменителей лежит, предпочтительно, между 1 и 3. В группах R4 группа -Sглютатиона обозначает группу, которая образована путем удаления одного атома водорода из тиолового остатка глютатиона, в то время как группа -Sаминокислоты обозначает группу,которая образована путем удаления одного атома водорода из тиолового остатка, содержащей тиол -аминокислоты. Примеры группы арилалкила (аралкила) содержат группу бензила. R4 и R5 образуют, предпочтительно, единственную связь. Настоящее изобретение содержит, в частности, соединение 2-фенил-1,2-бензоизоселеназол-3(2 Н)-она, которое выражено следующей формулой: Соединения, которые выражаются следующими ниже формулами и которые следует рассматривать как активные метаболиты указанных выше соединений, являются предпочтительными. Кроме того, в настоящем изобретении могут применяться фармацевтически приемлемые соли, которые могут быть получены из перечисленных выше соединений. Описанные выше соединения (1) или (1') уже известны. Они могут быть получены, например, в соответствии со способом, описанным в японских выложенных заявках (kokai)5942373, 57-6756, 59-39894, 60-226868, 61-50963 или в журнале Biochemical Pharmacology, том 6, 20, 3235-3239 и 3241-3245 (1984). Соединения (1) или (1') и их фармацевтически приемлемые соли обладают превосходной эффективностью в отношении подавления непосредственных или поздних астматических реакций при бронхиальной астме, в частности при поздних астматических реакциях, как это доказывается в нижеследующих примерах выполнения. Кроме того, было установлено, что соединения очень безопасны, что доказывается приведенными ниже в таблице 1 величинами LD50,причем эти величины представляют собой результаты теста на токсичность, проведенного на мышах и крысах, которым эти соединения вводили орально или интраперитонеально. Даже в тех случаях, когда эти соединения вводились в высоких дозах, не было выявлено никаких побочных эффектов, которые бы приводили к серьезным проблемам. Животное Мышь Крыса Применение Оральное Интраперитонеальное Оральное Интраперитонеальное Средства, согласно изобретению для лечения астмы могут применяться в различных формах для орального или парентерального применения, как, например, в виде таблеток,капсул, пудры, мелкого гранулята, жидкости,суспензии, эмульсии, сухих сиропов, средств для ингаляции, инъекции и свечей. Такие препараты приготавливаются обычным способом тем, что к соединению (1) или (1') или к его фармацевтически приемлемой соли добавляют смазывающие средства, разрыхляющие средства, связывающие средства или носители. Доза соединения (1), (1') или его фармацевтически приемлемой соли зависит от способа введения, состояния пациента, веса тела пациента и т.п. В случае орального применения доза варьируется, обычно для взрослых между 100 и 2000 мг/день, предпочтительно, 200-1000 мг/день. Как уже указывалось выше, средства согласно изобретению подавляют как непосредственные, так и поздние астматические реакции при бронхиальной астме. В частности, средства оказывают превосходное действие в отношении поздних астматических реакций. Кроме того,средства согласно изобретению имеют малую токсичность и потому безопасны для человека. 6 Настоящее изобретение ниже поясняется подробней на примерах выполнения, причем примеры выполнения не должны ограничивать настоящее изобретение. Пример испытаний. Эффективность эбселена испытывалась на морских свинках, имеющих индуцированную антигеном астму, посредством проверки функций легких в сознательном состоянии и при самопроизвольном дыхании. Способ: 1. Животные. Каждая морская свинка-самка Хартлей(SLC) (возраст 4 недели, вес тела, примерно,250-300 г) предварительно обрабатывалась циклофосмидом (2 мг/кг). После двух дней инъецировали интраперитонеально овальбумин (ОА, 1 мг) и алюминиевый гель (1 г). Спустя три недели снова инъецировали интраперитонеально овальбумин (0,1 мг) и алюминиевый гель (1 г). Обработанные таким образом морские свинки использовались в качестве сенсибилизированных животных. К моменту проведения теста морские свинки имели возраст 11 недель и имели вес тела от 450 до 580 г. 2. Аппараты и инструменты. Прессмограф тела нажимного типа; пульматакограф (TP-601G, Ниппон Коденжа); дифференциальный измерительный преобразователь (Т-601, Ниппон Коденша); трубка измерения сопротивления газового потока (тип Лилли, Ниппон Коденша); осциллоскоп (DS-9121, Ивасаки Цушинки); компьютер (Макинтош Центрис 660 AV,Эппл); программное обеспечение (для анализа дыхание на основе LabView для Макинтош 3.01),распылитель (NE-U10, Татейши Денки). 3. Способ введения средств и индуцирования антигенов. Группа морских свинок, предварительно обработанная дексаметазоном. Дексаметазон (1 мг/кг) растворяли в 100%DMSO (1 мл). Этот раствор в течение следующих четырех дней инъецировали интраперитонеально. Последнюю интраперитонеальную инъекцию проводили за 24 ч перед индуцированием антигенов. Группа морских свинок, предварительно обработанная эбселеном. Эбселен (5 мг/кг) растворяли в 100%DMSO (1 мл). Этот раствор инъецировали интраперитонеально за 30 мин перед индуцированием антигенов. Контрольная группа. Инъецировали 100% DMSO (1 мл) интраперитонеально за 30 мин перед индуцированием антигенов. Способ индуцирования антигенов. 7 Овальбумин ОА (40 мг) растворяли в физиологическом растворе соли (4 мг/л). Этот раствор в течение 2 мин ингалировался с применением ультразвукового распылителя. 4. Способ контроля функций легких. В соответствии со способом Аргаваля (Аргаваль К. П.; удельная проводимость воздушных путей у морских свинок: "Нормальные величины и в случае индуцирования гистамина", Respiratory Physiology 43:23, 1981) каждую морскую свинку фиксировали в прессмографе тела нажимного типа и измеряли процентное изменение удельной проводимости дыхательных путей(sGaw). Поток воздуха через нос и изменение внутреннего давления бокса записывались. Соответствующие волновые формы цифровым способом собирались при 1,024 Гц и точки от конца выдоха до начала вдоха записывались как обратные линии. Из наклона (тангенса) обратных линий определяли удельную проводимость дыхательных путей. Величину удельной проводимости измеряли перед индуцированием антигенов. После ингаляции в течение 2 мин физиологического раствора соли снова измеряли удельную проводимость, чтобы удостовериться,что никакие данные не были изменены. Измеренное в этот момент времени значение принималось за 100% и затем измеряли процентное изменение удельной проводимости дыхательных путей после индуцирования антигенов. Результаты представлены на фиг.1. В группе морских свинок, предварительно обработанных эбселеном, были особенно эффективно подавлены как непосредственные, так и поздние астматические реакции, чем в контрольной группе морских свинок. Если сравнить группу, предварительно обработанную эбселеном, с группой, предварительно обработанной дексаметазоном, то области подавления непосредственных астматических реакций в большинстве случаев равны. Однако,в группе, предварительно обработанной эбселеном, были в значительной степени и полностью подавлены поздние астматические реакции, в то время как в контрольной группе поздние астматические реакции наблюдались в промежутке между 180 и 420 мин. В этой связи следует обратить внимание на то, что доза дексаметазона, равная 1 мг/кг, которая в течение 4 дней вводилась морским свинкам, примерно соответствует дозе дексаметазона для человека (вес тела 60 кг), равной 240 мг(60 мг х 4 дня). Эта доза дексаметазона соответствует 2400 мг преднизолона (0,5 мг дексаметазона эквивалентна 5 мг преднизолона). Это количество преднизолона (2400 мг) соответствует количеству, которое расходуется при импульсной терапии, когда по 1 г/день преднизолона вводят в течение 3 дней. Указанные выше аргументы однозначно доказывают, что эбселен имеет более высокую эффективность по сравнению с лечением, кото 001066 8 рое применяли в прежней клинической ситуации. Пример 1. Таблетки. С помощью известных способов были изготовлены таблетки со следующим составом: Эбселен 50 мг Карбоксиметилцеллюлоза 25 мг Крахмал 5 мг Кристаллическая целлюлоза 40 мг Стеарат магния 2 мг Сумма 122 мг Суммируя, следует установить, что настоящее изобретение описывает безопасное терапевтическое средство для лечения астмы, которое подавляет как непосредственные, так и поздние астматические реакции при бронхиальной астме. Терапевтическое средство согласно изобретению охватывает в качестве активного вещества соединение, которое выражается следующей формулой (1) и/или (1') и/или фармацевтически приемлемую соль этого соединения. Средство, согласно изобретению проявляет высокую эффективность как в отношении непосредственных, так и поздних астматических реакций и, в частности, в отношении поздних астматических реакций. Вследствие незначительной токсичности средство, согласно изобретению может безопасно приниматься человеком. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение селенорганических соединений общей формулы (1) и/или (1') или их фармацевтически приемлемых солейR1 и R2 представляют собой независимо друг от друга атом водорода, атом галогена,группу трифторметила, нитрогруппу, группу C1C6-алкила или группу C1-C6-алкоксила, причемR1 и R2 могут совместно образовывать поперечные связи с образованием метилендиоксигруппы;R3 является группой арила, ароматической гетероциклической группой, содержащей 5-7 циклов группой циклоалкила или содержащей 5-7 циклов группой циклоалкенила, причем группа арила, ароматическая гетероциклическая группа, группа циклоалкила и/или группа циклоалкенила может быть замещена;R4 представляет собой атом водорода, гидроксильную группу, группу S-глютатиона,группу-Sаминокислоты или группу аралкила(арилалкила), которая может быть замещена в ее арилостатке.R5 является атомом водорода или группойC1-C6-алкила, или при этом R4 и R5 могут быть соединены друг с другом с образованием единственной связи;Y представляет собой атом кислорода или атом серы,n является целым числом между 0 и 5 включительно,и атом селена может быть окислен,в качестве терапевтического средства для лечения астмы. 2. Применение 2-фенил-1,2-бензоизоселеназол-3(2 Н)-она или его фармацевтически приемлемой соли в качестве терапевтического средства для лечения астмы. 3. Применение по п.1 для лечения бронхиальной астмы. 4. Применение по п.2 для лечения бронхиальной астмы. 5. Применение по п.1 для подавления поздних астматических реакций. 6. Применение по п.2 для подавления поздних астматических реакций.
МПК / Метки
МПК: A61P 11/06, A61K 31/165
Метки: астмы, против, терапевтическое, средство
Код ссылки
<a href="https://eas.patents.su/6-1066-terapevticheskoe-sredstvo-protiv-astmy.html" rel="bookmark" title="База патентов Евразийского Союза">Терапевтическое средство против астмы.</a>
Предыдущий патент: Порошок вспенивателя и способ его получения
Следующий патент: Офтальмологические растворы, загущенные с помощью полисахаридов семян тамаринда
Случайный патент: Бис-платиновые комплексы с противоопухолевой активностью










