Производные пирролизина, индолизина и хинолизина, их получение и их применение в терапии
Номер патента: 15974
Опубликовано: 30.01.2012
Авторы: Ренон Мария Кармен, Эстенн-Буту Женевьев, Даргазанли Жиад, Медеско Флоранс
Формула / Реферат
1. Соединение в форме чистого энантиомера или эритро- или треодиастереоизомера или смеси таких изомеров, отвечающее общей формуле (I)
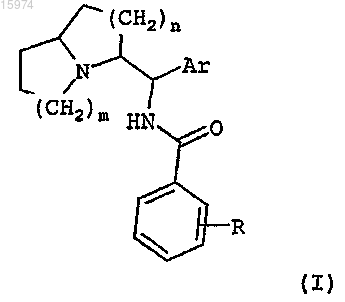
в которой
m и n означают, каждый независимо друг от друга, число 1 или 2;
Ar означает группу, выбираемую из фенила, нафтила-1, нафтила-2, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, фуран-2-ила, фуран-3-ила, тиен-2-ила, тиен-3-ила, тиазол-2-ила и оксазол-2-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями, выбираемыми из атомов галогенов и (C1-C6)алкила, (C3-C7)циклоалкила, (C3-C7)циклоалкил-(C1-C6)-алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы;
R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга, заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов, разветвленных или циклических (C3-C7)алкилов, (C3-C7)-циклоалкил-(C1-C6)-алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, цианогруппы, аминогруппы, фенила, ацетила, бензоила, (C1-C6)алкилсульфонила, карбоксила, (C1-C6)алкоксикарбонила и пентафторсульфанила;
в виде основания, аддитивной соли кислоты и/или сольвата или гидрата.
2. Соединение по п. 1, отличающееся тем, что Ar означает группу, выбираемую из фенила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, тиен-2-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими, одинаковыми или отличными друг от друга, заместителями, выбираемыми из атомов галогенов и (C1-C6)алкилов, (C3-C7)циклоалкилов, (C3-C7)циклоалкил-(C1-C6)алкилов, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)-циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата.
3. Соединение по п.1 или 2, отличающееся тем, что Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими, одинаковыми или отличными друг от друга, заместителями, выбираемыми из атомов галогенов; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата.
4. Соединение по любому из пп.1-3, отличающееся тем, что R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга, заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов и пентафторсульфанила; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата.
5. Соединение по любому из пп.1-4, отличающееся тем, что
m и n означают, каждый независимо друг от друга, число 1 или 2;
Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими атомами галогенов;
R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга заместителей, выбираемых из атома хлора и метила, трифторметила, трифторметоксигруппы и пентафторсульфанила;
в виде основания, аддитивной соли кислоты и/или сольвата или гидрата.
6. Соединение по п.1, отличающееся тем, что его выбирают из следующих соединений:
гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид цис-эритро-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид 2-хлор-N-[(S)-(3R,8aR)(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид 2-хлор-N-[(S)-(3R,8aR)(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2,6-дихлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-хлор-3-метил-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1;
гидрохлорид транс-трео-2-хлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-эритро-2-хлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1;
гидрохлорид транс-трео-2-метил-3-метокси-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1;
гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметоксибензамида 1:1;
гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-(пентафторсульфанил)бензамида 1:1;
гидрохлорид 2-хлор-N-[(гексагидропирролизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1.
7. Способ получения соединения по п.1, отличающийся тем, что нитрил общей формулы (II)
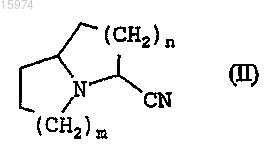
в которой m и n имеют указанные в п.1 значения, вводят во взаимодействие с литийсодержащим производным общей формулы Ar-Li, в которой Ar имеет значение, раскрытое в п.1, в простом эфире в качестве растворителя при температуре от -90 до -30°C, получая промежуточный имин общей формулы (IV)
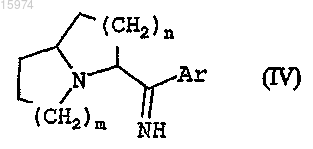
который восстанавливают до первичного амина общей формулы (V)
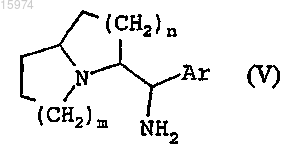
с помощью восстановителя в протонном растворителе при температуре от 0°C до комнатной температуры, затем осуществляют амидное связывание между диамином общей формулы (V) и активированной кислотой или хлорангидридом кислоты общей формулы (VI)
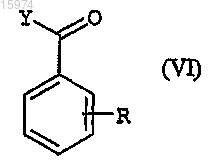
в которой Y означает активированную группу OH или атом хлора и R имеет указанное в п.1 значение.
8. Соединение общей формулы (V)
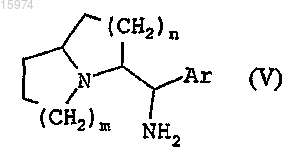
отличающееся тем, что m, n и Ar имеют значения, указанные по любому из пп.1-5.
9. Соединение по п.8, отличающееся тем, что его выбирают из следующих соединений:
транс-трео/эритро-1-(октагидроиндолизин-5-ил)-1-фенилметанамин;
транс-трео-1-(октагидроиндолизин-3-ил)-1-фенилметанамин;
цис-эритро-1-(октагидроиндолизин-3-ил)-1-фенилметанамин;
транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-фенилметанамин;
транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-(4-фторфенил)метанамин;
транс-трео-1-(октагидро-2H-хинолизин-4-ил)-1-пиридин-3-илметанамин;
транс-трео/цис-эритро-1-(октагидро-2H-хинолизин-4-ил)-1-тиен-3-илметанамин.
10. Фармацевтическая композиция, отличающаяся тем, что она содержит соединение по п.1 в комбинации с эксципиентом.
11. Применение соединения по п.1 для получения лекарственного средства - ингибитора переносчиков глицина glytl.
12. Применение соединения по п.1 для получения лекарственного средства для лечения поведенческих нарушений, ассоциированных с деменцией, психозов и острых или хронических экстрапирамидальных симптомов, провоцируемых нейролептическими средствами, для лечения различных форм беспокойства, приступов паники, фобий, компульсивных навязчивых расстройств, для лечения различных форм депрессии, включая психотическую депрессию, для лечения нарушений, возникающих вследствие злоупотребления или прекращения приема алкоголя, нарушений сексуального поведения, нарушений в отношении приема пищи, для лечения мигрени и для лечения генерализованных, первичных и вторичных, частичных с простой или комплексной симптоматологией, эпилепсии, смешанных форм и других эпилептических синдромов, в виде дополнения другого антиэпилептического лечения или в виде монотерапии.
13. Применение по п.12 для получения лекарственного средства для лечения шизофрении (дефицитная форма и продуктивная форма).
Текст
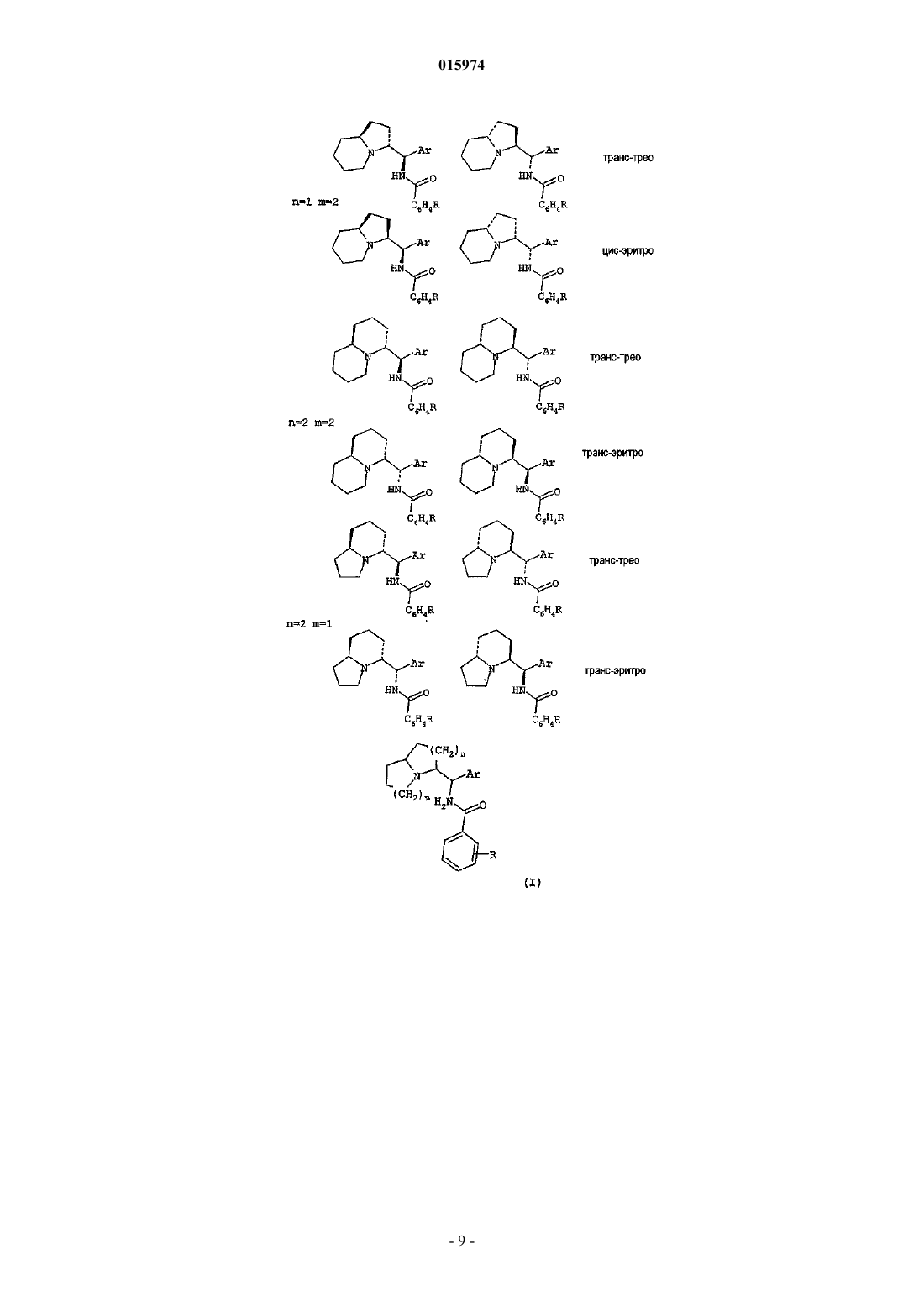
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента Описывается соединение, отвечающее общей формуле, в которой m и n означают, каждый,число 1 или 2; Ar означает группу, выбираемую из фенила, нафтила-1, нафтила-2, пиридин-2 ила, пиридин-3-ила, пиридин-4-ила, фуран-2-ила, фуран-3-ила, тиен-2-ила, тиен-3-ила, тиазол-2 ила и оксазол-2-ила, причем эта группа Ar может быть, в случае необходимости, замещена; R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга,заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов, разветвленных или циклических Даргазанли Жиад, Эстенн-Буту Женевьев, Медеско Флоранс, Ренон Мария Кармен (FR) Медведев В.Н. (RU) 015974 Объектом настоящего изобретения являются производные пирролизина, индолизина и хинолизина,их получение и их применение в терапии. Соединения согласно изобретению отвечают общей формуле (I)m и n означают, каждый, независимо друг от друга, число 1 или 2 ;Ar означает группу, выбираемую из фенила, нафтила-1, нафтила-2, пиридин-2-ила, пиридин-3-ила,пиридин-4-ила, фуран-2-ила, фуран-3-ила, тиен-2-ила, тиен-3-ила, тиазол-2-ила и оксазол-2-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями,выбираемыми из атомов галогенов и (C1-C6)алкила, (C3-C7)циклоалкила, (C3-C7)циклоалкил-(C1C6)алкила,(C1-C6)алкоксила,(C3-C7)циклоалкилоксигруппы,(C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы;R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга,заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов, разветвленных или циклических (C3-C7)алкилов, (C3-C7)циклоалкил-(C1-C6)алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, цианогруппы, аминогруппы, фенила,ацетила, бензоила, (C1-C6)алкилсульфонила, карбоксила, (C1-C6)алкоксикарбонила и пентафторсульфанила. Соединения общей формулы (I) обладают тремя асимметрическими центрами; они могут находиться в форме энантиомеров или трео- или эритродиастереоизомеров со стереохимией заместителя бицикла цис или транс или в виде смеси таких изомеров. Они также могут находиться в виде свободных оснований, аддитивных солей кислот и/или сольватов или гидратов, а именно, в форме ассоциаций или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты и сольваты также составляют часть изобретения. Среди соединений согласно изобретению первую группу соединений образуют соединения, в которых:Ar означает группу, выбираемую из фенила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, тиен-2 ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями, выбираемыми из атомов галогенов и (C1-C6)алкилов, (C3-C7)циклоалкилов,(C3-C7)циклоалкил-(C1-C6)алкилов,(C1-C6)алкоксила,(C3-C7)циклоалкилоксигруппы,(C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы; причем m, n и R имеют вышеуказанные значения. Среди соединений согласно изобретению вторую группу соединений образуют соединения, в которых:Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими, одинаковыми или отличными друг от друга, заместителями, выбираемыми из атомов галогенов, причем m, n и R имеют вышеуказанные значения. Среди соединений согласно изобретению третью группу соединений образуют соединения, в которых:R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга,заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно-или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов и пентафторсульфанила, причем m, n и R имеют вышеуказанное значение. Среди соединений согласно изобретению четвертую группу соединений образуют соединения, в которых:m и n означают, каждый, независимо друг от друга, число 1 или 2,Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими атомами галогенов;R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга-1 015974 заместителей, выбираемых из атома хлора и метила, трифторметила, трифторметоксигруппы и пентафторсульфанила. Среди соединений согласно изобретению, пятую группу соединений образуют следующие соединения: гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид цис-эритро-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3R,8aR)-(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3R,8aR)-(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(4-фторфенил)-(октагидрохинолизин-4-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)(пиридин-3-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-3-метил-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(4-фторфенил)-(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(4-фторфенил)-(октагидрохинолизин-4-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-3-метокси-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1; гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметоксибензамида 1:1; гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-(пентафторсульфанил)бен-2 015974 замида 1:1; гидрохлорид 2-хлор-N-[(гексагидропирролизин-3-ил)фенилметил]бензамида 1:1. Соединения общей формулы (I) могут быть получены способом, проиллюстрированным нижеследующей схемой 1. Схема 1 Нитрил общей формулы (II), в которой m и n имеют вышеуказанные значения, вводят во взаимодействие с литийсодержащим производным общей формулы (III), в которой Ar имеет вышеуказанное значение, в простом эфире в качестве растворителя, таком, как диэтиловый эфир или тетрагидрофуран,при температуре от -90C до -30C; получают промежуточный имин общей формулы (IV), который восстанавливают до первичного амина общей формулы (V) с помощью восстановителя, такого, как боргидрид натрия, в протонном растворителе, таком, как метанол, при температуре от 0C до комнатной температуры. Затем осуществляют амидное связывание между диамином общей формулы (V) и активированной кислотой или хлорангидридом кислоты общей формулы (VI), в которой Y означает активированную группу OH или атом хлора и R имеет вышеуказанное значение, используя известные специалисту в данной области способы, с получением амида общей формулы (I). Соединения общей формулы (II) с n = 1 и m = 2 обладают относящейся к цис- и транс- стереохимией и они приводят, соответственно, к соединениям общей формулы (I) со стереохимией цис-эритро и транс-трео. Соединения общей формулы (II) с n = 2 и m = 1 или n и m = 2 обладают относящейся к транс стереохимией и они приводят к соединениям общей формулы (I) со стереохимией транс-эритро и транстрео. Наконец, соединение общей формулы (II) с n и m = 1 обладает относящейся к транс- и цис- стереохимией и оно приводит к соединениям общей формулы (I) в виде смеси изомеров, разделяемых с помощью жидкостной хроматографии. Кроме того, хиральные соединения общей формулы (I) могут быть получены путем разделения рацемических смесей с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) при использовании колонки с хиральной фазой или путем расщепления рацемического амина общей формулы (V) при использовании хиральной кислоты, такой как винная кислота, камфорсульфокислота, дибензоилвинная кислота, N-ацетиллейцин, путем фракционной и предпочтительной перекристаллизации диастереоизомерной соли из растворителя спиртового типа, или еще путем энантиоселективного синтеза, используя хиральный нитрил общей формулы (II). Нитрилы общей формулы (II) описываются в Synlett, 619-522(1995), когда n и m означают 1, со стереохимией цис и транс; в J.O.C., 55, 4688-4693 (1990) и J.O.C., 56,4868-4874 (1991), когда n означает 2 и m означает 1, со стереохимией транс; в Org. Letters, 2, 2085-2088(2000), когда n означает 1 и m означает 2, со стереохимией транс и цис, и, наконец, они могут быть получены согласно способам, аналогичным таковым, описанным выше, когда n и m означают 2, со стереохимией транс, в виде рацемической или хиральной серии. Литийсодержащие производные общей формулы(III) являются коммерчески доступными или они могут быть получены способами, известными специалисту в данной области и аналогичными таковым, описанным в J.O.C., 62, 5484-5496 (1997), и Tetrahedron Letters, 35, 3673-3674 (1994). Некоторые кислоты и хлорангидриды кислот общей формулы (VI) являются коммерчески доступными или могут быть получены способами, аналогичными таковым, описанным в Европейском патенте 0556672, патенте США 3801636 и в J. Chem. Soc, 25 (1927), Chem. Pharm. Bull., 1789-1792 (1992), Aust. J.Chem., 1938-1950 (1984), и J.O.C., 527 (1980). Объектом изобретения согласно другому из его аспектов являются также соединения общей формулы (V)m и n означают, каждый, независимо друг от друга, число 1 или 2;Ar означает группу, выбираемую из фенила, нафтила-1, нафтила-2, пиридин-2-ила, пиридин-3-ила,пиридин-4-ила, фуран-2-ила, фуран-3-ила, тиен-2-ила, тиен-3-ила, тиазол-2-ила и оксазол-2-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями,выбираемыми из атомов галогенов и (C1-C6)алкила, (C3-C7)циклоалкила, (C3-C7)циклоалкил-(C1C6)алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил-(C1-C6)алкилоксигруппы,(C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моноили полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы. Эти соединения пригодны в качестве промежуточных продуктов синтеза соединений формулы (I). Среди соединений общей формулы (V), объекта изобретения, первую группу соединений образуют соединения, в которыхm и n означают, каждый, независимо друг от друга, число 1 или 2;Ar означает группу, выбираемую из фенила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, тиен-2 ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями, выбираемыми из атомов галогенов и (C1-C6)алкилов, (C3-C7)циклоалкилов,(C3-C7)циклоалкил-(C1-C6)алкилов,(C1-C6)алкоксила,(C3-C7)циклоалкилоксигруппы,(C3-C7)циклоалкил-(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1C6)алкилоксигруппы. Среди соединений общей формулы (V) объекта изобретения вторую группу соединений образуют соединения, в которыхAr означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями, выбираемыми из атомов галогенов, причем m и n имеют вышеуказанные значения. Среди соединений общей формулы (V), объекта изобретения, третью группу соединений образуют соединения, в которыхm и n означают, каждый, независимо друг от друга, число 1 или 2;Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими атомами галогенов. Из соединений общей формулы (V) можно, в частности, назвать следующие соединения: транс-трео/эритро-1-(октагидроиндолизин-5-ил)-1-фенилметанамин; транс-трео-1-(октагидроиндолизин-3-ил)-1-фенилметанамин; цис-эритро-1-(октагидроиндолизин-3-ил)-1-фенилметанамин; транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-фенилметанамин; транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-(4-фторфенил)метанамин; транс-трео-1-(октагидро-2H-хинолизин-4-ил)-1-пиридин-3-илметанамин; транс-трео/цис-эритро-1-(октагидро-2H-хинолизин-4-ил)-1-тиен-3-илметанамин. Нижеследующие примеры иллюстрируют получение нескольких соединений согласно изобретению. Элементные микроанализы, ИК- и ЯМР-спектры и ВЭЖХ при использовании колонки с хиральной фазой подтверждают структуры и энантиомерную чистоту полученных соединений. Номера, указанные между скобками в заголовках примеров, соответствуют таковым первой колонки нижеприводимой таблицы. Пример 1 (соединения 1 и 2). Гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1 и гидрохлорид транс-эритро-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3 трифторметилбензамида 1:1. 1.1. транс-трео/эритро-1-(Октагидроиндолизин-5-ил)-1-фенилметанамин. В колбу емкостью 50 мл, снабженную магнитной мешалкой, вводят, в атмосфере аргона, 0,62 г (4 ммоль) бромбензола в виде раствора в 5 мл безводного тетрагидрофурана, затем среду охлаждают до температуры -75C. Добавляют 1,6 мл (4 ммоль) 2,5 М раствора бутиллития в тетрагидрофуране и смесь выдерживают при перемешивании в течение 40 мин. При температуре -75C, добавляют 0,3 г (2 ммоль) транс-октагидроиндолизин-5-карбонитрила в виде раствора в 5 мл тетрагидрофурана и смесь оставляют возвращаться к комнатной температуре в течение 3 ч. Добавляют воду и этилацетат, водную фазу отделяют и экстрагируют этилцетатом. Объединенные органические фазы сушат над сульфатом натрия, отфильтровывают и концентрируют при пониженном давлении, получая имин, вносят его в колбу емкостью 50 мл при использовании 10 мл метанола. Смесь охлаждают до температуры -5C и медленно добавляют 0,38 г (10 ммоль) боргидрида натрия. Продолжают перемешивание при возврате температуры смеси к комнатной температуре в течение 12 ч. Смесь концентрируют при пониженном давлении и ее обрабатывают водой и этилацетатом. Фазы разделяют и водную фазу экстрагируют этилацетатом. После промывки объединенных органических фаз, высушивания над сульфатом натрия, фильтрации и выпари-4 015974 вания получают 0,5 г продукта в виде масла желтого цвета, которое используют таким, какое есть, на следующей стадии. 1.2. Гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3 трифторметилбензамида 1:1 и гидрохлорид транс-эритро-2-хлор-N-[(октагидроиндолизин-5 ил)фенилметил]-3-трифторметилбензамида 1:1. В колбу емкостью 50 мл вводят последовательно, в 10 мл дихлорметана, 0,5 г (2,17 ммоль) 1(октагидроиндолизин-5-ил)-1-фенилметанамина, 0,36 мл (2,6 ммоль) триэтиламина, 0,63 г (2,6 ммоль) хлорангидрида 2-хлор-3-трифторметилбензойной кислоты и смесь перемешивают при комнатной температуре в течение 1 ч. Смесь обрабатывают водой, экстрагируют несколько раз дихлорметаном. После промывки органических фаз водой, затем 1 н водным раствором гидроксида натрия, высушивания над сульфатом магния, фильтрации и выпаривания растворителя при пониженном давлении, остаток очищают хроматографией на колонке с силикагелем, элюируя смесью дихлорметана и метанола. Получают в виде бесцветного масла 0,06 г и 0,130 г продуктов, соответствующих транс-трео- и транс-эритроизомерам. Эти продукты затем превращают в гидрохлориды, используя 0,1 н раствор хлороводорода в пропан-2-оле. В конечном счете выделяют 0,039 г соответствующего транс-трео-изомера: температура плавления: 132-134C; 1(4,12 ммоль) транс-октагидроиндолизин-3-карбонитрила в виде раствора в 25 мл безводного тетрагидрофурана. Среду охлаждают до температуры -75C, добавляют 6,22 мл (12,24 ммоль) 2 М раствора фениллития в дибутиловом эфире и перемешивают при возврате температуры к комнатной в течение 5 ч. Добавляют 3 мл метанола, затем добавляют воду и этилацетат, водную фазу отделяют и экстрагируют ее этилацетатом. Объединенные органические фазы сушат над сульфатом натрия, фильтруют, концентрируют при пониженном давлении, получая имин, вносят его в колбу емкостью 50 мл при использовании 25 мл метанола. Смесь охлаждают до температуры -5C и медленно добавляют 0,78 г (20,6 ммоль) боргидрида натрия. Продолжают перемешивание при возврате температуры смеси к комнатной температуре в течение 12 ч. Смесь концентрируют при пониженном давлении и ее обрабатывают водой и этилацетатом, фазы разделяют и водную фазу экстрагируют этилацетатом. После промывки объединенных органических фаз, высушивания над сульфатом натрия, фильтрации и выпаривания получают 0,8 г продукта в виде масла желтого цвета, которое используют таким, какое есть, на следующей стадии. 2.2. Гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1. В колбу емкостью 50 мл вводят последовательно, в 15 мл дихлорметана, 0,4 г (1,77 ммоль) транстрео-1-(октагидроиндолизин-3-ил)-1-фенилметанамина, 0,3 мл (2,1 ммоль) триэтиламина, 0,57 г (2,35 ммоль) хлорангидрида 2-хлор-3-трифторметилбензойной кислоты и смесь перемешивают при комнатной температуре в течение 12 ч. Смесь обрабатывают водой, экстрагируют несколько раз дихлорметаном. После промывки органических фаз водой, затем 1 н водным раствором гидроксида натрия, высушивания над сульфатом магния, фильтрации и выпаривания растворителя при пониженном давлении, остаток очищают хроматографией на колонке с силикагелем, элюируя смесью дихлорметана и метанола. Получают в виде бесцветного масла 0,35 г продукта, соответствующего транс-треоизомеру. Его затем превращают в гидрохлорид, используя 0,1 н раствор хлороводорода в пропан-2-оле. В конечном счете выделяют 0,28 г продукта в виде твердого вещества белого цвета. Температура плавления: 138-139C. 1-5 015974 3.1. Цис-эритро-1-(октагидроиндолизин-3-ил)-1-фенилметанамин. Согласно методике, описанной в примере 1.1, из 0,61 г (4 ммоль) цис-октагидроиндолизин-3 карбонитрила получают 0,9 г продукта в виде масла желтого цвета, которое используют таким, какое есть, на следующей стадии. 1H-ЯМР (200 МГц, CDCl3)(м.д.): 1,00-2,00 (м, 12H), 2,35-2,50 (м, 1H), 3,00-3,15 (м, 1H), 4,15 (д,1H), 7,1-7,4 (м, 5H). 3.2. Гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1. Согласно методике, описанной в примере 2.2, из 0,47 г (2 ммоль) цис-эритро-1(октагидроиндолизин-3-ил)-1-фенилметанамина и 0,58 г (2,4 ммоль) хлорангидрида 2-хлор-3 трифторметилбензойной кислоты получают 0,44 г продукта в виде бесцветного масла, соответствующего цис-эритроизомеру. Этот продукт затем превращают в гидрохлорид, используя 0,1 н раствор хлороводорода в пропан-2 оле. В конечном счете выделяют 0,28 г продукта в виде твердого вещества белого цвета. Температура плавления: 138-139C. 1(1,77 ммоль) транс-октагидрохинолизин-4-карбонитрила в виде раствора в 10 мл безводного тетрагидрофурана. Среду охлаждают до температуры -75C, добавляют 2 мл (4 ммоль) 2 М раствора фениллития в смеси циклогексана и диэтилового эфира (70/30) и перемешивают при повышении температуры до -50C в течение 3 ч. Добавляют 1 мл метанола, затем при температуре 25C добавляют воду и этилацетат, водную фазу отделяют и экстрагируют ее этилацетатом. Объединенные органические фазы сушат над сульфатом натрия, фильтруют, концентрируют при пониженном давлении, получая имин, и вносят его в колбу емкостью 50 мл при использовании 10 мл метанола. Смесь охлаждают до температуры -5C и медленно добавляют 0,33 г (8,85 ммоль) боргидрида натрия. Продолжают перемешивание при возврате температуры смеси к комнатной температуре в течение 12 ч. Смесь концентрируют при пониженном давлении и обрабатывают ее водой и этилацетатом. Фазы разделяют и водную фазу экстрагируют этилацетатом. После промывки объединенных органических фаз, высушивания над сульфатом натрия, фильтрации и выпаривания получают 0,18 г продукта в виде масла желтого цвета, которое используют таким, какое есть, на следующей стадии. 4.2. Гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1 и гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3 трифторметилбензамида 1:1. В колбу емкостью 50 мл вводят последовательно, в 10 мл дихлорметана, 0,18 г (0,74 ммоль) транстрео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-фенилметанамина, 0,20 г (0,89 ммоль) 2-хлор-3 трифторметилбензойной кислоты, 0,17 г (0,9 ммоль) гидрохлорида 1-(3-диметиламинопропил)-3 этилкарбодиимида (EDCI) и 0,045 г (0,37 ммоль) диметиламинопиридина и смесь перемешивают при комнатной температуре в течение 12 ч. Смесь обрабатывают водой, экстрагируют несколько раз дихлорметаном. После промывки органических фаз водой, затем 1 н водным раствором гидроксида натрия, высушивания над сульфатом магния, фильтрации и выпаривания растворителя при пониженном давлении,остаток очищают хроматографией на колонке с силикагелем, элюируя смесью дихлорметана и метанола. Получают в виде бесцветного масла 0,13 г соединения, соответствующего транс-треоизомеру, и 0,024 г соединения, соответствующего транс-эритроизомеру. Их затем превращают в гидрохлориды, используя 0,1 н раствор хлороводорода в пропан-2-оле. В конечном счете выделяют 0,13 г транс-треоизомера в виде твердого вещества белого цвета: температура плавления: 161-163C. 1H-ЯМР (200 МГц, C5D5N)(м.д.): 1,20-2,0 (м, 10H), 2,15-2,35 (м, 2H), 3,2 (т, 1H), 3,65-3,8 (м, 1H),3,85-4,0 (м, 2H), 6,30 (д, 1H), 7,3-7,6 (м, 6H), 7,8 (д, 2H) и 0,014 г транс-эритроизомера в виде твердого вещества белого цвета. температура плавления: 245-247C. 1(7,61 ммоль) 1-бром-4-фторбензола в виде раствора в 10 мл безводного диэтилового эфира, затем среду охлаждают до температуры -75C. После этого добавляют 3,35 мл (8,37 ммоль) 2,5 М раствора бутиллития в гексане и перемешивают при повышении температуры смеси до -40C в течение 90 мин. Затем добавляют, при температуре -75C, 0,5 г (3 ммоль) транс-октагидрохинолизин-4-карбонитрила в виде раствора в 10 мл диэтилового эфира и выдерживают при этой температуре в течение 90 мин. Выдерживают до повышения температуры до 0C и добавляют 2 мл метанола, затем, при температуре 25C, добавляют воду и этилацетат, водную фазу отделяют и экстрагируют ее этилацетатом. Объединенные органические фазы сушат над сульфатом натрия, фильтруют, концентрируют при пониженном давлении, получая имин, и вносят его в колбу емкостью 50 мл при использовании 20 мл метанола. Смесь охлаждают до температуры -5C и медленно добавляют 0,57 г (15,2 ммоль) боргидрида натрия. Продолжают перемешивание при возврате температуры смеси к комнатной температуре в течение 12 ч. Смесь концентрируют при пониженном давлении и обрабатывают ее водой и этилацетатом. Фазы разделяют и водную фазу экстрагируют этилацетатом. После промывки объединенных органических фаз, высушивания над сульфатом натрия, фильтрации и выпаривания получают 0,97 г продукта в виде масла желтого цвета, которое используют таким, какое есть, на следующей стадии. 5.2. Гидрохлорид транс-трео-2-хлор-N-[(4-фторфенил)-(октагидрохинолизин-4-ил)метил]-3 трифторметилбензамида 1:1 и гидрохлорид транс-эритро-2-хлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1. В колбу емкостью 50 мл вводят последовательно, в 10 мл дихлорметана, 0,4 г (1,52 ммоль) транстрео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-(4-фторфенил)метанамина, 0, 23 мл (1,8 ммоль) триэтиламина, 0,4 г (1,67 ммоль) хлорангидрида 2-хлор-3-трифторметилбензойной кислоты и смесь перемешивают при комнатной температуре в течение 12 ч. Смесь обрабатывают водой, экстрагируют несколько раз дихлорметаном. После промывки органических фаз водой, затем 1 н водным раствором гидроксида натрия, высушивания над сульфатом магния,фильтрации и выпаривания растворителя при пониженном давлении, остаток очищают хроматографией на колонке с силикагелем, элюируя смесью дихлорметана и метанола. Получают в виде бесцветного масла 0,11 г соединения, соответствующего транс-треоизомеру, и 0,15 г соединения, соответствующего транс-эритроизомеру. Эти продукты затем превращают в гидрохлориды, используя 0,1 н раствор хлороводорода в пропан 2-оле. В конечном счете выделяют 0,082 г транс-треоизомера в виде твердого вещества белого цвета: температура плавления: 176-178C. 1(т, 1H), 7,15 (т, 2H), 7,35 (т, 2H), 7,5 (т, 1H), 7,8 (д, 1H), 8,05 (д, 1H), 8,75 (д, 1H, NH). И 0,095 г транс-эритроизомера в виде твердого вещества белого цвета: температура плавления: 188-189C. 1H-ЯМР (200 МГц, CDCl3)(м.д.): 1,1-2,6 (м, 12H), 2,7-3,2 (м, 3H), 3,95 (д, 1H), 5,80 (т, 1H), 7,15 (т,2H), 7,35 (т, 2H), 7,5 (т, 1H), 7,8 (д, 1H), 7,95 (д, 1H), 9,3 (д, 1H, NH). Пример 6 (соединение 20). Гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)пиридин-3-илметил]-3-трифторметилбензамида 1:1. 6.1. транс-трео-1-(октагидро-2H-хинолизин-4-ил)-1-пиридин-3-илметанамин. Согласно методике, описанной в примере 5.1, из 0,8 г (5,32 ммоль) 3-бромпиридина и 0,35 г (2,13 ммоль) транс-октагидрохинолизин-4-карбонитрила получают 0,57 г продукта в виде масла коричневого цвета, которое используют таким, какое есть, на следующей стадии. 6.2. Гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)пиридин-3-илметил]-3 трифторметилбензамида 1:1. Согласно методике, описанной в примере 5.2, из 0,57 г (2,32 ммоль) транс-трео-1-(октагидро-2Hхинолизин-4-ил)-1-пиридин-3-илметанамина и 0,62 г (2,55 ммоль) хлорангидрида 2-хлор-3 трифторметилбензойной кислоты получают 0,21 г соединения, соответствующего транс-треоизомеру. Этот продукт затем превращают в гидрохлорид, используя 0,1 н раствор хлороводорода в пропан-2 оле. В конечном счете выделяют 0,042 г транс-треоизомера в виде твердого вещества белого цвета: температура плавления: 236-238C. 1H-ЯМР (200 МГц, CDCl3)(м.д.): 1,3-2,4 (м, 12H), 2,6-2,9 (м, 1H), 3,2 (т, 1H), 3,65-3,90 (м, 2H),-7 015974 5,75 (т, 1H), 7,3-7,55 (м, 2H), 7,8 (т, 2H), 8,05 (д, 1H), 8,65 (д, 1H), 8,8 (с, 1H), 9,1 (д, 1H, NH). Пример 7 (соединения 10 и 12). Гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)тиен-3-илметил]-3-трифторметилбензамида 1:1 и гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)тиен-3-илметил]-3 трифторметилбензамида 1:1. 7.1. Транс-трео/цис-эритро-1-(октагидро-2H-индолизин-3-ил)-1-тиен-3-илметанамин. Согласно методике, описанной в примере 5.1, из 1,1 г (6,9 ммоль) 3-бромтиофена и 0,41 г (2,76 ммоль) хиральной смеси транс/цис-октагидроиндолизин-5-карбонитрила получают 0,51 г продукта в виде масла коричневого цвета, которое используют таким, какое есть, на следующей стадии. 7.2. Гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)тиен-3-илметил]-3 трифторметилбензамида 1:1 и гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)тиен-3 илметил]-3-трифторметилбензамида 1:1. Согласно методике, описанной в примере 5.2, из 0,51 г (2,15 ммоль) транс-трео/цис-эритро-1(октагидро-2H-индолизин-3-ил)-1-тиен-3-илметанамина и 0,57 г (2,37 ммоль) хлорангидрида 2-хлор-3 трифторметилбензойной кислоты получают 0,25 г соединения, соответствующего транс-треоизомеру, и 0,14 г соединения, соответствующего цис-эритроизомеру. Эти продукты затем превращают в гидрохлориды, используя 0,1 н раствор хлороводорода в пропан 2-оле. В конечном счете выделяют 0,22 г транс-треоизомера в виде твердого вещества белого цвета (стереохимия RSS): температура плавления: 159-161C;(т, 1H), 7,1 (д, 1H), 7,2-7,35 (м, 2H), 7,5 (т, 1H), 7,8 (т, 2H) и 0,16 г цис-эритроизомера в виде твердого вещества белого цвета (стереохимия RRS): температура плавления: 170-172C;(т, 1H), 7,1 (д, 1H), 7,2 (с, 1H), 7,35 (д, 2H), 7,5 (т, 1H), 7,8 (т, 2H). На следующей странице представлена стереохимия соединений. В нижеследующей таблице представлены химические структуры и физические свойства некоторых соединений согласно изобретению. В колонке Ar, C6H5 означает фенильную группу, z-X-C6H4 означает фенильную группу, замещенную с помощью X в положении z, C5H4N-3 означает пиридин-3-ильную группу, C4H3S-3 означает тиен-3 ильную группу. В колонке Соль, - означает соединение в виде основания и HCl означает гидрохлорид. В колонке Т.пл. (C) (d) означает температуру плавления с разложением. В колонке Стереохимия, т-т означает конфигурацию транс-трео, т-э означает конфигурацию транс-эритро и ц-э означает конфигурацию цис-эритро, рац. означает рацемат. Соединения согласно изобретению подвергали ряду фармакологических тестов, которые показали,что они представляют интерес в качестве веществ с терапевтическими активностями. Исследование транспорта глицина в клетки SK-N-MC, экспрессирующие нативный человеческий переносчик glytl Захват [14C]глицина исследовали в случае клеток SK-N-MC (человеческие нейроэпителиальные клетки), экспрессирующие нативный человеческий переносчик glytl, путем измерения включенной радиоактивности в присутствии или в отсутствие тестируемого соединения. Клетки культивировали в монослое в течение 48 ч на планшетах, предварительно обработанных 0,02%-ным фибронектином. В день эксперимента культуральную среду удаляли и клетки промывали буфером Krebs-HEPES (4-(2 гидроксиэтил)пиперазин-1-этансульфокислота) с pH = 7,4. После предварительной инкубации в течение 10 мин при температуре 37C в присутствии либо буфера (контрольный образец), либо тестируемого соединения в различных концентрациях или 10 мМ глицина (определение неспецифического захвата),затем добавляли 10 мкМ [14C]глицина (удельная активность 112 мКи/ммоль). Инкубацию продолжали в течение 10 мин при температуре 37C и реакцию прекращали путем 2 промывок с помощью буфераKrebs-HEPES с pH = 7,4. Включенную клетками радиоактивность затем оценивали после добавления 100 мкл сцинтиллирующей жидкости и перемешивания в течение 1 ч. Подсчет осуществляли на компьютереMicrobeta Tri-lux. Эффективность соединения определяли путем CI50, концентрации соединения, которая снижает на 50% специфический захват глицина, определяемой по разности радиоактивности, включенной контрольным образцом и образцом, который получил 10 мМ глицина. Соединения согласно изобретению в этом тесте, имеют CI50 порядка 0,001-0,20 мкМ. Соединение 1 CI50 = 0,08 мкМ Соединение 2 CI50 = 0,023 мкМ Соединение 5 CI50 = 0,003 мкМ Как показывают эти результаты, соединения согласно изобретению обладают особой активностью- 10015974 как ингибиторы переносчиков глицина glytl. Соединения согласно изобретению, следовательно, могут быть использованы для получения лекарственных средств, в частности, лекарственных средств - ингибиторов переносчиков глицина glytl. Эти результаты наводят на мысль, что соединения согласно изобретению могут быть использованы для лечения поведенческих нарушений, ассоциированных с деменцией, психозов, в частности, шизофрении (дефицитная форма и продуктивная форма), и острых или хронических экстрапирамидальных симптомов, провоцируемых нейролептическими средствами, для лечения различных форм беспокойства,приступов паники, фобий, компульсивных навязчивых расстройств, для лечения различных форм депрессии, включая психотическую депрессию, для лечения нарушений, возникающих вследствие злоупотребления или прекращения приема алкоголя, нарушений сексуального поведения, нарушений в отношении приема пищи, для лечения мигрени и для лечения генерализованных, первичных и вторичных,частичных с простой или комплексной симптоматологией, эпилепсии, смешанных форм и других эпилептических синдромов, в виде дополнения другого антиэпилептического лечения или в виде монотерапии. Поэтому объектом настоящего изобретения также являются фармацевтические композиции, включающие эффективную дозу по меньшей мере одного соединения согласно изобретению, в виде основания или соли или фармацевтически приемлемого сольвата, и в смеси, в желательном случае, с подходящими эксципиентами. Вышеуказанные эксципиенты выбирают в зависимости от фармацевтической формы и желательного способа введения. Фармацевтические композиции согласно изобретению, таким образом, могут быть предназначены для перорального, сублингвального, подкожного, внутримышечного, внутривенного, топического, интратрахеального, интраназального, чрескожного, ректального, внутриглазного введения. Стандартными лекарственными формами могут быть, например, таблетки, желатиновые капсулы,гранулы, порошки, пероральные или инъецируемые растворы или суспензии, трансдермические пластыри (пэтч), суппозитории. Для топического введения можно предусмотреть мази, лосьоны и примочки для глаз. Вышеуказанные стандартные лекарственные формы обеспечивают возможность ежедневного введения от 0,01 до 20 мг действующего начала на кг массы тела, в зависимости от галеновой формы. Для получения таблеток к действующему началу, микронизированному или нет, добавляют фармацевтический наполнитель, который может представлять собой разбавитель, такой как, например, лактоза,микрокристаллическая целлюлоза, крахмал, и адъюванты готовой лекарственной формы, такие как связующие (поливинилпирролидон, гидроксипропилметилцеллюлоза и т.д.), способствующие текучести агенты, такие как диоксид кремния, лубриканты, такие как стеарат магния, стеариновая кислота, трибегенат глицерина, стеарилфумарат натрия. Также могут быть добавлены смачиватели или поверхностноактивные вещества, такие как лаурилсульфат натрия. Способами осуществления могут быть прямое прессование, сухое гранулирование, мокрое гранулирование или расплавление при нагревании. Таблетки могут быть без защитной оболочки, дражированными, например, при использовании сахарозы, или покрытыми различными полимерами или другими соответствующими веществами. Они могут быть приспособлены для возможности быстрого, замедленного или пролонгированного высвобождения действующего начала благодаря полимерным матрицам или специфическим полимерам, используемым в нанесенном покрытии. Для получения желатиновых капсул действующее начало смешивают с сухими (простое смешение,сухое или мокрое гранулирование или расплавление при нагревании), жидкими или полутвердыми фармацевтическими наполнителями. Желатиновые капсулы могут быть твердыми или мягкими, покрытыми пленкой или нет, чтобы обладать быстрой, пролонгированной или замедленной активностью (например, для энтеральной формы). Композиция в форме сиропа или эликсира или для введения в форме капель может содержать действующее начало вместе с подслащивающим, предпочтительно, некалорийным, средством, метилпарабеном или пропилпарабеном в качестве антисептика, вкусовым агентом и красителем. Порошки и гранулы, диспергируемые в воде, могут содержать действующее начало в смеси с диспергаторами или смачивателями или диспергирующими добавками, такими как поливинилпирролидон,также как с подслащивающими веществами и улучшающими вкус средствами. Для ректального введения используютсуппозитории, получаемые со связующими, плавящимися при температуре прямой кишки, например, масло какао или полиэтиленгликоли. Для парентерального введения используют водные суспензии, изотонические солевые растворы или инъецируемые стерильные растворы, содержащие фармакологически приемлемые диспергаторы и/или смачиватели, например, пропиленгликоль или бутиленгликоль. Действующее начало также может быть использовано для получения готовой лекарственной формы в виде микрокапсул, в случае необходимости, с одним (одной) или несколькими носителями или добавками, или же с полимерной матрицей или с циклодекстрином (трансдермальные пластыри, формы с про- 11015974 лонгированным высвобождением). Топические композиции согласно изобретению включают среду, совместимую с кожей. Они могут находиться, в частности, в виде водных, спиртовых или водно-спиртовых растворов, гелей, эмульсий вода-в-масле или масло-в-воде, имеющих внешний вид крема или геля, микроэмульсий, аэрозолей, или еще в форме везикулярных дисперсий, содержащих ионные и/или неионные липиды. Эти галеновые формы получают способами, обычными в рассматриваемых областях. Наконец, фармацевтические композиции согласно изобретению могут содержать, наряду с соединением общей формулы (I), другие действующие начала, которые могут быть пригодными при лечении вышеуказанных нарушений и заболеваний. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение в форме чистого энантиомера или эритро- или треодиастереоизомера или смеси таких изомеров, отвечающее общей формуле (I)m и n означают, каждый независимо друг от друга, число 1 или 2;Ar означает группу, выбираемую из фенила, нафтила-1, нафтила-2, пиридин-2-ила, пиридин-3-ила,пиридин-4-ила, фуран-2-ила, фуран-3-ила, тиен-2-ила, тиен-3-ила, тиазол-2-ила и оксазол-2-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими заместителями,выбираемыми из атомов галогенов и (C1-C6)алкила, (C3-C7)циклоалкила, (C3-C7)циклоалкил(C1C6)алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил-(C1-C6)алкилоксигруппы,(C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил-(C1-C6)алкилтиогруппы, моноили полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы;R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга,заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных (C1-C6)алкилов, разветвленных или циклических (C3-C7)алкилов,(C3-C7)циклоалкил(C1-C6)алкила, (C1-C6)алкоксила, (C3-C7)циклоалкилоксигруппы, (C3-C7)циклоалкил(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, цианогруппы, аминогруппы, фенила, ацетила, бензоила, (C1-C6)алкилсульфонила, карбоксила, (C1-C6)алкоксикарбонила и пентафторсульфанила; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата. 2. Соединение по п. 1, отличающееся тем, чтоAr означает группу, выбираемую из фенила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, тиен-2 ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими, одинаковыми или отличными друг от друга, заместителями, выбираемыми из атомов галогенов и (C1-C6)алкилов, (C3-C7)циклоалкилов, (C3-C7)циклоалкил(C1-C6)алкилов, (C1-C6)алкоксила, (C3C7)циклоалкилоксигруппы, (C3-C7)циклоалкил(C1-C6)алкилоксигруппы, (C1-C6)алкилтиогруппы, (C3-C7)циклоалкилтиогруппы, (C3-C7)циклоалкил(C1-C6)алкилтиогруппы, моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата. 3. Соединение по п.1 или 2, отличающееся тем, что Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими, одинаковыми или отличными друг от друга, заместителями, выбираемыми из атомов галогенов; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата. 4. Соединение по любому из пп.1-3, отличающееся тем, что R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга, заместителей, выбираемых из атомов галогенов и моно- или полифтор-(C1-C6)алкила и моно- или полифтор-(C1-C6)алкилоксигруппы, линейных(C1-C6)алкилов и пентафторсульфанила; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата. 5. Соединение по любому из пп.1-4, отличающееся тем, чтоm и n означают, каждый независимо друг от друга, число 1 или 2;Ar означает группу, выбираемую из фенила, пиридин-3-ила, тиен-3-ила, причем эта группа Ar может быть, в случае необходимости, замещена одним или несколькими атомами галогенов;R означает либо атом водорода, либо один или несколько, одинаковых или отличных друг от друга- 12015974 заместителей, выбираемых из атома хлора и метила, трифторметила, трифторметоксигруппы и пентафторсульфанила; в виде основания, аддитивной соли кислоты и/или сольвата или гидрата. 6. Соединение по п.1, отличающееся тем, что его выбирают из следующих соединений: гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидроиндолизин-5-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид цис-эритро-2-метил-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3S,8aR)-(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид цис-эритро-2-хлор-N-[(октагидроиндолизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3R,8aR)(октагидроиндолизин-3-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид 2-хлор-N-[(S)-(3R,8aR)(октагидроиндолизин-3-ил)(пиридин-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2,6-дихлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2,6-дихлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)(пиридин-3-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(октагидрохинолизин-4-ил)фенилметил]-5-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-метил-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(октагидрохинолизин-4-ил)(тиофен-3-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-трео-2-хлор-3-метил-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1; гидрохлорид транс-трео-2-хлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3-трифторметилбензамида 1:1; гидрохлорид транс-эритро-2-хлор-N-[(4-фторфенил)(октагидрохинолизин-4-ил)метил]-3 трифторметилбензамида 1:1; гидрохлорид транс-трео-2-метил-3-метокси-N-[(октагидрохинолизин-4-ил)фенилметил]бензамида 1:1; гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-трифторметоксибензамида 1:1; гидрохлорид транс-трео-N-[(октагидрохинолизин-4-ил)фенилметил]-3-(пентафторсульфанил)бензамида- 13015974 1:1; гидрохлорид 2-хлор-N-[(гексагидропирролизин-3-ил)фенилметил]-3-трифторметилбензамида 1:1. 7. Способ получения соединения по п.1, отличающийся тем, что нитрил общей формулы (II) в которой m и n имеют указанные в п.1 значения, вводят во взаимодействие с литийсодержащим производным общей формулы Ar-Li, в которой Ar имеет значение, раскрытое в п.1, в простом эфире в качестве растворителя при температуре от -90 до -30C, получая промежуточный имин общей формулы который восстанавливают до первичного амина общей формулы (V) с помощью восстановителя в протонном растворителе при температуре от 0C до комнатной температуры, затем осуществляют амидное связывание между диамином общей формулы (V) и активированной кислотой или хлорангидридом кислоты общей формулы (VI) в которой Y означает активированную группу OH или атом хлора и R имеет указанное в п.1 значение. 8. Соединение общей формулы (V) отличающееся тем, что m, n и Ar имеют значения, указанные по любому из пп.1-5. 9. Соединение по п.8, отличающееся тем, что его выбирают из следующих соединений: транс-трео/эритро-1-(октагидроиндолизин-5-ил)-1-фенилметанамин; транс-трео-1-(октагидроиндолизин-3-ил)-1-фенилметанамин; цис-эритро-1-(октагидроиндолизин-3-ил)-1-фенилметанамин; транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-фенилметанамин; транс-трео/эритро-1-(октагидро-2H-хинолизин-4-ил)-1-(4-фторфенил)метанамин; транс-трео-1-(октагидро-2H-хинолизин-4-ил)-1-пиридин-3-илметанамин; транс-трео/цис-эритро-1-(октагидро-2H-хинолизин-4-ил)-1-тиен-3-илметанамин. 10. Фармацевтическая композиция, отличающаяся тем, что она содержит соединение по п.1 в комбинации с эксципиентом. 11. Применение соединения по п.1 для получения лекарственного средства - ингибитора переносчиков глицина glytl. 12. Применение соединения по п.1 для получения лекарственного средства для лечения поведенческих нарушений, ассоциированных с деменцией, психозов и острых или хронических экстрапирамидальных симптомов, провоцируемых нейролептическими средствами, для лечения различных форм беспокойства, приступов паники, фобий, компульсивных навязчивых расстройств, для лечения различных форм депрессии, включая психотическую депрессию, для лечения нарушений, возникающих вследствие злоупотребления или прекращения приема алкоголя, нарушений сексуального поведения, нарушений в отношении приема пищи, для лечения мигрени и для лечения генерализованных, первичных и вторичных, частичных с простой или комплексной симптоматологией, эпилепсии, смешанных форм и других эпилептических синдромов, в виде дополнения другого антиэпилептического лечения или в виде монотерапии.- 14015974 13. Применение по п.12 для получения лекарственного средства для лечения шизофрении (дефицитная форма и продуктивная форма).
МПК / Метки
МПК: C07D 487/04, C07D 471/04, A61K 31/437
Метки: терапии, применение, производные, получение, пирролизина, индолизина, хинолизина
Код ссылки
<a href="https://eas.patents.su/16-15974-proizvodnye-pirrolizina-indolizina-i-hinolizina-ih-poluchenie-i-ih-primenenie-v-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пирролизина, индолизина и хинолизина, их получение и их применение в терапии</a>
Предыдущий патент: Способ селективного выделения, очистки и разделения моногидроксилированных 3,17-дикетостероидных соединений
Следующий патент: Охлаждающее устройство для листовой заготовки
Случайный патент: Фармацевтическая композиция