Способ отделения промежуточных соединений, который может быть использован для получения эсциталопрама
Формула / Реферат
1. Способ выделения и очистки соединения, имеющего формулу
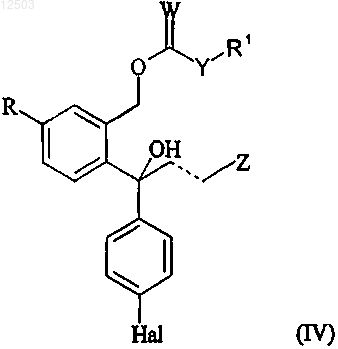
где R представляет собой циано или группу, которая может быть превращена в цианогруппу, где такая группа выбрана из хлора, брома, йода, фтора, CF3-(CF2)n-SO2-O-, где n принимает значения от 0 до 8, -ОН, -СНО, -СН2ОН, -CH2NH2, -CH2NO2, -CH2Cl, -CH2Br, -СН3, -NHR5, -CHNOH, -COOR6, -CONR6R7, где R5 представляет собой водород или C1-6-алкилкарбонил и R6 и R7 выбраны из водорода, необязательно замещенного C1-6-алкила и группы, имеющей формулу (VII)
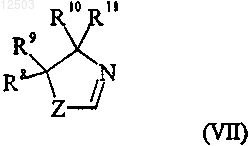
где Z в формуле (VII) представляет собой О или S; каждый R8 и R9 независимо выбраны из водорода и C1-6-алкила, или R8 и R9 вместе образуют цепь из С2-5-алкилена, образуя таким образом спирокольцо; R10 выбран из водорода и C1-6-алкила, R11 выбран из водорода, C1-6-алкила, карбоксигруппы или группы ее предшественников, или R10 и R11 вместе образуют цепь из С2-5-алкилена, образуя, таким образом, спирокольцо, пунктирная линия представляет собой двойную или прямую связь, Hal представляет собой галоген,
где Z в формуле (IV) представляет собой диметиламинометильную группу или группу, которая может быть превращена в диметиламинометильную группу, где такая группа выбрана из -CH2-L, -CH2-NO2, -MgHal, циано, альдегид, -CH2-O-Pg, -CH2-N(Pg1)(Pg2), -CH2-NMe(Pg1), -CH2-NHCH3, -CH2-NH2, -CO-N(CH3)2, -CH(A1RI2)(A1R13), -C(A1R14)(A2R15)(A3R16), -COOR17, -CH2-CONH2, -CH=CH-R18OR-CONHR19, где Pg - защитная группа для спиртовой группы, Pg1 и Pg2 являются защитными группами для аминогруппы, R12 и R13 независимо выбраны из C1-6-алкила, С2-6-алкенила, С2-6-алкинила, или R12 и R13 вместе образуют цепь из 2-4 атомов углерода, каждый из Rl4-R18 независимо выбран из C1-6-алкила, С1-6-алкенила и C1-6-алкинила, R19 является водородом или метилом, и А1, А2 или А3 выбраны из О и S; L представляет собой удаляемую группу, такую как галоген или -O-SO2-A-, где А представляет собой C1-6-алкил, С2-6-алкенил и С2-6-алкинил,
W представляет собой О или S, Y представляет собой связь, О, S или NH, и R1 представляет собой С1-10-алкил, С2-10-алкенил или С2-10-алкинил, все из которых необязательно могут быть замещены одним или более заместителями, выбранными из С1-10-алкокси, С1-10-алкилтио, гидрокси, галогена, амино, нитро, циано, С1-10-алкиламино и ди-(С1-10-алкил)амино, или его соли, и/или диола формулы (II)
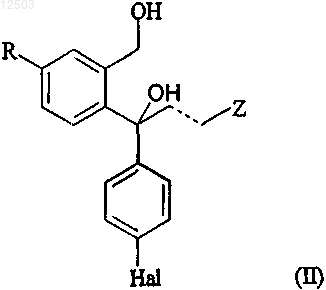
где R, Z, Hal и пунктирная линия определены выше, или его соли,
из смеси, содержащей соединение формулы (IV) и диол формулы (II), включающий:
а) введение смеси, содержащей соединение формулы (IV) и диол формулы (II), в реакцию с циклическим ангидридом или имидом формулы
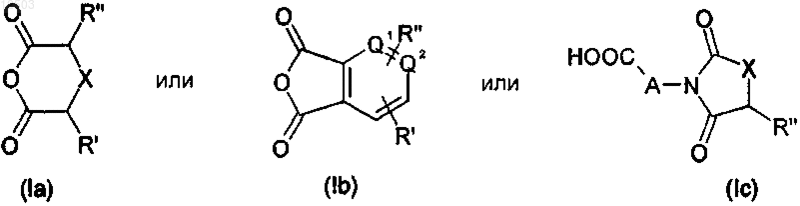
где X представляет собой -(CHR'")n-, где n принимает значения 0-2;
и R', R" и R'" независимо выбраны из водорода, C1-6-алкила, C1-6-алкокси, C1-6-ацилокси, или R' и R" в ангидриде формулы (Ia) вместе представляют собой -O-CR4R5-O-, где R4 и R5 независимо представляют собой водород или C1-6-алкил, или R' и R" в ангидриде формулы (Ib) являются смежными и вместе с двумя атомами углерода, к которым они присоединены, образуют бензольное кольцо;
один из Q1 и Q2 представляет собой азот, а другой - углерод, или оба они представляют собой углерод;
А представляет собой C1-6-алкилен, фенилен или нафтилен, где C1-6-алкиленовая, фениленовая или нафтиленовая группы необязательно могут быть замещены один или более раз C1-6-алкилом;
с образованием смеси соединения формулы (IV) и сложного эфира формулы (V)
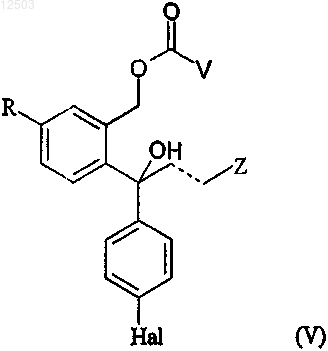
где R, Z и Hal определены выше, и V представляет собой -CHR'-X-CR"-COOH, -X-CHR"-CO-NH-A-СООН, -CHR''-X-CO-NH-А-СООН,

где R', R", X и А определены выше;
b) отделение соединения формулы (IV) от сложного эфира формулы (V) способом, выбранным из группы, состоящей из
iv) способа, согласно которому позволяют кислоте формулы (V) или ее соли выпасть в осадок из реакционной смеси и отделяют осадок соединения формулы (V) или его соли от реакционной смеси, необязательно, с последующим выделением соединения формулы (IV) или его соли из реакционной смеси;
v) способа распределения между органическим растворителем и водным растворителем, посредством которого соединение формулы (IV) будет растворено в органической фазе, тогда как соединение формулы (V) будет растворено в водной фазе, разделения фаз и, необязательно, выделения соединения формулы (IV) или его соли и/или выделения соединения формулы (V) или его соли; и
vi) способа адсорбции соединения формулы (V) на основе из смолы, отделения растворителя, содержащего соединение формулы (IV), от смолы, десорбции соединения формулы (V) от смоляной основы и, необязательно, выделения соединения формулы (IV) или его соли и/или выделения соединения формулы (V) или его соли.
2. Способ по п.1, где разделение соединения формулы (IV) и сложного эфира формулы (V) производят, позволяя кислоте формулы (V) выпасть в осадок из реакционной смеси, и разделение выпавшего осадка соединения формулы (V) и реакционной смеси производят, необязательно, с последующим выделением соединения формулы (IV) или его соли из реакционной смеси.
3. Способ по любому из пп.1 или 2, где R', R" и R"' независимо выбраны из водорода и C1-6-алкила, a Q1 и Q2 оба представляют собой углерод.
4. Способ по любому из пп.1-3, где S-энантиомер соединения формулы (V) или смесь энантиомеров соединения формулы (V), содержащая более чем 50% S-энантиомера соединения формулы (V), отделяли от R-энантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы (IV).
5. Способ по п.4, согласно которому S-энантиомер соединения формулы (V) отделяют от R-энантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы (IV).
6. Способ по п.5, где S-энантиомер соединения формулы (V) отделяют от R-энантиомера ацильного производного формулы (IV).
7. Способ по любому из пп.1-3, согласно которому S-энантиомер ацильного производного формулы (IV) или смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% S-энантиомера ацильного производного формулы (IV), отделяют от R-энантиомера соединения формулы (V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V).
8. Способ по п.7, согласно которому S-энантиомер ацильного производнюую формулы (IV) отделяют от R-энантиомера соединения формулы (V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V).
9. Способ по п.8, согласно которому S-энантиомер ацильного производного формулы (IV) отделяют от R-энантиомера соединения формулы (V).
10. Способ по любому из пп.4-6, согласно которому R-группа в соединении формулы (V), полученная в виде S-энантиомера, необязательно превращается в циано, полученная Z-группа в соединении формулы V необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно, превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы (V) в эсциталопрам или его производное, имеющее формулу
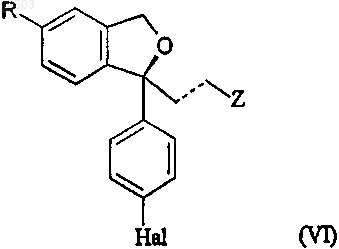
где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно, с последующим превращением эсциталопрама или производного формулы (VI) в их соль.
11. Способ по любому из пп.7-9, согласно которому R-группа в соединении формулы (IV), полученном в виде S-энантиомера, необязательно превращается в циано, Z-группа в полученном соединении формулы (IV) необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы (IV) в эсциталопрам или его производное
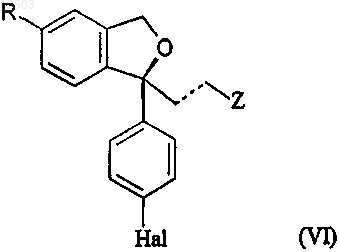
где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно с последующим превращением эсциталопрама или производного формулы (VI) в их соль.
12. Способ по любому из пп.10 или 11, где замыкание кольца в основных условиях проводили при обработке основанием таким как KOC(CH3)3 или другими алкоголятами, NaH или другими гидридами, или аминами, такими как триэтиламин, этилдиизопропиламин или пиридин.
13. Способ по любому из пп.1-12, где Hal представляет собой фтор, a R представляет собой галоген или циано, предпочтительно R представляет собой циано.
14. Способ по любому из пп.1-13, где пунктирная линия представляет собой прямую связь.
15. Способ по любому из пп.1-14, где Z представляет собой диметиламинометил.
16. Способ по пп.1-15, где ангидрид представляет собой соединение, имеющее формулу (Ia).
17. Способ по п.16, где ангидрид представляет собой янтарный ангидрид или глутаровый ангидрид.
18. Способ по пп.1-17, где ангидрид представляет собой соединение, имеющее формулу (Ib).
19. Способ по п.18, где ангидрид представляет собой ангидрид фталевой кислоты.
20. Способ по пп.1-15, где реагент представляет собой имид, имеющий формулу (Ic).
21. Способ по п.20, где имид представляет собой N-фенилсукцинимид, замещенный в фенильном кольце карбоксигруппой.
22. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой связь.
23. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой О или S.
24. Способ по п.23, где Y в соединении формулы (IV) представляет собой О.
25. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой NH.
26. Способ по любому из пп.22-25, где R1 выбран из C1-4-алкила, С2-4-алкенила и С2-4-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из С1-4-алкокси, C1-4-алкилтио, гидрокси, галогена, амино, нитро, циано, С1-4-алкиламино и ди-(С1-4-алкил)амино.
27. Способ по п.26, где R1 выбран из C1-3-алкила, С2-3-алкенила и С2-3-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-3-алкокси, C1-3-алкилтио, гидрокси, галогена, амино, нитро, циано, C1-3-алкиламино и ди-(С1-3-алкил)амино.
28. Способ по п.26, где R1 представляет собой С1-4-алкил.
29. Способ по п.27, где R1 представляет собой C1-3-алкил.
30. Способ по п.29, где R1 представляет собой метил, этил или пропил, предпочтительно пропил.
31.Способ по любому из пп.1-30, где смесь соединений формулы (II) и формулы (IV) получают посредством селективного энзиматического ацилирования или селективного энзиматического деацилирования.
Текст
012503 Настоящее изобретение связано с новым способом получения оптически активных промежуточных соединений, пригодным для получения эсциталопрама. Основы изобретения Циталопрам представляет собой хорошо известное антидепрессивное лекарственное средство, которое имеется в продаже уже несколько лет. Циталопрам является селективным, централизованно действующим ингибитором обратного захвата серотонина (5-гидрокситриптамин; 5-НТ), имеющим соответствующую антидепрессивную активность. Циталопрам впервые был описан в документе DE 2657013, соответствующем документу США 4136193. В указанной патентной публикации, помимо прочего, в общих чертах намечен способ получения циталопрама из соответствующего 5-бром-производного, при взаимодействии его с меднозакисным цианидом в подходящем растворителе и алкилированием 5-бром-фталана. В патенте США 4 943 590, соответствующем документу ЕР-В 1-347066, описано два способа получения эсциталопрама (S-энантиомер циталопрама). В обоих способах используют рацемический диол,имеющий формулу В качестве исходного материала, согласно первому способу диол формулы (I) реагирует с энантиомерно чистым производным кислоты, такой как (+) или (-)метокситрифторметилфенилацетилхлорид, с образованием смеси диастереомерных сложных эфиров, который разделяют с помощью HPLC или фракционной кристаллизации, вследствие чего сложный эфир с корректной стереохимией энантиоселективно превращается в эсциталопрам. Согласно второму способу диол формулы (II) разделяют на энантиомеры с помощью стереоселективной кристаллизации с энантиомерно чистой кислотой, такой как (+)-ди-п-толуоилвиннокаменная кислота, вследствие чего S-энантиомер диола формулы (I) энантиоселективно преобразуется в эсциталопрам. Эсциталопрам в настоящее время производится как антидепрессант. Следовательно, существует потребность в усовершенствовании способа получения эсциталопрама. Было обнаружено, что S-энантиомер диола формулы (I), указанной выше, также как и его ацилированные производные, может быть получен путем селективного энзиматического ацилирования исходной гидроксильной группы в рацемическом диоле, с получением S-диола формулы (I) или его ацилированных производных высокой оптической чистоты, и что кроме того полученные энантиомеры могут быть эффективно разделены в результате реакции диола формулы (I) с соединением, которое образует производную диола формулы (I), содержащую группу карбоновой кислоты. Образовавшиеся производные сразу же при образовании выпадают в осадок и могут быть легко выделены из реакционной смеси. Сущность изобретения Настоящее изобретение представляет собой способ выделения и очистки соединения, имеющего формулу где R представляет собой циано или группу, которая может быть превращена в цианогруппу, где такая группа выбрана из хлора, брома, йода, фтора, CF3-(CF2)n-SO2-O-, где n принимает значения от 0 до 8, -ОН, -СНО, -СН 2 ОН, -CH2NH2, -CH2NO2, CH2Cl, -CH2Br, -СН 3, -NHR5, -CHNOH, -COOR6, -CONR6R7,где R5 представляет собой водород или С 1-6-алкилкарбонил, и R6 и R7 выбраны из водорода, необязательно замещенного C1-6-алкила и группы, имеющей формулу (VII)R8 и R9 независимо выбраны из водорода и C1-6-алкила, или R8 и R9 вместе образуют цепь из С 2-5-1 012503 алкилена, образуя, таким образом, спирокольцо; R10 выбран из водорода и C1-6-алкила, R11 выбран из водорода, C1-6-алкила, карбоксигруппы или группы ее предшественников, или R10 и R11 вместе образуют цепь из С 2-5-алкилена, образуя, таким образом, спирокольцо, пунктирная линия представляет собой двойную или прямую связь,Hal представляет собой галоген,где Z в формуле (IV) представляет собой диметиламинометильную группу или группу, которая может быть превращена в диметиламинометильную группу, где такая группа выбрана из -CH2-L, -CH2-NO2,-MgHal, циано, альдегид, -СН 2-О-Pg, -CH2-N(Pg1)(Pg2), -CH2-NMe (Pg1), -CH2-NHCH3, -CH2-NH2, -CON(CH3)2, -CH(A1R12) (A1R13), -C(A1R14)(A2R15) (A3R16), COOR17, -CH2-CONH2, -CH=CH-R18OR-CONHR19,где Pg - защитная группа для спиртовой группы, Pg1 и Pg2 являются защитными группами для аминогруппы, R12 и R13 независимо выбраны из C1-6-алкила, С 2-6-алкенила, С 2-6-алкинила, или R12 и R13 вместе образуют цепь из 2-4 атомов углерода, каждый из R14-R18 независимо выбран из C1-6-алкила, С 2-6 алкенила и C1-6-алкинила, R19 является водородом или метилом, и А 1, А 2 или А 3 выбраны из О и S; L представляет собой удаляемую группу, такую как галоген или -O-SO2-A-, где А представляет собой C1-6 алкил, С 2-6-алкенил и С 2-6-алкинил,W представляет собой О или S, Y представляет собой связь, О, S или NH, иR1 представляет собсй C1-10-алкил, С 2-10-алкенил или С 2-10-алкинил, все из которых необязательно могут быть замещены одним или более заместителями, выбранными из C1-10-алкокси, C1-10-алкилтио,гидрокси, галогена, амино, нитро, циано, C1-10-алкиламино и ди-(C1-10-алкил) амино, или его соли,и/или диола формулы (II) где R, Z, Hal и пунктирная линия определены выше, или его соли,из смеси, содержащей соединение формулы (IV) и диол формулы (II), включающий: а) введение смеси, содержащей соединение формулы (IV) и диол формулы (II), в реакцию с циклическим ангидридом или имидом формулы где X представляет собой -(CHR)n-, где n принимает значения 0-2; и R, R и R независимо выбраны из водорода, C1-6-алкила, C1-6-алкокси, C1-6-ацилокси, или R' и R" в ангидриде формулы (Ia) вместе представляют собой -O-CR4R5-O-, где R4 и R5 независимо представляют собой водород или C1-6-алкил, или R' и R" в ангидриде формулы (1b)явпяются смежными и, вместе с двумя атомами углерода, к которым они присоединены, образуют бензольное кольцо; один из Q1 и Q2 представляет собой азот, а другой - углерод, или оба они представляют собой углерод; А представляет собой C1-6-алкилен, фенилен или нафтилен, где C1-6-алкиленовая, фениленовая или нафтиленовая группы необязательно могут быть замещены один или более раз C1-6-алкилом; с образованием смеси соединения формулы (IV) и сложного эфира формулы (V)b) отделение соединения формулы (IV) от сложного эфира формулы (V) способом, выбранным из группы, состоящей изiv) способа, согласно которому позволяют кислоте формулы (V) или ее соли выпасть в осадок из реакционной смеси, и отделяют осадок соединения формулы (V) или его соли от реакционной смеси,необязательно с последующим выделением соединения формулы (IV) или его соли из реакционной смеси;v) способа распределения между органическим растворителем и водным растворителем, посредством которого соединение формулы (IV) будет растворено в органической фазе, тогда как соединение формулы (V) будет растворено в водной фазе, разделения фаз и необязательно выделения соединения формулы (IV) или его соли и/или выделения соединения формулы (V) или его соли; иvi) способа адсорбции соединения формулы (V) на основе из смолы, отделения растворителя, содержащего соединение формулы (IV), от смолы, десорбции соединения формулы (V) от смоляной основы и необязательно выделения соединения формулы (IV) или его соли и/или выделения соединения формулы (V) или его соли. В предпочтительном варианте разделение соединения формулы (IV) и сложного эфира формулы(V) производят, позволяя кислоте формулы (V) выпасть в осадок из реакционной смеси, и разделение выпавшего осадка соединения формулы (V) и реакционной смеси, необязательно с последующим выделением соединения формулы (IV) или его соли из реакционной смеси. Наиболее предпочтителен вариант, когда R', R" и R независимо выбраны из водорода и C1-6 алкила, a Q1 и Q2 оба представляют собой углерод. Предпочтителен вариант, когда S-энантиомер соединения формулы (V) или смесь энантиомеров соединения формулы (V), содержащая более чем 50% S-энантиомера соединения формулы (V), отделяли отR-энантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы (IV). Ещ более предпочтителен вариант, согласно которому S-энантиомер соединения формулы (V) отделяют от R-энантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы (IV). Причем наиболее предпочтительно, когда S-энантиомер соединения формулы (V) отделяют от R-энантиомера ацильного производного формулы (IV). В предпочтительном варианте S-энантиомер ацильного производного формулы (IV) или смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% S-энантиомера ацильного производного формулы (IV), отделяют от R-энантиомера соединения формулы (V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V). Ещ более предпочтительно, когда S-энантиомер ацильного производного формулы (IV) отделяют от R-энантиомера соединения формулы (V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V). Причем наиболее предпочтительно, когда S-энантиомер ацильного производного формулы (IV) отделяют от R-энантиомера соединения формулы (V). В предпочтительном варианте настоящего изобретения R-группа в соединении формулы (V), полученная в виде S-энантиомера, необязательно превращается в циано, полученная Z-группа в соединении формулы V необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы (V) в эсциталопрам или его производное, имеющее формулу где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно с последующим превращением эсциталопрама или производного формулы (VI) в их соль. Предпочтительным является способ, согласно которому R-группа в соединении формулы (IV), полученном в виде S-энантиомера, необязательно превращается в циано, Z-группа в полученном соединении формулы (IV) необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы(IV) в эсциталопрам или его производное где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно с последующим превращением эсциталопрама или производного формулы (VI) в их соль. При этом наиболее предпочтительно, когда замыкание кольца в основных условиях проводили при обработке основанием, таким как КОС(СН 3)3 или другими алкоголятами, NaH или другими гидридами,или аминами, такими как триэтиламин, этилдиизопропиламин или пиридин. Предпочтительно, когда в способе согласно настоящему изобретению Hal представляет собой фтор,a R представляет собой галоген или циано, предпочтительно, R представляет собой циано. Предпочтительно, когда пунктирная линия представляет собой прямую связь. Предпочтительно, когда Z представляет собой диметиламинометил. Предпочтительно, когда ангидрид представляет собой соединение, имеющее формупу (Ia). Более предпочтительно, когда ангидрид представляет собой янтарный ангидрид или глутаровый ангидрид. Ещ один предпочтительный вариант настоящего изобретения предусматривает, что ангидрид представляет собой соединение, имеющее формулу (Ib). Причем наиболее предпочтительно, когда ангидрид представляет собой ангидрид фталевой кислоты. Предпочтительно, когда в способе согласно настоящему изобретению реагент представляет собой имид, имеющий формулу (Ic). Причем наиболее предпочтительно, если имид представляет собой Nфенил-сукцинимид, замещенный в фенильном кольце карбоксигруппой. Предпочтительно, когда в способе согласно настоящему изобретению Y в соединении формулы(IV) представляет собой связь. Другой предпочтительный вариант настоящего изобретения предусматривает, что Y в соединении формулы (IV) представляет собой О или S, причем более предпочтительно, если Y в соединении формулы (IV) поедставляет собой О. Ещ один предпочтительный вариант настоящего изобретения предусматривает, что Y в соединении формулы (IV) представляет собой NH. Наиболее предпочтительно, когда R1 выбран из C1-4-алкила, С 1-4-алкенила и С 2-4-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-4 алкокси, C1-4-алкилтио, гидрокси, галогена, амино, нитро, циано, C1-4-алкиламино и ди-(C1-4-алкил)амино. При этом ещ более предпочтитлеьно, если R1 выбран из C1-3-алкила, С 2-3-алкенила и С 2-3-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-3 алкокси, C1-3-алкилтио, гидрокси, галогена, амино, нитро, циано, C1-3-алкиламино и ди- (C1-3-алкил) амино. Предпочтительно, когда R1 представляет собой С 1-4-алкил, ещ более предпочтительно, когда R1 представляет собой С 1-3-алкил,и наиболее предпочтительно, если R1 представляет собой метил, этил или пропил, предпочтительно, пропил. Предпочтительный вариант настоящего изобретения предусматривает способ, в котором смесь соединений формулы (II) и формулы (IV) получают посредством селективного энзиматического ацилирования или селективного энзиматического деацилирования. Подробное описание изобретения Используемые в отношении соединений формул (II), (IV), (V) и (VI), термины "энантиомер", "Rэнантиомер", "S-энантиомер", "R-форма", "S-форма", "R-диол" и "S-диол" относятся к ориентации групп вокруг атома углерода, к которому 4-На 1-фенильная группа присоединена. Используемый в данном документе термин C1-10-алкил относится к разветвленной или неразветвленной алкильной группе, имеющей от одного до десяти атомов углерода, включающей в себя такие как. метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-2-пропил, 2-метил-1-пропил, пентил, гексил и гептил. C1-6-алкил относится к разветвленной или неразветвленной алкильной группе, имеющей от одного до шести атомов углерода включительно, такой как метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил,2-метил-2-пропил, 2-метил-1-пропил, пентил и гексил. C1-4-алкил относится к разветвленной или неразветвленной алкильной группе, имеющей от одного до четырех атомов углерода включительно, такой как метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-2-пропил и 2-метил-1-пропил. C1-3-алкил относится к разветвленной или неразветвленной алкильной группе, имеющей от одного до трех атомов углерода включительно, такой как метил, этил, 1-пропил, 2-пропил. Сходным образом С 2-10-алкенил и С 2-10-алкинил означают разветвленные или неразветвленные ал-4 012503 кенильную и алкинильную группы, соответственно, имеющие от двух до десяти атомов углерода, включающие в себя одну двойную связь и одну тройную связь, соответственно, такие как этенил, пропенил,бутенил, этинил, пропинил и бутинил. С 2-6-алкенил и С 2-6-алкинил означают разветвленную или неразветвленную алкенильную и алкинильную группы, соответственно, имеющие от двух до шести атомов углерода, включающие в себя одну двойную связь и одну тройную связь, соответственно, такие как этенил, пропенил, бутенил, этинил, пропинил и бутинил. С 2-4-алкенил и С 2-4-алкинил означают разветвленную или неразветвленную алкенильную и алкинильную группы, соответственно, имеющие от двух до четырех атомов углерода, включающие в себя одну двойную связь и одну тройную связь, соответственно, такие как этенил, пропенил, бутенил, этинил, пропинил и бутинит. С 2-3-алкенил и С 2-3-алкинил означают разветвленную или неразветвленную алкенильную и алкинильную группы, соответственно, имеющие от двух до трех атомов углерода, включающие в себя одну двойную связь и одну тройную связь,соответственно, такие как этенил, пропенил, этинил и пропинил. Термины C1-10-алкокси, C1-10-алкилтио, C1-10-алкиламино и ди-(C1-10-алкил)амино и т.д. означают такие группы, в которых алкильная группа является C1-10-алкилом, как определено выше. Термины C1-6 алкокси, C1-6-алкилтио, C1-6-алкиламино и ди-(С 1-6-алкил)амино и т.д. означают такие группы, в которых алкильная группа является C1-6-алкилом, как определено выше. Термины С 1-4-алкокси, C1-4-алкилтио,С 1-4-алкиламино и ди-(C1-4-алкил)амино и т.д. означают такие группы, в которых алкильная группа является C1-4-алкилом, как определено выше. Термины C1-3-алкокси, С 1-3-алкилтио, C1-3-алкиламино и ди-(C1-3-алкил)амино и т.д. означают такие группы, в которых алкильная группа является C1-3-алкилом,как определено выше. Галоген означает фтор, хлор, бром или йод. Используемый в данном документе термин "антирастворитель" означает жидкость, которая при добавлении в систему раствор-растворенное вещество уменьшает растворимость растворенного вещества. В конкретном воплощении настоящего изобретения отделение соединения формулы (IV) от сложного эфира формулы (V) проводят, давая возможность кислоте формулы (V) выпасть в осадок из реакционной смеси и отделяя осадок соединения формулы (V) от реакционной смеси, необязательно с последующим выделением соединения формулы (IV) или его соли из реакционной смеси. В конкретном воплощении настоящего изобретения, R', R" и R"' независимо выбраны из водорода и С 1-6-алкила, a Q1 и Q2 оба представляют собой углерод. В конкретном воплощении настоящего изобретения смесь энантиомеров соединения формулы (V) содержит более чем 60% S-энантиомера соединения формулы (V), например более чем 70, более чем 80,более чем 90, более чем 95, более чем 98 или более чем 99%. В другом столь же конкретном воплощении настоящего изобретения смесь энантиомеров соединения формулы (V) содержит более чем 60% R-энантиомера соединения формулы (V), например более чем 70, более чем 80, более чем 90, более чем 95, более чем 98 или более чем 99%. Еще в одном столь же конкретном воплощении настоящего изобретения смесь энантиомеров ацильного производного формулы (IV) содержит более чем 60% S-энантиомера соединения формулы(V), например более чем 70, более чем 80, более чем 90, более чем 95, более чем 98 или более чем 99%. В другом столь же конкретном воплощении настоящего изобретения смесь энантиомеров ацильного производного формулы (IV) содержит более чем 60% R-энантиомера соединения формулы (V), например более чем 70, более чем 80, более чем 90, более чем 95, более чем 98 или более чем 99%. В предпочтительном воплощении настоящего изобретения R представляет собой галоген или циано, более предпочтительно, циано. В следующем предпочтительном воплощении настоящего изобретения Hal представляет собой фтор. В следующем предпочтительном воплощении настоящего изобретения пунктирная ллния в формулах (II), (IV) и (V) представляет собой прямую связь. В следующем предпочтительном воплощении Z представляет собой диметиламинометил или группу, которая может превращаться в диметиламинометил. В предпочтительном воплощении Z представляет собой диметиламинометил. Наиболее предпочтительно, когда Hal представляет собой фтор, R представляет собой циано, пунктирная линия представляет собой прямую связь, a Z представляет собой диметиламинометил. Согласно одному из воплощений настоящего изобретения, Y в соединении формулы (IV) представляет собой О или S. Согласно другому воплощению настоящего изобретения, Y в соединении формулы (IV) представляет собой NH. Однако согласно предпочтительному воплощению настоящего изобретения, Y в соединении формулы (IV) означает связь. Соответственно, заместитель R1 в соединении формулы (IV), как определено в любом из вышеперечисленных воплощений, представляет собой следующее: R1 представляет собой C1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-6-алкокси, C1-6-алкилтио, гидрокси, галогена, амино, нитро, циано, C1-4-5 012503 алкиламино и ди-(C1-6-алкил)амино, предпочтительнее, когда R1 представляет собой C1-4-алкил, С 2-4 алкенил или С 2-4-алкинил, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-4-алкокси, C1-4-алкилтио, гидрокси, галогена, амино, нитро, циано, С 1-4 алкиламино и ди-(C1-4-алкил)амино, предпочтительно R1 представляет собой C1-3-алкил, С 2-3-алкенил или С 2-3-алкенил или С 2-3-алкинил, все из которых необязательно могут быть замещены один или более разC1-3-алкокси, С 1-3-алкилтио, гидрокси, галогеном, амино, нитро, циано, C1-3-алкиламино и ди-(C1-3 алкил)амино, более предпочтительно, R1 представляет собой C1-3-алкил, С 2-3-алкенил или С 2-3-алкинил, и более предпочтительно, R1 представляет собой C1-3-алкил, в частности, неразветвленный C1-3-алкил, такой как метил, этил или пропил. Настоящее изобретение, в частности, предназначено для разделения соединений формулы (II),представленных в виде S или R-энантиомера, и соединения формулы (IV), представленного в форме противоположного энантиомера, полученного с помощью энзиматического разложения, согласно способу,описанному в Международной заявке WOPCT/DK/0300537, опубликованной как W02004/014821. Таким образом, согласно воплощению настоящего изобретения, смесь соединений формулы (II) и формулы (IV), используемую в способе, готовят посредством селективного энзиматического ацилирования или селективного энзиматического деацилирования. Конкретным преимуществом данного изобретения является то, что после образования соединения формулы (V) оно выпадает в осадок из реакционной смеси, после чего его легко можно выделить. Другим конкретным преимуществом данного изобретения является (в зависимости от применения конкретного реагента формул (Ia)-(Ic то, что оно в результате приводит к разделению и выделению продукта, который может быть напрямую замкнут в кольцо, с образованием эсциталопрама или его производного, посредством обработки основанием. Взаимодействие смеси соединения формулы (II) в виде одного из энантиомеров с соединением формул (Ia), (Ib) или (Ic) можно проводить в инертном органическом растворителе, таком как тетрагидрофуран, предпочтительно, в растворителе, в котором кислота формулы (V) образует осадок, и в конкретном количестве такого растворителя, в котором кислота формулы (V) образует осадок. Подходящие растворители могут быть подобраны специалистом в данной области. Альтернативно, реакцию проводили в растворителе, из которого кислота формулы (V) не выпадает в осадок, и после образования соединения формулы (V) добавляли анти-растворитель, вследствие чего кислота формулы (V) выпадала в осадок. Подходящей температурой проведения реакции приблизительно является комнатная температура(25 С). Соединение формулы (V) подходящим образом отделяют от соединения формулы (IV) посредством фильтрования или декантирования или с помощью любого другого подходящего способа отделения твердого вещества от жидкости. Если выделенное соединение формулы V представляет собой S-энантиомер, оно может быть напрямую замкнуто в кольцо посредством обработки основанием в подходящем органическом растворителе. Энантиоселективное замыкание кольца S-энантиомера формулы (V) с образованием эсциталопрама или другого соединения формулы (VI) может быть подходящим образом проведено путем обработки соединения формулы (V) основанием, таким как KOC(CH3)3 или другими алкоголятами, NaH или другими гидридами, или аминами, такими как триэтиламин, этилдиизопропиламин или пиридин, при низких температурах, в инертном органическом растворителе, таком как тетрагидрофуран, толуол, DMSO, DMF,трет-бутиловый метиловый эфир, диметоксиэтан, диметоксиметан, диоксан, ацетонитрил или дихлорометан. Данный процесс может быть проведен аналогично тому, как описано в патенте США 4943590. Таким же образом соединение формулы (IV) в виде S-энантиомера и отделенное от реакционной смеси может быть подвергнуто замыканию кольца посредством обработки основанием. В некоторых случаях может быть предпочтительна замена группы -CW-Y-R1 в соединении формулы (IV) или группы -CO-V в соединении формулы (V) более лабильной группой перед тем, как проводить замыкание кольца. Такие лабильные группы (удаляемые группы) обычно могут представлять собой группу, выбранную из метансульфонилокси, пара-толуолсульфонилокси, 10-камфорсульфонилокси,трифторацетилокси и трифторметансульфонилокси или галогена. Обычно соединение формулы (IV) или формулы (V) подвергают затем гидролизу с водным основанием до образования соединения формулы (II), с таким основаниями как NaOH, KOH или LiOH в воде или спирте или в их смеси, и затем подвергают взаимодействию с активированной удаляемой группой,такой как группа -O-SO2-A, где А представляет собой С 1-6-алкил, С 2-6-алкенил, С 2-6-алкинил или необязательно C1-6-алкил, замещенный арилом или арил-С 1-6-алкилом, в частности, метилсульфонилхлоридом или тозилхлоридом, или трифторацетилхлоридом, ацетилхлоридом или в виде муравьиной кислоты, таком как смесь муравьиной кислоты и уксусного ангидрида в органическом растворителе в присутствии органического основания. Предпочтительно, заместитель V в соединении формулы (V) представляет собой заместитель, который способствует прямому замыканию кольца соединения формулы (V) при обработке основанием. Бо-6 012503 лее предпочтительно, если V представляет собой -СН 2-СН 2-СООН или -СН 2-СН 2-СН 2-СООН. Оптическая чистота продукта-эсциталопрама может быть улучшена после замыкания кольца. Улучшение оптической чистоты можно получить с помощью хроматографии на хиральной стационарной фазе или посредством кристаллизации рацемического основания циталопрама или его соли, согласно способам, описанным в Международной заявке WO 03/000672.R-энантиомер соединений формулы (V) и формулы (IV), полученный согласно настоящему изобретению, может быть использован для получения рацемического циталопрама и эсциталопрама путем замыкания кольца в кислотной среде, согласно способу, описанному в Международной заявке WO 03/000672. Подходящими кислотами для проведения кислотного замыкания кольца являются неорганическая кислота, карбоновая кислота, сульфоновая кислота или производное сульфоновой кислоты, более предпочтитепьно H2SO4 или Н 3 РО 4. Стартовая смесь, применяемая для способа разделения согласно настоящему изобретению, может быть получена путем энзиматического ацилированя или деацилирования с применением гидролазы, такой как липаза, эстераза, ацилаза или протеаза, как описано в Международной заявке WOPCT/DK/0300537, опубликованной как WO 2004/014821. Было обнаружено, что энзиматическое ацилирование согласно изобретению можно провести с использованием Novozyme435 из Candida antartica, LipoZyme TL IM из Thermomyces lanuginosus, оба из которых предоставляются компанией Novozymes A/S, или липопротеинлипазы pseudomonas sp. (выделенной из Pseudomonas Cepacia и полученной от Fluka), и, в частности, хорошие результаты получаются при использовании Novozyme4 35 из Candida antartica или липопротеинлипазы pseudomonas sp."Фермент" или "гидролаза" могут быть иммобилизованы в виде фермента как такового или в виде клеточной массы с помощью известных технических приемов, и могут быть использованы в иммобилизационной форме. Иммобилизацию можно провести с помощью способов, известных специалистам в данной области, и такие способы включают в себя, например, связывание носителя, поперечную сшивку,энкапсулирование и пр. Таким образом, гидролазу можно использовать в виде иммобилизованного фермента или в виде перекрестно-сшитых ферментов в кристаллической форме (CLEC). Вышеупомянутые ферменты могут быть использованы также в виде культивируемых продуктов,содержащих фермент, таких как культуральная жидкость, содержащая клеточную массу, или культивируемые клетки, переработанный культивируемый продукт и любые иммобилизованные формы таких ферментов/культивируемых продуктов. Мутанты, варианты или любые эквиваленты вышеупомянутых специально указанных ферментов,которые могут выполнять селективное ацилирование или деацилирование, также могут быть использованы. Варианты или их эквиваленты могут быть выделены из различных штаммов Pseudomonas, Candida или Thermomyces, или любого другого источника, или же они могут быть получены в результате мутирования ДНК, кодирующей указанные выше ферменты, приводящего к различиям в аминокислотном составе фермента. Подходящие мутанты или варианты указанных выше ферментов представляют собой варианты и мутанты, где отдельные аминокислоты удалены или замещены другими аминокислотами, и подходящая аминокислотная последовательность варианта или мутанта содержит более чем 60% идентичной последовательности, предпочтительно более чем 80% и наиболее предпочтительно более чем 90% последовательности, идентичной указанным выше ферментам. Предпочтительные условия реакции для энзиматического ацилирования/деацилирования сильно варьируют, в зависимости от конкретного используемого фермента, от того является ли он иммобилизованным или нет, и т.д. Подходящая температура для такой реакции составляет от 0 до 80 С, более предпочтительно от 20 до 60 С или более предпочтительно от 30 до 50 С. Количество используемого фермента практически не ограничено, но обычно оно составляет 0,011,0, предпочтительно 0,02-0,5 и более предпочтительно 0,02-0,3 в виде весового отношения к субстрату. Реакция может проводиться в виде периодического процесса, или же она может проводиться в виде непрерывного процесса. Фермент может быть многократно использован периодически или непрерывно. Время реакции особо не ограничено и будет зависеть от используемого фермента и масштаба и типа выбранного способа продуцирования (периодического или непрерывного). Согласно Международной заявке WOPCT/DK/0300537, опубликованной как WO2004/014821,ацилирующим агентом, используемым для энзиматического ацилирования, может быть агент, имеющий формулу или может быть изоцианат, имеющий формулу R1-N=C=O, или изотиоцианат, имеющий формулуR0 представляет собой C1-10-алкил, С 2-10-алкенил или C2-10-алкинил, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-10-алкокси, C1-10-алкилтио,гидрокси, галогена, амино, нитро, циано, C1-10-алкиламино, ди-(C1-10-алкил)амино, арила, арилокси, арилтио и гетероарила, или R0 представляет собой арил, где любая из арильных и гетероарильных групп необязательно может быть замещена один или более раз заместителями, выбранными из C1-10-алкила, С 2-10 алкенила, С 2-10-алкинила, C1-10-алкокси, С 1-10-алкилтио, гидрокси, галогена, амино, нитро, циано, C1-10 алкиламино и ди-(C1-10-алкил)амино;R1 представляет собой то же, что и определено для R0;R2 представляет собой то же, что и определено для R0, или R2 представляет собой подходящую необратимую ацильную донорскую группу; или R0 и R1 вместе образуют цепь из 3-5 атомов углерода; при условии, что W и U не являются S,когда X представляет собой S. Предпочтительно, U представляет собой О в соединении формулы (IIIa). Предпочтительно, W представляет собой О в любом из указанных выше ацилирующих агентов. Предпочтительно, X представляет собой О в любом из указанных выше ацилирующих агентов. Предпочтительно, R1 и R0 представляют собой C1-3-алкил, в частности, неразветвленный C1-3-алкил,такой как этил или пропил, и предпочтительно R2 представляет собой C1-3-алкил, замещенный один или более раз галогеном, или R2 представляет собой С 2-3-алкенил, и, наиболее предпочтительно, R2 представляет собой С 2-3-алкенил, такой как винил. Предпочтительным ацилирующим агентом является винилбутират. Энзиматическое деацилирование можно проводить, используя соединение формулы в качестве исходного материала, где R, Z, W, Y, Hal, пунктирная линия и R1 представляют собой то же, что и определено выше. Соответственно, R1 представляет собой C1-10-алкил, предпочтительно, неразветвленный C1-10-алкил,и более предпочтительно, R1 представляет собой неразветвленный С 4-10-алкил в исходном материале,используемом для энзиматического деацилирования. Селективное энзиматическое ацилирование предпочтительно проводят в условиях, существенно подавляющих гидролиз. Гидролиз, который представляет собой реакцию, обратную реакции ацилирования, имеет место в присутствии в реакционной системе воды. Таким образом, селективное энзиматическое ацилирование предпочтительно проводят в безводном органическом растворителе или почти безводном органическом растворителе (ферментам обычно необходимо некоторое количество воды для активности). Процентное содержание воды, допустимое в конкретной реакционной системе, может определить специалист в данной области. Неважно, какой конкретно органический растворитель будет использован в реакции ацилирования,пока он не инактивирует используемый фермент. Подходящие растворители включают в себя такие углеводороды как гексан, гептан, бензол и толуол; эфиры, такие как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, 1,4-диоксан, трет-бутилметиловый эфир и диметоксиэтан; такие кетоны как ацетон, диэтилкетон, бутанон и метилэтилкетон; такие сложные эфиры как метилацетат, этилацетат, этилбутират, винилбутират и этилбензоат; галогенизированные углеводороды, такие как метиленхлорид, хлороформ и 1,1,1-трихлорэтан; вторичные и третичные спирты, такие как трет-бутанол; азотсодержащие растворители, такие как диметилформамид, ацетоамид, формамид, ацетонитрил и пропионитрил; и апротонные, полярные растворители, такие как диметилсульфоксид, N-метилпирролидон и гексаметилфосфорный триамид. Среди них предпочтительными являются такие углеводороды как гексан, гептан, бензол и толуол,эфиры, такие как диэтиловый эфир, диизопропиловый эфир, 1,4-диоксан и трет-бутилметиловый эфир, и сложные эфиры, такие как винилбутират. Для одного фермента наиболее предпочтительными могут быть такие эфиры и ароматические углеводороды как бензол или толуол, наиболее предпочтителен толуол, а для другого фермента более предпочтительными растворителями могут быть эфиры, такие как 1,4-диоксан. Вышеперечисленные растворители могут применяться поодиночке или в сочетании с двумя или более растворителями. Концентрация рацемического диола формулы (II) и ацилирующего агента не должна быть слишком высокой, так как высокая концентрация реагентов в растворителе может привести к неселективному ацилированию рацемического диола формулы (II). Подходящей концентрацией рацемического диола-8 012503 формулы (II) и ацилирующего реагента является для каждого ниже 1,0 М, более предпочтительно, ниже 0,5 М, даже более предпочтительно, 0,2 М, или даже более предпочтительно, ниже 0,1 М. Специалист в данной области способен определить оптимальную концентрацию рацемического диола формулы (II) и ацилирующего агента. Селективное энзиматическое деацилирование предпочтительно проводят в воде или смеси воды и органического растворителя, лучше в присутствии буфера. Органический растворитель, который может быть использован в реакции, не особо важен, пока он не инактивирует используемый фермент. Подходящими органическими растворителями являются растворители, смешивающиеся с водой, такие как спирты, ацетонитрил, DMF, DMSO, диоксан, DME и простой диметиловый эфир циэтиленгликоля. Специалист в данной области способен идентифицировать другие подходящие растворители. Специалист способен определить оптимальную концентрацию рацемического соединения формулы (IV), используемого в реакции. Стереоселективность используемого фермента может быть увеличена путем проведения ацилирования или деацилирования в присутствии органической кислоты и/или органического основания. В частности, энзиматическое ацилирование или энзиматическое деацилирование проводят в присутствии органической кислоты, лучше органической карбоновой кислоты. Лучше, чтобы указанная выше органическая кислота представляла собой ароматическую карбоновую кислоту или алифатическую карбоновую кислоту. Подходящими органическими кислотами, которые могут быть использованы в реакции, являются алкилкарбоновые кислоты, циклоалкилкарбоновые кислоты, циклоалкилалкилкарбоновые кислоты, необязательно замещенные фенилалкилкарбоновые кислоты и необязательно замещенные фенилкарбоновые кислоты. Подходящими алифатическими карбоновыми кислотами являются такие карбоновые кислоты как муравьиная кислота, уксусная кислота, пропионовая кислота, н-масляная ккслота, изомасляная кислота, 2-этилмасляная кислота, н-валериановая кислота, изо-валериановая кислота, триметилуксусная кислота, н-капроновая кислота, изокапроновая кислота, декановая кислота, кротоновая кислота, пальмитиновая кислота, циклопентанкарбоновая кислота, циклогексанкарбоновая кислота; такие фенил-С 1-4-алкилкарбоновые кислоты как 3-фенилпропионовая кислота, 4-фенилмасляная кислота, щавелевая кислота, малоновая кислота и винная кислота. Подходящие ароматические карбоновые кислоты включают в себя, например, такие кислоты как бензойная кислота, пара-хлорбензойная кислота, паранитробензойная кислота, пара-метоксибензойная кислота, пара-толуиловая кислота, о-толуиловая кислота, м-толуиловая кислота, нафтойная кислота, фталевая кислота и терефталевая кислота, салициловая кислота, гидрокоричная кислота. Предпочтительно, органическая кислота, применяемая для улучшения стереоселективности фермента, выбрана из н-пропионовой кислоты, изопропионовой кислоты, н-масляной кислоты, изомасляной кислоты, изовалериановой кислоты, 2-этилмасляной кислоты, кротоновой кислоты, пальмитиновой кислоты, циклогексанкарбоновой кислоты, триметилуксусной кислоты, бензойной кислоты и паратолуиловой кислоты, салициловой кислоты и 3-фенилпропионовой кислоты. Наиболее предпочтительно,если используемая карбоновая кислота представляет собой триметилуксусную кислоту. Количество используемой органической кислоты практически не ограничено, но молярное отношение к субстрату обычно составляет от 0,1 до 10, предпочтительно от 1,0 до 3,0 и более предпочтительно от 1,0 до 2,0. С другой стороны, для улучшения селективности фермента можно использовать органическое основание, либо отдельно, либо вместе с любой из вышеперечисленных органических кислот. В качестве подходящего органического основания может быть назван триэтиламин, пиридин и 4-диметиламинопиридин, и предпочтительным является пиридин. Подходящими комбинациями органической кислоты и органического основания являются, например, бензойная кислота и пиридин. Количество используемого органического основания практически не ограничено, но молярное отношение к субстрату обычно составляет от 0,5 до 3,0, и предпочтительно, от 0,5 до 2,0. Как указано выше, группа R означает циано или любую другую группу, которая может быть превращена в цианогруппу. Группы, которые могут быть превращены в цианогруппу, включают в себя галогены, такие как хлор, бром, йод или фтор, предпочтительно хлор или бром. Другие группы, которые могут быть превращены в циано, включают в себя CF3-(CF2)n-SO2-O-, где n принимает значения от 0 до 8, -ОН, -СНО, -СН 2 ОН, -CH2NH2, -CH2NO2, -CH2Cl, -CH2Br, -СН 3, -NHR5,-CHNOH, -COOR6, -CONR6R7, где R5 представляет собой водород или C1-6-алкилкарбонил, и R6 и R7 выбраны из водорода, необязательно замещенного C1-6-алкилом, арил-С 1-6-алкилом или арилом и группой,имеющей формулу где Z представляет собой О или S; каждый R8-R9 независимо выбран из водорода и C1-6-алкила, илиR8 и R9 вместе образуют цепь из С 2-5-алкилена, образуя, таким образом, спирокольцо; R10 выбран из водорода и C1-6-алкила, R11 выбран из водорода, С 1-6-алкила, карбоксигруппы или группы ее предшественника, или R10 и R11 вместе образуют цепь из С 2-5-алкилена, образуя, таким образом, спирокольцо. Когда R представляет собой галоген, в частности, бром или хлор, превращение в циано может быть проведено, как описано в патенте США 4136193, Международной заявке WO 00/13648, Международной заявке WO 00/11926 и Международной заявке WO 01/02383. Согласно патенту США 4136193, превращение группы брома в цианогруппу проводят в результате реакции с CuCN. В Международной заявке WO 00/13648 и Международной заявке WO 00/1192 6 описано превращение галогена или трифлатной группы в цианогруппу посредством цианирования с источником цианида и в присутствии катализатора Pd или Ni. Соединения, в которых группа R представляет собой группу формулы (VII), могут быть превращены в соответствующее цианосоединение с помощью способов, аналогичных описаным в Международной заявке WO 00/23431. Соединения, в которых R представляет собой ОН, -СН 2 ОН, -CH2NH2, -CH2NO2, -CH2Cl, -CH2Br,-СН 3 или любую из вышеназванных групп, могут быть превращены в соответствующие цианосоединения способами, аналогичными описанным в Международной заявке WO01/68632. Рацемические соединения формулы (II) могут быть получены посредством способов, описанных в вышеуказанных патентах или посредством способа алкилирования, описанного в патенте США 4136193 или с помощью способа двойной реакции Гриньяра, описанной в ЕР 171943, или аналогичными способами. Рацемические соединения формулы (IV) могут быть получены из соединений формулы (II) способом неселективного ацилирования с применением ангидридов, сложных эфиров, карбонатов, изоцианатов или изотиоцианатов, что определено выше формулами (IIIa), (IIIb), (IIIc), R1-N=C=O и R1N=C=S. В некоторых случаях рацемическое соединение формулы (II) может быть представлено в виде соли присоединения кислоты, такой как соль серной кислоты, и в этом случае свободное основание соединения формулы (II) может быть получено путем обработки соли основанием в смеси воды и органического растворителя для переноса соединения формулы (II) в органическую фазу. Предпочтительно R представляет собой циано. Если R не является циано, превращение группы R в цианогруппу соответствующим образом проводят после замыкания кольца, с образованием соединения формулы (V). Предпочтительно Hal представляет собой фтор. Если Hal не является фтором, превращение группыHal во фтор соответствующим образом проводят после замыкания кольца с образованием соединения формулы (V). Способ проведения данного превращения описан в Speciality Chemicals Magazine, апрель 2003, стр. 36-38.Z-группы, которые могут быть превращены в диметиламинометил, представляют собой такие группы как -CH2-L, -CH2-NO2, -MgHal, циано, альдегид, -CH2-O-Pg, -CH2-NPg1Pg2, -CH2-NMePg1,-CH2NHCH3, -CH2-NH2, -CO-N(CH3)2, -CH (A1R12)(A1R13), -(A1R14)(A2R15)(A3R16), -CCOR17, -CH2-CO-NH2,-CH=CH-R18 или -CONHR19, где Pg представляет собой защитную группу для группы спиртов, Pg1 и Pg2 представляют собой защитные группы для аминогрупп, R12 и R13 независимо выбраны из C1-6-алкила,С 2-6-алкенила, С 2-6-алкинила и необязательно алкила замещенного арильной или аралкильной группами,или R12 и R13 вместе образуют цепь из 2-4 атомов углерода, каждый из R14-R18 независимо выбран из C1-6 алкила, С 2-6-алкенила, C1-6-алкинила и необязательно C1-6-алкила, замещенного арилом или арил-С 1-6 алкилом, R19 представляет собой водород или метил, и А, А 2 и А 3 выбраны из О и S; L представляет собой удаляемую группу, такую как галоген или -O-SO2-A, где А представляет собой C1-6-алкил, С 2-6 алкенил, С 2-6-алкинил или необязательно C1-6-алкил, замещенный арилом или арил-С 1-6-алкилом. Спиртовая защитная группа Pg может представлять собой триалкилсилильную грушу, бензильную группу или тетрагидропиранильную группу (ТНР). Подходящими группами Pg1 и Pg2 являются аралкил или -SO2-R0-группы, где R0 представляет собой алкил, аралкил, арил или арил, замещенный алкилом, обычно метилом, бензилом или тозилом, или Pg1 иPg2, вместе с атомом N, к которому они присоединены, образуют необязательно замещенную фталимидную группу. Соединения, в которых Z представляет собой -СН 2-О-Pg, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так, как описано в Международных заявках WO 01/43525, WO 01/51478 или WO 01/68631, или аналогичными способами. Соединения, где Z представляет собой -CH2-L, где L представляет собой удаляемую группу, могут быть превращены в диметиламинометильную группу таким же способом. Соединения, где Z представляет собой -CO-N(CH3)2 и -CO-NHR19, где R19 представляет собой водород или метил, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так, как описано в Международных заявках WO 01/43525 или WO 01/68631, или аналогичными способами. Соединения, где Z представляет собой -CH2-NMe(Pg1) или -CH2-N(Pg1) (Pg2), могут быть превраще- 10012503 ны в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международных заявках WO 01/43525 или WO 01/68631, или аналогичными способами. Соединения, где Z представляет собой -CH(A1R12)(A2R13) могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международных заявках WO 01/43525 или WO 01/68631 или аналогичными способами. Соединения, где Z представляет собой -С(A1R14)(A2R15)(A3R16), могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международной заявке WO 01/68 631 или аналогичными способами. Соединения, где Z представляет собой -COOR17, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано выше, начиная со сложного эфира карбоновой кислоты. Соединения, где Z представляет собой -CH2-CONH2, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, как описано в Международной заявке WO 01/43525 или WO 01/68631 или аналогичными способами. Соединения, где Z представляет собой -CH=CHR18, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международных заявках WO 01/43525 или WO 01/68631 или аналогичными способами. Соединения, где Z представляет собой циано или -CH2-NO2, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международной заявке WO 01/68629 или аналогичными способами. Соединения, где Z представляет собой -MgHal, могут быть превращены в соответствующие соединения, где Z представляет собой диметиламинометил, так как описано в Международной заявке WO 01/68629, или аналогичными способами. Предпочтительно, Z представляет собой диметиламинометил. Если Z не является диметиламинометилом, превращение Z в диметиламинометильную группу соответствующим образом проводят после замыкания кольца. Соединения, где пунктирная линия представляет собой двойную связь, могут быть превращены в соответствующие соединения, где пунктирная линия представляет собой прямую связь, с помощью способов, описанных в Международной заявке WO 01/68630, или аналогичными способами. Предпочтительно, восстановление проводят после замыкания кольца. Эксперимент В следующих примерах % превращения и оптическую чистоту измеряли и рассчитывали, как описано ниже. Условия анализа HPLC (для определения степени превращения): Колонка: колонка Lichrospher RP-8, 2504 мм (размер частиц 5 мкм). Элюент: забуференный МеОН/вода получают следующим образом: 1,1 мл Et3N добавляют к 150 мл воды, 10% Н 3 РО 4 (водн.) доводят до рН=7 и добавляют воду до полного объема 200 мл. Смесь добавляют к 1,8 л МеОН. Температура:35 С. Скорость потока: 1 мл/мин. Давление: 16,0 Мпа. Детектирование: УФ 254 нм. Вводимый объем: 10 мкл. Скорость превращения (%) = P/(S+P)l00, (P: количество продукта, S: количество остаточного субстрата). Жидкостная хроматография высокого разрешения. Условия анализа (для оптической чистоты). Колонка: колонка Daicel AD с размерами 2504,6 мм (размер частиц 5 мкм). Подвижная фаза: диоксид углерода. Модификатор: метанол с диэтиламином (0,5%) и трифторуксусной кислотой (0,5%). Градиент модификатора: 1-2% за 4 мин 2-4% за 4 мин 4-8% за 4 мин 8-16% за 4 мин 16-32% за 4 мин 32-45% за 1,62 мин Температура: температура окружающей среды. Скорость потока: 2 мл/мин. Давление: 20 мПа. Детектирование: УФ 230 нм и 254 нм. Вводимый объем: 10 мкл.- 11012503 Оптическая чистота (% ее)= (А-В) /(А+В) 100, (А и В представляют собой соответствующий стереоизомер, АВ). Значение Е = ln1-c/100)(l-Es/100/ln1-c/100)(l+Es/100 (с: скорость превращения, Es: оптическая чистота остаточного субстрата). Пример 1. (S)-1-(3-Диметиламин(пропил)-1-(4-фторфенил)-1,3-дигидроизобензофуран-5-карбонитрил гидрооксалат. К смеси 3,7 г 4-[(S)-4-диметиламино-1-(4'-фторфенил)-1-гидроксибутил]-3-гидроксиметилбензонитрила и 6,3 г эфира 5-циано-2-[4-диметиламино-1-(4-фторфенил)-1-гидроксибутил]-бензилмасляной кислоты (R/S = 3:1) в 50 мл тетрагидрофурана добавляли 1,2 г (1,1 экв.) янтарного ангидрида. Оставляли на ночь при комнатной температуре при постоянном перемешивании. Выпадающий в осадок эфир моно 5-циано-2-[(S)-4-диметиламино-1-(4-фторфенил)-1-гидроксибутил]бензилянтарной кислоты фильтровали и промывали холодным тетрагидрофураном, с получением 3,1 г сложного эфира 98% чистоты. Кристаллы сушили в сушильном шкафу и затем растворяли в 50 мл обезвоженного диметилформамида. К раствору добавляли 1,1 г NaH (60% суспензия в масле) и встряхивали в течение ночи при комнатной температуре. Смесь гасили водой и экстрагировали 3 раза 50 мл диэтилэфира. Объединенные органические фазы промывали 50 мл воды и сушили Na2SO4, и выпаривали в вакууме. Оставшееся масло растворяли в 14 мл ацетона, и добавляли 630 мг щавелевой кислоты. После встряхивания в течение 1 ч при комнатной температуре осажденные кристаллы фильтровали и промывали холодным ацетоном, получая 2,02 г эсциталопрама гидрооксалата (значение ее соответствует 95%). Пример 2. (Получение смеси, используемой в примере 1).(S)-4-[4-Диметиламино-1-(4'-фторфенил)-1-гидроксибутил]-3-гидроксиметилбензонитрил. К встряхиваемому раствору рацемического 4-[4-диметиламино-1-(4-фторфенил)-1-гидроксибутил]3-гидроксиметилбензонитрила (29 ммоль, 10 г) и винилбутирата (58 ммоль, 7,5 мл) в безводном 1,4 диоксане (142,5 мл) добавляли липопротеинлипазу pseudomonas sp. (160 Ед., 250 мг). Реакционную смесь подогревали до 50 С, с последующим HPLC. Через 192 ч, после 41% превращения, дополнительно добавляли 250 мг липазы. Через 504 ч, после 63% превращения, реакцию останавливали. Фермент фильтровали и промывали в небольшом количестве 1,4-диоксана. Объединенные органические фазы выпаривали в вакууме и затем анализировали методом жидкостной хроматографии высокого разрешения. Полученное значение ее S-диол)=95% (S-диол/R-диол=40 :1). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ выделения и очистки соединения, имеющего формулу где R представляет собой циано или группу, которая может быть превращена в цианогруппу, где такая группа выбрана из хлора, брома, йода, фтора, CF3-(CF2)n-SO2-O-, где n принимает значения от 0 до 8, -ОН, -СНО, -СН 2 ОН, -CH2NH2, -CH2NO2, -CH2Cl, -CH2Br, -СН 3, -NHR5, -CHNOH, -COOR6, -CONR6R7,где R5 представляет собой водород или C1-6-алкилкарбонил и R6 и R7 выбраны из водорода, необязательно замещенного C1-6-алкила и группы, имеющей формулу (VII) где Z в формуле (VII) представляет собой О или S; каждый R8 и R9 независимо выбраны из водорода и C1-6-алкила, или R8 и R9 вместе образуют цепь из С 2-5-алкилена, образуя таким образом спирокольцо;R10 выбран из водорода и C1-6-алкила, R11 выбран из водорода, C1-6-алкила, карбоксигруппы или группы ее предшественников, или R10 и R11 вместе образуют цепь из С 2-5-алкилена, образуя, таким образом, спирокольцо, пунктирная линия представляет собой двойную или прямую связь, Hal представляет собой галоген,где Z в формуле (IV) представляет собой диметиламинометильную группу или группу, которая может быть превращена в диметиламинометильную группу, где такая группа выбрана из -CH2-L, -CH2-NO2,-MgHal, циано, альдегид, -CH2-O-Pg, -CH2-N(Pg1)(Pg2), -CH2-NMe(Pg1), -CH2-NHCH3, -CH2-NH2, -CON(CH3)2, -CH(A1RI2)(A1R13), -C(A1R14)(A2R15)(A3R16), -COOR17, -CH2-CONH2, -CH=CH-R18OR-CONHR19,где Pg - защитная группа для спиртовой группы, Pg1 и Pg2 являются защитными группами для аминогруппы, R12 и R13 независимо выбраны из C1-6-алкила, С 2-6-алкенила, С 2-6-алкинила, или R12 и R13 вместе- 12012503 образуют цепь из 2-4 атомов углерода, каждый из Rl4-R18 независимо выбран из C1-6-алкила, С 1-6 алкенила и C1-6-алкинила, R19 является водородом или метилом, и А 1, А 2 или А 3 выбраны из О и S; L представляет собой удаляемую группу, такую как галоген или -O-SO2-A-, где А представляет собой C1-6 алкил, С 2-6-алкенил и С 2-6-алкинил,W представляет собой О или S, Y представляет собой связь, О, S или NH, и R1 представляет собой С 1-10-алкил, С 2-10-алкенил или С 2-10-алкинил, все из которых необязательно могут быть замещены одним или более заместителями, выбранными из С 1-10-алкокси, С 1-10-алкилтио, гидрокси, галогена, амино, нитро, циано, С 1-10-алкиламино и ди-(С 1-10-алкил)амино, или его соли, и/или диола формулы (II) где R, Z, Hal и пунктирная линия определены выше, или его соли,из смеси, содержащей соединение формулы (IV) и диол формулы (II), включающий: а) введение смеси, содержащей соединение формулы (IV) и диол формулы (II), в реакцию с циклическим ангидридом или имидом формулы где X представляет собой -(CHR'")n-, где n принимает значения 0-2; и R', R" и R'" независимо выбраны из водорода, C1-6-алкила, C1-6-алкокси, C1-6-ацилокси, или R' и R" в ангидриде формулы (Ia) вместе представляют собой -O-CR4R5-O-, где R4 и R5 независимо представляют собой водород или C1-6-алкил, или R' и R" в ангидриде формулы (Ib) являются смежными и вместе с двумя атомами углерода, к которым они присоединены, образуют бензольное кольцо; один из Q1 и Q2 представляет собой азот, а другой - углерод, или оба они представляют собой углерод; А представляет собой C1-6-алкилен, фенилен или нафтилен, где C1-6-алкиленовая, фениленовая или нафтиленовая группы необязательно могут быть замещены один или более раз C1-6-алкилом; с образованием смеси соединения формулы (IV) и сложного эфира формулы (V)b) отделение соединения формулы (IV) от сложного эфира формулы (V) способом, выбранным из группы, состоящей изiv) способа, согласно которому позволяют кислоте формулы (V) или ее соли выпасть в осадок из реакционной смеси и отделяют осадок соединения формулы (V) или его соли от реакционной смеси, необязательно, с последующим выделением соединения формулы (IV) или его соли из реакционной смеси;v) способа распределения между органическим растворителем и водным растворителем, посредством которого соединение формулы (IV) будет растворено в органической фазе, тогда как соединение формулы (V) будет растворено в водной фазе, разделения фаз и, необязательно, выделения соединения формулы (IV) или его соли и/или выделения соединения формулы (V) или его соли; иvi) способа адсорбции соединения формулы (V) на основе из смолы, отделения растворителя, содержащего соединение формулы (IV), от смолы, десорбции соединения формулы (V) от смоляной основы и, необязательно, выделения соединения формулы (IV) или его соли и/или выделения соединения- 13012503 формулы (V) или его соли. 2. Способ по п.1, где разделение соединения формулы (IV) и сложного эфира формулы (V) производят, позволяя кислоте формулы (V) выпасть в осадок из реакционной смеси, и разделение выпавшего осадка соединения формулы (V) и реакционной смеси производят, необязательно, с последующим выделением соединения формулы (IV) или его соли из реакционной смеси. 3. Способ по любому из пп.1 или 2, где R', R" и R"' независимо выбраны из водорода и C1-6-алкила, aQ1 и Q2 оба представляют собой углерод. 4. Способ по любому из пп.1-3, где S-энантиомер соединения формулы (V) или смесь энантиомеров соединения формулы (V), содержащая более чем 50% S-энантиомера соединения формулы (V), отделяли от R-энантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы(IV). 5. Способ по п.4, согласно которому S-энантиомер соединения формулы (V) отделяют от Rэнантиомера ацильного производного формулы (IV) или от смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% R-энантиомера ацильного производного формулы (IV). 6. Способ по п.5, где S-энантиомер соединения формулы (V) отделяют от R-энантиомера ацильного производного формулы (IV). 7. Способ по любому из пп.1-3, согласно которому S-энантиомер ацильного производного формулы(IV) или смеси энантиомеров ацильного производного формулы (IV), содержащей более чем 50% Sэнантиомера ацильного производного формулы (IV), отделяют от R-энантиомера соединения формулы(V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V). 8. Способ по п.7, согласно которому S-энантиомер ацильного производного формулы (IV) отделяют от R-энантиомера соединения формулы (V) или от смеси энантиомеров соединения формулы (V), содержащей более чем 50% R-энантиомера соединения формулы (V). 9. Способ по п.8, согласно которому S-энантиомер ацильного производного формулы (IV) отделяют от R-энантиомера соединения формулы (V). 10. Способ по любому из пп.4-6, согласно которому R-группа в соединении формулы (V), полученная в виде S-энантиомера, необязательно превращается в циано, полученная Z-группа в соединении формулы V необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно, превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы (V) в эсциталопрам или его производное, имеющее формулу где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно, с последующим превращением эсциталопрама или производного формулы (VI) в их соль. 11. Способ по любому из пп.7-9, согласно которому R-группа в соединении формулы (IV), полученном в виде S-энантиомера, необязательно превращается в циано, Z-группа в полученном соединении формулы (IV) необязательно превращается в диметиламинометильную группу, Hal необязательно превращается во фтор и/или пунктирная линия, представляющая собой двойную связь, необязательно превращается в прямую связь, в любом порядке; с последующим превращением соединения формулы (IV) в эсциталопрам или его производное где R, Z и Hal представляют собой то же, что и определено выше, посредством обработки основанием, необязательно с последующим, в любом порядке, превращением группы R в цианогруппу, превращением группы Z в диметиламинометильную группу, превращением Hal во фтор и превращением пунктирной линии, представляющей собой двойную связь, в прямую связь; необязательно с последующим превращением эсциталопрама или производного формулы (VI) в их соль.- 14012503 12. Способ по любому из пп.10 или 11, где замыкание кольца в основных условиях проводили при обработке основанием таким как KOC(CH3)3 или другими алкоголятами, NaH или другими гидридами,или аминами, такими как триэтиламин, этилдиизопропиламин или пиридин. 13. Способ по любому из пп.1-12, где Hal представляет собой фтор, a R представляет собой галоген или циано, предпочтительно R представляет собой циано. 14. Способ по любому из пп.1-13, где пунктирная линия представляет собой прямую связь. 15. Способ по любому из пп.1-14, где Z представляет собой диметиламинометил. 16. Способ по пп.1-15, где ангидрид представляет собой соединение, имеющее формулу (Ia). 17. Способ по п.16, где ангидрид представляет собой янтарный ангидрид или глутаровый ангидрид. 18. Способ по пп.1-17, где ангидрид представляет собой соединение, имеющее формулу (Ib). 19. Способ по п.18, где ангидрид представляет собой ангидрид фталевой кислоты. 20. Способ по пп.1-15, где реагент представляет собой имид, имеющий формулу (Ic). 21. Способ по п.20, где имид представляет собой N-фенилсукцинимид, замещенный в фенильном кольце карбоксигруппой. 22. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой связь. 23. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой О или S. 24. Способ по п.23, где Y в соединении формулы (IV) представляет собой О. 25. Способ по любому из пп.1-21, где Y в соединении формулы (IV) представляет собой NH. 26. Способ по любому из пп.22-25, где R1 выбран из C1-4-алкила, С 2-4-алкенила и С 2-4-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из С 1-4 алкокси, C1-4-алкилтио, гидрокси, галогена, амино, нитро, циано, С 1-4-алкиламино и ди-(С 1-4-алкил)амино. 27. Способ по п.26, где R1 выбран из C1-3-алкила, С 2-3-алкенила и С 2-3-алкинила, все из которых необязательно могут быть замещены один или более раз заместителями, выбранными из C1-3-алкокси, C1-3 алкилтио, гидрокси, галогена, амино, нитро, циано, C1-3-алкиламино и ди-(С 1-3-алкил)амино. 28. Способ по п.26, где R1 представляет собой С 1-4-алкил. 29. Способ по п.27, где R1 представляет собой C1-3-алкил. 30. Способ по п.29, где R1 представляет собой метил, этил или пропил, предпочтительно пропил. 31.Способ по любому из пп.1-30, где смесь соединений формулы (II) и формулы (IV) получают посредством селективного энзиматического ацилирования или селективного энзиматического деацилирования.
МПК / Метки
МПК: C07C 255/59, C07D 307/87, C07C 253/30, C07C 253/34
Метки: быть, соединений, получения, эсциталопрама, может, отделения, промежуточных, способ, использован
Код ссылки
<a href="https://eas.patents.su/16-12503-sposob-otdeleniya-promezhutochnyh-soedinenijj-kotoryjj-mozhet-byt-ispolzovan-dlya-polucheniya-escitaloprama.html" rel="bookmark" title="База патентов Евразийского Союза">Способ отделения промежуточных соединений, который может быть использован для получения эсциталопрама</a>
Предыдущий патент: Соединения, специфичные к меланокортиновым рецепторам
Случайный патент: Ингалятор для вдыхания лекарственных веществ и способ сборки ингалятора




















