Производные тетрагидрофуро[2,3-c]пиридина, способ их получения и применение в качестве ингибиторов металлопротеазы
Номер патента: 2527
Опубликовано: 27.06.2002
Авторы: Бонне Жаклин, Атасси Ганем, Сабатини Массимо, Пьер Ален, Де Нантей Гийом, Бенуа Ален
Формула / Реферат
1. Соединения формулы (I)
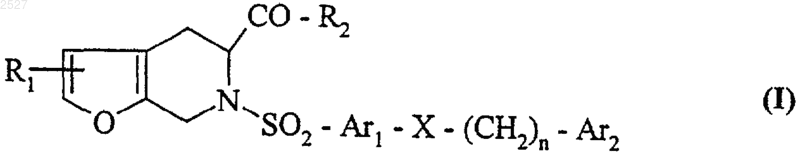
где R1 - атом водорода или галогена, либо линейный или разветвленный (C1-С6)алкил, либо линейная или разветвленная (C1-C6)алкоксигруппа,
R2 - гидрокси, линейная или разветвленная (C1-C6)алкокси или -NHОН-группа,
Ar1 - фениленовая или бифениленовая группа,
Х - атом кислорода или серы, NR-группа, -Сº С-группа или связь,
R - атом водорода, либо линейная или разветвленная (C1-С6)алкильная группа,
n - целое число от 0 до 6, включительно,
Аr2:
- фенильная группа, замещенная гетероарильной группой,
- бифенильная группа, замещенная гетероарильной группой,
- пиридинильная группа, замещенная гетероарильной группой, или
- гетероциклическая группа,
их изомеры и соли присоединения фармацевтически приемлемой кислоты или основания, при этом
- под "гетероарильной группой" подразумевается моноциклическая ароматическая группа или бициклическая ароматическая группа, в которой, по крайней мере, один цикл является ароматическим, содержащим один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенным одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-С6)алкила, линейного или разветвленного (C1-С6)алкоксила, линейного или разветвленного тригало-(C1-С6)алкила, линейного или разветвленного тригало-(C1-C6)алкоксила и гидроксила;
- под "гетероциклической группой" подразумевается насыщенная или частично насыщенная моно- или бициклическая неароматическая группа, содержащая один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенная одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-С6)алкила, линейного или разветвленного (C1-С6)алкоксила, линейного или разветвленного тригало-(C1-С6)алкила, линейного или разветвленного тригало-(C1-С6)алкоксила и гидроксила.
2. Соединения формулы (I) по п.1, отличающиеся тем, что Х - атом кислорода или серы.
3. Соединения формулы (I) по любому из пп.1 или 2, отличающиеся тем, что R2 - -NHОН-группа.
4. Соединения формулы (I) по любому из пп.1, 2 и 3, отличающиеся тем, что Ar1 - фениленовая группа, а n = 0.
5. Соединения формулы (I) по п.4, отличающиеся тем, что Ar2 - фенильная группа, замещенная гетероарильной группой.
6. Соединения формулы (I) по п.5, отличающиеся тем, что Ar2 - фенильная группа, замещенная группой, выбранной из имидазолила, триазолила и пиридинила.
7. Соединения формулы (I) по любому из пп.1-6, отличающиеся тем, что Х - атом кислорода или серы, R2 - -NHOH-группа, Ar1 - фениленовая группа, n = 0, а Аr2 - фенильная группа, замещенная группой, выбранной из имидазолила, триазолила и пиридинила.
8. Соединения формулы (I) по любому из пп.1, 2 и 3, отличающиеся тем, что Ar1 - бифениленовая группа, а Аr2 - гетероциклическая группа.
9. Соединение формулы (I) по п.1, представляющее собой 6-{4-[4-(имидазол-1-ил)фенокси]бензолсульфонил}-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения фармацевтически приемлемой кислоты или основания.
10. Соединение формулы (I) по п.1, представляющее собой 6-{4'-[2-(пирролидин-1-ил) этокси]бифенил-4-сульфонил}-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид гидрохлорид, а также его соли присоединения фармацевтически приемлемой кислоты или основания.
11. Соединение формулы (I) по п.1, представляющее собой 6-{4-[4-(1,3,4-триазол-1-ил) фенокси]бензолсульфонил}-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения с фармацевтически приемлемой кислотой или основанием.
12. Соединение формулы (I) по п.1, представляющее собой 6-{4-[4-(пиридин-4-ил)фенокси]бензолсульфонил}-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения фармацевтически приемлемой кислоты или основания.
13. Соединение формулы (I) по п.1, представляющее собой 6-{4-[4-(1,3,4-триазол-1-ил) фенилтио]бензолсульфонил}-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения фармацевтически приемлемой кислоты или основания.
14. Способ получения соединений формулы (I) по п.1, отличающийся тем, что в качестве исходного материала используют соединение формулы (II) в рацемическом виде или в виде конкретного изомера
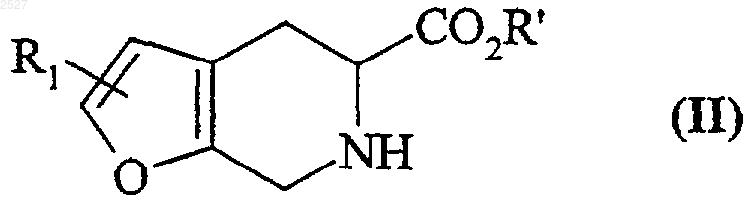
где R1 имеет такие же значения, как и в формуле (I), a R' - атом водорода либо линейная или разветвленная (C1-С6)алкильная группа, которое замещают по аминогруппе галогенсодержащим соединением формулы (III)
СlSO2-Аr1-Х-(СН2)n-Аr2 (III)
где Ar1, X, n и Аr2 имеют такие же значения, как и в формуле (I), с получением
- когда R' - атом водорода, соединения формулы (I/a), представляющего частный случай соединений формулы (I)
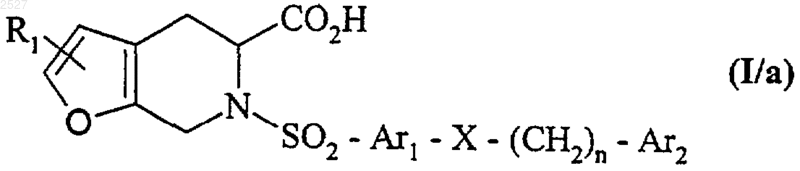
где R1, Ar1, X, N и Аr2 имеют вышеуказанные значения,
- либо, когда R' - линейная или разветвленная (C1-С6)алкильная группа (R"), соединение формулы (I/a1), представляющие частный случай соединений формулы (I)

где R1, Ar1, X, n, Ar2 и R" имеют вышеуказанные значения, которое может быть подвергнуто воздействию кислоты с получением вышеописанного соединения формулы (I/a),
*при этом соединение формулы (I/a)
при желании, подвергают воздействию O-замещенного гидроксиламина, получая, после снятия защиты с функции гидроксиламина, соединение формулы (I/b)
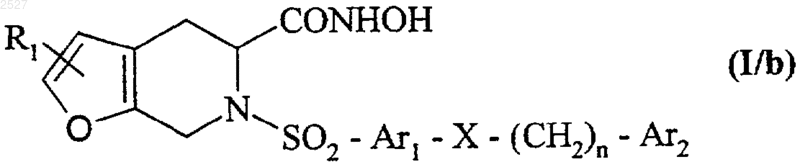
где R1, Ar1, X, n, и Ar2 имеют вышеуказанные значения;
*при этом соединения формул (I/a), (I/a1) и (I/b) составляют всю совокупность соединений формулы (I),
которые при необходимости очищают в соответствии с известными способами очистки, при необходимости разделяют на изомеры в соответствии с известными способами разделения и при желании превращают в соли присоединения фармацевтически приемлемой кислоты или основания.
15. Фармацевтическая композиция, включающая в качестве активного ингредиента соединение по любому из пп.1-13 в сочетании с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми эксципиентами или носителями.
16. Фармацевтическая композиция по п.15, включающая в качестве активного ингредиента соединение по любому из пп.1-13, применяемое в качестве ингибиторов металлопротеаз.
Текст
1 Настоящее изобретение относится к новым ингибиторам металлопротеазы, способу их получения и к содержащим их фармацевтическим композициям. В физиологическом состоянии синтез соединительных тканей находится в динамическом равновесии с распадом внеклеточного матрикса. Этот распад происходит благодаря протеазам цинка (металлопротеазы), выделяемым клетками существующего матрикса: они,не предполагая каких-либо ограничений, представляют собой коллагеназы (ММР-1, ММР-8,ММР-13), желатиназы или коллагеназы типа 1 У(ММР-2, ММР-9) и стромелизины (ММР-3). В нормальном состоянии эти катаболические ферменты регулируются, исходя из их синтеза и секреции, а также, исходя из их внеклеточной ферментативной активности, природными ингибиторами, такими как 2-макроглобулин или тканевые ингибиторы металлопротеиназ(ТIMP), образующими неактивные комплексы с металлопротеазами. Общим признаком патологий, в которых участвуют эти ферменты, является дисбаланс между активностью активированных ферментов и активностью их природных ингибиторов, последствием которого является избыточный распад ткани. Неконтролируемый и ускоренный распад мембран в результате резорбции внеклеточной матрицы, катализируемой металлопротеазами,является параметром, общим для многих патологических состояний, таких как ревматоидный артрит, артроз, инвазия и рост опухоли, включая злокачественное распространение и образование метастаз, образование язв, атеросклероз и т.д. Недавно было обнаружено, что ВВ 94, ингибитор металлопротеазы, проявляет противоопухолевую активность при клиническом применении, где он продемонстрировал свою активность против различных видов рака яичника(Becket et al., DDT 1996, 1 (1), (16. Поэтому можно ожидать, что ингибитор металлопротеазы способен восстанавливать равновесие между протеазой и ингибитором и таким образом положительно изменять развитие этих патологий. Определенное количество ингибиторов металлопротеазы было описано в литературе. Особенно следует отметить соединения, раскрытые в WO 95/35275, WO 95/35276, ЕР 606 046, WO 96/00214 и ЕР 803 505. Соединения в соответствии с данным изобретением не только новы, но они также оказались более сильными ингибиторами металлопротеазы, чем ингибиторы, описанные в литературе, что делает их потенциально применимыми при лечении рака, ревматических заболеваний,таких как артроз и ревматоидный артрит, атеросклероз и т.д. Более конкретно, данное изобретение относится к соединениям формулы (I)R1 - атом водорода или галогена, либо линейный или разветвленный (C1-С 6) алкил, либо линейная или разветвленная (C1-C6) алкоксигруппа,R2 - гидрокси, линейная или разветвленная(C1-C6) алкокси или -NHOH-группа,Ar1 - фениленовая или бифениленовая группа,Х - атом кислорода или серы, NR-группа,СС- группа или простая связь,R - атом водорода либо линейная или разветвленная (C1-C6) алкильная группа,n - целое число от 0 до 6, включительно,Аr2: фенильная группа, замещенная гетероарильной группой,бифенильная группа, замещенная гетероарильной группой,пиридинильная группа, замещенная гетероарильной группой, или гетероциклическая группа,их изомерам и солям присоединения фармацевтически приемлемой кислоты или основания,при этом: под "гетероарильной группой" подразумевается моноциклическая ароматическая группа или бициклическая ароматическая группа, в которой, по крайней мере, один цикл является ароматическим, содержащим один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенным одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-С 6) алкила, линейного или разветвленного (C1-С 6)алкоксила, линейного или разветвленного тригало-(C1-C6) алкила, линейного или разветвленного тригало-(C1-С 6) алкоксила и гидроксила,под гетероциклической группой подразумевается насыщенная или частично насыщенная моно- или бициклическая неароматическая группа, содержащая один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенная одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-C6) алкила, линейного или разветвленного (C1-С 6) алкоксила, линейного или разветвленного тригало-(C1-C6) алкила, линейного или разветвленного тригало-(C1-C6)алкоксила и гидроксида. Среди фармацевтически приемлемых кислот могут быть упомянуты, в качестве неограничивающего примера, хлористо-водородная,бромисто-водородная, серная, фосфоновая, уксусная, трифторуксусная, молочная, пировиноградная, малоновая, янтарная, глутаровая, фу 3 маровая, винная, малеиновая, лимонная, аскорбиновая, щавелевая, метансульфоновая, камфарная кислота и т.д. Среди фармацевтически приемлемых оснований могут быть упомянуты, в качестве неограничивающего примера, гидроокись натрия,гидроокись калия, триэтиламин, трет-бутиламин и т.д. Предпочтительными гетероарильными группами являются имидазолил-, тиазолил-,оксазолил-, пирролил-, пиридил-, пиримидил-,триазолил-, пиразолил- и бензимидазолилгруппы. Предпочтительными гетероциклическими группами являются пирролидинил-, морфолино-,пиперидино-, имидазолидинил-, тиазолидинил-,оксазолидинил-, пиперазинил-, изоиндолил-,2,3-дигидроизоиндолил- и циклопента[с]пирролидинилгруппы. Предпочтительными соединениями в соответствии с данным изобретением являются соединения формулы (I), где Х - атом кислорода или серы. Предпочтительная R1-группа представляет собой атом водорода. Предпочтительная R2-группа представляет собой -NHOH-группу. Когда Ar1 - фениленовая группа, то n предпочтительно равен нулю. Когда Ar1 - фениленовая группа, то Аr2 предпочтительно фенильная группа, замещенная гетероарильной группой, предпочтительно,представляющей собой имидазолил-, триазолилили пиридинилгруппу. Более конкретно, предпочтительные соединения в соответствии с данным изобретением представляют собой соединения формулы (I),где Ar1 - фениленовая группа, Х - атом кислорода или серы, n = О, a Ar2 - фенильная группа,замещенная гетероарильной группой, выбранной из имидазолила, триазолила и пиридинила. Когда Ar1 - бифениленовая группа, то Аr2,предпочтительно гетероциклическая группа. 4,5,6,7-Тетрагидрофуро[2,3-с]пиридиновое кольцо предпочтительно имеет конфигурацию-6-4-[4-(имидазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид и его соответствующие соли присоединения,-6-4'-[2-(пирролидин-1-ил)этокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с] пиридин-(5R)-(N-гидрокси)карбоксамид и его соответствующие соли присоединения,-6-4-[4-(1,3,4-триазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с] пиридин-(5R)-(N-гидрокси)карбоксамид и его соответствующие соли присоединения,-6-4-[4-(пиридин-4-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пири 002527 4 дин-(5R)-(N-гидрокси)карбоксамид и его соответствующие соли присоединения,-6-4-[4-(1,3,4-триазол-1-ил)фенилтио] бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3 с]пиридин-(5R)-(N-гидрокси)карбоксамид и его соответствующие соли присоединения. Данное изобретение также относится к способу получения соединений формулы (I),отличающемуся тем, что в качестве исходного материала используют соединение формулы (II) в рацемическом виде или в виде конкретного изомера: где R1 имеет такие же значения, как и в формуле(I), a R' - атом водорода, либо линейная или разветвленная (C1-С 6) алкильная группа, которое замещается по аминогруппе галогенсодержащим соединением формулы (III)(III) где Ar1, X, n и Аr2 имеют такие же значения, как и в формуле (I), с получением:- когда R' - атом водорода, соединения формулы (I/a), являющегося частным случаем соединений формулы (I) где R1, Ar1, X, N и Аr2 имеют вышеуказанные значения,- либо, когда R' - линейная или разветвленная (C1-C6) алкильная группа (R"), соединение формулы (I/a1) также представляющего частичный случай соединений формулы (I) где R1, Ar1, X, n, Аr2 и R имеют вышеуказанные значения,которое может быть подвергнуто воздействию кислоты для получения вышеописанного соединения формулы (I/a),при этом соединение формулы (I/a): при желании, подвергают действию Озамещенного гидроксиламина, получая, после снятия защиты с функции гидроксиламина, соединение формулы (I/b) где R1, Ar1, X, n и Аr2 имеют вышеуказанные значения; при этом соединения формул (I/a), (I/a1) и(I/b) составляют всю совокупность соединений формулы (I),которые, при необходимости очищают в соответствии с известными способами очистки,при необходимости разделяют на изомеры в соответствии с известными способами разделения и при желании превращают в соли присое 5 динения фармацевтически приемлемой кислоты или основания. Соединения формул (II) и (III) либо являются готовыми промышленными продуктами,либо их получают в соответствии с известными процедурами. Данное изобретение также относится к фармацевтическим композициям, включающим в качестве активного ингредиента одно соединение формулы (I) с одним или несколькими подходящими инертными, нетоксичными эксципиентами. Среди фармацевтических композиций в соответствии с данным изобретением более конкретно могут быть упомянуты композиции, подходящие для перорального, парентерального (внутривенного или подкожного) либо назального введения, таблетки или драже, подъязычные таблетки, желатиновые капсулы, пастилки, суппозитории, кремы, мази, гели для кожи, препараты для инъекций, суспензии для питья и т.д. Необходимая доза может быть подобрана в соответствии с природой и тяжестью расстройства, способом введения, возрастом и весом пациента, и может варьироваться от 0,01 до 2 г в сутки за один или несколько приемов. Следующие примеры иллюстрируют данное изобретение, но никоим образом не ограничивают его. Применяемые исходные материалы являются известными соединениями либо их получают в соответствии с известными процедурами. Препаративные примеры описывают синтез промежуточных соединений, применяемых при получении соединений в соответствии с данным изобретением. Структуры соединений, описанных в примерах и препаративных примерах, определяют в соответствии с обычными спектрофотометрическими способами (инфракрасный,ЯМР, масс-спектрометрии и т.д.). Препаративный пример А. Хлорангидрид 4-[4-(имидазол-1-ил)фенокси]-бензолсульфокислоты. Стадия А. 4-[4-(Имидазол-1-ил)фенокси] бензолсульфокислота. 137 ммол 1-(4-феноксифенил)имидазола растворяют в 250 мл хлороформа. Затем по каплям добавляют 190 ммол хлорсульфоновой кислоты. Смесь оставляют на ночь при 45 С. После охлаждения и удаления растворителя выпариванием полученное масло поглощают диэтиловым эфиром. Полученное твердое вещество отфильтровывают и сушат, получая ожидаемый продукт. Температура плавления: 80 С. Стадия В. Хлорангидрид 4-[4-(имидазол-1 ил)фенокси]-бензосульфокислоты. 80 ммол продукта, описанного на предыдущей стадии, и 90 ммол PCl5 помещают в 100 мл РОСl3. Суспензию нагревают при дефлегма 002527 6 ции в течение 3 ч. После охлаждения масляный остаток промывают эфиром, а затем поглощают ацетонитрилом. Полученный осадок отфильтровывают и промывают изопропиловым эфиром,получая целевое соединение. Температура плавления: 170 С. Препаративный пример В. Хлорангидрид 4'-[2-(пирролидин-1-ил)этокси]бифенил-4 сульфокислоты. Стадия А. 1-[2-(Бифенокси)этил]пирролидин. 1,76 мол 4-гидроксибифенила, 2,29 мол 1(2-хлорэтил)пирролидина и 5,3 мол карбоната калия помещают в 2,5 л диметилформамида. Смесь нагревают при 50 С в течение ночи. После охлаждения твердое вещество отфильтровывают и растворитель удаляют выпариванием. Остаток поглощают этилацетатом. После промывания органической фазы, сушки и выпаривания, получают остаток, который очищают хроматографией на двуокиси кремния, применяя смесь этилацетата/этанола (80/20) в качестве элюента. Ожидаемый продукт получают после кристаллизации остаточного масла. Стадия В. 4'-[2-(Пирролидин-1-ил)этокси] бифенил-4-сульфокислота. Ожидаемый продукт получают в соответствии со способом, описанным на стадии В препаративного примера А, используя в качестве исходного продукт, описанный на стадии А. Стадия С. Хлорангидрид 4'-[2-(пирролидин-1-ил)этокси]бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным на стадии С препаративного примера А, исходя из соединения,описанного на стадии В, поддерживая температуру кипения с обратным холодильником в течение 9 ч и отфильтровывая образующийся осадок. Температура плавления: 234 С. Препаративный пример С. Хлорангидрид 4'-[(пиридин-4-ил)фенокси]бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 4-(4-хлорфенил)пиридин вместо 1-(2-хлорэтил)пирролидина. Препаративный пример D. Хлорангидрид 4'-[(2-морфолино)этокси]бифенилсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 4-(2 хлорэтил)морфолин вместо 1-(2-хлорэтил)пирролидина. Препаративный пример Е. Хлорангидрид 4'-[(2-пиперидино)этокси]бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 1-(2-хлор 7 этил)пиперидин вместо 1-(2-хлорэтил)пирролидина. Препаративный пример F. Хлорангидрид 4'-(имидазол-1-ил)бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя имидазол вместо 1-(2-хлорэтил)пирролидина и 4-бромбифенил вместо 4-гидроксибифенила. Препаративный пример G. Хлорангидрид 4'-[2-(пергидроазепин-1-ил)этокси]бифенил-4 сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 1-(2 хлорэтил)пергидроазепин вместо 1-(2-хлорэтил) пирролидина. Препаративный пример Н. Хлорангидрид 4'-[3-(пирролидин-1-ил)пропокси]бифенил-4 сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 1-(3 хлорпропил)пирролидин вместо 1-(2 хлорэтил)пирролидина. Препаративный пример I. Хлорангидрид 4'-[2-(1,3-дигидроизоиндол-2-ил)этокси]бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 2-(2 хлорэтил)-1,3-дигидроизоиндол вместо 1-(2 хлорэтил)пирролидина. Препаративный пример J. Хлорангидрид 4'-[2-(циклопента[с]пирролидин-2-ил)этокси] бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 2-(2 хлорэтил)циклопента[c]пирролидин вместо 1(2-хлорэтил)пирролидина. Препаративный пример К. Хлорангидрид 4'-(пирролидин-1-ил)бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя пирролидин вместо 1-(2-хлорэтил)пирролидина и 4-бромбифенил вместо 4-гидроксибифенила. Препаративный пример L. Хлорангидрид 4'-(пиперидино)бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя пиперидин вместо 1-(2-хлорэтил)пирролидина и 4 бромбифенил вместо 4-гидроксибифенила. Препаративный пример М. Хлорангидрид 4'-(морфолино)бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя морфолин вместо 1-(2-хлорэтил)пирролидина и 4 бромбифенил вместо 4-гидроксибифенила. 8 Препаративный пример N. Хлорангидрид 4'-(циклопента[с]-пирролидин-2-ил)бифенил-4 сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя циклопента[с]пирролидин вместо 1-(2-хлорэтил)пирролидина и 4-бромбифенил вместо 4-гидроксибифенила. Препаративный пример О. Хлорангидрид 4'-[2-(пергидроазепин-1-ил)этокси]бифенил-4 сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 1,3 дигидроизоиндол вместо 1-(2-хлорэтил)пирролидина и 4-бромбифенил вместо 4-гидроксибифенила. Препаративный пример Р. Хлорангидрид 4-[4-(1,3,4-триазол-1-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4-феноксифенил)-1,3,4-триазол вместо 1-(4-феноксифенил)имидазола. Препаративный пример Q. Хлорангидрид 4-[4-(1,2,4-триазол-1-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4 феноксифенил)-1,2,4-триазол вместо 1-(4 феноксифенил)имидазола. Препаративный пример R. Хлорангидрид 4-[4-(пиррол-1-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4-феноксифенил)пиррол вместо 1-(4-феноксифенил) имидазола. Препаративный пример S. Хлорангидрид 4-[4-(пиразол-1-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4 феноксифенил)пиразол вместо 1-(4-феноксифенил)имидазола. Препаративный пример Т. Хлорангидрид 4-[4-(имидазол-2-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 2-(4-феноксифенил)имидазол вместо 1-(4-феноксифенил) имидазола. Препаративный пример U. Хлорангидрид 4-[4-(бензимидазол-1-ил)фенокси]бензолсульфокислоты. 9 Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4-феноксифенил)бензимидазол вместо 1-(4-феноксифенил)имидазола. Препаративный пример V. Хлорангидрид 4-[4-(пиридин-4-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 4-(4-феноксифенил)пиридин вместо 1-(4-феноксифенил) имидазола. Препаративный пример W. Хлорангидрид 4-[4-(пиримидин-5-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 5-(4-феноксифенил)пиримидин вместо 1-(4-феноксифенил)имидазола. Препаративный пример X. Хлорангидрид 4-[4-(пиримидин-2-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 2-(4-феноксифенил)пиримидин вместо 1-(4-феноксифенил)имидазола. Препаративный пример Y. Хлорангидрид 4-[2-(имидазол-1-ил)пиридин-5-илокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(5-феноксипиридин-2-ил)имидазол вместо 1-(4-феноксифенил)имидазола. Препаративный пример Z. Хлорангидрид 4-[5-(имидазол-1-ил)пиридин-2-илокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(2-феноксипиридин-5-ил)имидазол вместо 1-(4-феноксифенил)имидазола. Препаративный пример АА. Хлорангидрид 4-[4'-(имидазол-1-ил)бифенил-4-окси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере на стадии А, применяя 1-[4'-фенокси-4 бифенил]имидазол вместо 1-(4-феноксифенил) имидазола. Препаративный пример АВ. Хлорангидрид 4'-[4-(имидазол-1-ил)фенокси]бифенил-4-сульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере В, на стадии А, применяя 1-(4-хлорфенил)имидазол вместо 1-(2-хлорэтил)пирролидина. 10 Препаративный пример АС. Хлорангидрид 4-[(4-хлорпиразол-1-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4 феноксифенил)-4-хлорпиразол вместо 1-(4 феноксифенил)имидазола. Препаративный пример AD. Хлорангидрид 4-[4-(имидазол-1-ил)фенилтио]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4-фенилтиофенил)имидазол вместо 1-(4-феноксифенил)имидазола. Препаративный пример АЕ. Хлорангидрид 4-[4-(пиридин-3-ил)фенокси]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 3-(4-феноксифенил)пиридин вместо 1-(4-феноксифенил) имидазола. Препаративный пример AF. Хлорангидрид 4-[4-(1,3,4-триазол-1-ил)фенилтио]бензолсульфокислоты. Ожидаемый продукт получают в соответствии со способом, описанным в препаративном примере А, на стадии А, применяя 1-(4-фенилтиофенил)-1,3,4-триазол вместо 1-(4-феноксифенил)имидазола. Пример 1. Натриевая соль 6-4-[4-(имидазол-1-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновой кислоты. Стадия А. Трет-бутиловый эфир 6-4-[4(имидазол-1-ил)фенокси]бензолсульфонил 4,5,6,7-тетрагидрофуро[2,3-с]-пиридин-(5R)карбоновой кислоты. 30 ммол трет-бутилового эфира 4,5,6,7 тетрагидрофуро-[2,3-с]пиридин-(5R)-карбоновой кислоты (полученного в соответствии со способом, описанным M.S. Allen, Synth. Comm.,22 (14), 2077-2102, 1992) растворяют в 60 мл пиридина. Затем порциями добавляют 33 ммол соединения, описанного в препаративном примере А. Смесь перемешивают при комнатной температуре в течение ночи, а затем выливают в 300 мл воды. После экстрагирования этилацетатом органическую фазу промывают водой, а затем сушат. После фильтрации и удаления растворителя выпариванием остаток очищают хроматографией на силикагеле, применяя смесь этилацетата/пентана (8/2) в качестве элюента с получением ожидаемого продукта. Стадия В. Натриевая соль 6-4-[4-(имидазол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновой кислоты. 10 ммол сложного эфира, полученного на стадии А, растворяют в 70 мл метиленхлорида. Затем добавляют 10 ммол анизола с последующим добавлением при 0 С 70 мл трифторуксусной кислоты. Затем реакционную смесь перемешивают при комнатной температуре в течение ночи. После выпаривания полученный остаток очищают хроматографией на силикагеле,применяя смесь дихлорметана/этанола (9/1) в качестве элюента с получением ожидаемого продукта после лиофилизации соответствующей натриевой соли. Элементарный микроанализ: Рассчитано Найдено[2,3-с]пиридин-(5R)-(N-аллилокси)карбоксамид. 9 ммол Cоединения, описанного в примере 1, растворяют в 70 мл дихлорметана и 10 мл диметилформамида. Затем к этой смеси добавляют 45 ммол диизопропилэтиламина, 9 ммол дигидроксибензотриазола, 13 ммол O-аллилгидроксиламина гидрохлорида и 11 ммол О(бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний тетрафторбората. После отстаивания в течение ночи при комнатной температуре смесь выпаривают. Остаток поглощают хлорметаном. После сушки раствор фильтруют и выпаривают. Остаток очищают хроматографией на силикагеле, применяя смесь дихлорметана/этанола (95/5) в качестве элюента для получения ожидаемого продукта. Стадия В. Гидрохлорид 6-4-[4-(имидазол 1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси) карбоксамида. 8,5 ммол соединения, описанного на предыдущей cтадии, растворяют в 120 мл дихлорметана. К полученной смеси добавляют 0,4 ммол (Рh3 Р)2 РdСl2 и 2,5 ммол уксусной кислоты и перемешивают в течение 5 мин перед добавлением 4,8 мл гидрида трибутилолова. После пятиминутного перемешивания растворитель удаляют выпариванием, а остаток поглощают смесью ацетонитрила/метанола. После промывания гексаном и выпаривания остаток очищают колоночной хроматографией с обращенной фазой, применяя смесь ацетонитрила/метанола в качестве элюента. После лиофилизации полученное твердое вещество растворяют в ацетонитриле и превращают в соответствующий гидрохлорид добавлением 4,32 мл 1N НСl. Затем целевой продукт получают лиофилизацией. Соединения в следующих примерах получают в соответствии со способами, описанными в примере 1 или 2, исходя из соответствующих исходных материалов. Пример 3. 6-4'-[2-(Пирролидин-1-ил) этокси]бифенил-4-сульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере В. Элементарный микроанализ: Рассчитано Найдено Пример 4. Гидрохлорид 6-4'-[2-(пирролидин-1-ил)этокси]бифенил-4-сульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 3. Элементарный микроанализ: Рассчитано Найдено Пример 5. 6-4'-[4-(Пиридин-4 ил)фенокси] бифенил-4-сульфонил-4,5,6,7 тетрагидрофуро [2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере С. Пример 6. Гидрохлорид 6-4'-[4-(пиридин 4-ил)фенокси]бифенил-4-сульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 5. Пример 7. 6-4'-[2-(Морфолино)этокси] бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 7. Элементарный микроанализ: Рассчитано Найдено[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Е. Пример 10. Гидрохлорид 6-4'-[2-(пиперидино)этокси]бифенил-4-сульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 9. Элементарный микроанализ: Рассчитано Найдено Пример 11. Гидрохлорид 6-[4'-(имидазол 1-ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновой кислоты. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Пример 12. Гидрохлорид 6-[4'-(имидазол 1-ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 11. Элементарный микроанализ: Рассчитано Найдено Пример 13. 6-4'-[2-(Пергидроазепин-1-ил) этокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]лиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере 14 Целевой продукт получают в соответствии со способом, описанным в Примере 2, исходя из продукта, описанного в примере 13. Пример 15. 6-4'-[3-Пирролидин-1-илпропокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Н. Пример 16. Гидрохлорид 6-4'-[3-пирролидин-1-илпропокси]бифенил-4-сульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 15. Пример 17. 6-4'-[2-(1,3-Дигидроизоиндол 2-ил)этокси]бифенил-4-сульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереI. Пример 18. Гидрохлорид 6-4'-[2-(1,3 дигидроизоиндол-2-ил)этокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 17. Пример 19. 6-4'-[2-(Циклопента[с]пирролидин-2-ил)этокси]бифенил-4-сульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереJ. Пример 20. Гидрохлорид 6-4'-[2-(Циклопента[с]пирролидин-2-ил)этокси]бифенил-4 сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 19. Пример 21. 6-4'-[(Пирролидин-1-ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с] пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере К. Пример 22. Гидрохлорид 6-4'-(пирролидин-1-ил)бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси) карбоксамида. 15 Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 21. Пример 23. 6-4'-(Пиперидино)бифенил-4 сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереL. Пример 24. Гидрохлорид 6-4'-(пиперидино)бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 23. Пример 25. 6-4'-(Морфолино)бифенил-4 сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере М. Пример 26. Гидрохлорид 6-4'-(морфолино)бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 25. Пример 27. 6-[4'-(Циклопента[с]пирролидин-2-ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере[с]пирролидин-2-ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с]-пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя их продукта, описанного в примере 27. Пример 29. 6-[4'-(1,3-Дигидроизоиндол-2 ил)бифенил-4-сульфонил]-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере О. Пример 30. Гидрохлорид 6-[4'-(1,3-дигидроизоиндол-2-ил)бифенил-4-сульфонил]-4,5,6,7 тетрагидрофуро[2,3-с]-пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 29. 16 Пример 31. 6-4-[4-(1,3,4-Триазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Р. Пример 32. Гидрохлорид 6-4-[4-(1,3,4 триазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]-пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 31. Элементарный микроанализ: Рассчитано Найдено Пример 33. 6-4-[4-(1,2,4-Триазол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереQ. Пример 34. Гидрохлорид 6-4-[4-(1,2,4 триазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 33. Элементарный микроанализ: Рассчитано Найдено Пример 35. 6-4-[4-(Пиррол-1-ил)фенокси] бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3 с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереR. Пример 36. Гидрохлорид 6-4-[4-(пиррол 1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 35. Пример 37. 6-4-[4-(Пиразол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Пример 38. Гидрохлорид 6-4-[4-(пиразол 1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 37. Пример 39. 6-4-[4-(Имидазол-2-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере Т. Пример 40. Гидрохлорид 6-4-[4-(имидазол-2-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 39. Пример 41. 6-4-[4-(Бензимидазол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереU. Пример 42. Гидрохлорид 6-4-[4-(бензимидазол-1-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 41. Элементарный микроанализ: Рассчитано Найдено Пример 43. 6-4-[4-(Пиридин-4-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидро[2,3-с] пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереV. Пример 44. Гидрохлорид 6-4-[4-(пиридин-4-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 43. Пример 45. 6-4-[4-(Пиримидин-5-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. 18 Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереW. Пример 46. Гидрохлорид 6-4-[4-(пиримидин-5-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 45. Элементарный анализ: Рассчитано Найдено Пример 47. 6-4-[4-(Пиримидин-2-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереX. Пример 48. Гидрохлорид 6-4-[4-(пиримидин-2-ил)фенокси]бензолсульфонил-4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 47. Пример 49. 6-4-[2-(Имидазол-1-ил)пиридин-5-илокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереY. Пример 50. Гидрохлорид 6-4-[2-(имидазол-1-ил)пиридин-5-илокси]бензолсульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 49. Пример 51. 6-4-[5-(Имидазол-1-ил)пиридин-2-илокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереZ. Пример 52. Гидрохлорид 6-4-[5-(имидазол-1-ил)пиридин-2-илокси]бензолсульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 51. Пример 53. 6-4-[4'-(Имидазол-1-ил)бифенил-4-окси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере АА. Пример 54. Гидрохлорид 6-4-[4'-(имидазол-1-ил)бифенил-4-окси]бензолсульфонил 4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(Nгидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 53. Элементарный микроанализ: Рассчитано Найдено Пример 55. 6-4'-[(4-Имидазол-1-ил)фенокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере АВ. Пример 56. Гидрохлорид 6-4'-[4-(имидазол-1-ил)фенокси]бифенил-4-сульфорил-4,5,6,7-тетрагрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 55. Пример 57. 6-4-[4-(4-Хлорпиразол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереAC. Пример 58. 6-4-[4-(4-Хлорпиразол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 57. Элементарный микроанализ: Рассчитано Найдено[2,3-с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере 20 Пример 60. Гидрохлорид 6-[4-(имидазол-1 ил)фенилтио]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 59. Элементарный микроанализ: Рассчитано Найдено Пример 61. 6-(4-(Пиридин-3-ил)фенокси) бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3 с]пиридин-(5R)-карбоновая кислота, натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примере АЕ. Пример 62. Гидрохлорид 6-(4-(пиридин 3-ил)фенокси)бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 61. Элементарный микроанализ: Рассчитано Найдено Пример 63. 6-4-[4-(1,3,4-Триазол-1-ил) фенилтио]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновая кислота,натриевая соль. Целевой продукт получают в соответствии со способом, описанным в примере 1, исходя из продукта, описанного в препаративном примереAF. Пример 64. Гидрохлорид 6-4-[4-(1,3,4 триазол-1-ил)фенилтио]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамида. Целевой продукт получают в соответствии со способом, описанным в примере 2, исходя из продукта, описанного в примере 63. Пример 65. Гидрохлорид этилового эфира 6-4-[4-(имидазол-1-ил)фенокси]бензолсульфо нил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин(5R)-карбоновой кислоты. Ожидаемый продукт получают в соответствии со способом, описанным на стадии А примера 1, исходя из этилового эфира 4,5,6,7 тетрагидрофуро[2,3-с]пиридин-(5R)-карбоновой кислоты и продукта, описанного в препаративном примере А. Элементарный микроанализ: Рассчитано Найдено 21 Фармакологическое исследование соединений по данному изобретению Пример А. Ферментативное ингибирование металлопротеаз. Шесть рекомбинантных ферментов человека, ММР-1 (интерстициальная коллагеназа),ММР-2 (желатиназа А), ММР-3 (стромелизин 1), ММР-8 (нейтрофильная коллагеназа), ММР 9 (желатиназа В) и ММР-13-(коллагеназа 3),активируют, применяя АРМА (4-аминофенилацетат ртути). Ферментные тесты ММР-1, -2, -8,-9 и -13 проводят, применяя следующий пептидомиметический субстрат:DnpProGhaGlyCys(Me)HisAlaLys(Nma)NH2 который расщепляют между глицином и цистеином для получения флуоресцентного продукта, описанного D.M. BICKETT et al., Anal.Biochem., 212, 58-64, 1993. Ферментный тест ММР-3 проводят, применяя следующий пептидомиметический субстрат:McaArgProLysProTyrAlaNvaTrpMetLys (Dnp) NH2,который расщепляют между аланином и норвалином для получения флуоресцентного продукта, как описано H.NAGASE et al. (J.Biol.Brij35 при рН 7,7, инициируют, применяя 20 мкМ субстрата общим объемом 100 мкл при 37 С. Флуоресценцию, полученную через 6 ч,определяют в 96-луночном планшете на флуориметре, оборудованном как 360-нм, так и 460 нм фильтрами для возбуждения и эмиссии. Величина IС 50 соединений по изобретению составляет от 10-10 до 10-8 М для всех ММР, за исключением ММР-1. Коллагеназы ММР-13 и ММР-8 проявляют специфичность с коэффициентом 1000 по сравнению с коллагеназой ММР-1. Пример В. Распад in vitro хрящевого матрикса. Соединения в соответствии с данным изобретением исследуют на модели повреждения хрящевого матрикса, индуцируемом интерлейкином IL-1. Тест, проводимый на хряще кролика, сводится- с одной стороны, к распаду коллагена: колориметрическое измерение в соответствии со способом Grant (GRANT R.A. Estimation of- с другой стороны, к распаду протеогликанов: радиоизотопическое измерение фракции глюкозаминогликанов, выделяемых после 24 часовой стимуляции интерлейкином-1 (10 мг/мл) тканью, предварительно меченной 35SO4,на протяжении 24 ч в контакте с АРМА (5x104 22 Соединения в соответствии с данным изобретением исследуют, добавляя их к культуральной среде на 3 дня тестирования. При концентрации от 10-8 до 10-6 М они сильно ингибируют распад коллагена и протеогликанов. В качестве примера, некоторые соединения в соответствии с данным изобретением имеют следующую активность:% Защиты при 10-7 М Коллаген Протеогликаны Пример 2 82 83 Пример 4 34 70 Пример 8 62 77 Пример 10 39 73 Пример 12 27 71 Пример 32 84 86 Пример 34 84 93 Пример 42 65 83 Пример 44 96 82 Пример 46 87 93 Пример 54 56 72 Пример 58 67 60 Пример 60 65 81 Пример С. Ангиогенез in vitro. Части торакальной аорты самцов крысFischer 344 в возрасте от 8 до 12 недель погружают в коллагеновый гель, тип I, в соответствии со способом Nicosia and Ottinetti (1990). Через 5 дней культивирования в среде без сыворотки препараты исследуют под микроскопом и определяют количество образовавшихся псевдососудов с позиций сосудистой плотности после цифрового анализа и анализа изображения. В качестве примера, IC50 соединения из примера 2 составляет 2,3 нм, а IС 50 соединения из примера 4 составляет 100 нм. Пример D. Абсорбция после перорального введения у мышей - биоактивность плазмы. Абсорбцию соединений оценивают в кровотоке после перорального введения мышам(CDl, самцы, 25-30 г), измеряя потенциал плазмы к ингибированию ММР-13 в экспериментальных условиях, идентичных условиям, применяемым in vitro (пример А). Биоактивность определяют в плазме после удаления белков этиловым спиртом (18 ч при -20 С) в различное время после введения соединений. В качестве примера, % ингибирования ММР-13, получаемый после введения 30 мг/кг, является следующим:% Защиты МMР-13 - 30 мг/кг перорально 30 мин 2 ч 8 ч Пример 2 88% 83% 51% Пример 4 91% 94% 68% Пример 8 92% 72% 76% Пример Е. Артрит, вызываемый адъювантом Фрейнда у крыс - защита от суставной деградации. Защитную активность соединений против деградации суставной ткани исследуют на мо 23 дели артрита, вызванного адъювантом Фрейнда у крыс (Lewis, самки, 62 дня). Аутоиммунная патология, вызываемая интраплантарной (в подошву стопы) инъекцией 0,1 мл адъюванта (Mycobacterium butyricum, 4 мг/мл) в одну из задних лап вызывает суставное повреждение помимо воспалительной реакции. Через 21 день повреждение лапы, не получавшей инъекцию, оценивают с точки зрения костей (денситометрическое измерение проксимальной части бедра) и надколенного хряща (содержание ОН-пролина и глюкозаминогликана измеряют в соответствии со способом Farndale et al. (Biophysica Acta,1986, 883, 173-177), а также способом, описанным Grant (J. Clin. Path., 1964, 17, 685), соответственно). В качестве примера, соединение из примера 2, вводимое перорально дважды в сутки при дозе 40 мг/кг (по 10 животных в группе), вызывает снижение потери минерального содержания костей в проксимальном бедре контрольных животных с артритом на 42% (Р 0,01) и снижение потери глюкозаминогликанов и ОН-пролина в надколенном хряще на 61% (Р 0,05) и 98% (Р 0,01), соответственно. Пример F. Фармацевтическая композиция. Состав препарата для 1000 таблеток, содержащих дозу 100 мг: Соединение из примера 2 100 мг Гидроксипропилцеллюлоза 2 г Пшеничный крахмал 10 г Лактоза 100 г Магний стеарат 3 г Тальк 3 г ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения формулы (I) где R1 - атом водорода или галогена, либо линейный или разветвленный (C1-С 6) алкил, либо линейная или разветвленная (C1-C6)алкоксигруппа,R2 - гидрокси, линейная или разветвленная(C1-C6)алкокси или -NHОН-группа,Ar1 - фениленовая или бифениленовая группа,Х - атом кислорода или серы, NR-группа,-СС-группа или связь,R - атом водорода, либо линейная или разветвленная (C1-С 6)алкильная группа,n - целое число от 0 до 6, включительно,Аr2: 24 их изомеры и соли присоединения фармацевтически приемлемой кислоты или основания, при этом- под "гетероарильной группой" подразумевается моноциклическая ароматическая группа или бициклическая ароматическая группа, в которой, по крайней мере, один цикл является ароматическим, содержащим один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенным одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-С 6)алкила, линейного или разветвленного (C1-С 6)алкоксила, линейного или разветвленного тригало-(C1-С 6)алкила, линейного или разветвленного тригало-(C1-C6)алкоксила и гидроксила;- под "гетероциклической группой" подразумевается насыщенная или частично насыщенная моно- или бициклическая неароматическая группа, содержащая один, два или три одинаковых или различных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенная одной или несколькими одинаковыми или различными группами, выбранными из галогена, линейного или разветвленного (C1-С 6) алкила, линейного или разветвленного (C1-С 6) алкоксила, линейного или разветвленного тригало-(C1-С 6)алкила, линейного или разветвленного тригало-(C1-С 6)алкоксила и гидроксила. 2. Соединения формулы (I) по п.1, отличающиеся тем, что Х - атом кислорода или серы. 3. Соединения формулы (I) по любому из п.1 или 2, отличающиеся тем, что R2 - -NHОНгруппа. 4. Соединения формулы (I) по любому из пп.1, 2 и 3, отличающиеся тем, что Ar1 - фениленовая группа, а n = 0. 5. Соединения формулы (I) по п.4, отличающиеся тем, что Ar2 - фенильная группа, замещенная гетероарильной группой. 6. Соединения формулы (I) по п.5, отличающиеся тем, что Ar2 - фенильная группа, замещенная группой, выбранной из имидазолила,триазолила и пиридинила. 7. Соединения формулы (I) по любому из пп.1-6, отличающиеся тем, что Х - атом кислорода или серы, R2 - -NHOH-группа, Ar1 - фениленовая группа, n = 0, а Аr2 - фенильная группа,замещенная группой, выбранной из имидазолила, триазолила и пиридинила. 8. Соединения формулы (I) по любому из пп.1, 2 и 3, отличающиеся тем, что Ar1 - бифениленовая группа, а Аr2 - гетероциклическая группа. 9. Соединение формулы (I) по п.1, представляющее собой 6-4-[4-(имидазол-1-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбокса 25 мид, а также его соли присоединения фармацевтически приемлемой кислоты или основания. 10. Соединение формулы (I) по п.1, представляющее собой 6-4'-[2-(пирролидин-1-ил) этокси]бифенил-4-сульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид гидрохлорид, а также его соли присоединения фармацевтически приемлемой кислоты или основания. 11. Соединение формулы (I) по п.1, представляющее собой 6-4-[4-(1,3,4-триазол-1-ил) фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения с фармацевтически приемлемой кислотой или основанием. 12. Соединение формулы (I) по п.1, представляющее собой 6-4-[4-(пиридин-4-ил)фенокси]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения фармацевтически приемлемой кислоты или основания. 13. Соединение формулы (I) по п.1, представляющее собой 6-4-[4-(1,3,4-триазол-1-ил) фенилтио]бензолсульфонил-4,5,6,7-тетрагидрофуро[2,3-с]пиридин-(5R)-(N-гидрокси)карбоксамид, а также его соли присоединения фармацевтически приемлемой кислоты или основания. 14. Способ получения соединений формулы (I) по п.1, отличающийся тем, что в качестве исходного материала используют соединение формулы (II) в рацемическом виде или в виде конкретного изомера где R1 имеет такие же значения, как и в формуле(I), a R' - атом водорода либо линейная или разветвленная (C1-С 6)алкильная группа, которое замещают по аминогруппе галогенсодержащим соединением формулы (III) СlSO2-Аr1-Х-(СН 2)n-Аr2(III) где Ar1, X, n и Аr2 имеют такие же значения, как и в формуле (I), с получением- когда R' - атом водорода, соединения формулы (I/a), представляющего частный случай соединений формулы (I) где R1, Ar1, X, N и Аr2 имеют вышеуказанные значения,- либо, когда R' - линейная или разветвленная (C1-С 6)алкильная группа (R"), соединение формулы (I/a1), представляющие частный случай соединений формулы (I) где R1, Ar1, X, n, Ar2 и R" имеют вышеуказанные значения, которое может быть подвергнуто воздействию кислоты с получением вышеописанного соединения формулы (I/a),при этом соединение формулы (I/a) при желании, подвергают воздействию Oзамещенного гидроксиламина, получая, после снятия защиты с функции гидроксиламина, соединение формулы (I/b) где R1, Ar1, X, n, и Ar2 имеют вышеуказанные значения; при этом соединения формул (I/a), (I/a1) и(I/b) составляют всю совокупность соединений формулы (I),которые при необходимости очищают в соответствии с известными способами очистки,при необходимости разделяют на изомеры в соответствии с известными способами разделения и при желании превращают в соли присоединения фармацевтически приемлемой кислоты или основания. 15. Фармацевтическая композиция, включающая в качестве активного ингредиента соединение по любому из пп.1-13 в сочетании с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми эксципиентами или носителями. 16. Фармацевтическая композиция по п.15,включающая в качестве активного ингредиента соединение по любому из пп.1-13, применяемое в качестве ингибиторов металлопротеаз.
МПК / Метки
МПК: A61K 31/4355, C07D 491/048, A61P 19/02
Метки: производные, тетрагидрофуро[2,3-c]пиридина, способ, металлопротеазы, получения, ингибиторов, применение, качестве
Код ссылки
<a href="https://eas.patents.su/14-2527-proizvodnye-tetragidrofuro23-cpiridina-sposob-ih-polucheniya-i-primenenie-v-kachestve-ingibitorov-metalloproteazy.html" rel="bookmark" title="База патентов Евразийского Союза">Производные тетрагидрофуро[2,3-c]пиридина, способ их получения и применение в качестве ингибиторов металлопротеазы</a>
Предыдущий патент: Применение фанхинона для лечения болезни альцгеймера
Следующий патент: Коррекция смещения фазы эхо-сигнала в системе демодуляции множества несущих
Случайный патент: Система и способ для электронной передачи, хранения и извлечения аутентифицированных документов












