Производные триазина, способ их получения и применение в качестве гербицидов
Формула / Реферат
1. Производное триазина общей формулы (I)
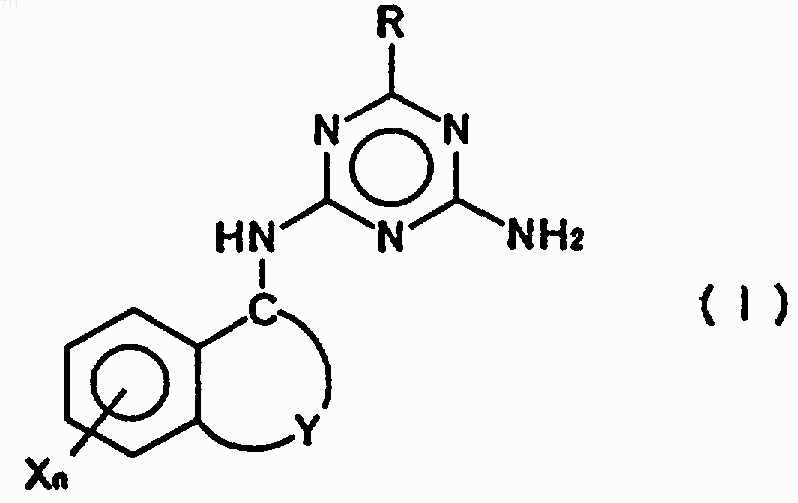
где X представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу, C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу, C1-C4 алкилсульфонильную группу, C1-C6 галогеналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу при условии, что, когда заместителей Х несколько, они могут быть одинаковыми или отличными друг от друга, или два соседних заместителя Х могут образовывать насыщенное или ненасыщенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью в бензольном кольце, n обозначает целое число 0 или 1-4,
R представляет
(1) C1-C6 алкильную группу, или
(2) замещенную C1-C6 алкильную группу, имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего из
i) атома галогена,
ii) гидроксильной группы и
iii) C1-C8 алкоксигруппы, алкильная часть которой может содержать гетероатом, и
Y представляет С2-С4 алкиленовую группу, которая может быть замещена 1-8 C1-C6 алкильными группами, или двухвалентную группу формулы (а),
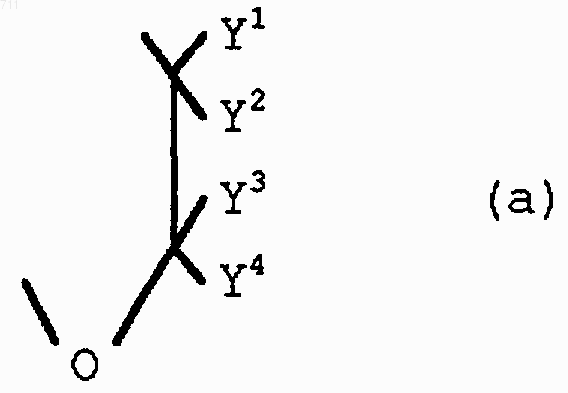
где каждый из Y1 - Y4 независимо представляет атом водорода или C1-С4 алкильную группу.
2. Производное триазина по п.1, где Х представляет C1-C4 алкильную группу или атом галогена.
3. Производное триазина по п.1, где Х выбран из класса, состоящего из метокси, метилтио, метилсульфонила, трифторметила, трифторметокси, феноксиэтила, фенила и фенокси.
4. Производное триазина по п.2, где n представляет целое число 1 или 2.
5. Производное триазина по п.4, где, когда n равно 2, каждый из двух заместителей Х является независимо C1-C6 алкильной группой или атомом галогена.
6. Производное триазина по п.1, где n равно 0.
7. Производное триазина по п.1, где Y представляет группу пропилена, которая замещена одной C1-C4 алкильной группой.
8. Производное триазина по п.7, где Y представляет группу пропилена, которая замещена метилом.
9. Производное триазина по п.1, где Y является двухвалентной группой формулы (а),
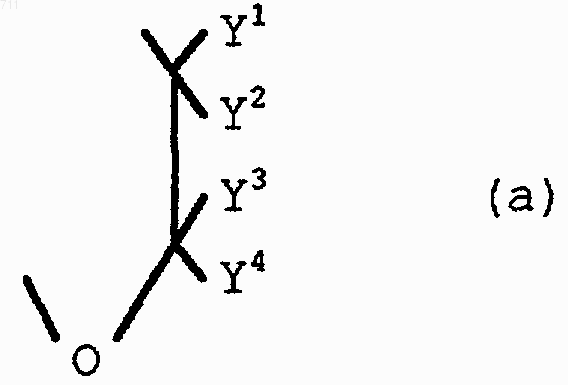
где каждый из Y1 - Y4 независимо представляет атом водорода или C1-C4 алкильную группу.
10. Производное триазина по п.9, где каждый из Y1-Y4 независимо представляет атом водорода или метил.
11. Производное триазина по п.1, где R представляет C1-C6 алкильную группу.
12. Производное триазина по п.1, где R представляет C1-C6 алкильную группу, которая замещена атомом фтора, атомом хлора или атомом брома.
13. Производное триазина по п.12, где R выбирают из класса, состоящего из -СF3, -ССl3, -CH2F, -CH2Cl, -CH2Br, -C2F5, -CH2CH2F, -СНF(СН3), -СНСl(СН3), -CHBr(СН3), -СНF(СF3), -СF(СН3)2, -ССl(СН3)2, -СВr(СН3)2, -СНF(СН2СН3), -СНСl(СН2СН3) и -CHBr(СН2СН3) групп.
14. Производное триазина по п.1, где R представляет C1-C6 алкильную группу, которая замещена гидроксильной группой.
15. Производное триазина по п.14, где R выбирают из класса, состоящего из -СН2ОН, -С2Н4ОН, -СН(ОН)СН3, -СН(ОН)С2Н5, -С(СН3)2OН и -С(СН3)2СН2ОН групп.
16. Производное триазина по п.1, где R является C1-C6 алкильной группой, замещенной группой, в которой гетероциклическая группа, содержащая атом кислорода, и атом кислорода связаны друг с другом.
17. Способ получения производного триазина общей формулы (I)
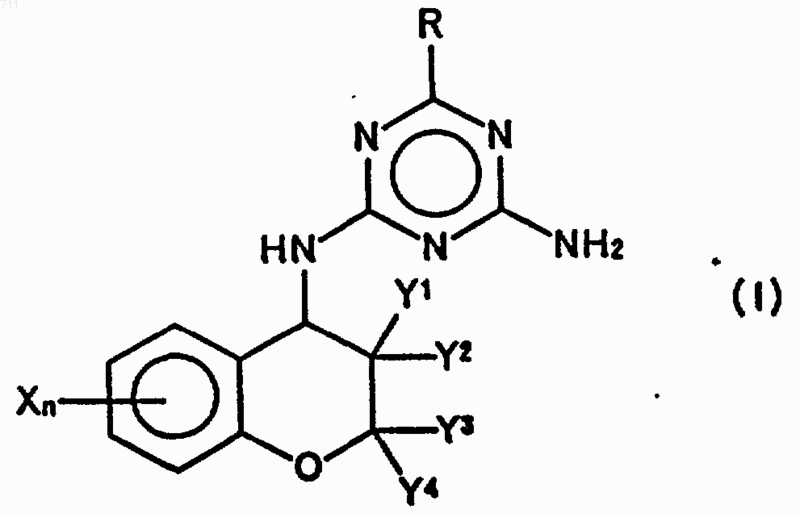
где Х представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу, C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу, C1-C4 алкилсульфонильную группу, C1-C6галогеналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу, при условии что, когда заместителей Х несколько, они могут быть одинаковыми или отличными друг от друга, или два соседних заместителя Х могут образовывать насыщенное или ненасыщенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью в бензольном кольце, n представляет целое число 0 или 1-4, R представляет
(1) C1-C6 алкильную группу, или
(2) замещенную C1-C6 алкильную группу, имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего из
i) атома галогена,
ii) гидроксильной группы и
iii) C1-C6 алкоксигруппы, алкильная часть которой может содержать гетероатом, и
Y представляет C2-C4 алкиленовую группу, которая может быть замещена 1-8 C1-C6 алкильными группами, или двухвалентную группу формулы (а),
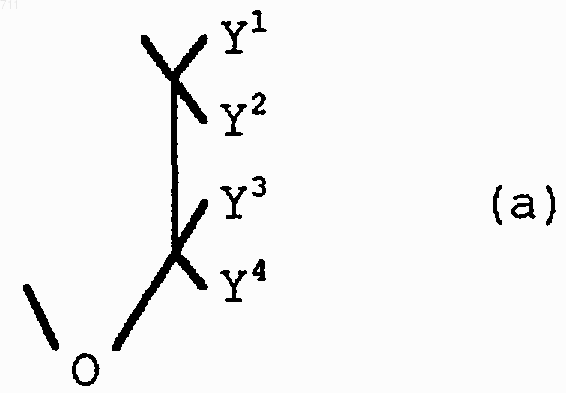
где каждый из Y1-Y4 независимо представляет атом водорода или C1-C4 алкильную группу, включает взаимодействие соединения общей формулы (II)
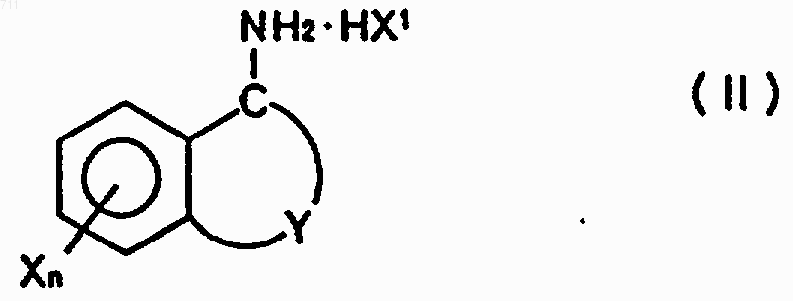
где X, n и Y являются такими, как определено выше, и X1 представляет атом галогена, с цианогуанидином формулы (III)
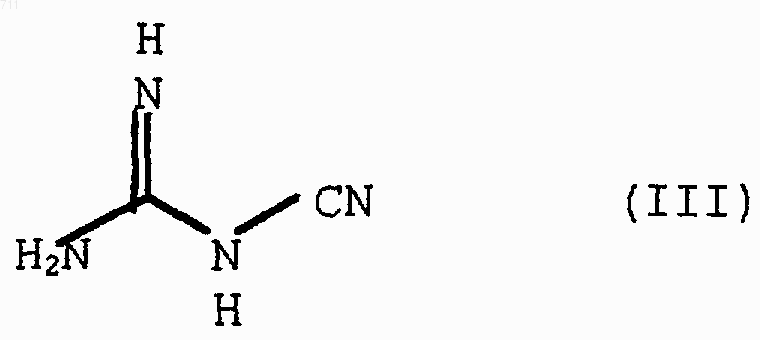
и затем взаимодействие продукта реакции со сложным эфиром общей формулы (IV),
RCOOR1 (IV)
где R имеет значения, определенные выше, и R1 представляет C1-C4 алкильную группу.
18. Гербицид, содержащий производное триазина общей формулы I по п.1 или его соль в качестве активного ингредиента.
Текст
1 Область техники Данное изобретение относится к новому производному триазина, способу его получения и гербициду, содержащему упомянутое производное триазина в качестве активного ингредиента. Более конкретно, оно относится к производному триазина, которое не вызывает фитотоксичность в отношении хлопчатника и может избирательно бороться, при низкой дозировке, с широким диапазоном наземных сорняков,включая канатник Теофраста (канатник), принадлежащий к сорнякам из семейства мальвовых, к которому также принадлежит хлопчатник, к способу эффективного получения упомянутого производного триазина и гербициду, содержащему упомянутое производное триазина в качестве активного ингредиента. Предпосылки к созданию изобретения Гербициды являются очень важными химическими продуктами для снижения затрат труда в борьбе с сорняками и повышения продуктивности сельскохозяйственных и садовых культур. Поэтому гербициды активно изучаются и разрабатываются в течение многих лет и разнообразные гербициды использовались и используются на практике. Однако даже в настоящее время все еще желательно разработать новые гербициды, имеющие гербицидные свойства, в частности химикаты, которые могут избирательно бороться с конкретными сорняками при низкой дозировке, не будучи фитотоксичными для выращиваемых культур. С другой стороны, известно (как раскрыто в книге "Theory and Practice of Weeding in DryHakunyosha Publishing Company), что однолетние травянистые сорняки, такие как росичка кровяная (ползучий сорняк), и однолетние широколистные сорняки, такие как вьюнок пурпурный, амарант тонкий, дурнишник и канатник, встречаются на хлопковых полях. При выращивании хлопчатника очень важно эффективно бороться с этими сорняками при низкой, с точки зрения загрязнения окружающей среды,дозировке и без фитотоксичного воздействия на хлопчатник. Так как хлопчатник, в частности,относится к представителям семейства мальвовых, химикат, имеющий гербицидную активность в отношении канатника, который также относится к сорнякам из семейства мальвовых,способен оказывать фитотоксичное воздействие на хлопчатник. Поэтому важной целью является разработка химиката, который имеет высокую гербицидную активность в отношении канатника и имеет превосходную межродовую селективность между хлопчатником и канатником. Различные соединения известны (как раскрыто в "Comprehensive Bibliography of Research 2 амино)-s-триазина имеют широкий гербицидный спектр и пригодны для использования в качестве гербицидов. Однако эти известные триазинсодержащие гербициды требуют больших дозировок для достижения высокой гербицидной эффективности. И эти химикаты вызывают проблемы с окружающей средой, так как они загрязняют грунтовые воды и т.д., из-за их высокого просачивания через почву. Описание изобретения Настоящее изобретение направлено на обеспечение гербицидного соединения, которое проявляет достаточную гербицидную эффективность при низкой дозировке и является безопасным для окружающей среды и которое имеет превосходную межродовую селективность между хлопчатником и канатником. Для достижения указанной цели были проведены тщательные исследования и было обнаружено, что новое производное триазина, в котором углеродная циклическая группа, конденсированная с фенильной группой, и кольцо триазина связаны друг с другом, или кольцо хромана и кольцо триазина связаны друг с другом через аминогруппу, не вызывает фитотоксичности в отношении хлопчатника и проявляет превосходную гербицидную активность в отношении канатника, который является сорняком из семейства мальвовых так же, как хлопчатник. Таким образом, объектом данного изобретения является производное триазина общей формулы (I), где X представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу, C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу, C1-C4 алкилсульфонильную группу,C1-C6 галогеналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу, при условии что, когда заместителей Х несколько, они могут быть одинаковыми или отличными друг от друга, или два соседних заместителя Х могут образовывать насыщенное или ненасыщенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью в бензольном кольце, n представляет целое число 0 или 1-4;(2) замещенную C1-C6 алкильную группу,имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего изiii) C1-C8 алкоксигруппы, алкильная часть которой может содержать гетероатом, иY представляет С 2-С 4 алкиленовую группу,которая может быть замещена 1-8 C1-C6 алкильными группами, или двухвалентную группу формулы (а), где каждый из Y1 - Y4 независимо представляет атом водорода или C1-C4 алкильную группу. Кроме того, объектом данного изобретения является способ получения производного триазина общей формулы (I) где X, n, Y и R имеют значения, определенные выше, который включает взаимодействие соединения общей формулы (II) и затем взаимодействие продукта реакции со сложным эфиром общей формулы (IV),RCOOR1(IV) где R принимает значения, определенные выше,и R1 представляет C1-C4 алкильную группу. Кроме того, объектом данного изобретения является гербицид, содержащий производное триазина указанной выше общей формулы (I) или его соль в качестве активного ингредиента. Наилучшие варианты осуществления изобретения Производное триазина данного изобретения (называемое иногда далее как "производное триазина (I)") является соединением, имеющим следующую общую формулу (I) В приведенной выше общей формуле (I) X представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу,C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу,C1-C4 алкилсульфонильную группу, C1-C6 гало 000711 4 геналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу. Когда указанный Х представляет атом галогена, конкретные примеры атома галогена включают атом хлора, атом брома, атом фтора и атом иода. Атом галогена предпочтительно является атомом хлора, атомом фтора или атомом брома. Когда Х представляет C1-C6 алкильную группу, конкретные примеры ее включают метил, этил, пропил, бутил, пентил и гексил. Алкильные группы, которые имеют от 3 до 6 атомов углерода, могут быть линейными или разветвленными. Кроме того, C1-С 6 алкильная группа может быть циклоалкильной группой как таковой, такой как циклопропил, циклобутил, циклопентил и циклогексил. Далее, это может быть алкильная группа, содержащая циклоалкильную группу, такая как циклопропилметил. Указанная C1-C6 алкильная группа предпочтительно является метилом, этилом, изопропилом или трет-бутилом, особенно предпочтительно метилом. Когда Х представляет C1-C4 алкоксигруппу, конкретные примеры ее включают метокси,этокси, пропокси и бутокси. Алкоксигруппа,имеющая 3 или 4 атома углерода, может быть линейной или разветвленной. Конкретные примеры C1-C4 алкоксигруппы также включают циклопропокси, в которой метил может быть замещенным, и циклобутокси. C1-C4 алкоксигруппа предпочтительно является метокси. Когда Х представляет C1-C4 алкилтиогруппу, конкретные примеры ее включают -SСН 3,-SС 2 Н 5, -SС 3 Н 7 и -SC4H9 группы. Из них алкилтиогруппа, имеющая 3 или 4 атома углерода,может быть линейной или разветвленной. C1-C4 алкилтиогруппа предпочтительно является-SСН 3. Когда Х представляет C1-C4 алкилсульфонильную группу, конкретные примеры ее включают -SO2 СН 3, -SО 2 С 2 Н 5, -SО 2 С 3 Н 7 и -SO2 С 4 Н 9 группы. Из них алкилсульфонильная группа,имеющая 3 или 4 атома углерода, может быть линейной или разветвленной. C1-C4 алкилсульфонильная группа предпочтительно являетсяC1-C6 галогеналкильная группа, как одно воплощение X, является группой, образованной путем замещения 1 - 13 атомов водорода, связанных с атомом (атомами) углерода вышеуказанной C1-C6 алкильной группы, указанным атомом (атомами) галогена. Конкретные примеры C1-C6 галогеналкильной группы включают-СF3, -CH2F, -ССl3 и -СН 2 СF3 группы. Предпочтительной C1-C6 галогеналкильной группой является -СF3.C1-C4 галогеналкоксигруппа, как одно воплощение X, является группой, образованной путем замещения 1-9 атомов водорода, связанных с атомом (атомами) углерода вышеуказан 5 ной C1-C4 алкоксигруппы, указанным атомом(атомами) галогена. Конкретные примеры C1-C4 галогеналкоксигруппы включают -ОСF3, -ОССl3 и -OCH2F группы. Предпочтительной C1-C4 галогеналкоксигруппой является -ОСF3. Фенилзамещенная C1-C4 алкильная группа,как одно воплощение X, является группой, образованной путем замещения одного или, по меньшей мере, двух атомов водорода, связанных с атомом (атомами) углерода C1-C4 алкильной группы, фенильной группой (группами). Указанная C1-C4 алкильная группа включает метил, этил, пропил и бутил, и из них пропил и бутил могут быть линейными или разветвленными. Конкретные примеры фенилзамещеннойC1-C4 алкильной группы включают группы-СН 2 СН 2 Рh и предпочтительно -СН 2 Рh. Положение, на котором Х является замещенным, представляет следующее. Когда Y,который будет разъяснен позднее, является C2C4 алкиленовой группой, которая может быть замещена 1-8 C1-C4 алкильными группами, Х может находиться на любом атоме углерода ароматической группы, конденсированной с углеродным кольцом, содержащим Y. Предпочтительно, из положений (1) - (4), показанных в следующей общей формуле (I), в которых Х может быть замещен, положение (2) , положение (3) или положение 4, оба положения 2 и 4 или оба положения 3 и 4 является (являются) предпочтительным(и). Когда Y, который будет разъяснен позднее, является двухвалентной группой формулы где Y1 -Y4 имеют значения, определенные выше,Х может быть замещен на любом одном из четырех атомов углерода в 5-м - 8-м положениях кольца хромана. В приведенной выше общей формуле (I) n,которое представляет число заместителей(ля) X,равно целому числу 0 или 1-4, предпочтительно 0, 1 или 2. Когда n равно 2 - 4, т.е. когда число заместителей (ля) Х равно 2 - 4, два или более заместителей X могут быть одинаковыми или отличающимися друг от друга. Кроме того, два соседних заместителя Х могут образовывать насыщенное или ненасы 000711 6 щенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью бензольного кольца. То есть, заместители Х могут образовывать кольцо индена, кольцо индана, кольцо нафталина или кольцо тетралина вместе с бензольным кольцом, с которым связаны заместители X. В приведенной выше общей формуле (I) Y представляет C2-C4 алкиленовую группу, которая может быть замещена 1-8 C1-C4 алкильной группой (группами), или двухвалентную группу формулы (а). Когда Y представляет указанную выше С 2-С 4 алкиленовую группу, особенно группа, в которой углеродное кольцо конденсировано с фенильной группой, является так называемой инданильной группой, когда Y представляет этиленовую группу (группу С 2 алкилена) и является так называемой тетралинильной группой,когда Y представляет пропиленовую группу(группу С 3 алкилена). Конкретными примерами C1-C4 алкильной группы (групп), которая может быть замещена на C2-C4 алкиленовой группе как Y, являются те же самые как C1-C4 алкильные группы C1-C6 алкильной группы в X. Указанная C1-C4 алкильная группа предпочтительно является метилом. Число C1-C4 алкильных групп, которые могут быть замещены на С 2-С 4 алкиленовой группе как Y, составляет от 1 до 8. C1-C4 алкильная группа (группы), которая может быть замещена на алкиленовой группе как Y, может быть замещена на любой атом (атомы) водорода из четырех атомов водорода этиленовой группы, когда алкиленовая группа представляет этиленовую группу (С 2), на любые атомы водорода из шести атомов водорода пропиленовой группы,когда алкиленовая группа представляет пропиленовую группу (С 3), или на любые атомы водорода из восьми атомов водорода бутиленовой группы, когда алкиленовая группа представляет бутиленовую группу (C4). Когда Y представляет двухвалентную группу указанной выше формулы (а), производное триазина данного изобретения может быть представлено следующей общей формулой (I'), где X, n и R имеют те же значения, определенные выше в общей формуле (I). 7 В указанной выше общей формуле (I') каждый из Y1 - Y4 независимо представляет атом водорода или C1-C4 алкильную группу, предпочтительно атом водорода или метил. В общей формуле (I) R представляет(2) замещенную C1-C6 алкильную группу,имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего изiii) C1-C8 алкоксигруппы, алкильная часть которой может содержать гетероатом. Конкретные примеры C1-C6 алкильной группы в (I) включают те, которые упоминаются в отношении X, и C1-C6 алкильная группа предпочтительно является трет-бутилом. Конкретные примеры i) атома галогена как заместителя одного вида в замещенной C1-C6 алкильной группе в (2) включают те, которые указаны в отношении X, и атом галогена является предпочтительно атомом фтора или атомом хлора. Следовательно, конкретными примерами галогензамещенной C1-C6 алкильной группы,включенными в замещенную C1-C6 алкильную группу в (2), являются -СF3, -ССl3, -CH2F,-CH2Cl, -CH2Br, -C2F5, -CH2CH2F, -CHF-(СН 3),-СНСl(СН 3), -СНВr(СН 3), -СНF(СF3), -СF(СН 3)2,-ССl(СН 3)2,-СВr(СН 3)2,-СНF(СН 2 СН 3),-СНСl(СН 2 СН 3) и -СНВr(СН 2 СН 3) группы. Галогензамещенная C1-C6 алкильная группа предпочтительно является-СF3,-СНF(СН 3),-СНF(СF3), -СF(СН 3)2 или -ССl(СН 3)2. Конкретными примерами гидроксилзамещенной C1-C6 алкильной группы, включенными в замещенную C1-C6 алкильную группу в(2), являются -CH2OH, -C2H4OH, -СН(ОН)СН 3,-СН(ОН)С 2 Н 5, -С(СН 3)2OН и -С(СН 3)2 СН 2 ОН группы, и гидроксилзамещенная C1-C6 алкильная группа предпочтительно является-СН(ОН)С 2 Н 5. Конкретные примеры iii) C1-C8 алкоксигруппы, алкильная часть которой может содержать гетероатом в качестве заместителя другого вида в замещенной C1-C6 алкильной группе в(гетероциклическая группа относится к циклической группе, содержащей, по меньшей мере,один гетероатом (например атом кислорода,атом азота, атом серы или т.п. и атом кислорода связаны друг с другом, такие как Группы, в которых гетероциклическая группа и атом кислорода связаны друг с другом,являются группами, в которых атом кислорода связывается с указанной гетероциклической группой так, что образуется простая эфирная связь. Конкретные примеры C1-C8 алкоксизамещенной C1-C6 алкильной группы, которая включается в замещенную C1-C6 алкильную группу в (2) и содержит в качестве заместителяC1-C8 алкоксигруппу, алкильная часть которой может содержать гетероатом, предпочтительно включают алифатические алкоксизамещенные алкильные группы, такие как -СН 2-ОСН 3,-СН 2OС(СН 3)3, -С 2 Н 4-ОСН 3, -С 3 Н 6-ОСН 3, -С 3 Н 6 ОС 2 Н 5, -СН(СН 3)ОСН 3, -СН(СН 2 СН 3)ОСН 3,-СН(СН 3)-СН 2 ОСН 3 и -С(СН 3)2 СН 2 ОСН 3 группы; и алкильные группы, в которых комбинация гетероциклической группы и атома кислорода замещена, такие как Указанная замещенная алкильная группа,имеющая гетероцикл, является предпочтительно Замещенная C1-C6 алкильная группа относится к C1-C6 алкильной группе, имеющей заместитель (заместители) одного или двух видов,выбранных из указанных выше трех заместителей i) , ii) и iii), который является (являются) замещенным (замещенными). Общее число заместителей составляет от 1 до 13. Конкретные примеры C1-С 6 алкильной группы, имеющей заместители двух видов,включают-СН(СF3)ОН, -СН(СF3)ОСН 3 и -СF2 ОСН 3 группы. Способ получения производного триазина(I) по настоящему изобретению включает первую стадию, на которой соединение общей формулы (II) где X, n и Y являются такими, как определено в указанном выше производном триазина (I), и X1 чтобы связать аминогруппу соединения (II) и цианогруппу цианогуанидина (III) друг с другом, и вторую стадию, на которой продукт реакции затем взаимодействует со сложным эфиром общей формулы (IV),RCOOR1(IV) где R имеет значения, определенные в указанном выше производном триазина (I), и R1 представляет C1-C4 алкильную группу, в присутствии катализатора. Способ получения производного триазина по данному изобретению показан схемой реакции ниже. Реакция на первой стадии может быть проведена в присутствии растворителя или без него. Когда реакцию проводят в присутствии растворителя, растворитель может быть выбран из спиртов, таких как метанол, этанол и изопропанол; кетонов, таких как ацетон, метилэтилкетон и циклогексанон; алифатических углеводородов, таких как н-гексан, н-гептан и н-декан; циклических углеводородов, таких как бензол,декалин и алкилнафталин; хлорированных углеводородов, таких как тетрахлорид углерода,метилендихлорид, хлорбензол и дихлорбензол; простых эфиров, таких как тетрагидрофуран и диоксан; а также керосина. Алифатические углеводороды являются предпочтительными и особенно предпочтительным является н-декан. Предпочтительно, соль аминопроизводного (II) и цианогуанидин (III) взаимодействуют в эквивалентном отношении. Конкретные примеры кислоты (НХ 1) для образования соли аминопроизводного (II) включают хлористоводородную кислоту (НСl), бро 000711 10 мистоводородную кислоту (НВr) и фтористоводородную кислоту (HF), и предпочтительной является хлористоводородная кислота (НСl). Несмотря на то, что температура реакции конкретно не ограничивается, она обычно составляет 80-200 С, предпочтительно 120-150 С. Время реакции обычно составляет от 2 до 15 ч,предпочтительно приблизительно от 4 до 7 ч. Реакцию на второй стадии проводят предпочтительно в присутствии катализатора. Катализатор, который может быть использован в этой реакции, включает, например, алкоксиды,такие как метоксид натрия, этоксид натрия и диэтоксид магния; неорганические основания,такие как фосфат натрия, карбонат калия, гидроксид натрия и гидроксид калия; и органические основания, такие как 1,8-диазабицикло[4,3,0]-5-нонен (DBN), триэтиламин и пиридин. Метоксид натрия и этоксид натрия являются предпочтительными. Количество основания на основе аминопроизводного (II) составляет обычно от 1,1 до 10-кратного эквивалентного количества предпочтительно от 1,5 до 4-кратного эквивалентного количества. Количество сложного эфира (IV), используемое в указанной выше реакции, равно обычно от 1 до 10-кратному эквивалентному количеству, предпочтительно от 1 до 4-кратному эквивалентному количеству, на основе аминопроизводного (II). Предпочтительно, указанную выше реакцию проводят в присутствии растворителя. Растворитель, который может быть использован в указанной выше реакции, включает, например,спирты, такие как метанол, этанол и изопропанол; кетоны, такие как ацетон, метилэтилкетон и циклогексанон; алифатические углеводороды,такие как н-гексан, н-гептан и н-декан; циклические углеводороды, такие как бензол, декалин и алкилнафталин; хлорированные углеводороды,такие как тетрахлорид углерода, метилендихлорид, хлорбензол и дихлорбензол; и простые эфиры, такие как тетрагидрофуран и диоксан. Спирты являются предпочтительными, и особенно предпочтительны метанол и этанол. В указанной выше реакции температура реакции обычно составляет от -10 до 100 С,предпочтительно от 0 до 70 С. Время реакции составляет обычно от 2 до 30 ч, предпочтительно приблизительно от 5 до 15 ч. После завершения реакции, согласно обычному способу, реакционную смесь выливают в воду и экстрагируют органическим растворителем, таким как этилацетат. Полученный органический слой дегидратируют осушителем,таким как безводный сульфат натрия, и органический растворитель удаляют посредством отгонки его при пониженном давлении или некоторыми другими средствами. Полученный остаток очищают посредством колоночной хромато 11 графии на силикагеле или некоторыми другими средствами, посредством которых производное триазина (I), которое хотят получить, может быть выделено в кристаллической форме. Гербицид по данному изобретению, содержащий в качестве активного ингредиента производное триазина (I) или его соль данного изобретения, будет пояснен ниже. Гербицид данного изобретения содержит новое производное триазина общей формулы (I) по данному изобретению или его соль в качестве активного ингредиента. Эти соединения используют путем смешивания их с жидким носителем, таким как растворитель, или с твердым носителем, таким как тонкий минеральный порошок, и приготовления полученных смесей в форме смачиваемого порошка, эмульгируемого концентрата, дуста или гранул. Когда готовят указанные выше составы, может быть добавлено поверхностно-активное вещество для придания указанным соединениям эмульгируемости,диспергируемости или распространяемости. Когда гербицид данного изобретения используют в виде смачиваемого порошка, обычно 10 - 55 мас.% производного триазина (I) или его соли по данному изобретению, 40 - 88 мас.% твердого носителя и 2 - 5 мас.% поверхностноактивного вещества смешивают для получения состава, и состав может быть использован. Когда гербицид данного изобретения используют в виде эмульгируемого концентрата,обычно достаточно получить состав путем смешивания 20 - 50 мас.% производного триазина(I) или его соли по данному изобрететению, 35 75 мас.% растворителя и 5 - 15 мас.% поверхностно-активного вещества. Когда гербицид данного изобретения используют в виде дуста, обычно достаточно получить состав путем смешивания 1 - 15 мас.% производного триазина (I) или его соли по данному изобретению, 80 - 97 мас.% твердого носителя и 2 - 5 мас.% поверхностно-активного вещества. Далее, когда гербицид данного изобретения используют в форме гранул, обычно достаточно получить состав путем смешивания 1-15 мас.% производного триазина (I) или его соли по данному изобретению, 80-97 мас.% твердого носителя и 2-5 мас.% поверхностно-активного вещества. Упомянутый твердый носитель выбирают из тонких минеральных порошков, и примеры тонких минеральных порошков включают оксиды, такие как диатомовая земля и гашеная известь, фосфаты, такие как апатит, сульфаты,такие как гипс, и силикаты, такие как тальк, пироферрит, глина, каолин, бентонит, кислая глина, белая сажа, порошкообразный кварц и порошкообразный кремнезем. Растворитель выбирают из органических растворителей. Конкретные примеры растворителей включают ароматические углеводороды, 000711 12 такие как бензол, толуол и ксилол, хлорированные углеводороды, такие как о-хлортолуол,трихлорэтан и трихлорэтилен, спирты, такие как циклогексанол, амиловый спирт и этиленгликоль, кетоны, такие как изофорон, циклогексанон и циклогексенил-циклогексанон, простые эфиры, такие как бутилцеллозольв, диэтиловый эфир и метилэтиловый эфир, сложные эфиры,такие как изопропилацетат, бензилацетат и метилфталат, амиды, такие как диметилформамид,и их смеси. Кроме того, поверхностно-активное вещество может быть выбрано из анионогенных поверхностно-активных веществ, неионогенных поверхностно-активных веществ, катионогенных поверхностно-активных веществ и амфотерных поверхностно-активных веществ (аминокислота и бетаин). Гербицид данного изобретения может содержать в качестве активного ингредиента другой гербицидно активный компонент, когда требуется, в сочетании с производным триазина(I) или его солью. "Другой" гербицидно активный компонент включает известные гербициды,такие как фенокси-, дифениловый эфир-, триазин-, мочевина-, карбамат-, тиолкарбамат, кислотный анилид-, пиразол-, фосфорную кислоту-,сульфонилмочевинаи оксадиазонсодержащие гербициды, и он может быть соответственно выбран из этих гербицидов, когда необходимо. Кроме того, гербицид данного изобретения может быть использован как смесь с каким-либо одним из инсектицидов, бактерицидов, регуляторов роста растений и удобрений. Данное изобретение будет конкретно объяснено ниже со ссылкой на Примеры и Примеры гербицидов, в то же время данное изобретение не должно ограничиваться ими. Пример 1. 0,95 г (5,2 ммоль) гидрохлорида 1 аминотетралина и 0,44 г (5,2 ммоль) цианогуанидина добавляют к 20 мл н-декана и смесь перемешивают при нагревании при 135 С в течение 6 ч. После завершения реакции реакционную смесь охлаждают, образовавшийся осадок извлекают путем фильтрования и промывают 5 мл н-гексана три раза и растворитель удаляют при пониженном давлении, чтобы получить твердое вещество. 1 г полученного твердого вещества растворяют в 25 мл абсолютного метанола и к полученному раствору добавляют 1,9 г (10 ммоль) 28 мас.% раствора метоксид натрия/метанол при комнатной температуре. Далее по каплям добавляют 1,2 г (10 ммоль) этил-фторпропионата и смесь перемешивают при комнатной температуре 12 ч. После завершения реакции реакционную смесь выливают в 100 мл воды и проводят экстракцию 50 мл этилацетата три раза. Полученный слой этилацетата сушат над безводным сульфатом натрия и этилацетат отгоняют при пониженном давлении. Получен 13 ный в результате остаток очищают колоночной хроматографией на силикагеле (элюент: гексан/этилацетат = 1/1 (объемное отношение,чтобы получить 0,68 г 2-амино-4-(-фторэтил)6-(1'-тетралиниламино)-s-триазина в качестве конечного продукта в форме белых кристаллов. Таблица 1, которая будет описана ниже, показывает структурные формулы соли производного циклоалкиламина и сложного эфира, которые оба используются в качестве исходных материалов, и структурные формулы полученного производного триазина и его выход. Таблица 8,которая будет описана далее, показывает ИК и ЯМР данные полученного производного триазина. Примеры 2-4. Производные триазина как конечные продукты получают тем же способом, как в примере 1, за исключением того, что этил-фторпропионат заменяют сложными эфирами,показанными в таблице 1. Таблица 1, которая будет описана далее, показывает структурные формулы соли производного циклоалкиламина и сложных эфиров, которые оба используются в качестве исходных материалов, и структурные формулы полученных производных триазина и их выходы. Таблица 8, которая приводится далее, показывает ИК и ЯМР данные полученных производных триазина. 14 Таблицы 2 и 3, которые будут описаны далее,показывают структурные формулы солей производных циклоалкиламина и сложных эфиров,которые оба используются в качестве исходных материалов, структурные формулы полученных производных триазина и их выходы. Таблица 8,которая приводится далее, показывает ИК и ЯМР данные полученных производных триазина. Таблица 2 Ппримеры 5-8. Производные триазина, как конечные продукты, получают тем же способом, как в примере 1, за исключением того, что гидрохлорид 1 аминотетралина заменяют солями производных циклоалкиламина, показанными в таблице 2. Пример 9. К 20 мл н-декана добавляют 1,1 г (5,6 ммоль) гидрохлорида 1-амино-2-метилтетралина и 0,48 г (5,6 ммоль) цианогуанидина и смесь перемешивают при нагревании при 135 С в течение 6 ч. После завершения реакции реакционную смесь охлаждают, образовавшийся осадок извлекают путем фильтрования и промывают 5 мл н-гексана три раза и растворитель удаляют при пониженном давлении, чтобы получить твердое вещество. 1 г полученного твердого вещества растворяют в 25 мл абсолютного метанола и к полученному раствору добавляют 2,5 г (13 ммоль) 28 мас.% раствора метоксид натрия/метанол при комнатной температуре. Далее, по каплям добавляют 1,85 г (13 ммоль) этилтрифторацетата и смесь перемешивают при комнатной температуре 12 ч. После завершения реакции реакционную смесь выливают в 100 мл воды и проводят экстракцию 50 мл этилацетата три раза. Полученный слой этилацетата сушат над безводным сульфатом натрия и этилацетат отгоняют при пониженном давлении. Полученный в результате остаток очищают колоночной хроматографией на силикагеле (элюент : гексан/этилацетат = 1/1 (объемное отношение,чтобы получить 1,0 г 2-амино-4-трифторметил 6-(2'-метил-1'-тетралиниламино)-s-триазина в качестве конечного продукта в форме белых кристаллов. Таблица 4, которая будет описана позднее, показывает структурные формулы соли производного циклоалкиламина и сложного эфира, которые оба используются в качестве исходных материалов, структурную формулу полученного производного триазина и его выход. Таблица 8, которая будет описана далее,показывает ИК и ЯМР данные полученного производного триазина. Таблица 4 16 исходных материалов, структурную формулу полученного производного триазина и его выход. Таблица 8, которая будет описана далее,показывает ИК и ЯМР данные полученного производного триазина. Примеры 11-14. Производные триазина, как конечные продукты, получают тем же способом, как в примере 10, за исключением того, что метил-фторизобутират заменяют сложными эфирами,показанными в таблицах 5 и 6. Таблицы 5 и 6,которые будут описаны далее, показывают структурную формулу соли производного циклоалкиламина и сложных эфиров, которые оба используются в качестве исходных материалов,и структурные формулы полученных производных триазина и их выходы. Таблица 9, которая приводится далее, показывает ИК и ЯМР данные полученных производных триазина. Таблица 5(5,6 ммоль) цианогуанидина и смесь перемешивают при нагревании при 135 С в течение 6 ч. После завершения реакции реакционную смесь охлаждают, образовавшийся осадок извлекают путем фильтрования и промывают 5 мл нгексана три раза и растворитель удаляют при пониженном давлении, чтобы получить твердое вещество. 1 г полученного твердого вещества растворяют в 25 мл абсолютного метанола и к полученному раствору добавляют 2,5 г (13 ммоль) 28 мас.% раствора метоксид натрия/метанол при комнатной температуре. Далее по каплям добавляют 1,56 г (13 ммоль) метилфторизобутирата и смесь перемешивают при комнатной температуре 12 ч. После завершения реакции реакционную смесь выливают в 100 мл воды и проводят экстракцию 50 мл этилацетата три раза. Полученный слой этилацетата сушат над безводным сульфатом натрия и этилацетат отгоняют при пониженном давлении. Полученный в результате остаток очищают колоночной хроматографией на силикагеле (элюент : гексан/этилацетат = 1/1 (объемное отношение, чтобы получить 0/99 г 2-амино-4-(-фтор-метилэтил)-6-(1'-инданиламино)-s-триазина в качестве конечного продукта в форме белых кристаллов. Таблица 5, которая будет описана позднее, показывает структурные формулы соли производного циклоалкиламина и сложного эфира, которые оба используются в качестве Пример 15-17. Производные триазина, как конечные продукты, получают тем же способом, как в примере 10, за исключением того, что гидрохлорид 1 аминотетралина заменяют солями производных циклоалкиламина, показанными в таблице 7. Таблица 7, которая будет описана далее, пока 17 зывает структурные формулы солей производных циклоалкиламина и сложных эфиров, которые оба используются в качестве исходных материалов, структурные формулы полученных производных триазина и их выходы. Таблица 9,которая приводится далее, показывает ИК и ЯМР данные полученных производных триазина. 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS) Примеры 18-31. Производные триазина, как конечные продукты, получают из солей производных циклоалкиламина и сложных эфиров, показанных в таблицах 10-14, таким же способом, как в примерах 1-17. Таблицы 10-14, приводимые далее,показывают структурные формулы солей производных циклоалкиламина и сложных эфиров,которые оба используются как исходные материалы, структурные формулы полученных производных триазина и их выходы. Таблица 10 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). Пример 32. 0,98 г (5,2 ммоль) гидрохлорида 6-фтор-4 хроманиламина, 0,44 г (5,2 ммоль) цианогуанидина и 20 мл н-декана помещают в реактор и перемешивают при 135 С в течение 6 ч. После завершения реакции реакционную смесь охлаждают, образовавшийся осадок извлекают путем фильтрования и промывают 5 мл н-гексана три раза и растворитель, содержащийся в полученном осадке, удаляют при пониженном давлении,чтобы получить 1 г твердого вещества. Это твердое вещество растворяют в 25 мл абсолютного метанола. К полученному раствору добавляют 1,9 г (10 ммоль) 28 мас.% раствора метоксид натрия/метанол при комнатной температуре. Затем по каплям добавляют 1,2 г (10 ммоль) метилфторизобутирата и смесь перемешивают при комнатной температуре 12 ч. После завершения реакции реакционную смесь выливают в 100 мл воды и проводят экстракцию 50 мл этилацетата три раза. Полученный слой этилацетата сушат над безводным сульфатом натрия и этилацетат отгоняют при пониженном давлении. Полученный в результате остаток очищают колоночной хроматографией на силикагеле 2-амино-4-(-фторметилэтил)-6-(6-фтор-4 хроманил)амино-s-триазина в качестве конечного продукта в форме белых кристаллов. Таблица 15 показывает структуру и выход полученного продукта, и таблица 33 показывает ИК и ЯМР данные для него. Примеры 33-38. Те же процедуры, как в примере 32, повторяют за исключением того, что метил-фторизобутират, используемый в примере 32,заменяют сложными эфирами, показанными в таблице 15 или 16. Таблица 15 или 16 показывает структуры и выходы полученных продуктов,и таблица 33 показывает ИК и ЯМР данные полученных продуктов. 22 Примеры 39-75. Те же процедуры, как в примере 32, повторяют за исключением того, что гидрохлорид 6 фтор-4-хроманиламина, используемый в примере 32,заменяют гидрохлоридами 4 хроманиламина, показанными в таблицах 17-25. Таблицы 17-25 показывают структуры и выходы полученных продуктов, и таблицы 33-37 показывают ИК и ЯМР данные полученных продуктов. Таблица 17 Примеры 76-97. Те же процедуры, как в примере 32, повторяют за исключением того, что гидрохлорид 6 фтор-4-хроманиламина и метилфторизобутират, используемые в примере 32, заменяют гидрохлоридами 4-хроманиламина и сложными эфирами, показанными в таблицах 26-31. Таблицы 26-31 показывают структуры и выходы полученных продуктов и таблицы 37-40 показывают ИК и ЯМР данные полученных продуктов. Таблица 26 30 слой экстрагируют этилацетатом и экстракт сушат над безводным сульфатом натрия. Затем растворитель отгоняют при пониженном давлении. Полученный в результате остаток очищают колоночной хроматографией на силикагеле [силикагель: 150 г, элюент: н-гексан/этилацетат = 1/1 (объемное отношение)], чтобы получить 2,4 г(выход 87%) 2-амино-4-(6-циано-4 хроманил)амино-6-(-фторметилэтил)-sтриазина в качестве конечного продукта. Таблица 32 показывает структуру и выход полученного продукта ,и таблица 40 показывает ИК и ЯМР данные продукта. Таблица 32 Пример 98. 1 г (2,87 ммоль) 2-амино-4-(-фтор-(метилэтил)-6-(6-метилтио-4-хроманил)амино-sтриазина, полученного в примере 48, растворяют в 15 мл этилацетата и к этой смеси добавляют 1,1 г (6,38 ммоль) м-хлорпербензойной кислоты при комнатной температуре. Реакционную смесь перемешивают при комнатной температуре 12 ч и затем промывают 10 мл 5 мас.% водного раствора сульфита натрия и слой этилацетата промывают 10 мл воды дважды. Слой этилацетата сушат над безводным сульфатом натрия и затем этилацетат отгоняют при пониженном давлении. Полученный в результате остаток очищают колоночной хроматографией на силикагеле (элюент: н-гексан/этилацетат = 1/1 (объемное отношение, чтобы получить 0,89 г (выход 82%) 2-амино-4-(-фторметилэтил)-6-(6-метансульфонил-4-хроманил)аминоs-триазина в качестве конечного продукта. Таблица 32 показывает структуру и выход полученного продукта, и таблица 40 показывает ИК и ЯМР данные продукта. Примеры 99. 2-Амино-4-(-фторметилэтил)-6-(8 метансульфонил-4-хроманил)амино-s-триазин получают тем же способом, как в примере 98, за исключением того, что 2-амино-4-(-фтор-метилэтил)-6-(6-метилтио-4-хроманил)амино-sтриазин, используемый в примере 98, заменяют 2-амино-4-(-фторметилэтил)-6-(8-метилтио 4-хроманил)амино-s-триазином. Таблица 32 показывает структуру и выход полученного продукта ,и таблица 40 показывает ИК и ЯМР данные продукта. Пример 100. 0,9 г (10,0 ммоль) цианида меди (I) добавляют к раствору 3,2 г (8,4 ммоль) 2-амино-4-(6 бром-4-хроманил)амино-6-(-фторметилэтил)-s-триазина, полученного в примере 50, в 3 мл DMF и смесь нагревают с обратным холодильником в течение 4 ч. К реакционной смеси добавляют насыщенный водный раствор хлорида аммония, смесь фильтруют и твердое вещество промывают этилацетатом. Фильтрат и промывочную жидкость объединяют, органический 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS); 3 Растворитель: Дейтероацетон; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). 4 Растворитель: Дейтерохлороформ + дейтерометанол; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS) 3 Растворитель: Дейтероацетон; Внутренний стандарт: Тетраметилсилан (TMS). 4 Растворитель: Дейтерохлороформ + дейтерометанол; Внутренний стандарт: Тетраметилсилан (TMS). Таблица 39. Данные ИК ЯМР 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS). 1 Метод с использованием таблетки бромида калия; 2 Растворитель: Дейтерохлороформ; Внутренний стандарт: Тетраметилсилан (TMS); 3 Растворитель: Дейтероацетон; Внутренний стандарт: Тетраметилсилан (TMS); 4 Растворитель: Дейтерохлороформ + дейтерометанол; Внутренний стандарт: Тетраметилсилан (TMS).Zeaklite) в качестве носителя, 1,5 мас.ч. алкиларилсульфоната (товарное наименование: Neoplex, поставляемый фирмой Kao-Atias К. К.) в качестве поверхностно-активного вещества и 1,5 мас.ч. неионогенного и анионогенного поверхностно-активного вещества (товарное наименование: Sorpol 800A, поставляемый фирмой Toho Chemical Co., Ltd.) равномерно распыляют и смешивают для получения носителя для смачиваемого порошка. 90 мас. ч. указанного выше носителя для смачиваемого порошка и 10 мас.ч. одного из соединений данного изобретения, полученных в примерах 1-3, 5-13, 15, 16, 32-90, 98 и 99 (Номера примеров используются как номера соединений) равномерно распыляют и смешивают для получения гербицидов.(2) Испытание обработки после появления всходов. Семена сорняков, таких как дурнишник,канатник, вьюнок пурпурный, горец бледный,дурман обыкновенный, ширица колосистая и паслен черный, и семена хлопчатника высевают в вегетационные сосуды Вагнера размером 1/5000 ара, заполненные почвой плакорных условий и покрытые почвой плакорных условий. Семена выращивают в теплице и на стадии 1-2 листьев у этих растений на листья и стеблевые части равномерно распыляют суспензию заданного количества гербицида, приготовленного,как указано выше в (1), и суспендированного в воду при расходе 2000 литров/гектар. Затем растения выращивают в теплице и на 20 сутки после обработки оценивают гербицид по его гербицидной эффективности и фитотоксичности для культуры. Таблицы 41-44 показывают результаты. Гербицидная эффективность и фитотоксичность показаны соответственно следующим оценкам. Отношение остаточной массы растения к массе растения на необработанной делянке (%) Отношение остаточной массы растения к массе растения на необработанной делянке (%) Отношение остаточной массы растения к массе растения на необработанной делянке определяют на основе отношения остаточной массы растения к массе растения на необработанной делянке = (остаточная масса растения на обработанной делянке/масса растения на необработанной делянке)х 100. Таблица 41. Испытание обработки после появления всходов Гербицидная эффективность ДозиАктивный инФитотоксичность гредиент в гер- ровка,АА ВВ СС Таблица 42. Испытание обработки после появления всходов ДозиГербицидная эффективность ровка,АА ВВ СС" 5 5 4 5 5 5 5 АА - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -горец бледный, ЕЕ - дурман обыкновенный, FF - ширица колосистая GG - паслен черный Таблица 43. Испытание обработки после появления всходов Активный инДозиГербицидная эффективность Фитотоксичность гредиент в гер- ровка,для хлопчатникаAA - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -горец бледный, ЕЕ - дурман обыкновенный, FF - ширица колосистая GG - паслен черный Таблица 44. Испытание обработки после появления всходов ДозиАктивный инГербицидная эффективность Фитотоксичность гредиент в гер- ровка,для хлопчатника АА ВВ СС" 3 3 3 4 5 4 5 АА - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD - горец бледный, ЕЕ - дурман обыкновенный, FF - ширица колосистая, GG - паслен черный. Результаты в таблицах 41-44 показывают,что гербицид, содержащий производное триазина данного изобретения, может подавлять широкий спектр наземных сорняков при низкой дозировке, не оказывая фитотоксичного воздействия на хлопчатник при обработке после появления всходов. Все указанные выше соединения 2, 7, 9, 13, 15, 34, 35, 37, 50, 54, 61, 62, 73, 76 и 85 проявляют высокую безопасность для хлопчатника и проявляют высокую гербицидную эффективность против канатника, принадлежа щего к сорнякам семейства мальвовых, к которому принадлежит и хлопчатник, и они, в особенности, имеют превосходную внутриродовую селективность.(3) Испытание обработки почвы плакорных условий до появления всходов. Семена сорняков, таких как дурнишник,канатник, вьюнок пурпурный, дурман обыкновенный, ширица колосистая, щетинник зеленый и росичка кровяная, и семена хлопчатника высевают в горшки Wagner размером 1/5000 ара, 39 заполненные почвой плакорных условий и покрытые почвой плакорных условий. Затем заданное количество гербицида, полученного, как указано выше в (1), суспендируют в воде и равномерно распыляют на поверхность почвы. Затем семена выращивают в теплице и на 20 сутки после обработки оценивают гербицид по его 40 гербицидной эффективности и фитотоксичности для культуры. Таблицы 45-48 показывают результаты. Данные гербицидной эффективности и фитотоксичности для культуры показаны на основе оценок, показанных в (2) испытании обработки после появления всходов. Таблица 45. Испытание обработки почвы плакорных условий до появления всходов Гербицидная эффективность Активный инДозиФитотоксичность гредиент в гер- ровка,для хлопчатника АА ВВ СС+ АА - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -дурман обыкновенный, ЕЕ - ширица колосистая, FF - щетинник зеленый, GG - росичка кровяная. Таблица. 46. Испытание обработки почвы плакорных условий до появления всходов ДозиАктивный инГербицидная эффективность Фитотоксичность гредиент в гер- ровка,для хлопчатника АА ВВ СС+ АА - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -дурман обыкновенный, ЕЕ - ширица колосистая, FF - щетинник зеленый, GG - росичка кровяная. Таблица 47. Испытание обработки почвы плакорных условий до появления всходов ДозиАктивный инГербицидная эффективность Фитотоксичность гредиент в гер- ровка,для хлопчатника АА ВВ СС" 3 5 3 5 5 5 5 АА - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -дурман обыкновенный, ЕЕ - ширица колосистая, FF - щетинник зеленый, GG - росичка кровяная. Таблица 48. Испытание обработки почвы плакорных условий до появления всходов ДозиАктивный инГербицидная эффективность Фитотоксичность гредиент в гер- ровка,для хлопчатникаAA - дурнишник, ВВ - канатник, СС - вьюнок пурпурный, DD -дурман обыкновенный, ЕЕ - ширица колосистая, FF - щетинник зеленый, GG - росичка кровяная. Результаты в таблицах 45-48 показывают,что гербицид, содержащий производное триазина данного изобретения, может подавлять широкий спектр наземных сорняков при низкой дозировке, не оказывая фитотоксичного воздействия на хлопчатник при обработке до появления всходов. Все указанные выше соединения 1,2, 13, 15, 34, 35, 37, 44, 46, 48, 49, 50, 52, 53, 54,59, 60, 65, 71, 73, 80, 84, 86 и 89 проявляют высокую безопасность для хлопчатника и проявляют высокую гербицидную эффективность против канатника, принадлежащего к сорнякам семейства мальвовых, к которому принадлежит и хлопчатник, и они, в особенности, имеют превосходную внутриродовую селективность. Промышленная полезность Производное триазина данного изобретения не оказывает фитотоксичного воздействия на хлопчатник и может избирательно подавлять,при низкой дозировке, широкий спектр сорняков, включая канатник, принадлежащий к сорнякам семейства мальвовых, к которому принадлежит и хлопчатник, и производное триазина данного изобретения является, следовательно,весьма эффективным в качестве активного ин 43 гредиента гербицида для нанесения на хлопковые поля. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производное триазина общей формулы где X представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу, C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу, C1-C4 алкилсульфонильную группу, C1C6 галогеналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу при условии, что, когда заместителей Х несколько, они могут быть одинаковыми или отличными друг от друга, или два соседних заместителя Х могут образовывать насыщенное или ненасыщенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью в бензольном кольце, n обозначает целое число 0 или 1-4,R представляет(2) замещенную C1-C6 алкильную группу,имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего изiii) C1-C8 алкоксигруппы, алкильная часть которой может содержать гетероатом, иY представляет С 2-С 4 алкиленовую группу,которая может быть замещена 1-8 C1-C6 алкильными группами, или двухвалентную группу формулы (а), где каждый из Y1 - Y4 независимо представляет атом водорода или C1-С 4 алкильную группу. 2. Производное триазина по п.1, где Х представляет C1-C4 алкильную группу или атом галогена. 3. Производное триазина по п.1, где Х выбран из класса, состоящего из метокси, метилтио, метилсульфонила, трифторметила, трифторметокси, феноксиэтила, фенила и фенокси. 4. Производное триазина по п.2, где n представляет целое число 1 или 2. 5. Производное триазина по п.4, где, когдаn равно 2, каждый из двух заместителей Х является независимо C1-C6 алкильной группой или атомом галогена. 44 6. Производное триазина по п.1, где n равно 0. 7. Производное триазина по п.1, где Y представляет группу пропилена, которая замещена одной C1-C4 алкильной группой. 8. Производное триазина по п.7, где Y представляет группу пропилена, которая замещена метилом. 9. Производное триазина по п.1, где Y является двухвалентной группой формулы (а), где каждый из Y1 - Y4 независимо представляет атом водорода или C1-C4 алкильную группу. 10. Производное триазина по п.9, где каждый из Y1-Y4 независимо представляет атом водорода или метил. 11. Производное триазина по п.1, где R представляет C1-C6 алкильную группу. 12. Производное триазина по п.1, где R представляет C1-C6 алкильную группу, которая замещена атомом фтора, атомом хлора или атомом брома. 13. Производное триазина по п.12, где R выбирают из класса, состоящего из -СF3, -ССl3,-CH2F, -CH2Cl, -CH2Br, -C2F5, -CH2CH2F,-СНF(СН 3),-СНСl(СН 3),-CHBr(СН 3),-СНF(СF3), -СF(СН 3)2, -ССl(СН 3)2, -СВr(СН 3)2,-СНF(СН 2 СН 3),-СНСl(СН 2 СН 3) и-CHBr(СН 2 СН 3) групп. 14. Производное триазина по п.1, где R представляет C1-C6 алкильную группу, которая замещена гидроксильной группой. 15. Производное триазина по п.14, где R выбирают из класса, состоящего из -СН 2 ОН,-СН(ОН)СН 3,-СН(ОН)С 2 Н 5,-С 2 Н 4 ОН,-С(СН 3)2OН и -С(СН 3)2 СН 2 ОН групп. 16. Производное триазина по п.1, где R является C1-C6 алкильной группой, замещенной группой, в которой гетероциклическая группа,содержащая атом кислорода, и атом кислорода связаны друг с другом. 17. Способ получения производного триазина общей формулы (I) где Х представляет атом галогена, гидроксильную группу, цианогруппу, C1-C6 алкильную группу, C1-C4 алкоксигруппу, C1-C4 алкилтиогруппу, C1-C4 алкилсульфонильную группу, C1C6 галогеналкильную группу, C1-C4 галогеналкоксигруппу, фенилзамещенную C1-C4 алкильную группу, фенильную группу или феноксигруппу, при условии что, когда заместителей Х несколько, они могут быть одинаковыми или отличными друг от друга, или два соседних заместителя Х могут образовывать насыщенное или ненасыщенное пятичленное или шестичленное кольцо вместе с углерод-углеродной связью в бензольном кольце, n представляет целое число 0 или 1-4, R представляет(2) замещенную C1-C6 алкильную группу,имеющую от 1 до 13 заместителей одного или двух видов, выбранных из класса, состоящего изiii) C1-C6 алкоксигруппы, алкильная часть которой может содержать гетероатом, иY представляет C2-C4 алкиленовую группу,которая может быть замещена 1-8 C1-C6 алкильными группами, или двухвалентную группу формулы (а), 46 где каждый из Y1-Y4 независимо представляет атом водорода или C1-C4 алкильную группу,включает взаимодействие соединения общей формулы (II) и затем взаимодействие продукта реакции со сложным эфиром общей формулы (IV),RCOOR1(IV) где R имеет значения, определенные выше, и R1 представляет C1-C4 алкильную группу. 18. Гербицид, содержащий производное триазина общей формулы I по п.1 или его соль в качестве активного ингредиента.
МПК / Метки
МПК: A01N 43/68, C07D 251/18
Метки: применение, гербицидов, способ, триазина, производные, получения, качестве
Код ссылки
<a href="https://eas.patents.su/24-711-proizvodnye-triazina-sposob-ih-polucheniya-i-primenenie-v-kachestve-gerbicidov.html" rel="bookmark" title="База патентов Евразийского Союза">Производные триазина, способ их получения и применение в качестве гербицидов</a>
Предыдущий патент: (имидазол-5-ил) метил-2-хинолиноновые производные, ингибирующие фарнезилпротеин-трансферазу.
Следующий патент: Способ получения нефтяных фракций












