Новые производные эритромицина, способ их получения и их применение в качестве медикаментов
Номер патента: 2168
Опубликовано: 28.02.2002
Авторы: Дени Алексис, Пежак Жан-Мари, Шанто Жан-Франсуа, Агуридас Константэн
Формула / Реферат
1. Производные эритромицина формулы I
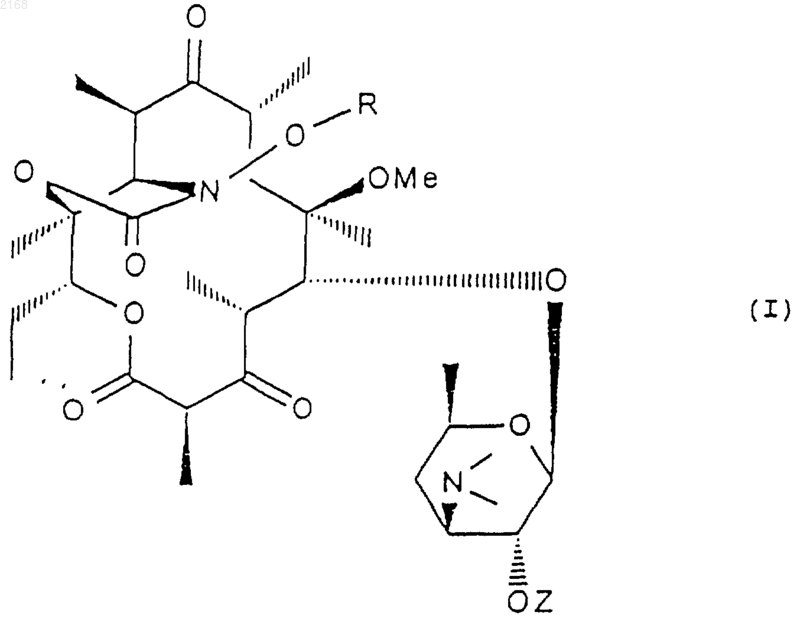
в которой R означает атом водорода; алкильный радикал, содержащий до 12 атомов углерода, который может быть замещен галогеном или радикалами (СН2)mАr или
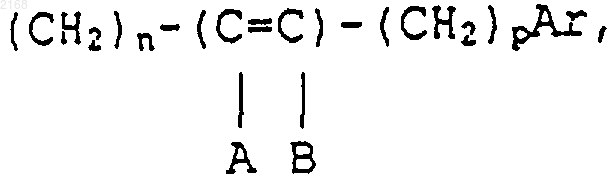
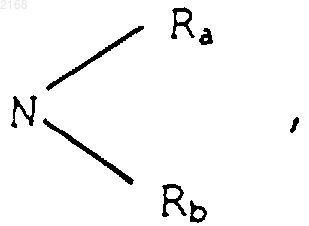
где Ra и Rb, одинаковые или различные - атом водорода или алкил, содержащий до 12 атомов углерода, радикал 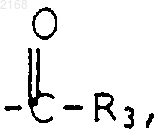
в котором R3 - алкил, содержащий до 12 атомов углерода, или арил или гетероарильный радикал с 5 или 6 звеньями, содержащий один или несколько гетероатомов, которые могут быть замещены одним или несколькими заместителям, указанными выше, и Z - атом водорода или остаток карбоновой кислоты, содержащей до 18 атомов углерода.
2. Соединения формулы I по п.1, в которых Z - атом водорода.
3. Соединения формулы I по п.1 или 2, в которых R - атом водорода.
4. Соединения формулы I по пп.1, 2 или 3, в которых R означает группу (СН2)mАr, где m и Аr имеет то же значение, что и в п.1.
5. Соединения формулы I по п.4, в которых R означает группу (СН2)m'Аr, где m' - целое число 3, 4, 5 или 6.
6. Соединения формулы I по п.5, в которых Аr - радикал 4-хинолинил, который может иметь заместители в одном и/или в другом из двух циклов хинолина.
7. Соединения формулы I по п.6, в которых Аr представляет собой незамещенный 4-хинолинил.
8. Соединения формулы I по п.5, в которых Аr представляет собой радикал формулы
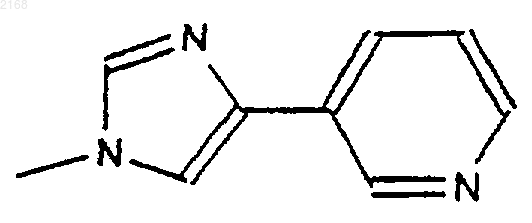
который может иметь заместители в одном и/или в другом из двух циклов.
9. Соединения формулы I по п.8, в которых Аr не имеет заместителей.
10. Соединения формулы I по п.1, имеющие следующие названия:
11,12-дидезокси-3-де[(2,6-дидезокси-3-С-метил-3-О-метил-альфа-L-рибогексопиранозил)окси]-6-O-метил-3-оксо-12,11-{оксикарбонил[3-(4-хинолинил)пропокси]имино}эритромицин.
11. Соединения формулы I, описанные в любом из пп.1-10, в качестве медикаментов.
12. Фармацевтическая композиция, содержащая в качестве активного начала, по меньшей мере, один медикамент в соответствии с п.11.
13. Способ получения соединений формулы I в соответствии с любым из пп.1-10, отличающийся тем, что соединение формулы II
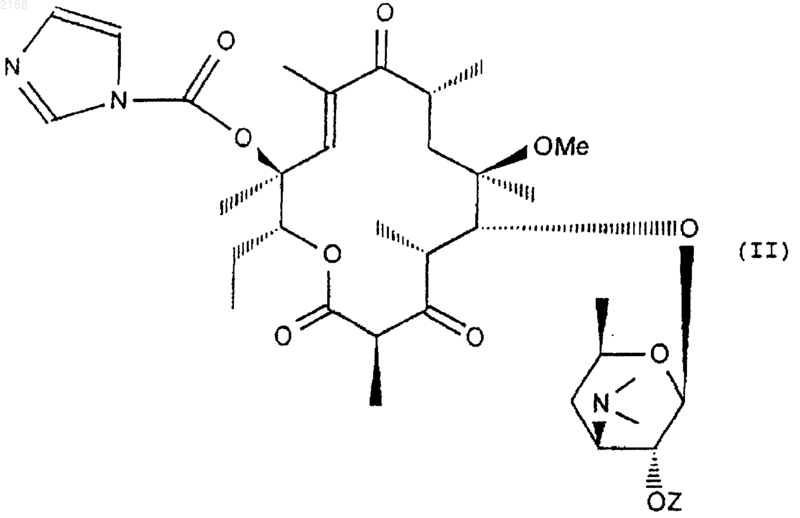
в которой Z имеет значения, описанные в п.1, подвергают взаимодействию с гидроксиламином или его галогенгидратом с получением соединения формулы IA
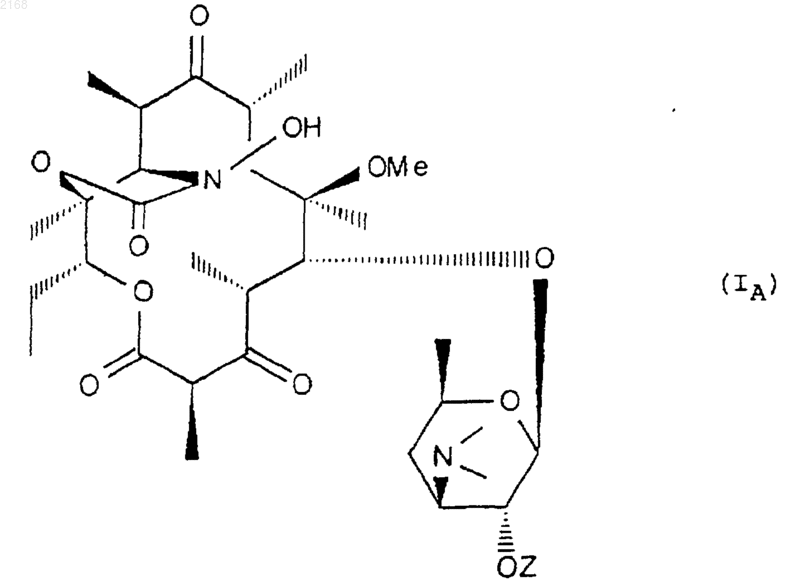
которое при желании подвергают действию реагента, осуществляющего метанолиз гидроксила в положении 2', с целью получения соответствующего соединения формулы IB, в котором Z означает атом водорода
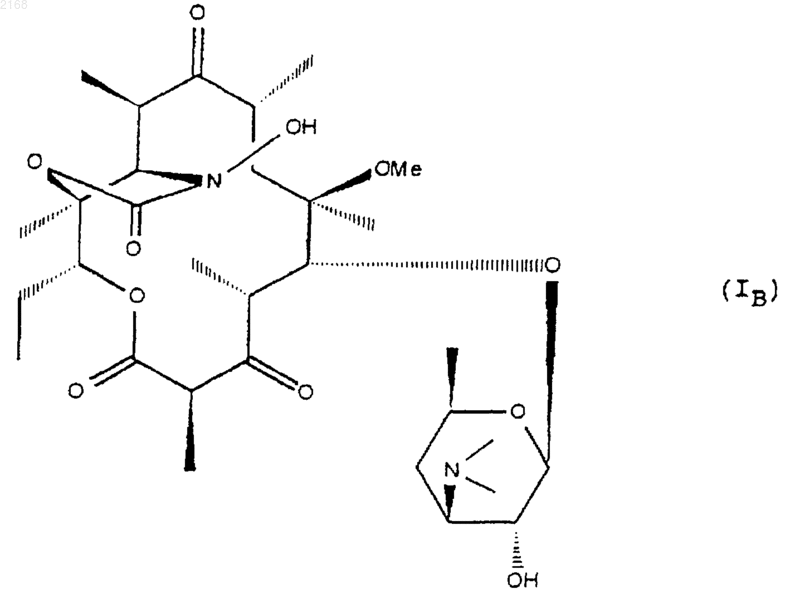
после чего соединение IA или IB вводят в реакцию с соединением формулы
R'Hal (III),
в которой R' имеет то же значение, что и R, за исключением водорода, a Hal является атомом галогена, с целью получения соответствующего соединения формулы IC, которое может быть подвергнуто действию агента гидрирования возможной двойной связи в радикале
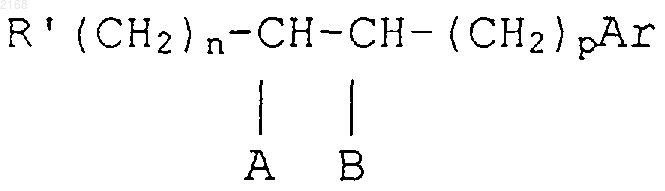
и/или агента, освобождающего гидроксильную группу в положении 2'.
14. Соединения формулы (III), имеющие следующие названия:
4-(3-иодопропил)-хинолин,
3-[1-(3-бромпропил)-1Н-имидазол-4-ил]-пиридин
в качестве промежуточных продуктов.
Текст
1 Настоящее изобретение касается новых производных эритромицина, способа их получения и их применения в качестве антибиотиков. Объектом изобретения являются соединения формулы I 2 в котором R3 - алкил, содержащий до 12 атомов углерода, или арил или гетероарильный радикал с 5 или 6 звеньями, содержащий один или несколько гетероатомов, которые могут быть замещены одним или несколькими указанными выше заместителями. В качестве предпочтительных гетероарильных радикалов могут быть названы следующие радикалы: в которой R означает атом водорода; алкильный радикал, содержащий до 12 атомов углерода,который может быть замещен галогеном или радикалами (CH2)mAr или в которых m - целое число от 1 до 8, n и p, одинаковые или различные, означают целые числа от 0 до 6; А и В, одинаковые или различные,означают атом водорода или галогена или алкил, содержащий до 8 атомов углерода; Ar арильный или гетероарильный радикалы, возможно замещенные, и Z - атом водорода или остаток карбоновой кислоты, содержащей до 18 атомов углерода. В приведенном выше описании заместителей алкильный радикал может означать метил,этил, пропил, изопропил, н-бутил, изо- или третбутил, циклобутил, циклопентил, циклогексил,децил или додецил. Галоген преимущественно является атомом фтора, хлора или брома. Арильный радикал может быть фенилом или нафтилом. Гетероарильный радикал может представлять собой тиенил, фурил, пирролил,тиазолил, оксазолил, имидазолил, тиадиазолил,пиразолил или изопиразолил, пиридил, пиримидил, пиридазинил или пиразинил, а также индолил, бензофуранил, бензотиазил или хинолинил. Арильный или гетероарильный радикалы могут быть замещены одним или несколькими заместителями из группы, в которую входят гидроксил, атомы галогена, радикалы NO2 и CN, алкил, алкенил или алкинил, O-алкал, O-алкенил или O-алкинил, S-алкил, S-алкенил или Sалкинил, N-алкил, N-алкенил и N-алкинил, содержащие до 12 атомов углерода, которые могут быть замещены одним или несколькими атомами галогена радикал где Ra и Rb, одинаковые или различные - атом водорода или алкил, содержащий до 12 атомов углерода, радикал гетероциклические радикалы, описанные в заявках Европейских патентов 487411, 596802,676409 и 680967. Радикалы могут быть замещены одним или несколькими названными выше заместителями. Более конкретно, объектом изобретения являются соединения формулы I, в которой Z атом водорода, соединения формулы I, в которой R - атом водорода, соединения формулы I, в которой R означает (СН 2)mАr, где m и Аr сохраняют указанные выше значения, в частности, те(CH2)m'Ar, где m'=3, 4, 5 или 6, как, например,соединения, в которых Аr означает 4 хинолинил, который может быть замещен в одном или обоих циклах хинолинила; и в особенности те соединения формулы I, в которых Аr представляет собой незамещенный 4 хинолинил, или же соединения формулы I, в которой Аr означает радикал который может быть замещен в одном и/или в другом из двух циклов, и наиболее предпочтительно те соединения, в которых радикал Аr не имеет заместителей. Наиболее конкретно, объектом изобретения являются соединения, получение которых приведено ниже в экспериментальной части, в частности, соединение из примера 4. Продукты общей формулы I обладают очень высокой антибиотической активностью в отношении грам-положительных бактерий, таких как стафилококки, стрептококки и пневмококки. Соединения согласно изобретению могут таким образом быть использованы в качестве медикаментов при лечении инфекций, вызванных чувствительными к медикаментам возбудителями, при лечении стафилококковых инфекций, таких как стафилококковый сепсис, злокачественные стафилококковые заболевания лица и злокачественные кожные болезни, пиодермиты, септические и гнойные раны, фурункулы,карбункулы, флегмоны, рожи, угри; такие стафилококковые инфекции как самостоятельные или послегрипповые ангины, бронхопневмонии,гнойные легочные заболевания, такие стрептококковые инфекции как острые ангины, отиты,синуситы, скарлатина; такие пневмококковые инфекции как пневмонии и бронхиты; бруцеллез, дифтерия и гонококковая инфекция. Продукты настоящего изобретения обладают также активностью в отношении инфекций, вызванных такими возбудителями как Наеmоphilus influenzae, Rickettsies, Mycoplasmapneumoniae, Chlamydia, Legionella, Ureaplasma,Toxoplasma и возбудители рода Муcobacterium. Объектом настоящего изобретения являются используемые в качестве медикаментов, в частности, в качестве антибиотиков описанные выше продукты формулы I, а также их фармацевтически приемлемые соли с минеральными и органическими кислотами. Более конкретно, объектом изобретения являются используемые в качестве медикаментов, в частности в качестве антибиотиков, продукты, описанные в примерах. Объектом изобретения являются также фармацевтические композиции, содержащие в качестве активного начала, по меньшей мере,определенные выше медикаменты. 4 Эти композиции могут вводиться перорально, ректально, парентерально или наноситься местно на кожу или слизистые ткани, но предпочтительным методом нанесения является пероральный метод. Композиции могут быть твердыми или жидкими и выпускаться в виде широко распространенных в практической медицине лекарственных форм, таких, например, как простые таблетки или драже, желатиновые капсулы, гранулы, свечи, инъекционные препараты, мази,кремы и гели. Они могут быть приготовлены с помощью обычных методов. Активное начало или активные начала могут быть в них введены вместе с экcципиентами, обычно применяемыми в фармкомпозициях, такими как тальк, гуммиарабик, лактоза, крахмал, стеарат магния, какао масло, водные и не водные носители, жировые вещества животного и растительного происхождения, парафиновые производные, гликоли, различные смачивающие агенты, диспергаторы или эмульгаторы и консерванты. Композиции могут также выпускаться в виде порошка, предназначенного для растворения непосредственно перед применением в подходящем растворителе, например, в стерильной апирогенной воде. Вводимая доза зависит от характера заболевания, от особенностей больного, от метода введения, от конкретного продукта. Например,для продукта, описанного в примере 4, перорально применяемая суточная доза для взрослого колеблется от 50 до 500 мг. Соединения формулы II, используемые в качестве исходных продуктов, описаны и заявлены в заявке Европейского патента 0596802. Объектом изобретения является также способ, состоящий в том, что соединение формулы II в которой Z имеет значение, указанное выше,подвергают действию гидроксиламина или его галогенгидрата, с получением соединения формулы IA которое при желании подвергают реакции с агентом метанолиза по положению 2', с получением соответствующего соединения формулы IB(III),в котором R' имеет те же значения, что и R, за исключением водорода, a Hal является атомом галогена, с получением соответствующего соединения формулы IC, которое может быть подвергнуто действию агента гидрирования возможной двойной связи в радикале и/или агента, освобождающего гидроксильную функцию в положении 2'. Объектом изобретения являются также соединения формулы III, способ получения которых приведен ниже в экспериментальной части. В предпочтительном варианте осуществления предлагаемого в изобретении способа работают в присутствии избытка гидроксиламина или его галогенгидрата в среде растворителя, которым может быть ацетонитрил,диоксан, диметилформамид, тетрагидрофуран,диметиловый эфир этиленгликоля или диметилсульфоксид,удаление гидроксила в положении 2' осуществляют с помощью метанолиза,этерификацию в положении 2' осуществляют в соответствии с классическими методами,Hal в соединении формулы III является преимущественно атомом брома, хлора или йода,реакция между соединением IA и соединением III осуществляют в присутствии гидрида натрия, осуществляют с помощью водорода в присутствии палладиевого или платинового катализатора независимо от наличия в реакционной среде хлористо-водородной или уксусной кислоты. Изобретение иллюстрируется следующими примерами. Пример 1. 11,12-Дидезокси-3-де[(2,6-дидезокси-3-С-метил-3-О-метил-альфа-L-рибогексопиранозил)окси]-6-O-метил-3-оксо-12,11-[оксикарбонил(гидроксиимино)]эритромицин. 200 см 3 ацетонитрила и 20 г 2'-ацетата 11 дезокси-10,11-дидегидро-3-де[(2,6-дидезокси-3 С-метил-3-О-метил-альфа-L-рибогексопиранозил)окси]-12-O-[(11 Н-имидазол-1-ил)карбонил]6-O-метил-3-оксоэритромицина добавляют к раствору, содержащему 5,9 г гидроксиламингидрохлорида и 20 см 3 воды, перемешивают в течение 3 ч, досуха упаривают, остаток поглощают метанолом и вновь перемешивают в течение 20 ч при комнатной температуре. После этого раствор досуха упаривают, остаток поглощают хлористым метиленом, промывают водой, экстрагируют этилацетатом, сушат и досуха упаривают, получая 17,4 г продукта, который хроматографируют на силикагеле, элюируя смесью этилацетат-триэтиламин-метанол(98/0,75/0,75). Хроматографируя полученный продукт с использованием в качестве элюента системы диизопропиловый эфир-триэтиламинметанол (90/5/5), получают 2,06 г конечного продукта. Спектр ЯМР (400 МГц, CDCl3), м.д. 0,88: СН 3 СН 2; 1,2: 8-Ме; 1,25: 5'-Ме; 1,31: 4-Ме; 1,39: 2-Ме; 1,33-1,49: 6 и 12 Me; 1,55 и 1,94: 13-СН 2; 1,67 и 1,89: 7-СН 2; 1,67: 3'-СН 2; 2,27: NMe2; 2,46:H3'; 2,68: 6-ОМе; 2,72: Н 8; 3,04: Н 4; 3,14: Н 10; 3,18: Н 2'; 3,57: Н 5': 3,82: Н 11; 3,84: Н 2; 4,26: Н 5; 4,35: H1'; 5,14: Н 13. Пример 2. (Е) 11,12-Дидезокси-3-де[(2,6 дидезокси-3-С-метил-3-О-метил-альфа-L-рибогексопиранозил)окси]-6-O-метил-3-оксо-12,11 оксикарбонил[(3-фенил-2-пропенил)окси] иминоэритромицин. Раствор, содержащий 328 мг продукта из примера 1 и 4 см 3 диметилформамида охлаждают до 0 С, добавляют 41 мг 60%-ного гидрида натрия в масле, перемешивают 15 мин при 0 С и добавляют 113 мг бромангидрида коричной кислоты в 2 мл диметилформамиде на силипорите. Смесь выливают на лед, экстрагируют хлористым метиленом, промывают водой, сушат и досуха упаривают. Получают 420 мг продукта,который очищают на силикагеле, элюируя смесью диизопропиловый эфир-триэтиламинметанол (9/0,4/0,4). Спектр ЯМР (300 МГц, СDСl3), м.д.: 0,74: СН 3 СН 2; 1,14: 8-Ме и 10-Ме; 1,24: 5'-Ме; 1,31: 4 Ме; 1,41 и 1,49: 6 и 12 Me; 1,39: 2-Ме; 1,50 иH1'; 4,52 и 4,61: ОСН 2 СН 3; 5,11: Н 13; 6,40 и 6,76: этиленовые группы; 7,2-7,43: ароматические группы. Пример 3. 11,12-Дидезокси-3-де[(2,6 дидезокси-3-С-метил-3-О-метил-альфа-L-рибогексопиранозил)окси]-6-O-метил-3-оксо-12,11[оксикарбонил(3-фенилпропокси)имино]эритромицин. Смесь, содержащую 57 мг продукта из примера 2, 15 мл этилацетата и 8 мг палладия на угле, перемешивают в течение 2 ч в атмосфере водорода, фильтруют, промывают этилацетатом и досуха упаривают, получая 56 мг неочищенного целевого продукта, который очищают на силикагеле, элюируя смесью диизопропиловый эфир-триэтиламин-метанол (9/0,45/0,45), в результате чего получают 45 мг чистого целевого продукта. Спектр ЯМР (СDСl3), м.д.: 0,89: СН 3 СН 2; 1,13-1,15-1,24-1,36; СН 3-СН; 1,37-1,50: 6 и 12 Ме; 1,99: СН 2 в середине цепи; 2,27; NMe2: 2,46: Н 3'; 2,69: 6-ОМе; 2,74: CH2Ph и Н 8; 2,97: Н 10; 3,08: Н 4; 3,17: Н 2'; 3,52: Н 5'; 3,82: Н 2; 3,90 и 3,98: CH2O-N; 4,2: Н 5; 4,21: Н 11; 4,26: H1'; 5,12:NO-CH2; 5,09: Н 13; 7,49 и 7,68: имидазол; 7,298,1-8,46-8,90: пиридин. Приготовление 1. 4-(3-Йодпропил)хинолин. Стадия А. Этиловый эфир 4-(3-хлорпропил)-2-(диэтоксифосфинил)-1(2 Н)-хинолинкарбоновой кислоты. Раствор 7,0 г этилового эфира 2(диэтоксифосфинил)-1(2 Н)-хинолинкарбоновой кислоты в 70 мл тетрагидрофурана охлаждают до -65 С, прибавляют в течение 15 мин 17,6 мл бутиллития в 4 мл бромхлорпропана, перемешивают в течение 3 ч 30 мин, выливают на 50 см 3 ледяной воды, экстрагируют этилацетатом,промывают водой, сушат и досуха упаривают,получая неочищенный целевой продукт, который очищают хроматографией на силикагеле,элюируя смесью циклогексан-этилацетат (4/6). Выход чистого целевого продукта 6,541 г. Спектр ЯМР (250 МГц, СDСl3), м.д. 0,981,19-1,33: группы СН 3; 2,01; СН 2 в середине цепи; 2,55-2,85: =СН 2; 3,59: СН 2-СН 2-Х; 3,71-4,14: СН 2 в POEt.; 4,30: CH2 в CO2Et; 4,30: СН 2 вCO2Et; 5,57: Р-СН; 5,92: =СН-СН-Р; 7,11-7,267,60: ароматические группы. Стадия Б. 4-(3-Хлорпропил)хинолин. 6,5 г продукта стадии А в течение 2 ч перемешивают при 120 С с 65 см 3 этилового спирта и 65 см 3 2N раствора гидроксида натрия, упаривают, экстрагируют эфиром, промывают водой, сушат и досуха упаривают, получая 1,87 г неочищенного продукта, который очищают хроматографией на силикагеле, элюируя смесью хлористый метилен-этилацетат (8/2). Выход чистого целевого продукта 0,617 г. Спектр ЯМР (СDСl3), м.д. 2,24: СН 3 в середине цепи; 3,27: СН 2 С=; 3,62: CH2-X; 7,287,59-7,72-8,06-8,13-8,83: хинолин. Стадия В. 4-(3-Йодпропил)хинолин. Смесь 268 мг продукта стадии Б, 5 мл ацетона, 1,042 г йодида натрия и 30 мг тетрабутиламмониййодида перемешивают в течение 4 ч при 60 С, отгоняют ацетон, остаток поглощают хлористым метиленом, промывают 10%-ным раствором сульфита натрия, сушат и досуха упаривают, получая 3,91 мг искомого продукта. Приготовление 2. 3-[1-(3-Бромпропил)-1 Нимидазол-4-ил]пиридин. Раствор, содержащий 400 мг 3-(1Hимидазол-4-ил)пиридина, 3 мл диметилформамида и 132 мг 60%-ного гидрида натрия в масле,перемешивают 1 ч при 60 С, прибавляют по каплям раствор 3,22 г дибромпропана в 2 мл диметилформамида и перемешивают еще 1 ч при комнатной температуре. Полученную смесь выливают на ледяную воду, экстрагируют этилацетатом, сушат и досуха упаривает. Остаток хроматографируют на силикагеле, элюируя смесью хлористый метилен-метанол (9/1). Выход чистого целевого продукта 306 мг. Пример фармацевтической композиции. Получают композицию, содержащую Продукт, полученный в примере 4 150 мг Эксципиент До 1 г В качестве эксципиента могут быть использованы крахмал, тальк, стеарат магния. Фармакологическое исследование продуктов согласно изобретению Метод разбавлений жидкой средой. Приготовляют ряд пробирок, в которые помещают одинаковые количества стерильной питательной среды. Затем в пробирки помещают возрастающие количества исследуемого продукта, после чего каждую из пробирок засевают штаммом бактерий. После 24-часовой инкубации в термостатируемом шкафу при 37 С методом просвечивания оценивают задержку роста, что позволяет определить минимальные ингибирующие концентрации, выраженные в микрограммах на 1 см 3. Для продукта, синтезированного в примере 4, получены следующие результаты (замер через 24 ч): Грамм(+) бактериальные штаммы: Помимо этого продукт примера 4 обнаружил полезную активность на грамотрицательных штаммах бактерий: HaemophilusInfluenzae 351HT3, 351 СВ 12, 351 СА 1 и 351GR6. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные эритромицина формулы I в которой R означает атом водорода; алкильный радикал, содержащий до 12 атомов углерода,который может быть замещен галогеном или радикалами (СН 2)mАr или в которых m - целое число от 1 до 8, n и р, одинаковые или различные,означают целые числа от 0 до 6; А и В, одинаковые или различные, означают атом водорода или галогена или алкил, содержащий до 8 атомов углерода; Аr - фенил или нафтил или гетероарильный радикал, выбранный из тиенила,фурила, пирролила, тиазолила, оксазолила,имидазолила, тиадиазолила, пиразолила, изопиразолила, пиридила, пиримидила, пиридазинила, пиразинила, индолила, бензофуранила, бензотиазила или хинолинила, причем перечисленные радикалы могут быть замещены одним или несколькими заместителями, выбранными из группы, в которую входят гидроксил, атомы галогена, радикалы NO2 и CN, алкил, алкенил или алкинил, O-алкил, O-алкенил или Oалкинил, S-алкил, S-алкенил или S-алкинил, Nалкил, N-алкенил и N-алкинил, содержащие до 12 атомов углерода, которые могут быть замещены одним или несколькими атомами галогена, радикал где Ra и Rb, одинаковые или различные - атом водорода или алкил, содержащий до 12 атомов углерода, радикал в котором R3 - алкил, содержащий до 12 атомов углерода, или арил или гетероарильный радикал с 5 или 6 звеньями, содержащий один или несколько гетероатомов, которые могут быть замещены одним или несколькими заместителям,указанными выше, и Z - атом водорода или остаток карбоновой кислоты, содержащей до 18 атомов углерода. 2. Соединения формулы I по п.1, в которыхZ - атом водорода. 3. Соединения формулы I по п.1 или 2, в которых R - атом водорода. 4. Соединения формулы I по пп.1, 2 или 3,в которых R означает группу (СН 2)mАr, где m и Аr имеет то же значение, что и в п.1. 5. Соединения формулы I по п.4, в которыхR означает группу (СН 2)m'Аr, где m' - целое число 3, 4, 5 или 6. 6. Соединения формулы I по п.5, в которых Аr - радикал 4-хинолинил, который может иметь заместители в одном и/или в другом из двух циклов хинолина. 7. Соединения формулы I по п.6, в которых Аr представляет собой незамещенный 4 хинолинил. 8. Соединения формулы I по п.5, в которых Аr представляет собой радикал формулы который может иметь заместители в одном и/или в другом из двух циклов. 9. Соединения формулы I по п.8, в которых Аr не имеет заместителей. 10. Соединения формулы I по п.1, имеющие следующие названия: 11,12-дидезокси-3-де[(2,6-дидезокси-3-Сметил-3-О-метил-альфа-L-рибогексопиранозил)окси]-6-O-метил-3-оксо-12,11-оксикарбонил[3-(4-хинолинил)пропокси]имино эритромицин. 11. Соединения формулы I, описанные в любом из пп.1-10, в качестве медикаментов. 12. Фармацевтическая композиция, содержащая в качестве активного начала, по меньшей мере, один медикамент в соответствии с п.11. 13. Способ получения соединений формулы I в соответствии с любым из пп.1-10, отличающийся тем, что соединение формулы II в которой Z имеет значения, описанные в п.1,подвергают взаимодействию с гидроксиламином или его галогенгидратом с получением соединения формулы IA 12 которое при желании подвергают действию реагента, осуществляющего метанолиз гидроксила в положении 2', с целью получения соответствующего соединения формулы IB, в котором Z означает атом водорода после чего соединение IA или IB вводят в реакцию с соединением формулы(III),в которой R' имеет то же значение, что и R, за исключением водорода, a Hal является атомом галогена, с целью получения соответствующего соединения формулы IC, которое может быть подвергнуто действию агента гидрирования возможной двойной связи в радикале и/или агента, освобождающего гидроксильную группу в положении 2'. 14. Соединения формулы (III), имеющие следующие названия: 4-(3-иодопропил)-хинолин,3-[1-(3-бромпропил)-1 Н-имидазол-4-ил]пиридин в качестве промежуточных продуктов.
МПК / Метки
МПК: A61P 31/04, C07H 17/08, A61K 31/7048
Метки: медикаментов, получения, эритромицина, производные, качестве, способ, новые, применение
Код ссылки
<a href="https://eas.patents.su/7-2168-novye-proizvodnye-eritromicina-sposob-ih-polucheniya-i-ih-primenenie-v-kachestve-medikamentov.html" rel="bookmark" title="База патентов Евразийского Союза">Новые производные эритромицина, способ их получения и их применение в качестве медикаментов</a>
Предыдущий патент: Вакцинная композиция против малярии
Следующий патент: Станция для использования геотермальной энергии
Случайный патент: Обнаружение пассивных сейсмических событий











