Таблетки безилата амлодипина с улучшенной стабильностью
Номер патента: 6826
Опубликовано: 28.04.2006
Авторы: Сентгроти Пальне, Лонкайне Мадьяр Ольга, Фекете Паль, Томпе Петер, Левентисне Гусар Магдолина, Туроци Пальне, Гора Ласлоне, Кирайне Игнац Мария
Формула / Реферат
1. Таблетки безилата амлодипина с улучшенной стабильностью активного ингредиента и пониженным весовым содержанием микрокристаллической целлюлозы, смазывающего агента и разрыхляющего агента, которые содержат 4-6 мас.% безилата амлодипина в качестве активного ингредиента, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 масс.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния.
2. Таблетки по п.1, характеризующиеся тем, что имеют массу от 60 до 80 мг и содержание активного ингредиента, соответствующее 2,5 мг основания амлодипина.
3. Таблетки по п.1, характеризующиеся тем, что имеют массу от 120 до 160 мг и содержание активного ингредиента, соответствующее 5 мг основания амлодипина.
4. Таблетки по п.1, характеризующиеся тем, что имеют массу от 240 до 320 мг и содержание активного ингредиента, соответствующее 10 мг основания амлодипина.
5. Способ получения таблеток безилата амлодипина по п.1, характеризующийся тем, что гомогенизируют 4-6 мас.% безилата амлодипина, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 мас.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния относительно суммарной массы таблеток с помощью методики смешивания порошков и прессуют таблетки из полученной порошкообразной смеси.
6. Способ по п.5, характеризующийся тем, что из порошкообразной смеси прессуют таблетки, содержащие безилат амлодипина в количестве, соответствующем 2,5, 5 или 10 мг основания амлодипина.
Текст
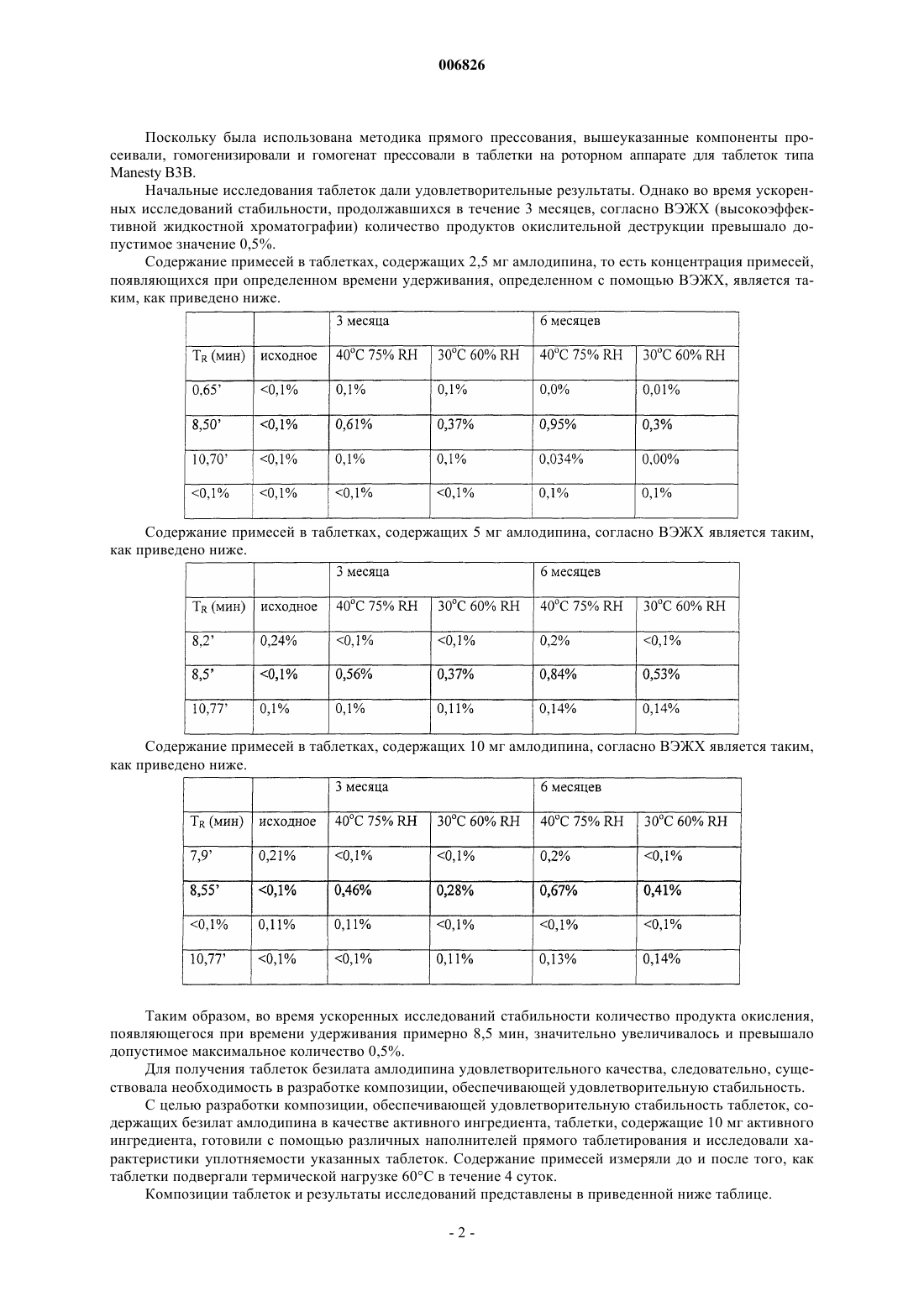
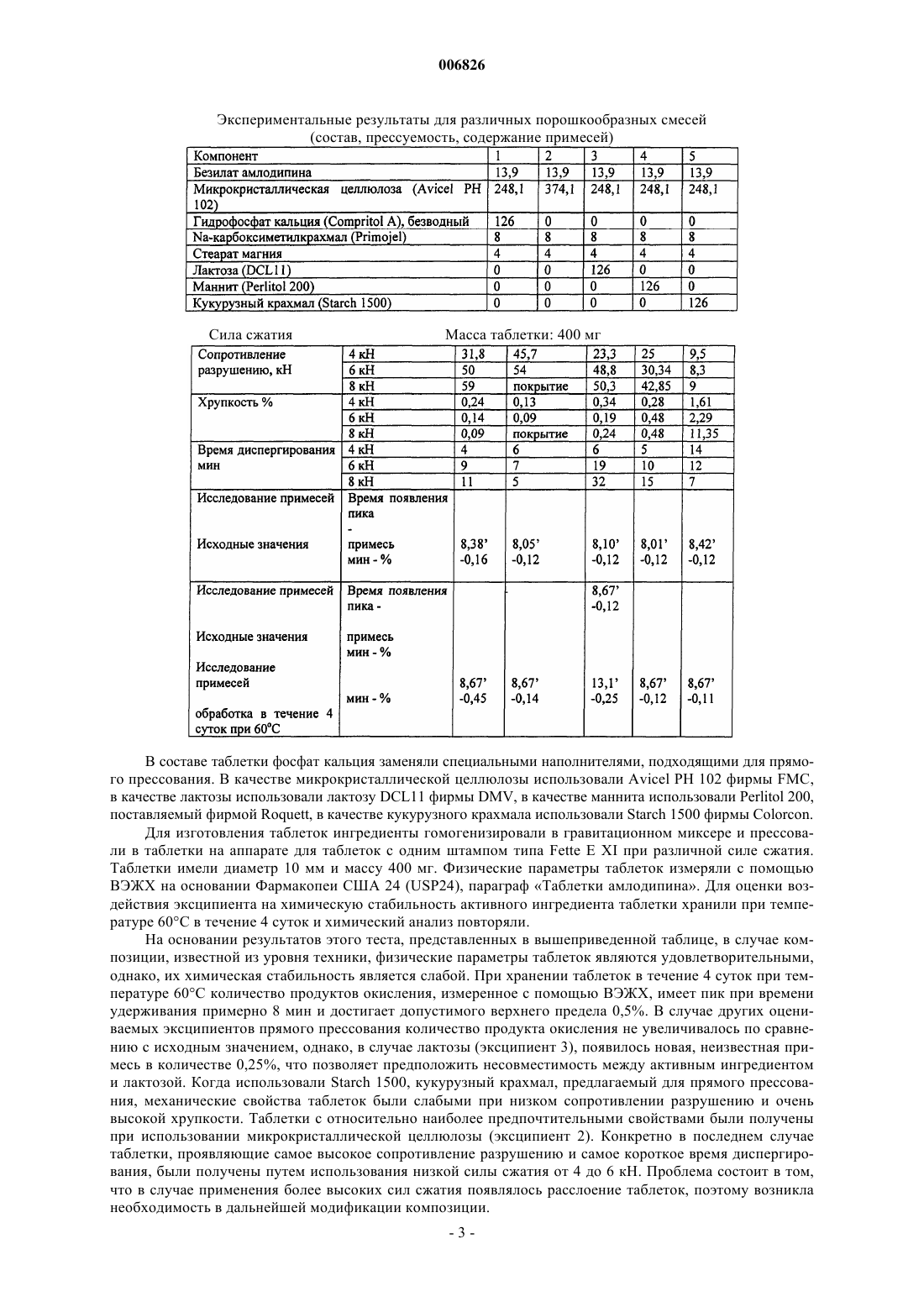
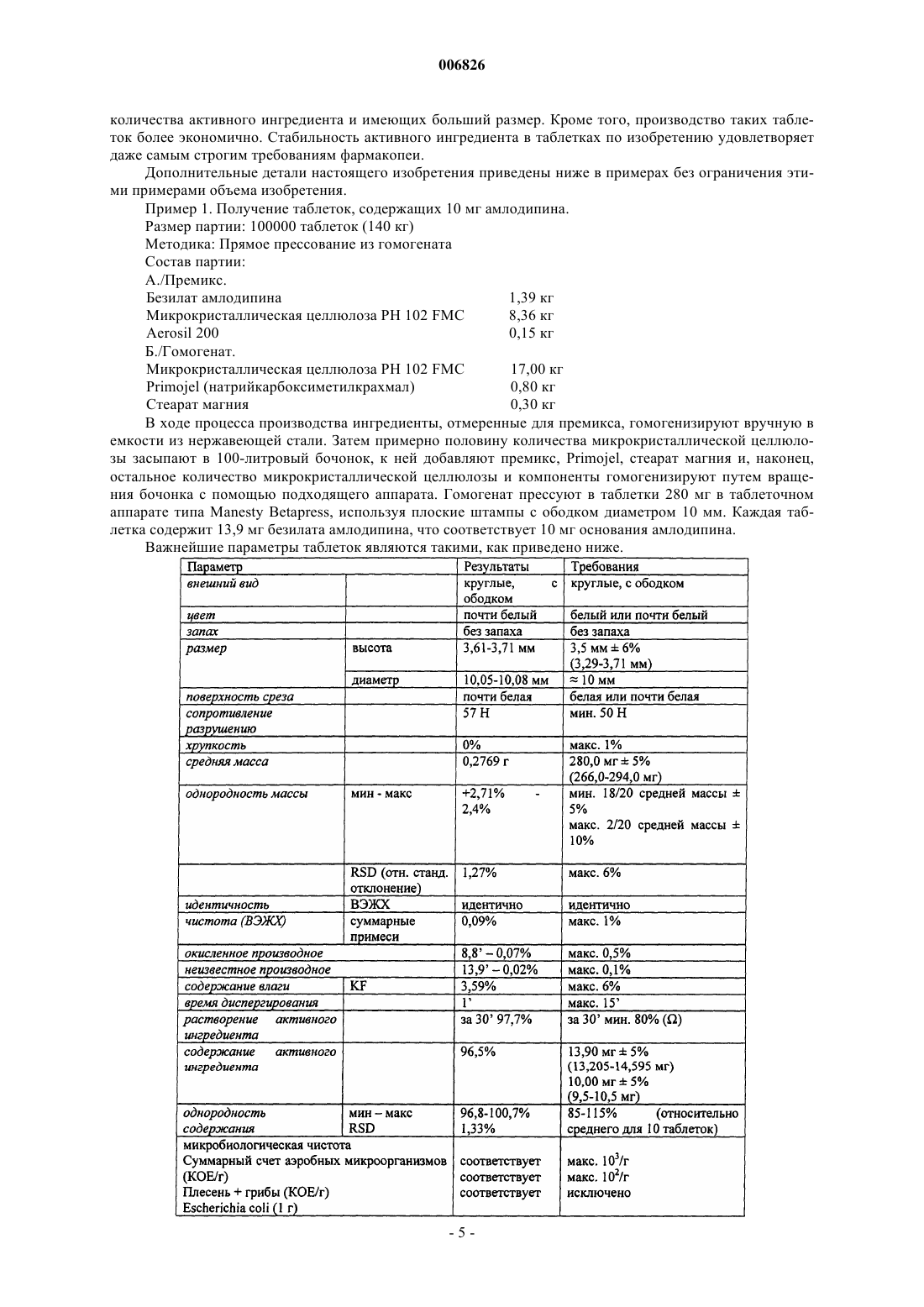
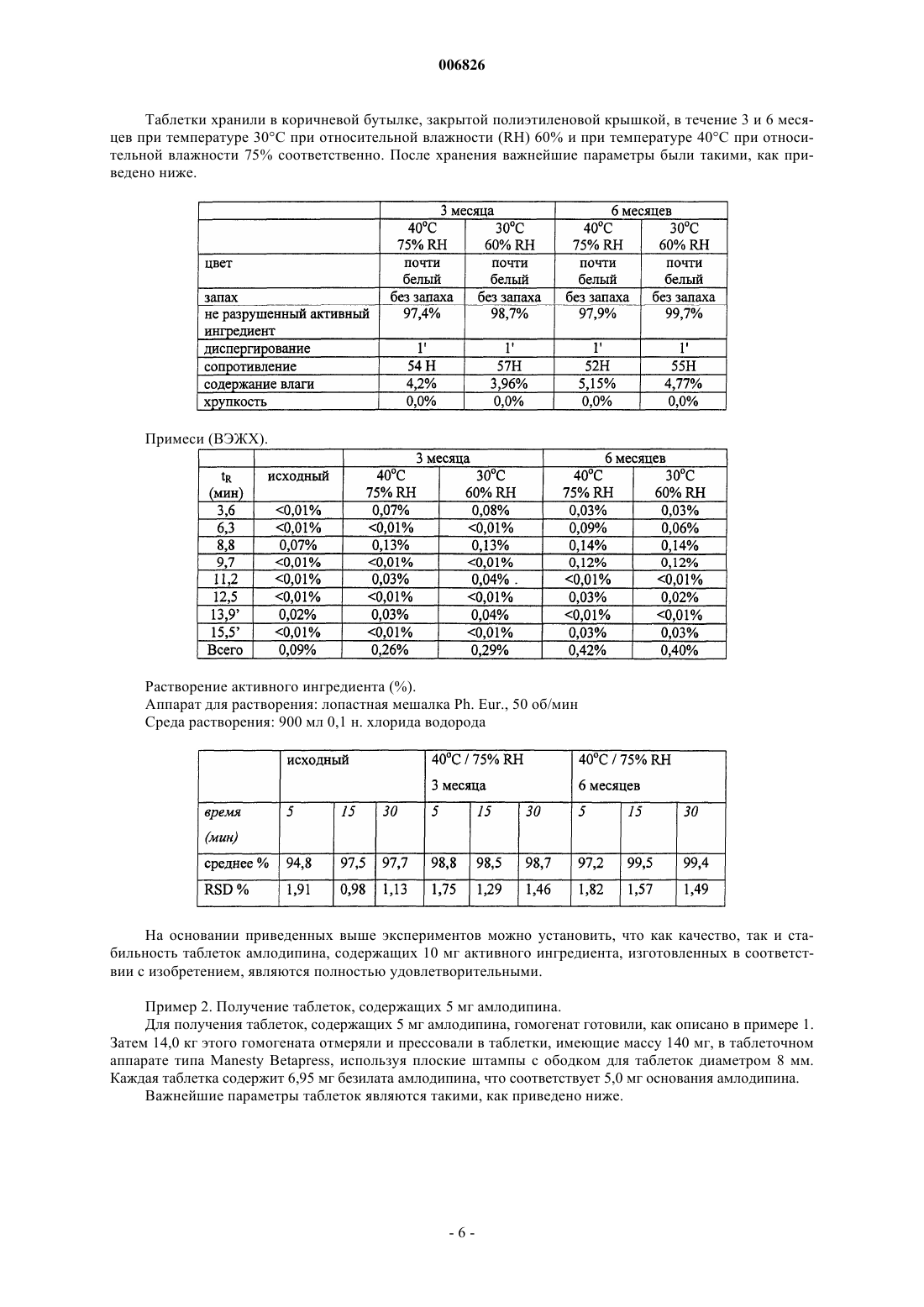
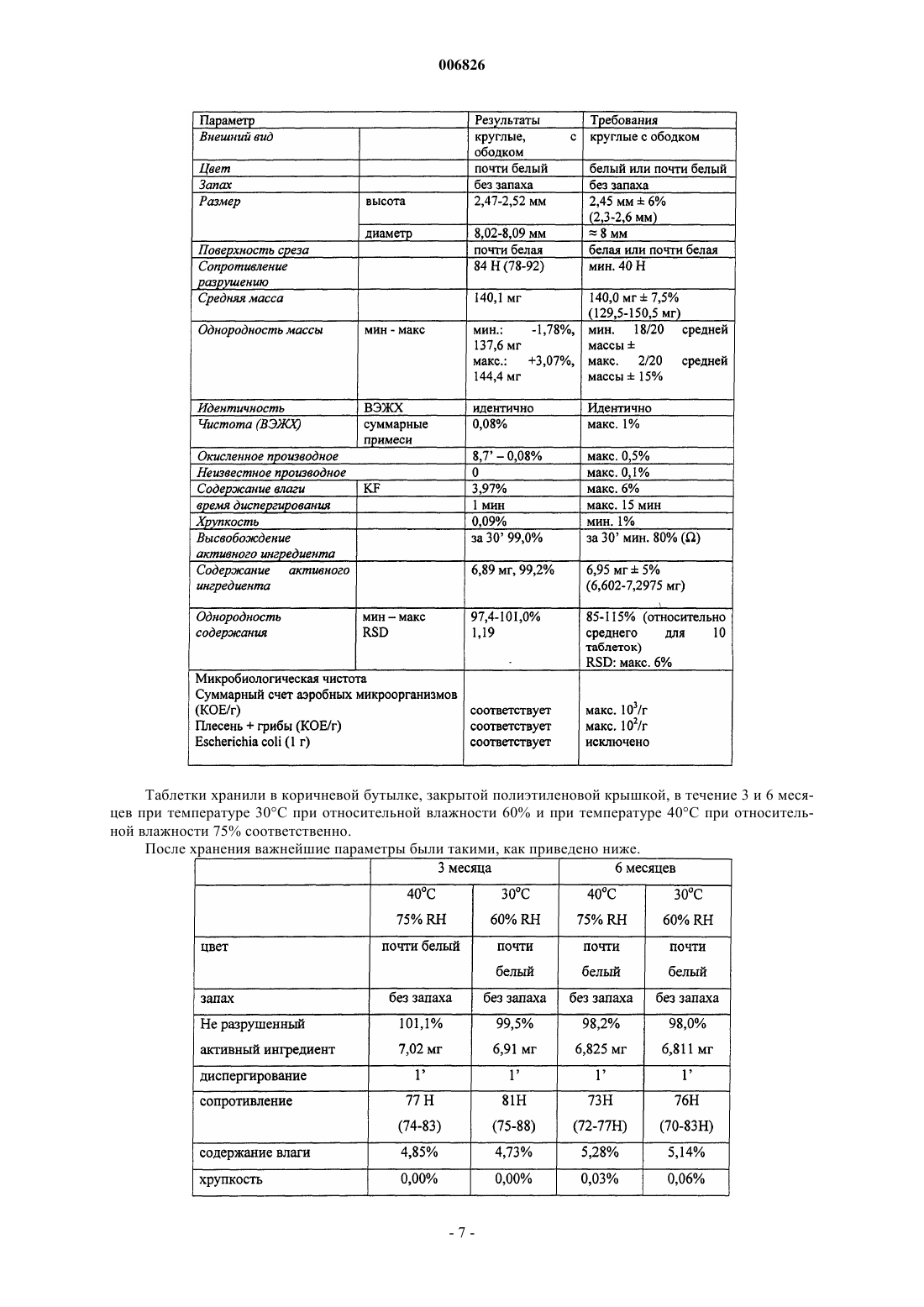
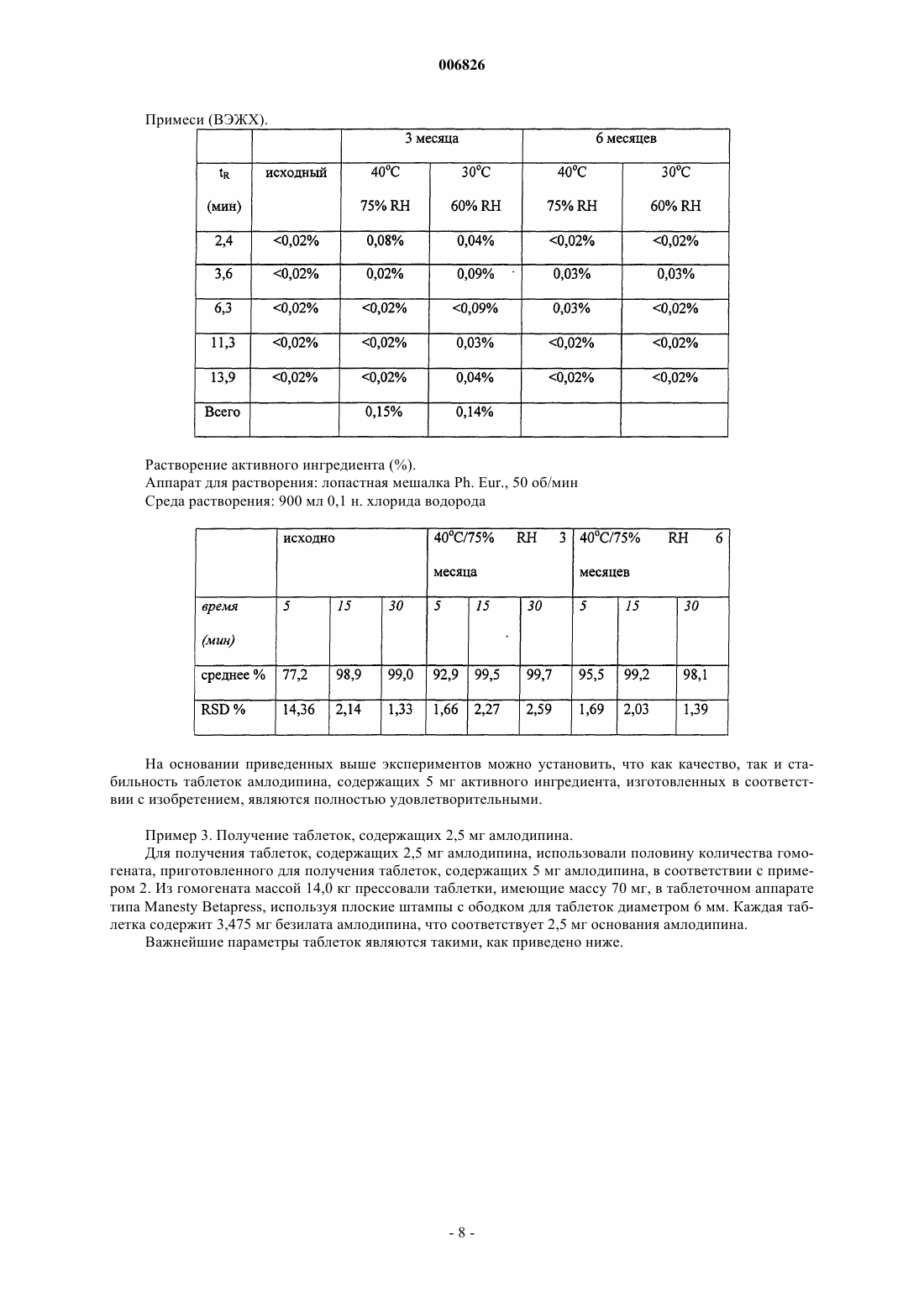
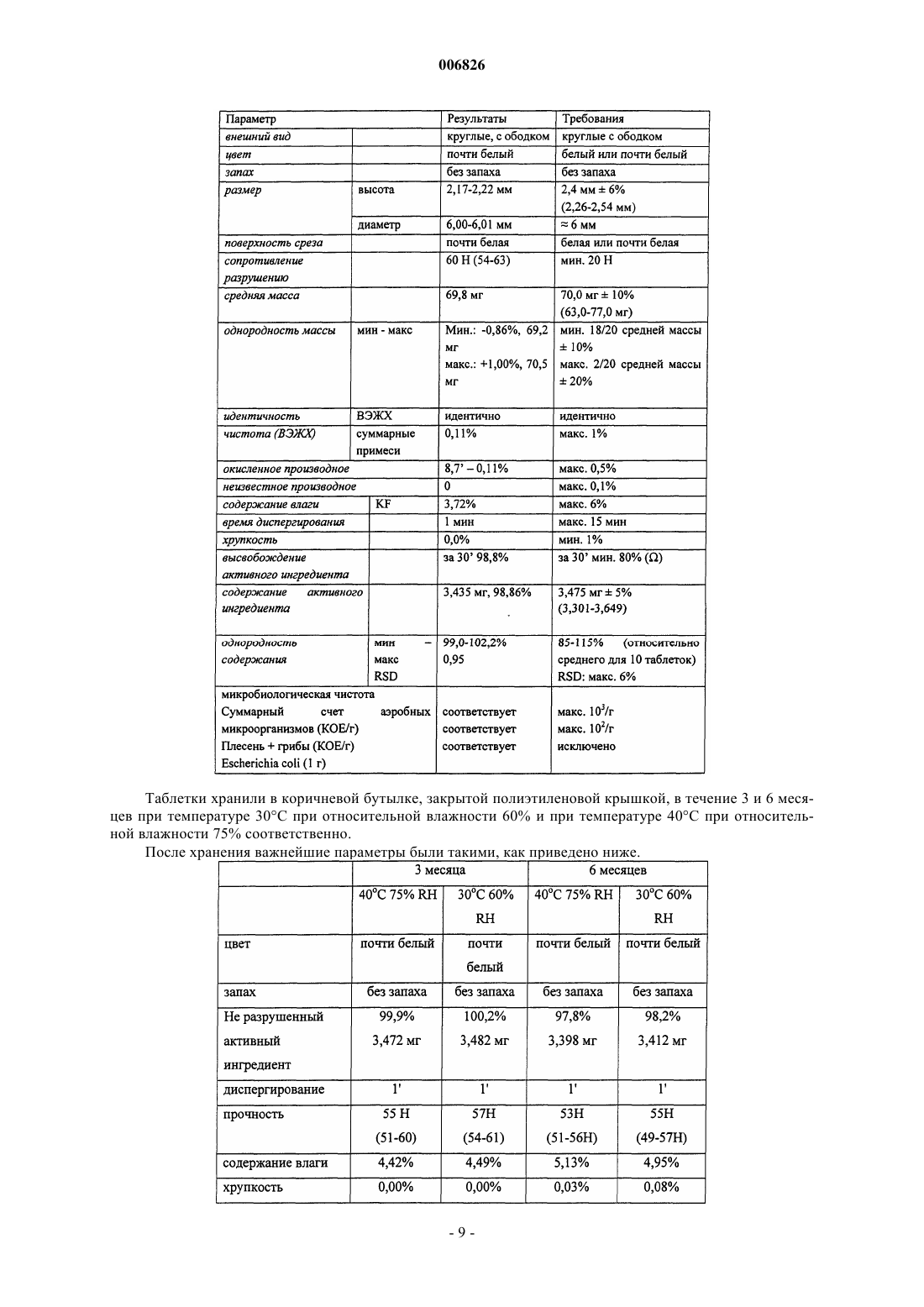
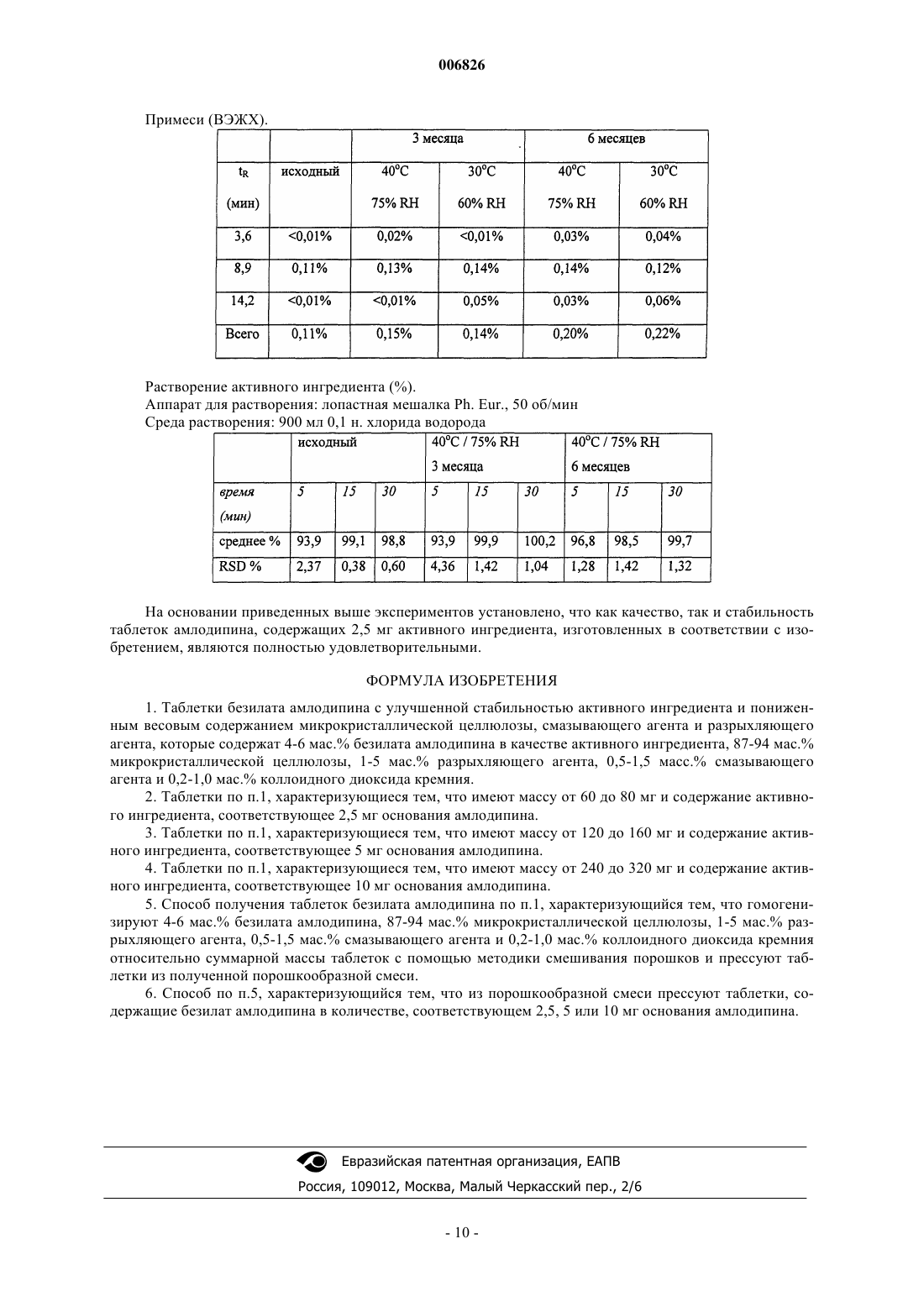
006826 Данное изобретение относится к таблеткам безилата амлодипина с улучшенной стабильностью активного ингредиента и пониженньм весовым содержанием микрокристаллической целлюлозы, смазывающего агента и разрыхляющего агента. Изобретение также относится к способу получения указанных таблеток. Известно, что безилат амлодипина, [безилат 5-метилового эфира 2-[(2-аминоэтокси)метил]-4-(2 хлорфенил)-1,4-дигидро-6-метил-3-этил-3,5-пиридиндикарбоновой кислоты] является одним из важнейших представителей фармацевтических ингредиентов, обладающих антагонистической активностью в отношении кальция. В терапевтической практике применяют таблетки, содержащие безилат амлодипина в количествах, соответствующих 2,5, 5 и 10 мг свободного основания амлодипина. Количества безилата амлодипина в этих таблетках составляют 3,472, 6,944 и 13,888 мг соответственно. Несмотря на относительно малое содержание активного ингредиента, массы известных таблеток удивительно высоки (100, 200 и 400 мг соответственно), так что концентрация активного ингредиента в известных композициях едва превышает 3%. Согласно публикации L'informatore Farmaceutico, 1994, количественный состав известных таблеток безилата амлодипина является таким, как приведено ниже. Таблетка Norvasc, 10 мг: Безилат амлодипина 13,889 мг Микрокристаллическая целлюлоза 248,111 мг Гидрофосфат кальция (безводный) 126,0 мг Натрийкарбоксиметилкрахмал 8,0 мг Стеарат магния 4,0 мг Номинальная масса таблетки 400,0 мг Для специалиста в области изготовления таблеток эта композиция однозначно предполагает методику прямого прессования, поскольку связующие агенты влажной грануляции, растворимые в воде или в каком-либо ином растворителе, полностью отсутствуют, а микрокристаллическая целлюлоза и безводный гидрофосфат кальция являются эксципиентами, типично применяемыми в методиках прямого прессования. Последствиями необычно малой концентрации активного ингредиента, применяемого в приведенной выше композиции, должны быть плохие характеристики таблетирования и слабая стабильность безилата амлодипина. В процессе методики прямого прессования, которая должна быть использована для изготовления известных таблеток, активный ингредиент смешивают с различными эксципиентами для таблеток(наполнителями, сухими связующими агентами, разрыхляющими агентами, глидантными агентами) в порошкообразной форме, а затем эту порошкообразную смесь таблетируют. Хорошо известно, что эксципиенты прямого таблетирования могут только незначительно улучшить слабые характеристики таблетирования активного ингредиента. В то же время методика влажной грануляции, способная дать лучший результат по усовершенствованию свойств прессования, не может быть использована в связи с химической нестабильностью активного ингредиента, поскольку высушивание, следующее за влажной грануляцией,может привести к усиленной деструкции активного ингредиента, а грануляция в органическом растворителе является весьма дорогостоящей, особенно когда точно учтены требования охраны окружающей среды. Препараты, имеющиеся в настоящее время в продаже, обладают несколькими недостатками. В связи с большим количеством эксципиентов размер таблетки относительно велик, а большие таблетки трудно глотать, особенно пожилым пациентам, которые находятся на первом месте по приему фармацевтических препаратов, содержащих амлодипин. Кроме того, вследствие высокого содержания эксципиентов стоимость материалов производственного процесса относительно высока, и в случае данной производственной линии выход является достаточно низким. При воспроизведении известной таблетки безилата амлодипина авторы изобретения обнаружили,что ее стабильность в условиях ускоренных исследований стабильности не соответствует требованиям. Конкретно эти исследования показали, что при хранении в течение периода 3 месяца при температуре 40 С при относительной влажности (RH) 75% количество продуктов окислительной деструкции в таблетках вышеуказанной композиции превышало количество 0,5%, допустимое Фармакопеей США 24(USP (United States Pharmacopoeia) 24) в параграфе Таблетки амлодипина ("Amlodipine Tablets"). Состав тестируемых таблеток был таким, как приведено ниже. Поскольку была использована методика прямого прессования, вышеуказанные компоненты просеивали, гомогенизировали и гомогенат прессовали в таблетки на роторном аппарате для таблеток типаManesty B3B. Начальные исследования таблеток дали удовлетворительные результаты. Однако во время ускоренных исследований стабильности, продолжавшихся в течение 3 месяцев, согласно ВЭЖХ (высокоэффективной жидкостной хроматографии) количество продуктов окислительной деструкции превышало допустимое значение 0,5%. Содержание примесей в таблетках, содержащих 2,5 мг амлодипина, то есть концентрация примесей,появляющихся при определенном времени удерживания, определенном с помощью ВЭЖХ, является таким, как приведено ниже. Содержание примесей в таблетках, содержащих 5 мг амлодипина, согласно ВЭЖХ является таким,как приведено ниже. Содержание примесей в таблетках, содержащих 10 мг амлодипина, согласно ВЭЖХ является таким,как приведено ниже. Таким образом, во время ускоренных исследований стабильности количество продукта окисления,появляющегося при времени удерживания примерно 8,5 мин, значительно увеличивалось и превышало допустимое максимальное количество 0,5%. Для получения таблеток безилата амлодипина удовлетворительного качества, следовательно, существовала необходимость в разработке композиции, обеспечивающей удовлетворительную стабильность. С целью разработки композиции, обеспечивающей удовлетворительную стабильность таблеток, содержащих безилат амлодипина в качестве активного ингредиента, таблетки, содержащие 10 мг активного ингредиента, готовили с помощью различных наполнителей прямого таблетирования и исследовали характеристики уплотняемости указанных таблеток. Содержание примесей измеряли до и после того, как таблетки подвергали термической нагрузке 60 С в течение 4 суток. Композиции таблеток и результаты исследований представлены в приведенной ниже таблице.-2 006826 Экспериментальные результаты для различных порошкообразных смесей В составе таблетки фосфат кальция заменяли специальными наполнителями, подходящими для прямого прессования. В качестве микрокристаллической целлюлозы использовали Avicel PH 102 фирмы FMC,в качестве лактозы использовали лактозу DCL11 фирмы DMV, в качестве маннита использовали Perlitol 200,поставляемый фирмой Roquett, в качестве кукурузного крахмала использовали Starch 1500 фирмы Colorcon. Для изготовления таблеток ингредиенты гомогенизировали в гравитационном миксере и прессовали в таблетки на аппарате для таблеток с одним штампом типа Fette E XI при различной силе сжатия. Таблетки имели диаметр 10 мм и массу 400 мг. Физические параметры таблеток измеряли с помощью ВЭЖХ на основании Фармакопеи США 24 (USP24), параграф Таблетки амлодипина. Для оценки воздействия эксципиента на химическую стабильность активного ингредиента таблетки хранили при температуре 60 С в течение 4 суток и химический анализ повторяли. На основании результатов этого теста, представленных в вышеприведенной таблице, в случае композиции, известной из уровня техники, физические параметры таблеток являются удовлетворительными,однако, их химическая стабильность является слабой. При хранении таблеток в течение 4 суток при температуре 60 С количество продуктов окисления, измеренное с помощью ВЭЖХ, имеет пик при времени удерживания примерно 8 мин и достигает допустимого верхнего предела 0,5%. В случае других оцениваемых эксципиентов прямого прессования количество продукта окисления не увеличивалось по сравнению с исходным значением, однако, в случае лактозы (эксципиент 3), появилось новая, неизвестная примесь в количестве 0,25%, что позволяет предположить несовместимость между активным ингредиентом и лактозой. Когда использовали Starch 1500, кукурузный крахмал, предлагаемый для прямого прессования, механические свойства таблеток были слабыми при низком сопротивлении разрушению и очень высокой хрупкости. Таблетки с относительно наиболее предпочтительными свойствами были получены при использовании микрокристаллической целлюлозы (эксципиент 2). Конкретно в последнем случае таблетки, проявляющие самое высокое сопротивление разрушению и самое короткое время диспергирования, были получены путем использования низкой силы сжатия от 4 до 6 кН. Проблема состоит в том,что в случае применения более высоких сил сжатия появлялось расслоение таблеток, поэтому возникла необходимость в дальнейшей модификации композиции.-3 006826 Во время исследования, направленного на разработку правильной композиции таблеток безилата амлодипина, авторы изобретения неожиданно обнаружили, что расслоение можно элиминировать посредством уменьшения количества микрокристаллической целлюлозы, которая сама по себе обладает очень хорошей прессуемостью, или посредством использования в композиции коллоидного диоксида кремния в количестве 0,5% мас./мас. Уменьшение количества микрокристаллической целлюлозы также приводит в результате к значительному снижению массы таблеток, что дает дополнительные преимущества. Во-первых, может быть достигнуто снижение стоимости производства. Кроме того, как следствие меньших размеров таблеток, облегчается глотание таблеток, особенно в случае таблеток, содержащих безилат амлодипина в количестве, соответствующем 10 мг основания амлодипина. Уменьшение количества микрокристаллической целлюлозы, однако, ограничено тем фактом, что масса таблеток, содержащих наименьшее количество безилата амлодипина, соответствующее 2,5 мг основания амлодипина, не может быть меньше, чем от примерно 60 до 70 мг, предпочтительно примерно 70 мг. Низший предел массы таблетки определяется размером таблетки, физически удобным в обращении для пациентов. Обычно это означает круглую таблетку диаметром от 6 до 7 мм и высотой примерно 2,5 мм, соответствующей этому диаметру, данные параметры оптимально обеспечиваются массой таблетки от примерно 60 до 70 мг. В соответствии с настоящим изобретением предложены таблетки безилата амлодипина с улучшенной стабильностью активного ингредиента и пониженным весовым содержанием микрокристаллической целлюлозы, смазывающего агента и разрыхляющего агента, которые содержат 4-6 мас.% безилата амлодипина в качестве активного ингредиента, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 мас.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния. Масса самых больших таблеток, содержащих безилат амлодипина в количестве, соответствующем 10 мг свободного основания амлодипина, составляет от 240 до 280 мг, предпочтительно примерно 280 мг. В соответствии с исследованиями авторов изобретения обнаружено, что наиболее предпочтительными таблетками безилата амлодипина с точки зрения как производства или физических параметров таблетки, так и химической стабильности активного ингредиента являются таблетки, содержащие примерно 5 мас.% безилата амлодипина, примерно 90 мас.% микрокристаллической целлюлозы, примерно 3 мас.% разрыхляющего агента (предпочтительно натрийкарбоксиметилкрахмала), примерно 1 мас.% смазывающего агента (предпочтительно стеарата магния) и примерно 0,5 мас.% глидантного агента, предпочтительно коллоидного диоксида кремния. Вместо натрийкарбоксиметилкрахмала в качестве разрыхляющего агента для таблеток по изобретению могут быть также использованы натрий- или кальцийкарбоксиметилцеллюлоза, кросповидон или низкозамещенная гидроксипропилцеллюлоза (L-HPC). В качестве смазывающего агента вместо стеарата магния можно также использовать стеарат кальция. В соответствии с другим аспектом настоящего изобретения предложен способ получения таблеток безилата амлодипина с улучшенной стабильностью активного ингредиента и пониженной массой, при котором гомогенизируют 4-6 мас.% безилата амлодипина, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 мас.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния относительно суммарной массы таблеток с помощью методики смешивания порошков и прессуют таблетки из полученной таким образом порошкообразной смеси. Можно заметить, что получение таблеток безилата амлодипина согласно изобретению является очень простым. Ингредиенты превращают в порошок и гомогенизируют в соответствующем соотношении, и из полученного таким образом гомогенного порошка можно прессовать таблетки, содержащие желаемое количество активного ингредиента, на таблеточном аппарате любого типа. В соответствии с исследованиями авторов изобретения было доказано, что следующие композиции являются весьма предпочтительными Вышеописанные композиции приведены только в качестве примера, изменения количеств индивидуальных компонентов примерно на +/-20% не приводят к снижению качества таблеток. При одинаковом содержании активного ингредиента таблетки безилата амлодипина согласно изобретению имеют значительно меньшую массу, чем известные таблетки. Таким образом, достигнута улучшенная терапевтическая применимость, особенно в случае таблеток, содержащих более высокие-4 006826 количества активного ингредиента и имеющих больший размер. Кроме того, производство таких таблеток более экономично. Стабильность активного ингредиента в таблетках по изобретению удовлетворяет даже самым строгим требованиям фармакопеи. Дополнительные детали настоящего изобретения приведены ниже в примерах без ограничения этими примерами объема изобретения. Пример 1. Получение таблеток, содержащих 10 мг амлодипина. Размер партии: 100000 таблеток (140 кг) Методика: Прямое прессование из гомогената Состав партии:A./Премикс. Безилат амлодипина 1,39 кг Микрокристаллическая целлюлоза РН 102 FMC 8,36 кгAerosil 200 0,15 кг Б./Гомогенат. Микрокристаллическая целлюлоза РН 102 FMC 17,00 кгPrimojel (натрийкарбоксиметилкрахмал) 0,80 кг Стеарат магния 0,30 кг В ходе процесса производства ингредиенты, отмеренные для премикса, гомогенизируют вручную в емкости из нержавеющей стали. Затем примерно половину количества микрокристаллической целлюлозы засыпают в 100-литровый бочонок, к ней добавляют премикс, Primojel, стеарат магния и, наконец,остальное количество микрокристаллической целлюлозы и компоненты гомогенизируют путем вращения бочонка с помощью подходящего аппарата. Гомогенат прессуют в таблетки 280 мг в таблеточном аппарате типа Manesty Betapress, используя плоские штампы с ободком диаметром 10 мм. Каждая таблетка содержит 13,9 мг безилата амлодипина, что соответствует 10 мг основания амлодипина. Важнейшие параметры таблеток являются такими, как приведено ниже.-5 006826 Таблетки хранили в коричневой бутылке, закрытой полиэтиленовой крышкой, в течение 3 и 6 месяцев при температуре 30 С при относительной влажности (RH) 60% и при температуре 40 С при относительной влажности 75% соответственно. После хранения важнейшие параметры были такими, как приведено ниже. Растворение активного ингредиента (%). Аппарат для растворения: лопастная мешалка Ph. Eur., 50 об/мин Среда растворения: 900 мл 0,1 н. хлорида водорода На основании приведенных выше экспериментов можно установить, что как качество, так и стабильность таблеток амлодипина, содержащих 10 мг активного ингредиента, изготовленных в соответствии с изобретением, являются полностью удовлетворительными. Пример 2. Получение таблеток, содержащих 5 мг амлодипина. Для получения таблеток, содержащих 5 мг амлодипина, гомогенат готовили, как описано в примере 1. Затем 14,0 кг этого гомогената отмеряли и прессовали в таблетки, имеющие массу 140 мг, в таблеточном аппарате типа Manesty Betapress, используя плоские штампы с ободком для таблеток диаметром 8 мм. Каждая таблетка содержит 6,95 мг безилата амлодипина, что соответствует 5,0 мг основания амлодипина. Важнейшие параметры таблеток являются такими, как приведено ниже. Таблетки хранили в коричневой бутылке, закрытой полиэтиленовой крышкой, в течение 3 и 6 месяцев при температуре 30 С при относительной влажности 60% и при температуре 40 С при относительной влажности 75% соответственно. После хранения важнейшие параметры были такими, как приведено ниже. Растворение активного ингредиента (%). Аппарат для растворения: лопастная мешалка Ph. Eur., 50 об/мин Среда растворения: 900 мл 0,1 н. хлорида водорода На основании приведенных выше экспериментов можно установить, что как качество, так и стабильность таблеток амлодипина, содержащих 5 мг активного ингредиента, изготовленных в соответствии с изобретением, являются полностью удовлетворительными. Пример 3. Получение таблеток, содержащих 2,5 мг амлодипина. Для получения таблеток, содержащих 2,5 мг амлодипина, использовали половину количества гомогената, приготовленного для получения таблеток, содержащих 5 мг амлодипина, в соответствии с примером 2. Из гомогената массой 14,0 кг прессовали таблетки, имеющие массу 70 мг, в таблеточном аппарате типа Manesty Betapress, используя плоские штампы с ободком для таблеток диаметром 6 мм. Каждая таблетка содержит 3,475 мг безилата амлодипина, что соответствует 2,5 мг основания амлодипина. Важнейшие параметры таблеток являются такими, как приведено ниже. Таблетки хранили в коричневой бутылке, закрытой полиэтиленовой крышкой, в течение 3 и 6 месяцев при температуре 30 С при относительной влажности 60% и при температуре 40 С при относительной влажности 75% соответственно. После хранения важнейшие параметры были такими, как приведено ниже. Растворение активного ингредиента (%). Аппарат для растворения: лопастная мешалка Ph. Eur., 50 об/мин Среда растворения: 900 мл 0,1 н. хлорида водорода На основании приведенных выше экспериментов установлено, что как качество, так и стабильность таблеток амлодипина, содержащих 2,5 мг активного ингредиента, изготовленных в соответствии с изобретением, являются полностью удовлетворительными. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Таблетки безилата амлодипина с улучшенной стабильностью активного ингредиента и пониженным весовым содержанием микрокристаллической целлюлозы, смазывающего агента и разрыхляющего агента, которые содержат 4-6 мас.% безилата амлодипина в качестве активного ингредиента, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 масс.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния. 2. Таблетки по п.1, характеризующиеся тем, что имеют массу от 60 до 80 мг и содержание активного ингредиента, соответствующее 2,5 мг основания амлодипина. 3. Таблетки по п.1, характеризующиеся тем, что имеют массу от 120 до 160 мг и содержание активного ингредиента, соответствующее 5 мг основания амлодипина. 4. Таблетки по п.1, характеризующиеся тем, что имеют массу от 240 до 320 мг и содержание активного ингредиента, соответствующее 10 мг основания амлодипина. 5. Способ получения таблеток безилата амлодипина по п.1, характеризующийся тем, что гомогенизируют 4-6 мас.% безилата амлодипина, 87-94 мас.% микрокристаллической целлюлозы, 1-5 мас.% разрыхляющего агента, 0,5-1,5 мас.% смазывающего агента и 0,2-1,0 мас.% коллоидного диоксида кремния относительно суммарной массы таблеток с помощью методики смешивания порошков и прессуют таблетки из полученной порошкообразной смеси. 6. Способ по п.5, характеризующийся тем, что из порошкообразной смеси прессуют таблетки, содержащие безилат амлодипина в количестве, соответствующем 2,5, 5 или 10 мг основания амлодипина.
МПК / Метки
МПК: A61K 31/4422, A61K 9/20
Метки: безилата, стабильностью, улучшенной, таблетки, амлодипина
Код ссылки
<a href="https://eas.patents.su/11-6826-tabletki-bezilata-amlodipina-s-uluchshennojj-stabilnostyu.html" rel="bookmark" title="База патентов Евразийского Союза">Таблетки безилата амлодипина с улучшенной стабильностью</a>
Предыдущий патент: Способы получения биологически активных молекул
Следующий патент: Способ выделения рнк из залитых в парафин образцов ткани
Случайный патент: Способ изменения состояния предохранительного клапана