Промежуточные соединения агомелатина и способ их получения
Номер патента: 20271
Опубликовано: 30.09.2014
Авторы: Шань Ханьбинь, Юань Чжэдун, Чжан Пэн, Хуан Ю, Юй Сюй
Формула / Реферат
1. Соединение А следующей формулы:
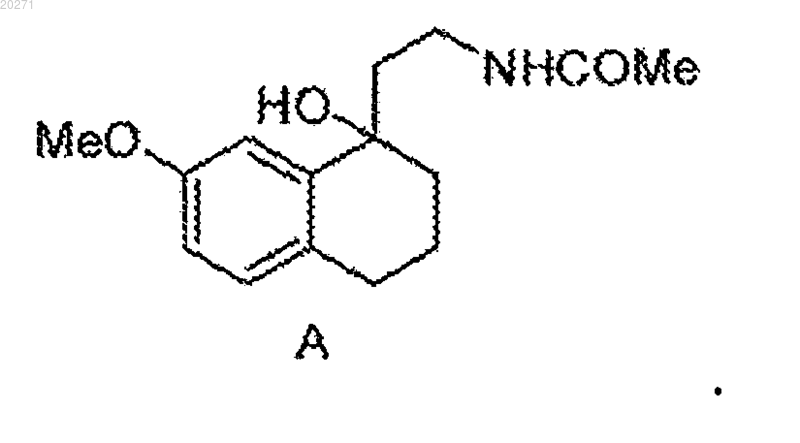
2. Соединение В следующей формулы:
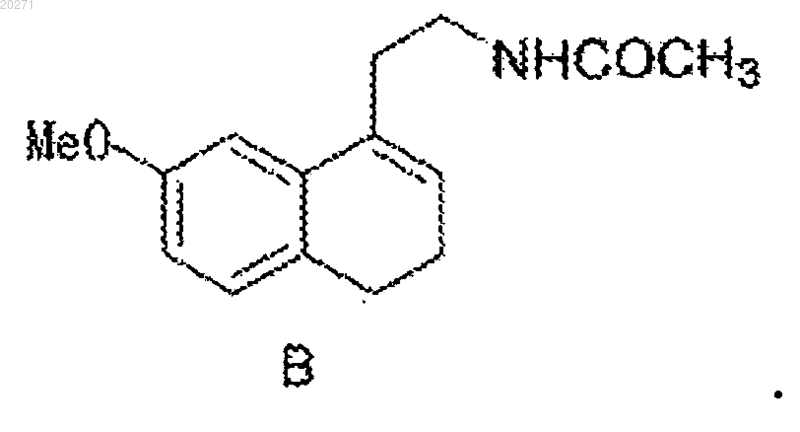
3. Способ получения соединения А по п.1, включающий восстановительное ацилирование соединения С в условиях каталитической гидрогенизации и в присутствии уксусного ангидрида
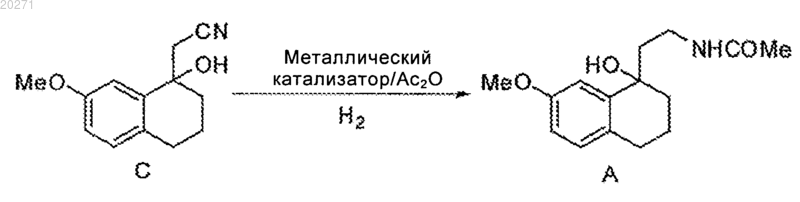
4. Способ по п.3, который отличается тем, что металлический катализатор представляет собой никель Ренея, количество которого составляет 0,1-0,3 мас.экв. по отношению к количеству соединения С.
5. Способ по п.3, который отличается тем, что количество уксусного ангидрида составляет 1-1,3 мол.экв. по отношению к количеству соединения С.
6. Способ получения агомелатина, включающий дегидратацию и ароматизацию соединения А до получения продукта формулы I
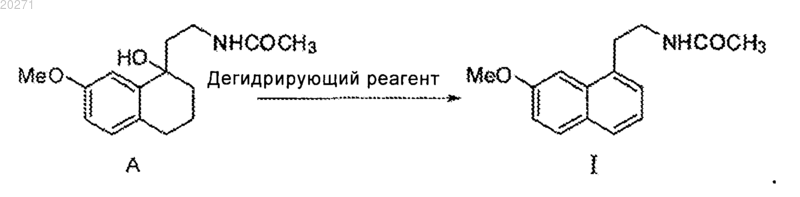
7. Способ получения агомелатина по п.6, который отличается тем, что применяемый дегидрирующий реагент при ароматизации представляет собой дихлордицианобензохинон.
8. Способ получения агомелатина по п.6, который отличается тем, что количество дегидрирующего реагента составляет 1-3 мол.экв. по отношению к количеству соединения А.
9. Способ получения агомелатина по п.6, который отличается тем, что применяемый в реакции растворитель представляет собой смесь толуола и ледяной уксусной кислоты, смесь ацетонитрила и ледяной уксусной кислоты или ледяную уксусную кислоту.
10. Способ получения соединения В по п.2, включающий дегидратацию соединения А в кислотных условиях
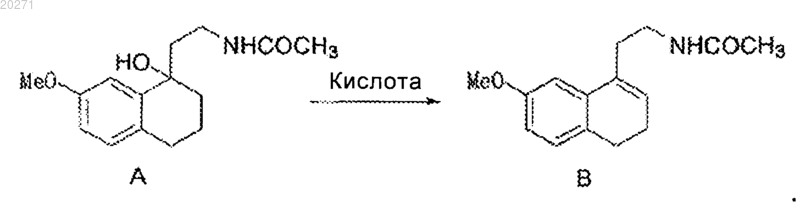
11. Способ получения агомелатина, включающий реакцию соединения В с дегидрирующим реагентом до получения продукта формулы I
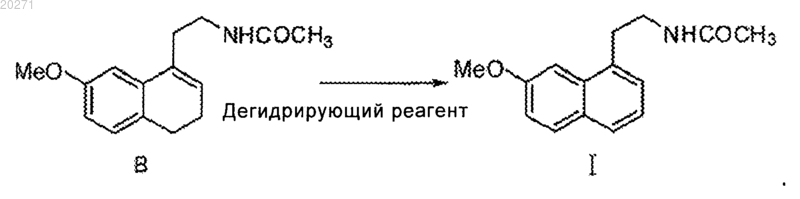
12. Способ получения агомелатина по п.11, который отличается тем, что дегидрирующий реагент представляет собой дихлордицианобензохинон.
13. Способ получения агомелатина по п.11, который отличается тем, что количество дегидрирующего реагента составляет 1-3 мол.экв. по отношению к количеству соединения В.
14. Способ получения агомелатина по п.11, который отличается тем, что применяемый органический растворитель представляет собой дихлорметан или толуол.
15. Способ получения агомелатина, включающий следующие стадии:
a) восстановительное ацилирование соединения С в условиях каталитической гидрогенизации и в присутствии уксусного ангидрида до получения соединения А
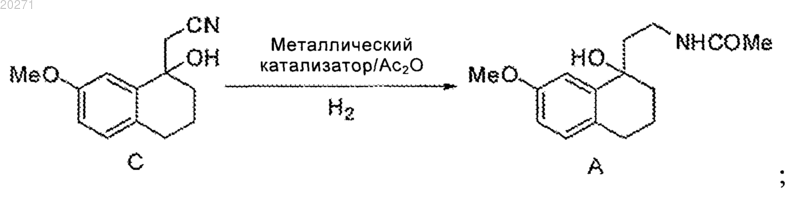
b) дегидратация и ароматизация соединения А с дегидрирующим реагентом до получения продукта формулы I

16. Способ получения агомелатина по п.15, который отличается тем, что проводят дегидратацию соединения А в кислотных условиях до получения соединения В, затем осуществляют реакцию соединения В с дегидрирующим реагентом до получения продукта формулы I
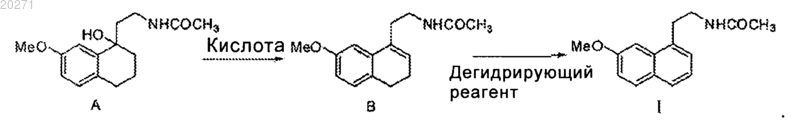
Текст
ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ АГОМЕЛАТИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ Настоящее изобретение относится к промежуточным соединениям для получения агомелатина,так же, как и к способам их получения. Промежуточное соединение настоящего изобретения для получения агомелатина представляет собой соединение А в соответствии с следующей формулой. Также обеспечены два новых промежуточных соединения. Когда применяются эти новые промежуточные соединения для получения агомелатина, способ является простым для управления, хорошо контролируемым и дает продукт с высокой чистотой, без сложных операций, таких как ректификация и разделение хроматографией на колонке, и является подходящим для промышленного производства. При этом способы получения самих двух новых промежуточных соединений являются простыми и с высоким выходом, только когда применяют наиболее широкоиспользуемый 7-метокситетралон в качестве исходного стартового материала и проводят одну стадию реакции для получения промежуточных соединений, с последующей еще одной стадией преобразования промежуточного соединения в желаемый продукт агомелатин. Упомянутые процессы реакции очень упрощены, с улучшенным выходом реакции, а также преодолевают трудности в очистке предыдущего способа при сравнении с предыдущей методикой получения агомелатина. Обычно выход настоящего изобретения составляет свыше 70%.(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) Область изобретения Изобретение относится к промежуточному соединению веществ для получения агомелатина, так же как и к способам их получения. Предпосылка создания изобретения Агомелатин имеет химическую структуру в соответствии с формулой (I) с химическим названиемN-[2-(7-метокси-1-нафтил)этил]ацетамид и торговым наименованием Valdoxan. Он обладает двойным фармакологическим действием, является не только агонистом рецепторов мелатонергической системы, а также антагонистом 5 НТ 2 С рецептора. Упомянутые свойства имеют активность в центральной нервной системе, особенно в лечении глубокой депрессии, сезонных эмоциональных нарушений, диссомнии, сердечно-сосудистых заболеваний, заболеваний пищеварительной системы, инсомнии и утомления, вызванного расстройством биоритмов в связи с перелтом через несколько часовых поясов, нарушений аппетита и ожирения. Это первый антидепрессивный агент мелатонинового типа, который может эффективно лечить депрессивные расстройства, улучшать параметры сна и поддерживать сексуальную функцию. Он был одобрен EU 24 февраля 2009 г., с торговым наименованием Valdoxan/Thymanax. Принимая во внимание фармацевтическую ценность вещества важно получить вещество эффективным промышленным синтетическим способом, который может быть легко преобразован в крупномасштабное производство в промышленности, и получить агомелатин с хорошим выходом и высокой чистоты. Описано много способов синтеза агомелатина, которые могут быть условно разделены на четыре типа, в которых все исходные материалы являются соединением формулы (II). Описание европейского патента ЕР 0447285 представляет способ получения агомелатина (I): реакция 7-метокситетралона (II) с этилбромацетатом реакцией Реформатского и затем дегидроароматизация с серой до получения этилового эфира (7-метокси-1-нафтил)уксусной кислоты (IV) с последующим гидролизом, ацильным хлорированием, аммонификацией, дегидратацией и восстановлением до выхода соединения (VIII), которое в конце ацетилируют до получения агомелатина (I), как показано ниже: Тем не менее, у вышеупомянутого способа есть некоторые недостатки:(1) он имеет восемь стадий синтеза 2-(7-метокси-1-нафтил)этиламина, таким образом производится средний выход меньше чем 30%;(2) когда вышеупомянутый способ переводят в промышленный масштаб, трудно осуществить реакцию, главным образом, из-за плохой воспроизводимости первой стадии; первая стадия включает реакцию 7-метокситетралона (II) с этилбромацетатом путем реакции Реформатского до получения этил (7 метокси-3,4-дигидронафтален-1(2 Н)-илиден)ацетата, которая требует бензол в качестве растворителя; рассматривая факторы окружающей среды, очевидно, что стадия не отвечает требованиям крупномасштабного производства;(3) следующая стадия ароматизации этил(7-метокси-3,4-дигидронафтален-1(2 Н)-илиден)ацетата обычно является незавершнной и после сапонификации часто приводит к смеси, из которой трудно выделить чистый продукт (IV). Китайский патент CN 1680284 описывает другой способ синтеза агомелатина: в результате реакции 7-метокситетралона (II) с циано-уксусной кислотой получают промежуточное соединение (IX), промежуточное соединение (IX) дегидрировано в присутствии гидрирующего катализатора Pd-C с аллилметакрилатом в качестве дегидрирующего реагента с последующим восстановлением, чтобы генерировать соединение (VIII), и в заключение соединение (VIII) преобразовывают в агомелатин (I) ацетилированием. Общий выход составляет около 72%, как показано ниже: Но в вышеупомянутом способе есть некоторые недостатки:(1) в ходе реакции применяются некоторые канцерогенные агенты, например, при преобразовании формулы (II) в формулу (IX) применяется бензиламиновая/гептановокислотная система катализатора с высокой токсичностью;(2) во время преобразования формулы (IX) в (VII) в качестве дегидрирующего реагента применяется пропилметакрилат, который приводит к значительному загрязнению окружающей среды, более того,эта стадия реакции фактически, как было найдено, имеет низкий выход и трудно воспроизводится; и(3) во время процесса гидрогенизации при преобразовании формулы (VII) в (VIII) образуется побочный продукт с формулой (XII); так как природа побочного продукта подобна желаемому продукту и эта стадия является предпоследней стадией, трудно очистить желаемый продукт и существует значительная потеря выхода после перекристаллизации. Рассматривая лекарственную ценность и хорошие перспективы рынка агомелатина, важно синтезировать соединение формулы (I) эффективным для индустриализации способом. Раскрытие изобретения Одна задача настоящего изобретения - обеспечить два новых промежуточных соединения веществ для получения агомелатина. Когда применяются эти новые соединения для получения агомелатина, способ просто контролировать, он является легким для работы (без сложных операций, таких как ректификация и хроматографическое разделение на колонке), хорошо управляемым, получают продукт с высокой чистотой и выходом, он является подходящим для промышленного производства. Другая задача настоящего изобретения - обеспечить способы получения двух вышеупомянутых промежуточных соединений веществ и их применение. В этих целях в настоящем изобретении применяются следующие технические решения. Применяется соединение формулы (А) Способ получения соединения формулы (А) представляет собой восстановительное ацилирование соединения формулы (С) в условиях каталитической гидрогенизации в присутствии уксусного ангидрида. Применяемый катализатор при преобразовании соединения формулы (С) в соединение формулы(А) представляет собой общепринятый металлический катализатор, такой как активированный кобальт,активированный никель (Ni), предпочтительно никель Ренея; количество катализатора может составлять 0,1-0,3 мас.экв. по отношению к количеству соединения С; количество уксусного ангидрида составляет 1-3 мол.экв. по отношению к количеству соединения С, более предпочтительно 1-1,3 мол.экв. Применяемый органический растворитель в этой реакции представляет собой широко используемые органические растворители, такие как диоксан, ТГФ, ацетонитрил или уксусный ангидрид, предпочтительно ТГФ. Оптимальная температура реакции составляет 10-50 С, более предпочтительно 20-30 С. Время реакции зависит от полноты расхода обнаруживаемого реагента, обычно составляет 6-12 ч. После завершения реакции методика обработки может быть выполнена согласно общепринятым в уровне техники способам. В настоящем изобретении обеспечен способ получения агомелатина, применяя соединение А,включающий дегидратацию и ароматизацию соединения А до получения желаемого продукта формулы I При преобразовании соединения А в соединение I путем ароматизации, как показано выше, дегидрирующий реагент предпочтительно представляет собой дихлордицианобензохинон (ДДХ), количество упомянутого дегидрирующего реагента предпочтительно составляет 1-3 мол.экв. по отношению к количеству соединения А, более предпочтительно 1-1,3 мол.экв. Применяемый органический растворитель в этой реакции представляет собой широко используемые органические растворители, например один из толуола, диоксана, ТГФ, ацетонитрила или ледяной уксусной кислоты или любой их смеси, предпочтительно смесь толуола и ледяной уксусной кислоты,смесь ацетонитрила и ледяной уксусной кислоты или ледяная уксусная кислота. Количество упомянутого органического растворителя в основном составляет 10-50 мл/г соединения А. Температура реакции предпочтительно составляет 30-150 С, более предпочтительно 50-100 С. Время реакции зависит от полноты расхода обнаруживаемого реагента, обычно составляет от 30 мин до 12 ч. После завершения реакции методика обработки может быть выполнена согласно общепринятым в уровне техники способам. Применяется соединение формулы (В) Способ получения соединения формулы (В) представляет собой дегидратацию соединения А в кислотных условиях Применяемая кислота при преобразовании соединения А в соединение В является общепринятой кислотой, такой как галогеноводородная кислота, серная кислота, уксусная кислота и подобное. Применяемый органический растворитель представляет собой широко используемый органический растворитель, такой как спирты, диоксан, ТГФ или ацетонитрил, предпочтительно спиртовый растворитель, например этилацетат, ацетон и подобное. Количество упомянутого органического растворителя в основном составляет 10-50 мл/г соединения А. Температура реакции предпочтительно составляет 20-40 С, более предпочтительно 0-30 С. Время реакции зависит от полноты расхода обнаруживаемого реагента, обычно составляет 1-3 ч. После завершения реакции методика обработки может быть выполнена согласно общепринятым в уровне техники способом. В настоящем изобретении обеспечен способ получения агомелатина, применяя соединение В,включающий реакцию соединения В с дегидрирующим реагентом до получения желаемого продукта формулы I При преобразовании соединения В в соединение I дегидрирующий реагент предпочтительно представляет собой дихлордицианобензохинон (ДДХ), количество упомянутого дегидрирующего реагента предпочтительно составляет 1-3 мол.экв. по отношению к количеству соединения В, более предпочтительно 1-1.3 мол.экв. Применяемый органический растворитель в этой реакции представляет собой широко используемые органические растворители, такие как дихлорметан, диоксан, ТГФ, ацетонитрил, ледяная уксусная кислота или подобное, предпочтительно дихлорметан или толуол. Количество упомянутого органического растворителя в основном составляет 10-50 мл/г соединения В. Температура реакции предпочтительно составляет 0-50 С, более предпочтительно 10-30 С. Время реакции зависит от полноты расхода обнаруживаемого реагента, обычно составляет от 30 мин до 6 ч. После завершения реакции методика обработки может быть выполнена согласно общепринятым в уровне техники способам. Способ получения агомелатина включает следующие стадии:a) восстановительное ацилирование соединения С в условиях каталитической гидрогенизации и в присутствии уксусного ангидрида до получения соединения Аb) дегидратация и ароматизация соединения А с дегидрирующим реагентом до получения желаемого продукта формулы I В способе получения агомелатина в настоящем изобретении также можно применить следующий ход реакции, включающий, во первых, дегидратацию соединения А в кислотных условиях до получения соединения В, затем реакцию соединения В с дегидрирующим реагентом до получения желаемого продукта формулы I Промежуточное соединение формулы С может быть получено конденсацией формулы II и ацетонитрила в присутствии катализатора Применяемый катализатор при преобразовании соединения формулы II в соединение формулы С является бутиллитием. И количество катализатора, и количество ацетонитрила составляют 1-3 мол.экв. по отношению к количеству соединения II, более предпочтительно 1-1,3 мол.экв. Применяемым органическим растворителем в этой реакции является безводный органический растворитель, такой как диоксан, ТГФ и подобное, которому нужна дегидратационная обработка или он может быть куплен непосредственно от коммерческих поставщиков. Количество упомянутого органического растворителя обычно составляет 5-20 мл/г соединения II. Оптимальная температура реакции составляет от -80 до -50 С, более предпочтительно от -70 до -60 С. Время реакции зависит от полноты расхода обнаруживаемого реагента,-4 020271 обычно составляет от 1 мин до 3 ч. После завершения реакции методика обработки может быть выполнена согласно общепринятым в уровне техники способом. Соединение С также может быть получено согласно способам, раскрытым в литературе по этой тематике, такой как Journal of Medicinal Chemistry, 1976, 19(6), 803. Реагенты и исходные материалы, применяемые в настоящем изобретении, коммерчески доступны,если не определено иначе. Преимущества настоящего изобретения: изобретение обеспечивает два новых промежуточных соединения; когда применяются эти новые соединения для получения агомелатина, способ просто контролировать, он легкий для обработки, без сложных операций, таких как ректификация и разделение хроматографией на колонке, хорошо управляемый, дает продукт с высокой чистотой, является подходящим для промышленного производства. При этом способ получения самих двух новых промежуточных соединений является простым и с высоким выходом, только когда применяют наиболее широко используемый 7-метокситетралон (II) в качестве исходного стартового материала и проводят одну стадию реакции для получения промежуточных соединений с последующей еще одной стадией преобразования промежуточного соединения в желаемый продукт агомелатин. Упомянутые процессы реакции очень упрощены, улучшен выход реакции, а также преодолевают трудности в очистке предыдущего способа при сравнении с предыдущей методикой получения агомелатина. Обычно выход настоящего изобретения составляет свыше 70%. Примеры Следующие примеры используются для дополнительной иллюстрации настоящего изобретения, но они не предназначены, чтобы каким-либо образом ограничить область изобретения. Пример 1. Синтез 2-(1-гидроксил-7-метокси-1,2,3,4-тетрагидронафтален-1-ил)ацетонитрила (соединение С). В реакционную мкость добавляли ацетонитрил (19,0 мл) и безводный ТГФ (50 мл), охлаждали до-70 С сухим льдом/этанолом, затем медленно по каплям добавляли раствор н-бутиллития в н-гексане(2,5 М, 142,0 мл). После перемешивания на протяжении получаса при этой температуре медленно по каплям добавляли раствор соединения II (44,6 г) в безводном ТГФ (300 мл) и перемешивали на протяжении 1 ч при той же температуре. Реакцию быстро охлаждали путем добавления насыщенного водного хлорида аммония (700 мл), экстрагировали этилацетатом (350 мл 3). Органические слои объединяли, промывали насыщенным водным NaCl (350 мл), сушили над безводным сульфатом натрия и концентрировали до получения грязно-белого названного продукта (54,3 г). Выход: 98,3%. Пример 2. Синтез N-[2-(1-гидроксил-7-метокси-1,2,3,4-тетрагидронафтален-1-ил)этил]ацетамида (соединение А). Соединение С (54,3 г) растворяли в ТГФ (500 мл) и затем добавляли уксусный ангидрид (33,1 г) и никель Ренея (10 г). Реакционную смесь гидрогенизировали давлением водорода, выдерживая 1,1 МПа,при температуре 30 С, до завершения реакции. Смесь охлаждали до комнатной температуры, фильтровали и концентрировали для удаления ТГФ. Остаток разбавляли этилацетатом (500 мл), промывали насыщенным водным NaHCO3 (150 мл), водой (150 мл) и насыщенным водным NaCl (150 мл). Получившуюся органическую фазу сушили над безводным сульфатом натрия, фильтровали и концентрировали до получения грязно-белого продукта А (56,0 г). Выход: 85%. 1H-ЯМР (CDCl3) : 1.77-1.98 (m, 4 Н), 1.92 (s, 3 Н), 2.01-2.11 (m, 2H), 2.28 (s, 0 Н), 2.67-2.77 (m, 2 Н),3.28-3.50 (m, 2 Н), 3.80 (s, 3 Н), 6.32 (s, NH), 6.74-7.27 (m, 3H). ЭСИ-МС (м/з): 286.1 (M+Na). Тпл: 106-109 С. Пример 3. Синтез N-[2-(7-метокси-1-нафтил)этил]ацетамида (соединение I). Соединение А (56,0 г) растворяли в толуоле (500 мл) и добавляли уксусную кислоту (50 мл), ДДХ(53,2 г) и смесь нагревали при 40 С на протяжении около 5 ч. После завершения реакции смесь отфильтровывали, фильтрат промывали насыщенным водным NaHCO3 (250 мл 2), водой (250 мл) и насыщенным водным NaCl (250 мл). Получившуюся органическую фазу сушили над безводным сульфатом натрия, фильтровали и выпаривали растворитель. Остаток перекристаллизовывали из смеси этанол-вода(1:1), сушили в печи до получения названного продукта в виде белого порошка (43,8 г). Выход: 85%. 1 Н-ЯМР (CDCl3) : 1.922 (s, 3 Н), 3.21-3.24 (t, 2H), 3.56-3.61 (q, 2H), 3.96 (s, 3 Н), 5.97 (s, 1 Н), 7.147.16 (q, 1H), 7.22-7.26 (m, 2H), 7.46-7.47 (m, 1H), 7.64-7.67 (m, 1H), 7.72-7.74 (d, 1H). ЭСИ-МС (м/з): 244.14 (M+H). Пример 4. Синтез 2-(1-гидроксил-7-метокси-1,2,3,4-тетрагидронафтален-1-ил)ацетонитрила (соединение С). В реакционную мкость добавляли ацетонитрил (9,5 мл) и безводный ТГФ (25 мл), охлаждали до-70 С сухим льдом/этанолом и затем медленно по каплям добавляли раствор н-бутиллития в н-гексане(2,5 М, 71,0 мл). После перемешивания на протяжении получаса при этой температуре медленно по каплям добавляли раствор соединения II (22,3 г) в безводном ТГФ (150 мл) и перемешивали на протяжении 1 ч при той же температуре. Реакцию быстро охлаждали путем добавления насыщенного водного хлори-5 020271 да аммония (350 мл), экстрагировали этилацетатом (200 мл 3). Органические слоя объединяли, промывали насыщенным водным NaCl (200 мл), сушили над безводным сульфатом натрия и концентрировали до получения грязно-белого названного продукта (27,2 г). Выход: 98,4%. Пример 5. Синтез N-[2-(1-гидроксил-7-метокси-1,2,3,4-тетрагидронафтален-1-ил)этил]ацетамида (соединение А). Соединение С (27,2 г) растворяли в ТГФ (250 мл) и затем добавляли уксусный ангидрид (15,6 г) и никель Ренея (4 г). Реакционную смесь гидрогенизировали давлением водорода, выдерживая 1,1 МПа,при температуре 30 С, до завершения реакции. Смесь охлаждали до комнатной температуры, фильтровали и концентрировали для удаления ТГФ. Остаток разбавляли этилацетатом (250 мл), промывали насыщенным водным NaHCO3 (100 мл), водой (100 мл) и насыщенным водным NaCl (100 мл). Получившуюся органическую фазу сушили над безводным сульфатом натрия, фильтровали и концентрировали до получения грязно-белого названного продукта (28,0 г). Выход: 85%. 1H-ЯМР (CDCl3) : 1.77-1.98 (m, 4 Н), 1.92 (s, 3 Н), 2.01-2.11 (m, 2 Н), 2.28 (s, 0H), 2.67-2.77 (m, 2H),3.28-3.50 (m, 2 Н), 3.80 (s, 3 Н), 6.32 (s, NH), 6.74-7.27 (m, 3H). ЭСИ-МС (м/з): 286.1 (M+Na). Тпл: 106-109 С. Пример 6. Синтез N-[2-(7-метокси-3,4-дигидронафтален-1-ил)этил]ацетамида (соединение В). Соединение А (28,0 г) растворяли в этилацетате (300 мл) до образования суспензии, к которой затем по каплям добавляли концентрированную HCl (12 М, 13,3 мл) при КТ. Суспензия постепенно становилась прозрачной. Реакционный раствор дополнительно перемешивали на протяжении 2 ч и выливали в воду(150 мл). После разделения слоев органическую фазу промывали насыщенным водным NaHCO3 (150 мл 2) и насыщенным водным NaCl (150 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали до получения названного продукта в виде масла (25,5 г). Выход: 97,8%. 1 Н-ЯМР (CDCl3) : 1.944 (s, 3 Н), 2.21-2.27 (m, 2H), 2.61-2.69 (m, 4H), 3.40-3.45 (m, 2 Н), 3.80 (s, 3 Н),5.59 (s, NH), 5.90-5.93 (m, 1H), 6.68-7.05 (m, 3 Н). ЭСИ-МС (м/з): 268,3 (M+Na). Пример 7. Синтез N-[2-(7-метокси-1-нафтил)этил]ацетамида (соединение I). Соединение В (25,5 г) растворяли в дихлорметане (250 мл), ДДХ (26,1 г) добавляли порциями и смесь перемешивали всю ночь при КТ. После завершения реакции смесь отфильтровывали и фильтрат промывали насыщенным водным NaHCO3 (150 мл 2), водой (150 мл) и насыщенным водным NaCl (150 мл). Полученную органическую фазу сушили над безводным сульфатом натрия, фильтровали и выпаривали растворитель. Остаток перекристаллизовывали из смеси этанол-вода (1:1), сушили в печи до получения белого порошка (46.4 г). Выход: 91,8%. 1 Н-ЯМР (CDCl3) : 1.922 (s, 3 Н), 3.21-3.24 (t, 2H), 3.56-3.61 (q, 2H), 3.96 (s, 3 Н), 5.97 (s, 1H), 7.147.16 (q, 1 Н), 7.22-7.26 (m, 2 Н), 7.46-7.47 (m, 1 Н), 7.64-7.67 (m, 1 Н), 7.72-7.74 (d, 1H). ЭСИ-МС (м/з): 244,14 (М+Н). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение А следующей формулы: 3. Способ получения соединения А по п.1, включающий восстановительное ацилирование соединения С в условиях каталитической гидрогенизации и в присутствии уксусного ангидрида 4. Способ по п.3, который отличается тем, что металлический катализатор представляет собой никель Ренея, количество которого составляет 0,1-0,3 мас.экв. по отношению к количеству соединения С. 5. Способ по п.3, который отличается тем, что количество уксусного ангидрида составляет 1-1,3 мол.экв. по отношению к количеству соединения С. 6. Способ получения агомелатина, включающий дегидратацию и ароматизацию соединения А до получения продукта формулы I 7. Способ получения агомелатина по п.6, который отличается тем, что применяемый дегидрирующий реагент при ароматизации представляет собой дихлордицианобензохинон. 8. Способ получения агомелатина по п.6, который отличается тем, что количество дегидрирующего реагента составляет 1-3 мол.экв. по отношению к количеству соединения А. 9. Способ получения агомелатина по п.6, который отличается тем, что применяемый в реакции растворитель представляет собой смесь толуола и ледяной уксусной кислоты, смесь ацетонитрила и ледяной уксусной кислоты или ледяную уксусную кислоту. 10. Способ получения соединения В по п.2, включающий дегидратацию соединения А в кислотных условиях 11. Способ получения агомелатина, включающий реакцию соединения В с дегидрирующим реагентом до получения продукта формулы I 12. Способ получения агомелатина по п.11, который отличается тем, что дегидрирующий реагент представляет собой дихлордицианобензохинон. 13. Способ получения агомелатина по п.11, который отличается тем, что количество дегидрирующего реагента составляет 1-3 мол.экв. по отношению к количеству соединения В. 14. Способ получения агомелатина по п.11, который отличается тем, что применяемый органический растворитель представляет собой дихлорметан или толуол. 15. Способ получения агомелатина, включающий следующие стадии:a) восстановительное ацилирование соединения С в условиях каталитической гидрогенизации и в присутствии уксусного ангидрида до получения соединения Аb) дегидратация и ароматизация соединения А с дегидрирующим реагентом до получения продукта формулы I 16. Способ получения агомелатина по п.15, который отличается тем, что проводят дегидратацию соединения А в кислотных условиях до получения соединения В, затем осуществляют реакцию соединения В с дегидрирующим реагентом до получения продукта формулы I
МПК / Метки
МПК: A61K 31/165, C07C 233/18, C07C 231/12, C07C 231/06
Метки: получения, соединения, способ, агомелатина, промежуточные
Код ссылки
<a href="https://eas.patents.su/9-20271-promezhutochnye-soedineniya-agomelatina-i-sposob-ih-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Промежуточные соединения агомелатина и способ их получения</a>
Предыдущий патент: Твердая лекарственная форма, обладающая желчегонным действием (варианты)
Следующий патент: Способ изготовления домашнего сыра с использованием streptococcus thermophilus
Случайный патент: Способ и устройство для непрерывного контроля внутренних областей оборудования и трубопроводов бензохранилища













