Способ получения циталопрама
Формула / Реферат
1. Способ получения циталопрама
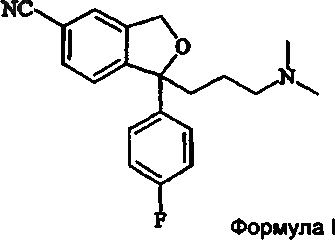
включающий взаимодействие 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и 3-галоген-N,N-диметилпропиламином реактива Гриньяра и затем проведение замыкания цикла полученного соединения формулы XI
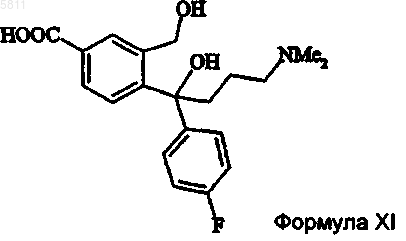
до соединения формулы IV
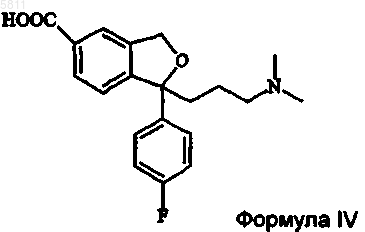
с последующим превращением соединения формулы IV в циталопрам.
2. Способ по п.1, отличающийся тем, что соединение формулы IV взаимодействует с дегидратирующим агентом и сульфонамидом формулы H2N-SO2-R, где R представляет
a) необязательно замещенный NH2 или C1-6-алкилокси,
b) арилокси или гетероарилокси, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4-алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-C1-4-алкиламино, или
c) арил или гетероарил, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4-алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-C1-4-алкиламино.
3. Способ по п.1, отличающийся тем, что соединение формулы IV превращается в соответствующий амид формулы V
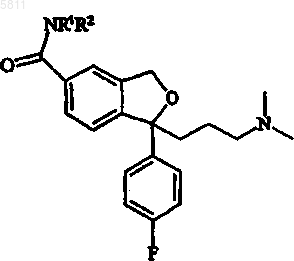
Формула V
где каждый из R1 и R2 независимо представляет водород, C1-6-алкил, C1-6-алкил, замещенный одним или более заместителями, выбранными из группы, содержащей арил и гетероарил, гидрокси, C1-6-алкокси, арилокси, гетероарилокси, арил-C1-6-алкокси или тризамещенный силил, где заместители независимо представляют C1-6-алкил, арил, гетероарил или арил-C1-6-алкил; и затем амид формулы V взаимодействует с дегидратирующим агентом;
при этом получается циталопрам в виде основания или его фармацевтически приемлемой соли.
4. Способ по п.2, где соединение формулы IV взаимодействует с SOCl2 и сульфамидом.
5. Способ по п.4, отличающийся тем, что реакция проводится в сульфолане.
6. Способ по п.3, где соединение формулы IV взаимодействует с POCl3 и трет-бутиламином.
7. Способ по п.1, отличающийся тем, что получение соединения формулы IV и превращение соединения формулы IV проводится без выделения соединения формулы IV.
8. Способ по п.1, отличающийся тем, что соединение формулы IV, по меньшей мере, частично выделяется перед превращением в циталопрам.
9. Способ получения циталопрама
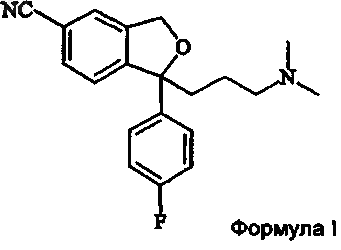
включающий взаимодействие соединения формулы IV
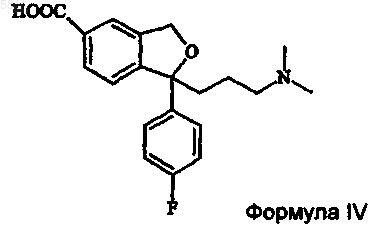
с дегидратирующим агентом и сульфонамидом формулы H2N-SO2-R, где R представляет:
d) необязательно замещенный NH2 или C1-6-алкилокси,
e) арилокси или гетероарилокси, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4-алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-C1-4-алкиламино, или
f) арил или гетероарил, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4-алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-C1-4-алкиламино.
10. Способ получения соединения формулы IV, отличающийся тем, что соединение формулы IV получается при взаимодействии 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и 3-галоген-N,N-диметилпропиламином реактива Гриньяра и с последующим проведением замыкания цикла полученного соединения формулы XI
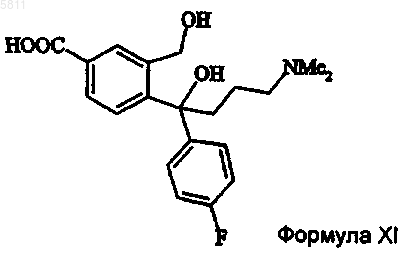
Текст
005811 Настоящее изобретение относится к способу получения известного лекарственного препаратаантидепрессанта циталопрама, 1-[3-(диметиламино)пропил]-1-(4-фторфенил)-1,3-дигидро-5-изобензофуранкарбонитрила, к способам получения промежуточных соединений, применяемых при получении циталопрама, и к способам превращения указанных промежуточных соединений в циталопрам. Предшествующий уровень техники Циталопрам является известным антидепрессантом, который уже в течение нескольких лет поступает в продажу и имеет следующую структурную формулу: Он является селективным ингибитором обратного захвата серотонина (5-гидрокситриптамина; 5-НТ) центрального действия, соответственно обладающим активностями антидепрессанта. Об антидепрессантной активности соединения сообщалось в нескольких публикациях, например J. Hyttel Prog. Neuro-Psychopharmacol.Biol. Psychiat. 1982, 6, 277-295 и A. Gravem Acta Psychiatr. Scand. 1987, 75, 478-486. Кроме того, соединение было раскрыто для демонстрации эффектов, наблюдаемых при лечении деменции (слабоумия) и цереброваскулярных расстройств (ЕР-А 474580). Впервые циталопрам был описан в публикации DE 2657013, соответствующей патенту США 4136193. В данной патентной публикации описано получение циталопрама одним из способов и описан еще один способ, который можно применить для получения циталопрама. Согласно описанному способу соответствующий 1-(4-фторфенил)-1,3-дигидро-5-изобензофуранкарбонитрил взаимодействует с 3-(N,N-диметиламино)пропилхлоридом в присутствии метилсульфинилметина в качестве конденсирующего агента. Исходное вещество получали из соответствующего 5-бромпроизводного путем реакции с цианидом меди (I). Согласно способу, который описан только общими терминами, циталопрам можно получить при замыкании цикла соединения в присутствии дегидратирующего агента и последующего обмена атома брома в положении 5 с цианидом меди (I). Исходное вещество формулы II получали из 5-бромфталида с помощью двух последовательных реакций Гриньяра, то есть с помощью 4-фторфенилмагнийхлорида и с помощью N,Nдиметиламинопропилмагнийхлорида, соответственно. Новый и неожиданный способ и промежуточное соединение для получения циталопрама были описаны в патенте США 4650884, согласно которому промежуточное соединение формулы III подвергают реакции замыкания цикла при дегидратации сильной (концентрированной) серной кислотой для получения циталопрама. Промежуточное соединение формулы III было получено из 5-цианофталида с помощью двух последовательных реакций Гриньяра, то есть с помощью 4-фторфенилмагнийгалогенида и с помощью N,N-диметиламинопропилмагнийгалогенида, соответственно. Еще некоторые способы раскрыты в международных заявках на патентW0 98019511, WO 98019512 и WO 98019513. Заявки WO 98019512 и WO 98019513 касаются способов, где 5-амино-, 5-алкоксикарбонил- или 5-'(втор-аминокарбонил)фталид подвергают двум последовательным реакциям Гриньяра,замыканию цикла и превращению образующегося производного 1,3-дигидроизобензофурана в соответствующее 5-цианосоединение, то есть циталопрам. Международная заявка на патентWO 98019511 раскрывает способ промышленного изготовления циталопрама, где соединение 4-замещенный-2 гидроксиметилфенил-(4-фторфенил)метанола подвергают замыканию цикла и образовавшийся в резуль-1 005811 тате замещенный в положении 5 1-(4-фторфенил)-1,3-дигидроизобензофуран превращают в соответствующее 5-цианопроизводное, которое алкилируют с помошью (3-диметиламино)пропилгалогенида, чтобы получить циталопрам. Наконец, способы получения индивидуальных энантиомеров циталопрама раскрыты в патенте США 4943590, из которого также следует, что замыкание цикла промежуточного соединения формулы III можно провести через неустойчивый сложный эфир в присутствии основания. Теперь неожиданно установлено, что циталопрам можно изготовить с помощью новой удобной и надежной методики, применяя подходящие исходные вещества. Краткое содержание изобретения Настоящее изобретение соответственно относится к новому способу получения циталопрама,имеющего формулу I включающему взаимодействие 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и 3-галоген-N,N-диметилпропиламином реактива Гриньяра с последующим проведением замыкания цикла полученного соединения формулы XI до соединения формулы IV сопровождаемым превращением соединения формулы IV в циталопрам. В частности, изобретение относится к такому способу, который включает:i) взаимодействие соединения формулы IV с дегидратирующим агентом и сульфонамидом формулыii) превращение соединения формулы IV в соответствующий амид формулы V где каждый из R1 и R2 независимо представляет водород, C1-6-алкил, C1-6-алкил, замещенный одним или более заместителями, выбранными из группы, содержащей арил и гетероарил, гидрокси, C1-6-алкокси,арилокси, гетероарилокси, арил-С 1-6-алкокси или тризамещенный силил, где заместители независимо представляют C1-6-алкил, арил, гетероарил или арил-С 1-6-алкил; и затем взаимодействие амида формулыV с дегидратирующим агентом с получением таким образом циталопрама в виде основания или его фармацевтически приемлемой соли. Превращение 5-карбоксипроизводного формулы IV в амид формулы V может быть проведено через активированное кислотой производное формулы VI Формула VI где R представляет галоген, C1-6-алкокси, арилокси, гетероарилокси, арил-С 1-6-алкокси, гетероарил-С 1-6 алкокси, алкилкарбонат, арилкарбонат, алкилкарбамат, арилкарбамат, алкилтиокарбонат, арилтиокарбонат, алкилтиокарбамат, арилтиокарбамат, алкилацилокси, арилацилокси, гетероарилацилокси, замещенный или незамещенный арил или замещенный или незамещенный гетероарил. Другой аспект изобретения относится к способам получения промежуточного соединения формулыIV, включающим реакцию 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и с 3-галоген-N,N-диметилпропиламином реактива Гриньяра и затем проведение замыкания цикла образующегося соединения формулы XI до соединения формулы IV. 4-Галогенфторфенил реактива Гриньяра представляет галогенид магния, такой как хлорид, бромид или иодид. Предпочтительно применяют бромид магния. 3-галоген-N,N-диметилпропиламин реактива Гриньяра представляет галогенид магния, такой как хлорид, бромид или иодид, предпочтительно хлорид магния. Предпочтительно, когда две реакции проводятся последовательно без выделения промежуточного соединения, образующегося в результате первой реакции Гриньяра. Замыкание цикла соединения формулы XI проводится с помощью кислоты или через неустойчивый сложный эфир с основанием или без него. Замыкание цикла в присутствии кислоты проводится с помощью неорганической кислоты, такой как серная или фосфорная кислота, или органической кислоты, такой как метилсульфоновая, п-толуолсульфоновая или трифторуксусная кислота. Замыкание цикла в присутствии основания проводится через неустойчивый сложный эфир, такой как метансульфониловый, п-толуолсульфониловый, 10-камфорсульфониловый, трифторуксусный или трифторметансульфониловый сложный эфир с добавлением основания, такого как триэтиламин, диметиланилин, пиридин и т.д. Реакция проводится в инертном растворителе, предпочтительно при охлаждении, в частности, около 0 С, и предпочтительно проводится в одной емкости, то есть этерификация с одновременным добавлением основания. 5-Карбоксифталид, применяемый в качестве исходного вещества, может быть получен с помощью способов, описанных в патенте США 3607884 или в патенте Германии 2630927, то есть при взаимодействии концентрированного раствора терефталевой кислоты с формальдегидом в жидком SО 3 или при электрохимическом гидрировании тримеллитовой кислоты. Еще один аспект изобретения относится к способу получения циталопрама-3 005811 включающему взаимодействие соединения формулы IVc) арил или гетероарил, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4 алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-С 1-4-алкиламино. Еще один аспект настоящего изобретения относится к фармацевтической композиции с антидепрессивным действием, содержащей циталопрам в виде основания или любой его подходящей соли, изготовленной с помощью способов согласно изобретению. Повсюду в описании и в формуле изобретения термин дегидратирующий агент относится к любому подходящему дегидратирующему агенту, и специалист в данной области может легко определить оптимальный агент. Примерами подходящих дегидратирующих агентов являются SOCl2, POCl3, PCl5,SОВr2, РОВr3, РВr5, SOI2, РОI3, PI5, P4O10, оксалилхлорид, карбонилдиимидазол и реактивы Вильсмайера. Предпочтительно применяют хлор-содержащий агент, наиболее предпочтительно применяют SOC12 или РОС 13. Реактивы Вильсмайера представляют реактивы, образованные смешиванием N,N-диметилформамида (ДМФ) и дегидратирующих агентов, примерами которых являются ДМФ/SОС 12 и ДМФ/РОС 13. Повсюду в описании и в формуле изобретения C1-6-алкил относится к алкильной группе с разветвленной и неразветвленной цепью, содержащей от одного до шести атомов углерода включительно, такой как метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-2-пропил, 2,2-диметил-1-этил и 2-метил 1-пропил. Точно так же C1-4-алкил относится к такой же группе, содержащей от одного до четырех атомов углерода включительно, а C1-6-алкокси, C1-4-алкокси и C1-4-алкиламин определяют такие группы, в которых алкильная часть имеет значение, определенное выше. Галоген означает фтор, хлор, бром или йод. В способе i) изобретения одним из возможных, но нелимитирующим механизмом реакции является тот, при котором 5-карбоксисоединение формулы IV реагирует с дегидратирующим агентом для того,чтобы образовать соответствующее активированное производное, которое затем реагирует с сульфонамидом H2N-SO2-R, образуя при этом циталопрам. Во время последней реакции может быть необходимо каталитическое количество кислоты. Сульфонамид H2N-SO2-R, применяемый в способе, предпочтительно представляет сульфамид NH2SO2-NH2. Применяемый в способе необязательно замещенный NH2 предпочтительно представляет третбутиламин. Реакции с дегидратирующими агентами в способе согласно изобретению проводят без разбавления или в подходящем растворителе, таком как сульфолан или ацетонитрил. Когда в реакции дегидратацииii) применяется растворитель, может быть необходимо присутствие каталитического количества N,Nдиметилформамида. При одном из воплощений изобретения изготовление соединения формулы IV и превращение соединения формулы IV в циталопрам выполняется без выделения соединения формулы IV, так называемый синтез в одной емкости. При другом воплощении изобретения соединение формулы IV, по меньшей мере, частично выделяют до превращения в циталопрам. Соединение формулы I можно применять в виде свободного основания или в виде его фармацевтически приемлемой кислой аддитивной соли. В качестве кислотно-аддитивных солей можно применять такие соли, образованные с органическими или неорганическими кислотами. Примерами таких органических солей являются соли с малеиновой, фумаровой, бензойной, аскорбиновой, янтарной, щавелевой,бис-метиленсалициловой, метансульфоновой, этандисульфоновой, уксусной, пропионовой, винной, салициловой, лимонной, глюконовой, молочной, яблочной, миндальной, коричной, цитраконовой, аспаргиновой, стеариновой, пальмитиновой, итаконовой, гликолевой, п-аминобензойной, глутаминовой, бензолсульфоновой и с теофиллинуксусной кислотами, также как с 8-галогентеофиллинами, например с 8 бромтеофиллином. Примерами таких неорганических солей являются соли с хлористо-водородной, бромисто-водородной, серной, сульфаминовой, фосфорной и азотной кислотами. Кислые аддитивные соли соединений можно получить известными в данной области способами.-4 005811 Основание подвергают взаимодействию или с расчетным количеством кислоты в растворителе, смешивающимся с водой, в таком как ацетон или этанол, с последующим выделением соли при концентрировании и охлаждении, или взаимодействию с избытком кислоты в растворителе, несмешивающимся с водой, в таком как диэтиловый эфир, этилацетат или дихлорметан, со спонтанным выделением соли. Фармацевтические композиции согласно изобретению можно вводить любым подходящим способом и в любой подходящей форме, например перорально в виде таблеток, капсул, порошков или сиропов или парентерально в виде обычных стерильных растворов для инъекции. Фармацевтические составы согласно изобретению можно получить обычными в данной области способами. Например, таблетки можно получить, смешивая активный компонент с обычными вспомогательными веществами и/или разбавителями и затем прессуя смесь в обычной машине для таблетирования. Примеры вспомогательных веществ или разбавителей включают: кукурузный крахмал, картофельный крахмал, тальк, стеарат магния, желатин, лактозу, связующие и т.п. Любое другое вспомогательное вещество или добавки красителей, ароматизаторов, консервантов и т.д. могут быть применимы при условии, что они совместимы с активными ингредиентами. Растворы для инъекций можно приготовить при растворении активного ингредиента и возможных вспомогательных веществ в части растворителя для инъекции, предпочтительно стерильной воды, доводя раствор до требуемого объема, стерилизуя раствор и заполняя им подходящие ампулы или пузырьки. Можно добавлять любые подходящие добавки, традиционно применяемые в данной области, такие как тонизирующие агенты, консерванты, антиоксиданты и т.д. Примеры Далее изобретение иллюстрируется следующими примерами, которые не должны рассматриваться,как ограничение объема изобретения. Пример 1. 5-карбоксициталопрам. К перемешиваемой суспензии/раствору 5-карбоксифталида (1,0 г, 5,7 ммоль) в сухом ТГФ (20 мл) в атмосфере азота добавляют N,N,N',N',-тетраметилэтилендиамин (2,2 мл, 1,7 г, 14 ммоль). Добавляют по каплям раствор п-фторфенилмагнийбромида (около 0,5 М) и бромида магния (около 0,125 М) в ТГФ (около 60 мл) до тех пор, пока не останется 5-карбоксифталида. Затем добавляют по каплям раствор 3-(N,Nдиметиламино)пропилмагнийхлорида в ТГФ/гептане (около 2 М, около 15 мл), пока совсем не останется предшествующего промежуточного соединения. Затем раствор выпаривают, получая при этом хрупкое твердое вещество. Полученное твердое вещество обрабатывают насыщенным водным раствором хлорида аммония (2 мл) и водой и водным раствором хлористоводородной кислоты (10 М) доводят рН до 6. Раствор промывают простым эфиром. ВЭЖХ-анализ водного слоя показал, что в нем присутствует диол,достаточно чистый для продолжения эксперимента (чистота 90%, область пика ВЭЖХ -УФ 220 нм). рН доводят до рН 1 водным раствором хлористо-водородной кислоты (10 М) и перемешивают раствор в течение 2 ч. ВЭЖХ-анализ показал, что присутствует 5-карбоксициталопрам, достаточно чистый для дальнейшего применения (чистота 80%, область пика ВЭЖХ - УФ 220 нм). Пример 2. 5-циано-1-(4-фторфенил)-1-(3-диметиламинопропил)-1,3-дигидроизобензофуран (Циталопрам, свободное основание) 5-карбокси-1-(4-фторфенил)-1-(3-диметиламинопропил)-1,3-дигидроизобензофуран (5 г, 0,015 моль) и сульфамид (1,65 г, 0,017 моль) растворяют в сульфолане (15 мл). Добавляют тионилхлорид (2,25 г, 0,019 моль) при комнатной температуре и повышают температуру реакционной смеси до 130 С в течение 2 ч. Реакционной смеси дают охладиться до 75 С и добавляют воду (25 мл). Температуру поддерживают при 75 С в течение 15 мин и затем охлаждают реакционную смесь до комнатной температуры. С помощью гидроксида аммония доводят рН до 9 и затем добавляют н-гептан (75 мл). Повышают температуру до 70 С и отделяют горячий н-гептановый слой, из которого при охлаждении кристаллизуется указанное в заголовке соединение. Выход 3,77 г. Чистота (область пика ВЭЖХ) 97%. Пример 3. Оксалат 5-циано-1-(4-фторфенил)-1-(3-диметиламинопропил)-1,3-дигидроизобензофурана (Циталопрам, оксалат) К перемешиваемому раствору/суспензии 5-карбоксифталида (57 ммоль) N,N,N',N'-тетраметилэтилендиамина (144 ммоль) в ТГФ (200 мл) добавляют по каплям раствор пфторфенилмагнийбромида (около 0,5 М) и бромида магния (около 0,125 М) в ТГФ до тех пор, пока не останется исходного фталида. Добавляют по каплям раствор 3-(N,N-диметиламино)пропилмагнийхлорида(около 2M в ТГФ/гептане), пока совсем не останется предшествующего промежуточного соединения. В экзотермическую реакционную смесь в течение 5 мин добавляют по каплям метансульфонилхлорид (228 ммоль). Через 30 мин добавляют ДМФ (5 мл), после чего в умеренно экзотермическую реакционную смесь в течение 10 мин по каплям добавляют РОСl3 (228 ммоль) и смесь перемешивают в течение 2 ч. В течение 15 мин по каплям добавляют т-бутиламин (285 ммоль) и смесь перемешивают в течение ночи. По каплям добавляют ДМФ (5 мл), после чего в течение 1 ч добавляют РОСl3 (2,3 моль). Смесь перемешивают в течение ночи и затем нагревают с обратным холодильником в течение 1 ч. Смесь охлаждают на ледяной бане и в экзотермическую реакционную смесь в течение 1 ч осторожно по каплям добавляют воду (200 мл). Смесь подщелачивают до рН 9 водным раствором аммиака в воде (25% мас./об.). Добав-5 005811 ляют толуол (100 мл) и отфильтровывают смесь. Остаток промывают толуолом, объединенные фильтраты отделяют и собирают органическую фракцию. Органическую фракцию дважды экстрагируют водным раствором H2SO4 (10% об./об.). Объединенные кислотные экстракты подщелачивают до рН 9 водным раствором аммиака в воде (25% мас./об.) и экстрагируют толуолом. Объединенные слои толуола сушат и выпаривают, получая при этом циталопрам (основание) в виде темного маслянистого вещества. Оксалатную соль получают, применяя стандартные методики для получения оксалата циталопрама. Выход 9,2 г. Чистота (область пика ВЭЖХ) 90%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения циталопрама включающий взаимодействие 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и 3-галоген-N,N-диметилпропиламином реактива Гриньяра и затем проведение замыкания цикла полученного соединения формулы XI до соединения формулы IV с последующим превращением соединения формулы IV в циталопрам. 2. Способ по п.1, отличающийся тем, что соединение формулы IV взаимодействует с дегидратирующим агентом и сульфонамидом формулы H2N-SO2-R, где R представляетa) необязательно замещенный NH2 или C1-6-алкилокси,b) арилокси или гетероарилокси, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4-алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-С 1-4-алкиламино, или с) арил или гетероарил, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4 алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-С 1-4-алкиламино. 3. Способ по п.1, отличающийся тем, что соединение формулы IV превращается в соответствующий амид формулы V Формула V где каждый из R1 и R2 независимо представляет водород, С 1-6-алкил, C1-6-алкил, замещенный одним или более заместителями, выбранными из группы, содержащей арил и гетероарил, гидрокси, C1-6-алкокси,-6 005811 арилокси, гетероарилокси, арил-С 1-6-алкокси или тризамещенный силил, где заместители независимо представляют C1-6-алкил, арил, гетероарил или арил-С 1-6-алкил; и затем амид формулы V взаимодействует с дегидратирующим агентом; при этом получается циталопрам в виде основания или его фармацевтически приемлемой соли. 4. Способ по п.2, где соединение формулы IV взаимодействует с SOCl2 и сульфамидом. 5. Способ по п.4, отличающийся тем, что реакция проводится в сульфолане. 6. Способ по п.3, где соединение формулы IV взаимодействует с РОСl3 и трет-бутиламином. 7. Способ по п.1, отличающийся тем, что получение соединения формулы IV и превращение соединения формулы IV проводится без выделения соединения формулы IV. 8. Способ по п.1, отличающийся тем, что соединение формулы IV, по меньшей мере, частично выделяется перед превращением в циталопрам. 9. Способ получения циталопрама включающий взаимодействие соединения формулы IVf) арил или гетероарил, необязательно замещенный галогеном, C1-4-алкилом, циано, гидрокси, C1-4 алкокси, трифторметилом, нитро, амино, C1-4-алкиламино или ди-С 1-4-алкиламино. 10. Способ получения соединения формулы IV, отличающийся тем, что соединение формулы IV получается при взаимодействии 5-карбоксифталида последовательно с 4-галогенфторфенилом реактива Гриньяра и 3-галоген-N,N-диметилпропиламином реактива Гриньяра и с последующим проведением замыкания цикла полученного соединения формулы XI
МПК / Метки
МПК: C07D 307/87
Метки: способ, циталопрама, получения
Код ссылки
<a href="https://eas.patents.su/8-5811-sposob-polucheniya-citaloprama.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения циталопрама</a>
Предыдущий патент: Бензоилсульфонамиды и сульфонилбензамидины для применения в качестве противоопухолевых агентов
Следующий патент: Ингибиторы тирозинкиназы
Случайный патент: Обувная подошва с убирающимися препятствующими скольжению средствами












