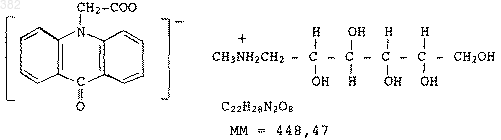Аминокислотные производные хиноксалин-2,3-диона, фармацевстическая композиция, обладающая антагонистической в отношении рецептора глутамата и противосудорожной активностью, способ лечения заболеванийсосудов мозга или судорог и промежуточный продукт
Формула / Реферат
1. Аминокислотные производные хиноксалин-2,3-диона общей формулы (I)
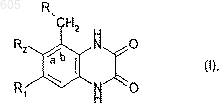
где R означает
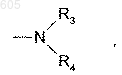
где R3 - водород или метил,
R4 - группа формулы
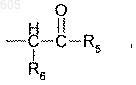
где R5 -гидроксил, низший, алкоксил, амид,
R6 -низший, алкил или аралкил,
R1 - водород, бром, нитро,
R2 - низший алкил, винил,
при этом R2 может находиться в b-положении, а группа R-CH2 - в а-положении кольца,
или их фармацевтически приемлемые соли.
2. Аминокислотные производные хиноксалин-2,3-диона общей формулы (I) по п.1, представляющие собой соединение из группы, включающей
[(7-бром-2,3-диоксо-6-винил-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту,
[(7-бром-6-этил-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту,
сложный этиловый эфир [(6-этил-7-нитро-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты,
[(6-этил-7-нитро-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту.
3. Фармацевтическая композиция, обладающая антагонистической в отношении рецептора глутамата и противосудорожной активностью, содержащая активное вещество и фармацевтически приемлемый носитель, отличающаяся тем, что в качестве активного вещества она содержит соединения по п.1 в терапевтически эффективном количестве.
4. Способ лечения заболеваний сосудов мозга или судорог путем введения активного вещества, отличающийся тем, что в качестве активного вещества используют соединения по п.1 в терапевтически эффективном количестве.
5. Сложный этиловый эфир [(2-амино-5-бром-3-нитро-6-винилбензил)-метиламино]-уксусной кислоты, являющийся промежуточным продуктом для получения соединения формулы I по п.1, у которого R означает остаток N-метиламиноуксусной кислоты, R1 - бром и R2 - винил.
Текст
1 Изобретение относится к новым производным хиноксалин-2,3-диона, обладающим ценными биологическими свойствами, более конкретно к аминокислотным производным хиноксалин-2,3-диона, фармацевтической композиции, обладающей антагонистической в отношении рецептора глутамата и противосудорожной активностью, способу лечения заболеваний сосудов мозга или судорог и промежуточному продукту. Из международной заявки WO 95/12417 от 11 мая 1995 г. известны производные хиноксалин-2,3-диона, обладающие биологическими свойствами, в частности являющиеся антагонистами рецептора глутамата. Задачей изобретения является расширение ассортимента производных хиноксалин-2,3 диона, обладающих ценными биологическими свойствами. Поставленная задача решается предлагаемыми аминокислотными производными хиноксалин-2,3-диона общей формулы (I) где R5 -гидроксил, низший алкоксил, амид,R6 -низший алкил или аралкил,R1 - водород, бром, нитро,R2 - низший алкил, винил,при этом R2 может находиться в b-положении, а группа R-СН 2 - в а-положении кольца,или их фармацевтически приемлемыми солями. Предпочитаются соединения формулы (I),выбранные из группы, включающей[(7-бром-2,3-диоксо-6-винил-1,2,3,4 тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту,[(7-бром-6-этил-2,3-диоксо-1,2,3,4 тетрагидрохиноксалин-5-илметил)метиламино]-уксусную кислоту,сложный этиловый эфир [(6-этил-7-нитро 2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5 илметил)-метиламино]-уксусной кислоты,[(6-этил-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту. К фармацевтически приемлемым кислотно-аддитивным солям соединений формулы I относятся соли с нетоксическими неорганическими кислотами, такими как хлористоводородная кислота, азотная кислота, фосфорная кислота, серная кислота, бромисто 000605 2 водородная кислота, иодистоводородная кислота, фосфористая кислота и др., а также соли с нетоксическими органическими кислотами, такими как алифатические моно- и дикарбоновые кислоты, замещенные фенилом алкановые кислоты, оксиалкановые кислоты, алкандикарбоновые кислоты, ароматические кислоты, алифатические и ароматические сульфокислоты и др. К таким солям причисляют сульфат, пиросульфат, бисульфат, сульфит, бисульфит, нитрат,фосфат, кислый фосфат, первичный фосфат,метафосфат, пирофосфат, хлорид, бромид, иодид, ацетат, пропионат, каприлат, изобутират,оксалат, малонат, сукцинат, суберат, себацинат,фумарат, малеи-нат, манделат, бензоат, хлорбензоат, метилбензоат, динитробензоат, фталат,фенилсульфонат, толуолсульфонат, фенилацетат, цитрат, лактат, тартрат, метансульфонат и др. Возможны и соли с аминокислотами, как,например, аргинат и др. и глюконат, галактуронат. Кислотно-аддитивные соли указанных основных соединений получают обычным образом путем контактирования свободного основания с достаточным количеством желаемой кислоты. Свободное основание можно регенерировать путем контактирования соли с основанием и выделения свободного основания обычным образом. Свободные основания отличаются от соответствующих солей определенными физическими свойствами, как растворимостью в полярных растворителях, однако для цели настоящего изобретения соли являются эквивалентами соответственных свободных оснований. Некоторые из соединений настоящего изобретения могут существовать в нерастворенной форме, а также в растворенной форме, включая гидратированную форму. Как правило, растворенные, в том числе и гидратированные формы являются эквивалентами нерастворенных форм. Некоторые из соединений настоящего изобретения могут иметься в виде смеси цис- и транс-изомеров или в виде отдельных цис- и транс-изомеров или R- и S-стереоизомеров. Смесь изомеров, а также отдельные изомеры входят в объем настоящего изобретения. Аминокислотными остатками вышеприведенной формулы являются, например, аланин,-аланин, цистеин, глицин, фенилаланин и валин. Предлагаемые соединения обладают ценными биологическими свойствами благодаря их сильному антагонизирующему возбудительную аминокислоту действию в одном из некоторых связывающих сайтов рецепторов глутамата: в связывающем сайте рецептора -амино-3 гидрокси-5-метил-4-изоксазолпропионовой кислоты (далее АМПК) или рецептора соли 3 карбоксиметил-4-изопропенилпролина (далее: КИПП) на рецепторах АМПК и рецепторах, не связывающихся с рецептором N-метил-D 3 аспартата (далее: NMDA) или в сайте глицина(далее: ГЛИ) рецептора NMDA. Сродство предлагаемых соединений с рецепторами АМПК определялось по способу,описанному Ноnоr Т. и др., Neuroscience Letters, 1985; 54: 27-32. В данном опыте соединения согласно изобретению проявляют выраженную как KT50 активность, равную 100 мкмоль. Сродство предлагаемых соединений со связывающим сайтом КИПП (рецептора, не связывающегося с NMDA) определялось по способу,описанному London E.D. и Coyle J., Mol. Pharmacol., 1979, 15:492. Сродство предлагаемых соединений со связывающим сайтом глицина рецептора NMDA определялось по способу,описанному Jones S.M. и др., Pharmacol. Methods, 1989; 21:161. Для определения активности функционального антагониста АМПК исследу 000605 4 ют действие предлагаемых соединений на повреждение нейронов, вызываемое АМПК, в культурах первичных кортикальных нейронов по способам, похожим на описанные Коh J.-Y. и др., J. Neurosci, 1990; 10:693. Кроме того, повреждение нейронов, вызываемое долговременным воздействием 100 мкмоль АМПК, можно определять высвобождением цитозольного энзима, дегидрогеназы молочной кислоты. Активность соединений настоящего изобретения исследовались в вышеупомянутых опытах. Достигнутые результаты приведены в табл. 1. Сведенные в табл. 1 данные по КТ 50 представляют собой концентрацию (в мкмоль) испытуемого вещества, обеспечивающую 50%ное ингибирование активности рецепторов. 1 3 2 4 6 7 8 9 10 Кроме того, предварительным показателем имеющейся ин виво активности на центральную нервную систему по отношению к активности противосудорожного средства и потенциальной нейрозащите является опыт максимального электрошока на мышах штамма CF-1 (20-25 г) при использовании роговых электродов по стандартным способам, описанным недавноKrall и др., Epilepsia, 1988; 19:409-428. Соединения настоящего изобретения, как правило, проявляет выраженную как ЭД 50 активность, равную 50 мг/кг. Благодаря указанной биологической активности вторым объектом настоящего изобретения является фармацевтическая композиция,обладающая антагонистической в отношении рецептора глутамата и противосудорожной активностью, которая помимо фармацевтически приемлемого носителя содержит соединения вышеприведенной общей формулы (I) в терапевтически эффективном количестве. Предлагаемая фармацевтическая композиция может представлять собой любой стандартный лекарственный препарат. Так, например, в качестве твердых препаратов можно назвать таблетки, капсулы, в качестве жидких препаратов - растворы, суспензии, эмульсии, эликсиры или наполненные ими капсулы, причем все эти формы применяют орально; фармацевтическая композиция может иметься и в виде суппозиториев для ректального применения или в виде стерильных инъецируемых растворов для парентерального (в том числе, подкожного) применения. Третьим объектом настоящего изобретения является способ лечения заболеваний сосудов мозга или судорог путем введения соединений вышеприведенной общей формулы (I) в терапевтически эффективном количестве. Под терапевтически эффективным количеством понимаются суточные дозы, которые в зависимости от конкретного способа дачи, лекарственной формы, показания, пациента, веса тела пациента и предпочтения и опыта врача находятся в пределах от 0,1 до 1000 мг, предпочтительно от 10 до 50 мг и, в частности, 30100 мг. Нижеследующие примеры поясняют получение аминокислотных производных хиноксалин-2,3-диона вышеприведенной общей формулы (I) и являющегося дополнительным объектом настоящего изобретения промежуточного продукта для получения целевого продукта, у которого R означает остаток N-метиламиноуксусной кислоты, R1 - бром и R2 винил. Получение сложного этилового эфира [(2 амино-5-бром-3-нитро-6-винилбензил)-метиламино]-уксусной кислоты. В суспензию 2,86 г (10 ммоль) 5-бром-2 метил-7-нитро-1,2,3,4-тетрагидроизохинолин-8 иламина и 2,76 г (20 ммоль) карбоната калия в среде 50 мл ацетона дают 1,67 г (10 ммоль) этилбромацетата. Реакционную смесь смешивают с обратным холодильником до завершения, определяемого тонкослойной хроматографией на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении, равном 1:1. Летучие вещества испаряются под вакуумом и 150 мл воды прибавляют к желтому остатку. Продукт экстрагируют два раза, используя по 150 мл этилацетата, экстракты этилацетата промывают два раза, используя по 50 мл воды, и сушат над сульфатом магния. Продукт очищают хроматографией на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении, равном 95:5-75:25. Выход: 2,25 г, 60%, температура плавления: 6870 С; масс-спектроскопия (химическая ионизация): М+1=373. Определяют содержание С, Н и Получение сложного этилового эфира[(2,3-диамино-5-бром-6-винилбензил)-метиламино]-уксусной кислоты. Суспензию 0,5 г (1,34 ммоль) сложного этилового эфира [(2-амино-5-бром-3-нитро-6 винилбензил)-метиламино]-уксусной кислоты и 0,5 г никеля Ранея в среде 75 мл тетрагидрофурана подвергают гидрированию газообразным водородом при примерно 350 кПа в устройстве Парра. Реакционную смесь фильтруют, фильтрат испаряется с получением 0,45 г диамина,который используют дальше без дополнительной очистки. Н-ЯМР (CDCl3): 1,59 (т, 3 Н, J=7,2 Гц), 2,27 (с, 3 Н), 3,22 (с, 2 Н), 3,79 (с, 2 Н), 4,03[(2,3-диамино-5-бром-6-винилбензил)-метиламино]-уксусной кислоты и 0,327 г (2,6 ммоль) щавелевой кислоты в среде водной 2-н. соляной кислоты нагревают до 80 С. Через 4 ч реакционную смесь охлаждают и растирают в порошок с помощью шпателя с получением не совсем белого осадка, который фильтруют и сушат. Кристаллизуют из смеси воды и ацетона. Выход: 0,162 г, температура плавления 300 С. Масс-спектроскопия (химическая ионизация): М+1=368. Определяют содержание С, Н и N соединения С 14 Н 14 ВrN3 О 4 НСl: С, 41,56; Н, 3,74; Получение сложного этилового эфира [2,3 диамино-6-этилбензил)-метиламино]-уксусной кислоты. Раствор 0,5 г (1,34 ммоль) сложного этилового эфира [(2-амино-5-бром-3-нитро-6-винилбензил)-метиламино]-уксусной кислоты и 0,13 г(1,34 ммоль) ацетата калия в среде этанола подвергают гидрированию газообразным водородом при примерно 350 кПа на 0,1 г 20%-ного палладия на угле в устройстве Парра. Реакционную смесь фильтруют и фильтрат испаряется в ротационном испарителе с получением 0,42 г полутвердого вещества, которое используют дальше без дополнительной очистки. Н-ЯМР[2,3-диамино-6-этилбензил)-метиламино]-уксусной кислоты и 0,327 г (2,6 ммоль) дигидрата щавелевой кислоты в среде 20 мл водной 2-н. соляной кислоты нагревают до 90 С. Реакционную смесь смешивают в течение 16 ч и охлаждают. Желто-коричневый осадок выделяют,фильтруют, сушат на воздухе и используют дальше без дополнительной очистки. Выход: 0,368 г, 84%. Масс-спектроскопия (химическая ионизация): М+1=292. Получение аммониевой соли [(6-этил-7 нитро-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты. 0,368 г [(6-этил-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты растворяют в 5 мл концентрированной серной кислоты. Темный раствор охлаждают до 0 С и 0,5 г (5 ммоль) нитрата калия прибавляют при одновременном смешивании. Реакционную смесь дают нагреваться до комнатной температуры и охлаждают льдом через 12 ч. Светло-коричневый остаток фильтруют, и маточный раствор подщелачивают путем барботирования аммиака. Получают светло-зеленый осадок, который фильтруют и сушат на воздухе. Выход: 0,100 г, 25,4%, температура плавления 300 С. Масс-спектроскопия (химическая ионизация): М+1=337. Пример 3 Получение сложного этилового эфира[(2,3-диамино-5-бром-6-этилбензил)-метиламино]-уксусной кислоты. Раствор 0,475 г (1,27 ммоль) сложного метилового эфира [(2-амино-5-бром-3-нитро-6 винилбензил)-метиламино]-уксусной кислоты в среде 75 мл этанола подвергают гидрированию газообразным водородом при примерно 350 кПа в присутствии 0,2 г никеля Ранея. Растворитель испаряется с получением 0,450 г белого продукта, который используют дальше без дополнительной очистки.[(7-бром-6-этил-2,3-диоксо 1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты. В раствор 0,450 г сложного этилового эфира [(2,3-диамино-5-бром-6-этилбензил)-метиламино]-уксусной кислоты в среде 5 мл 5-н. соляной кислоты при смешивании дают 0,327 г(2,6 ммоль) дигидрата щавелевой кислоты. Реакционную смесь нагревают до 90 С в течение 16 ч, после чего дополнительно прибавляют 0,163 г (1,3 ммоль) дигидрата щавелевой кислоты. Через два часа смесь охлаждают и выделяют 0,037 г белового осадка с примесями. После 8 дальнейшего охлаждения получают не совсем белое твердое вещество, которое фильтруют,промывают водой и метанолом и сушат. Выход: 0,174 г, 34%, температура плавления 245248 С. Масс-спектроскопия (химическая ионизация): М-СO2 Н+1=326 (-СO2 Н). 1 Н-ЯМР Получение сложного этилового эфира [(6 этил-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин 5-илметил)-метиламино]-уксусной кислоты. Раствор 0,57 г (1,9 ммоль) сложного этилового эфира[(2,3-диамино-6-этилбензил)метиламино]-уксусной кислоты и 0,472 г (4 ммоль) диметилоксалата в среде 5 мл этанола нагревают с обратным холодильником в течение 16 ч. Растворитель частично испаряется, а реакционную смесь охлаждают. Получают 0,828 г желто-коричневого осадка. Продукт очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении,равном 95:5-75:25. Выход: 0,274 г, 45%. Массспектроскопия Получение сложного этилового эфира [(6 этил-7-нитро-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты. В раствор 0,175 г (0,57 ммоль) сложного этилового эфира [(6-этил-2,3-диоксо-1,2,3,4 тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты в среде 2 мл концентрированной серной кислоты, при смешивании и 0 С дают 0,071 г (0,71 ммоль) нитрата калия. Реакционную смесь смешивают в течение 16 ч и дают на лед. Коричневый осадок фильтруют,промывают водой и сушат. Продукт очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси трихлорметана и метанола в соотношении, равном 95:5-80:20. Выход: 0,135 г, 65%, температура плавления 110 С (вскипание), 185 С. Массспектроскопия Получение 2-бромметил-3-метил-6 нитрофениламина. В раствор 2,18 г (6,6 ммоль) тетрабромметана и 1,73 г (6,6 ммоль) трифенилфосфина в среде 100 мл безводного простого эфира, при смешивании в атмосфере азота подают 1,08 г(5,9 ммоль) (2-амино-6-метил-3-нитрофенил)метанола. Реакцию останавливают после регулирования тонкослойной хроматографией на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении, равном 1:1. Реакционную смесь фильтруют, и фильтрат испаряется. Темножелтый остаток хроматографируют на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношениях 9:1-8:2. Желтое твердое вещество, 0,620 г,43%, Н-ЯМР (CDCl3): 2,38 (с, 3 Н), 4,49 (с, 2 Н),6,45 (шир. с, 2 Н), 6,57 (д, 1 Н, 8,7 Гц), 8,03 (д,1 Н, 8,7 Гц). Получение сложного этилового эфира [(2 амино-6-метил-3-нитробензил)-метиламино]уксусной кислоты. В суспензию 0,765 г (5 ммоль) сложного этилового эфира саркозина в виде хлоргидрата в среде 10 мл смеси диметилформамида и тетрагидрофурана в соотношении, равном 1:1, при смешивании подают 1,01 г (10 ммоль) триэтиламина. Через 15 мин прибавляют 0,6 г (2,4 ммоль) 2-бромметил-3-метил-6-нитрофениламина. Реакционную смесь смешивают при комнатной температуре в течение 18 ч и подвергают испарению до сухости. Продукт экстрагируют с использованием 100 мл трихлорметана, промывают водой и сушат над сульфатом магния. Растворитель испаряется с получением 0,711 г масла, которое хроматографируют на силикагеле с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении,равном 95:5-80:20. Получают оранжево-желтое твердое вещество. Выход: 0,530 г, 77%. Массспектроскопия 10 Получение сложного этилового эфира [(6 метил-2,3-диоксо-1,2,3,4-тетрагидрохиноксалин-5-илметил)-метиламино]-уксусной кислоты. Раствор 0,49 г сложного этилового эфира[(2-амино-6-метил-3-нитробензил)-метиламино]-уксусной кислоты в среде 75 мл тетрагидрофурана подвергают гидрированию газообразным водородом при примерно 350 кПа на 0,2 г никеля Ранея в устройстве Парра. Реакционную смесь фильтруют, 0,500 г темного твердого вещества обрабатывают 0,295 г (2,5 ммоль) диметилоксалата в среде метанола. Реакционную смесь нагревают с обратным холодильником в течение 16 ч и подвергают испарению до сухости. Продукт экстрагируют в среде 100 мл трихлорметана, промывают водой и сушат над сульфатом магния. 0,689 г неочищенного продукта хроматографируют на силикагеле с применением в качестве элюента смеси трихлорметана и метанола в соотношении, равном 100:195:5, с получением желтого твердого вещества. Выход: 0,38 г, 62%. Масс-спектроскопия (химическая ионизация): М+1=306. Аналогично примерам 1-5 получают еще соединения формулы (I), сведенные в табл. 2. Таблица 2 где R5 -гидроксил, низший, алкоксил, амид,R6 -низший, алкил или аралкил,R1 - водород, бром, нитро,R2 - низший алкил, винил,при этом R2 может находиться в b-положении, а группа R-CH2 - в а-положении кольца,или их фармацевтически приемлемые соли. 2. Аминокислотные производные хиноксалин-2,3-диона общей формулы (I) по п.1, представляющие собой соединение из группы,включающей[(6-этил-7-нитро-2,3-диоксо-1,2,3,4 тетрагидрохиноксалин-5-илметил)-метиламино]-уксусную кислоту. 3. Фармацевтическая композиция, обладающая антагонистической в отношении рецептора глутамата и противосудорожной активностью, содержащая активное вещество и фармацевтически приемлемый носитель, отличающаяся тем, что в качестве активного вещества она содержит соединения по п.1 в терапевтически эффективном количестве. 4. Способ лечения заболеваний сосудов мозга или судорог путем введения активного вещества, отличающийся тем, что в качестве активного вещества используют соединения по п.1 в терапевтически эффективном количестве. 5. Сложный этиловый эфир [(2-амино-5 бром-3-нитро-6-винилбензил)-метиламино]уксусной кислоты, являющийся промежуточным продуктом для получения соединения формулы I по п.1, у которого R означает остаток Nметиламиноуксусной кислоты, R1 - бром и R2 винил.
МПК / Метки
МПК: C07D 241/44, C07C 229/18, C07F 9/6509
Метки: глутамата, хиноксалин-2,3-диона, способ, рецептора, продукт, антагонистической, лечения, промежуточный, судорог, аминокислотные, мозга, противосудорожной, отношении, композиция, заболеванийсосудов, производные, обладающая, фармацевстическая, активностью
Код ссылки
<a href="https://eas.patents.su/7-605-aminokislotnye-proizvodnye-hinoksalin-23-diona-farmacevsticheskaya-kompoziciya-obladayushhaya-antagonisticheskojj-v-otnoshenii-receptora-glutamata-i-protivosudorozhnojj-aktivnostyu.html" rel="bookmark" title="База патентов Евразийского Союза">Аминокислотные производные хиноксалин-2,3-диона, фармацевстическая композиция, обладающая антагонистической в отношении рецептора глутамата и противосудорожной активностью, способ лечения заболеванийсосудов мозга или судорог и промежуточный продукт</a>
Предыдущий патент: Огнеупорный блок.
Следующий патент: Производные винилсульфеновых кислот и способ их получения
Случайный патент: Композиционное уплотнение