Сульфонамиды для профилактики диабета
Номер патента: 21788
Опубликовано: 31.08.2015
Авторы: Пьемонти Лоренцо, Даффонкьо Луиза, Аллегретти Марчелло
Формула / Реферат
1. Применение соединения формулы (I) или его фармацевтически приемлемой соли
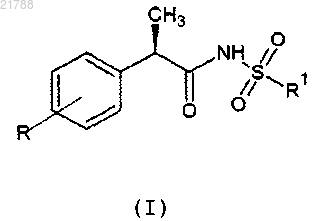
в которой R выбирают из линейного или разветвленного 4-(С1-С6)алкила, 4-трифторметансульфонилоксигруппы и 3-бензоила;
R1 представляет собой (С1-С6)алкил,
для получения лекарственного препарата для профилактики, замедления начала и прогрессирования диабета.
2. Применение по п.1, где диабет представляет собой диабет 1 типа.
3. Применение по любому из пп.1, 2, где соединение формулы (I) выбирают из R(-)-N-2-[(4-изобутилфенил)пропионил]метансульфонамида и R(-)-2-[(4'-трифторметансульфонилокси)фенил]пропионилметансульфонамида.
4. Применение по любому из пп.1-3, где соль выбирают из лизиновой и натриевой солей.
Текст
СУЛЬФОНАМИДЫ ДЛЯ ПРОФИЛАКТИКИ ДИАБЕТА Изобретение относится к профилактике диабета, в частности диабета 1 типа, а именно к применению сульфонамидов формулы (I) или их фармацевтически приемлемых солей: где R выбирают из линейного или разветвленного 4-(C1-C6)алкила, 4-трифторметансульфонилоксигруппы и 3-бензоила и R1 представляет собой (C1-C6)алкил, для получения лекарственного препарата. Полученный лекарственный препарат эффективен для профилактики,замедления начала и прогрессирования диабета. Область техники, к которой относится изобретение Настоящее изобретение относится к профилактике диабета. Уровень техники изобретения Диабет представляет собой заболевание, при котором организм не продуцирует достаточное количество инсулина или не способен реагировать на инсулин, гормон, который секретируется панкреатическими -клетками (клетками островка Лангерганса), который превращает глюкозу в энергию. Подробнее, диабет разделяют на диабет 1 типа, при котором клетки островка Лангерганса не продуцируют инсулин и который большей частью имеет аутоиммунную первопричину, и диабет 2 типа, патологическое состояние, обусловленное недостаточной чувствительностью клеток к инсулину, как правило, совмещенной с пониженной секрецией инсулина. Терапия диабета 1 типа заключается во введении искусственно полученного инсулина посредством подкожных инъекций, сопряженном с тщательным наблюдением за уровнем содержания глюкозы в крови. Терапия диабета 2 типа в его начальных стадиях заключается во введении пероральных лекарственных препаратов, которые нормализуют резистентность к инсулину, снижают выделение глюкозы печенью и стимулируют увеличение секреции инсулина, но на поздних стадиях требуется также введение инсулина. Учитывая то, что и диабет 1 типа и диабет 2 типа представляют собой по крайней мере отчасти наследуемые заболевания, пациенты, имеющие родственников, страдающих от этой патологии, имеют несомненный риск развития диабета. Кроме того, идентифицировали ряд прогностических маркеров, которые могут предсказать появление диабета, в частности диабета 1 типа (Curr. Diabetes Rev., 208, May 4(2), 110-121; Autoimmune Rev. 2006 Jul, 5(6), 424-428). Вследствие этого можно по низкой стоимости и с помощью простых методик идентифицировать людей с высоким риском развития заболевания. Осуществлен ряд попыток контроля и/или предотвращения развития диабета у людей с риском,предусматривающих, однако, необходимость использования методов лечения со слишком высоким соотношением стоимость/эффективность. Таким образом, в настоящее время, несмотря на то что имеются в наличии способы, с помощью которых можно предсказать это заболевание, не существует фармакологического лечения надлежащего уровня, которое способно предотвратить или, по крайней мере, замедлить его проявление. Наиболее подходящая стратегия, которую можно выбрать для применения к людям, подверженным риску заболеть, заключается в проведении периодического контроля гликемии и в здоровом образе жизни, включающем контроль массы тела, физические упражнения и надлежащий режим питания. Однако это имеет очень ограниченную эффективность. Таким образом, существует давно ощущаемая потребность в лекарственных препаратах для профилактики диабета. Патент EP 1123276 раскрывает N-(2-арилпропионил)сульфонамиды, в числе которых R(-)-2-[(4 изобутилфенил)пропионил]метансульфонамид (I), и их фармацевтически приемлемые соли для использования в качестве ингибиторов хемотаксической активности нейтрофилов и дегрануляции, вызванных интерлейкином IL-8, в частности для использования при лечении таких патологий, как псориаз, ревматоидный артрит, неспецифический язвенный колит, острая дыхательная недостаточность (ARDS), идиопатический фиброз и гломерулонефрит. ПатентR(-)-2-[(4-изобутилфенил)пропионил]метансульфонамида и его фармацевтически приемлемых солей, в частности его лизиновой соли, при проведении профилактики и лечения ишемии/реперфузионного повреждения трансплантированных органов и функционального повреждения, являющегося результатом реакций отторжения после трансплантации паренхиматозных органов, в частности почек, которые необходимо изымать у донора и сохранять перед трансплантацией. Такие повреждения, как полагают, ответственны за отсроченное отторжение трансплантата, что приводит к необходимости диализа в случае трансплантации почки. Патент EP 1579859 раскрывает применение N-(2-арилпропионил)сульфонамидов, в том числеR(-)-2-[(4-изобутилфенил)пропионил]метансульфонамида и его лизиновой соли, для получения лекарственных препаратов для лечения повреждения спинного мозга. Описание чертежей Фиг. 1 показывает процент мышей, выживших без диабета в течение периода времени (дни), в случае воздействия на мышей (ML)-стрептозотоцином ML)-streptozotocin (STZ со дня 0 в течение 5 дней,с последующим введением с первого дня носителя (плацебо) (Vehicle) (пунктирная линия) или Репариксина (Reparixin) (сплошная линия) в течение 7 дней. Фиг. 2 показывает уровни гликемии (мг/дл) в течение периода времени (дни) у мышей, которых подвергали воздействию (ML)-стрептозотоцином ML)-streptozotocin (STZ со дня 0 в течение 5 дней, с последующим введением с первого дня плацебо (Vehicle) (панель А) или Репариксина (Reparixin) (панель В) в течение 7 дней. Фиг. 3 показывает процент мышей, выживших без диабета в течение периода времени (дни), в случае воздействия на мышей (ML)-стрептозотоцином ML)-streptozotocin (STZ со дня 0 в течение 5 дней,-1 021788 с последующим введением с первого дня плацебо (Vehicle), Мераксина (Meraxin) (15 мг/кг) в течение 7 дней или Мераксина (Meraxin) (15 мг/кг) в течение 14 дней. Фиг. 4 показывает уровни гликемии (мг/дл) в течение периода времени (дни) у мышей, которых подвергали воздействию (ML)-стрептозотоцином ML)-streptozotocin (STZ со дня 0 в течение 5 дней, с последующим введением со дня +5 плацебо (Vehicle) (панель А) или Мераксина (Meraxin) (15 мг/кг) (панель В) в течение 14 дней. Подробное описание изобретения В настоящее время обнаружено, что соединения формулы (I) или их фармацевтически приемлемые соли в которой R выбирают из линейного или разветвленного 4-(C1-C6)алкила, 4-трифторметансульфонилоксигруппы и 3-бензоила;R1 представляет собой линейный или разветвленный (C1-C6)алкил,обладают способностью защищать панкреатические -клетки от механического/структурного и/или функционального повреждения и существенно замедлять начало проявления диабета, а также и снижать тяжесть заболевания, уже начавшегося. В особенности предпочтительные соединения в соответствии с изобретением представляют собойR(-)-2-[(4-изобутилфенил)пропионил]метансульфонамид (общеизвестный как Репертаксин (Repertaxin) или Репариксин (Reparixin), в дальнейшем в этом документе называемый как Репариксин) и R(-)-2-[(4'трифторметансульфонилокси)фенил]пропионилметансульфонамид (общеизвестный и в дальнейшем в этом документе называемый как Мераксин). Предпочтительные соли соединений изобретения представляют собой натриевую и лизиновую соль. В особенности предпочтительные соли соединений изобретения представляют собой лизиновую соль Репариксина и натриевую соль Мераксина. Как это будет описано далее в экспериментальной части, мышам вводили инъекцию STZ, соединения, способного вызвать патологическое состояние с клиническими и гистоиммунологическими характерными признаками диабета 1 типа человека, при этом развивалось заболевание более чем в два раза быстрее, чем в тех случаях, когда проводили лечение Репариксином или Мераксином, в сравнении с контрольными экспериментами. Что еще более важно, у мышей, которых лечили Репариксином или Мераксином, даже после проявления диабета уровни гликемии оставались существенно ниже, чем у контрольных мышей. Эти результаты явственно демонстрируют, что Репариксин и Мераксин способны защищать-клетки от нарушения функций. Таким образом, первая цель применения в данном случае представляет собой использование соединений формулы (I) или их фармацевтически приемлемых солей, предпочтительно лизиновой или натриевой солей, для получения лекарственного препарата для защиты панкреатических -клеток от механического/структурного и/или функционального повреждения. Предпочтительно, когда соединение формулы (I) представляет собой Репариксин или Мераксин. Следующая дополнительная цель изобретения представляет собой использование соединений формулы (I), предпочтительно Репариксина или Мераксина, для профилактики диабета, предпочтительно диабета 1 типа. Лекарственный препарат предпочтительно вводят пациентам, имеющим предрасположенность к диабету или имеющим начальное проявление самых первых симптомов диабета. А именно, это применение относится к использованию соединений изобретения, предпочтительно Репариксина или Мераксина, для производства лекарственного препарата для замедления начала и/или уменьшения прогрессирования диабета, предпочтительно диабета 1 типа. Соединения формулы (I) могут быть получены с помощью методик, хорошо известных в данной области техники. Например, Репариксин можно получить, как раскрыто в примере 1 патента EP 1123276 и в примере 1 патента EP 1355641, при этом лизиновую соль можно получить так, как раскрыто в примере 7 и примере 2 соответственно вышеуказанных патентов. Мераксин можно получить, например, в соответствии с примером 1 патента EP 1776336. Для целей настоящего изобретения вышеуказанные соединения вводят в состав фармацевтических композиций, подходящих для применения посредством перорального введения, такого как в форме таблеток, капсул, сиропов, предпочтительно в виде готовых лекарственных форм с контролируемым высвобождением, или для применения посредством парентерального введения в форме стерильных растворов,подходящих для внутривенного или внутримышечного введения. Фармацевтические композиции могут быть получены в соответствии со стандартными способами, например, как раскрыто в издании Remington, "The Science and Practice of Pharmacy", 21st ed. (Lippincott Williams and Wilkins). Предпочтительно,-2 021788 чтобы количество Репариксина или его фармацевтически приемлемой соли в каждой из вышеуказанных лекарственных форм для введения было бы таким, чтобы обеспечить от 2 до 15 мг соединения или соли на 1 кг массы тела, при этом количество Мераксина или его фармацевтически приемлемой соли было бы таким, чтобы обеспечить от 10 до 20 мг соединения или соли/на 1 кг массы тела. При любых обстоятельствах схема приема лекарства и количество вводимого лекарственного препарата будут определяться лечащим врачом в соответствии с потребностью пациента. Изобретение будет в дальнейшем проиллюстрировано подробнее в нижеприведенной экспериментальной части. Экспериментальная часть Результат действия Репариксина на индукцию диабета после воздействия многократных инъекций с небольшой дозой (MLD) - стрептозотоцина (STZ). Введение мышам восприимчивой породы многократных инъекций с небольшой дозой (STZ) вызывает патологическое состояние с клиническими и гистоиммунологическими характерными признаками,аналогичными человеческому сахарному диабету 1 типа (DM). Было установлено, что пять дневных доз,составляющих 40 мг/кг/день STZ, требуются для отсроченного начала продолжительной и прогрессирующей гипергликемии и инсулита у самцов мышей C57BL/6. Эта модель ранее использовалась для изучения роли провоспалительных цитокинов в развитии диабета 1 типа. 12 самцов мышей C57BL/6J подвергали воздействию MLD-STZ. STZ инъецировали интраперитонеально в дозе 40 мг/кг/день в течение 5 следующих друг за другом дней. Концентрации глюкозы в венозной крови измеряли каждый день, начиная с первого дня воздействия. Мыши с гликемией более чем 250 мг/дл по результатам трех последовательных тестов считались диабетическими, при этом первое определение гипергликемии принимали в расчет в качестве даты начала диабета. Мышей контролировали в течение 60 дней после воздействия первой инъекции STZ. Репариксин вводили подкожно непрерывной инфузией, начиная с 1 дня до дня 7 после первой инъекции STZ в дозе 8 мг/ч/кг. Введение Репариксина существенно влияло на распределение во времени развития диабета. Среднее значение времени без диабета составляло 2715 дней (n=8, p=0,026 в сравнении с контролем) и 70,5 дней (n=8) соответственно для мышей, подвергнутых Репариксин-введению и плацебо-введению(фиг. 1). Что еще более важно, даже после развития диабета в течение всего двухмесячного периода наблюдения уровни гликемии оставались постоянными и существенно более низкими в группе, подвергнутой Репариксин-введению по сравнению с группой, подвергнутой плацебо-введению (фиг. 2). Результат действия Мераксина на индукцию диабета после воздействия многократных инъекций с небольшой дозой (MLD) - стрептозотоцина (STZ). Самцов мышей C57BL/6J инъецировали интраперитонеально (ML) стрептозотоцином (STZ) в дозе 40 мг/кг/день в течение 5 следующих друг за другом дней. Концентрации глюкозы в венозной крови измеряли каждый день, начиная с первого дня воздействия (день 0). Мыши с гликемией более чем 250 мг/дл по результатам трех последовательных тестов считались диабетическими, при этом первое определение гипергликемии принимали в расчет в качестве даты начала диабета. Мышей контролировали в течение 60 дней после первой инъекции STZ. Мераксин вводили перорально в дозе 15 мг/кг в течение 7 или 14 дней, начиная с 1 дня от момента первой инъекции STZ. В обоих случаях лечение Мераксином способствовало продлению времени существования без диабета в сравнении с контрольным опытом. Среднее значение времени без диабета составляло 132,8 дней(p=0,67 в сравнении с контролем, n=8) и 2316 дней (p=0,016 в сравнении с контролем, n=8) соответственно для 7 и 14 дней лечения (фиг. 3). Во второй группе экспериментов лечение Мераксином в течение 14 дней начинали на +5 (n=4) день после первой инъекции STZ для иммитации клинических признаков начавшегося появления диабета. Как показано на фиг. 4, лечение Мераксином вплоть до дня 19 со всей очевидностью предотвращает появление диабета. Кроме того, уровни гликемии оставались постоянными и существенно более низкими в случае мышей, подвергнутых Мераксин-введению в сравнении с мышами, повергнутыми плацебо-введению на протяжении всего двухмесячного периода наблюдения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение соединения формулы (I) или его фармацевтически приемлемой соли в которой R выбирают из линейного или разветвленного 4-(С 1-С 6)алкила, 4-трифторметансульфонилоксигруппы и 3-бензоила;R1 представляет собой (С 1-С 6)алкил,для получения лекарственного препарата для профилактики, замедления начала и прогрессирования диабета. 2. Применение по п.1, где диабет представляет собой диабет 1 типа. 3. Применение по любому из пп.1, 2, где соединение формулы (I) выбирают изR(-)-N-2-[(4-изобутилфенил)пропионил]метансульфонамида и R(-)-2-[(4'-трифторметансульфонилокси)фенил]пропионилметансульфонамида. 4. Применение по любому из пп.1-3, где соль выбирают из лизиновой и натриевой солей.
МПК / Метки
МПК: A61K 31/185, A61P 3/10
Метки: диабета, профилактики, сульфонамиды
Код ссылки
<a href="https://eas.patents.su/7-21788-sulfonamidy-dlya-profilaktiki-diabeta.html" rel="bookmark" title="База патентов Евразийского Союза">Сульфонамиды для профилактики диабета</a>
Предыдущий патент: Панель с оптически прозрачной областью датчика
Следующий патент: Способ подъема баллера руля на судне
Случайный патент: Полиморфные формы стимулятора секреции гормона роста











