Замещенные 3-гидроксипиридины и содержащие их фармацевтические композиции
Номер патента: 17927
Опубликовано: 30.04.2013
Авторы: Помыткин Игорь Анатольевич, Бирюков Дмитрий Валерьевич
Формула / Реферат
1. Соединение общей формулы (I)
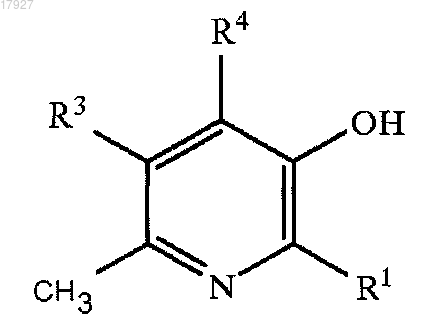
где R1 выбирают из группы, состоящей из алкилов, содержащих от 2 до 8 атомов углерода;
R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов углерода;
R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода,
или фармацевтически приемлемая соль такого соединения.
2. Соединение по п.1, отличающееся тем, что фармацевтически приемлемую соль выбирают из группы, состоящей из гидрохлорида, сукцината, фумарата, L-малата, кетоглутарата и цитрата.
3. Соединение по п.1, выбранное из группы, состоящей из соли, образованной 2-этил-4,6-диметил-3-гидроксипиридином и янтарной кислотой (1:1) и 2-этил-4,5,6-триметил-3-гидроксипиридом и янтарной кислотой (1:1).
4. Фармацевтическая композиция для лечения заболевания, связанного с нарушением действия инсулиновых рецепторов, содержащая соединение по п.1 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
5. Способ лечения заболевания, состояния или нарушения, связанного с нарушением действия инсулина, выбранного из группы, включающей сахарный диабет и его осложнения, диабет 2-го типа, резистентность к инсулину, гипергликемию, гиперинсулинемию, повышенное содержание жирных кислот или глицерина в крови, гиперлипидемию, ожирение, гипертриглицеридемию, дислипидемию, синдром X, синдром поликистозных яичников, или старение, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли.
Текст
ЗАМЕЩННЫЕ 3-ГИДРОКСИПИРИДИНЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ Настоящее изобретение относится к новым терапевтическим соединениям, отвечающим формуле в которой R1 выбирают из группы, состоящей из алкилов, содержащих от 2 до 8 атомов углерода,R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов углерода, R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода, или фармацевтически приемлемым солям таких соединений. Далее, объектами изобретения являются фармацевтические композиции, содержащие указанные соединения, и способы лечения заболеваний, связанных с нарушением действия инсулина, с использованием соединений формулы (I).(71)(73) Заявитель и патентовладелец: БИРЮКОВ ДМИТРИЙ ВАЛЕРЬЕВИЧ; ПОМЫТКИН ИГОРЬ АНАТОЛЬЕВИЧ; ПОВАЖНЫЙ ДМИТРИЙ БОРИСОВИЧ (RU) Область техники изобретения Настоящее изобретение относится к новым соединениям, имеющим лекарственные свойства, и их фармацевтически приемлемым солям; фармацевтическим композициям, содержащим эти соединения. Настоящее изобретение также относится к способу лечения, включающему назначение этих соединений для лечения заболеваний, связанных с нарушением действия инсулина. Предпосылки создания изобретения 3-Гидроксипиридины - класс имеющихся в продаже лекарственных препаратов. В патентах РФ 2168992, 2168993, 2185826 и 2190404 раскрыто использование 2-этил-6-метил-3-гидроксипиридина для лечения артрита, ишемии, метаболического синдрома и атеросклероза. Поскольку 2-этил-6-метил-3-гидроксипиридин является гидрофильным соединением, его способность к транспорту в нервные ткани и головной мозг ограничена. Таким образом, желательно разработать новые 3-гидроксипиридины с повышенной липофильностью. Цель настоящего изобретения заключается в том, чтобы обеспечить новые замещенные 3 гидроксипиридины или их фармацевтически приемлемые соли и содержащие их фармацевтические композиции. Подробное описание изобретения В настоящем изобретении представлено соединение, характеризующееся тем, что это соединение соответствует формуле (I)R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов углерода;R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода,или фармацевтически приемлемая соль такого соединения. Термин "фармацевтически приемлемая соль" относится к нетоксичным солям, образованным при присоединении основания. Фармацевтически приемлемые соли по данному изобретению получают посредством взаимодействия соединений, соответствующих формуле (I), с фармацевтически приемлемым основанием, используя методы, хорошо известные из уровня техники. Такие соли включают, в частности, гидрохлорид, гидробромид, сукцинат, фумарат, малат и ацетат. В предпочтительном варианте фармацевтически приемлемую соль по данному изобретению выбирают из группы, состоящей из гидрохлорида, сукцината, фумарата, L-малата, кетоглутарата и цитрата. Термин "алкил, содержащий от 2 до 8 атомов углерода", использованный в данном изобретении,означает радикал с прямой или разветвленной цепью, содержащий от 2 до 8 атомов углерода, за исключением тех случаев, когда длина цепи ограничена, как это указано здесь, включая, в частности, следующие радикалы: этил, н-пропил, изопропил, н-бутил, и трет-бутил, пентил, н-пентил, изопентил, неопентил, гексил и октил, а также простые алифатические изомеры этих соединений. Термин "алкил, содержащий от 1 до 8 атомов углерода", использованный в данном изобретении,означает радикал с прямой или разветвленной цепью, содержащий от 1 до 8 атомов углерода, за исключением тех случаев, когда длина цепи ограничена, как это указано здесь, включая, в частности, следующие радикалы: метил, этил, н-пропил, изопропил, н-бутил, и трет-бутил, пентил, н-пентил, изопентил,неопентил, гексил и октил, а также простые алифатические изомеры этих соединений. Предпочтительные соединения по данному изобретению включают 2-этил-4,6-диметил-3 гидроксипиридин, соль янтарной кислоты (1:1), и 2-этил-4,5,6-триметил-3-гидроксипиридин, соль янтарной кислоты (1:1). Далее, настоящее изобретение представляет собой фармацевтическую композицию для лечения заболевания, связанного с нарушением действия инсулиновых рецепторов, содержащую соединение, соответствующее формуле (I)R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов угле-1 017927R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода,или фармацевтически приемлемую соль такого соединения и фармацевтически приемлемый носитель. Термин "фармацевтически приемлемый носитель" относится к одному или нескольким совместимым твердым или жидким наполнителям-разбавителям или инкапсулирующим соединениям, которые пригодны для введения в любую часть тела млекопитающего, в предпочтительном варианте - человека. Для приготовления композиций по данному изобретению используют методы, хорошо известные из уровня техники, в соответствии с признанными фармацевтическими процедурами, например, описанными в Фармацевтическом научном справочнике Ремингтона, 17-е издание, под ред. Альфонсо Р. Дженнаро, Мак Паблишинг Компании, Истон, Пенсильвания, 18-е издание (Remington's Pharmaceutical Sciences,seventeenth edition, ed. Alfonso R. Gennaro, Mack Publishing Company, Easton, Pa., Eighteenth edition)(1990). Соединение, соответствующее формуле (I), или его фармацевтически приемлемая соль по данному изобретению, в форме свободного основания или солей, образованных при взаимодействии с фармацевтически приемлемыми кислотами, или их растворы, может быть введено в подходящие лекарственные формы, например композиции для орального, ректального, трансдермального, парентерального, назального или легочного введения, в соответствии с признанными фармацевтическими процедурами. Такие фармацевтические композиции по данному изобретению содержат соединения по данному изобретению в ассоциации с совместимыми фармацевтически приемлемыми материалами носителя или разбавителей,которые хорошо известны из уровня техники. Носители могут быть инертными материалами, органическими или неорганическими, пригодными для введения, и включают, например, воду, желатин, аравийскую камедь, лактозу, микрокристаллическую целлюлозу, крахмал, натрия крахмал гликолят, кальция гидрофосфат, магния стеарат, тальк, коллоидный диоксид кремния и подобные материалы. Такие композиции могут также содержать другие фармацевтически активные соединения и традиционные добавки,например стабилизаторы, смачивающие соединения, эмульгаторы, ароматизаторы, буферные компоненты, связующие соединения, дезагреганты, лубриканты, скользящие соединения, антиадгезивные соединения, пропелленты и подобные. Содержание соединения, соответствующего формуле (I), или его фармацевтически приемлемой соли составляет от 0,1 до 99%, в предпочтительном варианте от 0,5 до 10% от массы композиции. Композиции по данному изобретению могут быть использованы для приготовления разнообразных дозированных лекарственных форм. К таким формам относятся, в частности, растворы для инъекций,глазные капли, спрей, гель, мазь, таблетка, капсулы, лекарственные формы с замедленным высвобождением и порошок. Соединение, соответствующее формуле (I), или его фармацевтически приемлемая соль по данному изобретению могут быть введены в терапевтически эффективных количествах любым пригодным способом. Соединения по данному изобретению могут быть изготовлены в твердой или жидкой форме, например в форме таблеток, капсул, порошков, сиропов, эликсиров и т.п., аэрозолей, стерильных растворов, суспензий или эмульсий и т.п. Термин "терапевтически эффективное количество" относится к нетоксичному, но достаточному количеству активного соединения, для того чтобы обеспечить желаемый терапевтический эффект. В предпочтительном варианте терапевтически эффективное количество соединения, соответствующего формуле (I), в дозированной лекарственной форме, содержащей композиции, раскрытые в данном изобретении,составляет от 1 до 500 мг, в более предпочтительном варианте от 50 до 150 мг. Дозировка определенного соединения по данному изобретению будет варьировать в зависимости от его активности, способа введения, возраста и массы тела больного и тяжести состояния, по поводу которого проводится лечение. Например, лекарственный препарат может быть введен внутрь один или два раза в сутки, либо реже, либо периодически. Соединения и композиции по данному изобретению могут быть использованы в способе лечения заболевания, состояния или нарушения, связанного с нарушением действия инсулина, выбранного из группы, включающей сахарный диабет и его осложнения, диабет 2-го типа, резистентность к инсулину,гипергликемию, гиперинсулинемию, повышенное содержание жирных кислот или глицерина в крови,гиперлипидемию, ожирение, гипертриглицеридемию, дислипидемию, синдром X, синдром поликистозных яичников, или старение, включающем введение млекопитающему, нуждающемуся в таком лечении,терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. В данном документе термин "лечение заболевания" означает лечение, контроль, предотвращение и/или уменьшение проявления одного или нескольких клинических признаков (симптомов) заболевания у нуждающегося в таком лечении млекопитающего. Неисключительные примеры млекопитающих в контексте данного изобретения включают людей и домашних животных, например собак и кошек. В предпочтительном варианте млекопитающим является человек. Соединения настоящего изобретения могут быть приготовлены путем взаимодействия соединения,-2 017927R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов углерода;R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода. Исходные соединения, соответствующие формуле (II), могут быть приготовлены способами, хорошо известными из уровня техники. Например, соединения, соответствующие формуле (II), могут быть получены посредством взаимодействия между хорошо известными из уровня техники алкилзамещенными фуранами с ангидридами карбоновой кислоты в присутствии катализатора, предпочтительно фосфорной кислоты. Реакция, посредством которой получают 3-гидроксипиридины из 2-ацилфуранов, хорошо известна из литературы (P. Bosshard, C.H. Eugster, Adv. Heterocycl. Chem. 7, 377, 1966). В предпочтительном варианте осуществления изобретения эту реакцию осуществляют в абсолютном этаноле, который используют в качестве растворителя газообразного аммиака. В предпочтительном варианте реакцию осуществляют в автоклаве при высокой температуре, однако эта реакция может быть проведена и в других условиях. Готовую фармацевтически приемлемую соль получают посредством взаимодействия между образовавшимся 3-гидроксипиридином и кислотой в безводной среде. Ниже представлены примеры для демонстрации изобретения. Примеры имеют иллюстративное значение и не предназначены для ограничения объема изобретения тем или иным образом. Пример 1. 2-Этил-4,5,6-триметил-3-гидроксипиридин, соль янтарной кислоты (1:1).(1) 2-Пропионил-3,4,5-триметилфуран. 85%-ную фосфорную кислоту (0,05 моль) медленно, по каплям, добавляют к смеси 2,3,4 диметилфурана (0,3 моль, номер по реестру CAS [10599-57-2]) и пропионового ангидрида (78,1 г,0,6 моль), нагретой до 40C. Реакционную смесь прогревают при 60C в течение 2 ч. Оставляют до охлаждения до комнатной температуры, затем добавляют при перемешивании 120 мл воды и продолжают перемешивание в течение 1 ч. Органическую фазу отделяют и обрабатывают насыщенным раствором натрия карбоната, перемешивают в течение 24 ч, чтобы разрушить непрореагировавшие ангидрид и кислоты. После этого раствор экстрагируют хлороформом (300 мл 3), затем объединенные органические фазы сушат в присутствии Na2SO4 и выпаривают, чтобы получить маслянистый осадок, который отгоняют под вакуумом, получая фракцию, кипящую при температуре 86-89C (0,6 мм). Получен чистый кетон(2) 2-Этил-4,5,6-триметил-3-гидроксипиридин. Насыщенный раствор аммиака в абсолютном этаноле (50 мл), полученный при -20C, помещают в автоклав, затем добавляют к нему кетон (0,36 моль), приготовленный, как описано выше. Реакционную смесь прогревают при 170C в течение 15 ч при перемешивании. После охлаждения этанол выпаривают в условиях сниженного давления, чтобы получить маслянистый осадок, который собирают 2N раствором гидроксида натрия (400 мл). После перемешивания и тщательного растирания щелочной раствор экстрагируют хлороформом (100 мл 4), чтобы извлечь непрореагировавший кетон. Щелочные жидкости нейтрализуют концентрированной соляной кислотой, чтобы отделить 2-этил-4,5,6-триметил-3 гидроксипиридин. Жидкости экстрагируют хлороформом (200 мл 8), органические экстракты промывают водой, сушат в присутствии Na2SO4, фильтруют и выпаривают, чтобы получить дополнительное количество продукта. Две твердые фракции объединяют и повторно обрабатывают безводным эфиром(250 мл 6), чтобы отделить присутствующий хлорид. Из раствора эфира во время концентрации прогрессивно кристаллизуется 2-этил-4,5,6-триметил-3-гидроксипиридин (27 г, 61%); Rf=0,39 (AcOEt).(3) 2-Этил-4,5,6-триметил-3-гидроксипиридин, соль янтарной кислоты (1:1). Насыщенный раствор янтарной кислоты (0,1 моль) в безводном этаноле добавляют к раствору 2 этил-4,5,6-триметил-3-гидроксипиридина (0,1 моль) в безводном этаноле. Этанол выпаривают и продукт перекристаллизовывают из изопропанола-ацетона до получения чистого соединения. Элементарный анализ C14H21NO5 (283,3): расчетный состав, %, C 59,35, H 7,47, N 4,94; обнаруженный состав, % C 59,42, H 7,52, N 4,89. Ожидаемая структура подтверждена данными 1 Н-ЯМР-анализа. Пример 2. 2-Этил-4,6-диметил-3-гидроксипиридин, соль янтарной кислоты (1:1).(1) 2-Пропионил-3,5-диметилфуран. 85%-ную фосфорную кислоту (0,05 моль) медленно, по каплям, добавляют к смеси 2,4 диметилфурана (0,3 моль, номер по реестру CAS [3710-43-8]) и пропионового ангидрида (78,1 г, 0,6 моль), нагретой до 40 С. Реакционную смесь прогревают при 60C в течение 2 ч. Оставляют до охлаждения до комнатной температуры, затем добавляют при перемешивании 120 мл воды и продолжают перемешивание в течение 1 ч. Органическую фазу отделяют и обрабатывают насыщенным раствором натрия карбоната, перемешивают в течение 24 ч, чтобы разрушить непрореагировавшие ангидрид и кислоты. После этого раствор экстрагируют хлороформом (300 мл 3), затем объединенные органические фазы сушат в присутствии Na2SO4 и выпаривают, чтобы получить маслянистый осадок, который отгоняют под вакуумом, получая фракцию, кипящую при температуре 71-75C (0,6 мм). Получен чистый кетон (19,6 г,41%).(2) 2-Этил-4,6-диметил-3-гидроксипиридин. Насыщенный раствор аммиака в абсолютном этаноле (50 мл), полученный при -15C, помещают в автоклав, затем добавляют к нему кетон (0,36 моль), приготовленный, как описано выше. Реакционную смесь прогревают при 170C в течение 15 ч при перемешивании. После охлаждения этанол выпаривают в условиях сниженного давления, чтобы получить маслянистый осадок, который собирают 2N раствором гидроксида натрия (400 мл). После перемешивания и тщательного растирания щелочной раствор экстрагируют хлороформом (100 мл 4), чтобы извлечь непрореагировавший кетон. Щелочные жидкости нейтрализуют концентрированной соляной кислотой, чтобы отделить 2-этил-4,6-диметил-3 гидроксипиридин. Жидкости экстрагируют хлороформом (200 мл 8), органические экстракты промывают водой, сушат в присутствии Na2SO4, фильтруют и выпаривают, чтобы получить дополнительное количество продукта. Две твердые фракции объединяют и повторно обрабатывают безводным эфиром(250 мл 6), чтобы отделить присутствующий хлорид. Из раствора эфира во время концентрации прогрессивно кристаллизуется 2-этил-4,6-диметил-3-гидроксипиридин (29 г, 67%); Rf=0,37 (AcOEt).(3) 2-Этил-4,6-диметил-3-гидроксипиридин, соль янтарной кислоты (1:1). Насыщенный раствор янтарной кислоты (0,1 моль) в безводном этаноле добавляют к раствору 2 этил-4,6-диметил-3-гидроксипиридина (0,1 моль) в безводном этаноле. Этанол выпаривают и продукт перекристаллизовывают из изопропанола-ацетона до получения чистого соединения. Элементарный анализ C13H19NO5 (269,3): расчетный состав, %, С 57,98, Н 7,11, N 5,20; обнаруженный состав, % С 57,92, H 7,19, N 5,12. Ожидаемая структура подтверждена данными 1 Н-ЯМР-анализа. Пример 3. Данный пример демонстрирует лекарственную форму для инъекций, содержащую соединение, соответствующее формуле (I). Соединение, соответствующее формуле (I), растворяют в воде для инъекций до желаемого объема,добавляют 0,4 М раствор динатриевой соли фосфорной кислоты до pH 5,0. Приготовлен 5%-ный раствор соединения, соответствующего формуле (I). Раствор фильтруют через фильтр для стерилизации (с размером пор 0,2 мкм) и разливают по ампулам. Пример 4. Данный пример демонстрирует лекарственную форму для инъекций, содержащую 2-этил-4,6 диметил-3-гидроксипиридин, соль янтарной кислоты (1:1). 2-Этил-4,6-диметил-3-гидроксипиридин, соль янтарной кислоты (1:1), растворяют в воде для инъ-4 017927 екций до желаемого объема, добавляют 0,4 М раствор динатриевой соли фосфорной кислоты до рН 5,5. Приготовлен 5%-ный раствор 2-этил-4,6-диметил-3-гидроксипиридина, соли янтарной кислоты (1:1). Раствор фильтруют через фильтр для стерилизации (с размером пор 0,2 мкм) и разливают по ампулам. Пример 5. Данный пример демонстрирует лекарственную форму для инъекций, содержащую 2-этил-4,5,6 триметил-3-гидроксипиридин, соль янтарной кислоты (1:1). 2-Этил-4,5,6-триметил-3-гидроксипиридин, соль янтарной кислоты (1:1), растворяют в воде для инъекций до желаемого объема, добавляют 0,4 М раствор динатриевой соли фосфорной кислоты до рН 5,5. Приготовлен 5%-ный раствор 2-этил-4,5,6-триметил-3-гидроксипиридина, соли янтарной кислоты(1:1). Раствор фильтруют через фильтр для стерилизации (с размером пор 0,2 мкм) и разливают по ампулам. Пример 6. Данный пример демонстрирует эффективность соединений по данному изобретению при применении их для усиления активации инсулинового рецептора. Клетки человеческой гепатомы HepG2 в течение 10 мин обрабатывали 5 пМ инсулина; 50 мкМ 2 этил-4,5,6-триметил-3-гидроксипиридина, соли янтарной кислоты (1:1); 50 мкМ 2-этил-4,6-диметил-3 гидроксипиридина, соли янтарной кислоты (1:1); или их комбинацией в забуференном фосфатом растворе, содержащем 5 мМ глюкозы. Активацию инсулинового рецептора в клетках оценивали посредством фосфорилирования остатков тирозина 1162/1163 в области киназного домена рецептора, используя инсулиновый рецептор PhosphoDetect (pTyrl 162/1163), набора для твердофазного иммуноферментного анализа ELISA (Calbiochem). Общепризнано, что фосфорилирование усиливает активность рецептора приблизительно 200-кратно, по сравнению с активностью нефосфорилированного рецептора. Эти результаты, выраженные в процентах от ответа на воздействие 100 пМ инсулина, представлены в табл. 1 (среднееCOC (n=8. Таблица 1 Достоверно отличается от контроля (P0,05). Достоверно отличается от инсулина 5 нМ (P0,05). Данные, представленные в табл. 1, демонстрируют, что соединения по данному изобретению значимо усиливают активацию инсулинового рецептора. Пример 7. Данный пример демонстрирует эффективность соединений по данному изобретению при применении их для лечения резистентности к инсулину, дислипидемии и сахарного диабета. В хвостовую вену самцов-альбиносов крысы Вистар вводили инъекцию растворенного в цитратном буферном растворе (0,05 М, рН 5,5) стрептозотоцина (Sigma, Сент-Луси, штат Миссури, США) в дозе 35 мг/кг массы тела животного, чтобы вызвать декомпенсированную резистентность к инсулину. При проведении эксперимента через 1 неделю после инъекции стрептозотоцина использовали крыс с концентрацией глюкозы выше 14,0 ммоль/л. Для определения концентрации глюкозы в сыворотке натощак использовали глюкозооксидазный метод; концентрации инсулина в плазме определяли с помощью набора для сэндвич-радиоиммуноанализа; содержание триглицеридов в плазме определяли ферментативными методами. Крыс, индуцированных стрептозотоцином, распределяли по 3 группам: контрольная группа (n=10) и 2 экспериментальные группы (n=20). Контрольным крысам ежедневно в течение 7 дней вводили внутрибрюшинные инъекции солевого раствора. Экспериментальным крысам ежедневно в течение 7 дней вводили внутрибрюшинные инъекции 2-этил-4,6-диметил-3-гидроксипиридина, соли янтарной кислоты(1:1) в дозе 10 мг/кг, или 2-этил-4,5,6-триметил-3-гидроксипиридина, соли янтарной кислоты (1:1). Биохимические параметры определяли перед началом лечения и на 14-й день после начала лечения. Результаты представлены в табл. 2, среднееСОС (n=10). Таблица 2 Достоверно отличается от контроля (Р 0,05). Данные, представленные в табл. 2, демонстрируют, что соединения по данному изобретению полезны при применении для лечения сахарного диабета, резистентности к инсулину и гиперлипидемии. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I)R3 независимо выбирают из группы, состоящей из H и алкилов, содержащих от 1 до 8 атомов углерода;R4 независимо выбирают из группы, состоящей из алкилов, содержащих от 1 до 8 атомов углерода,или фармацевтически приемлемая соль такого соединения. 2. Соединение по п.1, отличающееся тем, что фармацевтически приемлемую соль выбирают из группы, состоящей из гидрохлорида, сукцината, фумарата, L-малата, кетоглутарата и цитрата. 3. Соединение по п.1, выбранное из группы, состоящей из соли, образованной 2-этил-4,6-диметил 3-гидроксипиридином и янтарной кислотой (1:1) и 2-этил-4,5,6-триметил-3-гидроксипиридом и янтарной кислотой (1:1). 4. Фармацевтическая композиция для лечения заболевания, связанного с нарушением действия инсулиновых рецепторов, содержащая соединение по п.1 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. 5. Способ лечения заболевания, состояния или нарушения, связанного с нарушением действия инсулина, выбранного из группы, включающей сахарный диабет и его осложнения, диабет 2-го типа, резистентность к инсулину, гипергликемию, гиперинсулинемию, повышенное содержание жирных кислот или глицерина в крови, гиперлипидемию, ожирение, гипертриглицеридемию, дислипидемию, синдромX, синдром поликистозных яичников, или старение, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2
МПК / Метки
МПК: A61K 31/44, C07D 213/65, A61P 3/00
Метки: фармацевтические, композиции, замещенные, содержащие, 3-гидроксипиридины
Код ссылки
<a href="https://eas.patents.su/7-17927-zameshhennye-3-gidroksipiridiny-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные 3-гидроксипиридины и содержащие их фармацевтические композиции</a>
Предыдущий патент: Устройство температурной защиты погружного электродвигателя
Следующий патент: Способ получения дарифенацина гидробромида
Случайный патент: Бифенилсульфонамидные ингибиторы матричных металлопротеиназ.











