Cпособ получения n-замещенных пиразолов
Формула / Реферат
1. Способ получения N-замещенных пиразолов общей формулы I
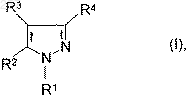
в которой
R1 означает алкил с 1-12 атомами углерода или фенилалкил с 7-20 атомами углерода и
R2, R3, R4 независимо друг от друга означают водород, алкил с 1 -12 атомами углерода, фенилалкил с 7-20 атомами углерода или замещенные, или незамещенные арильные остатки,
путем взаимодействия пиразолов общей формулы II

в которой R2, R3, R4 имеют вышеуказанные значения, со спиртом общей формулы III
R1-O-H (III)
в которой R1 имеет вышеуказанное значение, при повышенной температуре в присутствии катализатора, отличающийся тем, что взаимодействие пиразола II со спиртом III проводят при их молярном соотношении от 0,001:1 до 1:1 в жидкой фазе при температуре 50-400ш С и давлении 0,8-250 бар, а в качестве катализатора используют кислоты и/или их алкиловые эфиры, или их ангидриды при молярном соотношении их к пиразолу II от 0,0001:1 до 0,5:1.
2. Способ по п.1, отличающийся тем, что в качестве катализатора используют
серную кислоту, алкилсульфаты, диалкилсульфаты, фосфорную кислоту,
алкиловые эфиры фосфорной кислоты, алкилсульфокислоты или их алкиловые
эфиры, а также ангидриды указанных кислот, например, трехокись серы
или пятиокись фосфора.
3. Способ по п.1, отличающийся тем, что пиразол II и спирт III используют в молярном соотношении от 0,002:1 до 1:1.
4. Способ по п.1, отличающийся тем, что пиразол II и спирт III используют в молярном соотношении от 0,003:1 до 1:1.
5. Способ по п.1, отличающийся тем, что катализатор и пиразол II используют в молярном соотношении от 0,0005:1 до 0,5:1.
6. Способ по п.1, отличающийся тем, что катализатор и пиразол II используют в молярном соотношении от 0,01:1 до 0,2:1.
7. Способ по п.1, отличающийся тем, что взаимодействие проводят при давлении от 0,8 до 100 бар.
8. Способ по п.1, отличающийся тем, что взаимодействие проводят при давлении от 0,9 до 100 бар.
9. Способ по п.1, отличающийся тем, что взаимодействие проводят при температуре от 100 до 350 шС.
Текст
Настоящее изобретение относится к производству Ы-замещенных пиразолов, более конкретно к новому способу получения Мзамещенных пиразолов.Известен способ Ы-алкилирования 3,5 дифенилпиразолов путем обработки Мнезамещенных 3,5-дифенилпиразолов смесью диметилсульфата и водной натриевой щелочи в присутствии катализатора переноса фаз (см. заявку ВЕ Мг 35 06 972, кл. С 07 В 231/12, 1986).Недостатком известного способа является ИСПОЛЬЗОВЗНИС ОЧСНЬ ЯДОВИТЫХ И ОТНОСИТСЛЬНО дорогих диалкилсульфатов, так как большая часть их молекулы не используется, а также большое количество образующейся соли.Кроме того, из С 11 еш 1 са 1 Ьепегз, стр.575578 (1992) известен способ М-алкилирования пиразолов, по которому Ы-незамещенные пиразолы подвергают взаимодействию со спиртами в ПрИСуТСТВИИ КЗТЗЛИТИЧССКИХ КОЛИЧССТВ КОМплексов рутения, родия или иридия с триалкилфосфитом. Недостатком этого способа является высокая стоимость катализатора.Наиболее близким изобретению является способ получения Ы-замещенных пиразолов общей формулы А1 в]. где 121 означает алкил с 1-12 атомами углерода или фенилалкил с 7-20 атомами углерода и 122,123, 124 независимо друг от друга означают водород, алкил с 1-12 атомами углерода, фенил, фенилалкил с 7-20 атомами углерода или алкилфенил с 7-20 атомами углерода, путем взаимодействия пиразолов общей формулы Б вв которой 122, 123 и 124 имеют вышеуказанные значения, со спиртом общей формулы В кдо-к 5 (В)где 121 имеет вышеуказанное значение, а 125 означает водород или имеет значение радикала 121,при температуре 200-550 С и давлении 0,001-50 бар в газовой фазе в присутствии гетерогенного катализатора (см. заявку ЕР Не 0628 563 А], кл. С 07 В 521/00, С 07 В 231/12, 1994).Недостатком способа по ближайшему аналогу является осуществление процесса в газовой фазе на гетерогенном катализаторе, что отрицательно сказывается на экономичности процесса.Задачей изобретения является разработка более экономичного способа получения Мзамещенных пиразолов.Поставленная задача решается предлагаемым способом получения Ы-замещенных пиразолов общей формулы 1в которой 121 означает алкил с 1-12 атомами углерода или фенилалкил с 7-20 атомами углерода и 122, 123, 124 независимо друг от друга означают водород, алкил с 1-12 атомами углерода, фенилалкил с 7-20 атомами углерода или замещенные или незамещенные арильные остатки, путем взаимодействия пиразолов общей формулы 11в которой 122, 123, 124 имеют вышеуказанные значения, со спиртом общей формулы 111 к 1 он (111)в которой 121 имеет вышеуказанное значение,при повышенной температуре в присутствии катализатора за счет того, что взаимодействие пиразола 11 со спиртом 111 проводят при их молярном соотношении от 0,001:1 до 1:1 в Жидкой фазе при температуре 50-400 С и давлении 0,8250 бар, а в качестве катализатора используют Кислоты, и/или их алКиловЬ 1 е эфиры, или их ангидриды при молярном соотношении их к гшразолу П от 0,0001:1 до 0,521.В качестве катализатора предпочтительно используют серную кислоту, алкилсульфаты,диалкилсульфаты, фосфорную кислоту, алкгшовые эфиры фосфорной кислоты, алкилсульфоКислоты или их алКиловЬ 1 е эфиры, а также ангидриды названных кислот, например трехокись серы или пятиокись фосфора.Пиразол общей формулы 11 и спирт общей формулы 111 предпочтительно используют в молярном соотношении от 0,002:1 до 1:1, в частности в молярном соотношении от 0,003:1 до 1:1.Катализатор и пиразол общей формулы П предпочтительно используют в молярном соотношении от 0,0005:1 до 0,05:1, в частности в молярном соотношении от 0,01 :1 до 0,221.Реакцию предпочтительно проводят при температуре от 100 до 350 С и при давлении от 0,8 до 100 бар, в частности 0,9-100 бар.Пиразол общей формулы 11 и катализатор могут быть растворены или суспендированы в инертном растворителе, например в техническом белом минеральном масле или в вакуумном газовом масле.В качестве исходного соединения 11 пригодны пиразолы, например пиразол и замещенные пиразолы, например З-метилпиразол, 4 пиразол, 3,4-диметилпиразол, 3,5-диметилпиразол, 3,4,5-триметилпиразол, 3-этилпиразол,4-этилпиразол, З-арилпиразолы, например 3 фенилпиразол, 3,5-диарилпиразолы, например 3,5-дифенилпиразол, 3,4-диарилпиразолы, например 3,4-дифенилпиразол, 3,4,5-триарилпиразолы, например 3,4,5-трифеьшлпиразол.В качестве исходных соединений 111 пригодны спирты, например метанол, этанол, нпропанол, изопропанол, н-бутанол, трет. бутанол и н-октанол и т.д.Получаемые способом по изобретению Мзамещнные пиразолы 1 являются ценными исХОДНЫМИ СОСДИНСНИЯМИ ДЛЯ ПОЛУЧСНИЯ Красителей, фармацевтических препаратов и средств защиты растений.124, 122, 123, 124 независимо друг от друга означают алкил с 1-12 атомами углерода, предпочтительно алкил с 1-8 атомами углерода, такой как метил, этил, н-пропил, изопропил, нбутил, изобутил, втор.бутил, трет.бутил, нпентил, изопентил, втор.пентил, неопентил, 1,2 диметилпропил, н-гексил, изогексил,втор.гексил, н-гептил, изогептил, н-октил, изооктил, особенно предпочтительно алкил с 1-4 атомами углерода, такой как метил, этил, нпропил, изопропил, н-бутил, изобутил,втор.бутил и трет. бутил, а также фенилалкил с 7-20 атомами углерода, предпочтительно фенилалкил с 7-12 атомами углерода, например бензил, 1-фенетил, 2-фенетил, 1-фенил-пропил, 2 фенил-пропил, 3-фенил-пропил, 1-фенил-бутил,2-фе 1-Шл-бутил, 3-фенил-бутил и 4-фенил-бутил,особенно предпочтительно бензил, 1-фенетил и 2-фенетил, 122, 123, 124 независимо друг от друга означают водород, арил, предпочтительно фенил,замещнные арильные остатки, например алкилфенил с 7-20 атомами углерода, предпочтительно алкилфенил с 7-12 атомами углерода, например 2-метилфенил, 3-метилфенил, 4 Метилфенил, 2,4-димегилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 3,4-диметилфенил,3,5-диметилфенил, АЗА-триметилфенил, 2,3,5 триметилфенил, 2,3,6-триметилфенилметил,2,4,6-триметилфенил, 2-этилфенил, 3 этилфенил, 4-этилфенил, 2-н-пропилфенил, 3-нпропилфенил и 4-н-пропилфенил.Пример 1. В перегонную колонну помещают 50 г (0,227 3 Моля) 3,5-дифенилпиразола и 5 г (0,0437 моля) фосфорной кислоты (85%-ная) при 250 С, пропускают в течение 4 ч вместе с 158,2 г (4,94 моля) метанола и конденсируют газообразный продукт реакции. Затем ещ дваЖДЬ 1 заполняют по 50 г (0,2273 моля) 3,5 дифенилпиразола и, как прежде, подвергают его взаимодействию с метанолом, соответственнопо 158,2 г (4,94 моля), и конденсируют. Затем заполняют 31,5 г (0,143 Моля) 3,5-дифенилпиразола, снова пропускают 158,2 г (4,94 моля) метанола и конденсируют. Далее, не добавляя 3,5-дифенилпиразол, пропускают 158,2 г (4,94 моля) метанола. Каждую из этих пяти смесей собирают отдельно, подвергают газовой хроматографии и сгущают в вакууме.Молярное соотношение Продукт Смесь,1-метил-3,5-дифенилпира- реакции, г Не зол/3,5-дифенилпиразол 1 9426 29,4 2 96,9:3,1 46,4 3 97,8 : 2,2 47,1 4 94,7 : 5,3 35,3 5 100:0 23,7Всего используют 181,5 г (0,825 моля) 3,5 дифенилпиразола и 791 г (24,7 моля) метанола. Получают всего 175,8 г (91%) 1-метил-3,5 дифенилпиразола. Остаток в перегонной колонНС не УЧИТЫВЗСТСЯ.Пример 2. В электрически обогреваемой колонне диаметром 4 см с фриттой на нижнем конце, насаженной на двухгорловую колбу мкостью 250 мл, в течение 6 ч по каплям вьшаривают 308,5 г (9,64 моля) метанола при температуре 155 С и пропускают через горячий расплав(200 С) 10 г (0,0455 моля) 3,5-дифенилпиразола и 0,046 г (0,000455 моля) концентрированной серной кислоты. Газообразный продукт реакции конденсируют и сгущают в вакууме. Получают 10,2 г (92,5%) 1-метил-3,5-дифенилпиразола. Т. куш. 3 мбар/190 С, чистота 96,6% (ГХ).(13,6 молей) метанола при 155 С и пропускают через расплав с температурой 200 С. Получают 10,4 г (96%) 1-метил-3,5-дифенилпиразола. Т. куш. 3 мбар/190 С, чистота 99,2% (ГХ).(0,0122 моля) серной кислоты и 20 г стеклянных колец Ращига диаметром 3 мм до 145 С и подвергают взаимодействию в течение 5 ч с 118,65 г (3,7 моля) выпаренного при 170 С метанола. После сгущения при нормальном давлении получают 11,2 г (94,4%) 1,4-диметилпиразола. Т. куш. 151 С, чистота 98,6% (ГХ).Пример 12. Аналогично примеру 2 колонну заполняют 30 г стеклянных колец диаметром 3 мм, 16,4 г (0,24 моля) пиразола и 1,02 г (0,01 моля) 96%-ной по весу серной кислоты, нагревают до 195 С и подвергают взаимодействию в течение 7 ч с 703 г (9,5 молей) выпаренного при 180 С трет.-бутанола. Получают 21,7 г Ы-трет: бутилпиразола. Т. кип. 103 С, чистота 99,4%(ГХ), что соответствует выходу 72,5%.Пример 13. 20,5 г (0,25 моля) 4 метилпиразола, 82 г (О,65 моля) н-октанола и 1,28 г (0,0125 моля) 96%-ной по весу серной кислоты перемешивают 33 ч при 175 С. Реакци 000257оштую смесь после охлаждения трижды экстрагируют по 15 мл 5%-ной серной кислоты.Объединнные сернокислотные экстракты нейтрализуют 25%-ной натриевой щлочью. Последующая перегонка дат 13,5 г, по данным газохроматографического анализа 99,3% непревращнного 4-метилпиразола.Из органической фазы получают 17,4 г 4 метил-Ы-октилпиразола с т. куш. 75 С/7 мбар,чистотой 95% (ГХ) при степени превращения 34,6% и селективности 98,5%.Пример 14. Перемешивают в автоклаве 6,8 г (0,1 моль) пиразола, 23,7 г (0,32 моля) трет.бутанола и 0,51 г (0,О 05 моля) 96%-ной по весу серной кислоты в течение 3 ч при 200 С и 35 бар. После охлаждения, снятия давления (вЬ 1 пуск изобутилена) и разделения фаз получают из водной фазы 6,5 г 10,2%-ного по весу (по данным ГХ-анализа) водного раствора пиразола,перегонка которого дат 0,66 г пиразола. Из органической фазы получают 10,5 г (83,6%) Мтрет.-бутилпиразола. Т. куш. 102 С, чистота 98,8% (ГХ).(0,64 моля) 2-этил-1-гексанола перемешивают с 2,55 г (О,025 моля) 96%-ной по весу серной кислоты 20 ч при 175 С.Реакционную смесь после охлаждения трижды экстрагируют по 15 мл 5%-ной серной КИСЛОТЫ.Объединнные сернокислотные экстракты нейтрализуют 25%-ной натриевой щлочью. Последующая перегонка дат 27,0 г, по данным газохроматографического анализа 99,1% непревращнного пиразола.Из органической фазы получают 19,6 г Ыгексил-2-этилпиразола с т. кип. 65 С/50 мбар,чистотой 92% (ГХ) при степени превращения 21,3% и селективности 93,9%.1. Способ получения Ы-замещенных пиразолов общей формулы 1 123 к:31 в которой В означает алкил с 1-12 атомами углерода или фенилалкил с 7-20 атомами углерода и 122, 123, 124 независимо друг от друга означают водород, алкил с 1-12 атомами углерода, фенилалкил с 7-20 атомами углерода или замещенные или незамещенные арильные остатки, путем взаимодействия пиразолов общей формулы 11
МПК / Метки
МПК: C07D 231/12
Метки: пиразолов, cпособ, получения, n-замещенных
Код ссылки
<a href="https://eas.patents.su/5-257-cposob-polucheniya-n-zameshhennyh-pirazolov.html" rel="bookmark" title="База патентов Евразийского Союза">Cпособ получения n-замещенных пиразолов</a>
Предыдущий патент: Крыша транспортного средства, по меньшей мере, с одним люком
Следующий патент: Альтернативная кристаллическая форма тазофелона
Случайный патент: Устройство для производства пресной воды









