Способ получения циталопрама
Формула / Реферат
1. Способ получения циталопрама, включающий взаимодействие соединения формулы (IV)
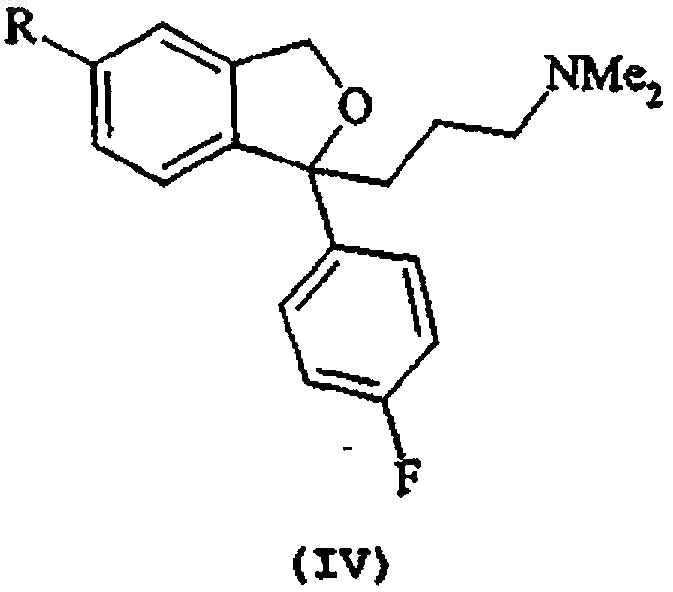
в которой R представляет собой галоген или группу СF3-(СF2)n-SO2-O-, в которой n представляет целое число в интервале 0-8 включительно, с источником цианида в присутствии палладиевого катализатора и каталитического количества Cu+ или Zn2+ или с Zn(CN)2 в присутствии палладиевого катализатора, и выделение соответствующего 5-цианосоединения, т.е. циталопрама
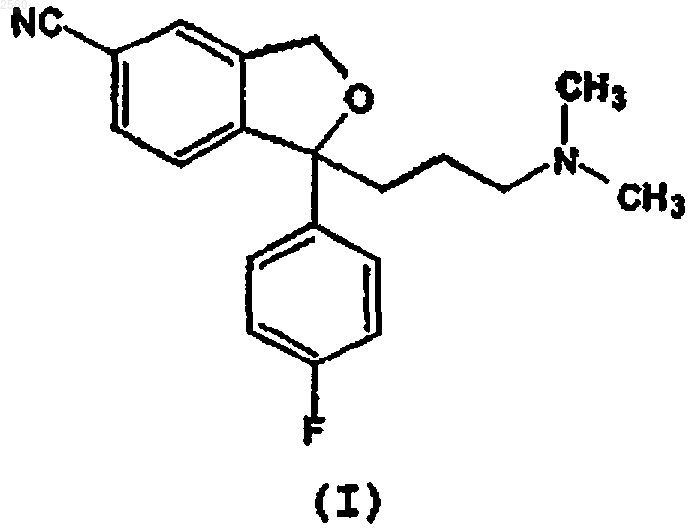
в виде основания или его фармацевтически приемлемой соли.
2. Способ по п.1, в котором источником цианида является KCN, NaCN или (R')4NCN, где (R')4 обозначает четыре группы, которые могут быть одинаковыми или различными и их выбирают из атома водорода и C1-С6 алкила с прямой или разветвленной цепью.
3. Способ по п.1 или 2, в котором R представляет собой группу СF3-(CF2)n-SO2-O-, в которой n представляет целое число в интервале 0-8, предпочтительно СF3-SO2-O-.
4. Способ по пп.1, 2 или 3, в котором R представляет собой атом брома или иода.
5. Способ по любому из пп.1-4, в котором соединение формулы (IV) взаимодействует с Zn(CN)2 в присутствии палладиевого катализатора, предпочтительно Pd(PPh3)4.
6. Способ по любому из пп.1-4, в котором используемым цианидным соединением является KCN, NaCN или Zn(CN)2.
7. Способ по любому из пп.1-4 и 6, в котором палладиевым катализатором является Рd(РРh3)4, Pd2(dba)3 или Pd(PPh)2Cl2.
8. Способ по п.7, в котором палладиевым катализатором является Pd(PPh3)4.
9. Способ по любому из пп.1-8, в котором взаимодействие осуществляют в присутствии каталитического количества Сu+, предпочтительно в форме CuI.
10. Способ по любому из пп.1-8, в котором взаимодействие осуществляют в присутствии каталитического количества Zn2+, предпочтительно в виде Zn(CN)2.
11. Способ по любому из пп.1-10, в котором соединение формулы (IV) является S-энантиомером.
12. Соединение формулы (IV)
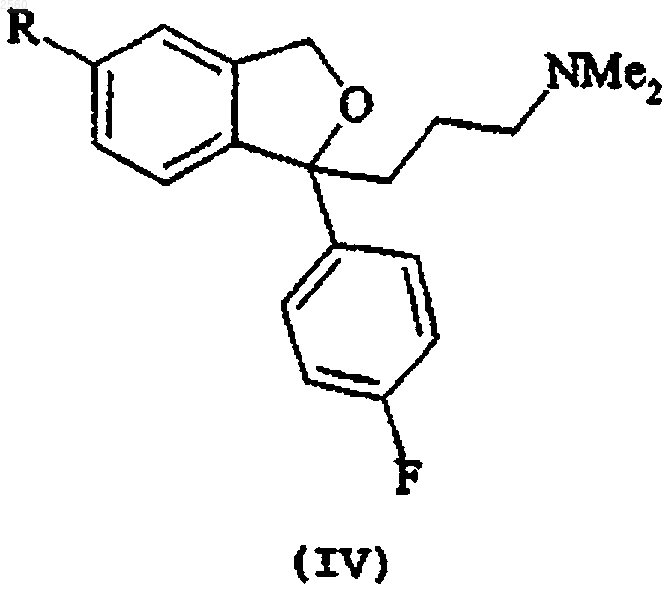
в которой R представляет собой группу СF3-(СF2)n-SO2-O-, в которой n представляет число в интервале 0-8, или R представляет собой атом иода.
Текст
1 Область техники Настоящее изобретение относится к способу получения хорошо известного антидепрессантного лекарственного средства, циталопрама, 1-[3-(диметиламино)пропил]-1-(4-фторфенил)-1,3-дигидро-5-изобензофуранкарбонитрила. Уровень техники Циталопрам представляет собой хорошо известное антидепрессантное лекарственное средство, которое уже в течение нескольких лет поступает на рынок и имеет следующую структуру: Он является селективным ингибитором повторного поглощения серотонина (5-гидрокситриптамина; 5-НТ) центрального действия, и соответственно обладает антидепрессантной активностью. Антидепрессантная активность этого соединения была описана в нескольких публикациях, например, J.Hyttel, Prog. NeuroPsychopharm.Biol. Psychiat., 1982, т.6, с.277295 и А. Gravem, Acta Psychiat. Scand, 1987,т.75, с. 478-486. Кроме того, было раскрыто, что это соединение дает эффект при лечении слабоумия и нарушений сосудов головного мозга, ЕРА 474580. Впервые циталопрам был описан в патентеDE 2657271, соответствующем патенту США 4136193. В этой патентной публикации описано получение циталопрама одним способом и рассмотрен дополнительный способ, который можно использовать для получения циталопрама. В соответствии с описанным способом, соответствующий 1-(4-фторфенил)-1,3-дигидро-5 изобензофуранкарбонитрил подвергают взаимодействию с 3-(N,N-диметиламино)пропилхлоридом в присутствии метилсульфинилметила в качестве конденсирующего агента. Исходный реагент получают из соответствующего 5 бром-производного путем взаимодействия с цианидом меди (1). В соответствии с этим способом, который рассмотрен только в общих чертах, циталопрам может быть получен путем замыкания цикла в соединении: в присутствии дегидратирующего агента с последующим обменом 5-бромгруппы с цианогруппой с использованием цианида меди (1). 2 Исходный реагент формулы (II) получают из 5 бромфталида по двум последовательным реакциям Гриньяра, т.е. соответственно с 4-фторфенилмагнийхлоридом и N,N-диметиламинопропилмагнийхлоридом. Новый и неожиданный способ получения и промежуточное соединение для получения циталопрама описан в патенте США 4650884, в соответствии с которым промежуточное соединение формулы подвергают реакции замыкания цикла посредством дегидратации с сильной серной кислотой для того, чтобы получить циталопрам. Промежуточное соединение формулы (III) получают из 5-цианофталида по двум последовательным реакциям Гриньяра, т.е. соответственно с 4 фторфенилмагнийгалогенидом и N,N-диметиламинопропилмагнийгалогенидом. Дальнейшие способы описаны в международных патентных заявкахWO 98019511,WO 98019512 и WO 98019513. WO 98019512 иWO 98019513 относятся к способам, в которых 5-амино, 5-карбокси или 5-(втор-аминокарбонил)фталид подвергают двум последовательным реакциям Гриньяра, реакции замыкания цикла и превращения образовавшегося 1,3-дигидроизобензофуранового производного в соответствующее 5-цианосоединение, т.е. циталопрам. ВWO 98019511 описан способ получения циталопрама, в котором (4-замещенное-2-гидроксиметилфенил-(4-фторфенил)метанольное соединение подвергают замыканию цикла и образовавшийся 5-замещенный 1-(4-фторфенил)-1,3 дигидроизобензофуран превращают в соответствующее 5-цианопроизводное, которое алкилируют (3-диметиламино)пропилгалогенидом для того, чтобы получить циталопрам. Наконец, в патенте США 4943590 раскрыты способы получения индивидуальных энантиомеров циталопрама, из которого также следует, что замыкание цикла промежуточного соединения формулы (III) может быть проведено через неустойчивый сложный эфир с основанием. Что касается указанных выше способов получения циталопрама, оказалось, что способ,включающий обмен 5-бромгруппы с цианогруппой, не является очень удобным в промышленном масштабе, так как выход продукта весьма мал, продукт не является чистым, и особенно трудно отделить образовавшийся циталопрам от соответствующего 5-бромсоединения. Авторы изобретения обнаружили, что циталопрам может быть получен с высоким выходом, в виде очень чистого продукта, с помощью нового каталитического способа, в котором 5 3 цианогруппа заменяет 5-галоидную или 5 трифлатную группу в 1-[3-(диметиламино) пропил]-1-(4-фторфенил)-1,3-дигидро-5-изобензофуране, и таким образом, исключается сложная обработка по старому способу обмена цианида. Сущность изобретения Таким образом, настоящее изобретение относится к новому способу получения циталопрама, включающего взаимодействие соединения формулы (IV) в которой R представляет собой атом иода, брома, хлора, или группу СF3-(CF2)n-SO2-O-, в которой n представляет целое число в интервале 08, включительно, с источником цианида, например, KCN, NaCN или (R')4N CN, где (R')4 обозначает четыре группы, которые могут быть одинаковыми или различными и их выбирают из атома водорода и C1-C6 алкила с прямой или разветвленной цепью, в присутствии палладиевого катализатора и каталитических количеств в виде основания или его фармацевтически приемлемой соли. В другом аспекте, настоящее изобретение обеспечивает новые промежуточные соединения формулы (IV), где R представляет собой группу СF3-(CF2)n-SO2-O-, в которой n представляет целое число в интервале 0-8, или R является атомом иода. В дополнительном аспекте, изобретение относится к указанному выше способу, в котором соединение формулы (IV) является Sэнантиомером. В еще одном аспекте, настоящее изобретение относится к антидепрессантой фармацевтической композиции, содержащей циталопрам,полученный по способу изобретения. По способу изобретения получают циталопрам в виде чистого продукта с высоким выходом, и таким образом, сокращаются дорогостоящие процессы очистки. Более того, реакцию можно осуществлять в более подходящих растворителях, при низкой температуре и с меньшим избытком цианид-иона, по сравнению с известным способом обмена цианогруппы. Экологическое преимущество этого способа состоит в том, что в нем используется только не 002560 4 большое количество тяжелых. Наконец, в этом способе получается улучшенный кристаллический продукт, что обеспечивает легкое превращение в требуемые соли. Было обнаружено, что промежуточные соединения формулы (IV), в которой R представляет собой группу СF3(CF2)n-SO2-O-, в которой n представляет целое число в интервале 0-8, или R является атомом иода, демонстрируют фармакологическую активность, т.е. эффект ингибирования повторного поглощения 5-НТ, и соответственно они полезны в качестве антидепрессантов. Применяемый источник цианида может быть любым подходящим источником. Предпочтительными источниками являются KCN,NaCN или (R'4N)CN, где R'4 является таким, как определено выше. Источник цианида используется в стехиометрическом количестве или в избытке, предпочтительно используют 1-2 эквивалента на 1 эквивалент исходного материала формулы (IV). Удобно, (R'4N)+ может представлять собой (Bu)4N+. Цианидным соединением предпочтительно является KCN, или NaCN, илиZn(CN)2. Палладиевым катализатором может быть любой подходящий катализатор, содержащийPd(0) или Pd(II), такой как Рd(РРh3)4, Pd2(dba)3,Pd(PPh)2Cl2 и др. Палладиевый катализатор удобно применять в количестве 1-10, предпочтительно 2-6, наиболее предпочтительно примерно 4-5 мол.%. Каталитическое количество Сu+ и Zn2+, соответственно, означает субстехиометрическое количество, такое как 0,1-5, предпочтительно 13 экв.%. Удобно, чтобы использовалось примерно 0,5 эквивалента на 1 экв. палладия. Можно использовать любой удобный источник Сu+ иCuI, a Zn2+ удобно использовать как сольZn(CN)2. В предпочтительном варианте изобретения, R представляет собой группу СF3-(CF2)nSO2-O-, в которой n представляет целое число в интервале 0-8, или R является атомом брома или иода, наиболее предпочтительно CF3-(CF2)8SO2-O-, СF3-SО 2-О-, атомом брома или иода,особенно бромом. В другом, особенно предпочтительном варианте изобретения, соединение формулы (IV) взаимодействует с Zn(CN)2 в присутствии палладиевого катализатора,предпочтительно Рd(РРh3)4, (тетракис (трифенилфосфин)палладий). Промежуточное соединение формулы (IV),в котором R является атомом брома или хлора,может быть получено из соответственно бром- и хлорфталида, как описано в DE 2657271 и соответствующем патенте США 4136193. Йодное производное может быть получено аналогично из соответствующих фталидных производных, и соединения, в которых R представляет собой группу СF3-(CF2)n-SO2-O-, могут быть получены 5 из соответствующих гидроксисоединений по традиционной реакции трифлатирования. Реакцию можно осуществлять в любом подходящем растворителе, предпочтительно в ацетонитриле, пропионитриле, тетрагидрофуране (ТГФ) и этилацетате. Другие условия реакции, растворители и т.д. представляют собой традиционные условия проведения таких реакций, и специалист в данной области техники может легко их определить. Соединение общей формулы (I) может применяться в виде свободного основания или в виде его фармацевтически приемлемой кислотно-аддитивной соли. В качестве кислотноаддитивных солей могут использоваться такие соли, образовавшиеся с органическими или неорганическими кислотами. Примерами таких органических солей являются соли с малеиновой, фумаровой, бензойной, аскорбиновой, янтарной, щавелевой, бисметиленсалициловой,метансульфоновой, этандисульфоновой, уксусной, пропионовой, винной, салициловой, лимонной, глюконовой, молочной, яблочной, миндальной, коричной, цитраконовой, аспарагиновой, стеариновой, пальмитиновой, итаконовой,гликолевой, п-аминобензойной, глутамовой,бензолсульфоновой и теофиллинуксусной кислотами, а также 8-галогентеофиллины, например, 8-бромтеофиллин. Примерами таких неорганических солей являются соли с хлористоводородной, бромисто-водородной, серной,сульфаминовой, фосфорной и азотной кислотами. Кислотно-аддитивные соли соединений могут быть получены способами, известными из уровня техники. Основание взаимодействует либо с расчетным количеством кислоты в смешивающемся с водой растворителе, таком как ацетон или этанол, с последующим выделением соли путем концентрирования и охлаждения,либо с избытком кислоты в несмешивающемся с водой растворителе, таком как диэтиловый эфир, этилацетат или дихлорметан, с самопроизвольным выделением соли. Примеры Изобретение дополнительно иллюстрируется следующими примерами. Пример 1. Оксалат циталопрама. Способ 1. Смесь Zn(CN)2 (1,2 г, 0,01 моль) и 1-(4'-фторфенил)-1-(3-диметиламинопропил)5-бромфталана (6,0 г, 0,016 моль) в 40 мл диметилформамида (ДМФ) перемешивают при комнатной температуре в атмосфере аргона в течение 30 мин. Растворенный кислород удаляют путем барботирования аргона через реакционную смесь в течение 10 мин, и затем добавляют тетракис(трифенилфосфин)палладий(0), (0,8 г,0,7 ммоль, 4,3 мол.%). Затем реакционную смесь нагревают при 75 С течение 3 ч, выливают в 200 мл воды и экстрагируют диэтиловым эфиром (2 х 100 мл), сушат (сульфат магния), 002560 6 фильтруют и концентрируют при пониженном давлении. Остаток растворяют в 10 мл ацетона и при перемешивании добавляют раствор (0,145 г,0,0016 моль) щавелевой кислоты в 10 мл ацетона. Оксалат циталопрама выделяют путем фильтрации, промывают его холодным диэтиловым эфиром и сушат в вакууме, чтобы очистить оксалат циталопрама (6,1 г, 92%). Способ 2. Смесь 1-(4'-фторфенил)-1-(3 диметиламинопропил)-5-бромфталана (2,5 г,0,007 моль), 0,68 г NaCN (0,014 моль) и 0,014 гZn(CN)2 (0,12 ммоль) в 40 мл ТГФ перемешивают при комнатной температуре в атмосфере аргона в течение 30 мин. Затем растворенный кислород удаляют путем барботирования аргона через реакционную смесь до добавления 0,3 г(0,3 ммоль, 3,7 мол.%) тетракис(трифенилфосфин)палладия(0). Затем реакционную смесь кипятят с обратным холодильником в течение ночи, охлаждают, разбавляют диэтиловым эфиром и затем фильтруют через целит. Фильтрат промывают рассолом, сушат (сульфат магния) и концентрируют при пониженном давлении. Остаток растворяют в 50 мл ацетона и при перемешивании добавляют раствор 0,63 г (7 ммоль) щавелевой кислоты в 10 мл ацетона. Оксалат циталопрама выделяют путем фильтрации, промывают его холодным диэтиловым эфиром и сушат в вакууме, чтобы очистить оксалат циталопрама (2,4 г, 82%) . Пример 2. Оксалат 1-(4'-фторфенил)-1-(3 диметиламинопропил)-5-иодфталана. Раствор бромистого 4-фторфенилмагния,полученного из 19,3 г (0,11 моль) 4-фторбромбензола и 2,92 г магниевых стружек (0,12 моль) в 100 мл сухого ТГФ, по каплям добавляют к суспензии 26,0 г (0,1 моль) 5-иодфталида в 100 мл сухого ТГФ. Температуру поддерживают ниже 0 С. После завершения добавления реакционную смесь перемешивают при 0 С в течение 3 ч. Второй раствор Гриньяра, приготовленный из 14,6 г (0,12 моль) хлористого 3-диметиламинопропила и 3,2 г магниевых стружек (0,13 моль) в 100 мл сухого ТГФ, добавляют к реакционной смеси. Температуру поддерживают ниже 0 С во время добавления. После завершения добавления охлаждение удаляют и реакционную смесь перемешивают еще 2 ч при температуре окружающей среды. Затем реакционную смесь выливают в смесь 200 мл ледяной воды и 100 мл насыщенного раствора NH4Cl. Выпаривают в вакууме ТГФ. Добавляют 200 мл толуола и выделяют органическую фазу и экстрагируют 1 М соляной кислотой (1 х 100 мл). Затем доводят значение рН водной фазы до 9, добавляя 15 мл 25%-го гидроксида аммония, и добавляют 100 мл толуола. Реакционную смесь оставляют на ночь при комнатной температуре. Отделяют органическую фазу и при комнатной температуре добавляют 10 мл 70%-й серной кислоты. Реакционную 7 смесь перемешивают при комнатной температуре в течение 2 ч, чтобы завершить реакцию замыкания цикла. Добавляют 20 мл 25%-го гидроксида аммония, и выделяют органическую фазу, фильтруют и выпаривают в вакууме, получая неочищенное соединение, указанное в заголовке, в виде его свободного основания. Образец этого неочищенного материала (5,0 г,11,3 ммоль) растворяют в этилацетате и фильтруют через диоксид кремния. Первый элюент этилацетат, который выливают. Второй элюент этилацетат : триэтиламин, 95:5, который собирают и выпаривают в вакууме, получая 3,5 г (8,2 ммоль) соединения, указанного в заголовке, в виде его свободного основания. Оксалатную соль осаждают из ацетона. Дифференциальная сканирующая калориметрия (ДСК), начало: 82 и 195 С. 1(2 Н, т, J=10 Гц), 5,0-5,2 (2 Н, 2 д, J=12,5 Гц), 6,57,05 (2 Н, шир.с), 7,16 (2 Н, т, J=7,5 Гц), 7,35 (1 Н,д, J=8,5 Гц), 7,55 (2 Н, дт, J=1,2 Гц, J=7,5 Гц),7,64 (1H, д, J=8,5 Гц), 7,69 (1H, с). Пример 3. Оксалат 1-(3-диметиламино-1 пропил)-1-(4-фторфенил)-5-гидрокси-1,3-дигидроизобензофурана. Раствор бромистого 4-фторфенилмагния,полученного из 24,0 г (0,14 моль) 4-фторбромбензола и 4,38 г магниевых стружек (0,17 моль) в 80 мл сухого ТГФ по каплям добавляют к суспензии 10,0 г (0,07 моль) 5-гидроксифталида в 100 мл сухого ТГФ при температуре ниже 8 С. После завершения добавления реакционную смесь перемешивают при комнатной температуре в течение ночи. Второй раствор Гриньяра, приготовленный из 8,50 г (0,07 моль) хлористого 3-диметиламинопропила и 1,93 г магниевых стружек (0,07 моль) в 40 мл сухого ТГФ, добавляют к реакционной смеси, поддерживая ее температуру ниже 10 С. Реакционную смесь оставляют перемешиваться в течение ночи. Реакционную смесь выливают в 200 мл ледяной воды и доводят значение рН до 1, добавляя водный раствор хлористого аммония (300 мл), что приводит к разделению смеси на две фазы. Водную фазу экстрагируют 300 мл этилацетата и затем подщелачивают до рН 8-9 25%(вес/об) гидроксидом аммония. Водную фазу экстрагируют смесью 3:2 толуол/этилацетат (3 х 100 мл). Толуольный экстракт сушат над безводным сульфатом натрия и перемешивают с углем. После фильтрации растворитель выпаривают в вакууме, и получают соединение, указанное в заголовке, в виде масла (10,2 г; 48%). Образец полученного масла (5,1 г, 16 ммоль) растворяют в 25 мл ацетона и обрабатывают безводной щавелевой кислотой (1,46 г, 16 ммоль). Смесь оставляют на ночь в холодильнике и выпавший осадок оксалата отфильтровывают. Выход составляет 4,77 г.N 3,42. Пример 4. Оксалат 1-(3-диметиламино-1 пропил)-1-(4-фторфенил)-5-[(трифторметил) сульфонилокси]-1,3-дигидроизобензофурана. Растворяют 1,79 г (5,7 ммоль) 1-(3 диметиламино-1-пропил)-1-(4-фторфенил)-5 гидрокси-1,3-дигидроизобензофурана в 35 мл дихлорметана и охлаждают в бане с ледяной водой. В атмосфере азота по каплям добавляют 0,73 мл (6,8 ммоль) хлорида трифторметансульфоновой кислоты, поддерживая температуру ниже 5 С. Реакционной смеси дают нагреться до комнатной температуре в течение ночи. Добавляют 40 мл воды и 1 мл триэтиламина, при этом фазы разделяются. Водную фазу экстрагируют 25 мл дихлорметана. Объединенные органические фазы сушат над сульфатом магния и растворитель выпаривают в вакууме. Остаток(2,09 г соединения, указанного в заголовке, в виде его свободного основания) растворяют в 10 мл ацетона и обрабатывают безводной щавелевой кислотой (0,51 г, 5,7 ммоль). После перемешивания при комнатной температуре в течение ночи, осадок отфильтровывают. Выход 0,84 г,33%. ДСК, начало 144 С. 1(0) в 10 мл ацетонитрила. Суспензию кипятят с обратным холодильником в течение 5 ч и затем дают охладиться до комнатной температуры в течение ночи при интенсивном перемешивании. Добавляют 30 мл этилацетата и смесь фильтруют через целит. Фильтрат промывают рассолом(60 мл) и сушат над сульфатом магния до выпаривания растворителя в вакууме. Неочищенный материал элюируют на диоксиде кремния (элюент - этилацетат : этанол : триэтиламин, 75: 25:4). Выход продукта 0,22 г, 30%. Оксалатную соль осаждают из ацетона. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения циталопрама, включающий взаимодействие соединения формулы в которой R представляет собой галоген или группу СF3-(СF2)n-SO2-O-, в которой n представляет целое число в интервале 0-8 включительно, с источником цианида в присутствии палладиевого катализатора и каталитического количества Cu+ или Zn2+ или с Zn(CN)2 в присутствии палладиевого катализатора, и выделение соответствующего 5-цианосоединения, т.е. циталопрама в виде основания или его фармацевтически приемлемой соли. 2. Способ по п.1, в котором источником цианида является KCN, NaCN или (R')4NCN, где(R')4 обозначает четыре группы, которые могут быть одинаковыми или различными и их выбирают из атома водорода и C1-С 6 алкила с прямой или разветвленной цепью. 3. Способ по п.1 или 2, в котором R представляет собой группу СF3-(CF2)n-SO2-O-, в которой n представляет целое число в интервале 08, предпочтительно СF3-SO2-O-. 10 4. Способ по пп.1, 2 или 3, в котором R представляет собой атом брома или иода. 5. Способ по любому из пп.1-4, в котором соединение формулы (IV) взаимодействует сZn(CN)2 в присутствии палладиевого катализатора, предпочтительно Pd(PPh3)4. 6. Способ по любому из пп.1-4, в котором используемым цианидным соединением является KCN, NaCN или Zn(CN)2. 7. Способ по любому из пп.1-4 и 6, в котором палладиевым катализатором является Рd(РРh3)4, Pd2(dba)3 или Pd(PPh)2Cl2. 8. Способ по п.7, в котором палладиевым катализатором является Pd(PPh3)4. 9. Способ по любому из пп.1-8, в котором взаимодействие осуществляют в присутствии каталитического количества Сu+, предпочтительно в форме CuI. 10. Способ по любому из пп.1-8, в котором взаимодействие осуществляют в присутствии каталитического количества Zn2+, предпочтительно в виде Zn(CN)2. 11. Способ по любому из пп.1-10, в котором соединение формулы (IV) является Sэнантиомером. 12. Соединение формулы (IV) в которой R представляет собой группу СF3-(СF2)n-SO2-O-, в которой n представляет число в интервале 0-8, или R представляет собой атом иода.
МПК / Метки
МПК: C07D 307/87
Метки: получения, способ, циталопрама
Код ссылки
<a href="https://eas.patents.su/6-2560-sposob-polucheniya-citaloprama.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения циталопрама</a>
Предыдущий патент: Устройство для манипулирования сейсмоприемной косой для использования на судах сейсмической разведки
Следующий патент: Способ получения фармацевтического препарата, обладающего фибринолитической и противовоспалительной активностью
Случайный патент: Пищевая фруктовая композиция, способ изготовления композиции и ее применение










