Способ получения 1-(аминометил)циклогексилуксусной кислоты
Формула / Реферат
1. Способ получения 1-(аминометил)циклогексилуксусной кислоты, характеризующийся превращением алкилового эфира циклогексилиденуксусной кислоты формулы (VI), где R2 представляет собой C1-C4алкильную группу, в алкиловый эфир 1-(нитрометил)циклогексилуксусной кислоты формулы (V), где значение R2 является таким, как определено выше, с помощью нитрометана в присутствии основания, гидролизом водно-метанольным раствором гидроксида калия и гидрированием полученной 1-(нитрометил)циклогексилуксусной кислоты формулы (IIa) в присутствии катализатора.

2. Способ получения 1-(аминометил)циклогексилуксусной кислоты, характеризующийся гидролизом алкилового эфира циклогексилиденуксусной кислоты формулы (VI), где R2 представляет собой C1-C4алкильную группу, в циклогексилиденуксусную кислоту формулы (IV) водно-метанольным раствором гидроксида калия, взаимодействием полученной кислоты формулы (IV) с реагентом формулы R1-X, где R1 представляет собой бензильную группу, дифенилметильную группу или при необходимости их производные, замещенные в ароматическом кольце C1-C4алкилом или алкокси, и X представляет собой атом галогена, с получением промежуточного производного циклогексилиденовой кислоты формулы (III), где значение R1 является таким, как определено выше, превращением этого промежуточного продукта в производное 1-(нитрометил)циклогексилуксусной кислоты формулы (IIb), где значение R1 является таким, как определено выше, и гидрированием последнего в растворителе в присутствии катализатора.

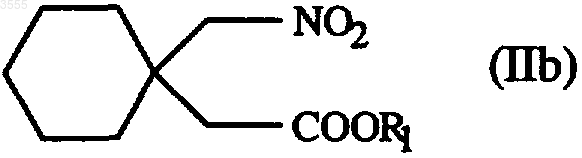
3. Способ по п.2, в котором в качестве реагента формулы R1-X используют бензилгалогенид.
4. Способ по п.2, в котором в качестве реагента формулы R1-X используют дифенилметилгалогенид.
5. Способ по пп.1-4, в котором гидрирование проводят в инертном органическом растворителе.
6. Способ по пп.1-4, в котором в качестве катализатора используют палладий на активированном угле.
7. Соединение формулы

где R представляет собой водород, бензил, дифенилметильную группу или при необходимости их производные, замещенные в ароматическом кольце C1-C4алкилом или алкокси.
8. 1-(Нитрометил)циклогексилуксусная кислота.
9. Бензил-1-(нитрометил)циклогексилацетат.
Текст
1 Изобретение относится к новому способу получения 1-(аминометил)циклогексилуксусной кислоты формулы (I) из нового промежуточного производного 1-(нитрометил)циклогексилуксусной кислоты общей формулы (II), где R представляет водород, бензильную группу, дифенилметильную группу или их производные, замещенные в ароматическом кольце C1-C4 алкилом или алкокси. 1-(аминометил)циклогексилуксусная кислота формулы (I), иначе известная как габапентин (gabapentin), является активным ингредиентом GABA-антагонистических лекарственных средств. Из уровня техники известно несколько способов синтеза этого соединения. В большинстве известных способов промежуточное соединение гидролизуют кислотой,при этом габапентин получают из образующейся соли гидрохлорида габапентина при использовании ионообменной смолы. Указанный способ описан в DE 2 460 891, в соответствии с ним ангидрид 1,1-циклогексилдиуксусной кислоты превращают в гидроксамовую кислоту и последнюю превращают с помощью реакции разложения по Лозену в гидрохлоридную соль продукта. US 4 024 175 описывает способ, в котором используют тот же ангидрид 1,1 циклогексилдиуксусной кислоты в качестве исходного реагента. Ангидрид сначала превращают в монометиловый эфир моносоли и затем из него получают моноазид монокислоты. Гидрохлорид габапентина получают из последнего с помощью реакции разложения по Курциусу. Подобным образом гидрохлорид образуется по способу, описанному в ЕР 414 274. В соответствии с этим изобретением алкиловый эфир 1-(нитрометил)уксусной кислоты превращают в производное 2-аза-спиро[4,5]декан-3 она каталитическим гидрированием. Гидрохлорид габапентина получают из последнего производного лактама путем его нагревания с обратным холодильником в присутствии соляной кислоты и габапентин выделяют с использованием ионообменной смолы. Недостатки указанных выше способов заключаются в следующем. Габапентин образуется в виде его гидрохлоридной соли и габапентин сам по себе может быть выделен только с использованием трудоемкого и дорогостоящего ионообменного метода. Для устранения нежелательного образования лактама при побочной реакции также требуется трудоемкая и дорогостоящая техника. Следующим недостатком этих способов является использование опасных реагентов, а именно, цианида калия, азида натрия и дорогостоящего оборудования, устойчивого к давлению. Способ, описанный в ЕР 414 275, устраняет образование лактамного соединения и гидрохлорида габапентина, и таким образом приме 003555 2 нение дорогостоящего ионообменного метода. В соответствии с этим способом производные цианоциклогексанмалеиновой кислоты гидролизуют основанием, декарбоксилируют и, наконец, нитрильную группу гидрируют в присутствии катализатора. С другой стороны этот патент не описывает синтез производных цианоциклогексанмалеиновой кислоты, который является многостадийным, утомительным процессом. Важно заметить, что синтез эфира малеиновой кислоты из циклогексанона включает четыре стадии, поэтому синтез габапентина в целом включает семь стадий. В противоположность другим патентам, которые описывают синтез габапентина, например, ЕР 414 274 в данном патенте не приведена характеристика чистоты полученного габапентина. Задачей изобретения является разработка экономичного, промышленно применимого способа синтеза габапентина, который устраняет неудобства приведенных выше способов и делает возможным осуществление простого синтеза очень чистого целевого продукта формулы (I) в несколько стадий с хорошим выходом. Синтез габапентина в соответствии со способом по изобретению заключается в следующем: а) алкильный эфир циклогексилиденуксусной кислоты общей формулы (VI) - где R2 представляет C1-C4 алкильную группу - превращают в алкильный эфир 1-(нитрометил)циклогексилуксусной кислоты общей формулы (V) - где значение R2 является таким, как определено выше - с нитрометаном в присутствии основания, затем последний гидролизуют воднометанольным раствором гидроксида калия и полученную 1-(нитрометил)циклогексилуксусную кислоту формулы (IIа) гидрируют в растворителе в присутствии катализатора с получением требуемого продукта формулы (I), илиb) алкильный эфир циклогексилиденуксусной кислоты общей формулы (VI) -где значение R2 определено выше - гидролизуют водно-метанольным раствором гидроксида калия и полученную циклогексилиденуксусную кислоту формулы (IV) подвергают взаимодействию с реагентом формулы R1-Х - где R1 представляет собой бензильную группу, дифенилметильную группу или при необходимости их производные,замещенные в ароматическом кольце C1C4 алкилом или алкокси, и Х представляет собой атом галогена - с получением соответствующего производного циклогексилиденовой кислоты общей формулы (III) - где значение R1 является таким, как определено выше - и этот промежуточный продукт превращают в производное 1 3(нитрометил)циклогексилуксусной кислоты общей формулы (IIb) - где значение R1 является таким, как определено выше - с нитрометаном и последующим гидрированием в растворителе в присутствии катализатора. Способ по изобретению представлен наcхеме 1. Изобретение основано на наблюдении, что восстановление новых соединений общей формулы (II) при атмосферном давлении непосредственно приводит к образованию требуемого чистого конечного продукта. Неожиданно было обнаружено, что использование соединений общей формулы (II) в качестве исходных на стадии восстановления не приводит к образованию лактамного соединения, но непосредственно получается очень чистый габапентин. Этого нельзя было ожидать при изучении предыдущих способов, так как из уровня техники известна способность такого типа соединений к образованию лактама (например, ЕР 414 274). Алкиловый эфир циклогексилиденуксусной кислоты общей формулы (VI), который используют в качестве исходного сырья, может быть получен в соответствии с известным уровнем техники с помощью реакции циклогексанона и соответствующего эфира диэтилфосфоноуксусной кислоты. На последней стадии гидрирования могут быть использованы любые катализаторы, которые обычно применяют в реакциях гидрирования, катализаторы на основе редких металлов,например, родия или палладия, никель-Ренея или кобальтовые катализаторы, в данном случае на носителе, например, угле, предпочтительно,палладий на активированном угле, более предпочтительно в количестве 10% от восстанавливаемого соединения. Гидрирование проводят в инертном органическом растворителе, предпочтительно в C1C4 спирте, более предпочтительно в метаноле,при 10-50 С, под давлением 1-20 кПа, предпочтительно при комнатной температуре и под атмосферном давлением. Конденсацию по Михаэлю эфира циклогексилиденуксусной кислоты с нитрометаном проводят в присутствии основания, предпочтительно гидроксида калия. Гидролиз алкильной эфирной группы проводят с помощью основания, предпочтительно водно-метанольного раствора гидроксида калия при комнатной температуре, затем кислоту высвобождают 10% водным раствором дигидрофосфата калия. После отфильтровывания катализатора продукт выделяют путем концентрирования 4 фильтрата. Продукт, полученный при концентрировании, имеет чистоту 98-99%, выход 5070%. Преимуществами этого способа являются следующие: полученный продукт является очень чистым; число реакционных стадий меньше, чем в известных способах; лактамное соединение, которое очень трудно удалить, не образуется; не требуется ни специального оборудования, устойчивого к давлению, ни дорогостоящего катализатора; конечный продукт может быть получен без применения трудного и сложного ионообменного метода; не требуется ядовитых или опасных веществ. Примеры Пример 1. a) Синтез 1-(нитрометил)циклогексилуксусной кислоты. Раствор 4,3 г (0,02 моль) метил-1(нитрометил)циклогексилацетата в смеси 50 мл метанола и 20 мл 10% водного раствора гидроксида калия перемешивают при комнатной температуре в течение 24 ч, затем метанол упаривают в вакууме. Значение рН полученного водного раствора доводят до 7 с помощью 10%ного водного раствора дигидрофосфата калия. Раствор трижды экстрагируют 30 мл этилацетата, органические слои объединяют, высушивают над сульфатом натрия и концентрируют с получением 3,2 г (80%) указанного в заглавии соединения в виде масла.b) Cинтез 1-(аминометил)циклогексилуксусной кислоты. Раствор 2,01 г (0,01 моль) 1-(нитрометил) циклогексилуксусной кислоты в 50 мл метанола гидрируют в присутствии 0,2 г палладия на активированном угле при атмосферном давлении. Катализатор отфильтровывают и фильтрат концентрируют до 10 мл. К остатку добавляют 20 мл тетрагидрофурана и выпавшие кристаллы отфильтровывают, высушивают и получают с выходом 1,3 г (80%) указанного в заглавии соединения. Тпл.: 164-169 С. Пример 2. Синтез 1-(аминометил)циклогексилуксусной кислоты. Раствор 5 г (0,017 моль) бензил-1-(нитрометил)циклогексилацетата в 50 мл метанола добавляют к смеси 0,5 г 10%-ного предварительно гидрированного палладия на активированном угле в 50 мл метанола. Эту смесь гидрируют при комнатной температуре под атмосферным давлением пока не израсходуется рассчитанное количество водорода, затем катализатор отфильтровывают, фильтрат концентрируют до около 15 мл и добавляют 30 мл тетрагидрофурана для осаждения указанного в заглавии соединения. Выход: 0,5 г (51%). Тпл: 168 С. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения 1-(аминометил)циклогексилуксусной кислоты, характеризующийся превращением алкилового эфира циклогексилиденуксусной кислоты формулы (VI), где R2 представляет собой C1-C4 алкильную группу, в алкиловый эфир 1-(нитрометил)циклогексилуксусной кислоты формулы (V), где значение R2 является таким, как определено выше, с помощью нитрометана в присутствии основания,гидролизом водно-метанольным раствором гидроксида калия и гидрированием полученной 1(нитрометил)циклогексилуксусной кислоты формулы (IIа) в присутствии катализатора. 2. Способ получения 1-(аминометил)циклогексилуксусной кислоты, характеризующийся гидролизом алкилового эфира циклогексилиденуксусной кислоты формулы (VI), где R2 представляет собой C1-C4 алкильную группу, в циклогексилиденуксусную кислоту формулы (IV) водно-метанольным раствором гидроксида калия, взаимодействием полученной кислоты формулы (IV) с реагентом формулы R1-X, где R1 представляет собой бензильную группу, дифенилметильную группу или при необходимости их производные, замещенные в ароматическом кольце C1-C4 алкилом или алкокси, и Х представляет собой атом галогена, с получением промежуточного производного циклогексилиденовой кислоты формулы (III), где значение R1 является таким, как определено выше, превращением этого промежуточного продукта в производное 1-(нитрометил)циклогексилуксусной кислоты формулы (IIb), где значение R1 является таким, как определено выше, и гидрировани 6 ем последнего в растворителе в присутствии катализатора. 3. Способ по п.2, в котором в качестве реагента формулы R1-X используют бензилгалогенид. 4. Способ по п.2, в котором в качестве реагента формулы R1-X используют дифенилметилгалогенид. 5. Способ по пп.1-4, в котором гидрирование проводят в инертном органическом растворителе. 6. Способ по пп.1-4, в котором в качестве катализатора используют палладий на активированном угле. 7. Соединение формулы где R представляет собой водород, бензил, дифенилметильную группу или при необходимости их производные, замещенные в ароматическом кольце C1-C4 алкилом или алкокси. 8. 1-(Нитрометил)циклогексилуксусная кислота. 9. Бензил-1-(нитрометил)циклогексилацетат.
МПК / Метки
МПК: C07C 227/04
Метки: кислоты, 1-(аминометил)циклогексилуксусной, способ, получения
Код ссылки
<a href="https://eas.patents.su/4-3555-sposob-polucheniya-1-aminometilciklogeksiluksusnojj-kisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения 1-(аминометил)циклогексилуксусной кислоты</a>
Предыдущий патент: Фармацевтическая композиция для генерации противовирусного иммунного ответа у человека и животного
Следующий патент: Четвертичные аммониевые соединения для пенной флотации силикатов из железной руды
Случайный патент: Снижение электромагнитного излучения








