Ингибиторы протеазы вич для лечения инфекции вич и фармацевтическая композиция
Номер патента: 8775
Опубликовано: 31.08.2007
Авторы: Чжан Цзяньцунь, Фардис Мерайя, Ван Цзян, Уильямс Метью Э., Пянь Хюн-Цзюн, Лиу Хонгтао, Ян Чжэн-Юй, Беккер Марк М., Сюй Ляньхонг, Нельсон Петер Х., Сваминатхан Сандарамурти, Чжан Лицзюнь, Дастгах Азар, Юй Ричард Х., Ким Чанг Ю., Эримилли Марти Н., Чен Джеймс М., Роу Таниша Д., Джин Хаолун, Ли Кристофер П., Линь Куэй-Ин, Митчел Майкл Л., Ли Уильям Э., Брайант Клиффорд, Чен Сяову, Спарасино Марк, Хэ Гон-Синь, Мэкмэн Ричард Л., Тейрио Джеймс Д.
Формула / Реферат
1. Соединение формулы
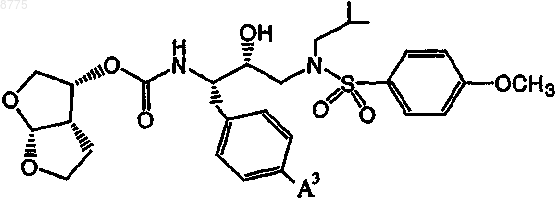
где А3 означает -OCH2P(O)R1R2, -P(O)R1R2 или -CH2P(O)R1R2, где R1 и R2 независимо выбраны из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси, бензилокси и О-пивалоилоксиметил;
или А3 означает -OCH2P(O)R1R2, где R1 и R2 независимо выбраны из группы, состоящей из Gly-Et, Ala-Et, Aba-Et, Val-Et, Leu-Et, Phe-Bu и Phe-Et;
или А3 означает -OCH2P(O)R1R2, или -OCH2CH2OCH2P(O)R1R2, где R1 выбран из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси и бензилокси, a R2 выбран из группы, состоящей из Glc-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Me, Lac-Et, Lac-Bn, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et и DiMePro-Me;
или А3 означает -OCH2P(O)R1R2, где R1 выбран из группы, состоящей из фенокси, бензилоксиэтокси, трифторэтокси и гидроксила, a R2 выбран из группы, состоящей из Gly-Bu, Ala-Me, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, Aba-Et, Aba-Bu и Ala-OH;
или А3 означает-CH2NH2CH2CH2P(O)R1R2, где R1 выбран из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси и бензилокси, a R2 выбран из группы, состоящей из Glc-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et, DiMePro-Me, Gly-Bu, Ala-Me, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, Aba-Et, Aba-Bu и Ala-OH;
и его энантиомеры и диастереомеры, а также физиологически приемлемые соли, гидраты и пролекарства.
2. Соединение по п.1, где А3 означает -OCH2P(O)R1R2 или -OCH2CH2OCH2P(O)R1R2, где R1 выбран из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси и бензилокси, a R2 выбран из группы, состоящей из Glc-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Me, Lac-Et, Lac-Bn, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et и DiMePro-Me, причем эфир молочной кислоты находится в (R)-конфигурации.
3. Соединение по п.1, где А3 означает -OCH2P(O)R1R2 или -OCH2CH2OCH2P(O)R1R2, где R1 выбран из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси и бензилокси, a R2 выбран из группы, состоящей из Glc-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Me, Lac-Et, Lac-Bn, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et и DiMePro-Me, причем эфир молочной кислоты находится в (S)-конфигурации.
4. Соединение по п.1, где А3 означает -OCH2P(O)R1R2, где R1 и R2 независимо выбраны из группы, состоящей из гидрокси и этокси.
5. Соединение по п.4, где R1 и R2 означают гидрокси или этокси.
6. Соединение формулы
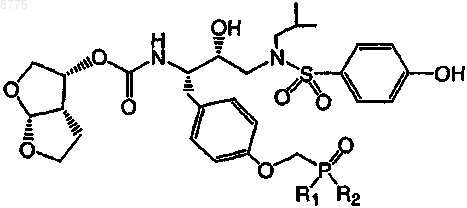
где R1 и R2 независимо выбраны из группы, состоящей из гидрокси, метокси, этокси, трифторэтокси, изопропокси, фенокси, бензилокси и О-пивалоилоксиметила.
7. Применение соединения по любому из пп.1-6 в качестве активного ингредиента при получении лекарственного средства для лечения инфекции ВИЧ.
8. Применение соединения по любому из пп.1-6 в качестве активного ингредиента при получении лекарственного средства для лечения нарушений, связанных с лейкоцитами.
9. Фармацевтическая композиция, содержащая соединение по любому из пп.1-6, приемлемые носители и эксципиенты.
Текст
008775 Изобретение в основном относится к соединениям, обладающим противовирусной активностью, и более подробно, активностью против протеазы ВИЧ. Предшествующий уровень техники Заболевание СПИД является серьезной проблемой здравоохранения во всем мире. Несмотря на широкое распространение эффективных лекарственных средств против вирусов ВИЧ, их применение ограничивается токсичностью и развитием устойчивых к лечению штаммов. В настоящее время требуются методы анализа, позволяющие определить присутствие, отсутствие или количество ВИЧ, такие методы могут быть использованы на практике для поиска ингибиторов, а также для диагностики присутствия ВИЧ. Инфекция вируса иммунодефицита человека (ВИЧ) и связанное с ней заболевание являются основной проблемой здравоохранения во всем мире. Ретровирус иммунодефицита человека, тип 1 (ВИЧ-1), член семейства первичных лентивирусов (см. статьи DeClercq E., Annals of the New York Academy of Science (1994), 724:438-456; BarreSinoussi F., Lancet (1996), 348:31-35), считается основным агентом, который вызывает синдром приобретенного иммунодефицита (СПИД) (см. статью Tarrago et al., FASEB Journal (1994), 8:497-503). Заболевание СПИД развивается в результате повторной репликации ВИЧ-1 (Biochemistry 63:133-173) с использованием трех ключевых ферментов: (i) протеазы (Пр) (von der Helm K., Biological Chemistry (1996), 377:765-774; (ii) обратной транскриптазы (ОТ) (Hottigeret al., Biological Chemistry Hoppe-Seyler (1996), 377:97-120), которая является уникальным ферментом ретровирусов,и (iii) интегразы (Asante et al., Advances in Virus Research (1999), 52:351-369; Wlodawer A., Advances in Virus Research(1999), 52:335-350; Esposito et al., Advances in Virus Research (1999), 52:319-333). Протеаза ответственна за процессинг вирусных белков-предшественников, интеграза отвечает за интеграцию двухцепочечной формы ДНК вирусного генома в ДНК хозяина, а ОТ является ключевым ферментом в репликации вирусного генома. В процессе вирусной репликации ОТ действует в качестве как РНК-зависимой, так и ДНК-зависимой ДНК полимеразы, при этом происходит превращение одноцепочечного РНК генома в двухцепочечную ДНК. Так как кодируемая вирусом ОТ опосредует специфические реакции в процессе природной репликации вируса, то ингибирование ОТ ВИЧ является основной терапевтической мишенью при лечении инфекции ВИЧ и связанного с ней заболевания. Определение последовательности всех компонентов генома некоторых инфекционных и неинфекционных изолятов вируса ВИЧ позволило установить строение вируса и типы молекул, которые имеют значение при репликации и созревании инфекционных вирусов. Протеаза ВИЧ играет существенную роль при процессинге вирусных полипептидов gag и gag-pol, в результате которого образуются зрелые белки вириона (см. статьи L.Ratner et al., Nature(1985) 313:277-284; L.H. Pearl and W.R. Taylor, Nature, 329:351 (1987). Вирус ВИЧ характеризуется строением комплекса gag/pol/env, идентичным строению других ретровирусов (см. статьи L. Ratner et al. (выше); S.Wain-Hobson etal., Cell, 40:9-17 (1985); R. Sanchez-Pescador et al., Science 227:484-492 (1985) и M.A. Muesing et al., Nature, 313:450458 (1985). Терапевтическая мишень при лечении СПИД включает ингибирование вирусной протеазы (или протеиназы),которая играет существенную роль при процессинге предшественников полипептидов, ответственных за слияние ВИЧ. Показано, что для вирусов ВИЧ и некоторых других ретровирусов процесс протеолитического созревания полипептидов слияния gag и gag/pol (процесс, который крайне необходим для накопления инфекционных вирусных частиц) опосредуется протеазой, которая сама по себе кодируется в pol-фрагменте вирусного генома (см. статьи Y.et al., J. Virol., 57:826-832 (1986) и K. von der Helm, Proc.Natl.Acad.Sci.USA, 74:911-915 (1977). Показано, что при ингибировании протеазы происходит ингибирование процессинга белка р 55 ВИЧ в клетках млекопитающих и репликация ВИЧ в Т лимфоцитах (см. статью T.J. McQuade et al., Science 247:454 (1990). Лекарственные средства, утвержденные в США для лечения СПИДа, включают нуклеозидные ингибиторы ОТ(Smith et al., Clinical Investigator, 17:226-243 (1994), ингибиторы протезы и ненуклеозидные ингибиторы ОТ (ННИОТ) (Johnson et al., Advances in Internal Medicine 45:1-40 (2000); Porche D.J., Nursing Clinics of North America, 34:95112 (1999. Протеаза (или протеиназа), содержащая только 99 аминокислотных остатков, является самым низкомолекулярным из известных ферментов и характеризуется гомологией с аспартилпротеазами, такими как пепсин и ренин(L.H. Pearl and W.R. Taylor, Nature 329:351-354 (1987) и I. Katoh et al., Nature 329:654-656 (1987), что предположительно свидетельствует об аналогичной трехмерной структуре и сходном механизме действия фермента (см. выше статью LH.Pearl and W.R.Taylor), что в настоящее время подтвеждено экспериментально. Активная протеаза ВИЧ была экспрессирована в бактериях (см., например, в статье P.L. Darke et al., J.Biol.Chem. 264:2307-2312 (1989 и синтезирована химическим способом (J. Schneider and S.B. Kent, Cell, 54:363-368 (1988) и R.F. Nutt et al.,Proc.Natl.Acad.Sci.USA, 85:7129-7133 (1988. На основании данных по сайт-направленному мутагенезу (P.L. Darke etDarke et al., J. Biol.Chem. 264:2307-2312 (1989); S. Seelmeier et al., Proc.Natl.Acad.Sci.USA, 85:6612-6616 (1988); C.Z.Giam and I.Borsos, J.Biol.Chem., 263:14617-14720 (1988) и J. Hansen et al., EMBO J., 7:1785-1791 (1988 показано,что протеаза ВИЧ проявляет механистическую функцию аспартилпротеазы. Исследования показали, что протеаза расщепляет пептидные связи в предполагаемых участках модельных пептидов, которые синтезировали по аналогии с пептидными фрагментами, которые реально расщепляются ферментом в белках-предшественниках gag и pol в процессе созревания вируса (P.L. Darke et al., Biochem.Biophys.Res.Communs., 156:297-303 (1988). Данные рентгеноструктурного анализа протеазы ВИЧ (М.А. Navia et al., Nature 337:615-620 (1989) и родственного ретровирусного фермента из вируса саркомы Rous (M. Miller et al., Nature, 337:576-579 (1989 позволили установить, что активный центр димера протеазы идентичен активному центру других аспартилпротеаз. Эти данные подтверждают предположение (см. выше статью L.H. Pearl and W.R. Taylor) о том, что активный фермент ВИЧ представляет собой димер(см. также статью Joseph A.Martin "Recent Advances in the Design of HIV Proteinase Inhibitors" (Современные успехи в разработке ингибиторов протеиназы ВИЧ), Antiviral Research, 17 (1992) 265-278). Ингибиторы протеазы ВИЧ используют для ограничения развития и распространения инфекции при введении в виде лекарственных средств, а также для диагностических анализов ВИЧ. Утвержденные комиссией по контролю качества пищевых и лекарственных препаратов США (FDA) лекарственные средства на основе ингибиторов протеа-1 008775 зы включают саквинавир (Invirase, Fortovase (Hoffman-La Roche, EP-00432695 и ЕР-00432694,ритонавир (Norvir, Abbott Laboratories),индинавир (Crixivan, MerckCo.),нелфинавир (Viracept, Pfizer),ампренавир (Agenerase, GlaxoSmithKline, Vertex Pharmaceuticals),лопинавир/ритонавир (Kaletra, Abbott Laboratories). Экспериментальные лекарственные средства на основе ингибиторов протеазы включают фосампренавир (GlaxoSmithKline, Vertex Pharmaceuticals),типранавир (Boehringer Ingelheim),атазанавир (Bristol-Mayers Squibb). В настоящее время существует необходимость в терапевтических агентах против ВИЧ, то есть в лекарственных средствах с улучшенной противовирусными и фармакокинетическими свойствами, характерзующихся повышенной активностью против развития устойчивости к ВИЧ, с улучшенной пероральной биодоступностью, более высокой активностью и более эффективным периодом полупревращения in vivo. Новые ингибиторы протеазы ВИЧ(ИП) должны обладать активностью против мутантных штаммов ВИЧ, характеризоваться различными профилями устойчивости, в меньшей степени проявлять побочные действия, обеспечивать курсы лечения без значительных осложнений и обладать пероральной активностью. Прежде всего требуются лекарственные средства, обеспечивающие легкопереносимый курс лечения дозами, такими как одна таблетка в сутки. Несмотря на то, что лекарственные средства, мишенью которых является протеаза ВИЧ, в настоящее сремя широко применяются и характеризуются эффективностью, прежде всего, при использовании в комбинации, их использование ограничивается токсичностью и развитием устойчивых штаммов (Palella et al., N.Engl.J.Med., (1998) 338:853-860; Richman D.D. Nature (2001) 410:9951001). Комбинированная терапия с использованием ингибиторов протеазы и ОТ является чрезвычайно эффективной в подавлении вирусной репликации до неопределяемого уровня в течение продолжительных периодов времени. Показано также, что комбинированная терапия с использованием ингибиторов ОТ и Пр обеспечивает синергетическое действие в подавлении репликации ВИЧ. К сожалению в настоящее время многие пациенты не поддаются комбинированной терапии из-за развития устойчивости к лекарственным средствам, в связи с отказом от курса лечения, который приводит к осложнениям, фармакокинетическим взаимодействиям, токсичности и отсутствию эффективности. Следовательно, существует необходимость в разработке новых ингибиторов протеазы ВИЧ, которые проявляют синергетическое действие в комбинации с другими ингибиторами ВИЧ. Особое внимание при исследованиях в течение многих лет уделялось улучшению доставки лекарственных средств и других агентов к клеткам-мишеням и тканям-мишеням. Несмотря на многисленные попытки разработки эффективных способов для доставки биологически активных молекул в клетки как in vivo, так и in vitro, ни один из подходов полностью не удовлетворяет предъявляемым требованиям. В большинстве случаев оптимизация ассоциации ингибирующего лекарственного средства с внутриклеточной мишенью с одновременным сведением к минимуму межклеточного распределения лекарственного средства, то есть в соседних клетках, оказывается затруднительной или неэффективной. В настоящее время многие агенты, введенные пациенту парентерально, не достигают мишени, что приводит к системной доставке агента в клетки и ткани организма, в которые доставка либо не требуется и в большинстве случаев нежелательна. В результате наблюдается отрицательное действие лекарственного средства и в большинстве случаев при этом ограничивается вводимая доза лекарственного средства (например, цитотоксических агентов и других противопухолевых или противовирусных лекарственных средств). Несмотря на то, что по сравнению с указанным выше способом введения, пероральный способ введения лекарственных средств в основном считается наиболее удобным и экономичным способом, пероральное введение может привести либо (а) к проникновению лекарственного средства через клеточные и тканевые барьеры, например, кровь/мозг, эпителиальные и клеточные мембраны, что в свою очередь приводит к нежелательному системному распределению, либо (б) к временному удерживанию лекарственного средства в желудочно-кишечном тракте. В связи с этим основная задача заключается в разработке способов специфичной доставки агентов к клеткам-мишеням или тканям-мишеням. Доставка внутрь клеток может быть достигнута способами и композициями, которые обеспечивают накопление или удерживание биологически активных соединений в клетках. Сущность изобретения В настоящем изобретении описаны новые соединения, проявляющие активность против протеазы ВИЧ, то есть новые ингибиторы протеазы ретровирусов человека. Следовательно, соединения по настоящему изобретению ингибируют протеазы ретровирусов и таким образом ингибируют репликацию вируса. Такие соединения можно использовать для лечения пациентов, инфицированных ретровирусом человека, таким как вирус иммунодефицита (штаммы ВИЧ-1 или ВИЧ-2) или вирус Т-клеточного лейкоза человека (ВТЛЧ-I или ВТЛЧ-II), которые приводят к развитию синдрома приобретенного иммунодефицита (СПИД) и/или других заболеваний. Настоящее изобретение включает новые фосфонатные ингибиторы протеазы (ИП) ВИЧ и фосфонатные аналоги известных утвержденных и экспериментальных ингибиторов протеаз. Соединения по изобретению по выбору обеспечивают накопление в клетке, как описано ниже. Настоящее изобретение в основном относится к накоплению или удерживанию терапевтических соединений внутри клетки. Прежде всего изобретение относится к обеспечению высокой концентрации фосфонатсодержащих молекул в инфицированных ВИЧ клетках. Доставку к внутриклеточной мишени осуществляют с использованием способов и композиций, которые обеспечивают накопление или удерживание биологически активных агентов внутри клеток. Такой эффективный способ доставки к мишени можно использовать в ряде терапевтических составов и процедур. Композиции по изобретению включают новые ИП, содержащие по крайней мере одну фосфонатную группу. Изобретение включает все известные утвержденные и экспериментальные ингибиторы протеаз, содержащие по-2 008775 крайней мере одну фосфонатную группу. В одном аспекте изобретение включает соединения формул I, II, III, IV, V, VI, VII и VIIIa-d где волнистая линия означает другие структурные фрагменты соединений. Структуры I-VIII замещены одной или более ковалентно присоединенных групп, включающих по крайней мере одну фосфонатную группу. Формулы I-VIII представляют собой "фрагменты-каркасы", то есть подструктуры,которые являются общими для всех специфических соединений, включенных в объем изобретения. Другой аспект изобретения относится к фармацевтической комбинации, включающей эффективное количество соединения, выбранного из формул I-VIII, и второго соединения, обладающего свойствами против ВИЧ. Еще один аспект изобретения относится к способу лечения или профилактики симптомов или проявлений инфекции ВИЧ у инфицированного животного, причем способ включает введение, то есть лечение упомянутого животного фармацевтической комбинацией, включающей эффективное количество соединения, выбранного из формулI-VIII и второе соединение, обладающее свойствами против ВИЧ. Изобретение включает фармацевтическую композицию, включающую эффективное количество соединения,выбранного из формул I-VIII, или его фармацевтически приемлемой соли в комбинации с фармацевтически приемлемым разбавителем или носителем. Изобретение относится также к способу увеличения накопления и удерживания лекарственных средств в клетках, что обеспечивает увеличение их терапевтической и диагностической ценности. Изобретение включает также способ ингибирования ВИЧ путем введения млекопитающему, инфицированному ВИЧ (ВИЧ-положительному), количества соединения формул I-VIII, эффективного для ингибирования роста упомянутых инфицированных ВИЧ клеток. Изобретение относится также к соединению, выбранному из формул I-VIII, для использования в терапии(предпочтительно для использования в терапии онкологических заболеваний, например солидных опухолей). Также изобретение относится к применению соединения формул I-VIII для получения лекарственного средства, пригодного для лечения онкологических заболеваний, например солидных опухолей. В изобретении описаны также способы и новые промежуточные соединения, представленные в данном контексте и пригодные для получения соединений по изобретению. Некоторые соединения формул I-VIII пригодны также для получения других соединений формул I-VIII. В другом аспекте изобретения активность протеазы ВИЧ ингибируют способом, включающим обработку образца, который предположительно содержит вирус ВИЧ, соединением или композицией по изобретению. Еще один аспект изобретения относится к способу ингибирования активности протеазы ВИЧ, включающему контактирование образца, предположительно содержащего вирус ВИЧ, с композицией по изобретению. Другое аспекты изобретения относятся к новым методам синтеза, анализа, разделения, выделения, очистки,характеризации и испытания соединений по настоящему изобретению.-3 008775 Перечень фигур чертежей На фиг. 1-5 представлены результаты проведения ВЭЖХ в различных условиях. Сведения, подтверждающие возможность осуществления изобретения Следует подробно описать некоторые варианты воплощения изобретения, примеры которых представлены в описании, структурах и формулах. В то время как изобретение будет описано в сочетании с пронумерованными вариантами воплощения, изобретение не ограничивается перечисленным. Наоборот, в объем изобретения включены все варианты, модификации и эквиваленты, которые могут быть внесены в объем настоящего изобретения, определенный в пунктах формулы изобретения. Определения Если не указано иное, следующие термины и выражения, использованные в настоящем описании, имеют следующие значения. Термин "фосфонат" или фосфонатная группа" означает функциональную группу или остаток в составе молекулы, который содержит по крайней мере одну связь фосфор-углерод и по крайней мере одну двойную связь фосфор-кислород. Кроме того, атом фосфора замещен группами, содержащими кислород, серу и азот. Как определено в данном описании, "фосфонат" и "фосфонатная группа" включают молекулы, содержащие функциональные группы фосфоновой кислоты, моноэфира фосфоновой кислоты, диэфира фосфоновой кислоты, фосфонамидата, фосфондиамидата и фосфонтионата. Термин "пролекарство", использованный в данном описании, означает любое соединение, которое при введении в биологическую систему образует субстанцию лекарственного средства, то есть активный компонент, который образуется в результате химической реакции (реакций), ферментативных химических реакций, фотолиза и/или метаболической химической реакции (реакций). Таким образом, пролекарство означает ковалентно модифицированный аналог или латентную форму терапевтически активного соединения."Фармацевтически приемлемое пролекарство" означает соединение, которое превращается в процессе метаболизма в организме хозяина, например, гидролизуется или окисляется под действием фермента или кислотного или основного сольволиза с образованием активного компонента. Типичные примеры пролекарств соединений по настоящему изобретению содержат лабильные защитные группы в функциональном остатке соединения. Пролекарства включают соединения, которые могут модифицироваться в результате окисления, восстанавления, аминирования,деаминирования, этерификации, омыления, алкилирования, деалкилирования, ацилирования, деацилирования, фосфорилирования, дефосфорилирования или изменения или превращения других функциональных групп, включая образование или разрыв химических связей в пролекарстве."Остаток пролекарства" означает лабильную функциональную группу, которая отделяется от активного ингибитора в процессе метаболизма по системному механизму, внутри клетки, в результате гидролиза, ферментативного расщепления или по иному механизму (см. книгу Bundgaard Hans "Design and Application of Prodrugs" (Конструирование и применение пролекарств), Textbook of Drug Design and Development (Учебник по созданию и разработке лекарственных средств) (1991), под ред. P.Krogsgaard-Larsen and H.Bundgaard, Harwood Academic Publishers, стр.113191). Ферменты, способные осуществлять ферментативную активацию пролекарств, содержащих фосфонат, по настоящему изобретению включают, без ограничения перечисленным, амидазы, эстеразы, микробные ферменты, фосфолипазы, холинэстеразы и фосфазы. Остатки пролекарства могут увеличивать растворимость, всасывание и липофильность, что позволит оптимизировать доставку лекарственного средства, а также его биодоступность и эффективность. Примеры остатков пролекарств включают чувствительные к гидролизу или лабильные ацилоксиметиловые эфиры -CH2OC(=O)R9 и ацилоксиметилкарбонаты -CH2OC(=O)OR9, где R9 означает С 1-С 6 алкил, замещенный С 1 С 6 алкил, С 6-С 20 арил или замещенный С 6-С 20 арил. Первоначально ацилоксиалкиловый эфир был использован при разработке пролекарств на основе карбоновых кислот, а затем применен к фосфатам и фосфонатам, как описано в статье Farquhar et al., J. Pharm.Sci., (1983) 72:324, и в патентах США 4816570, 4968788, 5663159 и 5792756. Позднее ацилоксиалкиловый эфир был использован для доставки фосфоновых кислот через клеточные мембраны и для повышения пероральной биодоступности. Родственный вариант ацилоксиалкилового эфира, то есть алкоксикарбонилоксиалкиловый эфир (карбонат), также может повышать пероральную биодоступность, если использовать его в качестве остатка пролекарства в соединениях, входящих в состав комбинации по настоящему изобретению. Пример ацилоксиметилового эфира включает пивалоилоксиметокси (РОМ) -СН 2 ОС(=О)С(СН 3)3. Пример ацилоксиметилкарбонатного остатка пролекарства включает пивалоилоксиметилкарбонат (РОС) -СН 2 ОС(=О)ОС(СН 3)3. Фосфонатная группа может означать фосфонатный остаток пролекарства. Остаток пролекарства может означать чувствительные к гидролизу группы, такие как, без ограничения перечисленным, пивалоилоксиметилкарбонатная (РОС) или РОМ-группы. В другом варианте остаток пролекарства может быть чувствительным к расщеплению ферментами, то есть содержать остатки эфира молочной кислоты или фосфонамидат-эфирные группы. Ариловые эфиры фосфорсодержащих групп, прежде всего, фениловые эфиры повышают пероральную биодоступность, как описано DeLambert et al., J.Med.Chem., (1994), 37:498. Описаны также фениловые эфиры, содержащие эфир карбоновой кислоты в орто-положении по отношению к фосфатной группе (см. статью Khamnei and Torrence,J.Med.Chem., (1996), 39:4109-4115). Описаны бензиловые эфиры, из которых образуется исходная фосфоновая кислота. В некоторых случаях заместители в орто- или пара-положении могут ускорять гидролиз. Бензиловые аналоги,содержащие ацилированный фенол или алкилированный фенол, при действии ферментов, например, эстераз, оксидаз и т.п. могут образовывать фенольное соединение, которое в свою очередь расщепляется по бензильной связи С-O с образованием фосфорной кислоты и промежуточного хинонметида. Примеры этого класса пролекарств описаны в статье Mitchel et al., J.Chem.Soc.Perkin Trans. (1992) I 2345; в заявке Brook et al., WO 91/19721. Описаны также другие бензильные пролекарства, содержащие остатки эфиров карбоновых кислот, присоединенные к метиленовой группе в составе бензильной группы (Glazier et al., WO 91/19721). Описаны тиосодержащие пролекарства, которые используют для внутриклеточной доставки фосфонатных лекарственных средств. Такие проэфиры содержат этилтиогруппу, в которой тиольная группа либо этерифицирована ацильной группой, либо объединена с другой тиольной группой с образованием дисульфида. Омыление или восстановление дисульфидов приводит к образованию промежуточного-4 008775 производного со свободной тиогруппой, которая затем отщепляется с образованием фосфорной кислоты и эписульфида (Puech et al., Antiviral Res. (1993), 22:155-174; Banzaria et al., J.Med.Chem. (1996), 39:4958). Циклические фосфонатные эфиры также описаны в качестве пролекарств на основе фосфорсодержащих соединений (Erion et al., патент США 6312662)."Защитная группа" означает остаток в соединении, который блокирует или изменяет свойства функциональной группы или свойства соединения в целом. Химическая структура защитной группы изменяется в широком диапазоне. Одной из функций защитной группы является получение производных при синтезе исходной лекарственной субстанции. Структура защитных групп и стратегия введения/удаления защитных групп известны в данной области техники. См. в книге "Protective Groups in Organic Chemistry", Theodora W. Greene (John Wiley and Sons, Inc., NewYork, 1991. В большинстве случаев защитные группы используют для блокирования реакционной способности функциональных групп с целью повышения эффективности требуемых химических реакций, например, для создания и расщепления химических связей по предназначенному и запланированному механизму реакции. Введение защитных групп в соединение наряду с изменением реакционной способности защищенной функциональной группы приводит к изменению других физических свойств, таких как полярность, липофильность (гидрофобность) и других свойств, которые можно определить с использованием обычных методов анализа. Сами по себе защищенные промежуточные соединения могут обладать биологической активностью или являются неактивными. Защищенные соединения могут также проявлять измененные, и в некоторых случаях оптимизированные in vitro и in vivo свойства, такие как проникновение через клеточную мембрану и устойчивость кферментативному расщеплению или секвестрации (изоляции). В этом смысле защищенные соединения с предназначенным терапевтическим действием можно назвать пролекарствами. Другой функцией защитной группы является превращение исходного лекарственного средства в пролекарство, причем исходное лекарственное средство высвобождается после превращения пролекарства in vivo. Так как активные пролекарства могут впитываться более эффективно по сравнению с исходным лекарственным средством, пролекарства могут обладать более высокой активностью in vivo по сравнению с исходным лекарственным средством. Защитные группы удаляют либо in vitro, например в случае химических производных, либо in vivo в случае пролекарств. Наличие физиологической приемлемости в случае химических производных после удаления защитных групп, например спиртов, не имеет существенного значения, хотя в основном желательно, чтобы продукты являлись фармацевтически безопасными. Любое упоминание любого соединения по настоящему изобретению включает упоминание его физиологически приемлемой соли. Примеры физиологически приемлемых солей соединений по настоящему изобретению включает соли, полученные с использованием соответствующего основания, такие как соли щелочного металла (например, натрия), щелочно-земельного металла (например, магния), аммония и NX4+ (где X означает С 1-С 4 алкил). Физиологически приемлемые соли по водородному атому или аминогруппе включают соли органических карбоновых кислот, таких как уксусная, бензойная, молочная, фумаровая, винная, малеиновая, малоновая, яблочная, изетионовая,лактобионовая и янтарная кислоты; органических сульфоновых кислот, таких как метансульфоновая, этансульфоновая, бензолсульфоновая и паратолуолсульфоновая кислоты; и неорганических кислот, таких как хлористоводородная, серная, фосфорная и сульфаминовая кислоты. Физиологически приемлемые соли соединения по гидроксильной группе включают анион упомянутого соединения в комбинации с подходящим катионом, таким как Na+ иNX4+ (где X независимо выбирают из водорода и С 1-С 4 алкильной группы). Соли активных компонентов соединений по настоящему изобретению, предназначенные для терапевтического применения, должны быть физиологически приемлемыми, то есть представлять собой соли, полученные из физиологически приемлемых кислоты или основания. Однако можно также использовать соли физиологически неприемлемых кислот и оснований, например при получении или очистке физиологически приемлемого соединения. Все соли,независимо от того, является ли соль или основание физиологически приемлемыми, включены в объем настоящего изобретения."Алкил" означает С 1-C18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода. Примеры включают метил (Me, -CH3), этил (Et, -CH2CH3), 1-пропил (n-Рr, н-пропил, -СН 2 СН 2 СН 3), 2 пропил (i-Pr, изопропил, -СН 2(СН 3)2. 1-бутил (n-Bu, н-бутил, -СН 2 СН 2 СН 2 СН 3), 2-метил-1-пропил (i-Bu, изобутил,-СН 2 СН(СН 3)2, 2-бутил (s-Bu, вторбутил, -СН 2(СН 3)СН 2 СН 3), 2-метил-2-пропил (t-Bu, трет-бутил, -С(СН 3)3),1-пентил (н-пентил, -СН 2 СН 2 СН 2 СН 2 СН 3), 2-пентил (-СН(СН 3)СН 2 СН 2 СН 3), 3-пентил (-СН(СН 2 СН 3)2), 2-метил-2 бутил (-С(СН 3)2 СН 2 СН 3), 3-метил-2-бутил (-СН(СН 3)СН(СН 3)2), 3-метил-1-бутил (-СН 2 СН 2 СН(СН 3)2), 2-метил-1 бутил (-СН 2 СН(СН 3)СН 2 СН 3), 1-гексил (-СН 2 СН 2 СН 2 СН 2 СН 2 СН 3), 2-гексил (-СН(СН 3)СН 2 СН 2 СН 2 СН 3), 3-гексил"Алкенил" означает С 2-С 18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода и по крайней мере одну ненасыщенную связь, то есть углерод-углеродную sp2 двойную связь. Примеры включают, без ограничения перечисленным, этилен или винил (-СН=СН 2), аллил (-СН 2 СН=СН 2), циклопентил"Алкинил" означает С 2-С 18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода и по крайней мере одну ненасыщенную связь, то есть углерод-углеродную sp тройную связь. Примеры включают, без ограничения перечисленным ацетиленовую (-ССН) и пропаргиловую (-СН 2 ССН) группы."Алкилен" означает насыщенный с разветвленной или прямой цепью или циклический углеводородный радикал, содержащий 1-18 атомов углерода и две валентности, образующиеся при удалении двух атомов водорода у одного и того же атома углерода или у двух различных атомов углерода в исходном алкане. Типичные алкиленовые радикалы включают, без ограничения перечисленным, метилен (-СН 2-), 1,2-этил (-СН 2 СН 2-), 1,3-пропил (СН 2 СН 2 СН 2-), 1,4-бутил (-СН 2 СН 2 СН 2 СН 2-) и т.п."Алкенилен" означает ненасыщенный углеводородный радикал с разветвленной или прямой цепью или цикли-5 008775 ческий радикал, содержащий 2-18 атомов углерода и две валентности, образующиеся при удалении двух атомов водорода у одного и того же атома углерода или у двух различных атомов углерода в исходном алкене. Типичные алкениленовые радикалы включают, без ограничения перечисленным, 1,2-этилен (-СН=СН-)."Алкинилен" означает ненасыщенный углеводородный радикал с разветвленной или прямой цепью или циклический радикал, содержащий 2-18 атомов углерода и две валентности, образующиеся при удалении двух атомов водорода у одного и того же атома углерода или у двух различных атомов углерода в исходном алкине. Типичные алкиниленовые радикалы включают, без ограничения перечисленным, ацетилен (-СС-), пропаргил (-СН 2 СС-) и 4 пентинил (-СН 2 СН 2 СН 2 ССН)."Арил" означает моновалентный ароматический углеводородный радикал, содержащий 6-20 атомов углерода,образующийся при удалении одного атома водорода у одного атома углерода в исходной ароматической кольцевой системе. Типичные арильные группы включают, без ограничения перечисленным, производные бензола, замещенного бензола, нафталина, антрацена, бифенила и т.п."Арилалкил" означает ациклический алкильный радикал, в котором один из атомов водорода, присоединенный к атому углерода, обычно к терминальному или sp3 атому углерода, заменен на арильный радикал. Типичные арилалкильные радикалы включают, без ограничения перечисленным, бензил, 2-фенилэтан-1-ил, 2-фенилэтен-1-ил,нафтилметил, 2-нафтилэтан-1-ил, 2-нафтилэтен-1-ил, нафтобензил, 2-нафтофенилэтан-1-ил и т.п. Арилалкильная группа включает от 6 до 20 атомов углерода, например алкильный остаток, включающий алканильные, алкенильные или алкинильные группы, причем арилалкильная группа содержит от 1 до 6 атомов углерода, а арильный остаток от 5 до 14 атомов углерода."Замещенный алкил", "замещенный арил" и "замещенный арилалкил" означает алкил, арил и арилалкил, соответственно, в которых один или более атомов водорода каждый независимо замещен заместителем. Типичные заместители включают, без ограничения перечисленным, -X, -R, -О-, -OR, -SR, -S, -NR2, -NR3, =NR, -CX3, -CN, -OCN,-SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, NC(=O)R, -C(=O)R, -C(=O)NRR, -S(=O)2O-, -S(=O)2OH, -S(=O)2R,-OS(=O)2OR, -S(=O)2NR, -S(=O)R, -OP(=O)O2RR, -P(=O)O2RR, -P(=O)(O-)2, -P(=O)(OH)2, -C(=O)R, -C(=O)X, -C(S)R,-C(O)OR, -C(O)O-, -C(S)OR, -C(O)SR, -C(S)SR, -C(O)NRR, -C(S)NRR, -C(NR)NRR, где каждый Х независимо означает галоген, F, Cl, Вr или I, а каждый R независимо означает -Н, алкил, арил, гетероцикл или остаток пролекарства. Алкилен, алкенилен и алкинилен могут быть также аналогичным образом замещены. Например, гетероцикл, связанный через атом углерода, присоединен, без ограничения перечисленным, в положениях 2, 3, 4, 5 или 6 пиридина, в положениях 3, 4, 5 или 6 пиридазина, в положениях 2, 4, 5 или 6 пиримидина, в положениях 2, 3, 5 или 6 пиразина, в положениях 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, в положениях 2, 4 или 5 оксазола, имидазола или тиазола, в положениях 3, 4 или 5 изоксазола, пиразола или изотиазола, в положениях 2 или 3 азиридина, в положениях 2, 3 или 4 азетидина, в положениях 2, 3, 4, 5, 6, 7 или 8 хинолина или в положениях 1, 3, 4, 5, 6, 7 или 8 изохинолина. Наиболее типичные гетероциклы, связанные через атом углерода, включают 2-пиридил, 3-пиридил, 4-пиридил, 5-пиридил, 6-пиридил, 3 пиридазинил, 4-пиридазинил, 5-пиридазинил, 6-пиридазинил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 6 пиримидинил, 2-пиразинил, 3-пиразинил, 5-пиразинил, 6-пиразинил, 2-тиазолил, 4-тиазолил или 5-тиазолил. Например, гетероцикл, связанный через атом азота, присоединен, без ограничения перечисленным, в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2 имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола,индолина, 1 Н-индазола, в положении 2 изоиндола или изоиндолина, в положении 4 морфолина и в положении 9 карбазола или -карболина. Наиболее типичные гетероциклы, связанные через атом азота, включают, 1-азиридил, 1 азетедил, 1-пирролил, 1-имидазолил, 1-пиразолил и 1-пиперидинил."Карбоцикл" означает насыщенное, ненасыщенное или ароматическое кольцо, содержащее от 3 до 7 атомов углерода в форме моноцикла или от 7 до 12 атомов углерода в форме бицикла. Моноциклические карбоциклы содержат от 3 до 6 циклических атомов, более типично, 5 или 6 циклических атомов. Бициклические карбоциклы содержат от 7 до 12 циклических атомов, например, образующих бицикло[4,5], [5,5], [5,6] или [6,6]систему, или со-6 008775 держат 9 или 10 циклических атомов, образующих бицикло[5,6] или [6,6]систему. Примеры моноциклических карбоциклов включают циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент 3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, фенил, спирил и нафтил."Связующее звено" или "связь" означает химический остаток, включающий ковалентную связь или цепочку атомов, через которые фосфонатная группа ковалентно присоединена к лекарственному средству. Связующие звенья включают фрагменты заместителей А 1 и А 3, указанных в формуле I, или заместителей А 1 и А 3, указанных в формулеII, которые включают остатки, такие как повторяющиеся звенья алкилокси (например, полиэтиленокси, PEG, полиметиленокси) и алкиламино (например, полиэтиленамино, Jeffamine), и сложные эфиры и амиды двухосновных кислот, включающих сукцинат, сукцинамид, дигликолят, малонат и капроамид. Термин "хиральный" относится к молекулам, структура которых не совпадает с их зеркальным отражением, а термин "ахиральный" относится к молекулам, структура которых совпадает с их зеркальным отражением. Термин "стереоизомеры" относится к соединениям с одинаковой химической структурой, но которые отличаются расположением атомов или групп в пространстве."Диастереомер" означает стереоизомер, содержащий два или более центров хиральности, а его молекулы не являются зеркальным отражением друг друга. Диастереомеры отличаются по физическим свойствам, например характеризуются различными температурами плавления, температурами кипения, спектральными характеристиками и реакционной способностью. Смеси диастереомеров можно разделять с использованием высокоэффективных аналитических методов, таких как электрофорез и хроматография."Энантиомеры" означают два стереоизомера соединения, структуры которых не совпадают с зеркальными отражениями друг друга. Для описания стереохимических определений и терминов использовали рекомендации, представленные в книгах под ред. S.P.Parker, McGraw-Hill Dictionary of Chemical Terms (1984), McGraw-Hill Book Company, New York, иEliel E. and Wilen S., Stereochemistry of Organic Compounds (1994), John Wiley and Sons, Inc., New York. Многие органические соединения существуют в оптически активной форме, то есть они способны вращать плоскость поляризованного света. При описании оптически активных соединений буквы D и L или R и S используют для обозначения абсолютной конфигурации молекулы в хиральном центре (центрах). Знаки d и l, D и L или (+) и (-) используют для обозначения знака вращения плоскополяризованного света соединением, причем знак l или (-) означают, что соединение является левовращающим, а знак (+) или d означает, что соединение является правовращающим. В случае данной химической структуры эти соединения, называемые стереоизомерами, являются идентичными, за исключением случая, когда они являются зеркальным отражением друг друга. Специфический стереоизомер называется также энантиомером, а смесь таких изомеров в большинстве случаев называют энантиомерной смесью. Смесь энантиомеров 50:50 называют рацемической смесью или рацематом, которые не проявляют стереоспецифичность или стереоселективность в химической реакции или процессе. Термины "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомеров, не проявляющей оптическую активность. Ингибиторы протеазы ВИЧ Соединения по изобретению включают соединения, которые проявляют ингибирующую активность в отношении протеазы ВИЧ. Прежде всего, соединения включают ингибиторы протеазы ВИЧ. Соединения по изобретению содержат фосфонатную группу, которая может означать остаток пролекарства. В различных вариантах воплощения изобретения описаны соединения, которые относятся к общей структуре,определенной терминами ILPPI (индинавирподобные фосфонатные ингибиторы протезы, формула I), AMLPPI (ампренавирподобные фосфонатные ингибиторы протеазы, формула II), KNILPPI (KNI-подобные фосфонатные ингибиторы протеазы, формула III), RLPPI (ритонавирподобные фосфонатные ингибиторы протеазы, формула IV), LLPPI(лопинавирподобные фосфонатные ингибиторы протеазы, формула IV), NLPPI (нелфинавирподобные фосфонатные ингибиторы протеазы, формула V), SLPPI (саквинавирподобные фосфонатные ингибиторы протеазы, формула V),ATLPPI (атанзавирподобные фосфонатные ингибиторы протеазы, формула VI), TLPPI (типранавирподобные фосфонатные ингибиторы протеазы, формула VII) и CCLPPI (циклические карбонилподобные фосфонатные ингибиторы протеазы, формула VIIIa-d), причем все перечисленные соединения содержат фосфонатную группу, например диэфирфосфонат, фосфонамидат-эфирное пролекарство или фосфонамидат-эфир (Jiang et al., заявка США 2002/ 0173490 А 1). Если соединение, описанное в данном контексте, замещено одной или более одинаково обозначенными группами, например, "R1" или "R6a", то следует понимать, что группы могут быть одинаковыми или различными, то есть каждую группу выбирают независимо. Волнистые линии означают места ковалентных связей с соседними группами,остатками или атомами. Соединения по настоящему изобретению описаны на схемах, в примерах, описании и пунктах формулы изобретения, представленной ниже, и изобретение включает соединения формул I, II, III, IV, V, VI, VII и VIIa-d: где волнистая линия означает другие остатки соединений. Формула I включает в качестве ядра 3-гидрокси-5-аминопентамид. Формула II включает в качестве ядра 2 гидрокси-1,3-аминопропиламид или 2-гидрокси-1,3-аминопропиламиносульфон. Формула III включает в качестве ядра 2-гидрокси-3-аминопропиламид. Формула IV включает в качестве ядра 2-гидрокси-4-аминобутиламин. Формула V включает в качестве ядра ацилированный 1,3-диаминопропан. Формула VI включает в качестве ядра 2 гидрокси-3-диазапропиламид. Формула VII включает в качестве ядра сульфонамид 5,6-дигидро-4-гидрокси-2-пирон. Формула VIIIa-d включает шести- или семичленное кольцо и в качестве ядра циклический карбонил, сульфгидрил,сульфоксид или силикон, где Y1 означает кислород, серу или замещенный азот, а m2 равно 0, 1 или 2. Структуры формул I, II, III, IV, V, VI, VII и VIIa-d замещены одной или более ковалентно присоединенных групп, включая по крайней мере одну фосфонатную группу. Структуры формул I, II, III, IV, V, VI, VII и VIIa-d замещены одной или более ковалентно присоединенных групп А 0, причем возможно замещение в любой группе А 0 или во всех группах А 0. А 0 означает А 1, А 2 или W3. Соединения формул I, II, III, IV, V, VI, VII и VIIIa-d включают по крайней мере один А 1. А 1 означаетRx независимо означает Н, W3, защитную группу или формулу:Ry означает Н, W3, R2 или защитную группу; при условии, что если m1a, m12c и m1d равны 0, то m1b, m1c и m1e равны 0; если m1 а и m12 с равны 0 и m1d не равно 0, то m1b и m1 с равно 0; если m1a и m1d равно 0 и m12 с не равно 0, то m1b и по крайней мере один из m1 с и m1 е равен 0; если m1a равно 0 и m12 с и m1d не равно 0, то m1b равно 0; если m12 с и m1d равно 0 и m1 а не равно 0, то по крайней мере два из m1d, m1c и m1e равно 0; если m12 с равно 0 и m1a и m1d не равно 0, то по крайней мере один из m1b и m1c равно 0; и если m1d равно 0 и m1 а и m 12 с не равно 0, то по крайней мере один из m1 с и m1e равно 0.R2 независимо означает Н, R1, R3 или R4, где каждый R4 независимо замещен группами R3 от 0 до 3. В другом варианте две группы R2 объединены с атомом углерода с образованием кольца, т.е. спироуглерода. Кольцо может представлять собой, например, циклопропил, циклобутил, циклопентил или циклогексил. Кольцо может быть замещено группами R3, от 0 до 3.R4 означает алкил, содержащий 1-18 атомов углерода, алкенил, содержащий 2-18 атомов углерода или алкинил, содержащий 2-18 атомов углерода.R5a независимо означает алкилен, содержащий 1-18 атомов углерода, алкенилен, содержащий 2-18 атомов углерода или алкинилен, содержащий 2-18 атомов углерода, причем любой из них может быть замещен группами R3,от 0 до 3.W5 означает карбоцикл или гетероцикл, где W5 независимо замещен группами R2 от 0 до 3.W5a означает мультивалентный замещенный карбоцикл и гетероцикл, где W5a независимо замещен группамиW5 и W5a означают карбоциклы и W5 и W5a означают гетероциклы, которые могут быть независимо замещены группами R2, от 0 до 3. W5 и W5a могут быть насыщенными, ненасыщенными или ароматическими кольцами, содер-9 008775 жащими моно- или бициклические карбоцикл или гетероцикл. W5 и W5a могут включать от 3 до 10 циклических атомов, например от 3 до 7 циклических атомов. Кольца W5 и W5a являются насыщенными, если содержат 3 циклических атома, насыщенными или мононенасыщенными, если содержат 4 циклических атома, насыщенными или моноили диненасыщенными, если содержат 5 циклических атомов, и насыщенными, моно- или диненасыщенными или ароматическими, если содержат 6 циклических атомов. Гетероциклы W5 или W5a могут означать моноцикл, содержащий от 3 до 7 циклических атомов (от 2 до 6 атомов углерода и от 1 до 3 гетероатомов, которые выбирают из группы, включающей N, О, Р и S), или бицикл, содержащий от 7 до 10 циклических атомов (от 4 до 9 атомов углерода и от 1 до 3 гетероатомов, которые выбирают из группы, включающей N, О, Р и S). W5 может означать гетероциклические моноциклы, содержащие от 3 до 6 циклических атомов (от 2 до 5 атомов углерода и от 1 до 2 гетероатомов, выбранных из N, О и S) или 5 или 6 циклических атомов (от 3 до 5 атомов углерода и от 1 до 2 гетероатомов, которые выбирают из группы, включающей N и S). Гетероциклические бициклы W5 и W5a содержат от 7 до 10 циклических атомов (от 6 до 9 атомов углерода и от 1 до 2 гетероатомов, которые выбирают из группы, включающей N, О и S), расположенных в бициклических системах[4,5], [5,5], [5,6] или [6,6]; или от 9 до 10 циклических атомов (от 8 до 9 атомов углерода или от 1 до 2 гетероатомов,котрые выбирают из группы, включающей N и S), расположенных в бициклических системах [5,6] или [6,6]. Гетероциклы W5 и W5a могут быть присоединены к Y2 через атом углерода, азота, серы или другой атом с образованием стабильной ковалентной связи. Гетероциклы W5 и W5a включают, например, пиридил, изомеры дигидропиридила, пиперидин, пиридазинил,пиримидинил, пиразинил, s-триазинил, оксазолил, имидазолил, тиазолил, изоксазолил, пиразолил, изотиазолил, фуранил, тиофуранил, тиенил и пирролил. W5 также включает, без ограничения перечисленным, следующие структуры: Карбоциклы и гетероциклы W5 и W5a могут быть независимо замещены группами R2, от 0 до 3, как определено выше. Например, замещенные карбоциклы W5 включают Примеры замещенных фенилкарбоциклов включают Варианты воплощения группы А 1 включают и где одни или более Y2 означают связь, такие какW5a означает мультивалентный замещенный карбоцикл и гетероцикл, где W5a независимо замещен группами где n равно целому числу от 1 до 18. Варианты А 3 включают заместитель, в котором М 2 равно 0, такой как где W5 означает карбоцикл, такой как фенил или замещенный фенил. Такой вариант воплощения настоящего изобретения включает где Y2b означает О или N(RX); M12d равно 1, 2, 3, 4, 5, 6, 7 или 8; и фенил карбоцикл замещен группами R2, от 0 до 3. Такие варианты воплощения группы А 3 включают фенилфосфонамидатные эфиры аминокислот и фенилфосфонатные эфиры молочной кислоты и Хиральный атом аминокислотного остатка и остатка молочной кислоты может находиться в R или S конфигурации или представлять рацемическую смесь. Варианты воплощения группы Rx включают сложные эфиры, карбаматы, карбонаты, тиоэфиры, амиды, тиоамиды и остатки мочевины: и Варианты воплощения группы А 2, где W3 означает W5, включают В другом варианте А 2 означает фенил, замещенный фенил, бензил, замещенный бензил, пиридил или замещенный пиридил. Примеры вариантов формулы I включают соединения, без ограничения перечисленным где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы II включают соединения, без ограничения перечисленным, где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы III включают соединения, без ограничения где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы IV включают соединения, без ограничения перечисленным где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы V включают соединения, без ограничения перечисленным где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы VI включают соединения, без ограничения перечисленным где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы VII включают соединения, без ограничения перечисленным где А 1 означает место ковалентного присоединения фосфонатной группы. Примеры вариантов формулы VIIIa включают структуры и Примеры вариантов формулы VIIIb включают структуры Примеры вариантов формулы VIIIc включают структуры- 14008775 Примеры вариантов формулы VIIId включают структуры, где А 1 означает и место ковалентного присоединения фосфонатной группы. Вариант воплощения изобретения в отношении накопления в клетках Другой вариант воплощения настоящего изобретения относится к ингибитору обратной транскриптазы (ННИОТ), который накапливается в клетках РВМС человека. Накопление в РВМС человека описано в приведенных ниже примерах. Обычно соединения по настоящему изобретению включают фосфонат и фосфонатное пролекарство. Более подробно, фосфонат или фосфонатное пролекарство характеризуется структурой А 3, описанной в данном контексте. Каждый из предпочтительных вариантов воплощения структуры А 3 является предпочтительным вариантом в настоящем варианте воплощения А 3. По выбору соединение по данному варианту воплощения настоящего изобретения характеризуется повышенным периодом полупревращения соединений или продуктов их метаболизма внутри клеток РВМС человека по сравнению с аналогами соединений, не содержащих фосфонат или фосфонатное пролекарство. Обычно период полупревращения повышается по крайней мере приблизительно на 50%, или более предпочтительно в интервале 50-100%,еще более предпочтительно по крайней мере приблизительно на 100%, наиболее предпочтительно более 100%. В предпочтительном варианте воплощения настоящего изобретения внутриклеточный период полупревращения метаболитов соединения в клетках РВМС человека увеличивается по сравнению с аналогичным соединением, не содержащим фосфоната или фосфонатного лекарства. В таких вариантах воплощения настоящего изобретения метаболит обычно образуется внутри клетки, более предпочтительно внутри клеток РВМС человека. Еще более предпочтительно метаболит является продуктом расщепления фосфонатного пролекарства внутри РВМС человека. Наиболее предпочтительно фосфонатное пролекарство расщепляется с образованием метаболита, характеризующегося по крайней мере одним отрицательным зарядом при физиологической величине рН. Наиболее предпочтительно фосфонатное пролекарство отщепляется под действием фермента внутри клеток РВМС человека с образованием фосфоната, содержащего по крайней мере один активный атом водорода в форме Р-ОН. Несмотря на другие определения в данном контексте, касающиеся роли или описания фосфонатных групп в соединениях по изобретению, другой вариант А 3 означает группу А 3a формулы В данном варианте изобретения любая группа А 3 может означать А 361. В другом аспекте изобретения А 3 означает формулу М 12 а не равно 0 и по крайней мере одна фосфонатная группа, присутствующая в соединении, не соединена прямой связью с W3. Более типично фосфонатная группа не соединена прямой связью с W5. В данном варианте атом фосфора фосфонатной группы не соединен прямой связью с циклическим атомом углерода. В другом аспекте изобретения ампренавирподобный фосфонатный ингибитор протеазы, описанный выше в описании и ниже в пунктах формулы изобретения, содержит группу А 3 формулы М 12 а не равно 0 и по крайней мере одна фосфонатная группа, присутствующая в соединении, не соединена прямой связью с W3. Более типично фосфонатная группа не соединена прямой связью с W5. В данном варианте атом фосфора фосфонатной группы не соединен прямой связью с циклическим атомом углерода. В другом варианте ампренавирподобный фосфонатный ингибитор протеазы, описанный выше в описании и ниже в пунктах формулы изобретения, не включает соединения формулы- 15008775 В другом аспекте изобретения А 3 означает формулу М 12 а равно 0 и по крайней мере одна фосфонатная группа, присутствующая в соединении, соединена прямой связью с W3. Более типично фосфонатная группа соединена прямой связью с W5. В данном варианте атом фосфора фосфонатной группы соединен прямой связью с циклическим атомом углерода. В другом аспекте изобретения ампренавирподобный фосфонатный ингибитор протеазы, описанный выше в описании и ниже в пунктах формулы изобретения, содержит группу А 3 формулы М 12 а равно 0 и по крайней мере одна фосфонатная группа, присутствующая в соединении, соединена прямой связью с W3. Более типично фосфонатная группа соединена прямой связью с W5. В данном варианте атом фосфора фосфонатной группы соединен прямой связью с циклическим атомом углерода. В другом аспекте ампренавирподобный фосфонатный ингибитор протеазы, описанный выше в описании и ниже в пунктах формулы изобретения, включает соединения формулы и Примеры пронумерованных соединений В качестве примеров и без ограничения перечисленным варианты воплощения настоящего изобретения включены в таблицу (табл.100), представленную ниже. Эти варианты воплощения настоящего изобретения характеризуются общей формулой MBF В каждый вариант воплощения формулы MBF включено замещенное ядро (Sc), в котором ядру приписан номер, а каждый заместитель обозначен буквой или цифрой. В табл. 1.1-1.5 приведен список ядер, используемых для получения соединений из таблицы 100. Каждое ядро (Sc) обозначено номером из табл. 1.1-1.5 и этот номер указан первым в названии каждого соединения. Аналогично, в табл. 10.1-10.19 и 20.1-20.36 приведены списки связующих звеньев (Lg) и заместителей пролекарств (Pd1 и Pd2), соответственно обозначенных буквой или цифрой. Соответственно, каждое соединение, приведенное в таблице 100, обозначено номером, приписанным ядру в таблицах 1.1-1.5, затем следует буква, обозначающая связующее звено (Lg) из таблиц 10.1-10.19 и две цифры, обозначающие две группы пролекарства (Pd1 и Pd2) из табл. 20.1-20.36. В графической форме название каждого соединения из таблицы 100 будет иметь следующий вид:Sc.Lg.Pd1.Pd2. Таким образом, без учета стереохимического строения, структура 10, схема 2, схема раздела А, будет выглядеть следующим образом: 12.АН.247.247. Каждая группа Sc изображается со знаком тильда . Этот знак означает место ковалентного присоединенияSc к Lg. Q1 и Q2 представляют собой связующие звенья (Lg), при этом следует понимать, что они не обозначают группы или атомы, а просто обозначают связь. Q1 означает ковалентную связь с ядром (Sc), a Q2 означает ковалент- 16008775 ную связь с атомом фосфора в структуре MBF. Каждая группа пролекарства (Pd1 и Pd2) ковалентно связана с атомом фосфора в структуре MBF через связь, обозначенную знаком тильда . Некоторые варианты воплощения соединений из таблиц 10.1-10.19 и 20.1-20.36 могут быть обозначены в виде комбинации букв и цифр (таблица 10.1-10.19) или цифры и буквы (табл. 20.1-20.36). Например, существуют соединения BJ1 и BJ2 из табл. 10. В каждом случае соединения в таблицах 10.1-10.19 всегда начинаются с буквы, а соединения в таблицах 20.1-20.36 всегда начинаются с цифры. Если ядро (Sc) изображено заключенным с квадратные скобки ([]), и ковалентная связь изображена за пределами скобок, то Sc может быть присоединено к Lg в любом замещенном положении структуры SC. Выбор места присоединения описан в данном контексте. В качестве примера и без ограничения перечисленным место присоединения выбирают из структур, изображенных на схемах и в примерах. Таблица 1.1
МПК / Метки
МПК: C07F 9/40, C07F 9/02, C07F 9/38
Метки: вич, инфекции, лечения, фармацевтическая, ингибиторы, протеазы, композиция
Код ссылки
<a href="https://eas.patents.su/30-8775-ingibitory-proteazy-vich-dlya-lecheniya-infekcii-vich-i-farmacevticheskaya-kompoziciya.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы протеазы вич для лечения инфекции вич и фармацевтическая композиция</a>
Предыдущий патент: Замещенные производные 1-пиперидин-3-ил-4-пиперидин-4-илпиперазина и их применение в качестве антагонистов нейрокинина
Следующий патент: Жидкая стабильная композиция оксазафосфорина с месной
Случайный патент: Применение полипептидов цитокина zcyto человека и мыши и антител к данным полипептидам для лечения различных заболеваний












