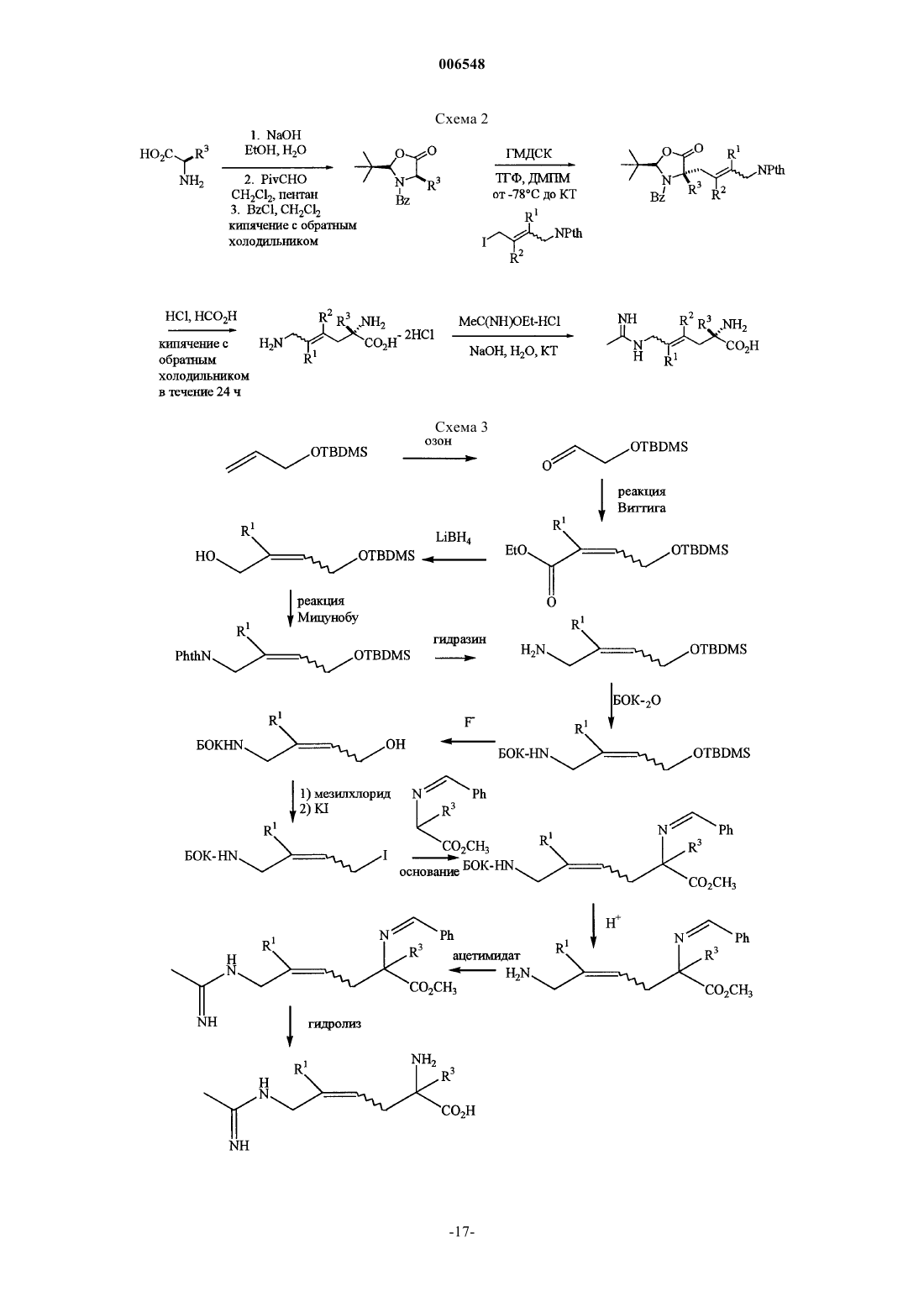
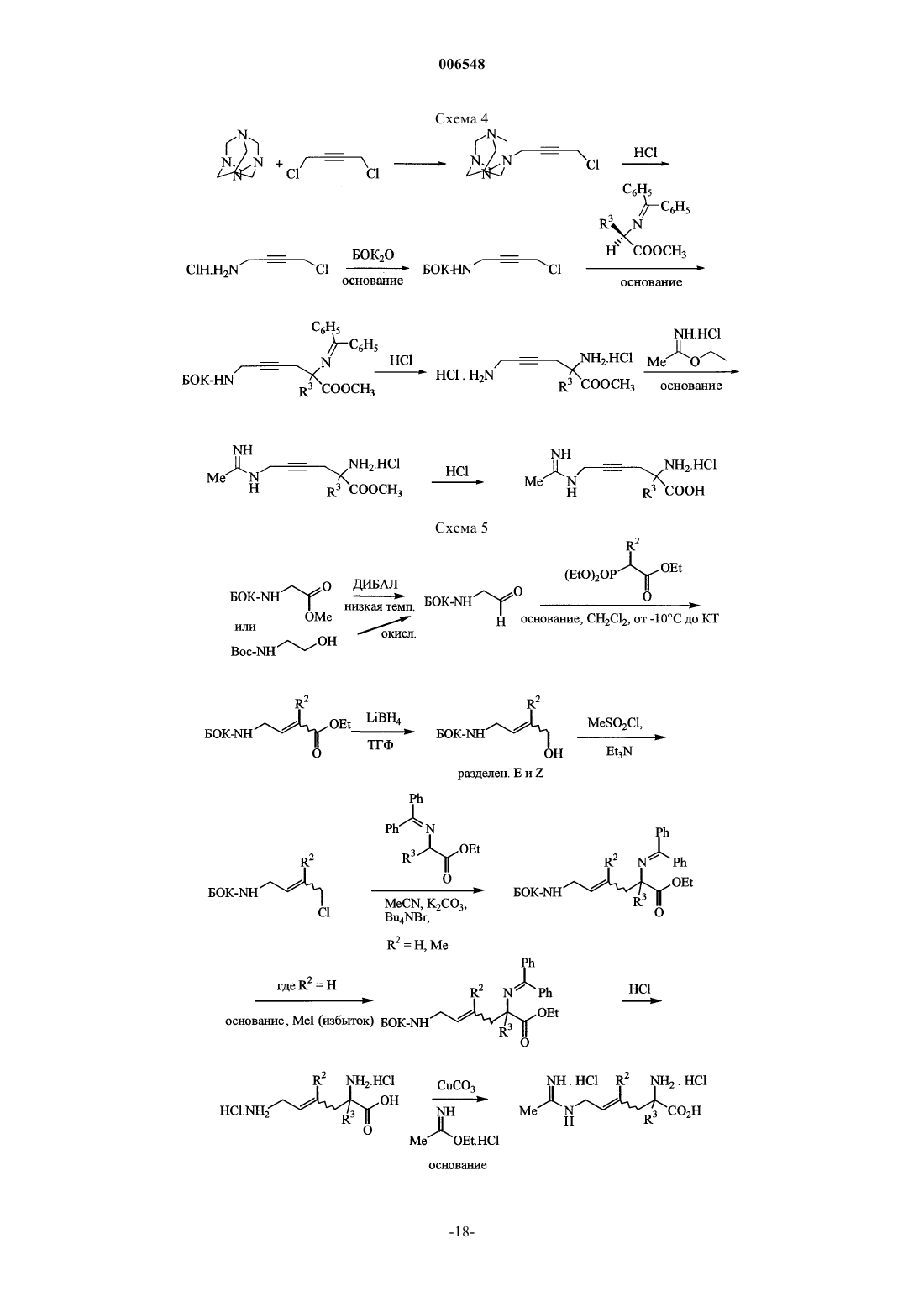
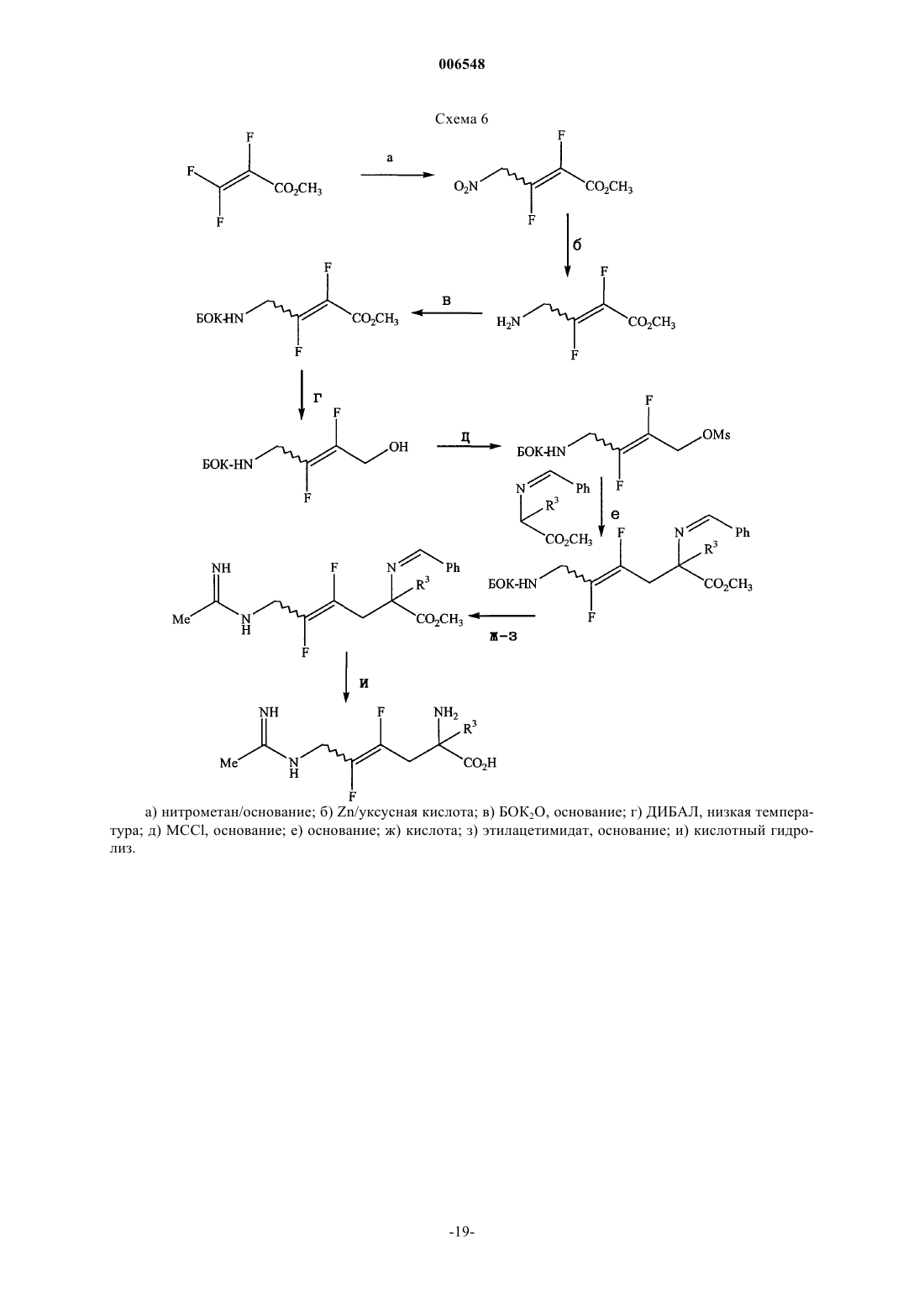
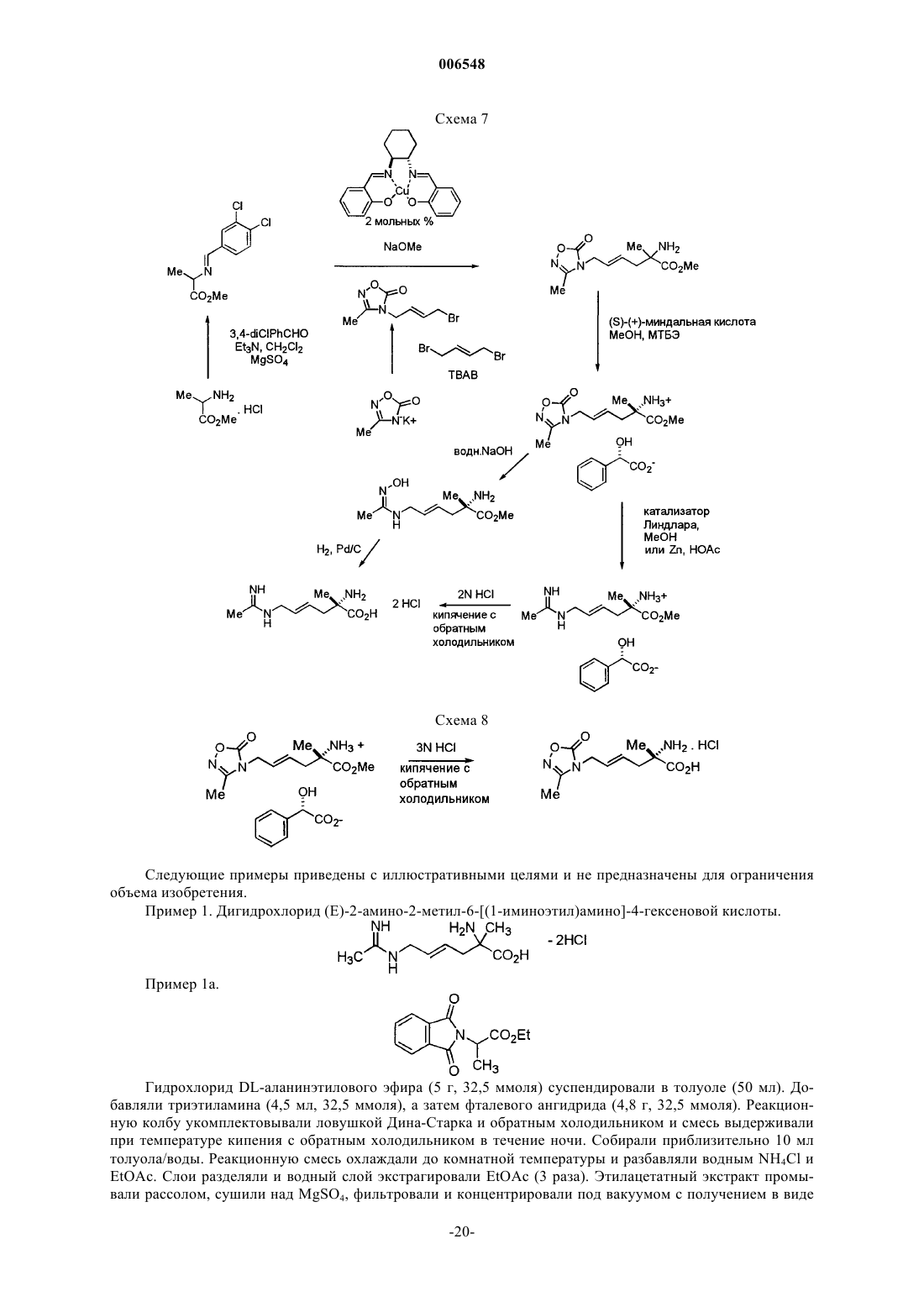
Производные 2-амино-2-алкил-4-гексеновой и -гексиновой кислот, которые могут быть использованы в качестве ингибиторов синтетазы оксида азота
Номер патента: 6548
Опубликовано: 24.02.2006
Авторы: Промо Мишел А., Уэббер Роналд Кит, Дарли Ричард С., Авасти Алок К., Морман Алан Э., Сикорски Джеймс, Питзеле Барнетт С., Хансен Доналд Джр.
Формула / Реферат
1. Соединение формулы I
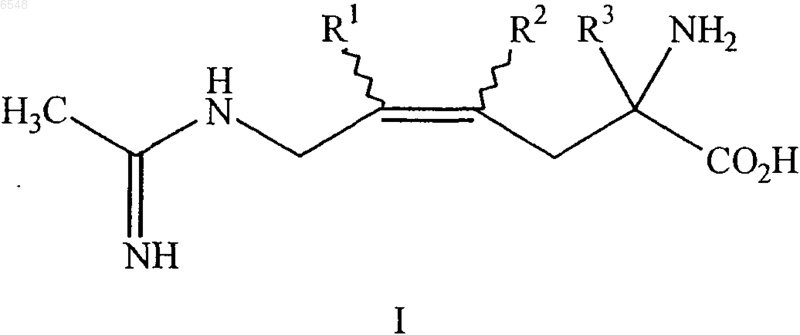
или его фармацевтически приемлемая соль, где
R1 означает водород;
R2 означает водород; а
R3 означает метил и
волнистые линии означают, что соединение может находиться в виде E- или Z-изомеров.
2. Соединение по п.1, где это соединение представляет собой Z-изомер.
3. Соединение по п.1, где это соединение представляет собой E-изомер.
4. Соединение формулы II
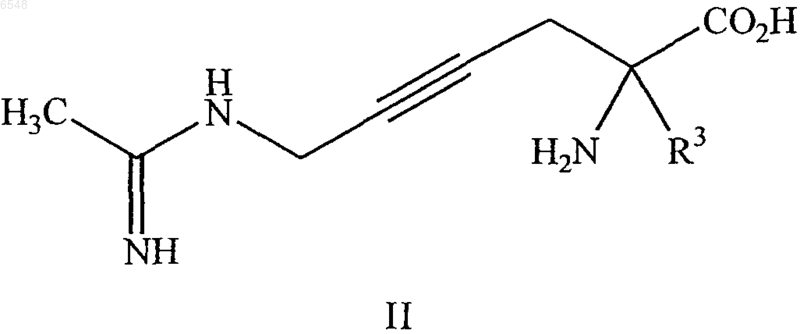
или его фармацевтически приемлемая соль, где R3 означает метил.
5. Соединение формулы III

или его фармацевтически приемлемая соль, где
R1 означает водород;
R2 означает водород; а
R3 означает метил; и
волнистые линии означают, что соединение может находиться в виде E- или Z-изомеров.
6. Соединение по п.5, где это соединение представляет собой Z-изомер.
7. Соединение по п.5, где это соединение представляет собой E-изомер.
8. Соединение формулы IV

или его фармацевтически приемлемая соль, где R3 означает метил.
9. Соединение формулы V
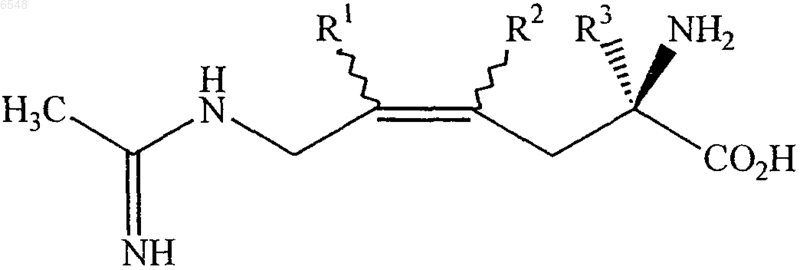
![]()
или его фармацевтически приемлемая соль, где
R1 означает водород;
R2 означает водород;а
R3 означает метил; и
волнистые линии означают, что соединение может находиться в виде E- или Z-изомеров.
10. Соединение по п.9, где это соединение представляет собой Z-изомер.
11. Соединение по п.9, где это соединение представляет собой E-изомер.
12. Соединение формулы VI
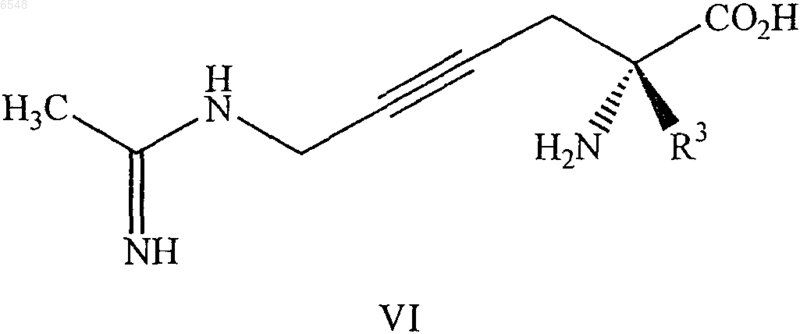
или его фармацевтически приемлемая соль, где R3 означает метил.
13. Соединения общей формулы
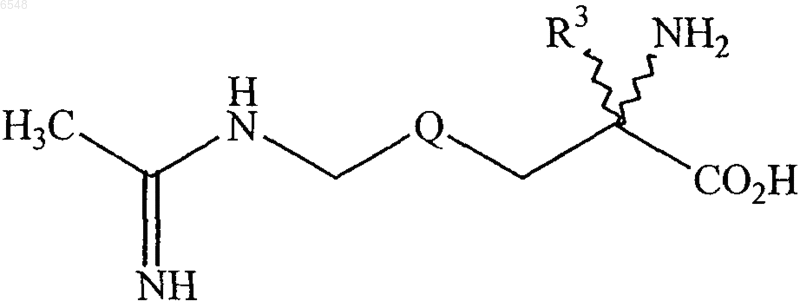
где
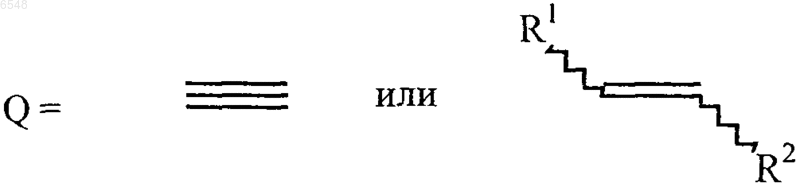
и R1, R2 и R3 имеют указанные в п.1 значения,
или их фармацевтически приемлемые соли, выбранные из группы, включающей
(E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(R,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексиновую кислоту;
(S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(2S,4E)-2-амино-2-метил-6-(3-метил-5-оксо-1,2,4-оксадиазол-4(5H)-ил)гекс-4-еновую кислоту;
дигидрохлорид (E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид (R,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид (S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид 2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексиновой кислоты;
дигидрохлорид (S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты и
гидрохлорид (2S,4E)-2-амино-2-метил-6-(3-метил-5-оксо-1,2,4-оксадиазол-4(5H)-ил)гекс-4-еновой кислоты.
14. Фармацевтическая композиция, содержащая по меньшей мере одно соединение, выбранное из группы, включающей
(E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(R,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексиновую кислоту;
(S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновую кислоту;
(2S,4E)-2-амино-2-метил-6-(3-метил-5-оксо-1,2,4-оксадиазол-4(5H)-ил)гекс-4-еновую кислоту;
(2S,5E)-2-амино-6{[(1Z-N-гидроксил)этанимидоил]амино}-2-метилгекс-4-еновую кислоту;
дигидрохлорид (E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид (R,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид (S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты;
дигидрохлорид 2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексиновой кислоты;
дигидрохлорид (S,E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты и
гидрохлорид (2S,4E)-2-амино-2-метил-6-(3-метил-5-оксо-1,2,4-оксадиазол-4(5H)-ил)гекс-4-еновой кислоты.
Текст
006548 Перекрестные ссылки на родственные заявки Объектом данной заявки является усовершенствование объекта предварительной заявки на патент США 60/232683, поданной 15 сентября 2000 г. Область техники, к которой относится изобретение Настоящее изобретение относится к производным 2-амино-2-алкил-4-гексеновой и -гексиновой кислот и к их применению в терапии, в частности к их применению в качестве ингибиторов синтетазы оксида азота. Существующий уровень техники С начала 1980-х гг. известно, что сосудистая релаксация, вызванная ацетилхолином, зависит от сосудистого эндотелия. Эндотелийзависимый релаксирующий фактор (EDRF), который в настоящее время известен как оксид азота (NO), генерируется в сосудах эндотелия синтетазой оксида азота (NOS). Активность NO как сосудорасширяющего фактора известна намного больше 100 лет. Кроме того, NO является активным соединением, образующимся из амилнитрита, глицирилтринитрата и других сосудорасширяющих нитросоединений. Идентификация EDRF как NO совпадает с открытием биохимического пути,по которому NO синтезируется из аминокислоты L-аргинина с помощью NO-синтетазы. Оксид азота представляет собой эндогенный стимулятор растворимой гуанилатциклазы. В дополнение к эндотелийзависимой релаксации, NO вовлекается в ряд биологических процессов, включая цитотоксичность фагоцитарных клеток и осуществление связи между клетками в центральной нервной системе. Существуют по крайней мере три следующих типа NO-синтетаз:(I) конститутивный, Са/кальмодулинзависимый фермент, локализованный в эндотелии, который высвобождает NO в ответ на рецепторную или физическую стимуляцию,(II) конститутивный, Са/кальмодулин зависимый фермент, локализованный в мозге, который высвобождает NO в ответ на рецепторную или физическую стимуляцию,(III) Са независимый фермент, который индуцируется после активации гладкой сосудистой мускулатуры, макрофагов, эндотелиальных клеток и ряда других клеток эндотоксинами и цитокинами. Другими словами, эта индуцируемая синтетаза оксида азота (в настоящем описании "iNOS") непрерывно в течение длительного периода времени генерирует NO. Высвобожденный каждым из двух конститутивных ферментов NO действует по механизму трансдукции, лежащему в основе нескольких физиологических реакций. NO, продуцируемый индуцируемым ферментом, представляет собой цитотоксическую молекулу для опухолевых клеток и инфицирующих микроорганизмов. Оказывается также, что обратное действие продуцирования избытка NO, в частности при патологическом расширении сосудов и повреждении тканей, может быть в значительной степени обусловлено NO, синтезированным под действием iNOS. Увеличивается число доказательств того, что NO может вовлекаться в процессы дегенерации хрящей, которые имеют место при некоторых состояниях, таких как артриты, и также известно, что при ревматоидном артрите и остеоартрите синтез NO возрастает. Некоторые ингибиторы NO-синтетазы, предложенные для терапевтического применения, действуют неселективно, они ингибируют и конститутивные, и индуцируемую NO-синтетазу. Применение такого неселективного ингибитора NO-синтетазы требует большой осмотрительности чтобы избежать потенциально серьезных последствий чрезмерного ингибирования конститутивной NO-синтетазы, таких как гипертензия, возможные тромбоз и повреждение тканей. В частности, в случае терапевтического применения L-NMMA (неселективный ингибитор NO-синтетазы) при лечении токсического шока рекомендуют осуществлять у пациента непрерывный мониторинг кровяного давления в течение всего периода лечения. Таким образом, хотя неселективные ингибиторы NO-синтетазы обладают терапевтической полезностью, если их использовать с соответствующей предосторожностью, селективные ингибиторы NOсинтетазы, в том смысле, что они ингибируют индуцируемую NO-синтетазу в значительно большей степени, чем конститутивные изоформы NO-синтетазы, должны быть гораздо более полезны как терапевтические средства и более удобны для применения (S.Moncada и E.Higgs, FASEB J., 9, 1319-1330, 1995). В международной публикации РСТWO 93/13055 и патенте США 5132453, содержание которых в полном объеме включено в настоящее описание в качестве ссылок, описаны соединения, которые ингибируют синтез оксида азота и преимущественно ингибируют индуцируемую изоформу синтетазы оксида азота. В международной публикации РСТWO 95/25717 описаны некоторые амидиновые производные как приемлемые для использования при ингибировании индуцируемой синтетазы оксида азота. Были предприняты самые разнообразные попытки с целью улучшить эффективность и селективность ингибиторов NOS добавлением в структуру ингибитора одного или нескольких жестких элементов. В публикациях Y.Lee и др., [Bioorg.Med.Chem. 7, 1097 (1999)] и R.J.Young и др. [Bioorg. Med. Chem.Lett. 10, 597, (2000)] говорится, что усиление конформационной жесткости с помощью одной или нескольких углерод-углерод двойных связей не является благотворным подходом к усилению селективности ингибиторов NOS.-1 006548 Краткое изложение сущности изобретения К настоящему времени найдены соединения, которые обладают преимуществом как очень эффективные в испытаниях на эксплантате хрящей человека, служащем моделью остеоартрита. Создание настоящего изобретения показывает, что углерод-углеродные двойные связи могут быть использованы в качестве элемента жесткости, а образующиеся соединения проявляют неожиданную эффективность и селективность при ингибировании индуцируемой NOS. Создание настоящего изобретения показывает, что углерод-углеродные двойные связи обуславливают благоприятное взаимодействие с индуцируемой NOS, в результате чего образующиеся соединения обладают неожиданными эффективностью и селективностью при ингибировании индуцируемой NOS в сравнении с проявляемой конститутивными изоформами. Более того, соединения по настоящему изобретению обладают тем преимуществом, что являются очень эффективными ингибиторами iNOS в опыте на эксплантате хряща человека-модели для остеоартрита. В то же самое время соединения по настоящему изобретению обладают неожиданно более низкой способностью проникать в не целевые органы в испытываемых системах, в особенности по сравнению с соединениями, предлагаемыми в WO 93/13055. Это неожиданное различие в предполагаемой доступности между целевым органом (хрящ) и другими органами создает неожиданное преимущество для соединений по настоящему изобретению. В общем по настоящему изобретению предлагаются соединения, отвечающие формуле или их фармацевтически приемлемые соли, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В одном из вариантов, представленном формулой I, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало,С 1-С 5 алкил и С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В одном варианте, представленном формулой II, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало.-2 006548 В варианте, представленном формулой III, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало,С 1-С 5 алкил и С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В варианте, представленном формулой IV, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В варианте, представленном формулой V, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В варианте, представленном формулой VI, объектом изобретения являются соединения или их фармацевтически приемлемые соли, гдеR3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В общем объектом настоящего изобретения являются новые соединения, фармацевтические композиции, способ получения новых соединений, способ приготовления фармацевтических композиций и способы применения этих соединений и композиций для подавления или модуляции синтеза оксида азота у субъекта, нуждающегося в таком подавлении или модуляции, введением в организм соединения,которое преимущественно подавляет или модулирует индуцируемую изоформу синтетазы оксида азота в сравнении с конститутивными изоформами синтетазы оксида азота. Кроме того, другим объектом настоящего изобретения является снижение уровня оксида азота у субъекта, нуждающегося в таком снижении. Предлагаемые соединения обладают способностью эффективно ингибировать синтетазу оксида азота, и, как полагают, они могут быть использованы при лечении или профилактике заболеваний или состояний, значительный вклад в развитие которых обусловлен синтезом или чрезмерным синтезом форм оксида азота. Соединения по настоящему изобретению могут быть использованы, среди прочего, при лечении у субъекта воспаления или лечении других расстройств, медиатором которых является синтетаза оксида азота, таких, как анальгетическое действие при лечении боли и головной боли. Соединения по настоя-3 006548 щему изобретению могут быть использованы при лечении болей, включая соматогенные (либо ноцирецепторные, либо невропатичные), как острых, так и хронических, и могут быть использованы в ситуации, включающей невропатичные боли, при которых традиционно вводят общий NSAID, опиоидные анальгетики или некоторые противосудорожные средства. Объемом настоящего изобретения охватываются новые промежуточные продукты, которые могут быть использованы для синтеза соединений по настоящему изобретению. Состояния, при которых соединения по настоящему изобретению проявляют преимущества при ингибировании продуцирования NO из L-аргинина, включают артритные состояния. Так, например, соединения по настоящему изобретению могут быть использованы при лечении артрита, включая, хотя ими их список не ограничен, ревматоидный артрит, спондилоартропатию, подагрический артрит, остеоартрит,системную красную волчанку, ювенильный артрит, острый суставной ревматизм, энтеропатический артрит, нейропатический артрит, псориатический артрит и пиогенный артрит. Более того, соединения по изобретению могут быть использованы при лечении астмы, бронхита,менструальных спазм, (например, дисменорреи), при преждевременных родах, тендините, бурсите, при кожно-связанных состояниях, таких, как псориаз, экзема, ожоги, солнечная эритема, дерматит, при панкреатите, гепатите и послеоперационном воспалении, включая воспаление после офтальмической операции, такой, как операция по поводу катаракты и операции, относящейся к рефракции. Соединения по изобретению также могут быть использованы при лечении желудочно-кишечных состояний, таких как воспалительное заболевание кишок, болезнь Крона, гастрит, синдром раздраженной толстой кишки и неспецифический язвенный колит. Соединения по изобретению могут быть использованы при лечении воспаления и повреждения ткани, при таких заболеваниях, как сосудистые заболевания, головная боль, узелковый периартерит, тиреоидит, гипопластическая анемия, болезнь Ходжкина, склеродом, ревматическая атака, диабет типа I, болезнь нервно-мышечного соединения, включая тяжелую миастению, заболевание белого вещества мозга,включая рассеянный склероз, саркоидоз, нефротический синдром, болезнь Бехчета, полимиозит, гингивит, нефрит, аллергию, опухоли в результате ранения, ишемию сердца и т.п. Такие соединения могут быть также использованы при лечении офтальмологических заболеваний, таких как глаукома, ретинит,ретинопатия, увеит, глазная фотофобия и воспаления, и боли, связанной с острыми повреждениями тканей глаза. Из применений предлагаемых по изобретению соединений особый интерес представляет лечение глаукомы, в особенности когда симптомы глаукомы вызваны продуцированном оксида азота, например при повреждении нерва, медиированном оксидом азота. Эти соединения также могут быть использованы при лечении воспаления легких, такого, которое связано с вирусной инфекцией и муковисцидозом. Соединения также могут быть использованы при лечении некоторых расстройств центральной нервной системы, таких, как кортикальное слабоумие, включая болезнь Альцгеймера, и повреждение центральной нервной системы в результате удара, ишемии и травмы. Эти соединения могут быть также использованы при лечении аллергического ринита, респираторного дистресс-синдрома, эндотоксинового бактериально-токсического шока и атеросклероза. Соединения могут быть также использованы при лечении боли, включая, хотя ими их список не ограничен, послеоперационные боли, зубную боль, мышечную боль, боль, вызванную височно-нижнечелюстным суставным синдромом, и боли при раке. Соединения могут быть использованы для предупреждения слабоумия, как при болезни Альцгеймера. Помимо эффективности этих соединений при лечении человека, они могут быть также использованы в ветеринарии при лечении домашних животных, экзотических животных и сельскохозяйственных животных, включая млекопитающих и других позвоночных. Более предпочтительные животные включают лошадей, собак и кошек. Предлагаемые соединения могут быть также использованы в совместной терапии, частично или полностью вместо других общепринятых терапевтических противовоспалительных средств, в частности совместно со стероидами, NSAIDs, селективными ингибиторами СОХ-2, ингибиторами основных металлопротеиназ, ингибиторами 5-липоксигеназ, ингибиторами антагонистов LTB4 и гидролаз LTA4. Другие состояния, при которых соединения по настоящему изобретению могут обладать преимуществом в ингибировании NO, включают сердечно-сосудистую ишемию, диабет (тип I или тип II), застойную сердечную недостаточность, миокардит, атеросклероз, мигрень, глаукому, аневризму аорты,рефлюкс-эзофагит, диарею, синдром раздраженной толстой кишки, муковисцидоз, эмфизему, астму,бронхоэктаз, гипералгезию (аллодинию), церебральную ишемию (как локализованную ишемию, тромботический шок, так и глобальную ишемию (например вторично к остановке сердца), множественный склероз и другие расстройства центральной нервной системы, медиированные NO, например болезнь Паркинсона. Другие нейродегеративные расстройства, при которых эффективным может оказаться ингибирование NO, включают нервные дегенерации и нервные некрозы, наблюдаемые при таких расстройствах, как гипоксия, гипогликемия, эпилепсия, и в случаях травмы центральной нервной системы (CNS)(такой, как травма спинного мозга и головы), гипербарические кислородные конвульсии и токсичность,слабоумие, например слабоумие, вызванное преждевременной старостью, и слабоумие, связанное сAIDS, кахексию, хорею Сиденгама, болезнь Хантингтона, боковой амиотрофический склероз, корсаковский психоз, слабоумие, связанное с нарушением церебральных сосудов, расстройство сна, шизофрению,-4 006548 депрессию или другие симптомы, связанные с предменструальным синдромом (PMS), страх и септический шок. Кроме того, другие расстройства или состояния, которые целесообразно лечить соединениями по настоящему изобретению, включают лечение, предотвращающее развитие толерантности к опиатам у пациентов, нуждающихся в продолжительном приеме опиатных анальгетиков, и толерантности к бензодиазепинам у пациентов, принимающих бензодиазепины, а также лечение других зависимостей, например лечение никотиновой зависимости, алкоголизма и расстройства питания. Соединения и способы по настоящему изобретению также могут быть полезны при лечении или профилактике симптомов, вызванных лекарственными средствами, например при лечении или профилактике симптомов, вызванных опиатами, алкоголем или табаком. Предлагаемые по изобретению соединения могут быть также использованы для предотвращения поражения тканей, когда терапевтическое лечение сочетают с антибактериальными или противовирусными препаратами. Соединения по настоящему изобретению также могут быть использованы при ингибировании продуцирования NO из L-аргинина, включая системную гипотензию, связанную с септическим и/или токсическим геморрагическим шоком, вызванным широким разнообразием препаратов, терапию цитокинами,такими как TNF, IL-1 и IL-2; и такими, как адъювант к короткоживущим иммунодепрессантам в трансплантатной терапии. Соединения по изобретению могут быть использованы для профилактики или лечения рака, такого как колоректальный рак, рак молочной железы, легкого, простаты, мочевого пузыря, шейки и кожи. Далее, объектом настоящего изобретения является применение соединений по настоящему изобретению при лечении и профилактике неоплазии. Неоплазия, которую обычно можно лечить или предупреждать с применением соединений и способов по настоящему изобретению, включает рак мозга, рак костей, лейкоз, такой как, например, хронический лимфолейкоз, лимфому, неоплазию, происходящую от эпителиальных клеток (эпительальная карцинома), такую как базалиома, аденокарцинома, желудочно-кишечный рак, такой как рак губы, рак рта, рак пищевода, рак тонкой кишки и рак желудка, рак толстой кишки, рак печени, рак мочевого пузыря, рак поджелудочной железы, рак мочеполовых органов, такой как рак яичника, цервикальный рак, рак наружных женских половых органов, рак легкого, рак молочной железы и рак кожи, такой как плоскоклеточный, меланома и базально-клеточный рак, рак простаты, почечноклеточный рак, и другие известные формы рака, которые воздействуют на эпителиальные клетки всего организма. Соединения по настоящему изобретению эффективны также при лечении мезенхимных производных неоплазии. Предпочтительнее лечить неоплазию, выбранную из желудочно-кишечного рака,рака печени, рака мочевого пузыря, рака поджелудочной железы, рака яичника, рака простаты, цервикального рака, рака наружных женских половых органов, рака легкого, рака молочной железы и рака кожи, такого как плоскоклеточный и базально-клеточный рак. Предлагаемые соединения и способы можно также применять при лечении фиброза, который наблюдается при лучевой терапии. Предлагаемые соединения и способы можно применять при лечении субъектов, страдающих аденоматозными полипами, включая лиц с врожденным семейным полипозом (FAP). Более того, предлагаемые соединения и способы можно применять для предупреждения полипов, образующихся у пациентов в результате рискаFAP. Объединенное лечение соединениями по настоящему изобретению совместно с другими противоопухолевыми средствами обычно приводит к синергическому эффекту или, в другом варианте, уменьшает токсическое побочное действие, связанное с химиотерапией, благодаря уменьшению терапевтической дозы средства, вызывающего побочное действие, необходимого для терапевтической эффективности,или непосредственно благодаря ослаблению симптомов побочного токсического действия, вызванного средством, способствующим побочному действию. Соединение по настоящему изобретению, кроме того,может быть использовано в качестве вспомогательного средства при радиотерапии для ослабления побочного действия или повышения эффективности. При выполнении настоящего изобретения другие средства, которые терапевтически можно объединять с соединением по настоящему изобретению, включают любые терапевтические средства, которые способны ингибировать фермент циклооксигеназу-2("СОХ-2"). В предпочтительном варианте такие ингибирующие СОХ-2 средства ингибируют СОХ-2 селективно относительно фермента циклооксигеназа-1 ("СОХ-1"). Такой ингибитор СОХ-2 известен как"селективный ингибитор СОХ-2". Более предпочтительное соединение по настоящему изобретению терапевтически можно совмещать с селективным ингибитором СОХ-2, когда селективный ингибитор СОХ-2 в опытах in vitro селективно ингибирует СОХ-2 при соотношении по крайней мере 10:1 относительно ингибирования СОХ-1, более предпочтительно при по крайней мере 30:1, а еще более предпочтительно при по крайней мере 50:1. Селективные ингибиторы СОХ-2, которые могут быть использованы в терапевтическом сочетании с соединениями по настоящему изобретению, включают целекоксиб, вальдекоксиб, деракоксиб, эторикоксиб, рофекоксиб, АВТ-963 [2-(3,4-дифторфенил)-4-(3-гидрокси-3-метил-1 бутокси)-5-[4-(метилсульфонил)фенил-3(2 Н)-пиридазинон, описанные в заявке РСТWO 00/24719] и мелоксикам. Соединение по настоящему изобретению можно также эффективно использовать в терапевтическом сочетании с пролекарством селективного ингибитора СОХ-2, например с парекоксибом.-5 006548 Другие химиотерапевтические средства, которые также могут быть использованы в сочетании с соединениями по настоящему изобретению, могут быть выбраны, например, из следующего не всеохватывающего и не ограничивающего списка. Альфа-дифторметилорнитин (DFMO), 5-FU-фибриноген, акантифолевая кислота, аминотиадиазол,натрийбрекинар, кармофур, CGP-30694 фирмы Ciba-Geigy, циклопентилцитозин, цитарабинфосфатостеарат, конъюгированный цитарабин, DATHF фирмы Lilly, DDFC фирмы Merrel Dow, дезагуанин, дидезоксицитидин, дидезоксигуанозин, дидокс, DMDC фирмы Yoshitomi, доксифлуридин, EHNA фирмыKyowa Hakko, UCN-1028 фирмы Kyowa Hakko, украин, USB-006 фирмы Eastman Kodak, винбластинсульфат, винкристин, виндезин, винэстрамид, винорелбин, винтриптол, винзолидин, витанолиды, YM534 фирмы Yamanouchi, урогуанилин, комбретастатин, доластатин, идарубицин, эпирубицин, эстрамустин, циклофосфамид, 9-амино-2-(S)-камптотецин, топотекан, иринотекан (камптозар), эксеместан, декапептил (трипторелин) и омега-3-жирная кислота. Примеры радиопротекторных агентов, которые могут быть использованы в совместной терапии с соединениями по настоящему изобретению, включают AD-5, адхнон, аналоги амифостина, детокс, димесну, 1-102, ММ-159, N-ацилированные дегидроаланины, TGF-Genentech, типротимод, амифостин, WR151327, FUT-187, трансдермальный кетопрофен, набуметон, супероксиддисмутазу (хирон) и супероксиддисмутазу Enzon. Соединения по настоящему изобретению могут быть также использованы при лечении или профилактике нарушений или состояний, связанных с развитием кровеносных сосудов, например с ростом опухоли, метастазами, дегенерацией желтого пятна и атеросклерозом. Еще в одном варианте по настоящему изобретению предлагаются также терапевтические сочетания для лечения или профилактики офтальмологических нарушений или состояний, таких, как глаукома. Например, соединения по настоящему изобретению целесообразно использовать в терапевтическом сочетании с лекарственным средством, которое снижает внутриглазное давление у пациента, пораженного глаукомой. Такие снижающие внутриглазное давление лекарственные средства включают, хотя ими их список не ограничен, латанопрост, травопрост, биматопрост и унопростол. Терапевтическое сочетание соединения по настоящему изобретению с лекарственным средством, снижающим внутриглазное давление, обычно эффективно, поскольку разные компоненты, как полагают, обеспечивают достижение своего эффекта воздействием на разные механизмы. В другом варианте выполнения настоящего изобретения предлагаемые по изобретению соединения могут быть использованы в терапевтическом сочетании с противогиперлипидимическими или холестеринпонижающими лекарственными средствами, такими, как бензотиепиновые или бензотиазепиновые противогиперлипидимические лекарственные средства. Примеры бензотиепиновых противогиперлипидимических лекарственных средств, которые могут быть использованы в терапевтическом сочетании по настоящему изобретению, можно найти в патенте US5994391, который включен в настоящее описание в качестве ссылки. Некоторые бензотиазепиновые противогиперлипидимические лекарственные средства описаны в WO 93/16055. По другому варианту противогиперлипидимическое или холестеринпонижающее лекарственное средство, которое может быть использовано в сочетании с соединением по настоящему изобретению, может быть ингибитором редуктазы HMG Со-А. Примеры ингибиторов редуктазы HMG Со-А, которые могут быть использованы в предлагаемом терапевтическом сочетании,включают по отдельности бенфлуорекс, флувастатин, ловастатин, провастатин, симвастин, аторвастин,церивастин, бервастин, ZD-9720 (описан в заявке РСТWO 97/06802), ZD-4522 (CAS147098-20-2 для кальциевой соли; CAS147098-18-8 для натриевой соли; описаны в ЕР 521471), BMS 180431(CAS129829-03-4) и NK-104 (CAS141750-63-2). Терапевтическое сочетание соединения по настоящему изобретению с противогиперлипидемическим или холестеринпонижающим лекарственным средством обычно эффективно, например, при снижении риска образования атеросклеротических повреждений в кровеносных сосудах. Так, например, атеросклеротические повреждения часто начинаются в кровеносных сосудах с воспаленных участков. Установлено, что противогиперлипидимическое или холестеринпонижающее лекарственное средство уменьшает риск образования атеросклеротических повреждений благодаря понижению уровня липидов в крови. Не ограничивая объем изобретения единственным механизмом действия, полагают, что один путь действия соединений предлагаемого сочетания-7 006548 состоит во взаимодействии, обеспечивающем улучшенное предотвращение атеросклеротических повреждений, например за счет ослабления воспаления кровеносных сосудов с одновременным понижением уровня липидов в крови. В другом варианте выполнения изобретения предлагаемые соединения могут быть использованы в сочетании с другими соединениями или терапевтическими приемами для лечения состояний или нарушений центральной нервной системы, таких как мигрень. Так, например, предлагаемые соединения могут быть использованы в терапевтическом сочетании с кофеином, агонистом 5-HT-1B/1D (например, с триптаном, таким, как суматриптан, наратриптан, золмитриптан, ризатриптан, алмотриптан и фроватриптан), антагонистом допамина D4 (например, с сонепипразолом), аспирином, ацетаминофеном, ибупрофеном, индометацином, натрийнапроксеном, изометептеном, дихлоральфеназоном, бутальбиталом,алкалоидом спорыньи (например, с эрготамином, дигидроэрготамином, бромкриптином, эргоновином или метилэргоновином), трициклическим антидепрессантом (например, с амитриптилином или нортриптилином), серотонергическим антагонистом (например, с метисергидом или ципрогептадином), бетаандренергическим антагонистом (например, с пропранололом, тимололом, атенололом, надололом или метпрололом) или ингибитором моноаминоксидазы (например, с фенелзином или изокарбоксазидом). По еще одному варианту предлагается терапевтическое сочетание соединения по настоящему изобретению с опиоидным соединением. Опиоидные соединения, которые могут быть использованы в таком сочетании, включают, хотя ими их список не ограничен, морфин, метадон, гидроморфон, оксиморфон,леворфанол, леваллорфан, кодеин, дигидрокодеин, дигидрогидроксикодеинон, пентазоцин, гидрокодон,оксикодон, налмефин, эторфин, леворфанол, фентанил, суфентанил, DAMGO, буторфанол, бупренорфин,налоксон, налтрексон, СТОР, дипренорфин, бета-фуналтрексамин, налоксоназин, налорфин, пентазоцин,налбуфин, налоксонбензоилгидразон, бремазоцин, этилкетоциклазоцин, U50,488, U69,593, спирадолин,норбиналторфимин, налтриндол, DPDPE, [D-ла 2,глу 2]делторфин, DSLET, метэнкефалин, лейэнкафалин,бета-эндорфин, динорфин А, динорфин В и альфа-неоэндорфин. Преимущество сочетания по настоящему изобретению с опиодным соединением состоит в том, что применение предлагаемых по настоящему изобретению соединений обычно дает возможность уменьшить дозу опиоидного соединения, снижая тем самым опасность или жесткость побочного действия опиоидов, такого как привыкание к опиодным препаратам. Подробное описание изобретения В общем объектом настоящего изобретения являются соединения, отвечающие формуле или их фармацевтически приемлемые соли, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало; аR3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В варианте, представленном формулой I, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало; аR3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало.-8 006548 В одном варианте объектом настоящего изобретения, представленном формулой I, таким соединением является изомер Z. В другом варианте выполнения настоящего изобретения, представленном формулой I, этим соединением является изомер Е. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулой I,R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало; R2 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало; а R3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен атомом фтора или алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, аR3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 3 алкил. Однако еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает водородный атом или гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает атом фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает гало, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает C1-С 3 алкил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает гало, R2 обозначает гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает атом фтора, R2 обозначает атом фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает атом фтора, R2 обозначает водородный атом или С 1-С 3 алкил, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает атом фтора, R2 обозначает водородный атом, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает метил, R2 обозначает водородный атом, a R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает метил и R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает метил, R2 обозначает метил и R3 обозначает метил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулой I,R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, R2 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, а R3 обозначает метил, необязательно замещенный одним или несколькими алкокси или гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает атом водорода или фтора, R2 обозначает С 1-С 3 алкил, замещенный одним или несколькими гало, аR3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает CH2F, a R3 обозначает метил. Однако в другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает CH2F, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает CH2F. В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает метоксиметил, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает метоксиметил, R2 обозначает водородный атом, а R3 обозначает метил.-9 006548 В другом варианте выполнения настоящего изобретения, представленном формулой I, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метоксиметил. В одном из вариантов, представленном формулой II, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими атомами фтора. Однако в другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метил, замещенный одним или несколькими гало. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойII, R3 обозначает метил, замещенный одним или несколькими атомами фтора. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает CH2F. Однако в другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метоксиметил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойII, R3 обозначает С 1-С 5 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метил. В одном из вариантов, представленном формулой III, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В одном варианте выполнения настоящего изобретения, представленном формулой III, этим соединением является изомер Z. В другом варианте выполнения настоящего изобретения, представленном формулой III, этим соединением является изомер Е. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойIII, R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало, R2 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало, а R3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен атомом фтора или алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а-10 006548 В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1 С 3 алкил. Однако еще в одном варианте выполнения настоящего изобретения, представленном формулой III,R1 обозначает водородный атом, R2 обозначает водородный атом или гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает атом фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает гало, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 3 алкил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает гало, R2 обозначает гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает атом фтора, R2 обозначает атом фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает атом фтора, R2 обозначает водородный атом или С 1-С 3 алкил, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает атом фтора, R2 обозначает водородный атом, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает метил, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом; R2 обозначает метил и R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает метил, R2 обозначает метил и R3 обозначает метил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойIII, R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, R2 обозначает водородный атом, гало или С 1-С 5 алкил,этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, a R3 обозначает метил, необязательно замещенный одним или несколькими алкокси или гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает атом водорода или фтора, R2 обозначает С 1-С 3 алкил, замещенный одним или несколькими гало, аR3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает CH2F, a R3 обозначает метил. Однако в другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает CH2F, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает СН 2F. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает метоксиметил, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает метоксиметил, R2 обозначает водородный атом, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой III, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метоксиметил. В одном из вариантов, представленном формулой IV, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими атомами фтора.-11 006548 Однако в другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метил, замещенный одним или несколькими гало. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойII, R3 обозначает метил, замещенный одним или несколькими атомами фтора. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает CH2F. Однако в другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает С 1-С 5 алкил, замещенный алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метоксиметил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойII, R3 обозначает С 1-С 5 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой II, R3 обозначает метил. В одном варианте, представленном формулой V, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR1 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R2 имеет значения, выбранные из группы, включающей водородный атом, гало, С 1-С 5 алкил и С 1 С 5 алкил, замещенный алкокси или одним или несколькими гало;R3 обозначает С 1-С 5 алкил или С 1-С 5 алкил, замещенный алкокси или одним или несколькими гало. В одном варианте выполнения настоящего изобретения, представленном формулой V, этим соединением является изомер Z. В другом варианте выполнения настоящего изобретения, представленном формулой V, этим соединением является изомер Е. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойV, R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало, R2 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен гало или алкокси, этот алкокси необязательно замещен одним или несколькими гало, а R3 обозначает С 1-С 5 алкил, причем этот С 1 С 5 алкил необязательно замещен гало или алкокси. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен атомом фтора или алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, гало или С 1-С 3 алкил, R2 обозначает водородный атом, гало или С 1-С 3 алкил, аR3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1 С 3 алкил. Однако еще в одном варианте выполнения настоящего изобретения, представленном формулой V,R1 обозначает водородный атом, R2 обозначает водородный атом или гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает атом водорода или фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает атом фтора, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает гало, R2 обозначает водородный атом, гало или С 1-С 3 алкил, а R3 обозначает С 1-С 3 алкил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает гало, R2 обозначает гало, а R3 обозначает С 1-С 3 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает атом фтора, R2 обозначает атом фтора, а R3 обозначает метил.-12 006548 В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает атом фтора, R2 обозначает водородный атом или С 1-С 3 алкил, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает атом фтора, R2 обозначает водородный атом, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает метил, R2 обозначает водородный атом, а R3 обозначает метил. В еще одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает метил и R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает метил, R2 обозначает метил и R3 обозначает метил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойV, R1 обозначает водородный атом, гало или С 1-С 5 алкил, этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, R2 обозначает водородный атом, гало или С 1-С 5 алкил,этот С 1-С 5 алкил необязательно замещен алкокси или одним или несколькими атомами фтора, а R3 обозначает метил, необязательно замещенный одним или несколькими алкокси или гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает атом водорода или фтора, R2 обозначает С 1-С 3 алкил, замещенный одним или несколькими гало, аR3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает CH2F, a R3 обозначает метил. Однако в другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает CH2F, R2 обозначает водородный атом, а R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает CH2F. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает метоксиметил, a R3 обозначает метил. Еще в одном варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает метоксиметил, R2 обозначает водородный атом, а R3 обозначает метил. В другом варианте выполнения настоящего изобретения, представленном формулой V, R1 обозначает водородный атом, R2 обозначает водородный атом, а R3 обозначает метоксиметил. В одном варианте, представленном формулой VI, объектом изобретения является соединение или его фармацевтически приемлемая соль, гдеR3 обозначает С 1-С 3 алкил или С 1-С 3 алкил, замещенный алкокси или одним или несколькими гало. В другом варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими гало. Еще в одном варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает С 1-С 5 алкил, замещенный одним или несколькими атомами фтора. Однако в другом варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает метил, замещенный одним или несколькими гало. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойVI, R3 обозначает метил, замещенный одним или несколькими атомами фтора. В другом варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает CH2F. Однако в другом варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает С 1-С 5 алкил, замещенный алкокси. Еще в одном варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает метоксиметил. Тем не менее в другом варианте выполнения настоящего изобретения, представленном формулойVI, R3 обозначает С 1-С 5 алкил. В другом варианте выполнения настоящего изобретения, представленном формулой VI, R3 обозначает метил. Объем настоящего изобретения охватывает также фармацевтические композиции, которые включают соединение формулы I, II, III, IV, V или VI. Способы применения соединения формулы I, II, III, IV, V или VI включают ингибирование синтеза оксида азота у субъекта, нуждающегося в таком ингибировании, путем введения терапевтически эффек-13 006548 тивного количества предлагаемого соединения, которое селективно ингибирует синтез оксида азота,продуцируемого индуцируемой синтетазой оксида азота, относительно оксида азота, продуцируемого конститутивными формами синтетазы оксида азота у субъекта, нуждающегося в таком ингибировании,путем введения терапевтически эффективного количества соединения формулы I, II, III, IV, V или VI,снижающего уровень оксида азота у субъекта, нуждающегося в таком введении терапевтически эффективного количества соединения формулы I, II, III, IV, V или VI, понижающего уровень оксида азота у субъекта, нуждающегося в таком введении терапевтически эффективного количества фармацевтической композиции, включающей соединение формулы I, II, III, IV, V или VI. Соединения по настоящему изобретению могут быть также эффективно использованы в сочетании со вторым фармацевтически активным веществом, в частности с селективным ингибитором индуцируемой изоформы циклооксигеназы (СОХ-2). Таким образом, в другом варианте выполнения изобретения предлагается применение предлагаемого соединения или его фармацевтически приемлемой соли в сочетании с ингибиром СОХ-2 при лечении воспаления, воспалительного заболевания и связанных с воспалением расстройств. Кроме того, предлагается способ лечения или снижения риска воспаления, воспалительного заболевания и связанных с воспалением расстройств у страдающего таким заболеванием или состоянием или подвергающегося опасности их возникновения пациента, причем этот способ включает введение пациенту терапевтически эффективного количества предлагаемого соединения или его фармацевтически приемлемой соли в сочетании с ингибиром СОХ-2. Примером ингибитора СОХ-2 является,хотя им их список не ограничен, целекоксиб Vioxx. Что касается ингибитора NOS и ингибитора СОХ-2,то их либо можно размещать в составе одной и той же фармацевтической композиции для введения в организм в виде изделий в дозах на один прием, либо каждый из этих компонентов размещать по отдельности в составе разных композиций таким образом, чтобы одновременно или последовательно вводить отдельными дозами. Понятие "алкил", взятое в отдельности или в сочетании, означает ациклический алифатический радикал, линейный или разветвленный, содержащий от 1 до 5 или от 1 до 3 углеродных атомов. Алкильные радикалы могут быть необязательно замещены одним или несколькими гало. Понятие "алкокси" охватывает линейные и разветвленные содержащие оксигруппы радикалы, каждый из которых включает алкильный фрагмент, содержащий от одного до пяти углеродных атомов, такой как метоксирадикал. Примеры таких радикалов включают метокси, этокси, пропокси, бутокси и трет-бутоксиалкилы. Понятие "гало" служит для обозначения галогенов, таких как атомы фтора, хлора, брома и иода. Семейство соединений формул I, II, III, IV, V и VI охватывает также их фармацевтически приемлемые соли. Понятие "фармацевтически приемлемые соли" охватывает соли, которые обычно используют для получения солей щелочных металлов и для получения аддитивных солей свободных кислот и свободных оснований. Природа такой соли решающего значения не имеет при условии, что она фармацевтически приемлема. Подходящие фармацевтически приемлемые кислотно-аддитивные соли соединений формул I, II, III, IV, V и VI могут быть получены из неорганической кислоты или из органической кислоты. Примерами таких неорганических кислот являются соляная, бромисто-водородная, иодистоводородная, азотная, карбоновые, серная и фосфорная кислоты. Соответствующие органические кислоты можно выбрать из органических кислот алифатического, циклоалифатического, ароматического, аралифатического, гетероциклического, карбонового и сульфонового классов, примерами которых служат муравьиная, уксусная, пропионовая, янтарная, гликолевая, глюконовая, молочная, яблочная, винная, лимонная, аскорбиновая, глюкороновая, малеиновая, фумаровая, пировиноградная, аспарагиновая, глутаминовая, бензойная, антраниловая, мезиловая, салициловая, п-гидроксибензойная, фенилуксусная, миндальная, эмбоновая (памовая), метансульфоновая, этилсульфоновая, бензолсульфоновая, сульфаниловая,стеариновая, циклогексиламиносульфоновая, альгеновая, галактуроновая кислоты. Подходящие фармацевтически приемлемые основно-аддитивные соли соединений формул I, II, III, IV, V и VI включают соли металлов, полученные из алюминия, кальция, лития, магния, калия, натрия и цинка, и органические соли, полученные из N,N'-дибензилэтилендиамина, холина, хлорпрокаина, диэтаноламина, этилендиамина, меглумина (N-метилглюкамина) и прокаина. Все эти соли могут быть получены с помощью обычных средств из соответствующих соединений формул I, II, III, IV, V и VI, например реакцией соответствующей кислоты или основания с соединением формулы I, II, III, IV, V или VI. Хотя для иллюстрации защитных групп азотного атома в качестве примера представлен третбутоксикарбонил, или трет-БОК, в синтезе соединений по настоящему изобретению для замещения можно было бы использовать любую приемлемую защитную группу для азотного атома. Многочисленные защищенные аминогруппы, которые могут быть использованы при выполнении настоящего изобретения,описаны в работе Theodora W. Greene и Peter G.M. Wuts (Protective Groups in Organic Synthesis, издание 3 е, John WileySons, New York, 1999, cc. 494-653). Так, например, NZ может быть 4 хлорбензилиминогруппой. В одном варианте выполнения настоящего изобретения защищенная аминогруппа представляет собой любую такую группу, которая образуется в результате реакции альдегида с соответствующей аминогруппой с получением шиффова основания. При выполнении настоящего изобретения для превращения промежуточного продукта в целевое соединение можно с успехом применять-14 006548 широкое разнообразие реагентов для удаления защитных групп. Множество таких реагентов для удаления защитных групп описано в вышеупомянутой работе Greene и Wuts. Так, например, когда защищенная аминогруппа представляет собой 4-хлорбензилиминогруппу или трет-бутоксикарбониламиногруппу,предпочтительный реагент для удаления защитной группы представляет собой кислоту. Некоторые эффективные кислотные агенты для удаления защитных групп включают без ограничений этими примерами соляную кислоту, бромисто-водородную кислоту, серную кислоту, трифторуксусную кислоту, фосфорную кислоту, фосфористую кислоту и уксусную кислоту. Когда соединение описывают как строением, так и наименованием, подразумевается, что это наименование соответствует указанному строению и точно так же такое строение соответствует приведенному наименованию. Хотя соединения формул I, II, III, IV, V и VI можно вводить в организм в виде сырых химических веществ, в предпочтительном варианте на их основе готовят фармацевтические композиции. В соответствии с еще одним объектом настоящего изобретения предлагается фармацевтическая композиция,включающая соединение формулы I, II, III, IV, V или VI или его фармацевтически приемлемую соль или сольват совместно с одним или несколькими фармацевтически приемлемыми носителями для него и необязательным одним или несколькими другими терапевтически эффективными компонентами. Носитель(носители) должен быть приемлемым в смысле совместимости с другими компонентами композиции и не причинять вреда реципиенту. Такие композиции включают те препараты, которые приемлемы для перорального, парентерального (включая подкожное, внутрикожное, внутримышечное, внутривенное и внутрисуставное), ректального и локального (включая кожное, внутриротовое, подъязычное и внутриглазное) введения в организм,хотя наиболее приемлемый путь может зависеть, например, от состояния и заболевания реципиента. Такие композиции могут быть эффективно приготовлены в форме доз на один прием, их можно готовить по любому из методов, которые хорошо известны в области фармации. Все методы включают стадию совмещения соединения формулы I, II, III, IV, V или VI или его фармацевтически приемлемой соли или сольвата с носителем, который включает один или несколько дополнительных компонентов. Обычно композиции готовят введением активного компонента в гомогенный и плотный контакт с жидкими носителями или тонко измельченными твердыми носителями, или и с теми, и другими с последующим, если необходимо, формованием композиции для придания ей целевой препаративной формы. Препараты из композиций по настоящему изобретению, приемлемые для перорального введения в организм, могут быть приготовлены в форме отдельных изделий, таких как капсулы, саше и таблетки,каждое из которых содержит заданное количество активного компонента, в виде порошка или гранул, в виде раствора или суспензии в водной жидкости или неводной жидкости, в виде эмульсии масла в водной жидкости или эмульсии воды в жидком масле. Активный компонент может также содержаться в виде болюса, электуария или пасты. Таблетку можно изготовить прессованием или формованием, необязательно вместе с одним или несколькими вспомогательными компонентами. Прессованные таблетки можно готовить прессованием в подходящей таблеточной машине активного компонента в легкосыпучей форме, такой как порошок или гранулы, необязательно смешанного со связующим веществом, скользящим веществом, инертным разбавителем, смазкой, поверхностно-активным или диспергирующим веществом. Формованные таблетки можно готовить формованием в подходящей таблеточной машине смеси порошкообразного соединения,смоченного инертным жидким разбавителем. На таблетки можно, что необязательно, наносить покрытия и надрезы, их можно готовить таким образом, чтобы обеспечить медленное или регулируемое высвобождение содержащегося в них активного компонента. Композиции для парентерального введения в организм включают водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферные добавки, бактериостатические вещества и растворенные вещества, которые придают композиции изотоничность с кровью потенциального реципиента, и водные и неводные стерильные суспензии, которые могут содержать суспендирующие агенты и сгустители. Такие композиции могут находиться в контейнерах для дозы на один прием или для множества доз, например в герметизированных ампулах и пузырьках, их можно хранить в высушенном вымораживанием (лиофилизированном) состоянии, в котором непосредственно перед применением требуется только добавление стерильного жидкого носителя, например солевого раствора, воды для инъекций. Растворы и суспензии для немедленного введения можно приготовить из стерильных порошков,гранул и таблеток вышеописанного типа. Композиции для ректального введения могут быть приготовлены в виде суппозиториев с обычными носителями, такими как масло какао или полиэтиленгликоль. Композиции для местного введения в полость рта, например трансбуккально или сублингуально,включают лепешки, содержащие активный компонент в основе с корригентом, такой как сахароза и гуммиарабик или трагакант, и пастилки, содержащие активный компонент в такой основе, как желатина и глицерин или сахароза и гуммиарабик.-15 006548 Предпочтительными композициями в дозах на один прием являются те, которые включают эффективную дозу, которая указана ниже в настоящем описании, или ее приемлемую долю активного компонента. Необходимо иметь в виду, что в дополнение к конкретно упомянутым выше компонентам композиции по настоящему изобретению могут включать другие обычные для данной области техники вещества с учетом типа конкретно рассматриваемой композиции. Так, например, те, которые пригодны для перорального введения, могут включать корригенты. Соединения по изобретению можно вводить в организм перорально или путем инъекций в ежедневной дозе от 0,001 до 2500 мг/кг. Интервал доз для взрослых людей обычно составляет от 0,005 мг до 10 г/день. Приемлемые таблетки или лекарства в других препаративных формах, приготовленных в виде отдельных изделий, могут содержать такое количество соединения по изобретению, которое эффективно в такой системе доз или в виде множества дробных доз, например как изделия, каждое из которых содержит от 0,5 до 200 мг, обычно от примерно 0,5 до 100 мг. В предпочтительном варианте соединения формул I, II, III, IV, V и VI вводят перорально или инъекциями (внутривенно или подкожно). За точное количество вводимого пациенту соединения обычно несет ответственность лечащий врач. Однако обычно используемая доза зависит от ряда факторов,включая возраст и пол пациента, конкретное заболевание, от которого проводят лечение, и его серьезность. Путь введения также может варьироваться в зависимости от состояния и его серьезности. Соединения по настоящему изобретению могут существовать в таутомерных, геометрических или стереоизомерных формах. По настоящему изобретению предусматриваются все такие соединения, включая цис- и трансгеометрические изомеры и их смеси. Е- и Z-геометрические изомеры и их смеси, R- и Sэнантиомеры, диастереоизомеры, d-изомеры, 1-изомеры, их рацемические смеси и другие их смеси, как охватываемые объемом изобретения. Объем изобретения включает также фармацевтически приемлемые соли таких таутомерных, геометрических или стереоизомерных форм. Понятиями "цис" и "транс" обозначают форму геометрической изомерии, в которой у каждого из двух углеродных атомов, связанных двойной связью, имеются по две группы высшего разряда с одной и той же стороны относительно двойной связи ("цис" или "Z") или с противоположных сторон относительно этой двойной связи ("транс" или "Е"). Некоторые из описанных соединений содержат алкенильные группы, а это означает, что они включают как цис-, так и транс-или "Z" и "Е" геометрические формы. Другие соединения по изобретению включают смеси как цис-/Z-, так и транс-/Е-изомеры. У описанных соединений имеются стереоцентры, а это значит, что они включают R-, S- и смеси Rи S-форм. Некоторые из описанных соединений включают геометрические изомеры, а это значит, что на каждый имеющийся стереоцентр они включают Е-, Z- и смеси Е- и Z-форм. При выполнении настоящего изобретения могут быть использованы следующие схемы. Когда изомеры не выделены, индивидуальные изомеры могут быть получены с помощью соответствующих хроматографических методов. Схема 1 Следующие примеры приведены с иллюстративными целями и не предназначены для ограничения объема изобретения. Пример 1. Дигидрохлорид (E)-2-амино-2-метил-6-[(1-иминоэтил)амино]-4-гексеновой кислоты. Гидрохлорид DL-аланинэтилового эфира (5 г, 32,5 ммоля) суспендировали в толуоле (50 мл). Добавляли триэтиламина (4,5 мл, 32,5 ммоля), а затем фталевого ангидрида (4,8 г, 32,5 ммоля). Реакционную колбу укомплектовывали ловушкой Дина-Старка и обратным холодильником и смесь выдерживали при температуре кипения с обратным холодильником в течение ночи. Собирали приблизительно 10 мл толуола/воды. Реакционную смесь охлаждали до комнатной температуры и разбавляли водным NH4Cl иEtOAc. Слои разделяли и водный слой экстрагировали EtOAc (3 раза). Этилацетатный экстракт промывали рассолом, сушили над MgSO4, фильтровали и концентрировали под вакуумом с получением в виде-20 006548 белого кристаллического твердого вещества с почти количественным выходом указанного в заглавии фталилзащищенного аминового эфира. 1 В 250-миллилитровую круглодонную колбу, содержавшую 1,4-бутендихлорид (25 г, 0,2 моля), вводили фталимид калия (18,5 г, 0,1 моля). Реакционную смесь выдерживали при 150 С в течение 1,5 ч. Смесь охлаждали до комнатной температуры и разделяли между рассолом и Et2O. Органический слой сушили MgSO4, фильтровали и концентрировали под вакуумом. Остаток перекристаллизовывали из горячего этанола с получением в виде оранжевых кристаллов указанного в заглавии 1-хлор-4 фталимидобутена (8,9 г, 39%-ный выход). МСВР, рассч. для C12H10ClNO2: m/z=236,0478 [М+Н]. Обнаруж.: 236,0449 (d, 2H), 5,9 (m, 2H), 7,7 Образец продукта примера 1 б (2,3 г, 9,8 ммоля) растворяли в ацетоне (50 мл). Добавляли NaI (3,2 г,21 ммоля) и смесь кипятили с обратным холодильником в течение ночи. После охлаждения до комнатной температуры добавляли Et2O и смесь последовательно промывали тиосульфатом натрия и рассолом. Органический слой сушили MgSO4, фильтровали и концентрировали под вакуумом с получением в виде светло-желтого твердого вещества указанного в заглавии иодида (2,8 г, 87,5%-ный выход), который использовали без дополнительной очистки. 1 Раствор ГМДСК (2,6 г, 13,3 ммоля) в ТГФ (50 мл) охлаждали до -78 С. Добавляли раствор продукта примера 1 а (2,2 г, 8,87 ммоля) в ТГФ (15 мл) и сразу же после этого добавляли 1,3-диметил-3,4,5,6 тетрагидро-2(1 Н)пиримидинон (ДМПМ, 1,0 мл, 8,87 ммоля). Далее раствор перемешивали при -78 С в течение 40 мин и добавляли раствор продукта примера 1 в (2,9 г, 8,87 ммоля) в ТГФ (15 мл). Колбу с холодной бани удаляли и содержимое перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь разделяли между насыщенным водным NaHCO3 и EtOAc. Органический экстракт промывали рассолом, сушили над MgSO4, фильтровали и концентрировали под вакуумом с получением в виде желтого твердого вещества целевого защищенного бисфталилом аминового эфира. Этот остаток хроматографировали на силикагеле (гексаны/EtOAc в соотношении 1:1) и в виде белого твердого вещества получали 1,4 г (35%-ный выход) указанного в заглавии продукта. 1 Продукт примера 1 г (0,78 г, 1,76 ммоля) растворяли в смеси муравьиной кислоты (10 мл, 95%-ная) и НСl (20 мл, концентрированная НСl) и кипятили с обратным холодильником в течение 3 дней. Реакционную смесь охлаждали до 0 С и фильтровали для удаления фталевого ангидрида. После концентрирования под вакуумом (Т 40 С) в виде белого твердого вещества получали указанный в заглавии ненасыщенный альфа-метиллизин (0,38 г, 95%-ный выход), который использовали без дополнительной очистки.H-ЯМР (300 МГц, D2O,част./млн): 1,4 (s, 3 Н), 2,4 (dd. 1H), 2,6 (dd, 1H), 3,5 (d, 2H), 5,7 (m, 2H). Масс-спектроскопия: (М+Н)=317. Пример 1 е. Продукт примера 1 д (0,2 г, 0,86 ммоля) растворяли в Н 2 О (8 мл) и с использованием 2,5 н. NaOH значение рН доводили до 9. Четырьмя порциями в течение 1 ч добавляли этилацетимидатНСl (0,42 г, 3,4 ммоля). По прошествии 1 ч 10%-ной НСl смесь подкисляли до рН 4 и концентрировали под вакуумом. Затем остаток пропускали через промытую водой колонку с DOWEX 50WX4-200 (смола в Н-форме, 0,5 н.NH4OH в качестве элюента). Остаток концентрировали под вакуумом, 10%-ной НСl подкисляли до рН 4 и концентрировали с получением в виде масла указанного в заглавии продукта (17 мг, 6%-ный выход). МСВР, рассч. для C9H17N3O2: m/z=200,1399 [М+Н]. Обнаруж.: 200,1417. 1 Раствор ГМДСК (0,65 г, 3,24 ммоля), ДМПМ (0,33 мл, 2,7 ммоля) и ТГФ (40 мл) охлаждали до -78 С. По каплям добавляли раствор (2S,4S)-3-бензоил-2-(трет-бутил)-4-метил-1,3-оксазолидин-5-она 5 а (0,70 г, 2,7 ммоля) в ТГФ (10 мл). По прошествии 45 мин добавляли раствор продукта примера 1 в (0,88 г, 2,7 ммоля) в ТГФ (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч и реакцию гасили насыщенным водным NaHCO3. Слои разделяли и водный слой экстрагировали EtOAc. Органические слои объединяли и промывали рассолом, сушили над MgSO4, фильтровали и концентрировали под вакуумом. Полученный продукт в виде желтого масла хроматографировали на силикагеле (гексаны/этилацетат в соотношении 9:1, затем 4:1) с получением в виде бесцветного масла указанного в заглавии защищенного ненасыщенного альфа-метил-Dлизина (0,26 г, 20%-ный выход). МСВР, рассч. для C27H28N2O5: m/z=461,2076 [M+H]. Обнаруж.: 461,2033. 1 Продукт примера 5 б (0,255 мг, 0,55 ммоля) растворяли в 6 н. НСl (6 мл) и муравьиной кислоте (6 мл) и раствор кипятили с обратным холодильником в течение 24 ч. Реакционную смесь охлаждали до комнатной температуры и концентрировали под вакуумом. Остаток суспендировали в воде и промывали СН 2 Сl2. Водный слой концентрировали и пропускали через промытую водой колонку с DOWEX 50WX4200 (смола в Н-форме, 0,5 н. NН 4 ОН в качестве элюента). Остаток концентрировали под вакуумом, 10%ной НСl подкисляли до рН 4 и концентрировали с получением в виде масла указанного в заглавии ненасыщенного D-лизина (71 мг, 55%-ный выход), который использовали без дополнительной очистки. 1H-ЯМР (400 МГц, D2O,част./млн): 1,4 (s, 3H), 2,5 (dd, 1H), 2,6 (dd, 1H), 3,4 (d, 2H), 5,6 (m, 2H),5,7 (m, 2H). Пример 5 г. Продукт примера 5 в (13 мг, 0,056 ммоля) растворяли в Н 2 О (5 мл) и с использованием 2,5 н. NaOH значение рН доводили до 9. Четырьмя порциями в течение 2 ч добавляли этилацетимидат'НСl (27 мг, 0,2 ммоля). По прошествии 2 ч 10%-ной НСl смесь подкисляли до рН 4 и концентрировали под вакуумом. Остаток пропускали через промытую водой колонку с DOWEX 50WX4-200 (смола в Н-форме, 0,5 н.NH4OH в качестве элюента). Остаток концентрировали под вакуумом, 10%-ной НСl подкисляли до рН 4 и концентрировали с получением в виде масла указанного в заглавии продукта (45 мг). МСВР, рассч. для С 9 Н 17N3 О 2: m/z=200,1399 [М+Н]. Обнаруж.: 200,1386. 1(2,0 г, 7,6 ммоля) в ТГФ (50 мл) охлаждали до -78 С. По каплям добавляли охлажденный до -78 С раствор ГМДСК (0,65 г, 3,24 ммоля) в ТГФ (25 мл). По прошествии 30 мин добавляли раствор продукта примера 1 в (2,8 г, 8,6 ммоля) в ТГФ (25 мл). Реакционную смесь перемешивали при комнатной температуре в течение 1 ч и реакцию гасили насыщенным водным NаНСО 3. Слои разделяли и водный слой экстрагировали EtOAc. Органические слои объединяли и промывали рассолом, сушили MgSO4, фильтровали и концентрировали под вакуумом. Полученный продукт в виде оранжевого масла хроматографировали на силикагеле (гексаны/этилацетат в соотношении 9:1, затем 4:1) с получением в виде белого твердого вещества указанного в заглавии защищенного ненасыщенного альфа-метил-L-лизина (0,5 г, 15%-ный выход). МСВР, рассч. для C27H28N2O5: m/z=461,2076 [M+H]. Обнаруж.: 461,2043. 1 Продукт примера 66 (0,5 г, 1 ммоля) растворяли в 12 н. НСl (10 мл) и муравьиной кислоте (5 мл) и эту смесь кипятили с обратным холодильником в течение 12 ч. Реакционную смесь выдерживали в моро-23 006548 зильной камере в течение 3 ч и твердые частицы удаляли фильтрованием. Остаток промывали CH2Cl2 иEtOAc. Водный слой концентрировали под вакуумом и в виде масла получали указанный в заглавии ненасыщенный альфа-метил-L-лизин (0,26 г, 99%-ный выход), который использовали без дополнительной очистки. 1H-ЯМР (300 МГц, D2O,част./млн): 1,4 (s, 3 Н), 2,5 (dd, 1H), 2,6 (dd, 1H), 3,4 (d, 2H), 5,7 (m, 2H). Пример 6 г. Продукт примера бв (0,13 г, 0,56 ммоля) растворяли в Н 2 О (1 мл) и с использованием 2,5 н. NaOH значение рН доводили до 9. Четырьмя порциями в течение 1 ч добавляли этилацетимидатНСl (0,28 г,2,2 ммоля). По прошествии 1 ч 10%-ной НСl смесь подкисляли до рН 4 и концентрировали под вакуумом. Получали остаток, который пропускали через промытую водой колонку с DOWEX 50WX4-200(0,5 н. NH4OH в качестве элюента). Остаток концентрировали под вакуумом, 10%-ной НСl подкисляли до рН 4 и концентрировали с получением в виде масла указанного в заглавии продукта (40 мг). МСВР, рассч. для C9H17N3O2: m/z=222,1218 [M+Na]. Обнаруж.: 222,1213. 1 Сухой ТГФ (1000 мл) помещали в колбу, которую предварительно продували аргоном, и вводили 60%-ный NaH, диспергированный в минеральном масле (9,04 г, 0,227 моля). В эту смесь добавляли продукт примера 7 б (30,7 г, 0,114 моля). Далее реакционную смесь в течение 30 мин перемешивали при температуре от 10 до 15 С. Добавляли иодида калия (4 г) и иода (2 г) и сразу же после этого в течение 30 мин добавляли продукт примера 7 а (23 г, 0,113 моля в 200 мл ТГФ). Затем реакционную смесь перемешивали при 55 С до тех пор, пока не исчезал исходный материал (2 ч). Потом реакционную смесь охлаждали до комнатной температуры и выпаривали растворитель. Добавляли этилацетат (500 мл) и смесь осторожно промывали 2 порциями по 200 мл деионизированной воды. Органический слой сушили над безводным MgSO4, фильтровали и выпаривали с получением 44 г сырого продукта. Очисткой хроматографией с использованием 20% этилацетата в гексане получали указанный в заглавии защищенный ненасыщенный альфа-метиллизин (28 г, 57%-ный выход). Элементный анализ; рассч. для C26H30N2O4 и 0,5 этилацетата: С,70,42; Н, 7,14; N, 5,91. Обнаруж.: С,70,95; Н, 7,73; N, 6,09. Продукт примера 7 в (16 г, 0,0368 моля) растворяли в 1 н. НСl (300 мл) и при 25 С перемешивали в течение 2 ч. Реакционную смесь промывали диэтиловым эфиром (2 порции по 150 мл) и водный слой отделяли и обесцвечивали углем. В концентрированном в виде белого вспененного твердого вещества получали 9 г (100% выход) не содержавшего защитной группы ненасыщенного альфа-метиллизинового эфира 7 г. Элементный анализ; рассч. для C8H14N2O2, содержавшего 2,26 НСl и 1,19 Н 2O: С, 35,06; Н, 6,86; N,1,22; Cl, 29,24. Обнаруж.: С, 35,31; Н, 7,38; N, 10,70; Cl, 29,77. 1 Продукт примера 7 г (2,43 г, 0,01 моля) растворяли в деионизированной воде (25 мл). При 25 С добавляли раствор NaOH (400 мг, 0,01 моля) в деионизированной воде (25 мл) для доведения рН до 7,95 и перемешивание продолжали в течение еще 10 мин. В реакционную смесь добавляли гидрохлорид этилацетимидата (988 мг, 0,008 моля) с одновременным доведением рН до 8,5 добавлением 1 н. NaOH. Реакционную смесь перемешивали при рН от 8 до 8,5 в течение 3 ч с последующим добавлением ацетимидата. В реакционную смесь добавляли 1 н. НСl (рН: 4,1). При 50 С выпаривали растворитель с получением желтого сырого гигроскопического остатка (4 г, 100%-ный выход). Очистку проводили в хроматографической системе Gilson с использованием 0,1% АсОН/СН 3 СN/Н 2O. Элементный анализ; рассч. для C10H17N3O2, содержавшего 2,25 НСl и 1,7 H2O: С, 37,08; Н, 7,05; N,12,97; Cl, 24,63. Обнаруж.: С, 37,01; Н, 6,79; N, 12,76; Cl, 24,87 ИК-спектрограмма (без примесей,max,cm-1): 2953, 2569, 1747, 1681, 1631. 1H-ЯМР (D2O,част./млн): 1,52 (s, 3H), 2,12 (s, 3 Н), 2,74-2,96 (2 dt, 2H), 3,75 (s, 3 Н), 3,95 (t, 2H). 13 С-ЯМР (D2O,част./млн): 23,89, 29,81, 32,05, 57,08, 61,90, 79,57, 82,43, 173,92. Масс-спектроскопия: (М+1)=212. Пример 7e. Продукт примера 7 д (100 мг, 0,0005 моля) растворяли в 8 н. НСl (20 мл) и перемешивали в течение 10 ч при кипячении с обратным холодильником. Реакционную смесь охлаждали до комнатной температуры и в роторном испарителе выпаривали водную НСl. Остаток растворяли в деионизированной воде(10 мл) и под вакуумом повторно концентрировали с получением в виде желтого стеклообразного твердого вещества с почти количественным выходом указанного в заглавии продукта (88 мг). Элементный анализ; рассч. для C9H15N3O2, содержавшего 2,4 НСl и 1,8 Н 2O: С, 34,08; Н, 6,67; N,13,25; Cl, 26,83. Обнаруж.: С, 34,32; Н, 6,75; N, 13,63; Cl, 26,47. ИК-спектроскопия (без примесей,max, cm-1): 1738, 1677, 1628, 1587. 1-25 006548 Калиевую соль 3-метил-1,2,4-оксадиазол-5(4 Н)-она получали так, как уже описано в работе В 1-литровую колбу загружали транс-1,4-дибром-2-бутен (50 г, 0,23 моля) и ацетон (500 мл). Добавляли гетероциклический продукт примера 9 а (16 г, 0,12 моля), после чего тетра-нбутиламмонийбромид (3,9 г, 0,012 моля, 0,1 экв.). Реакционную смесь перемешивали при КТ в течение 18 ч, разбавляли рассолом и экстрагировали EtOAc. Органический экстракт промывали рассолом, сушили над MgSO4, фильтровали и концентрировали под вакуумом с получением желтого полутвердого остатка. Добавляли метиленхлорид и фильтрованием удаляли твердый продукт. Фильтрат концентрировали и остаток обрабатывали горячими гексанами для растворения непрореагировавшего дибромбутена. Гексановый слой декантировали и полученный продукт в виде масла хроматографировали на диоксиде кремния, элюируя гексанами/ЕtOАс в соотношении 7:3. Указанный в заглавии продукт (14,2 г, 50%-ный выход) выделяли в виде желтого масла. 1 В суспензию гидрохлорида метилового эфира D,L-аланина (16,83 г, 120,5 ммоля) в CH2Cl2 (400 мл) вводили триэтиламин (16,2 мл, 116,4 ммоля), после чего 3,4-дихлорбензальдегид (19,07 г, 109 ммоля) иMgSO4 (20 г). Суспензию перемешивали при комнатной температуре в течение 18 ч и фильтровали. Фильтрат промывали водой (250 мл) и рассолом (250 мл), сушили (MgSO4) и выпаривали с получением в виде масла 27,65 г (97%-ный выход) целевого имина. 1 Хиральный межфазный катализатор (1S,2S)-(+)Cu(II)C6Salen получали в соответствии с методом,описанным в Inorganic Chemistry 1996, 35, 387. Пример 9 д. В продутой N2, высушенной в сушильном шкафу склянке в сухом толуоле (300 мл) суспендировали метоксид натрия (7,3 г, 134 ммоля). Добавляли хиральный межфазный катализаторный продукт примера 9 г (800 мг, 1,9 ммоля, 5% в пересчете на имин), после чего раствор продукта примера 9 в (10 г, 38,5 ммоля) в сухом толуоле (50 мл). Добавляли раствор продукта примера 96 (10 г, 42,9 ммоля) в 50 мл толуола и реакционную смесь перемешивали при комнатной температуре в течение 18 ч. Далее реакционную смесь фильтровали через слой броунмиллерита для удаления NaBr и катализатора. Толуольный слой в течение 40 мин обрабатывали 200 мл 6 н. НСl. Слои разделяли, толуольный слой промывали 200 мл 6 н. НСl и объединенные водные слои концентрировали под вакуумом. Остаток разбавляли 100 мл воды и насыщенным водным K2 СО 3 значение рН доводили до 7. Твердые частицы отфильтровывали через слой броунмиллерита и значение рН фильтрата доводили до 9. Его экстрагировали EtOAc (6 раз), сушили Na2SO4,фильтровали и концентрировали под вакуумом с получением в виде светло-зеленого масла указанного в заглавии свободного основания (5,77 г, 59%-ный выход). Хроматографией в хиральной колонке (Chiral-26 006548 В раствор продукта примера 9 д (2,51 г, 9,84 ммоля) в МеОН (40 мл) вводили (S)-(+)-миндальную кислоту (1,5 г, 9,84 ммоля). Образец концентрировали под вакуумом, а затем перекристаллизовывали из МТБЭ/МеОН (в соотношении 4:1) с получением в виде белого порошка указанного в заглавии продукта В 500-миллилитровую колбу загружали катализатор Линдлара (217 мг, 5 мас.%, 5% Pd на СаСО 3,отравлен Рb), МеОН (80 мл) и муравьиную кислоту (2 мл, 5 экв.). Добавляли суспензию продукта примера 9 е (4,34 г, 10,7 ммоля) в МеОН (20 мл) и реакционную смесь выдерживали при 60 С. По прошествии 4 ч добавляли дополнительно 30 мг катализатора Линдлара и муравьиной кислоты (200 мкл). Реакционную смесь перемешивали с броунмиллеритом, фильтровали и концентрировали под вакуумом с получением указанного в заглавии продукта, существовавшего в виде желтого масла, который использовали без дополнительной очистки (97%-ный выход). Элементный анализ; рассч. для C19H29N3O7 с 1,3 Н 2 О: С, 52,48; Н, 7,32; N, 9,66. Обнаруж.: С, 52,71; Н, 7,01; N, 9,29. 1 В сухую продутую N2 колбу загружали NaOMe (71,7 г, 1,3 моля) и сухой толуол (2 л). Добавляли катализаторный продукт примера 9 г (5,88 г, 15 ммолей), после чего раствор продукта примера 9 в (100 г,0,38 моля) в 200 мл толуола. По каплям добавляли раствор бромидного продукта примера 9 б (100 г, 0,43 моля) в 200 мл толуола. Реакцию гасили разбавлением реакционной смеси толуолом и ледяной НОАс при одновременном поддержании температуры на уровне 25 С. После перемешивания в течение 15 мин при комнатной температуре реакционную смесь фильтровали и фильтровальный пирог промывали толуолом. Фильтрат разбавляли Н 2 О и перемешивали в течение 1 ч. Слои разделяли и толуольный слой промывали Н 2 О. Водные слои объединяли и концентрировали под вакуумом. Остаток растворяли в 120 мл МеОН и добавляли (S)-(+)-миндальной кислоты. Добавляли горячего метил-трет-бутилового эфира(450 мл), раствор охлаждали до комнатной температуры и хранили в морозильной камере в течение ночи. Указанный в заглавии продукт в виде осадка собирали и промывали холодным метил-третбутиловым эфиром (43,94 г, 28%-ный выход). Данные хроматографии в хиральной колонке (ChiralPakAD, гексаны/изо-РrОН в соотношении 70:30, элюирование в течение 30 мин) свидетельствовали, что указанный в заглавии продукт существовал при соотношении (S:R) 99:1; (для S-время элюирования: 12,2 мин, для R- время элюирования: 16,5 мин). 1 Образец продукта примера 9 з (36,8 г, 90 ммолей) растворяли в воде (370 мл), насыщенным воднымK2 СО 3 значение рН доводили до 9 и экстрагировали CH2Cl2. Органический экстракт концентрировали под вакуумом с получением свободного основания. Этот остаток растворяли в смеси 1-бутанола (184 мл), ледяной уксусной кислоты (148 мл) и воды (184 мл). При интенсивном перемешивании реакционной смеси в нее добавляли цинковую пыль (37 г, 0,57 моля) и ее выдерживали при 50 С в течение ночи. Раствор фильтровали через броунмиллерит и фильтровальный пирог промывали МеОН. Фильтрат концентрировали, растворяли в воде (250 мл) и МеОН (55 мл) и насыщенным водным NaHCO3 значение рН доводили до 8. Раствор фильтровали и 6 н. НСl рН фильтрата доводили до 2, после чего его концентрировали под вакуумом с получением указанного в заглавии продукта. 1 Н-ЯМР (300 МГц, D2O,част./млн): 1,4 (s, 3 Н), 2,1 (s, 3 Н), 2,5 (m, 2H), 3,7 (s, 3 Н), 3,8 (d, 2H), 4,9MCBP, рассч. для С 10 Н 19N3 О 2: m/z=214,1550 [М+Н]. Обнаруж.: 214,1544. Пример 9 к. Образец продукта из примера 9 ж (8 г, 20,4 ммоля) растворяли в 6 н. НСl (100 мл) и кипятили с обратным холодильником в течение 3 ч. Раствор концентрировали под вакуумом с получением аминокислоты, которую очищали на ионообменной смоле Dowex 50WX4-200 в Н-форме. Смолу (120 г) промывали 25%-ной НСl, после чего Н 2 О с доведением рН до 6. Соединение помещали в воду. Смолу промывали последовательно 0, 1,7, 3,3, 5, 6,6 и 8,3%-ной НСl. Продукт начинали элюировать 5%-ной НСl. Фракции объединяли и концентрировали под вакуумом с получением указанного в заглавии продукта в виде дигидрохлоридной соли (4,3 г, 84%-ный выход). Элементный анализ; рассч. для С 9 Н 17N3O2 с 2,1 НСl и 0,1 Н 2 О: С, 38,94; Н, 7,01; N, 15,14, Cl, 26,82. Обнаруж.: С, 38,68; Н, 7,17; N, 14,74, Cl, 27,28. 1 Н-ЯМР (300 МГц, D2O,част./млн): 1,5 (s, 3 Н), 2,1 (s, 3 Н), 2,5 (dd, 1H), 2,6 (dd, 1H), 5,6 (m, 2H). Образец продукта из примера 9 д (0,5 г, 1,23 ммоля) растворяли в 3 н. НСl (50 мл) и кипятили с обратным холодильником в течение 4 ч. Раствор концентрировали под вакуумом с получением аминокислоты, которую очищали на ионообменной смоле Dowex 50WX4-200 в Н-форме. Смолу (10 г) промывали 100 мл 25%-ной НСl, после чего 300 мл Н 2 О с доведением рН до 6. Соединение помещали в воду. Смолу промывали последовательно 1,7, 3,3, 5, 6,6 и 8,3%-ной НСl. Продукт начинали элюировать 5%-ной НСl. Фракции объединяли и концентрировали под вакуумом с получением указанного в заглавии продукта в виде дигидрохлоридной соли (264 мг, 88%-ный выход). Элементный анализ; рассч. для C10H15N3O4 с 1,1 НСl и 0,5 H2O: С, 41,37; Н, 5,94; N, 14,47, Cl, 13,43. Обнаруж.: С, 41,41; Н, 6,14; N, 14,88, Cl, 13,14. 1 Образец продукта из примера 9 д (1,0 г, 2,46 ммоля) превращали в свободное основание его обработкой смолой с Dowex 50WX4-200 в Н-форме и элюированием 5%-ной НСl. Элюент концентрировали под вакуумом с получением остатка, который растворяли в 2,5 н. NaOH (4 мл, 9,84 ммоля, 4 экв.) и 4 мл Н 2 О. По прошествии 4 ч раствор концентрировали и указанный в заглавии продукт осаждали из холодной Н 2 О (0,215 г). Элементный анализ; рассч. для С 9 Н 17N3 О 3 с 5 NaCl: С, 21,30; Н, 3,38; N, 8,28, Cl, 33,93. Обнаруж.: С,20,30; Н, 3,26; N, 7,70, Cl, 33,46.(m, 1H). МСВР, рассч. для С 9 Н 17N3 О 3: m/z=216,1343 [М+Н]. Обнаруж.: 216,1354. Новые промежуточные продукты Новые промежуточные продукты, которые могут быть использованы при получении соединений по настоящему изобретению, включают метил-2-(1,3-диоксо-1,3-дигидро-2 Н-изоиндол-2-ил)пропаноат Биологические данные Некоторые или все последующие испытания использовали для демонстрации способности соединений по изобретению ингибировать активность синтетазы оксида азота, а также для демонстрации полезных фармакологических свойств. Определение активности синтетазы оксида азота с помощью цитруллина Активность синтетазы оксида азота (NOS) можно определить осуществлением мониторинга превращения L-[2,3-3 Н]-аргинина в L-[2,3-3 Н]-цитруллин (Bredt и Snyder, Proc. Natl. Acad. Sci. U.S.A., 87,682-685, 1990 и Мооrе и др. J. Med. Chem., 39, 669-672, 1996). Каждый из ферментов, индуцибельныйNOS человека (hiNOS), эндотелиальный конститутивный NOS человека (hecNOS) и нейрональный конститутивный NOS человека (hncNOS), клонируют, исходя из RNA, экстрагированной из тканей человека.cDNA индуцибельной NOS человека (hiNOS) выделяют из cDNA библиотеки, созданной из RNA, экстрагированной из образца ободочной кишки, взятой у пациента с неспецифическим язвенным колитом.cDNA для эндотелиальной конститутивной NOS человека (hecNOS) выделяют из cDNA библиотеки,-30
МПК / Метки
МПК: A61K 31/201, C07C 251/08, C07D 209/48, C07C 271/22, C07C 229/30, A61P 19/02, C07C 255/30
Метки: кислот, гексиновой, производные, ингибиторов, 2-амино-2-алкил-4-гексеновой, могут, использованы, которые, качестве, оксида, синтетазы, быть, азота
Код ссылки
<a href="https://eas.patents.su/30-6548-proizvodnye-2-amino-2-alkil-4-geksenovojj-i-geksinovojj-kislot-kotorye-mogut-byt-ispolzovany-v-kachestve-ingibitorov-sintetazy-oksida-azota.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 2-амино-2-алкил-4-гексеновой и -гексиновой кислот, которые могут быть использованы в качестве ингибиторов синтетазы оксида азота</a>
Предыдущий патент: Жидкая водосодержащая композиция, содержащая жирорастворимые витамины, и её применение
Следующий патент: Специфические для семян льна промоторы, способы их применения, трансгенные семена и растения льна
Случайный патент: Интегрированное адаптерное устройство для обеспечения многочастотных колебаний вибрационного рабочего узла