Ингибиторы фермента impdh
Номер патента: 4141
Опубликовано: 26.02.2004
Авторы: Сондерс Джеффри, Стамос Дин, Бэдиа Майкл, Трюдо Мартин, Бетиел Скотт
Формула / Реферат
1. Соединение формулы (А)
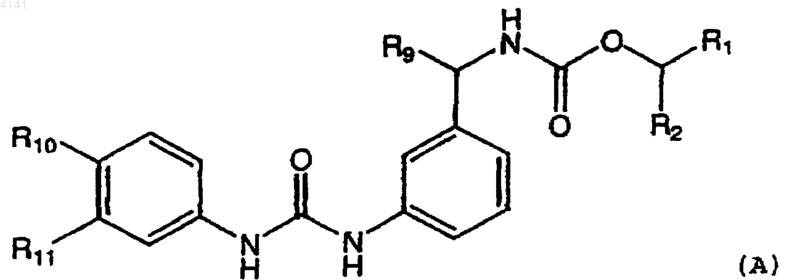
в которой каждый из R1 и R2 независимо выбран из группы, включающей водород; -CF3; -(C1-C6)-прямолинейный или разветвленный алкил; -(C2-C6)-прямолинейный или разветвленный алкенил или алкинил; -(C1-C6)-прямолинейный или разветвленный алкил-R7; -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7; и в которой по меньшей мере один из R1 или R2 представляет -(C1-C6)-прямолинейный или разветвленный алкил-R7; -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7, в которой вплоть до 4 атомов углерода в любом из указанных алкилов, алкенилов или алкинилов необязательно и независимо заменены группой R3 и в которой один или оба из R1 или R2 необязательно этерифицированы с образованием пролекарства; или
альтернативно, R1 и R2, взятые вместе, образуют тетрагидрофуранил, в которой когда R9 представляет водород, (R)-метил, (R)-этил или (R)-гидроксиметил, один атом водорода в указанном тетрагидрофуране заменен группой -OR6 или -R7, и в которой, если R9 представляет (S)-метил, (S)-этил или (S)-гидроксиметил, то один атом водорода в указанном тетрагидрофуране необязательно заменен группой -OR6 или -R7;
в которой, если R9 представляет водород, (R)-метил, (R)-этил или (R)-гидроксиметил, а каждый из R1 и R2 независимо представляет водород, незамещенный -(C1-C6)-прямолинейный или разветвленный алкил, либо незамещенный -(C2-C6)-прямолинейный или разветвленный алкенил или алкинил, то часть соединения, представленного -CH(R1)R2, представляет C5-C12 прямолинейный или разветвленный алкил, алкенил или алкинил;
каждый R3 независимо выбран из галогена, CN, -OR4 или -N(R5)2;
R4 выбран из группы, включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, -(C2-C6)-прямолинейный или разветвленный алкенил или алкинил, -[(C1-C6)-прямолинейный или разветвленный алкил]-R7, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7, -C(O)-[(C1-C6)-прямолинейный или разветвленный алкил], -C(O)-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-[(C1-C6)-прямолинейный или разветвленный алкил]-N(R8)2, -C(O)-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-N(R8)2, -P(O)(OR8)2, -P(O)(OR8)(R8), -C(O)-R7, -S(O)2N(R5)2, -[(C1-C6)-прямолинейный или разветвленный алкил]-CN или -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-CN;
каждый R5 независимо выбран из группы, включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, -(C2-C6)-прямолинейный или разветвленный алкенил или алкинил, -[(C1-C6)-прямолинейный или разветвленный алкил]-R7, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7, -[(C1-C6)-прямолинейный алкил]-CN, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-CN, -[(C1-C6)-прямолинейный или разветвленный алкил]-OR4, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-OR4, -C(O)-(C1-C6)-прямолинейный или разветвленный алкил, -C(O)-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-R7, -C(O)O-R7, -C(O)O-(C1-C6)-прямолинейный или разветвленный алкил, -C(O)O-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -S(O)2-(C1-C6)-прямолинейный или разветвленный алкил или -S(O)2-R7; или два фрагмента R5, когда связаны с одним и тем же атомом азота, соединены вместе с указанным атомом азота, образуя 3-7-членное гетероциклическое кольцо, в котором указанное гетероциклическое кольцо необязательно содержит от 1 до 3 дополнительных гетероатомов, независимо выбранных из N, O, S, S(O) или S(O)2;
R6 выбран из -C(O)-CH3, -CH2-C(O)-OH, -CH2-C(O)-O-трет-Bu, -CH2-CN или -CH2-Cу CH;
каждый R7 представляет моноциклическую или бициклическую кольцевую систему, в которой
i) каждое кольцо включает от 3 до 7 кольцевых атомов, независимо выбранных из C, N, O или S;
ii) не более 4 кольцевых атомов выбраны из N, O или S;
iii) любая CH2 группа необязательно заменена группой C(O);
iv) любой S необязательно заменен группой S(O) или S(O)2;
каждый R8 независимо выбран из водорода или -[C1-C4]-прямолинейного или разветвленного алкила;
где в любой кольцевой системе в указанном соединении вплоть до 3 атомов водорода, связанных с кольцевыми атомами, необязательно и независимо заменены галогеном, гидрокси, нитро, циано, амино, (C1-C4)-прямолинейным или разветвленным алкилом; O-(C1-C4)-прямолинейным или разветвленным алкилом, (C2-C4)-прямолинейным или разветвленным алкенилом или алкинилом или O-(C2-C4)-прямолинейным или разветвленным алкенилом или алкинилом; и
где кольцевая система необязательно бензоконденсирована;
R9 выбран из водорода, (R)-метила, (S)-метилa, (R)-этила, (S)-этила, (R)-гидроксиметила или (S)-гидроксиметила;
R10 выбран из -CуN или 5-оксазолила; а
R11 выбран из галогена, -O-(C1-C3)-прямолинейного алкила или -O-(C2-C3)-прямолинейного алкенила или алкинила.
2. Соединение по п.1, в котором указанное соединение имеет формулу (I)
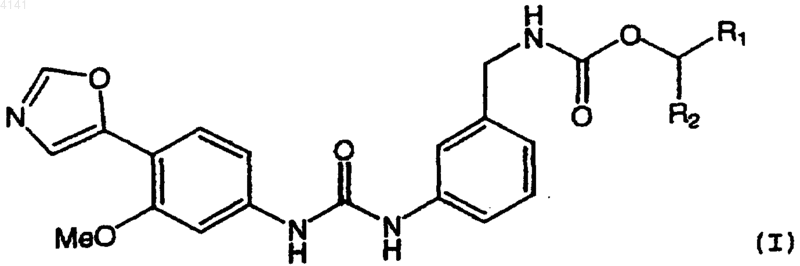
где R1 и R2 имеют значения, указанные в п.1.
3. Соединение по п.1, в котором указанное соединение имеет формулу (IA)
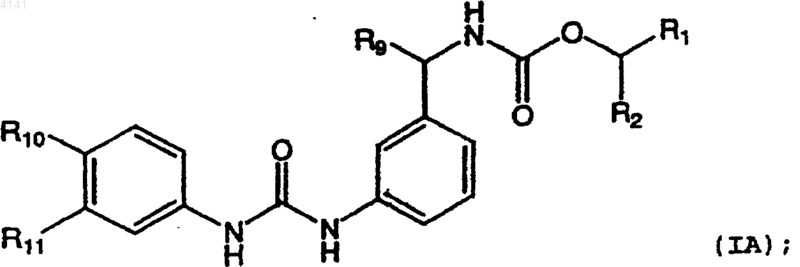
где R9 выбран из (R)-метила, (S)-метила, (R)-этила, (S)-этила, (R)-гидроксиметила или (S)-гидроксиметила; а R1 и R2 имеют значения, указанные в п.1.
4. Соединение по п.3, в котором R9 выбран из (S)-метила, (S)-этила или (S)-гидроксиметилметила.
5. Соединение по п.4, в котором R9 представляет (S)-метил.
6. Соединение по п.3, в котором R11 выбран из O-метила, O-этила или O-изопропила.
7. Соединение по п.1, в котором
по меньшей мере один из R1 или R2 выбран из водорода, метила, этила, н-пропила, изопропила, н-бутила, трет-бутила, н-пентила, фенила, пиридила, -CH2OCH3, -CH2CN, -CH2OCH2CH2CN, -CH2C(CH3)2CH2CH2CN, -CH2C(CH2CH3)2CH2CH2CN, -CH2CH2CN, -CH2N(CH2CH2CN)2, -CH2N(CH3)CH2CH2CN, -CH(NH2) CH2CN, -CH2Cl, -CH2OH, -CH2CH2OH, -CH2CH2CH2CH2OH, -CH2CH2OC(O)CH3, -CH2CH2OC(O)CH2NH2, -CH2CH2NHCH3, -CH2CH2N(CH3)2, -CH2N(CH2CH3)2, -CH2CH2N(CH2CH3)2, -CH2CH2CH2N(CH3)2, -CH2CH2CH2N+(CH3)3, -CH2OCH2CH(CH3)2, -CH2CH2N(CH3)C(O)OC(CH3)3, -CH2N(CH2CH2CN)CH2CH(CH3)2, -CH(CH2CN)N(CH3)2, -CH2CH(CH2CN)NHC(O)OC(CH3)3,
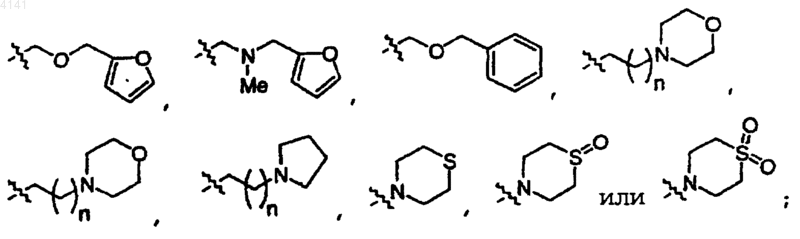
где n равно 0 или 1.
8. Соединение по п.2, в котором R1 и R2, взятые вместе, образуют 3-тетрагидрофуранил, замещенный в положении 5 -OR6.
9. Соединение по п.3, в котором один из R1 или R2 выбран из водорода, этила или фенила; а другой из R1 или R2 выбран из -CH2OH, -CH2CN, -CH2CH2CN или CH2N (CH2CH3)2 или R1 и R2, взятые вместе, образуют 3-тетрагидрофуранил.
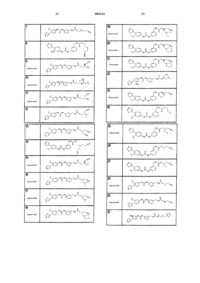
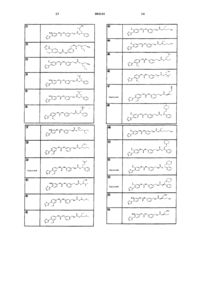
10. Соединение по п.1, представляющее собой соединение, выбранное из соединений 1-187.
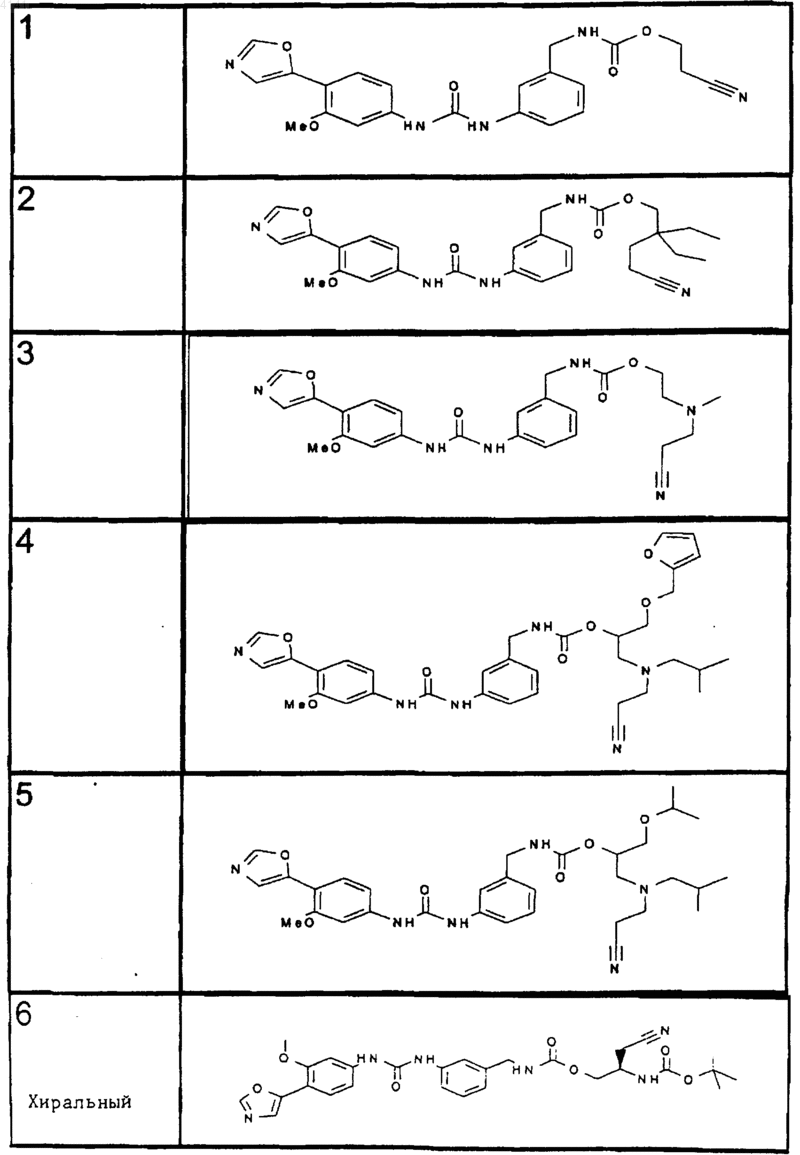
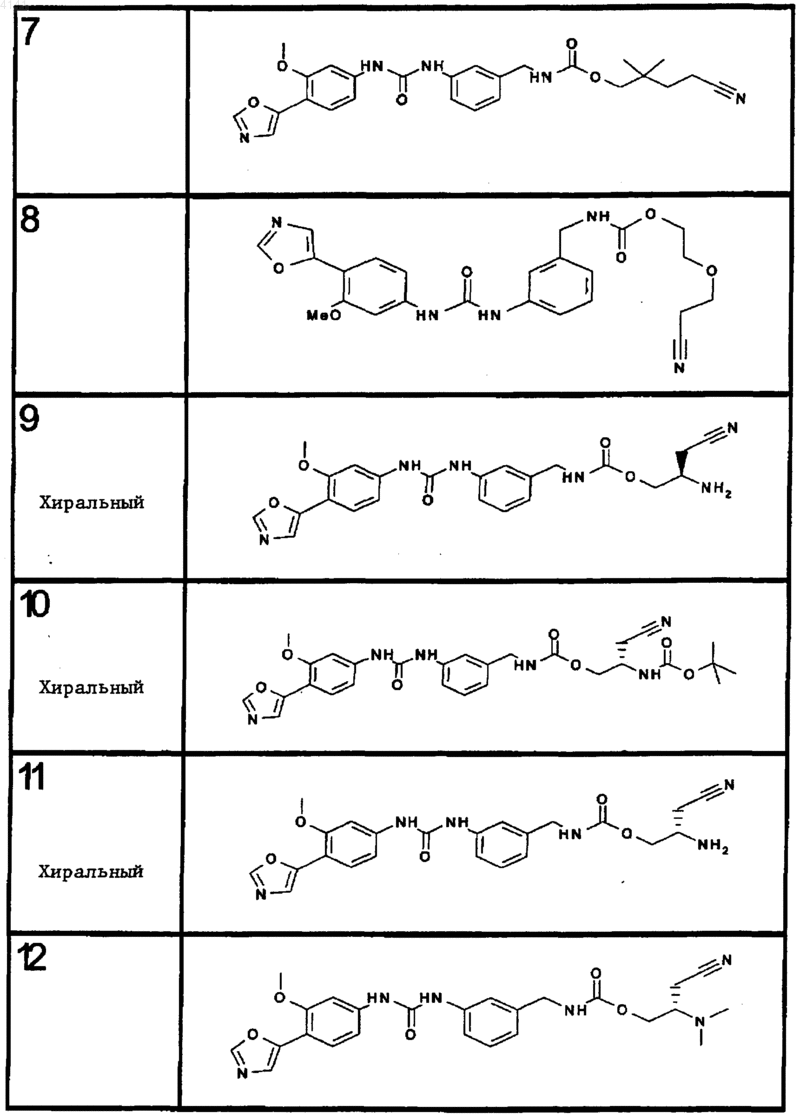
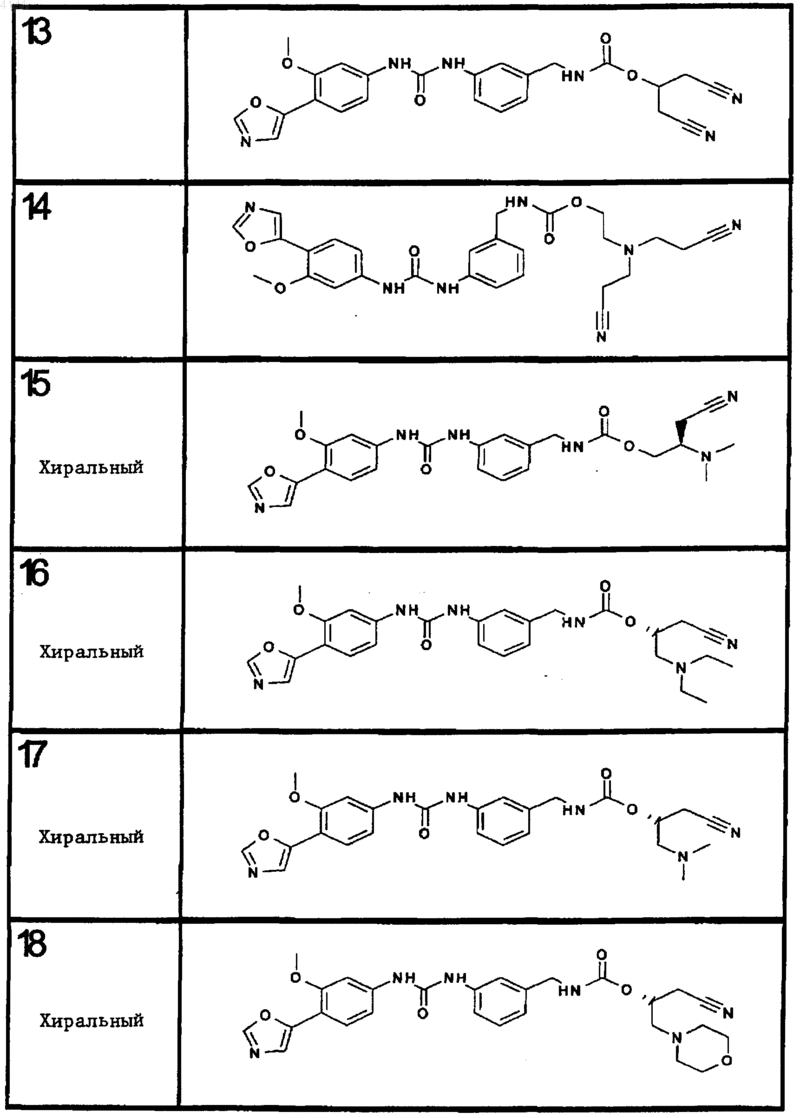
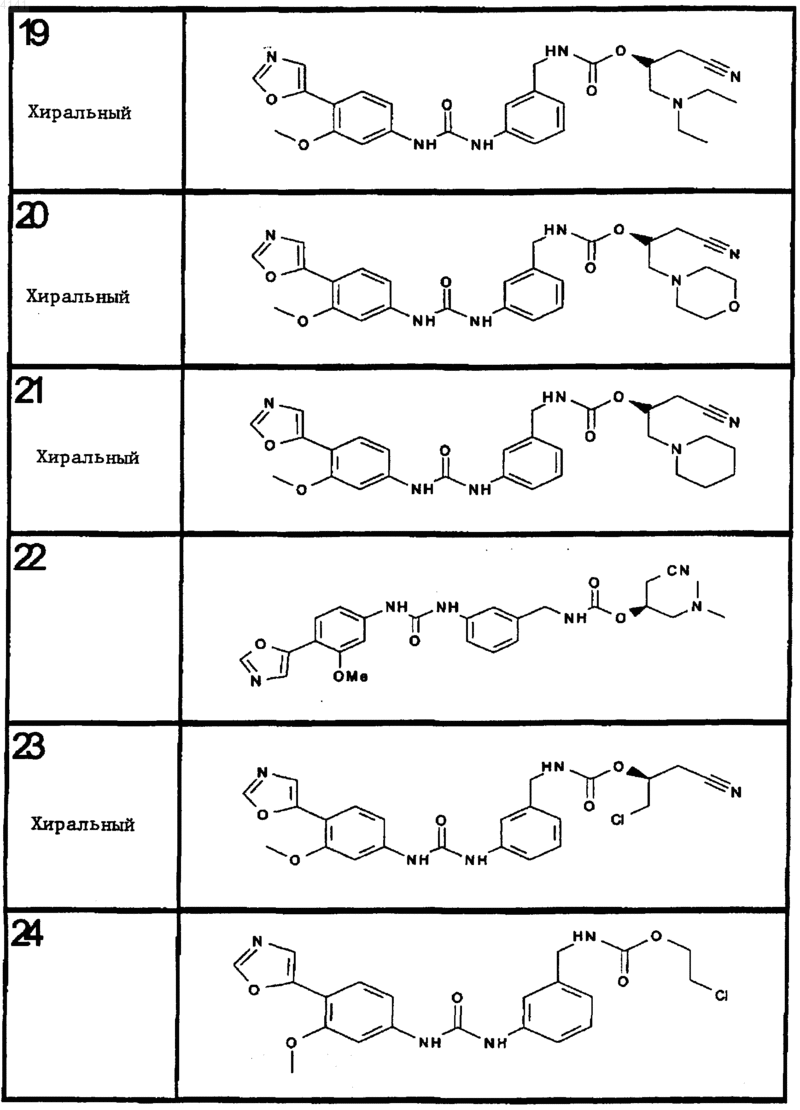
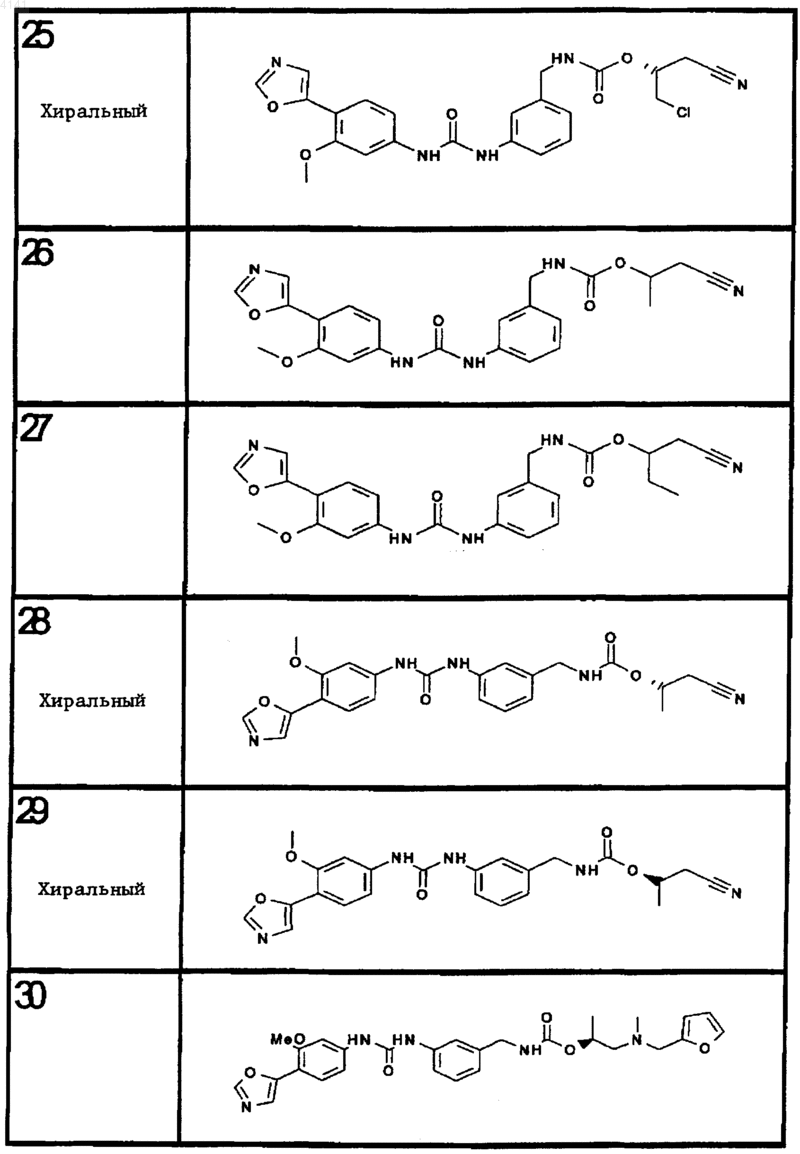
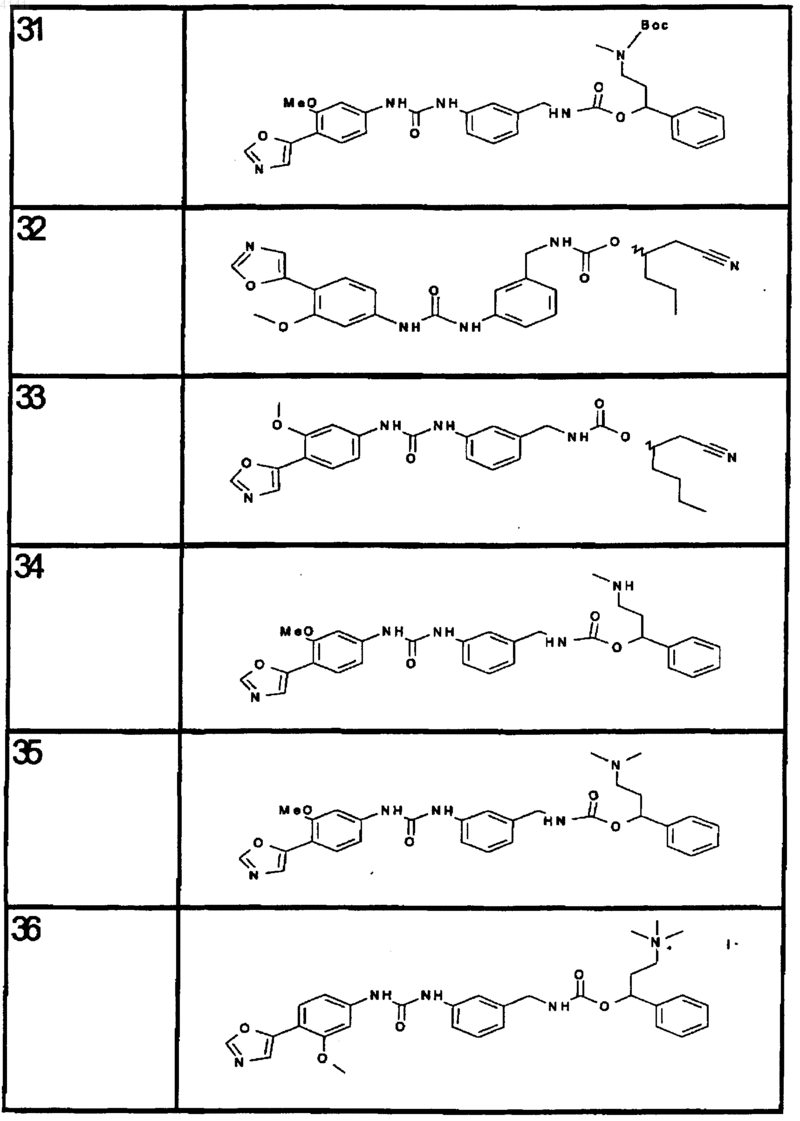
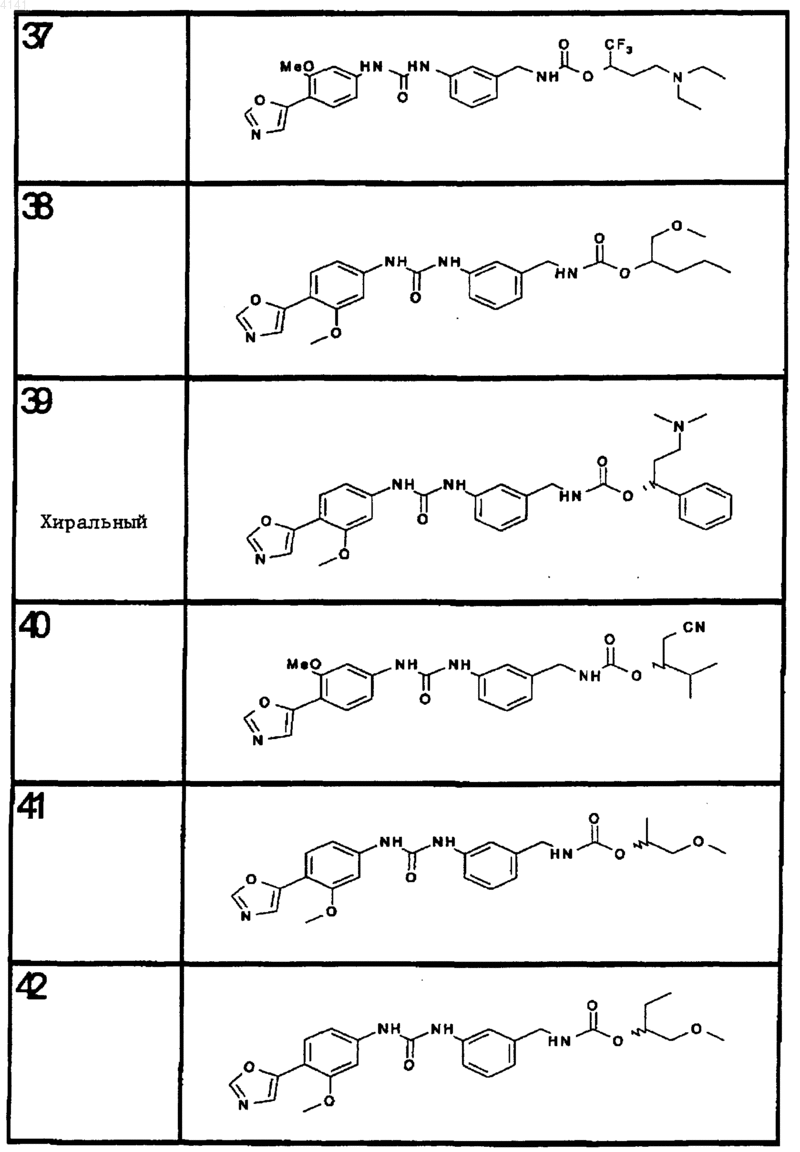
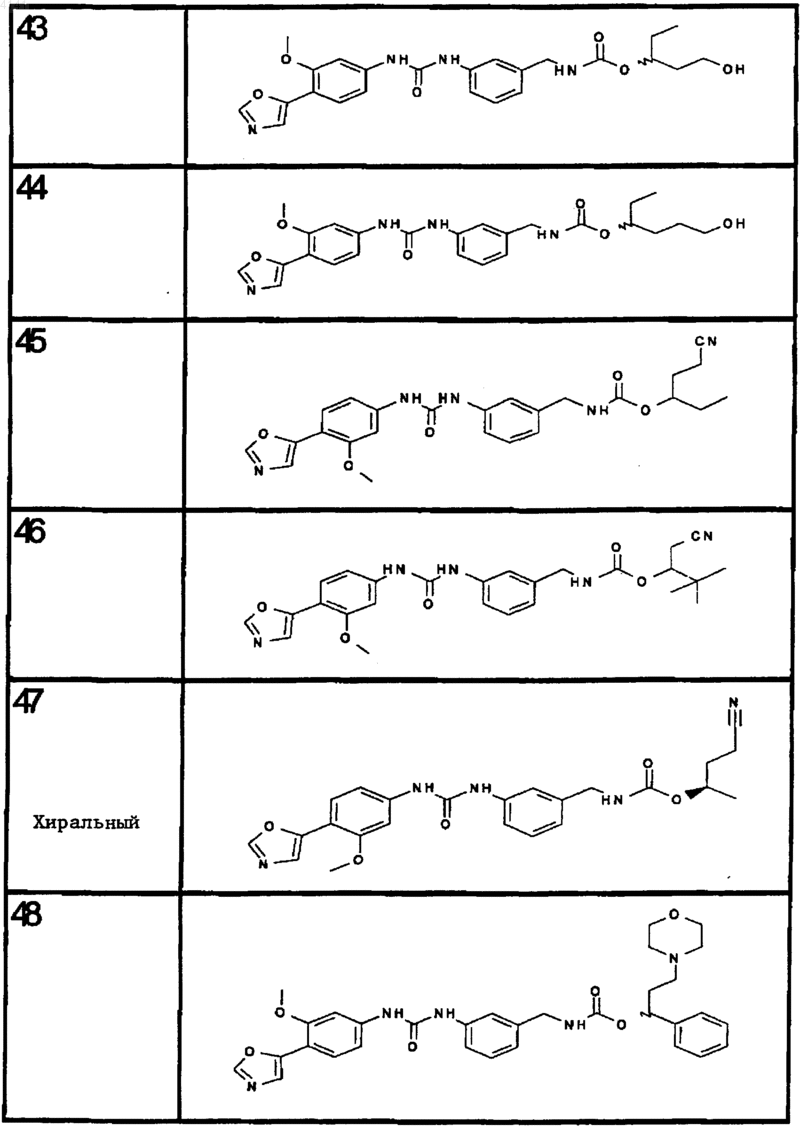
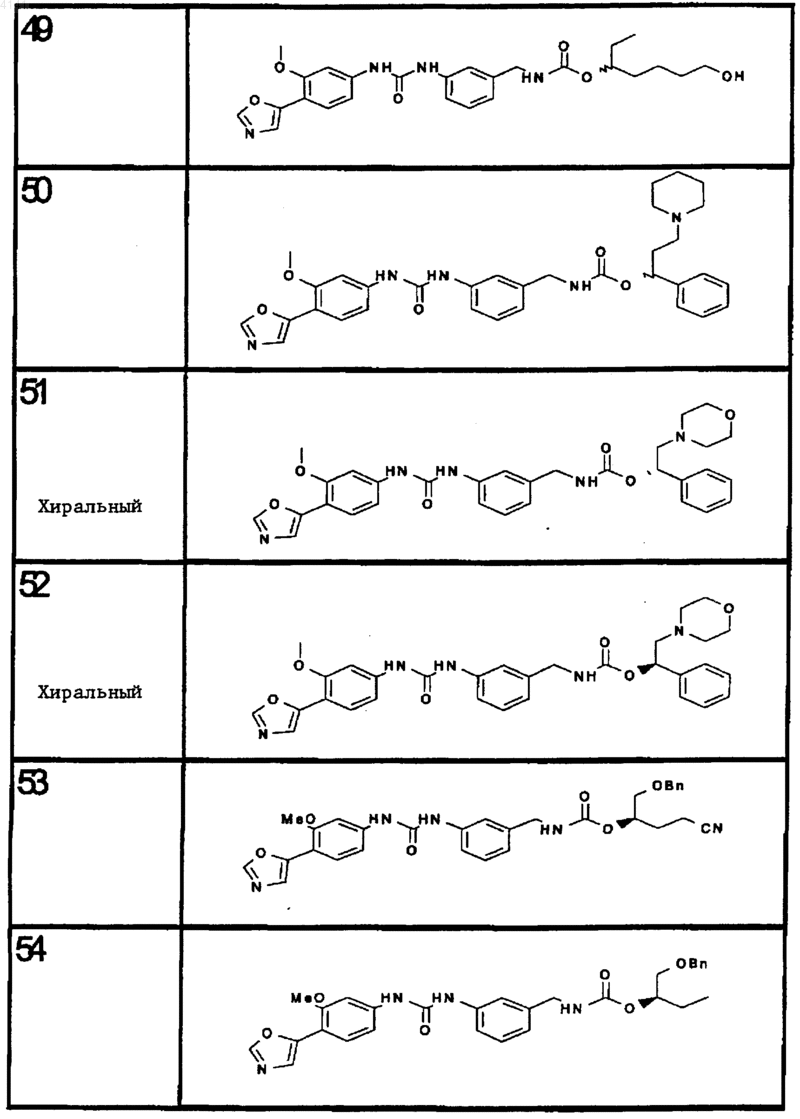
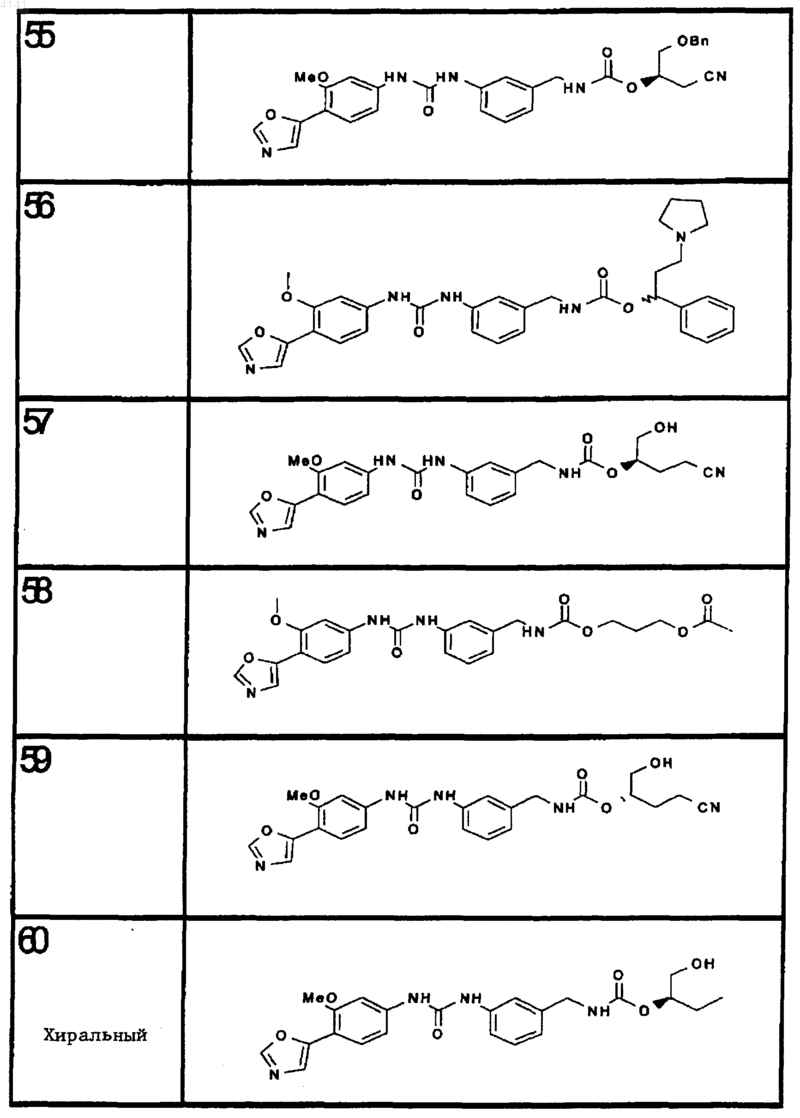
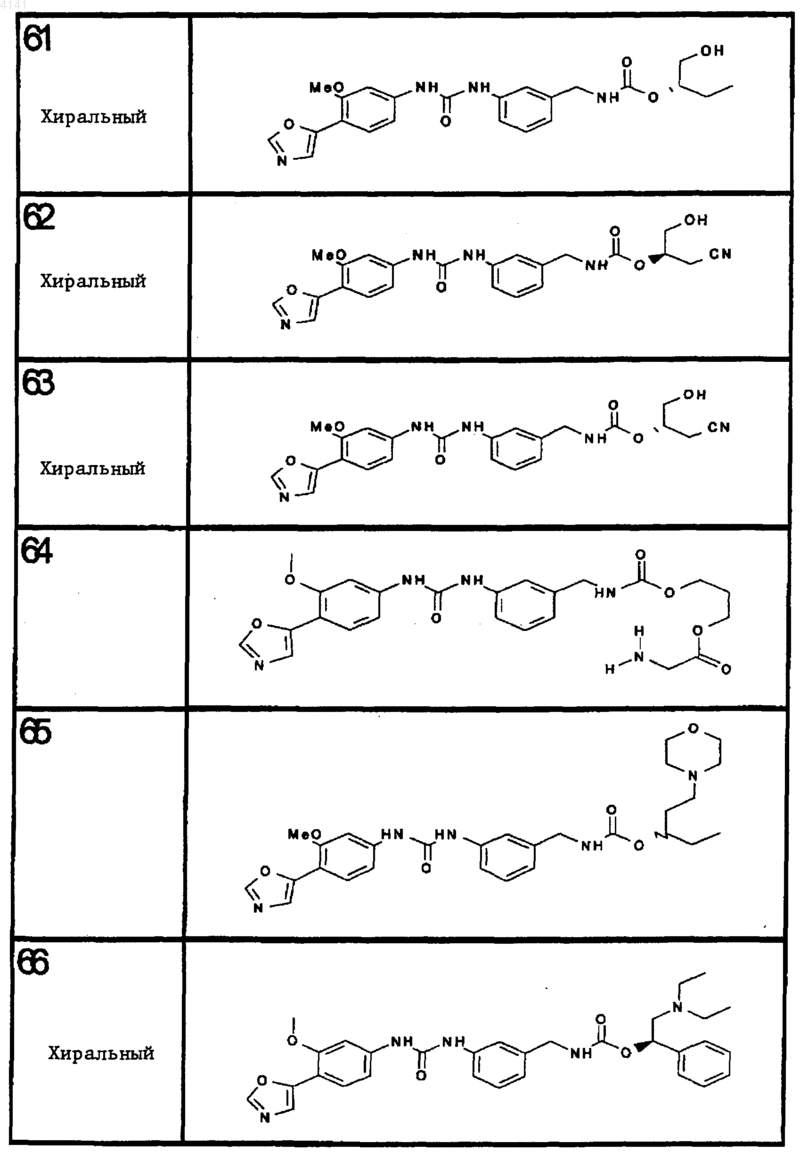
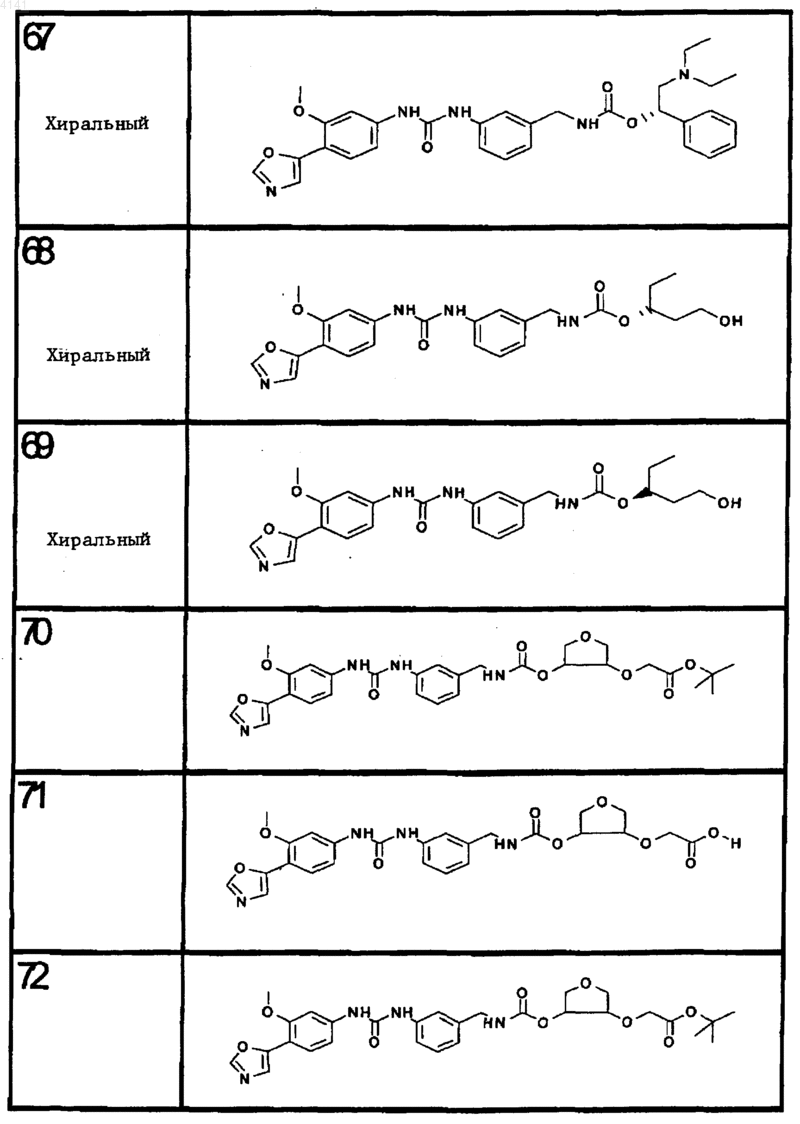
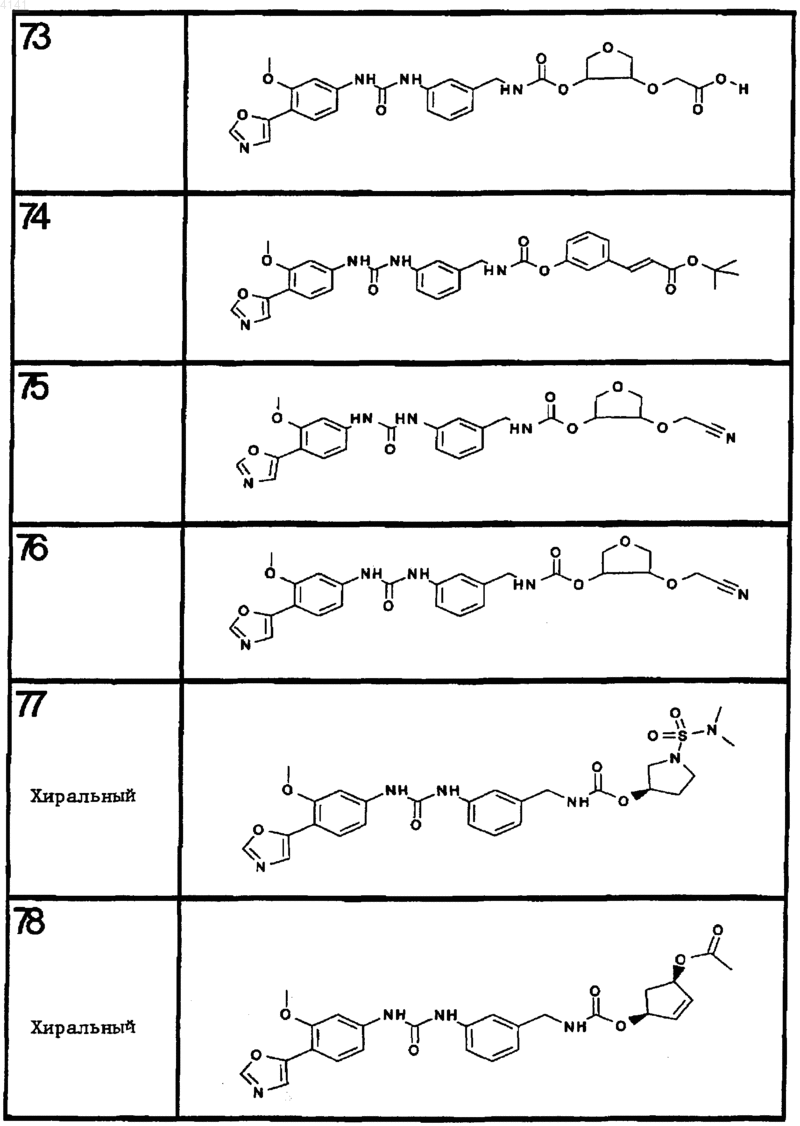
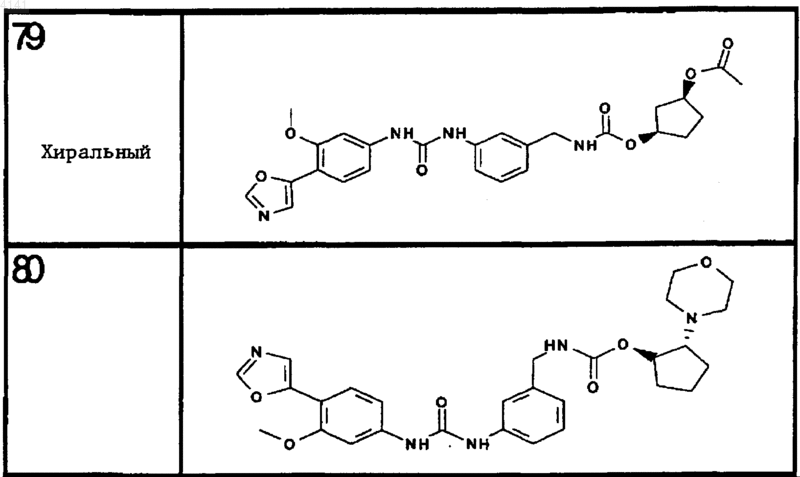
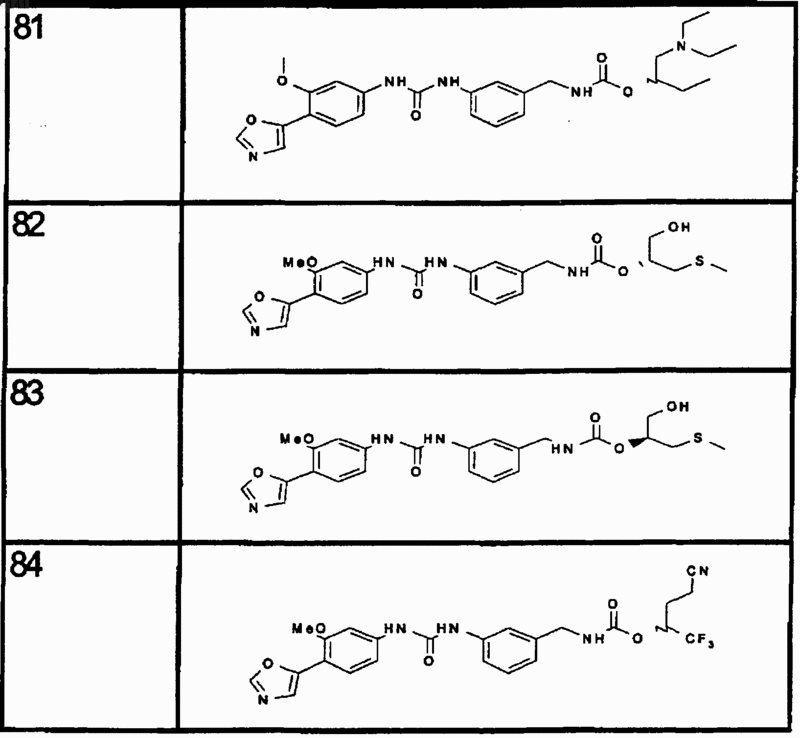
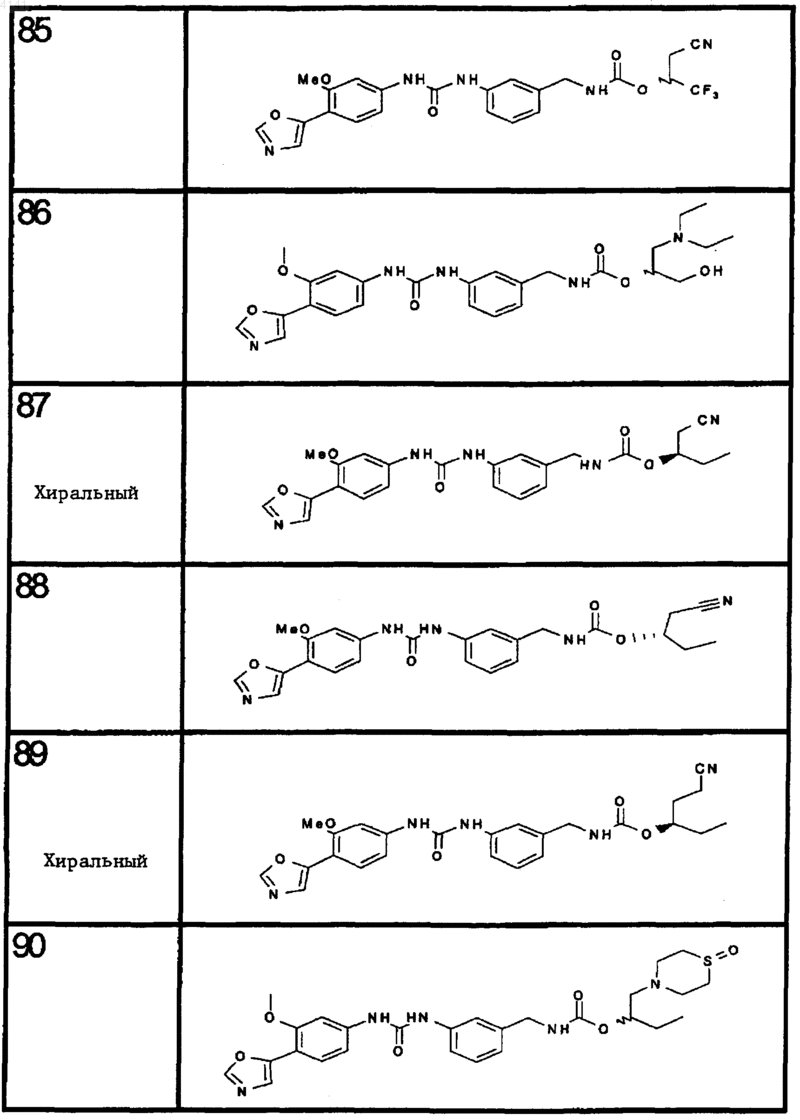
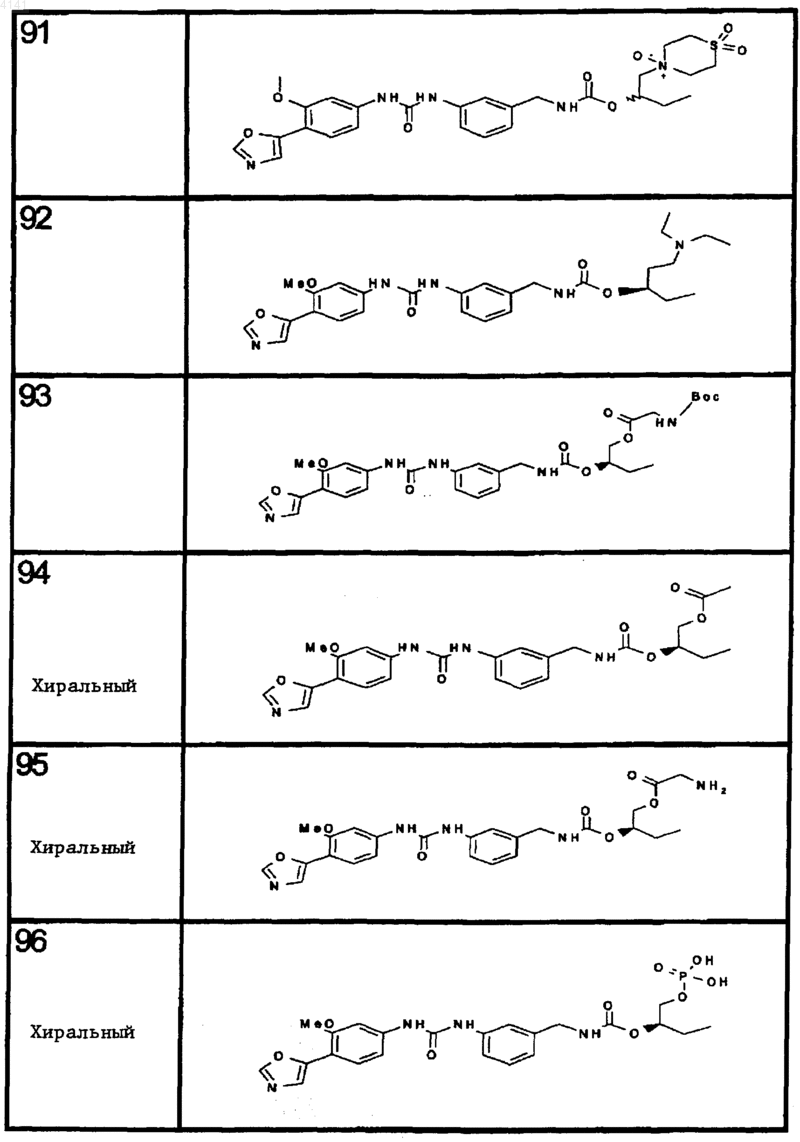
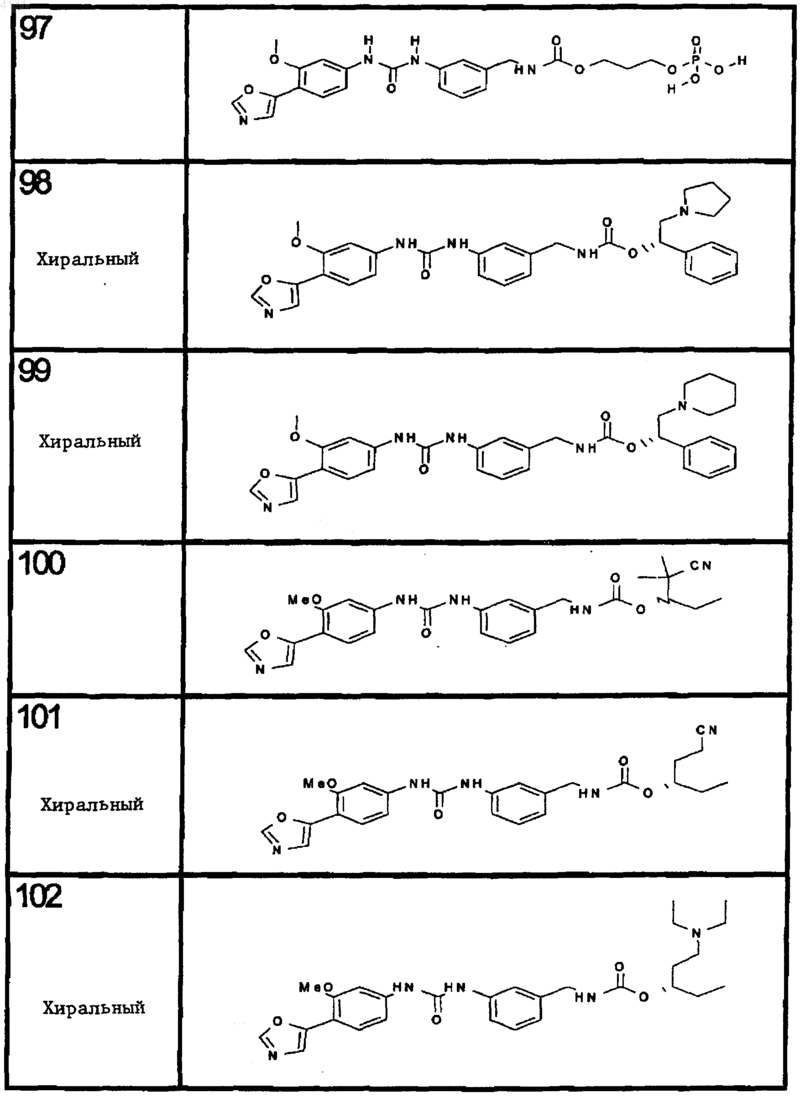
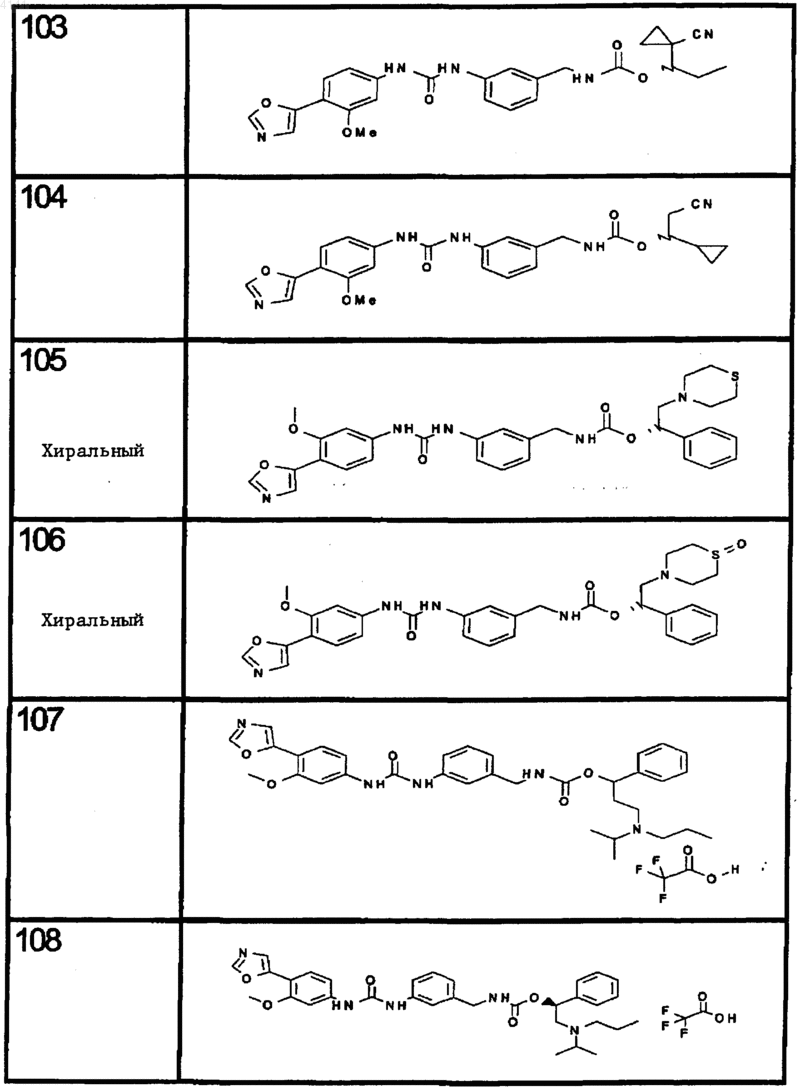
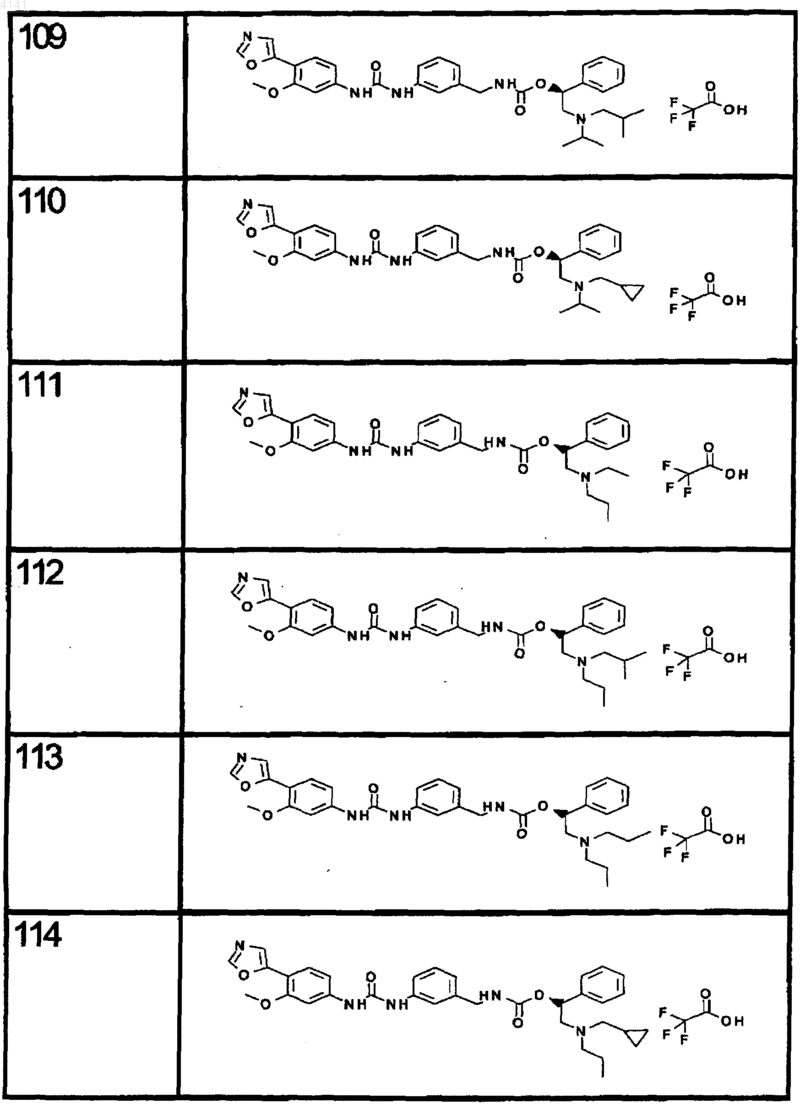
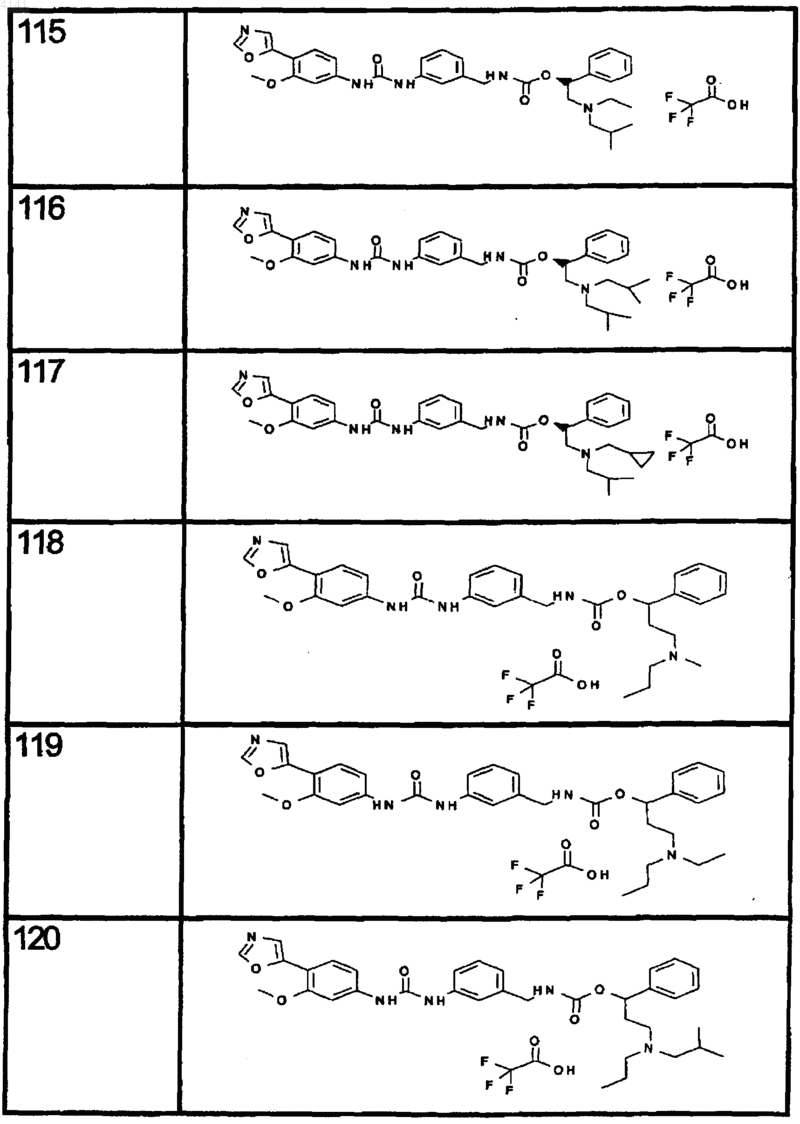
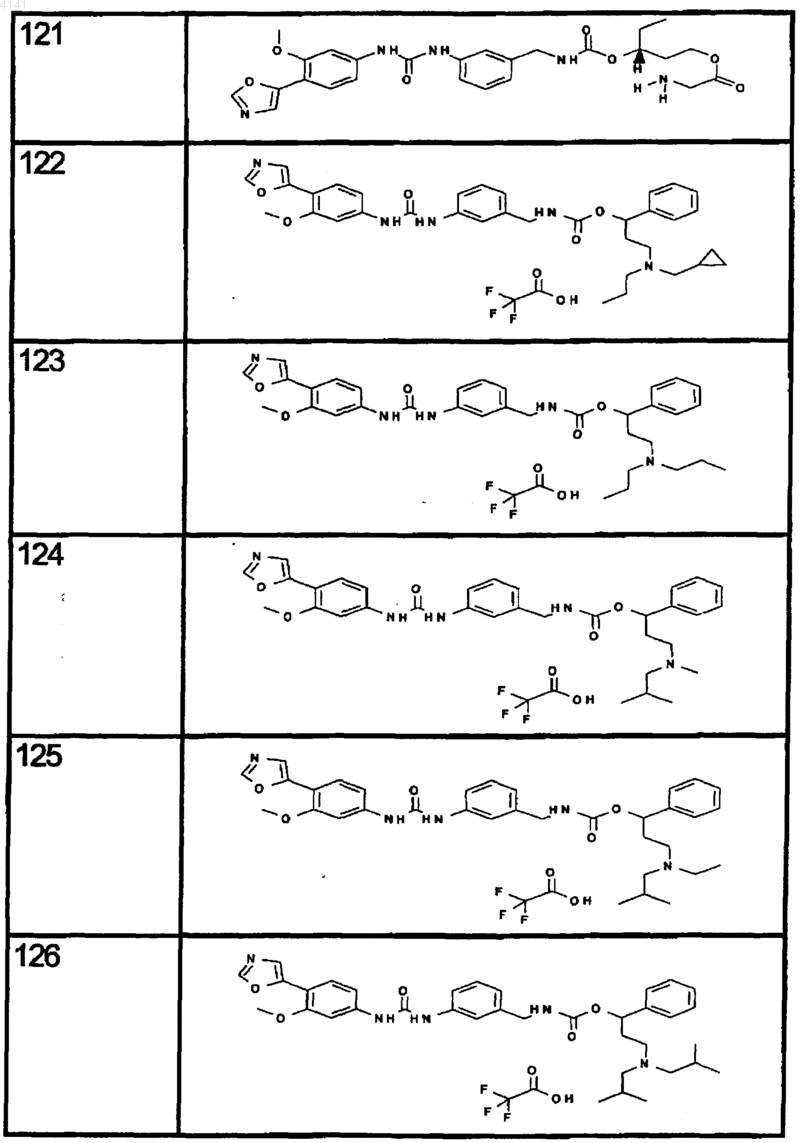
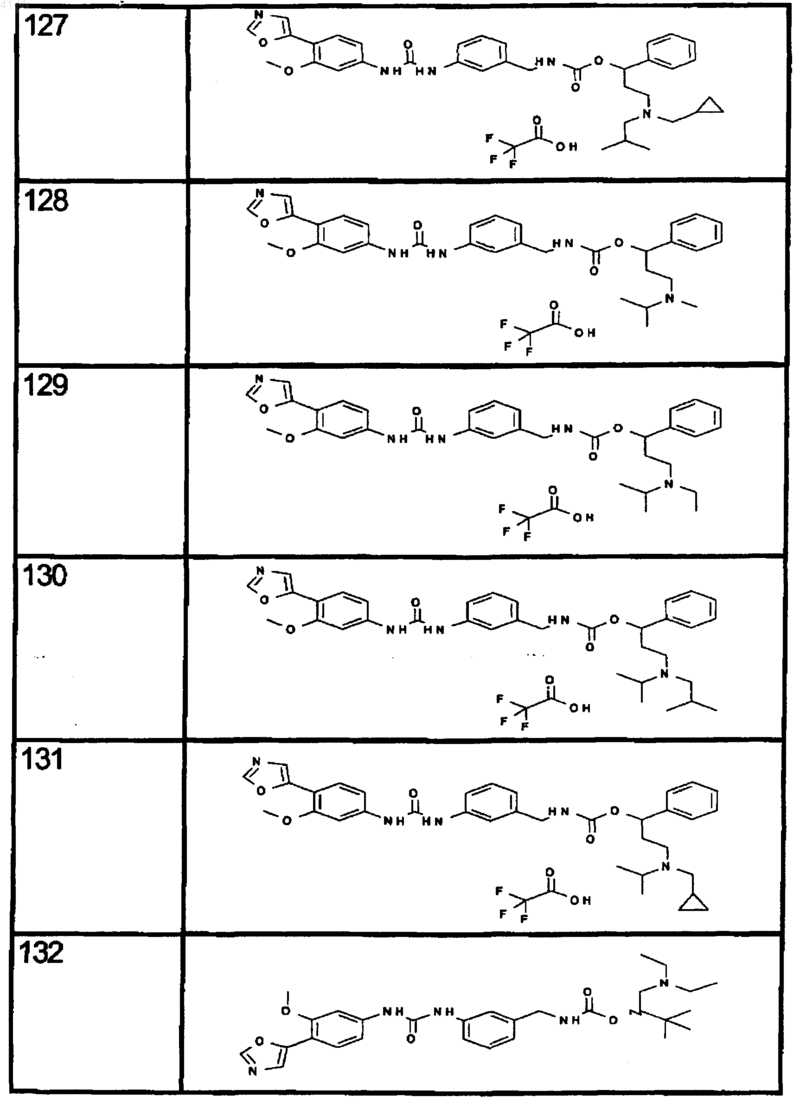
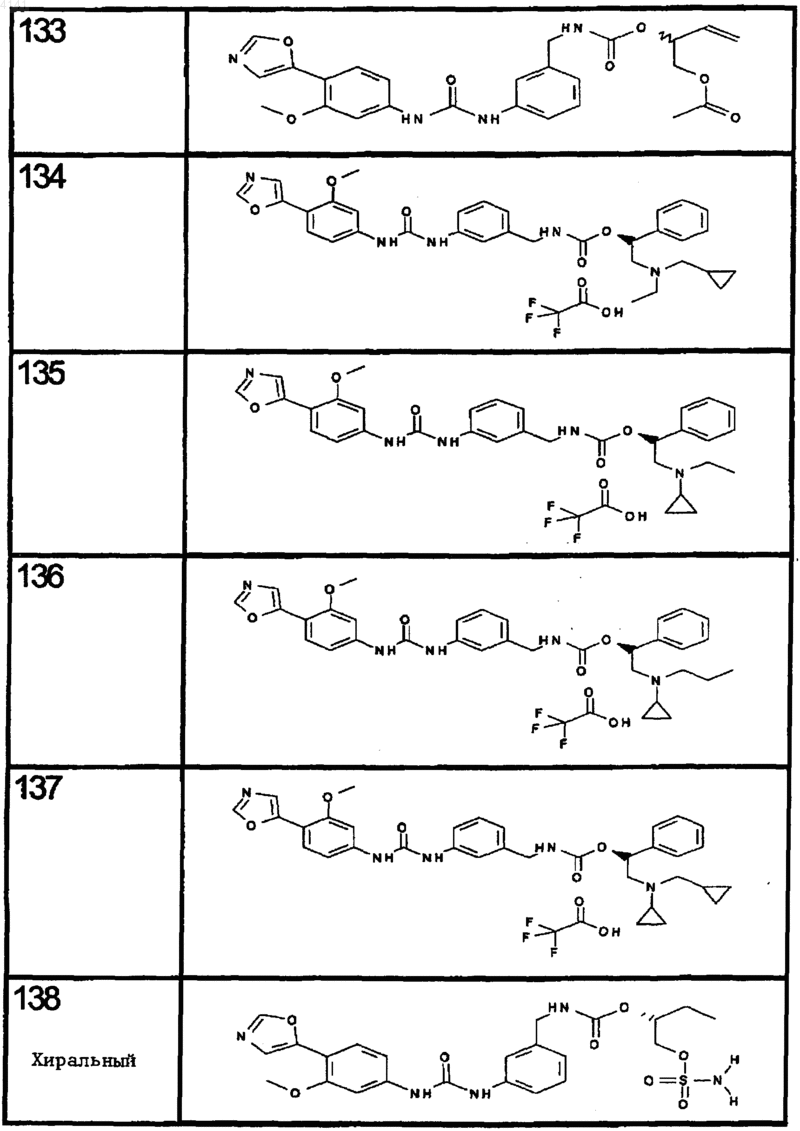

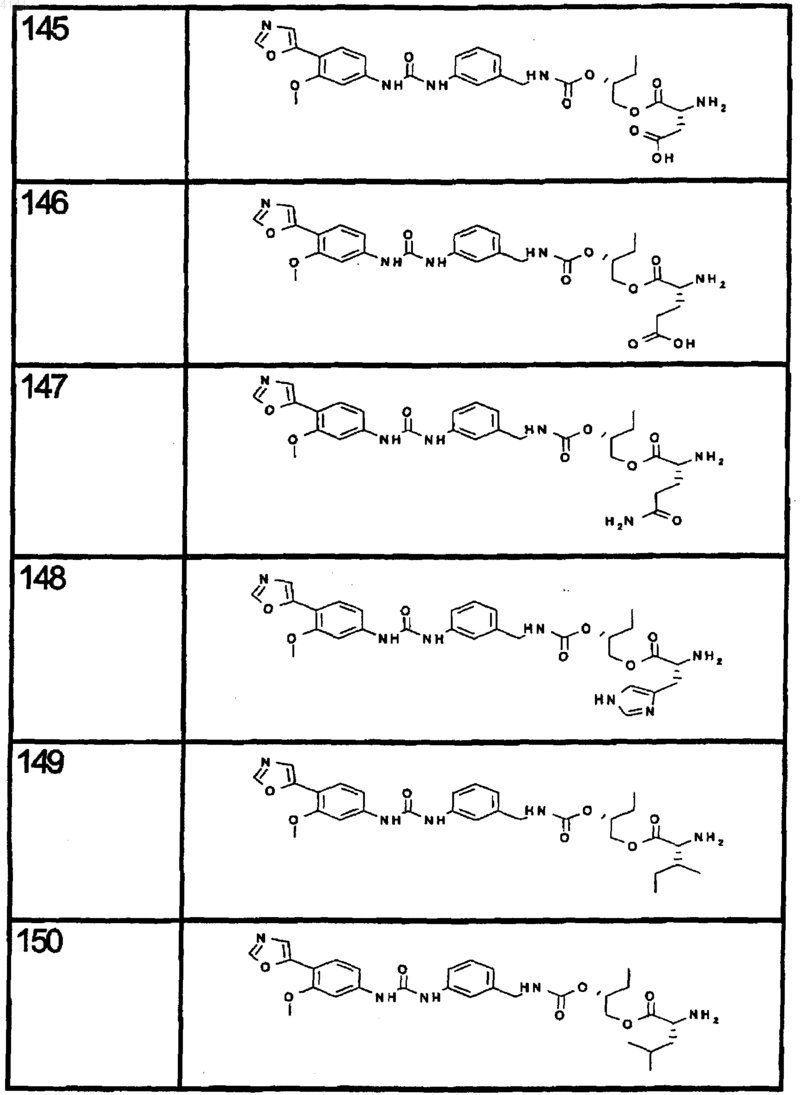
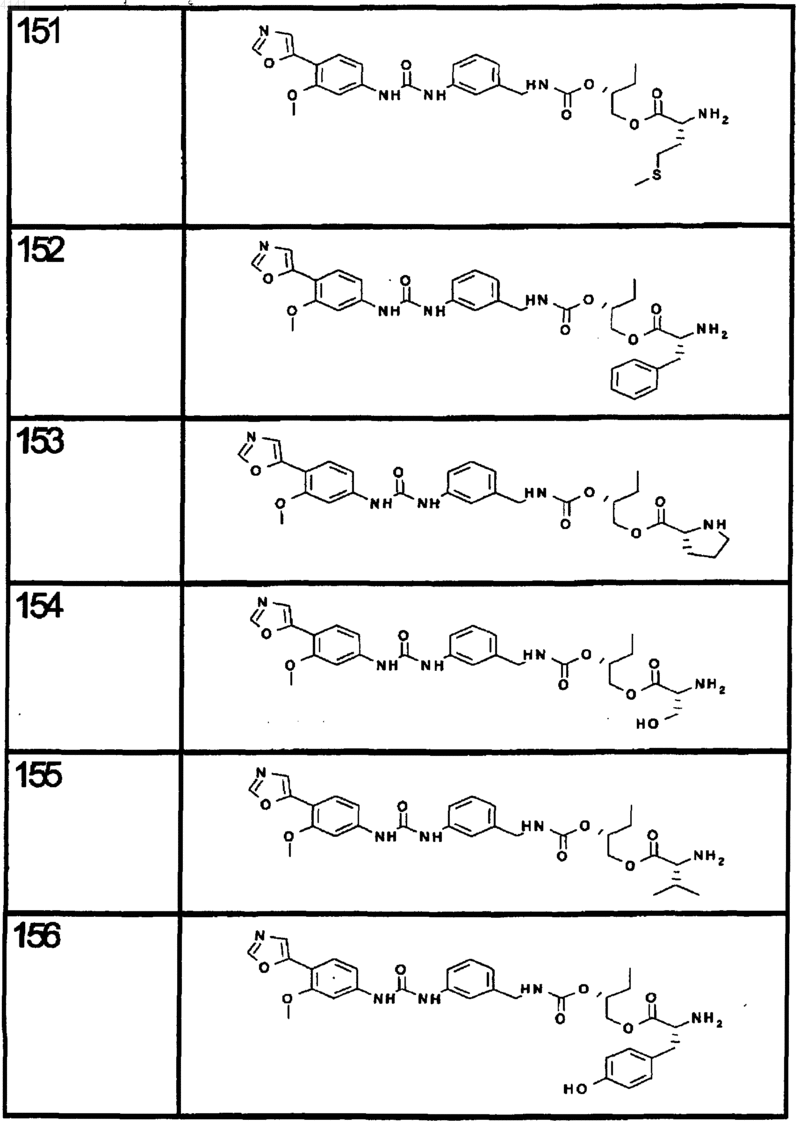
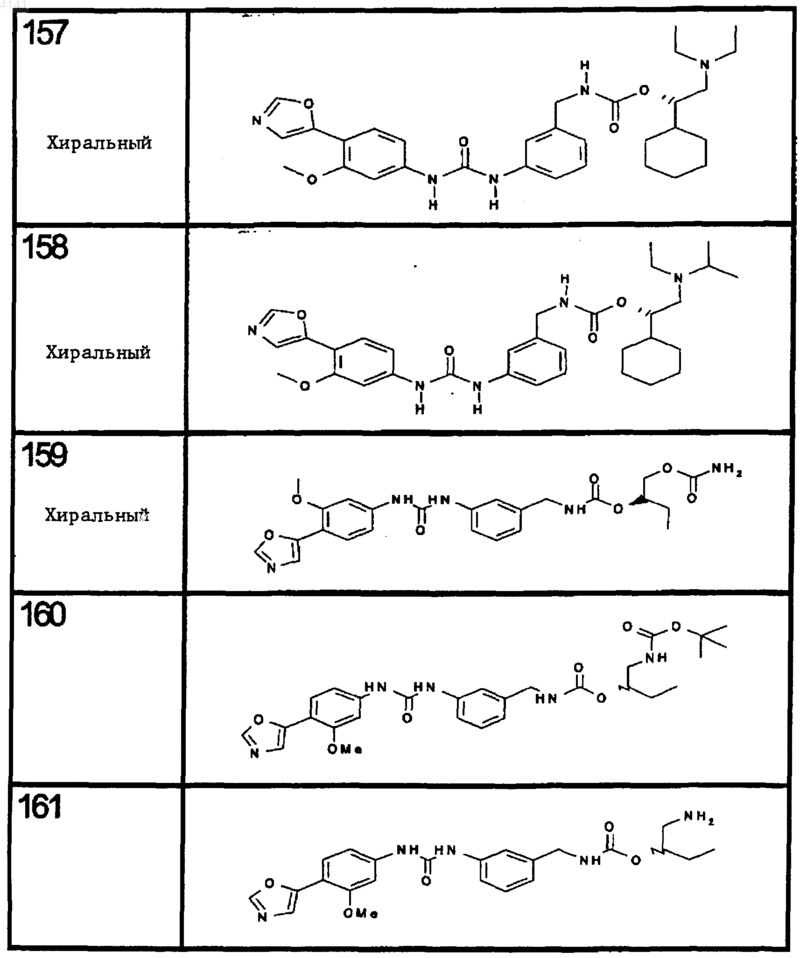
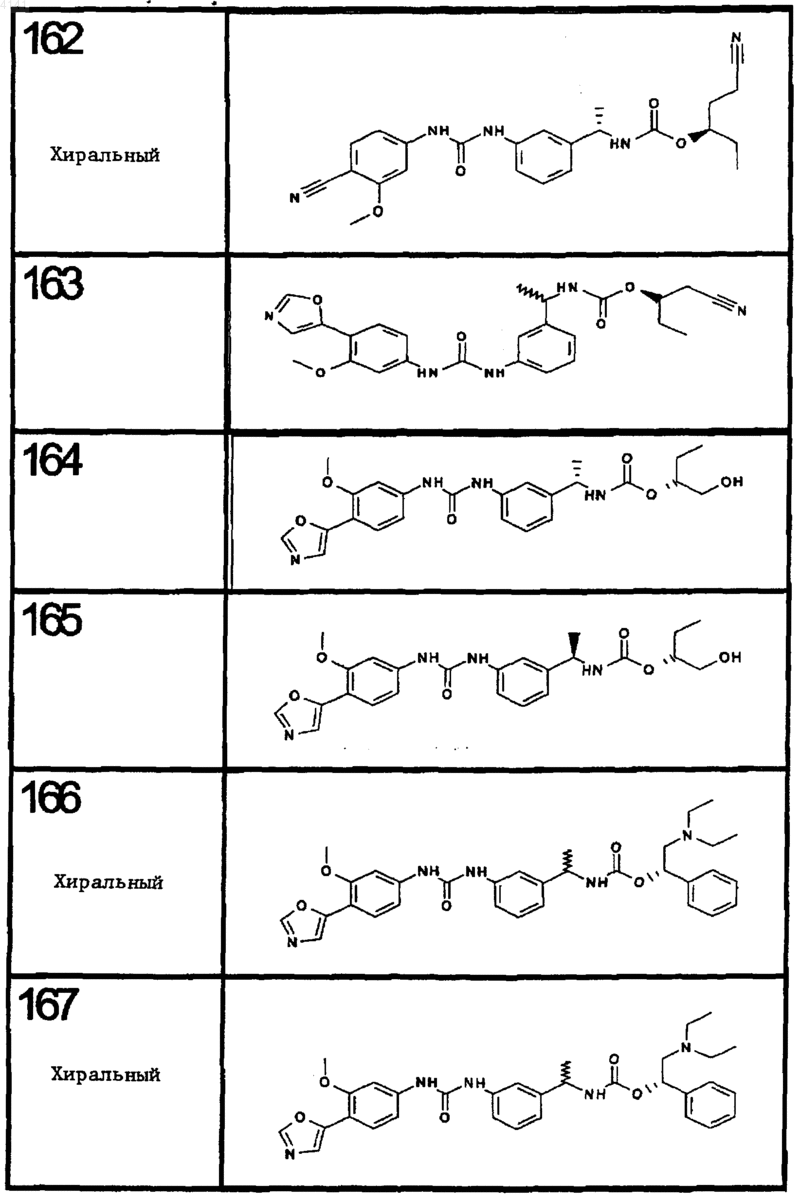
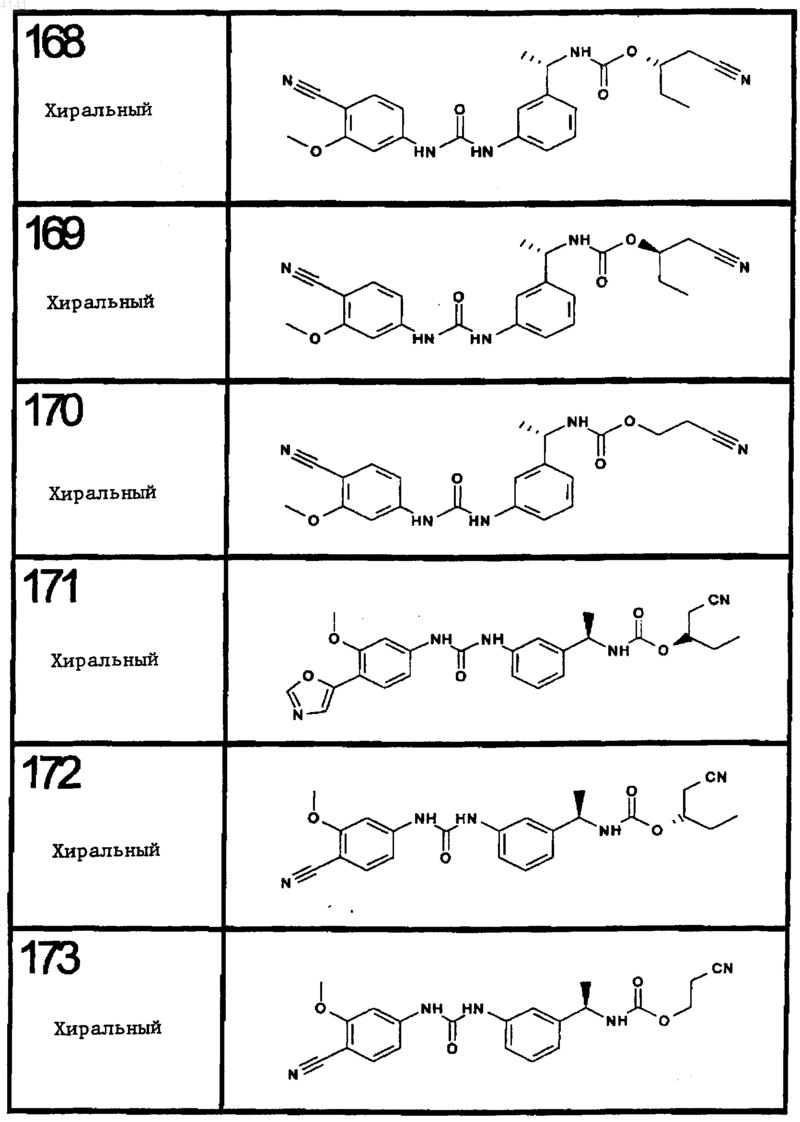
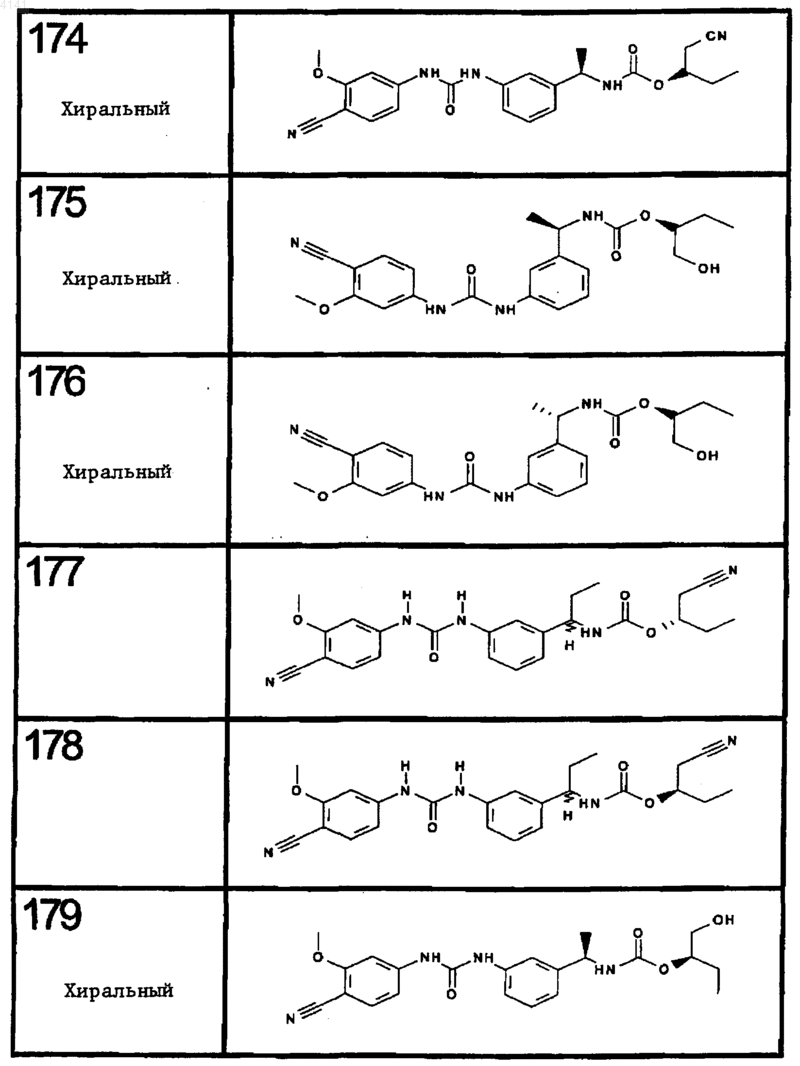
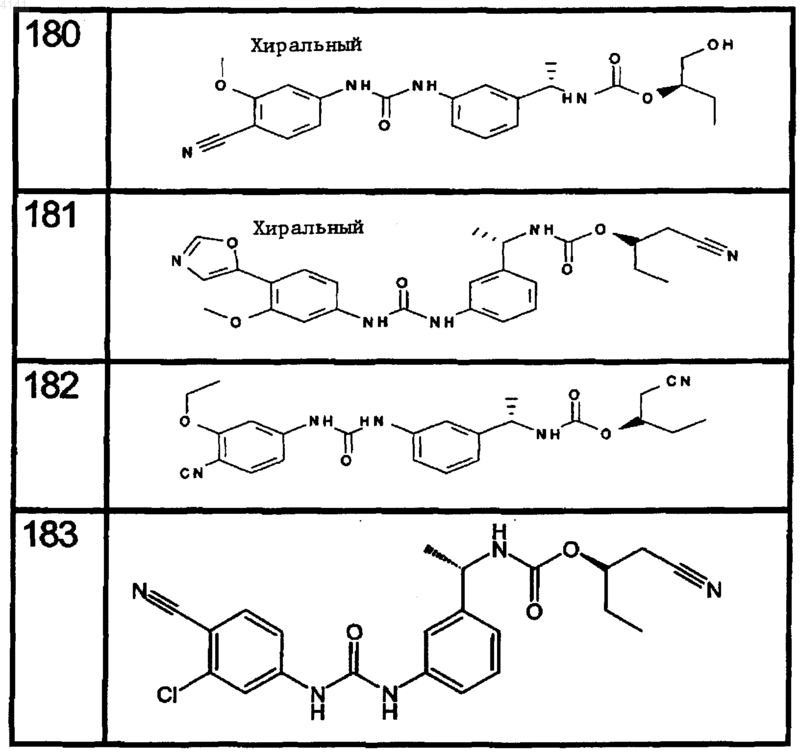
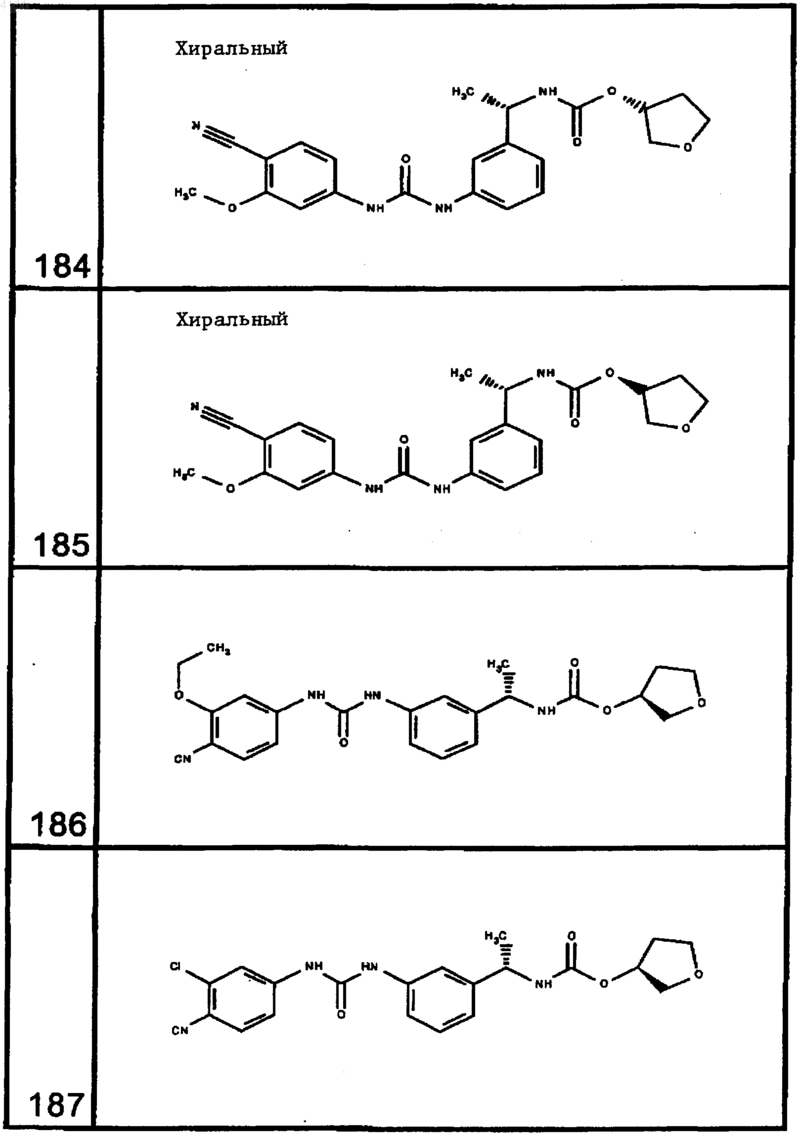
11. Соединение по п. 10, представляющее собой соединение, выбранное из соединений 1, 23, 26, 27, 29, 32, 76, 80, 87, 89, 98, 101, 103, 104, 106, 108, 110, 157, 163, 169, 171, 181, 185, 186 или 187
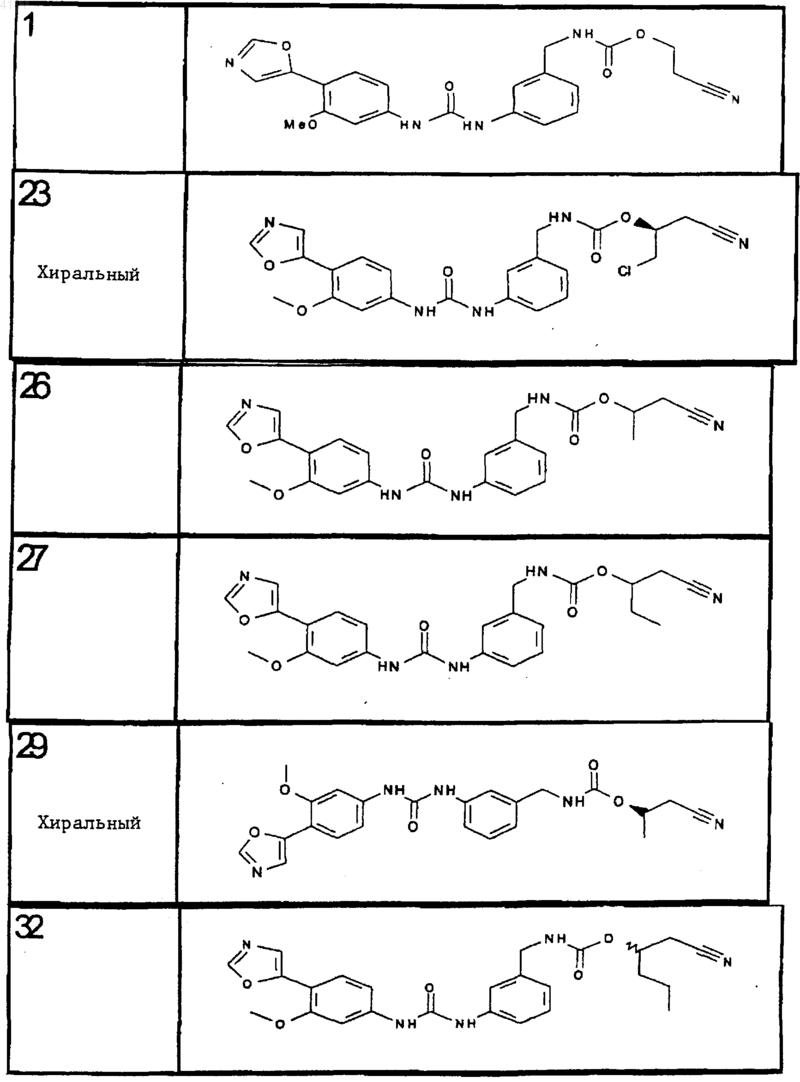
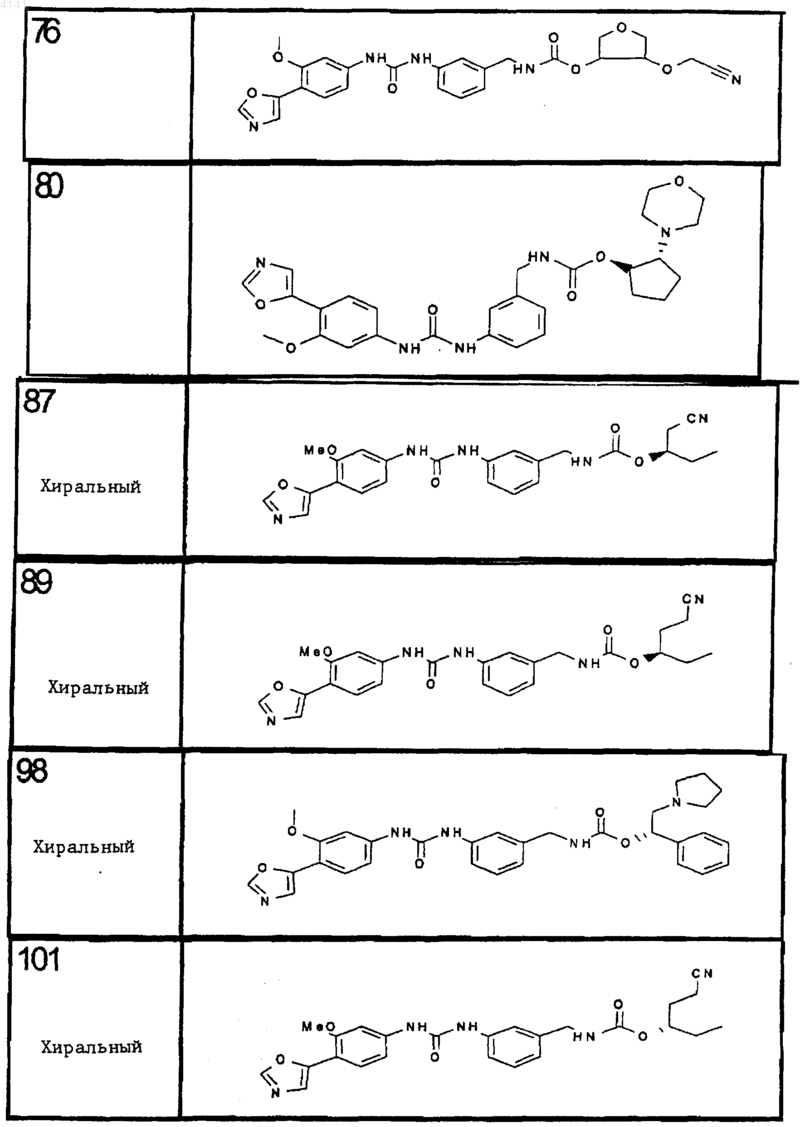
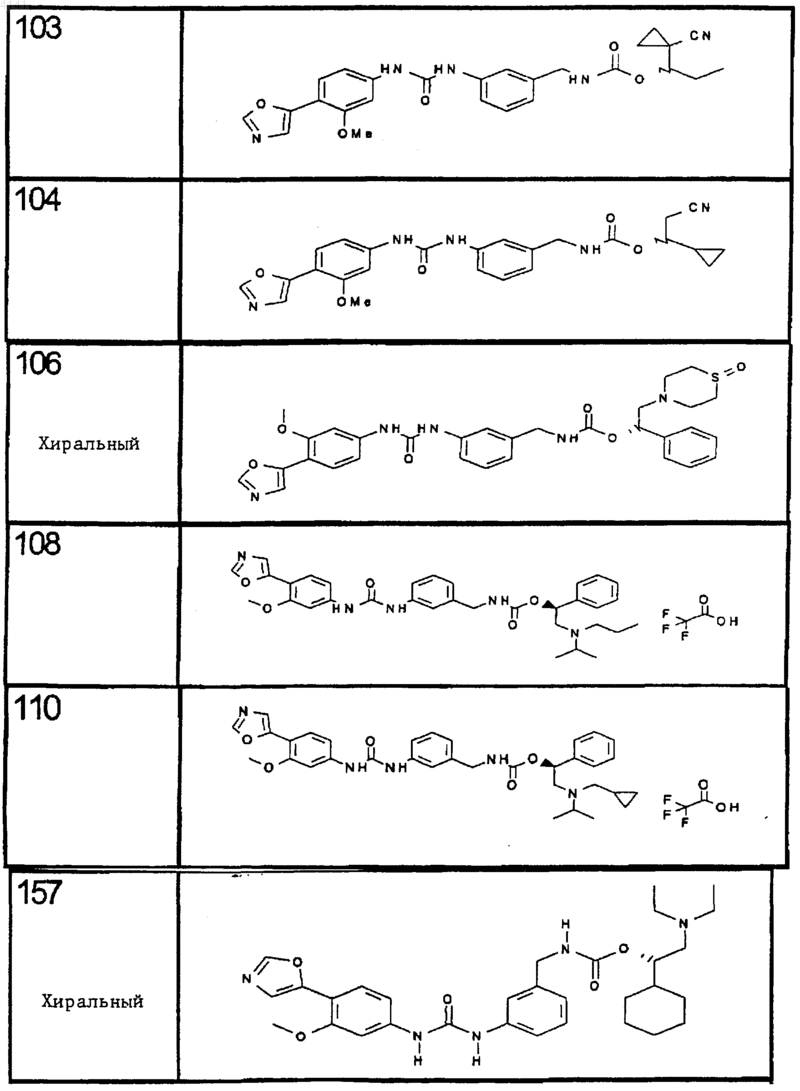
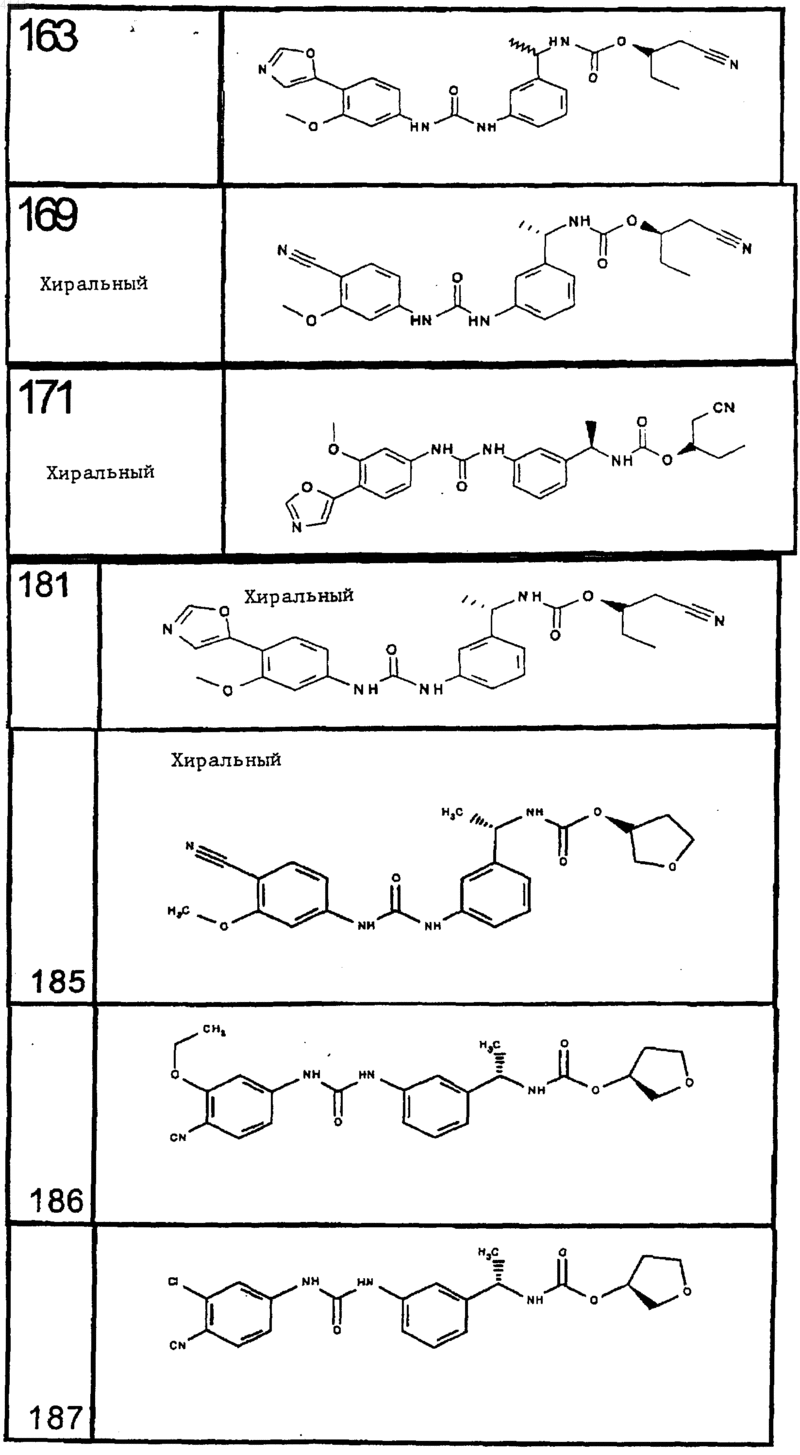
12. Композиция, включающая соединение по п.1 в количестве, эффективном для ингибирования IMPDH, и фармацевтически приемлемый носитель, адъювант или наполнитель.
13. Композиция по п.12, включающая дополнительно агент, выбранный из иммунодепрессанта, противоракового агента, противовирусного агента, противовоспалительного агента, противогрибкового агента, антибиотика или соединения против гиперпролиферации сосудов.
14. Способ лечения или профилактики IMPDH-опосредованного заболевания или состояния у млекопитающего, включающий стадию введения указанному млекопитающему композиции в соответствии с п.12 или 13.
15. Способ по п.14, в котором указанное IMPDH-опосредованное заболевание или состояние включает отторжение трансплантата, реакцию "трансплантат против хозяина", аутоиммунное заболевание.
16. Способ по п.14, в котором указанному млекопитающему вводят дополнительный иммунодепрессант в виде отдельной дозированной формы или как часть указанной композиции.
17. Способ ингибирования вирусной репликации у млекопитающего, включающий стадию введения указанному млекопитающему композиции в соответствии с п.12 или 13.
18. Способ по п.17, в котором вирусная инфекция вызвана вирусом, выбранным из ортомиксовируса, парамиксовируса, вируса герпеса, ретровируса, флавивируса, пестивируса, гепатотрофического вируса, бунъявируса (bunyavirus), вируса Hantaan, вируса Caraparu, вируса папилломы человека, вируса энцефалита, вируса арены, реовируса, вируса везикулярного стоматита, риновируса, энтеровируса, вируса лихорадки Ласса, тогавируса, вируса, вызывающего высыпания на коже, аденовируса, кори или краснухи.
19. Способ по п.17, в котором указанному млекопитающему вводят дополнительный противовирусный агент в виде отдельной дозированной формы или как часть указанной композиции.
20. Способ ингибирования сосудистой клеточной пролиферации у млекопитающего, включающий стадию введения указанному млекопитающему композиции в соответствии с п.12 или 13.
21. Способ по п.20, в котором указанный способ может быть использован для лечения или профилактики рестеноза, стеноза, атеросклероза или других гиперпролиферативных сосудистых заболеваний.
22. Способ по п.20, в котором указанному млекопитающему вводят дополнительный агент, предотвращающий гиперпролиферацию сосудов, в виде отдельной дозированной формы или как часть указанной композиции.
23. Способ ингибирования опухолей и рака у млекопитающего, включающий стадию введения указанному млекопитающему композиции в соответствии с п.12 или 13.
24. Способ по п.23, в котором указанный способ может быть использован для лечения или профилактики лимфомы, лейкемии и других видов рака.
25. Способ по п.24, в котором указанному млекопитающему вводят дополнительно противоопухолевый или противораковый агент в виде отдельной дозированной формы или как часть указанной композиции.
26. Способ ингибирования воспаления или воспалительного заболевания у млекопитающего, включающий стадию введения указанному млекопитающему композиции в соответствии с п.12 или 13.
27. Способ по п.26, в котором указанный способ может быть использован для лечения или профилактики остеоартрита, острого панкреатита, хронического панкреатита, астмы или респираторного дистресс-синдрома взрослых.
28. Способ по п.27, в котором указанному млекопитающему вводят дополнительно противовоспалительный агент в виде отдельной дозированной формы или как часть указанной композиции.
Текст
1 Область техники настоящего изобретения По данной заявке испрашивается приоритет на основании предварительной заявки США,серийный номер 60/125507, поданной 19 марта 1999 г., а также предварительной заявки США,серийный номер 60/174882, поданной 7 января 2000 г. Настоящее изобретение относится к соединениям, ингибирующим IMPDH. Данное изобретение также относится к фармацевтическим композициям, включающим указанные соединения. Соединения и фармацевтические композиции в соответствии с данным изобретением особенно хорошо подходят для ингибирования активности фермента IMPDH и, следовательно, могут быть наилучшим образом использованы в качестве терапевтических агентов дляIMPDH-опосредуемых процессов. Данное изобретение также относится к способам ингибирования активности IMPDH с применением соединений в соответствии с настоящим изобретением и родственных им соединений. Предпосылки изобретения Синтез нуклеотидов в организмах необходим для деления и репликации в них клеток. Синтез нуклеотидов у млекопитающих может быть осуществлен одним или двумя путями: путем синтеза de novo или путем утилизации имеющихся. Различные виды клеток используют указанные пути в различной степени. Инозин-5'-монофосфат дегидрогеназы(1993)]. Прокариотные формы имеют 30-40% идентичности последовательностей с ферментом человека. Две изоформы IMPDH человека,обозначенные как тип I и тип II, были идентифицированы и секвенированы [F.R. Collart andE. Huberman, J. Biol. Chem., 263, pp. 1576915772 (1988); Y. Natsumeda et al., J. Biol. Chem.,265, pp. 5292-5295, (1990)]. Каждая из них включает 514 аминокислот, имеющих 84% идентичности последовательностей. Как тип I,так и тип II IMPDH образуют в растворе активные тетрамеры с молекулярной массой субъединиц, составляющей 56 kDa [Y. Yamada et al.,Biochemistry, 27, pp. 2737-2745 (1988)].De novo синтез нуклеотидов гуанозина и,следовательно, активность IMPDH, особенно важна в В- и Т-лимфоцитах. Такие клетки зависят от de novo способа, а не от способа утилизации, для выработки достаточного уровня нуклеотидов, чтобы инициировать пролифератив 004141 2 ный ответ на митоген или антиген [А.С. Allisonet al., Lancet II, 1179 (1975) и А.С. Allison et al.,Ciba Found. Symp., 48, 207 (1977)]. Таким образом, IMPDH является привлекательной целью для селективного ингибирования иммунной системы без сопутствующего ингибирования пролиферации других клеток. Иммуносупрессия обеспечивалась путем ингибирования различных ферментов, включая,например, кальцийнейринфосфатазу (ингибируемую циклоспорином и FK-506); дигидрооротат дегидрогеназу, фермент, участвующий в биосинтезе пиримидинов (ингибируемых лефлуномидом и брехинаром); киназу FRAP (ингибируемую рапамицином); и белок теплового шока hsp70 (ингибируемый дезоксиспергуалином). [См. B.D. Kahan, Imminological Reviews,136, pp. 29-49 (1993); R.E. Morris, The Journal ofHeart and Lung Transplantation, 12(6), pp. S275S286 (1993)]. Ингибиторы IMPDH также известны. Патенты США 5380879 и 5444072, а также публикации РСТ WO 94/01105 и WO 94/12184 описывают микофенолкислоту (МРА) и ее производные в качестве сильных, неконкурентных, обратимых ингибиторов IMPDH человека, тип I(Ki=33 нМ) и тип II (Ki=9 нМ). Была продемонстрирована способность МРА блокировать ответ В- и Т-клеток на митоген или антиген [А. С.Allison et al., Ann. N. Y. Acad. Sci., 696, 63,(1993)]. Иммунодепрессанты, такие как МРА, могут быть использованы при лечении отторжения трансплантата и аутоиммунных заболеваний(1996)]. Однако MPA характеризуется нежелательными фармакологическими свойствами,такими как желудочно-кишечная токсичностьIMPDH. [L. Hedstrom, et al., Biochemistry, 29, pp. 849-854 (1990)]. Однако указанные соединения обладают недостаточной специфичностью по отношению к IMPDH. Недавно было установлено, что микофенолат мофетил, пролекарство, быстро освобождающее MPA in vivo, предотвращает острое почечное отторжение аллотрансплантата после пересадки почки. [L. M. Shaw et al., TherapeuticSollinger, Transplantation, 60, pp. 225-232 (1995)]. Однако некоторые клинические наблюдения ограничивают лечебный потенциал данного лекарственного препарата. [L. M. Shaw et al.,Therapeutic Drug Monitoring, 17, pp. 690-699(1993)]. Затем глюкуронид подвергается энтерогепатическому рециркулированию, вызывая 3 аккумуляцию МРА в желудочно-кишечном тракте, где он не может оказывать свое IMPDHингибирующее действие на иммунную систему. Это эффективно снижает действенность лекарственного препарата in vivo, в то же время усиливая его нежелательное действие в желудочнокишечном тракте. Недавно в публикациях РСТ WO 97/40028 и WO 98/40381 были описаны ингибиторыIMPDH различных классов. Также известно, что IMPDH играет определенную роль в других метаболических процессах. Повышенная активность IMPDH наблюдалась в быстро пролиферирующих линиях лейкозных клеток человека и других линиях опухолевых клеток, обозначая IMPDH в виде цели для противораковой, а также иммуноподавляющей химиотерапии [M. Nagai et al., Cancer Res., 51,pp. 3886-3890 (1991)]. Было также показано, чтоIMPDH играет роль в пролиферации клеток гладких мышц, демонстрируя тем самым, что ингибиторы IMPDH, такие как МРА или рапамицин, могут быть использованы для профилактики рестеноза или других гиперпролиферативных сосудистых заболеваний [C.R. Gregory etal., Transplantation, 59, pp. 655-61 (1995); публикация РСТ WO 94/12184; и публикация РСТ WO 94/01105]. Кроме того, было установлено, что IMPDH играет определенную роль в вирусной репликации в некоторых зараженных вирусами линиях клеток. [S.F. Carr, J. Biol. Chem., 268, pp. 2728627290 (1993)]. Подобно лимфоцитам, а также линиям лимфоцитарных и опухолевых клеток,смысл заключается в том, что путь de novo, a не путь утилизации, является критическим в процессе вирусной репликации. Таким образом, сохраняется потребность в эффективных ингибиторах IMPDH с улучшенными фармакологическими свойствами. Такие ингибиторы обладают терапевтической эффективностью в качестве иммунодепрессантов,противораковых агентов, сосудистых противогиперпролиферативных агентов, противовоспалительных, противогрибковых, антипсориатических и противовирусных веществ. Краткое описание изобретения Настоящее изобретение предусматривает соединения и их фармацевтически приемлемые производные, которые могут быть использованы как ингибиторы IMPDH. Соединения в соответствии с данным изобретением могут применяться отдельно или в сочетании с другими терапевтическими или профилактическими агентами, такими как противовирусные, противовоспалительные агенты, антибиотики и иммунодепрессанты для лечения или профилактики отторжения трансплантата и аутоиммунных заболеваний. Кроме того, указанные соединения могут быть использованы сами по себе или в сочетании с другими агентами как терапевтические и 4 профилактические средства для противовирусных, противоопухолевых, противовоспалительных, противогрибковых агентов, в схемах антипсориатической иммуноподавляющей химиотерапии и лечения рестеноза. Данное изобретение также предусматривает фармацевтические композиции, включающие соединения в соответствии с настоящим изобретением, а также многокомпонентные композиции, включающие дополнительные соединения IMPDH, вместе с иммунодепрессантом. Данное изобретение также предусматривает способы применения соединений в соответствии с настоящим изобретением, равно как и других родственных соединений, для ингибирования IMPDH. Подробное описание изобретения С целью более полного понимания описываемого здесь изобретения предлагается следующее подробное описание. В описании использованы следующие сокращения: Обозначение Ас Реагент или фрагмент Ацетил Метил Этил Бензил Карбонилдиимидазол 1,8-Диазабицикло[5.4.0] ундец-7-ен Диизопропилэтиламин Диметиламинопиридин Диметилформамид Диметилсульфоксид Дифенилфосфорилазид Гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида Этилацетат Изопропиловый спирт Ацетонитрил Тетрагидрофуран Триэтиламин трет-Бутил Бутилоксикарбонил В данном описании использованы следующие термины: Если четко не указано иначе, то термины"-SO2-" и "-S(O)2-" в данном описании относятся к сульфону или его производному (т.е. обе присоединенные группы, связанные с S), а не к сложному сульфинатному эфиру. Термины "гало" или "галоген" относятся к радикалу фтора, хлора, брома или иода. Термин "иммунодепрессант" относится к соединению или лекарственному препарату,обладающему действием, ингибирующим иммунный ответ. Примеры таких агентов включают циклоспорин А, FK506, рапамицин, лефлуномид, дезоксиспергуалин, преднизон, азатиоприн, микофенолат мофетил, ОКТЗ, ATAG, интерферон и мизорибин. Термин "интерферон" относится ко всем видам интерферонов, включая, но не ограничиваясь ими, альфа-, бета- и гамма-интерферон. 5 роль в метаболическом пути данного заболевания. Примеры IMPDH-опосредуемых заболеваний включают отторжение трансплантата и аутоиммунные заболевания, такие как ревматоидный артрит, рассеянный склероз, ювенильный диабет, астма и воспалительное заболевание кишечника, рак, вирусно-репликационные и сосудистые заболевания. Например, соединения, композиции и способы их применения в соответствии с данным изобретением могут быть использованы для лечения отторжения трансплантата (например,почка, печень, сердце, легкое, поджелудочная железа (островковые клетки), костный мозг,роговица, аллотрансплантаты тонкой кишки и кожи и ксенотрансплантаты сердечного клапана), ревматоидного артрита, рассеянного склероза, ювенильного диабета, астмы, воспалительного заболевания кишечника (болезнь Крона, язвенный колит), волчанки, сахарного диабета, тяжелой миастении, псориаза, дерматита,экземы, себореи, воспаления легких, увеита глаз, гепатита, болезни Грейвса, тироидита Хашимото, синдрома Бехчета или Шегрена (сухие глаза/рот), пернициозной или иммуногемолитической анемии, идиопатической недостаточности надпочечников, полиригландулярного аутоиммунного синдрома и гломерулонефрита,склеродермии, красного плоского лишая, вителиго (депигментация кожи), аутоиммунного тироидита и альвеолита, воспалительных заболеваний, таких как остеоартрит, острого панкреатита, хронического панкреатита, астмы и респираторного дистресс-синдрома взрослых, а также для лечения рака и опухолей, таких как твердые опухоли, лимфом и лейкемии, сосудистых заболеваний, таких как рестеноз, стеноз и атеросклероз, и вирусно-репликационных заболеваний ДНК и РНК, таких как ретровирусные заболевания, и герпеса. Кроме того, известно также, что ферментыIMPDH присутствуют в бактериях и могут таким образом регулировать бактериальный рост. Как таковые, соединения, ингибирующиеIMPDH, композиции и описываемые здесь способы могут быть использованы для лечения или профилактики бактериальных инфекций, по отдельности или в сочетании с другими антибиотиками. Применяемый в данном описании термин"лечение" относится к облегчению симптомов конкретного нарушения у пациента или улучшению поддающихся определению измерений,ассоциируемых с конкретным нарушением. В данном описании термин "пациент" относится к млекопитающему, включая человека. Термины "HBV", "HCV" и "HGV" относятся к вирусам гепатита В, С и G, соответственно. В соответствии с одним из вариантов его осуществления данное изобретение предусматривает соединения формулы А: в которой каждый из R1 и R2 независимо выбран из группы, включающей водород; -СF3; - (C1-C6) прямолинейный или разветвленный алкил; -(С 2 С 6)-прямолинейный или разветвленный алкенил или алкинил; -(C1-C6)-прямолинейный или разветвленный алкил-R7; -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7; и в которой по меньшей мере один изR1 или R2 представляет -(C1-С 6)-прямолинейный или разветвленный алкил-R7; -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7,в которой вплоть до 4 атомов углерода в любом из указанных алкилов, алкенилов или алкинилов необязательно и независимо заменены группой R3; и в которой один или оба из R1 или R2 необязательно этерифицированы с образованием пролекарства; или, альтернативно, R1 и R2, взятые вместе,образуют тетрагидрофуранил, в которой когдаR9 представляет водород, (R)-метил, (R)-этил или (R)-гидроксиметил, один атом водорода в указанном тетрагидрофуране заменен группой(S)-метил, (S)-этил или (S)-гидроксиметил, то один атом водорода в указанном тетрагидрофуране необязательно заменен группой -OR6 или-(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил, то часть соединения,представленного -CH(R1)R2, представляет C5-C12 прямолинейный или разветвленный алкил, алкенил или алкинил; каждый R3 независимо выбран из галогена,CN, -OR4 или -N(R5)2;R4 выбран из группы, включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, - (С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил, -[(C1-C6)прямолинейный или разветвленный алкил ]-R7,-[(С 2-С 6) -прямолинейный или разветвленный алкенил или алкинил]-R7, -С(О)-[(C1-C6)прямолинейный или разветвленный алкил],-С(О)-[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-[(C1-C6)прямолинейный или разветвленный алкил]N(R8)2, -С(O)-[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-N(R8)2,-P(O)(OR8)2, -P(O) (OR8)(R8), -C(O)-R7, -[(С 1-С 6)-S(O)2N(R5)2 или -[(С 2-С 6) -прямолинейный или разветвленный алкенил или алкинил]-CN; каждый R5 независимо выбран из группы,включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, -(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил,-[(C1-С 6)-прямолинейный или разветвленный алкил]-R7, -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-R7, -[(C1-С 6)прямолинейный алкил]-CN, -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-СN, -[(C1-C6)-прямолинейный или разветвленный алкил]-OR4, -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-ОR4,-С(O)-(C1-C6)-прямолинейный или разветвленный алкил, -С(О)-[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-R7,-C(O)O-R7, -С(О)О-(C1-C6)-прямолинейный или разветвленный алкил, -С(О)О-[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил], -S(O)2-(C1-С 6)-прямолинейный или разветвленный алкил или -S(O)2-R7; или два фрагмента R5, когда связаны с одним и тем же атомом азота, соединены вместе с указанным атомом азота, образуя 3-7-членное гетероциклическое кольцо, в котором указанное гетероциклическое кольцо необязательно содержит от 1 до 3 дополнительных гетероатомов, независимо выбранных из N, О, S, S(О) или S(O)2;R6 выбран из -С(O)-СН 3, -СН 2-С(O)-ОН,-СН 2-С(O)-O-трет-Bu, -CH2-CN или -CH2-CCH; каждый R7 представляет моноциклическую или бициклическую кольцевую систему, в которойi. каждое кольцо включает от 3 до 7 кольцевых атомов, независимо выбранных из С, N,О или S;ii. не более 4 кольцевых атомов выбраны из N, О или S;iii. любая СН 2 группа необязательно заменена группой С (О);iv. любой S необязательно заменен группой S(O) или S(O)2; каждый R8 независимо выбран из водорода или -[C1-C4]-прямолинейного или разветвленного алкила; где в любой кольцевой системе в указанном соединении вплоть до 3 атомов водорода,связанных с кольцевыми атомами, необязательно и независимо заменены галогеном, гидрокси,нитро, циано, амино, (C1-C4)-прямолинейным или разветвленным алкилом; O-(C1-C4)-прямолинейным или разветвленным алкилом, (C2-C4)прямолинейным или разветвленным алкенилом или алкинилом или O-(С 2-С 4)-прямолинейным или разветвленным алкенилом или алкинилом; и где кольцевая система необязательно бензоконденсирована;R11 выбран из галогена, -О-(C1-С 3)прямолинейного алкила или -O-(С 2-С 3) прямолинейного алкенила или алкинила. В объем формулы А также входят пролекарства, образуемые этерификацией любого изR1 или R2 или их обоих. Примерами таких пролекарств являются соединения от 143 до 156 в табл. 1, приведенной ниже. Термин "моноциклическая кольцевая система" в данном описании включает насыщенные, частично ненасыщенные и полностью ненасыщенные кольцевые структуры. Термин"бициклическая кольцевая система" в данном описании включает системы, в которых каждое кольцо независимо насыщено, частично ненасыщено и полностью ненасыщено. Примеры моноциклических и бициклических кольцевых систем, которые могут быть использованы в соединениях в соответствии с данным изобретением, включают, но не ограничиваются ими,циклопентан, циклопентен, индан, инден, циклогексан, циклогексен, циклогексадиен, бензол,тетрагидронафталин, декагидронафталин, нафталин, пиридин, пиперидин, пиридазин, пиримидин, пиразин, 1,2,3-триазин, 1,2,4-триазин,1,3,5-триазин, 1,2,3,4-тетразин, 1,2,4,5-тетразин,1,2,3,4-тетрагидрохинолин, хинолин, 1,2,3,4 тетрагидроизохинолин, изохинолин, циннолин,фталазин, хиназолин, хиноксалин, 1,5-нафтиридин, 1,6-нафтиридин, 1,7-нафтиридин, 1,8 нафтиридин, 2,6-нафтиридин, 2,7-нафтиридин,птеридин, акридин, феназин, 1,10-фенантролин,дибензопираны, 1-бензопираны, фенотиазин,феноксазин, тиантрен, дибензо-п-диоксин, феноксатиин, фенокстионин, морфолин, тиоморфолин, тетрагидропиран, пиран, бензопиран,1,4-диоксан, 1,3-диоксан, дигидропиридин, дигидропиран, 1-пириндин, хинуклидин, триазолопиридин, -карболин, индолизин, хинолизидин, тетрагидронафтеридин, диазафенантрены,тиопиран, тетрагидротиопиран, бензодиоксан,фуран, бензофуран, тетрагидрофуран, пиррол,индол, тиофен, бензотиофен, карбазол, пирролидин, пиразол, изоксазол, изотиазол, имидазол,оксазол, тиазол, 1,2,3-триазол, 1,2,4-триазол,1,2,3-оксадиазол, 1,2,4-оксадиазол, 1,3,4-оксадиазол, 1,2,5-оксадиазол, 1,2,3-тиадиазол, 1,2,4 тиадиазол, 1,3,4-тиадиазол, 1,2,5-тиадиазол, тетразол, бензотиазол, бензоксазол, бензотриазол,бензимидазол, бензопиразол, бензизотиазол,бензизоксазол и пурин. Дополнительные моноциклические и бициклические структуры, подпадающие под вышеприведенное описание, могут быть найдены в 9 Следует отметить, что гетероциклы могут быть прикреплены к остатку соединения через любой атом гетероцикла, что приводит к созданию устойчивой структуры. Термин "кольцевой атом" в данном описании относится к атому основы, составляющему кольцо. Такие кольцевые атомы выбраны из С,N, О или S и связаны с 2 или 3 другими такими кольцевыми атомами (3 в случае наличия определенных кольцевых атомов в бициклической кольцевой системе). Термин "кольцевой атом" не включает водород. Термин "-[(C1-C6)-прямолинейный или разветвленный алкил)-Х" и "-[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-Х", в которых X представляет любую группу, обозначенную как присоединенную к алкилу, алкенилу или алкинилу, означает, что одна и более Х-групп могут быть прикреплены к алкильной, алкенильной или алкинильной цепи в любом конце. В соответствии с одним из предпочтительных вариантов осуществления данного изобретения соединение имеет формулу (I):R1, R2, R10 и R11 имеют вышеуказанные значения. В соответствии с более предпочтительным вариантом формулы IA R9 выбран из (S)-метила,(S)-этила или (S)-гидроксиметилметила. Более предпочтительно, R9 представляет (S)-метил. Соединения, в которых R9 выбран из (S)-метила,(S)-этила или (S)-гидроксиметилметила, и в которых часть соединения, представленная-CH(R1)R2, является C1-C4 прямолинейным или разветвленным алкилом, либо С 2-С 4 прямолинейным или разветвленным алкенилом или алкинилом, принадлежат к роду соединений, описанных в WO 97/40028. Однако заявители обнаружили, что присутствие (S)-ориентированного остатка в R9 порождает удивительную и неожиданно сильную ннгибирующую IMPDH активность. В соответствии с другим предпочтительным вариантом формулы IA R11 выбран из Oметила, O-этила или O-изопропила. В соответствии с более предпочтительным вариантом формул (I) и (IA), по меньшей мере один из R1 или R2 выбран из водорода, метила,этила, н-пропила, изопропила, н-бутила, третбутила, н-пентила, фенила, пиридила, 004141CH2CN, -CH2CH2CN, -CH2N(CH2CH2CN)2,-CH2N(CH3)CH2CH2CN, -CH(NH2)CH2CN,-CH2Cl, -CH2OH, -CH2CH2OH,-CH2CH2CH2CH2OH, -CH2CH2OC(O)CH3,-CH2CH2OC(O)CH2NH2, -CH2CH2NHCH3,-CH2CH2N(CH3)2, -CH2CH2N(CH2CH3)2,-CH2N(CH2CH3)2, -CH2CH2CH2N(CH3)2,-CH2CH2CH2N+(CH3)3, -CH2OCH2CH(CH3)2,-CH2CH2N(CH3)С(О)ОС(СН 3)3,-CH2N(CH2CH2CN)CH2CH(CH3)2,-СН(CH2CN)N(СН 3)2,-СН 2 СН(CH2CN)NHC(О)ОС(СН 3)3, где n равно 0 или 1. В соответствии с еще более предпочтительным вариантом формулы IA, один из R1 илиR2 выбран из водорода, этила или фенила; а другой из R1 или R2 выбран из -СН 2 ОН, -CH2CN,-СН 2 СН 2 СN или -СН 2N(СН 2 СН 3)2; или R1 и R2,взятые вместе, образуют фрагмент 3-тетрагидрофуранил. В соответствии с очередным предпочтительным вариантом формулы I, R1 и R2, взятые вместе, образуют фрагмент 3-тетрагидрофуранил, замещенный -OR6. В соответствии с другим предпочтительным вариантом, соединение формулы А выбрано из соединений, представленных ниже в табл. 1. Таблица 1. Соединения 26 В вышеприведенной таблице некоторые соединения представлены в виде солей. Подразумевается, что объем соединений, представленных в таблице, охватывает все виды указанного соединения, а не только представленную соль. Если стереохимия конкретно не обозначена, то соединения в соответствии с данным изобретением могут содержать один или несколько асимметричных атомов углерода и, таким образом, могут иметь вид рацематов и рацемических смесей, простых энантиомеров, диастереоизомерных смесей и отдельных диастереоизомеров. Все подобные изомерные формы указанных соединений непременно входят в объем настоящего изобретения, если не указано иначе. Каждый стереогенный углерод может иметь Rили S-конфигурацию. Сочетаниями заместителей и переменных,предусматриваемыми данным изобретением,являются только те сочетания, которые приводят к образованию устойчивых соединений. Термин "устойчивый" в данном описании относится к соединениям, обладающим достаточной устойчивостью, обеспечивающей получение и сохранение целостности в течение достаточного периода времени, необходимого для указанных в данном описании целей (например, терапевтическое или профилактическое введение млекопитающему или использование в аффинной хроматографии). Обычно такие соединения устойчивы при температуре, составляющей 40 С и ниже, при отсутствии влаги или других химически реактивных условий в течение по меньшей мере недели. В данном описании подразумевается, что соединения в соответствии с настоящим изобретением включают их фармацевтически приемлемые производные или пролекарства. "Фармацевтически приемлемое производное или пролекарство" означает любую фармацевтически приемлемую соль, сложный эфир, соль сложного эфира или другого производного соединения в соответствии с данным изобретением, которое, после введения реципиенту, способно обеспечить (прямо или косвенно) соединение в соответствии с данным изобретением. Особенно предпочтительными производными и пролекарствами являются производные и пролекарства,повышающие биодоступность соединений в соответствии с данным изобретением, при введении таких соединений млекопитающим (например, позволяя перорально введенному соединению легче всасываться в кровь), или улучшающие доставку родительского соединения на биологический участок (например, мозг или лимфатическая система), относящийся к родительскому виду. Предпочтительные пролекарства включают производные, в которых группа, повышающая водорастворимость или активную транспортировку через кишечную 27 мембрану, присоединена к структуре соединений в соответствии с данным изобретением. Фармацевтически приемлемые соли соединений в соответствии с данным изобретением включают соли, полученные из фармацевтически приемлемых неорганических и органических кислот и оснований. Примеры подходящих кислых солей включают ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат,додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, полусульфат, гептаноат, гексаноат, гидрохлорид, гидробромид,гидроиодид, 2-гидроксиэтансульфонат, лактат,малеат, метансульфонат, 2-нафталинсульфонат,никотинат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат. Соли оснований включают соли аммония, соли щелочных металлов, такие как соли натрия и калия, соли щелочно-земельных металлов, такие как соли кальция и магния, соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глюкамина, и соли с аминокислотами, такие как аргинин, лизин и т.д. Основные азотсодержащие группы также могут быть использованы для образования четвертичных оснований с применением таких агентов, как галоиды низших алкилов, таких как метил, этил, пропил и бутилхлорид, бромиды и иодиды; диалкилсульфаты, такие как диметил,диэтил, дибутил и диамилсульфаты, длинноцепочечные галоиды, такие как децил, лаурил,миристил и стеарилхлориды, бромиды и иодиды, аралкилгалоиды, такие как бензил и фенетилбромиды и др. В результате получают водоили маслорастворимые или диспергируемые продукты. Соединения в соответствии с данным изобретением могут быть синтезированы с применением известных способов. Данные соединения целесообразнее всего синтезировать из готовых исходных материалов. Более конкретно,соединения в соответствии с данным изобретением могут быть синтезированы согласно схемам, представленным в примерах 1 и 2 с модификациями, очевидными для специалистов в данной области. Соединения в соответствии с данным изобретением могут быть модифицированы путем присоединения соответствующих функциональных групп для улучшения селективных биологических свойств. Такие модификации известны в данной области и включают модификации,повышающие биологическое проникновение на данном биологическом участке (например,кровь, лимфатическая система, центральная нервная система), улучшающие пероральную доступность, растворимость, обеспечивающую 28 введение путем инъекций, изменяющие метаболизм и скорость выделения. Новые соединения в соответствии с настоящим изобретением являются прекрасными лигандами для IMPDH. Соответственно, данные соединения способны к нацеливанию и ингибированию фермента IMPDH. Ингибирование может быть измерено различными способами,включая, например, анализы с применением ВЭЖХ дегидрогеназы IMP (определение ферментной выработки ХМР и NADH из IMP иNAD) и спектрофотометрические анализы дегидрогеназы IMP (определение ферментной выработки NADH из NAD). [См. С. Montero et al.,Clinica Chimica Acta, 238, pp. 169-178 (1995)]. Композиции в соответствии с данным изобретением включают соединение в соответствии с данным изобретением или его соль; дополнительный агент, выбранный из следующих агентов: иммунодепрессант, противораковый агент,противовирусный агент, противовоспалительный агент, противогрибковый агент, антибиотик или соединение, предотвращающее гиперпролиферацию сосудов; а также любой фармацевтически приемлемый носитель, адъювант или наполнитель. Альтернативные композиции в соответствии с данным изобретением включают соединение в соответствии с данным изобретением или его соль; а также фармацевтически приемлемый носитель, адъювант или наполнитель. Такие композиции могут необязательно включать дополнительный агент, выбранный из следующих агентов: иммунодепрессант, противораковый агент, противовирусный агент, противовоспалительный агент, противогрибковый агент, антибиотик или соединение, предотвращающее гиперпролиферацию сосудов. Композиции в соответствии с данным изобретением предпочтительно представляют собой фармацевтические композиции. Термин "фармацевтически приемлемый носитель или адъювант" относится к носителю или адъюванту, который может быть введен пациенту вместе с соединением в соответствии с данным изобретением и который не влияет на его фармакологическую активность, а также нетоксичен при введении в дозах, достаточных для доставки терапевтического количества соединения. Фармацевтически приемлемые носители,адъюванты и наполнители, которые могут быть использованы в фармацевтических композициях в соответствии с данным изобретением, включают, но не ограничиваются ими, ионообменники, окись алюминия, стеарат алюминия, лецитин, самоэмульгирующиеся системы по доставке лекарственных препаратов (SEDDS) , такие как сукцинат d-токоферолполиэтиленгликоля 1000, поверхностно-активные вещества, применяемые в виде фармацевтических лекарственных форм, такие как Tweens или другие подобные полимерные матрицы для доставки, сыво 29 роточные белки, такие как альбумин сыворотки человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия,частичные глицеридные смеси насыщенных растительных жирных кислот, вода, соли или электролиты, такие как сульфат протамина, гидрофосфат натрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон,основанные на целлюлозе вещества, полиэтиленгликоль, карбоксиметилцеллюлоза натрия,полиакрилаты, воски, блокполимеры полиэтилена-полиоксипропилена, полиэтиленгликоль и шерстяной жир. Циклодекстрины, такие как -,- и -циклодекстрины, или химически модифицированные производные, такие как гидроксиалкилциклодекстрины, включая 2- и 3 гидроксипропилциклодекстрины, или другие солюбилизированные производные, также могут быть наилучшим образом использованы для улучшения доставки соединений в соответствии с данным изобретением. Фармацевтические композиции в соответствии с данным изобретением могут быть введены перорально, парентерально, в виде аэрозоля для ингаляции, локально, ректально, назально, трансбукально, вагинально или через имплантированный резервуар. Авторы предпочитают пероральное введение или введение при помощи инъекций. Фармацевтические композиции в соответствии с данным изобретением могут содержать любые известные нетоксичные,фармацевтически приемлемые носители, адъюванты или наполнители. В некоторых случаях рН состава может быть отрегулирован при помощи фармацевтически приемлемых кислот,оснований или буферов для улучшения устойчивости полученного соединения или форм для его доставки. Термин парентеральный в данном описании включает подкожный, внутрикожный,внутривенный, внутримышечный, интраартикулярный, внутриартериальный, внутрисуставной,интрастернальный, подоболочечный, внутрираневой и внутричерепной методы инъекции или инфузии. Фармацевтические композиции могут быть в виде стерильных препаратов для инъекций,например, в виде стерильной, водной или маслянистой суспензии для инъекций. Такая суспензия может быть получена в соответствии со способами, известными в данной области, с применением подходящих диспергирующих или увлажняющих агентов (таких как, например,Tween 80) и суспендирующих агентов. Стерильный препарат для инъекций может также представлять собой стерильный раствор или суспензию для инъекций в нетоксичном, парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3 бутандиоле. Приемлемые наполнители и растворители, которые могут быть использованы, 004141 30 включают маннит, воду, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно применяют стерильные жидкие жиры. Для этой цели может быть использована любая смесь жидких жиров, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, могут быть использованы при получении препаратов для инъекций,равно как и натуральные фармацевтически приемлемые масла, такие как оливковое или касторовое масло, особенно в полиоксиэтилированном виде. Данные масляные растворы или суспензии могут также содержать длинноцепочечный спиртовой разбавитель или диспергатор,например, описанный в Pharmacopeia Helvetica,Ph. Helv., или подобный спирт, или карбоксиметилцеллюлозу или подобные диспергирующие агенты, обычно используемые при получении фармацевтически приемлемых лекарственных форм, таких как эмульсии и/или суспензии. При получении также могут быть использованы другие, обычно применяемые поверхностно-активные вещества, такие как Tweens или Spans и/или другие подобные эмульгирующие агенты или усилители биодоступности, обычно применяемые при получении фармацевтически приемлемого твердого вещества, жидкости или иных лекарственных форм. Фармацевтические композиции в соответствии с данным изобретением могут быть введены перорально в виде любой перорально приемлемой лекарственной формы, включая, но не ограничиваясь ими, капсулы, таблетки, эмульсии и водные суспензии, дисперсии и растворы. При получении таблеток для перорального применения, обычно используемые носители включают лактозу и кукурузный крахмал. Обычно также добавляют смазывающие агенты, такие как стеарат магния. Разбавители, которые могут быть использованы при получении капсул,предназначенных для перорального введения,включают лактозу и высушенный кукурузный крахмал. Если водные суспензии и/или эмульсии вводят перорально, то активный ингредиент может быть суспендирован или растворен в масляной фазе и соединен с эмульгирующим и/или суспендирующим агентами. При желании,могут быть добавлены определенные подслащивающие, и/или ароматизирующие, и/или красящие агенты. Фармацевтические композиции в соответствии с данным изобретением могут быть также введены в виде суппозиториев для ректального введения. Такие композиции могут быть получены путем смешивания соединения в соответствии с данным изобретением с подходящим нераздражающим формообразующим веществом, которое является твердым при комнатной температуре и жидким при ректальной температуре и поэтому плавится в прямой кишке, вы 31 свобождая активные компоненты. Такие материалы включают, но не ограничиваются ими,масло какао, пчелиный воск и полиэтиленгликоли. Местное введение фармацевтических композиций в соответствии с данным изобретением особенно целесообразно в тех случаях, когда лечению подвергают участки или органы, легко доступные для местного применения. Фармацевтическая композиция, предназначенная для местного нанесения на кожу, должна быть смешана с подходящей мазью, содержащей активные компоненты, суспендированные или растворенные в носителе. Носители для местного введения соединений в соответствии с данным изобретением включают, но не ограничиваются ими, минеральное масло, жидкий и белый вазелин, пропиленгликоль, соединение полиоксиэтилена-полиоксипропилена, эмульгирующий воск и воду. Альтернативно, фармацевтическая композиция может быть смешана с подходящим лосьоном или кремом, содержащим активное соединение, суспендированное или растворенное в носителе с подходящими эмульгирующими агентами. Подходящие носители включают,но не ограничиваются ими, минеральное масло,моностеарат сорбитана, полисорбат 60, воск сложных цетиловых эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду. Фармацевтические композиции в соответствии с данным изобретением также могут быть нанесены локально на нижнюю часть кишечного тракта при помощи ректального суппозитория или подходящей клизмы. Локальные трансдермальные накладки также входят в объем данного изобретения. Фармацевтические композиции в соответствии с данным изобретением могут быть введены в виде назального аэрозоля или ингаляции. Такие композиции получают в соответствии со способами, хорошо известными в области фармацевтической технологии приготовления лекарственных средств, и могут быть получены в виде растворов в солевом растворе с применением бензилового спирта или других подходящих консервантов, ускорителей всасывания для улучшения биодоступности, фторированных углеводородов и/или иных солюбилизирующих или диспергирующих агентов, известных в данной области. Дозы, составляющие приблизительно от 0,01 до 100 мг/кг массы тела в сутки, предпочтительно приблизительно от 0,5 до 75 мг/кг массы тела в сутки, описываемых здесь соединений, ингибирующих IMPDH, могут быть использованы в монотерапии или в комбинированной терапии для профилактики и леченияIMPDH-опосредованного заболевания. Обычно фармацевтические композиции в соответствии с данным изобретением вводят приблизительно от 1 до 5 раз в сутки или, альтернативно, в виде 32 непрерывной инфузии. Такое введение может быть использовано для лечения хронических или острых заболеваний. Количество активного ингредиента, которое может быть соединено с материалами-носителями для получения разовой лекарственной формы, варьируется в зависимости от подвергаемого лечению хозяина и конкретного способа введения. Типичный препарат содержит приблизительно от 5 до 95% активного соединения (маc./маc.). Такие препараты предпочтительно содержат приблизительно от 20 до 80% активного соединения. Если композиции в соответствии с данным изобретением включают сочетание ингибитораIMPDH в соответствии с данным изобретением и один или несколько дополнительных терапевтических или профилактических агентов, то уровень дозы как ингибитора IMPDH, так и дополнительного агента, должен составлять приблизительно от 10 до 100%, более предпочтительно приблизительно от 10 до 80% от дозы,обычно вводимой при монотерапии. Дополнительные агенты могут быть введены отдельно,как часть составной лекарственной схемы, от соединений в соответствии с данным изобретением. Альтернативно, указанные агенты могут составлять часть единой лекарственной формы,т.е. смешаны с соединениями в соответствии с данным изобретением в общую композицию. В соответствии с одним из вариантов осуществления данного изобретения фармацевтические композиции в соответствии с данным изобретением включают дополнительный иммуноподавляющий агент. Примеры дополнительных иммуноподавляющих агентов включают, но не ограничиваются ими, циклоспорин A,FK506, рапамицин, лефлуномид, дезоксиспергуалин, преднизон, азатиоприн, микофенолат мофетил, ОКТ 3, ATAG, интерферон и мизорибин. В соответствии с альтернативным вариантом фармацевтические композиции в соответствии с данным изобретением могут дополнительно включать противораковый агент. Примеры противораковых агентов включают, но не ограничиваются ими, цисплатин, актиномицинD, доксорубицин, винкристин, винбластин, этопозид, амсакрин, митоксантрон, тенипазид, таксол, колхицин, циклоспорин А, фенотиазины,интерферон и тиоксантеры. В соответствии с другим альтернативным вариантом фармацевтические композиции в соответствии с данным изобретением могут дополнительно включать антивирусный агент. Примеры антивирусных агентов включают, но не ограничиваются ими, цитовен, ганцикловир,тринатрийфосфоноформиат, рибавирин, d4T,ddI, AZT и ацикловир. В соответствии с очередным альтернативным вариантом фармацевтические композиции в соответствии с данным изобретением могут дополнительно включать агент, предотвращаю 33 щий гиперпролиферацию сосудов. Примеры таких агентов включают, но не ограничиваются ими, ингибиторы редуктазы Со-А HMG, такие как ловастатин, ингибиторы синтетазы А 2 тромбоксана, эйкозапентановая кислота, ципростен, трапидил, ингибиторы АСЕ, низкомолекулярный гепарин, микофеноловая кислота, рапамицин и 5-(3'-пиридинилметил)бензофуран-2 карбоксилат. После улучшения состояния пациента, при необходимости, можно вводить поддерживающую дозу соединения, композиции или их сочетания в соответствии с данным изобретением. Впоследствии доза или частота введения, либо то и другое, могут быть снижены как функция симптомов, до уровня, при котором сохраняется улучшенное состояние; после смягчения симптомов до желаемого уровня, лечение следует прекратить. Однако пациенту может потребоваться длительное прерывистое лечение при возникновении рецидивов симптомов заболевания. Как понятно опытному специалисту, могут потребоваться более низкие или более высокие дозы по сравнению с вышеуказанными дозами. Конкретные дозы и схемы лечения для каждого отдельного пациента зависят от множества факторов, включая активность конкретного применяемого соединения, возраста, массы тела, общего состояния здоровья, пола, диеты, времени введения, скорости выделения, сочетания лекарственных препаратов, тяжести и хода заболевания, отношения пациента к своему заболеванию и мнения лечащего врача. В соответствии с альтернативным вариантом его осуществления данное изобретение предусматривает способы лечения или профилактики IMPDH-опосредованного заболевания у млекопитающего, включающие стадию введения указанному млекопитающему любой из вышеописанных фармацевтических композиций и комбинаций. Если фармацевтическая композиция включает в качестве активного компонента только ингибитор IMPDH в соответствии с данным изобретением, то такие способы могут дополнительно включать стадию введения указанному млекопитающему агента, выбранного из противовоспалительных веществ, иммунодепрессантов, противораковых агентов, противовирусных агентов или соединений, предотвращающих гиперпролиферацию сосудов. Такой дополнительный агент может быть введен млекопитающему до, параллельно или после введения композиции, ингибирующей IMPDH. В соответствии с предпочтительным вариантом осуществления данного изобретения указанные способы могут быть использованы для подавления иммунной реакции млекопитающих. Такие способы могут быть использованы для лечения или профилактики заболеваний, включающих отторжение трансплантата (например,почка, печень, сердце, легкое, поджелудочная 34 железа (островковые клетки), костный мозг,роговица, аллотрансплантаты тонкой кишки и кожи и ксенотрансплантаты сердечного клапана), реакцию "трансплантат против хозяина" и аутоиммунные заболевания, такие как ревматоидный артрит, рассеянный склероз, ювенильный диабет, астма, воспалительное заболевание кишечника (болезнь Крона, язвенный колит), волчанка, сахарный диабет, тяжелая миастения,псориаз, дерматит, экзема, себорея, воспаление легких, увеит глаз, болезнь Грейвса, тироидит Хашимото, синдром Бехчета или Шегрена (сухие глаза/рот), пернициозная или иммуногемолитическая анемия, идиопатическая недостаточность надпочечников, плюригландулярный аутоиммунный синдром, гломерулонефрит,склеродермия, красный плоский лишай, вителиго (депигментация кожи), аутоиммунный тироидит и альвеолит. Указанные способы включают стадию введения млекопитающему композиции, включающей соединение в соответствии с данным изобретением и фармацевтически приемлемый адъювант. В соответствии с предпочтительным вариантом данный конкретный способ включает дополнительную стадию введения указанному млекопитающему композиции, включающей дополнительно иммунодепрессант и фармацевтически приемлемый адъювант. Альтернативно, данный способ включает стадию введения указанному млекопитающему композиции, включающей соединение в соответствии с настоящим изобретением; дополнительно иммуноподавляющего агента и фармацевтически приемлемого адъюванта. В соответствии с альтернативным предпочтительным вариантом указанные способы могут быть использованы для ингибирования вирусной репликации у млекопитающего. Такие способы могут быть использованы для лечения или профилактики вирусных заболеваний ДНК и РНК, вызванных инфекцией, например, ортомиксовирусами (вирусы гриппа типов А и В),парамиксовирусами (респираторносинцитиальный вирус (RSV), подострый склерозирующий вирус панэнцефалита (SSPE), корь и парагрипп типа 3), вирусами герпеса (HSV-1, HSV-2, HHV6, HHV-7, HHV-8, вирусом Эпстайна-Барра(EBV), цитомегаловирусом (HCMV) и вирусом ветряной оспы (VZV, ретровирусами (ВИЧ-1,ВИЧ-2, HTLV-1, HTLV-2), флави- и пестивирусами (вирус желтой лихорадки (YFV) , вирусом гепатита С (HCV), вирусом лихорадки денге,вирусом бычьей вирусной диареи (BVDV), гепатотрофическими вирусами (вирус гепатита A(bunyaviruses) (вирус Punta Того, вирус лихорадки долины Рифт (RVFV) и вирус сицилийской флеботомией лихорадки),вирусомTacaribe), реовирусами, вирусом везикулярного стоматита, риновирусами, энтеровирусами (полио вирус, вирусы коксаки, вирус энцефаломиокардита (ЕМС, вирусом лихорадки Ласса и тогавирусами (лесные вирусы Синдбиса и Семлике), а также вирусами, вызывающими высыпания на коже (вирус коровьей оспы), аденовирусами, корью и краснухой. Указанные способы включают стадию введения млекопитающему композиции, включающей соединение в соответствии с данным изобретением и фармацевтически приемлемый адъювант. В соответствии с предпочтительным вариантом данный конкретный способ включает дополнительную стадию введения указанному млекопитающему композиции, включающей дополнительно противовирусный агент и фармацевтически приемлемый адъювант. Альтернативно, данный способ включает стадию введения указанному млекопитающему композиции, включающей соединение в соответствии с настоящим изобретением; дополнительно противовирусного агента и фармацевтически приемлемого адъюванта. В соответствии с другим альтернативным предпочтительным вариантом указанные способы могут быть использованы для ингибирования сосудистой клеточной гиперпролиферации у млекопитающего. Такие способы могут быть использованы для лечения или профилактики заболеваний, включающих рестеноз, стеноз,атеросклероз и другие гиперпролиферативные сосудистые заболевания. Указанные способы включают стадию введения млекопитающему композиции, включающей соединение в соответствии с данным изобретением и фармацевтически приемлемый адъювант. В соответствии с предпочтительным вариантом данный конкретный способ включает дополнительную стадию введения указанному млекопитающему композиции, включающей дополнительно агент, предотвращающий гиперпролиферацию сосудов, и фармацевтически приемлемый адъювант. Альтернативно, данный способ включает стадию введения указанному млекопитающему композиции, включающей соединение в соответствии с настоящим изобретением; дополнительно агента, предотвращающего гиперпролиферацию сосудов, и фармацевтически приемлемого адъюванта. В соответствии с очередным альтернативным предпочтительным вариантом указанные способы могут быть использованы для ингибирования опухолей и рака у млекопитающего. Такие способы могут быть использованы для лечения или профилактики заболеваний, включающих опухоли и злокачественные заболева 004141 36 ния, такие как лимфома, лейкемия и другие виды рака. Указанные способы включают стадию введения млекопитающему композиции, включающей соединение в соответствии с данным изобретением и фармацевтически приемлемый адъювант. В соответствии с предпочтительным вариантом данный конкретный способ включает дополнительную стадию введения указанному млекопитающему композиции, включающей дополнительно противоопухолевый или противораковый агент и фармацевтически приемлемый адъювант. Альтернативно, данный способ включает стадию введения указанному млекопитающему композиции, включающей соединение в соответствии с настоящим изобретением; дополнительно противоопухолевого или противоракового агента и фармацевтически приемлемого адъюванта. В соответствии со следующим альтернативным предпочтительным вариантом указанные способы могут быть использованы для ингибирования воспаления и воспалительных заболеваний у млекопитающего. Такие способы могут быть использованы для лечения или профилактики заболеваний, включающих остеоартрит, острый панкреатит, хронический панкреатит, астму и респираторный дистресс-синдром взрослых. Указанные способы включают стадию введения млекопитающему композиции, включающей соединение в соответствии с данным изобретением и фармацевтически приемлемый адъювант. В соответствии с предпочтительным вариантом данный конкретный способ включает дополнительную стадию введения указанному млекопитающему композиции, включающей противовоспалительный агент и фармацевтически приемлемый адъювант. Следующие примеры представлены для более полного понимания данного изобретения. Указанные примеры предназначены только для иллюстрации и никоим образом не должны рассматриваться как ограничивающие объем данного изобретения. Пример 1. Синтез соединения 41. А. Синтез С 4 К раствору ледяной уксусной кислоты (46 мл), уксусного ангидрида (46 мл, 485 ммоль) и 2-метил-5-нитроанизола (10,0 г, 60 ммоль) при 0 С по каплям добавляют концентрированную(8,08 г, 80,8 ммоль). Еще через 15 мин перемешивания при 0 С реакционную смесь выливают в лед, полученный осадок выделяют фильтрацией и промывают холодной Н 2O. В результате очистки флэш-хроматографией, элюирования 37 градиентом 15-50% EtOAc в гексанах, получают 8,14 г (24%, 51% в расчете на восстановленный исходный материал) Сl в виде белого твердого вещества. 1 Н ЯМР соответствует 1 Н ЯМР желаемой структуры. С 2 Перемешиваемую суспензию Сl (81,94 г,307 ммоль) в диоксане (100 мл) обрабатывают концентрированной HCl (20 мл) и нагревают при кипячении с обратным холодильником в течение ночи. После охлаждения до температуры окружающей среды продукт С 2 выпадает в осадок в виде светло-желтого кристаллического твердого вещества, выход которого составляет 40,65 г (73,1%). Фильтрат концентрируют до объема, приблизительно составляющего 80 мл,получая из раствора путем добавления гексанов второй сбор кристаллов продукта, выход которого составляет 8,91 г (16,0%). 1 Н ЯМР и анализ ТСХ показывают идентичность обеих партий и их соответствие желаемому материалу. Общий выход С 2 составляет 49,56 г (89,1%). С 3 Раствор С 2 (456 мг, 2,51 ммоль), тозилметилизоцианид (490 мг, 2,51 ммоль) и К 2 СО 3 (347 мг, 251 ммоль) растворяют в метаноле и нагревают до температуры дефлегмации в течение 1,5 ч. Затем смесь продукта концентрируют в вакууме, повторно растворяют в CH2Cl2, промывают водой и рассолом, сушат над Na2SO4 и вновь концентрируют в вакууме. В результате перекристаллизации (Et2O/гексаны) получают очищенный продукт C3, выход которого составляет 375 мг (68%) . 1 Н ЯМР соответствует 1H ЯМР желаемой структуры.(150 мл) обрабатывают 10% Pd/C (1,05 г, 25 мас.% С 3) и подвергают воздействию давления,составляющего 40 фунтов на кв. дюйм (2,8124 кг/см 2) Н 2 (г) (устройство для гидрогенизации Парра), в течение ночи. Реакционную смесь фильтруют и концентрируют в вакууме. В результате флэш-хроматографии, элюирования градиентом 30-40% EtOAc/гексаны, получают чистый продукт С 4, выход которого составляет 3,4 г (93%). 1 Н ЯМР соответствует 1 Н ЯМР желаемой структуры. Раствор 3-аминобензиламина (826 мг, 6,87 ммоль) и триэтиламина (2,39 мл, 17,18 ммоль) обрабатывают ди-трет-бутилдикарбонатом (1,50 г, 6,87 ммоль) и смесь перемешивают при температуре окружающей среды в течение 8 ч. Затем реакционную смесь разбавляют CH2Cl2,промывают NаНСО 3 (волн.), водой и рассолом,сушат (Na2SO4) и концентрируют в вакууме. В результате флэш-хроматографии, элюирования 25% EtOAc в гексанах получают чистый Е 1,выход которого составляет 200 мг (46%). 1H ЯМР соответствует 1 Н ЯМР желаемой структуры. Раствор С 4 (150 мг, 0,789 ммоль) и 1,1 дикарбонилимидазола (160 мг, 0,986 ммоль) объединяют в ТГФ (5 мл) и перемешивают в течение 6 ч при температуре окружающей среды. Наблюдается осаждение имидазола. Затем к смеси добавляют Е 1 (351 мг, 1,58 ммоль) и N,Nдиметиламинопиридин (97 мг, 0,789 ммоль) и кипятят ее с обратным холодильником в течение ночи, получая гомогенный раствор. После охлаждения до температуры окружающей среды реакционную смесь разбавляют EtOAc (20 мл),промывают KHSO4 (водн.), водой и рассолом,сушат (MgSO4) и концентрируют. В результате флэш-хроматографии, элюирования градиентом 20-30-35% ацетона в гексанах получают чистыйI113, выход которого составляет 164 мг (47%). 1 Н-ЯМР (500 МГц, d6-ДМСО)8,90 (с), 8,75 (с),8,38 (с), 7,60 (д) , 7,51 (с), 7,3-7,46 (м) , 7,21-7,27(I168) К суспензии I113 (250 мг, 5,76 ммоль) в СН 2 Сl2 (1 мл) по каплям при температуре окружающей среды добавляют несколько эквивалентов трифторуксусной кислоты и перемешивают в течение 90 мин. Полученный раствор перемешивают в вакууме и титруют CH2Cl2 и метанолом. В результате фильтрации выделяют чистый продукт 1168, выход которого составляет 258 мгD. Синтез соединения 41. К раствору 1-метокси-2-пропанола, имеющему комнатную температуру (75 мг, 832 мкмоль), в ТГФ (1,0 мл) добавляют твердый 1,1'-карбонилдиимидазол (121 мг, 749 мкмоль) в виде одной порции. Полученную смесь перемешивают при комнатной температуре в течение ночи, а затем последовательно обрабатываютTEA (174 мкл, 1,25 ммоль), твердым соединением I168 (376 мг, 832 мкмоль) и ДМФ (1,0 мл). Полученный раствор перемешивают при комнатной температуре в течение одного дня, затем разбавляют этилацетатом, последовательно промывают водой и рассолом, сушат надMgSO4, фильтруют и концентрируют в вакууме. Затем сырой продукт очищают флэшхроматографией (силикагель, 97,5/1,5 СН 2 Сl2). После этого подвергнутый хроматографии продукт растирают со смесью этиловый эфир/ этилацетат 9/1, получая соединение 41 (65 мг, выход(дд, 1 Н); 7,10 (дд, 1 Н); 6,97 (д, 1 Н), 6,68 (м, 1 Н); 4,92 (м, 1 Н) ; 4,32 (д, 2 Н); 4,01 (с, 3H); 3,43 (дд,1 Н); 3,33 (дд, 1 Н) ; 3,31 (с, 3H); 1,18 (д, 3H). Другие соединения в соответствии с данным изобретением могут быть получены подобным образом, заменяя 1-метокси-2-пропанол соответствующим спиртом (т.е. НО-СН(R1)(R2 на стадии D. Пример 2. Получение соединения 169. А. Получение левостороннего связывающего промежуточного соединения (R10 = циано): Цианид меди (I) (7,2 г, 80,8 ммоль) объединяют с 2-бром-5-нитроанизолом (I) (15 г, 64,6 ммоль) в NMP (1-метил-2-пирролидинон) (70 мл) и нагревают до 150 С в течение ночи в атмосфере N2. Смесь обрабатывают целитом, охлаждают до комнатной температуры, затем разбавляют EtOAc и 1,0N NaOH и дают перемешиваться в течение 15 мин. Гетерогенную смесь фильтруют через подушку из целита с EtOAc,фазы разделяют и водную фазу трижды промывают EtOAc. Объединенные органические фазы последовательно промывают 1,0N NaOH, водой и рассолом, а затем сушат над Na2SO4, фильтруют и концентрируют в вакууме. Сырой продукт растворяют в СН 2 Сl2, фильтруют через тонкую подушку из силикагеля, удаляя твердые вещества и большую часть окрашенных примесей, а затем концентрируют в вакууме, получая(220-15 мл) добавляют 10% Ра/С (1,5 г), получая гетерогенную черную смесь. Данную смесь подвергают воздействию 1 атмосферы (баллон) Н 2, нагревают до 50 С и перемешивают в течение ночи. Смесь охлаждают до комнатной температуры, катализатор удаляют фильтрацией и фильтрат концентрируют в вакууме, получая III(5,56 г, 93%) в виде кристаллического твердого вещества. 1NaHCO3 (1M, 16 мл) в течение свыше 10 мин добавляют III (950 мг, 6,41 ммоль) в виде раствора в EtOAc (10 мл). Полученную гетерогенную смесь перемешивают при комнатной температуре в течение 30 мин, а затем фазы разделяют. Органическую фазу промывают рассолом,сушат над Na2SO4, фильтруют через подушку из силикагеля с EtOAc и концентрируют в вакууме, получая густое масло. Полученное масло разбавляют в толуоле (30 мл) и обрабатывают гексанами (30 мл), получая густой осадок. Данную смесь перемешивают в течение 30 мин,фильтруют, твердую фазу промывают смесью толуол:гексаны 1:1, затем только гексанами и сушат до постоянного веса в высоком вакууме,получая IV (1,65 г, 96%,) в виде белого порошка. 1(м, 3H); 7,15 (д, 1 Н); 3,85 (с, 3H). В. Получение правостороннего связывающего промежуточного соединения (R9 = Sметил): К раствору V (200 г, 1,21 моль), имеющему комнатную температуру, в EtOH (2 л) по порциям в течение 30 мин добавляют NaBH4 (50,3 г,1,33 моль), не позволяя внутренней температуре подниматься выше 40 С. Смеси дают перемешиваться при комнатной температуре в течение 4 ч. Затем ее гасят водой (100 мл), концентрируют в вакууме, разбавляют EtOAc, дважды промывают водой, один раз насыщенным NaHCO3, сушат над MgSO4, фильтруют и концен 41 трируют в вакууме, получая VI (191,7 г, 95%) в виде желтоватого порошка. 1(д, 1 Н); 7,70 (д, 1 Н); 7,49 (дд, 1 Н); 5,01 (дд, 1 Н); 2,45 (с, 1 Н); 1,52 (д, 3H). К имеющему комнатную температуру раствору VI (181 г, 1,08 моль) добавляют DPPA(250 мл, 1,16 моль) с достаточно низкой скоростью, чтобы поддерживать температуру реакции ниже 45 С. Завершив добавление DPPA, смесь обрабатывают DBU (177 мл, 1,18 моль) с достаточно низкой скоростью, чтобы поддерживать температуру реакции ниже 45 С. Завершив добавление, реакционную смесь нагревают до 60 С и поддерживают при данной температуре в течение ночи. Полученную двухфазную смесь охлаждают до комнатной температуры и последовательно промывают водой, а затем 0,5 М HCl. Органическую фазу сушат над Na2SO4, фильтруют и концентрируют в вакууме, получая желто-зеленое масло, которое впоследствии не подвергают очистке. 1(д, 1 Н); 7,68 (д, 1 Н); 7,56 (кв, 1 Н); 4,76 (дд, 1 Н); 1,59 (д, 3H). К имеющему комнатную температуру раствору VII (8,17 г, 42,51 ммоль) в смеси ТГФвода (80 мл-10 мл) добавляют Ph3 Р (12,3 г, 46,76 ммоль) в виде раствора в ТГФ (20 мл) в течение свыше 10 мин. Выделение азота начинается немедленно и остается постоянным на протяжении всего процесса добавления. После этого смесь нагревают до 65 С в течение ночи, а затем охлаждают до комнатной температуры. Сырую смесь концентрируют в вакууме, разбавляютEtOAc, промывают рассолом, сушат над Na2SO4 и фильтруют. Полученный фильтрат обрабатывают 1N HCl/Et2O при комнатной температуре на протяжении свыше 10 мин, что приводит к образованию осадка. Смесь перемешивают при комнатной температуре в течение 15 мин, а затем фильтруют. Твердую часть промываютEt2O, получая желтый порошок. Сырую соль гидрохлорида амина суспендируют в смеси рассол/EtOAc и обрабатывают 10N NaOH (5 мл, 50 ммоль) при комнатной температуре. Полученную смесь перемешивают при комнатной температуре до растворения всех твердых веществ. Фазы разделяют, водную фазу промываютEtOAc дважды, объединенные органические фазы промывают рассолом, сушат над Na2SO4,фильтруют и концентрируют в вакууме. Сырой амин разбавляют в МеОН (50 мл) и добавляют к кипящему с обратным холодильником растворуL-(+)-винной кислоты (5,33 г, 35,33 ммоль) в МеОН (450 мл). Сразу же образующийся осадок затем растворяется в МеОН смеси кипящей с обратным холодильником в течение 15 мин. Внутреннюю температуру понижают до 50 С и поддерживают на этом уровне в течение ночи. Затем внутреннюю температуру снижают до 30 С, поддерживая ее еще в течение 24 ч, после 42 чего раствор выдерживают еще в течение 24 ч при комнатной температуре. Полученные кристаллы (шипы) фильтруют, промывают МеОН иEt2O и маточный раствор сливают. Полученные кристаллы растворяют в 200 мл кипящего МеОН, медленно охлаждают как описано выше,фильтруют и промывают МеОН, затем Et2O,получая первую порцию VIII (2,21 г, 20%) в виде белого твердого вещества. Маточный раствор концентрируют в вакууме, твердые вещества растворяют в 50 мл кипящего МеОН, охлаждают как описано выше, фильтруют и промывают МеОН и Et2O, получая вторую порцию VIII(1,50 г, 13%) в виде твердого белого вещества. Было установлено, что оптическая чистота на соответствующем фенилкарбамате каждой порции составляет 97% ее. Энантиомерный избыток определяют,применяя колонку Chiralcel OD (0,46 х 25 см),изготовленную Daicel Chemical Industries и приобретенную у Chiral Technologies. В качестве подвижной фазы применяют смесь гексан: IРА 70:30 при изократическом вытекании до 65 мин при скорости потока, составляющей 0,8 мл/мин,применяя 3-4 мкл инжектирование 1-2 мг/мл раствора фенилкарбамата, растворенного в указанной выше смеси гексан: IРА. Желаемый Sметиловый энантиомер сначала элюируется через 47,2 мин, в то время как нежелательный Rметиловый энантиомер отделяется через 51,7 мин, как показывает наблюдение при длине волны, составляющей 214, 254, 280 нм. Все образцы обрабатывают на хроматографе для ВЭЖХ Hewlett Packard, серия 1050, с диодным решетчатым детектором. К гетерогенной суспензии VIII (1,11 г, 3,51 ммоль) в EtOAc (20 мл) и рассоле (20 мл) при комнатной температуре добавляют 10N NaOH(0,77 мл, 7,72 ммоль). Полученную смесь перемешивают при комнатной температуре до растворения всех солей. Затем фазы разделяют и водную фазу промывают EtOAc. Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют в вакууме. Сырой нитробензиламин разбавляют в 7 м NH3-MeOH (20 мл), добавляют 20% Pd(OH)2C и подвергают воздействию давления, составляющего 45 фунтов на кв. дюйм (310 кПа ) (Н 2) в течение 5 ч. Полученную смесь фильтруют,удаляя катализатор, концентрируют в вакууме,один раз подвергают азеотропной перегонке с СН 2 Сl2, а затем помещают в высокий вакуум,получая IX (455 мг, 95%.) в виде воскообразного белого твердого вещества. 1 К имеющему комнатную температуру раствору 3-(R)-гидроксипентанитрила (212 мг, 2,14 ммоль) одной порцией добавляют CDI (521 мг,3,21 ммоль). Полученную смесь перемешивают при комнатной температуре в течение 1 ч, а затем обрабатывает твердым силикагелем. Гетерогенную смесь энергично перемешивают в течение 10 мин, фильтруют через тонкую подушку из силикагеля со смесью EtOAc:IРА 4:1, концентрируют в вакууме, дважды подвергают азеотропной перегонке с MeCN, затем объединяют с IX (350 мг, 2,57 ммоль) в MeCN (2 мл) и перемешивают при комнатной температуре в течение 1 дня. Полученную смесь разбавляютEtOAc, промывают водой, а затем рассолом,сушат над Na2SО 4, фильтруют и подвергают флэш-хроматографии (силикагель, 1/2, 1/3, 0/1 гексаны/EtOAc, 4/1 EtOAc/IРА), получая X (472 мг, 84%) в виде прозрачного густого масла. 1 Н-ЯМР (500 МГц, ДМСО-d6): 7,73 (д, 1 Н); 6,94 (дд, 1 Н); 6,51 (с, 1 Н); 6,47 (д, 1 Н); 6,38 (д,1 Н); 4,98 (шир. с, 2 Н); 4,67 (м, 1 Н); 4,49 (м, 1 Н); 2,82 (м, 2 Н); 1,62 (м, 2 Н); 1,27 (д, 3H); 0,89 (дд,3H). К имеющему комнатную температуру раствору X (470 мг, 1,80 ммоль) в EtOAc (5 мл) добавляют IV (440 мг, 1,63 ммоль) и TEA (0,23 мл,1,63 ммоль). Полученную смесь нагревают до кипения с обратным холодильником и перемешивают при такой температуре в течение 6 ч. Полученную сырую смесь охлаждают до комнатной температуры, разбавляют EtOAc, промывают смесью рассол/1N HCl, затем только рассолом, сушат над Na2SO4, фильтруют, концентрируют в вакууме и подвергают флэшхроматографии (силикагель, 1/1, 1/2, 1/3, 1/4, 0/1 гексаны/EtOAc, 4/1 EtOAc/IРА), получая 169(д, 1 Н); 6,92 (д, 1 Н); 4,69 (м, 1 Н); 4,63 (м, 1 Н); 3,89 (с, 3H); 2,82 (м, 2 Н); 2,62 (м, 2 Н); 1,31 (д,3H); 0,90 (т, 3H). Пример 3. Исследование активности ингибирования IMPDH. Активность дегидрогеназы IMP исследуют в соответствии с адаптированным способом,впервые описанным Magasanik. [В. Magasanik etal., J. Biol. Chem., 226, p. 339 (1957), приводится здесь в качестве ссылки]. Ферментную активность измеряют спектрофотометрически, отслеживая усиление оптической плотности при 44 340 нм в результате образования NADH (340 составляет 6820 М-1 см-1). Реакционная смесь содержит 0,1 М фосфат калия 8,0, 0,5 мМ ЭДТА,2 мМ DTT, 200 мкМ IPM и фермент (IMPDH человека, тип II), имеющий концентрацию от 15 до 50 нМ. Данный раствор инкубируют при 37 С в течение 10 мин. Реакцию начинают, добавляя NAD к конечной концентрации, составляющей 200 мкМ, и измеряют начальную скорость, отслеживая линейное усиление оптической плотности при 340 нм в течение 10 мин. Для снятия показаний на стандартном спектрофотометре (длина шага = 1 см) конечный объем в кювете составляет 1,0 мл. Исследование также проводят в 96-луночном планшете для микротитрования; в таком случае концентрация всех реагентов остается одинаковой, а конечный объем снижается до 200 мкл. Для анализа ингибиторов исследуемое соединение растворяют в ДМСО до конечной концентрации, составляющей 20 мМ, и добавляют к исходной смеси для анализа для предварительной инкубации с ферментом при объеме,составляющем 2-5% (об./об.). Реакцию начинают, добавляя NAD, и начальную скорость измеряют вышеуказанным способом. Ki определяют,измеряя начальную скорость в присутствии различного количества ингибитора, и получают данные, применяя уравнения для плотного связывания Хендерсона (Henderson, P. J. F. (1972)Biochem. J. 127, 321). Полученные результаты представлены в табл. 2. Категория "А" означает Ki, составляющую 10 нМ и ниже, категория "В" означает Ki,составляющую более 10 и менее 50 нМ, категория "С" означает Ki, составляющую 50 нМ и выше, "ND" означает, что ингибирующая активность не установлена. Таблица 2. Ингибирующая IMPDH активность Соединение Соединение Соединение СоединениеB. РВМС и исследование пролиферации спленоцитов. 5 х 104 клеток (для Т-клеток РВМС человека) или 1x105 клеток (для В-клеток РВМС человека) добавляют в каждую лунку 96-луночного планшета. Для исследования Т-клеток добавляют фитогемагглютинин (РHА) до конечной концентрации, составляющей 10-20 мкг/мл на лунку для клетки. Для исследования В-клеток добавляют стафилококковый белок A (SPAS) до конечной концентрации, составляющей 2 мкг/мл на лунку. Осуществляют 4-кратное разбавление ингибирующей смеси в полной RPMI и добавляют к клеткам таким образом, чтобы конечная концентрация соединений составляла от 20 мкМ до 20 нМ, при этом поддерживая конечную концентрацию ДМСО на уровне 0,1%. Затем клетки инкубируют в течение 3 дней. Все образцы исследуют в трех экземплярах. На последние 24 ч исследования добавляют растертый тимидин Другие соединения в соответствии с дан(0,4 мкСi/лунка). Клетки собирают на фильтры ным изобретением также обладают активноBetaplate и подсчитывают с помощью сцинтилстью, ингибирующей IMPDH. ляционного счетчика. Применяя компьютерную Пример 4. Клеточные исследования. программу SoftMax Pro (Molecular Devices),A. Выделение периферических мононуклеопределяют концентрацию соединений, необхоарных клеток крови (PBMCs). димых для ингибирования пролиферации клеток У нормальных здоровых добровольцев зана 50%. бирают венозную кровь, применяя гепарин в Результаты данных исследований предкачестве антикоагулянта. PBMCs выделяют из ставлены в табл. 3. Категория "А" означает IC50,крови центрифугированием с применением грасоставляющую 100 нМ и ниже, категория "В" диента Ficoll-paque или трубок СРТ (Bectonозначает IC50, составляющую более 100 и менееDickinson) в стандартных условиях. PBMCs со 1000 нМ, категория "С" означает IC50, составбирают, промывают и вновь суспендируют в ляющую 1000 нМ и выше, "ND" означает, что в полной RPMI, подсчитывают и разбавляют до указанном клеточном исследовании ингиби 6 1x10 клеток/мл. рующая активность не установлена. Таблица 3. Клеточная активность Соед. ТВСоед. ТВСоед. ТВСоед. ТВклетки клетки клетки клетки клетки клетки клетки клетки Пример 5. Противовирусные исследования. Противовирусная эффективность соединений может быть установлена в результате различных исследований in vitro и in vivo. Например, соединения могут быть проанализированы в результате исследований на вирусную репликацию in vitro. При исследовании in vitro могут быть использованы целые клетки или отдельные клеточные компоненты. Исследования in vivo включают животные модели для вирусных заболеваний. Примеры таких животных моделей включают, но не ограничиваются ими, модели на грызунах для HBV- или HCV-инфекций, модель Woodchuck для HBV-инфекций и модель на шимпанзе для HCV-инфекций. Несмотря на несколько вышеприведенных вариантов осуществления данного изобретения,очевидно, что его основная конструкция может быть изменена для осуществления других вариантов с применением способов в соответствии с настоящим изобретением. Поэтому объем данного изобретения определяется прилагаемой формулой изобретения, а не конкретными вариантами, приведенными выше в качестве примеров. в которой каждый из R1 и R2 независимо выбран из группы, включающей водород; -СF3; -(C1-C6)прямолинейный или разветвленный алкил; -(С 2 С 6)-прямолинейный или разветвленный алкенил или алкинил; -(C1-C6)-прямолинейный или разветвленный алкил-R7; -[(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7; и в которой по меньшей мере один из-[(C2-C6)прямолинейный или разветвленный алкенил или алкинил]-R7 или -R7, в которой вплоть до 4 атомов углерода в любом из указанных алкилов,алкенилов или алкинилов необязательно и независимо заменены группой R3 и в которой один или оба из R1 или R2 необязательно этерифицированы с образованием пролекарства; или альтернативно, R1 и R2, взятые вместе, образуют тетрагидрофуранил, в которой когда R9 представляет водород, (R)-метил, (R)-этил или(R)-гидроксиметил, один атом водорода в указанном тетрагидрофуране заменен группой -OR6 или -R7, и в которой, если R9 представляет (S)метил, (S)-этил или (S)-гидроксиметил, то один 49 атом водорода в указанном тетрагидрофуране необязательно заменен группой -OR6 или -R7; в которой, если R9 представляет водород,(R)-метил, (R)-этил или (R)-гидроксиметил, а каждый из R1 и R2 независимо представляет водород, незамещенный -(C1-C6)-прямолинейный или разветвленный алкил, либо незамещенный-(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил, то часть соединения,представленного -CH(R1)R2, представляет C5-C12 прямолинейный или разветвленный алкил, алкенил или алкинил; каждый R3 независимо выбран из галогена,CN, -OR4 или -N(R5)2;R4 выбран из группы, включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, -(С 2-С 6)-прямолинейный или разветвленный алкенил или алкинил, -[(C1-C6)прямолинейный или разветвленный алкил]-R7,-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7, -С(О)-[(C1-C6)прямолинейный или разветвленный алкил],-С(О)-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-[(C1-С 6)прямолинейный или разветвленный алкил]N(R8)2, -С(О)-[(C2-С 6)-прямолинейный или разветвленный алкенил или алкинил]-N(R8)2,-P(O)(OR8)2,-P(O)(OR8)(R8),-C(O)-R7,-S(O)2N(R5)2, -[(C1-C6)-прямолинейный или разветвленный алкил]-CN или -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-CN; каждый R5 независимо выбран из группы,включающей водород, -(C1-C6)-прямолинейный или разветвленный алкил, -(C2-C6)-прямолинейный или разветвленный алкенил или алкинил, -[(C1-C6)-прямолинейный или разветвленный алкил]-R7, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-R7, -[(C1C6)-прямолинейный алкил]-CN,-[(C2-C6)прямолинейный или разветвленный алкенил или алкинил]-CN, -[(C1-C6)-прямолинейный или разветвленный алкил]-OR4, -[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил]-OR4, -C(O)-(C1-C6)-прямолинейный или разветвленный алкил, -С(О)-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -C(O)-R7, -C(O)O-R7, -С(О)О-(C1-C6)прямолинейный или разветвленный алкил,-С(О)О-[(C2-C6)-прямолинейный или разветвленный алкенил или алкинил], -S(O)2-(C1-C6)прямолинейный или разветвленный алкил или-S(O)2-R7; или два фрагмента R5, когда связаны с одним и тем же атомом азота, соединены вместе с указанным атомом азота, образуя 3-7 членное гетероциклическое кольцо, в котором указанное гетероциклическое кольцо необязательно содержит от 1 до 3 дополнительных гетероатомов, независимо выбранных из N, О, S,S(O) или S(O)2; 50 каждый R7 представляет моноциклическую или бициклическую кольцевую систему, в которойi) каждое кольцо включает от 3 до 7 кольцевых атомов, независимо выбранных из С, N,О или S;ii) не более 4 кольцевых атомов выбраны из N, О или S;iii) любая СН 2 группа необязательно заменена группой С(O);iv) любой S необязательно заменен группой S(O) или S(O)2; каждый R8 независимо выбран из водорода или -[C1-C4]-прямолинейного или разветвленного алкила; где в любой кольцевой системе в указанном соединении вплоть до 3 атомов водорода,связанных с кольцевыми атомами, необязательно и независимо заменены галогеном, гидрокси,нитро, циано, амино, (C1-C4)-прямолинейным или разветвленным алкилом; O-(C1-C4)-прямолинейным или разветвленным алкилом, (C2-C4)прямолинейным или разветвленным алкенилом или алкинилом или O-(С 2-С 4)-прямолинейным или разветвленным алкенилом или алкинилом; и где кольцевая система необязательно бензоконденсирована;R11 выбран из галогена, -O-(С 1-С 3) прямолинейного алкила или -O-(С 2-С 3)прямолинейного алкенила или алкинила. 2. Соединение по п.1, в котором указанное соединение имеет формулу (I) где R1 и R2 имеют значения, указанные в п.1. 3. Соединение по п.1, в котором указанное соединение имеет формулу (IA) 51 7. Соединение по п.1, в котором по меньшей мере один из R1 или R2 выбран из водорода, метила, этила, н-пропила, изопропила, н-бутила,трет-бутила, н-пентила, фенила, пиридила,-СН 2 ОСН 3, -CH2CN, -CH2OCH2CH2CN,-СН 2 С(СН 3)2 СН 2 СН 2 СN,-CH2C(CH2CH3)2CH2CH2CN, -CH2CH2CN,-CH2N(CH2CH2CN)2, -CH2N(CH3)CH2CH2CN,-CH(NH2) CH2CN, -CH2Cl, -CH2OH,-CH2CH2OH, -CH2CH2CH2CH2OH,-CH2CH2OC(O)CH3, -CH2CH2OC(O)CH2NH2,-CH2CH2NHCH3, -CH2CH2N(CH3)2,-CH2N(CH2CH3)2, -CH2CH2N(CH2CH3)2,-CH2CH2CH2N(CH3)2, -CH2CH2CH2N+(CH3)3,-CH2OCH2CH(CH3)2,-CH2CH2N(CH3)С(O)ОС(CH3)3,-CH2N(CH2CH2CN)CH2CH(CH3)2,-CH(CH2CN)N(CH3)2,-CH2CH(CH2CN)NHC(О)ОС(CH3)3, где n равно 0 или 1. 8. Соединение по п.2, в котором R1 и R2,взятые вместе, образуют 3-тетрагидрофуранил,замещенный в положении 5-OR6. 9. Соединение по п.3, в котором один из R1 или R2 выбран из водорода, этила или фенила; а другой из R1 или R2 выбран из -СН 2 ОН,-CH2CN, -CH2CH2CN или CH2N(CH2CH3)2 илиR1 и R2, взятые вместе, образуют 3-тетрагидрофуранил. 10. Соединение по п.1, представляющее собой соединение, выбранное из соединений 1187:
МПК / Метки
МПК: C07D 263/32, C07C 275/34, A61P 31/12, A61K 31/421
Метки: ингибиторы, фермента, impdh
Код ссылки
<a href="https://eas.patents.su/30-4141-ingibitory-fermenta-impdh.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы фермента impdh</a>
Предыдущий патент: Бета- карболиновые соединения, способ их получения и фармацевтическая композиция, их содержащая
Следующий патент: Способ лечения или профилактики вазоспазма коронарного трансплантата
Случайный патент: Сжижение природного газа