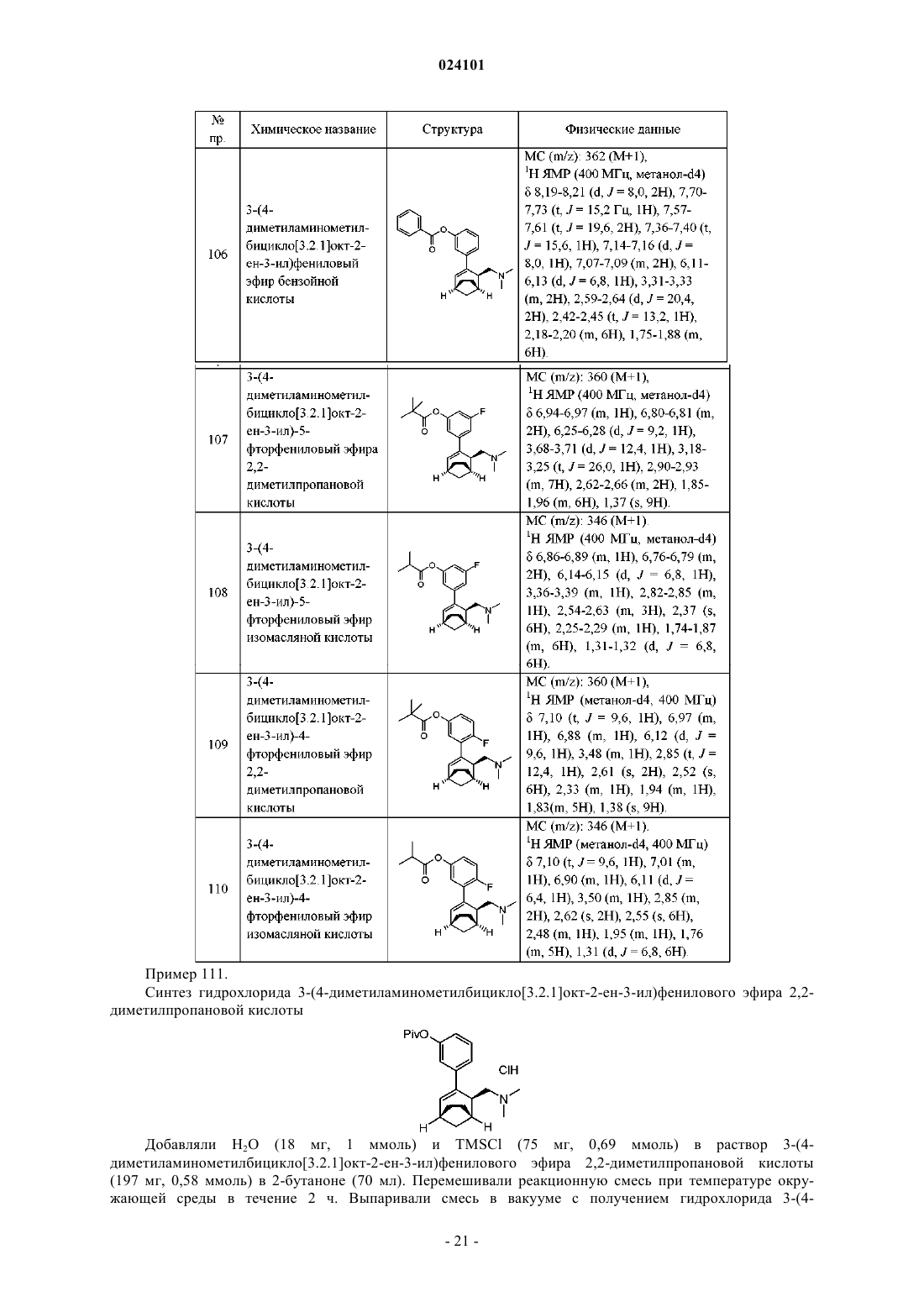
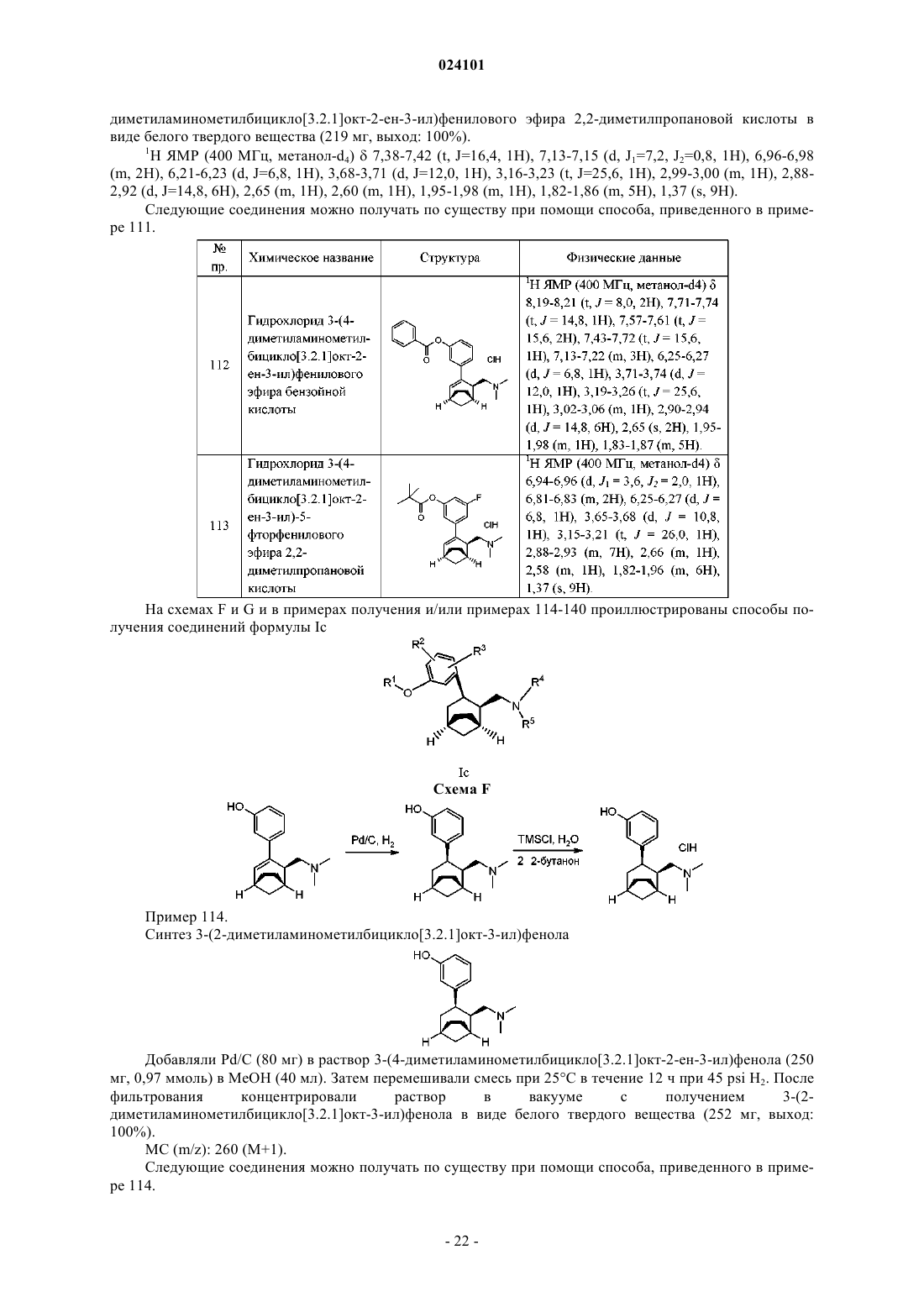
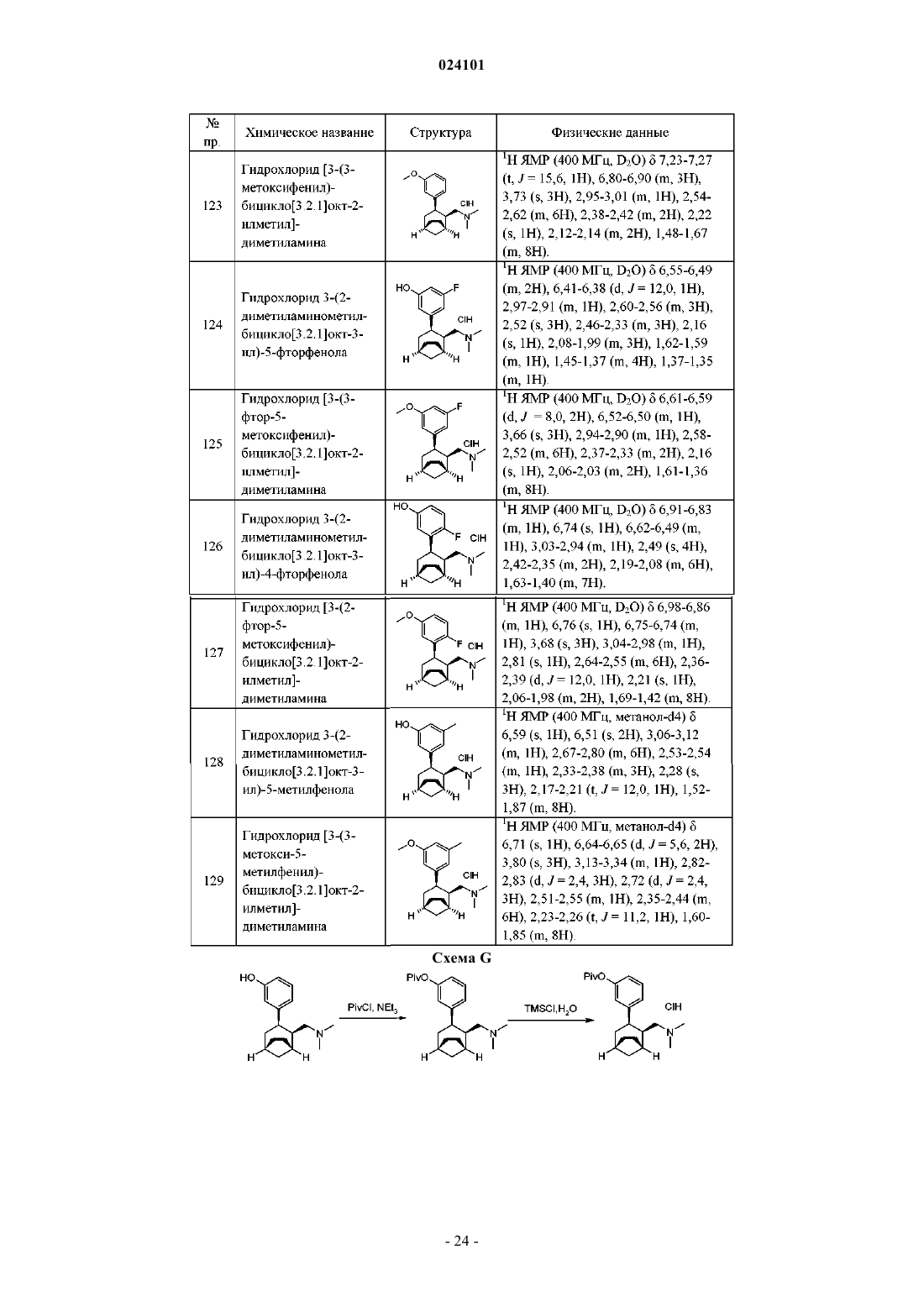
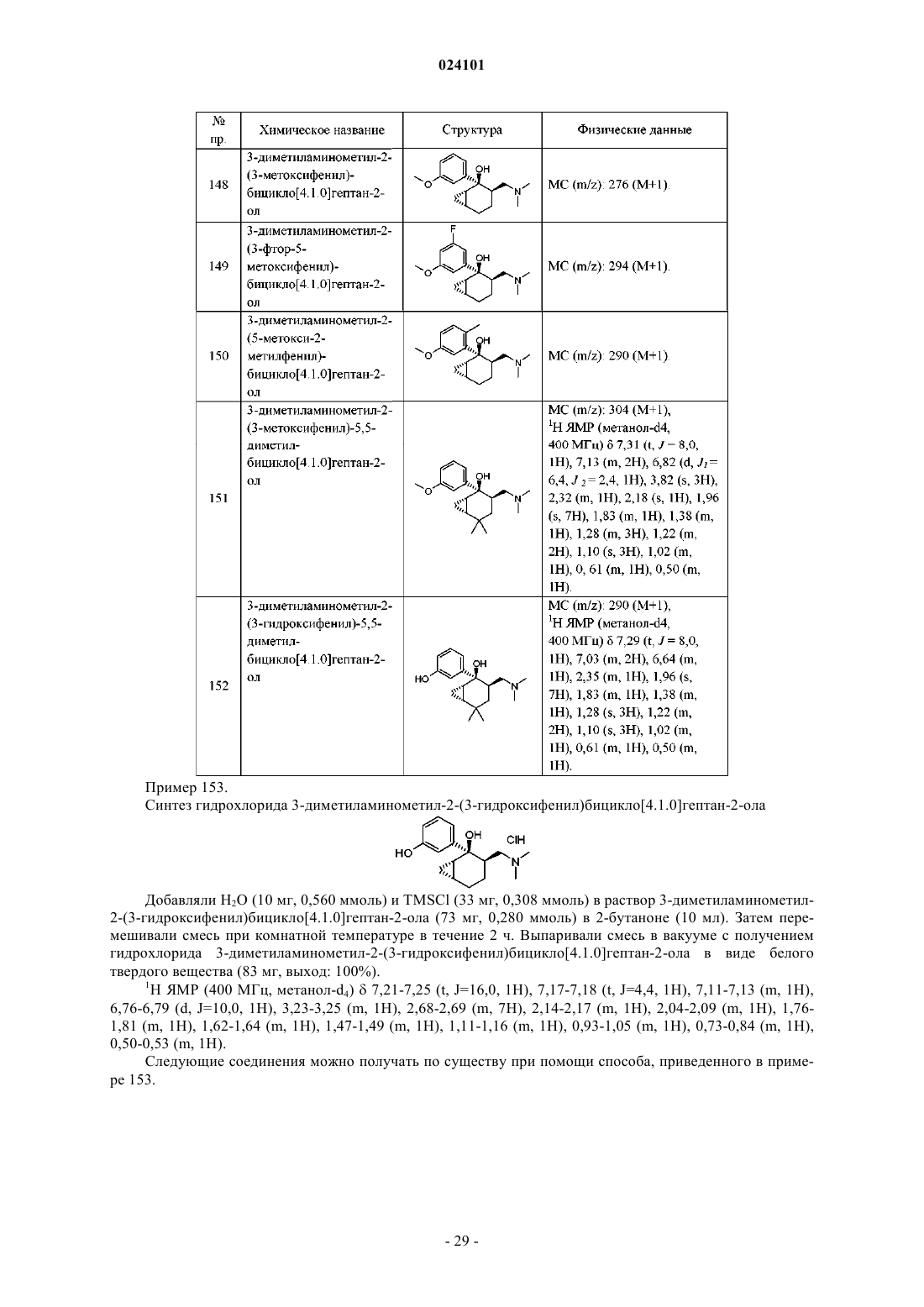
Соединения, обладающие анальгезирующими свойствами, содержащие их составы и их применение в терапии
Номер патента: 24101
Опубликовано: 31.08.2016
Авторы: Лу Лунь, Ма Юйцзюань, Холмстром Скотт Дейл, Чэнь Шухуй, Дефо Джин Мари, Чзан Ян, У Вэньтао, Пэн Сянь
Формула / Реферат
1. Соединение формулы I или его фармацевтически приемлемая соль
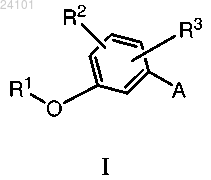
где А представляет собой
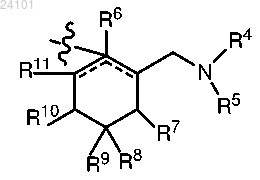
R1 представляет водород, C1-C5-алкил, C1-C5-галогеналкил, -(C1-C5-алкил)фенил или фенил или группу формулы -C(O)-R12, в которой R12 представляет собой C1-C5-алкил, C1-C5-алкокси, C1-C5-галогеналкил, -(C1-C5-алкил)фенил или фенил;
R2 представляет собой водород, C1-C5-алкил, C1-C5-алкокси, галоген, C1-C5-галогеналкил или C1-C5-галогеналкокси;
R3 представляет собой водород, C1-C5-алкил, C1-C5-алкокси, галоген, C1-C5-галогеналкил или C1-C5-галогеналкокси;
R4 представляет собой водород, C1-C5-алкил или -(C1-C5-алкил)фенил;
R5 представляет собой водород, C1-C5-алкил или -(C1-C5-алкил)фенил;
R6 представляет собой водород, гидрокси или отсутствует;
R7 представляет собой водород;
R8 представляет собой водород или метил;
R9 представляет собой водород или метил;
R10 представляет собой водород;
R11 представляет собой водород или C1-C5-алкил;
при условии, что присутствует одно из А), В) или С), где:
A) R7 и R10 объединены с образованием -СН2- или -(СН2)2-;
B) R8 и R9 совместно с атомом углерода, к которому они присоединены, объединены с образованием циклопропильной группы; или
C) R10 и R11 объединены с образованием -СН2- или -(СН2)3-.
2. Соединение по п.1 или его фармацевтически приемлемая соль, отличающееся тем, что А выбран из
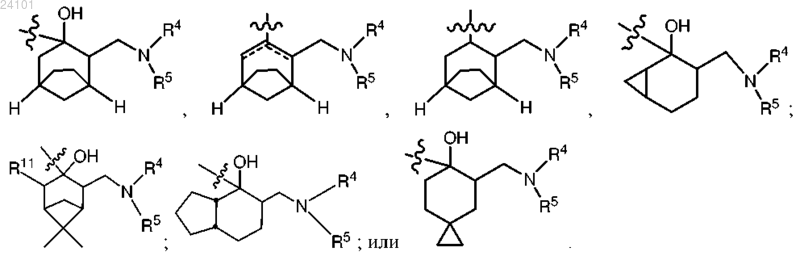
3. Соединение по п.2, имеющее формулу Ia
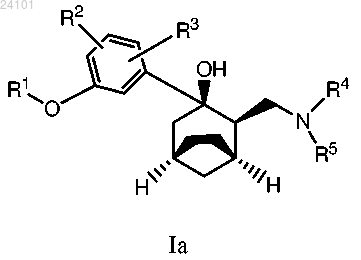
или его фармацевтически приемлемая соль.
4. Соединение по п.2, отличающееся тем, что указанное соединение представляет собой
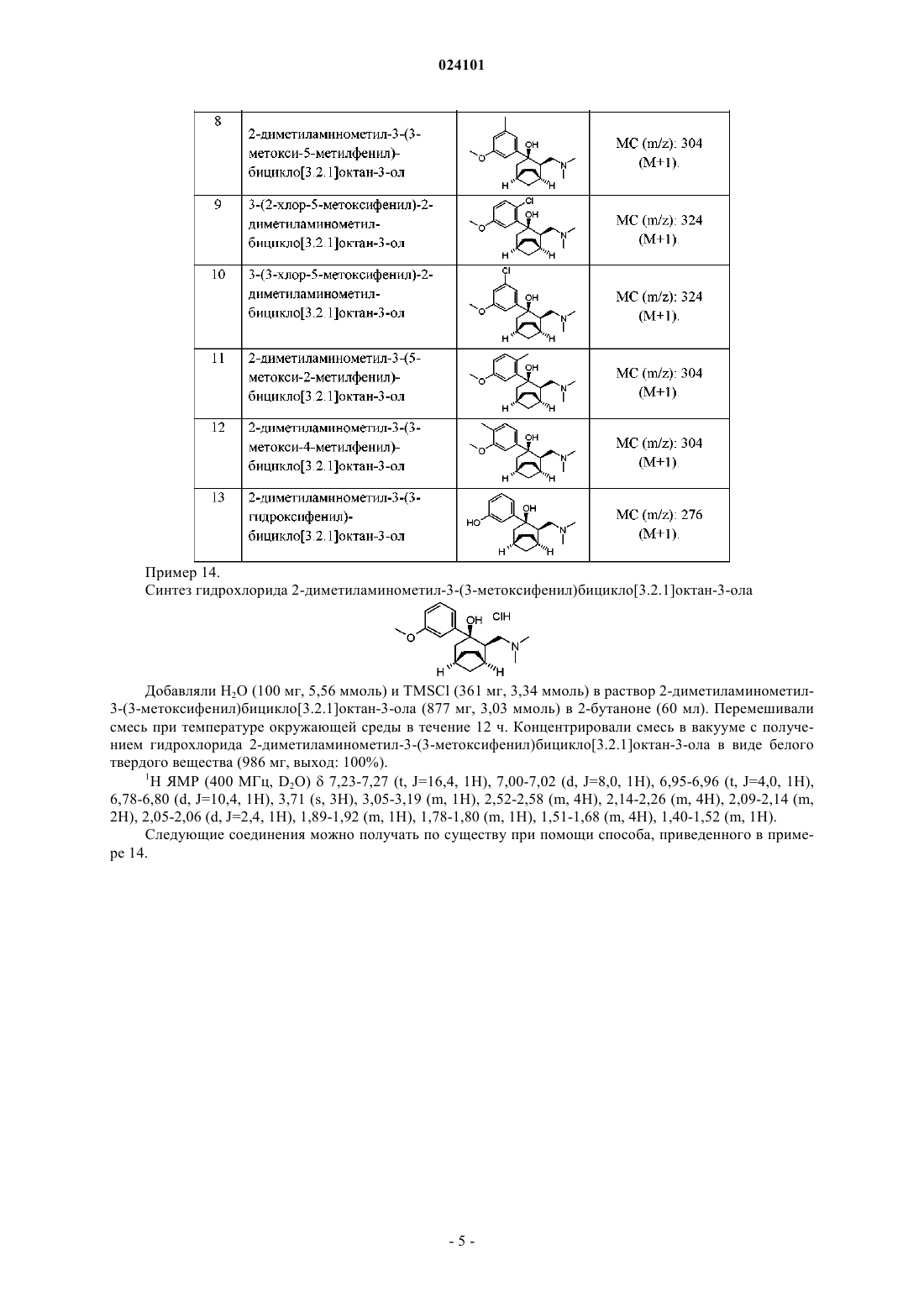
2-диметиламинометил-3-(3-метоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-фтор-5-метоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(5-метокси-2-трифторметоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(2-фтор-5-метоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(4-фтор-3-метоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(2-фтор-3-метоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-метокси-5-метилфенил)бицикло[3.2.1]октан-3-ол;
3-(2-хлор-5-метоксифенил)-2-диметиламинометилбицикло[3.2.1]октан-3-ол;
3-(3-хлор-5-метоксифенил)-2-диметиламинометилбицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(5-метокси-2-метилфенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-метокси-4-метилфенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-гидроксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(2-фтор-5-гидроксифенил)бицикло[3.2.1]октан-3-ол;
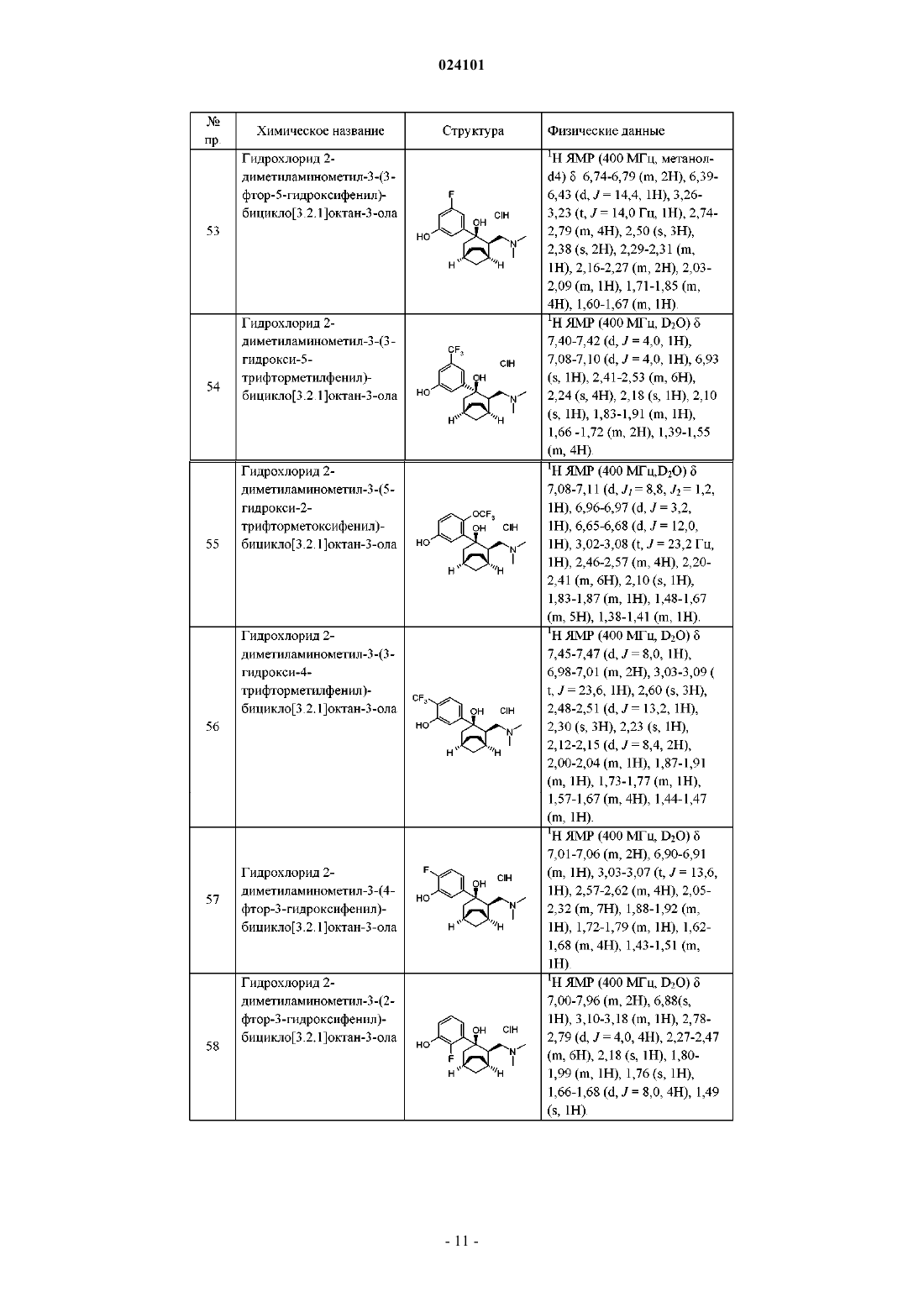
2-диметиламинометил-3-(3-фтор-5-гидроксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-гидрокси-5-трифторметилфенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(5-гидрокси-2-трифторметоксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-гидрокси-4-трифторметилфенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(4-фтор-3-гидроксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(2-фтор-3-гидроксифенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-гидрокси-5-метилфенил)бицикло[3.2.1]октан-3-ол;
3-(2-хлор-5-гидроксифенил)-2-диметиламинометилбицикло[3.2.1]октан-3-ол;
3-(3-хлор-5-гидроксифенил)-2-диметиламинометилбицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(5-гидрокси-2-метилфенил)бицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(3-гидрокси-4-метилфенил)бицикло[3.2.1]октан-3-ол;
3-(3,4-дифтор-5-гидроксифенил)-2-диметиламинометилбицикло[3.2.1]октан-3-ол;
2-диметиламинометил-3-(2-фтор-5-гидроксифенил)бицикло[3.2.1]октан-3-ол;
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)-4-фторфениловый эфир 2,2-диметилпропановой кислоты;
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)-4-фторфениловый эфир бензойной кислоты;
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)фениловый эфир 2,2-диметилпропановой кислоты;
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)фениловый эфир бензойной кислоты;
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)-5-фторфениловый эфир 2,2-диметилпропановой кислоты или
3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт-3-ил)-5-фторфениловый эфир бензойной кислоты;
или его фармацевтически приемлемая соль.
5. Соединение по п.2, имеющее формулу Ib
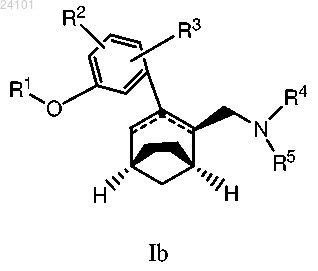
или его фармацевтически приемлемая соль.
6. Соединение по п.2, отличающееся тем, что указанное соединение представляет собой
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенол;
[3-(3-метоксифенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
[3-(5-метокси-2-трифторметоксифенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-4-трифторметоксифенол;
[3-(3-фтор-5-метоксифенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-5-фторфенол;
[3-(2-фтор-5-метоксифенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-4-фторфенол;
[3-(3-метокси-5-метилфенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-5-метилфенол;
3-хлор-5-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенол;
[3-(5-метокси-2-метилфенил)бицикло[3.2.1]окт-3-ен-2-илметил]диметиламин;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-4-метилфенол;
4-хлор-3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенол;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фениловый эфир 2,2-диметилпропановой кислоты;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фениловый эфир бензойной кислоты;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-5-фторфениловый эфир 2,2-диметилпропановой кислоты;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-5-фторфениловый эфир изомасляной кислоты;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-4-фторфениловый эфир 2,2-диметилпропановой кислоты или
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)-4-фторфениловый эфир изомасляной кислоты;
или его фармацевтически приемлемая соль.
7. Соединение по п.2, отличающееся тем, что указанное соединение имеет формулу Ic
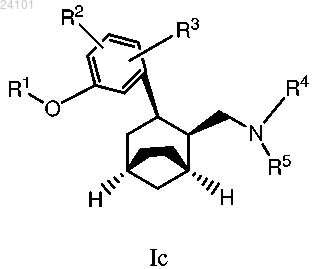
или его фармацевтически приемлемая соль.
8. Соединение по п.2, отличающееся тем, что указанное соединение представляет собой
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)фенол;
[3-(3-метоксифенил)бицикло[3.2.1]окт-2-илметил]диметиламин;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-5-фторфенол;
[3-(3-фтор-5-метоксифенил)бицикло[3.2.1]окт-2-илметил]диметиламин;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-4-фторфенол;
[3-(2-фтор-5-метоксифенил)бицикло[3.2.1]окт-2-илметил]диметиламин;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-5-метилфенол;
[3-(3-метокси-5-метилфенил)бицикло[3.2.1]окт-2-илметил]диметиламин;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)фениловый эфир 2,2-диметилпропановой кислоты;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)фениловый эфир бензойной кислоты;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-5-фторфениловый эфир 2,2-диметилпропановой кислоты;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-5-фторфениловый эфир изомасляной кислоты;
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-4-фторфениловый эфир 2,2-диметилпропановой кислоты или
3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)-4-фторфениловый эфир изомасляной кислоты;
или его фармацевтически приемлемая соль.
9. Соединение по п.2, отличающееся тем, что указанное соединение имеет формулу Id
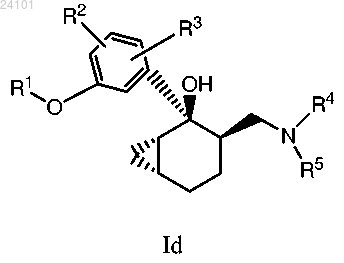
или его фармацевтически приемлемая соль.
10. Соединение по п.2, отличающееся тем, что указанное соединение представляет собой
3-диметиламинометил-2-(3-гидроксифенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-метоксифенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-фтор-5-метоксифенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(5-метокси-2-метилфенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-метоксифенил)-5,5-диметилбицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-гидроксифенил)-5,5-диметилбицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-фтор-5-гидроксифенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(2-фтор-5-гидроксифенил)бицикло[4.1.0]гептан-2-ол;
3-диметиламинометил-2-(3-гидрокси-5-метилфенил)бицикло[4.1.0]гептан-2-ол;
3-(3-диметиламинометил-2-гидроксибицикло[4.1.0]гепт-2-ил)-5-фторфениловый эфир 2,2-диметилпропановой кислоты или
3-(3-диметиламинометил-2-гидроксибицикло[4.1.0]гепт-2-ил)-4-фторфениловый эфир 2,2-диметилпропановой кислоты;
или его фармацевтически приемлемая соль.
11. Соединение по п.2, отличающееся тем, что указанное соединение имеет формулу Ie
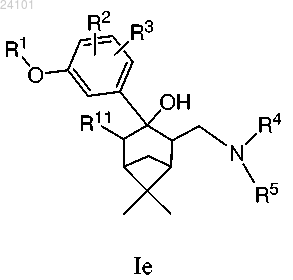
или его фармацевтически приемлемая соль.
12. Соединение по п.11, отличающееся тем, что указанное соединение представляет собой
(1R,2R,3S,4S,5S)-3-(3-гидроксифенил)-2,6,6-триметил-4-((метил(фенэтил)амино)метил)бицикло[3.1.1]гептан-3-ол;
(1R,2R,3S,4S,5S)-3-(3-метоксифенил)-2,6,6-триметил-4-((метил(фенэтил)амино)метил)бицикло[3.1.1]гептан-3-ол;
(1S,2S,3R,4R,5R)-3-(3-гидроксифенил)-2,6,6-триметил-4-((метил(фенэтил)амино)метил)бицикло[3.1.1]гептан-3-ол;
(1S,2S,3R,4R,5R)-3-(3-метоксифенил)-2,6,6-триметил-4-((метил(фенэтил)амино)метил)бицикло[3.1.1]гептан-3-ол;
или его фармацевтически приемлемая соль.
13. Соединение по п.2, отличающееся тем, что указанное соединение имеет формулу If
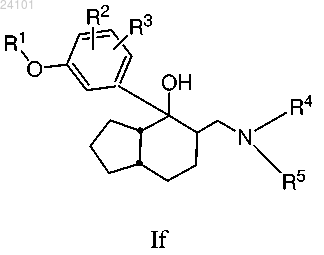
или его фармацевтически приемлемая соль.
14. Соединение по п.13, отличающееся тем, что указанное соединение представляет собой 5-((диметиламино)метил)-4-(3-гидроксифенил)октагидро-1Н-инден-4-ол, или его фармацевтически приемлемая соль.
15. Соединение по п.2, отличающееся тем, что указанное соединение представляет собой
(+)-(1S,2R,3R,5R)-2-((диметиламино)метил)-3-(3-гидроксифенил)бицикло[3.2.1]октан-3-ол;
(-)-(1R,2S,3S,5S)-2-((диметиламино)метил)-3-(3-гидроксифенил)бицикло[3.2.1]октан-3-ол;
(S)-3-((1S,2R,3R,5R)-2-((диметиламино)метил)-3-гидроксибицикло[3.2.1]октан-3-ил)фенил-2-фенилпропаноат;
(S)-3-((1R,2S,3S,5S)-2-((диметиламино)метил)-3-гидроксибицикло[3.2.1]октан-3-ил)фенил-2-фенилпропаноат;
3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенол;
3-((1S,5R)-2-((диметиламино)метил)бицикло[3.2.1]окт-2-ен-3-ил)фенол;
и его фармацевтически приемлемая соль.
16. Соединение по п.2, отличающееся тем, что указанное соединение имеет формулу Ig
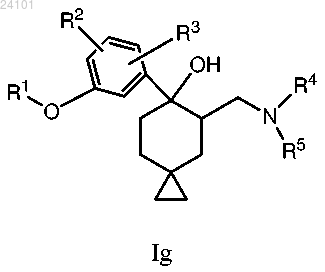
и его фармацевтически приемлемая соль.
17. Соединение по п.16, отличающееся тем, что указанное соединение представляет собой 5-диметиламинометил-6-(2-фтор-5-гидроксифенил)спиро[2.5]октан-6-ол или его фармацевтически приемлемую соль.
18. Соединение по п.4, отличающееся тем, что указанное соединение представляет собой 2-диметиламинометил-3-(3-метокси-5-метилфенил)бицикло[3.2.1]октан-3-ол или его фармацевтически приемлемую соль.
19. Соединение по п.4, отличающееся тем, что указанное соединение представляет собой 2-диметиламинометил-3-(3-гидрокси-5-метилфенил)бицикло[3.2.1]октан-3-ол или его фармацевтически приемлемую соль.
20. Соединение по п.10, отличающееся тем, что указанное соединение представляет собой 3-диметиламинометил-2-(3-фтор-5-гидроксифенил)бицикло[4.1.0]гептан-2-ол или его фармацевтически приемлемую соль.
21. Соединение по п.10, отличающееся тем, что указанное соединение представляет собой 3-диметиламинометил-2-(2-фтор-5-гидроксифенил)бицикло[4.1.0]гептан-2-ол или его фармацевтически приемлемую соль.
22. Соединение по п.10, отличающееся тем, что указанное соединение представляет собой 3-(3-диметиламинометил-2-гидроксибицикло[4.1.0]гепт-2-ил)-5-фторфениловый эфир 2,2-диметилпропановой кислоты или его фармацевтически приемлемую соль.
23. Соединение по п.10, отличающееся тем, что указанное соединение представляет собой 3-(3-диметиламинометил-2-гидроксибицикло[4.1.0]гепт-2-ил)-4-фторфениловый эфир 2,2-диметилпропановой кислоты или его фармацевтически приемлемую соль.
24. Соединение по любому из пп.15-23, отличающееся тем, что указанная фармацевтически приемлемая соль представляет собой гидрохлоридную соль указанных соединений.
25. Фармацевтический анальгезирующий состав, содержащий соединение по любому из пп.1-24 и один или более фармацевтически приемлемых носителей.
26. Фармацевтический состав по п.25, отличающийся тем, что указанный состав представляет собой фармацевтический состав для применения у людей.
27. Фармацевтический состав по п.25, отличающийся тем, что указанный состав представляет собой фармацевтический состав для применения в ветеринарии.
28. Способ подавления, ингибирования, ослабления, снижения или устранения степени тяжести или продолжительности боли у млекопитающего, включающий введение указанному млекопитающему эффективного количества соединения по любому из пп.1-24.
29. Способ по п.28, отличающийся тем, что указанное млекопитающее представляет собой человека.
30. Способ по п.28, отличающийся тем, что указанное млекопитающее представляет собой домашнее животное.
31. Способ по п.30, отличающийся тем, что указанное домашнее животное представляет собой собаку или кошку.
32. Применение соединения или фармацевтически приемлемой соли по любому из пп.1-24 в терапии, связанной с лечением боли.
33. Применение соединения или фармацевтически приемлемой соли по любому из пп.1-24 для подавления, ингибирования, ослабления, снижения или устранения степени тяжести или продолжительности боли.
Текст
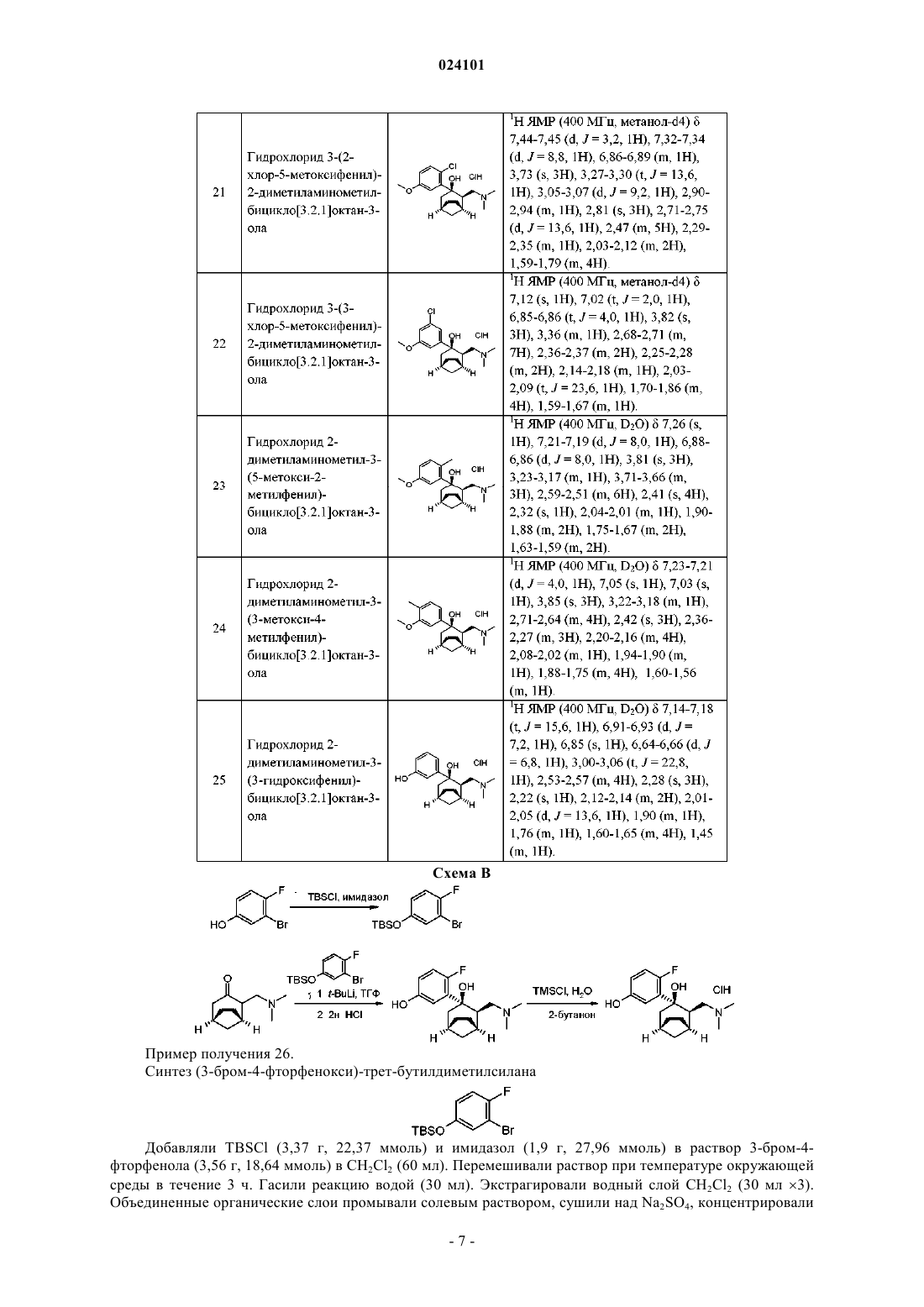
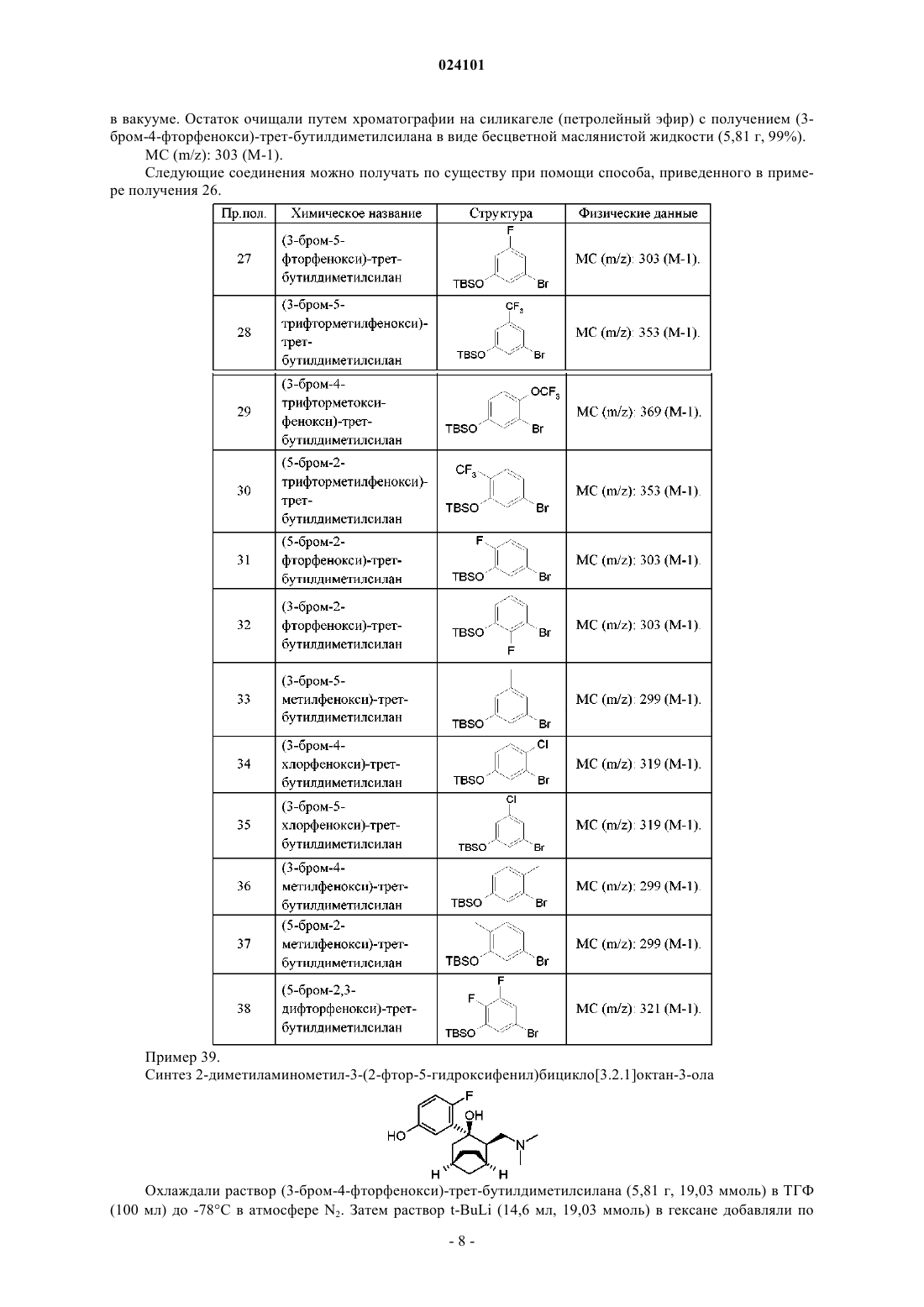
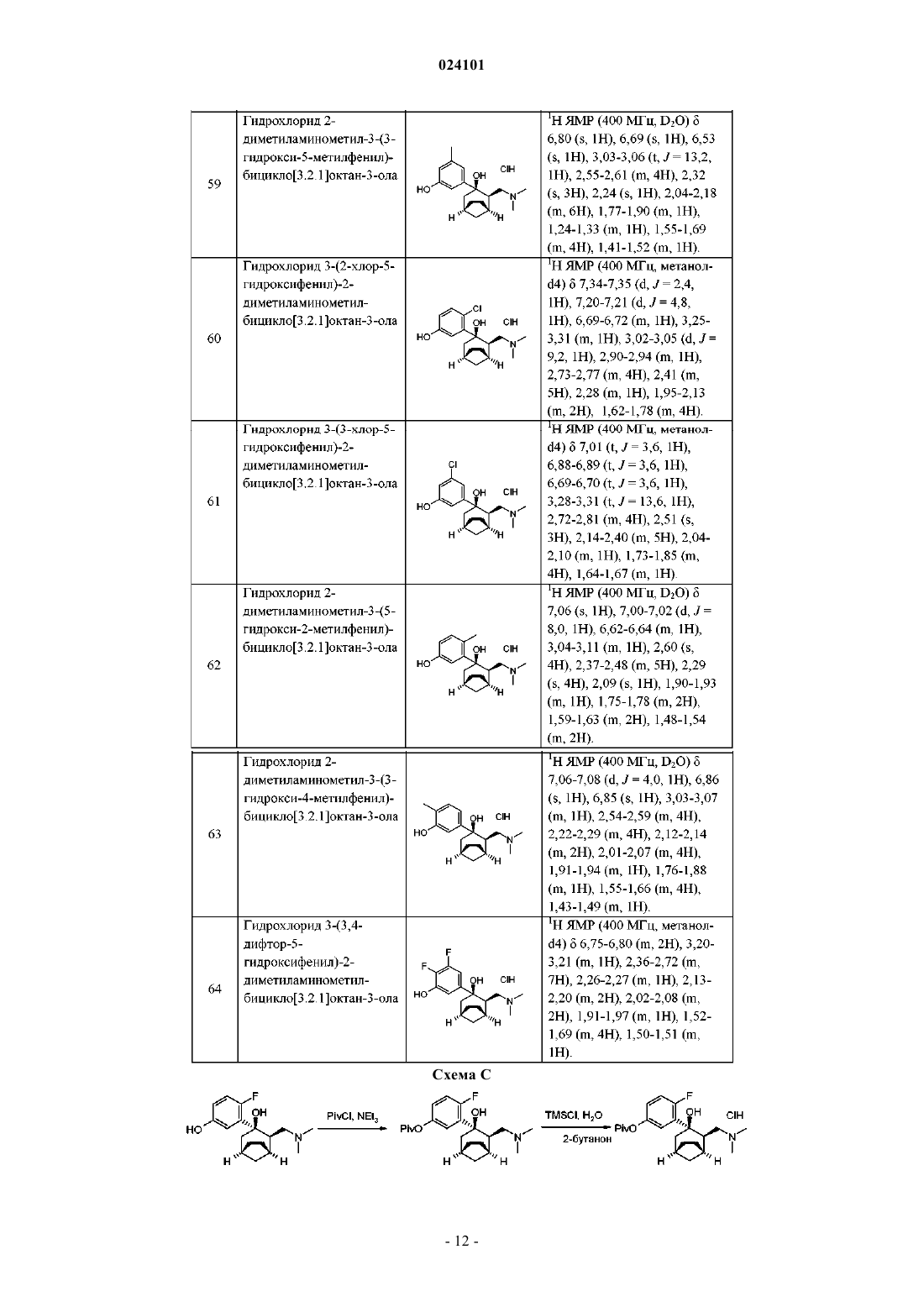
Предложены анальгезирующие соединения формулы I и их фармацевтически приемлемые соли и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10 и R11 раскрыты в описании и где присутствует одно из А, В или С:A) R7 и R10 объединены с образованием -СН 2- или -(СН 2)2-; B) R8 и R9 совместно с атомом углерода,к которому они присоединены, объединены с образованием циклопропильной группы; или C) R10 и R11 объединены с образованием -СН 2- или -(СН 2)3-. Кроме того, предложены анальгезирующие фармацевтические составы и способы применения, в которых используют предложенные выше соединения.(71)(73) Заявитель и патентовладелец: ЭЛИ ЛИЛЛИ ЭНД КОМПАНИ (US) Опиаты, представляющие собой класс соединений центрального действия, являются наиболее часто используемыми агентами для контролирования и ослабления боли, которые воздействуют на один или более опиатных рецепторов у человека или млекопитающего. Технически, опиаты представляют собой природные алкалоиды, содержащиеся в смоле опийного мака, но при использовании в настоящем изобретении данный термин включает и синтетические варианты, называемые опиоидами. Опиаты являются наркотическими анальгетиками агонистического действия и представляют собой лекарственные средства, содержащие или полученные из опиума, такие как морфин, кодеин и множество синтетических соединений, родственных морфину, причем наиболее широко используемыми опиатами являются препараты морфина и гидрокодона. Опиаты представляют собой природные и синтетические лекарственные средства, обладающие схожим с морфином действием, и контролируются Федеральным законом США по обороту наркотических средств (которые являются препаратами строгого учета), а также законодательствами большинства других стран и международных организаций, так как они вызывают привыкание и впоследствии оказывают разрушительное действие на лиц, злоупотребляющих опиатами, а также лиц, каким-либо образом связанных с ними. Трамадол является синтетическим аналогом фенантренового алкалоида кодеина и как таковой представляет собой опиоид, а также пролекарство (кодеин при метаболизме превращается в морфин,трамадол превращается в М-1, также называемый О-дезметилтрамадол). Применение трамадола, подобно другим опиатам, связано с отрицательными эффектами, такими как физическая и психологическая зависимость, тяжелые абстинентные симптомы, а также с другими менее серьезными побочными эффектами, включая тошноту, рвоту, потливость, запоры и сонливость. Несмотря на то что опиаты и родственные им лекарственные средства с очевидностью служат полезной цели, ввиду известных проблем, связанных с опиатами, желательно обеспечить альтернативные терапии и соединения для ослабления боли. В частности, такие альтернативные способы терапии могли бы обеспечиваться с помощью соединений, не подлежащих строгой учетности, позволяющих снизить частоту дозирования и/или не имеющих побочных эффектов совсем или имеющих побочные эффекты,но не в такой степени, как опиаты и родственные лекарственные средства. Предложены анальгезирующие соединения и их соли формулы IR1 представляет собой водород, C1-C5-алкил, C1-C5-галогеналкил, -(C1-C5-алкил)фенил или фенил или группу формулы -C(O)-R12, в которой R12 представляет собой C1-C5-алкил, C1-C5-алкокси, C1-C5 галогеналкил, -(C1-C5-алкил)фенил или фенил;R8 представляет собой водород или метил;R9 представляет собой водород или метил;R11 представляет собой водород или C1-C5-алкил; или R7 и R10 объединены с образованием -СН 2- или -(СН 2)2-; при условии, что присутствует одно из А), В) или С), где Среди первых четырех определений А, приведенных непосредственно выше, предпочтительными являются следующие:C1-C5-алкил относится к линейным и разветвленным алкилам, содержащим от одного до пяти атомов углерода и включает метил, этил, пропил, н-бутил, изобутил, пентил, изопентил и неопентил.C1-C5-алкокси относится к линейным и разветвленным алкоксигруппам, содержащим от одного до пяти атомов углерода, и включает метокси, этокси, пропокси, н-бутокси, изобутокси, пентокси, изопентокси и неопентокси. Галоген или галоген- относится к фтору, брому, хлору и йоду. Галогеналкил, используемый в настоящем описании, относится к алкилу (определенному выше),замещенному одним или более атомами галогенов. Указанные группы включают трифторметил, метилхлорид, дихлорметил, пентилхлорид, бутилхлорид и изопропилхлорид. Галогеналкокси относится к алкоксигруппе, описанной в настоящем изобретении, которая является замещенной и содержит от одной до шести галогеновых групп. Примеры фторалкоксигрупп включают фторметокси, дифторметокси, трифторметокси, пентафторэтокси и трифторэтокси. фрагмент может представлять собой или в зависимости от конкретного случая.PivCl относится к пивалоилхлориду. Снятие боли относится к подавлению, ингибированию, ослаблению, снижению или устранению боли, степени тяжести и/или продолжительности боли. Таким образом, изобретение можно применять для ослабления существующей боли, а также для подавления или ингибирования боли, которая в противном случае проявляется в результате явления, неизбежно вызывающего боль. Ослабляемая боль может быть хронической или острой. Млекопитающее включает человека и млекопитающих, отличных от человека. Млекопитающие,отличные от человека, включают домашних животных, таких как скот и комнатные животные. Скот включает коров, верблюдов, свиней, овец, коз и лошадей. Комнатные животные включают собак, кроликов, кошек и других животных, которых заводят и держат в тесном контакте с людьми как часть связи человек-животное. Эффективное количество относится к количеству соединения формулы I или его соли, достаточному для снятия или ослабления боли у млекопитающего, нуждающегося в этом, и, как таковое, зависит от нескольких факторов. Диапазоны количеств соединения формулы I или его солей, применяемого в способах, составляют от 0,01 до 1000 мг/кг, желательно от 0,1 до 100 мг/кг массы тела животного. Частота введения также зависит от нескольких факторов и может составлять одну дозу, которую вводят один раз в день или один раз в неделю в течение периода времени, определенного лечащим врачом или ветеринаром. Дозу также можно делить на две или более меньших доз, которые вводят с интервалами, для достижения снятия или ослабления боли. солей и компонентов состава, таких как носители, включает "ветеринарно приемлемый" и, таким образом, независимо охватывает применение у человека и животных. Фармацевтически приемлемые соли и общая методология их получения известны в данной области техники. См., например, P. Stahl, et al., HANDBOOK OF PHARMACEUTICAL SALTS: PROPERTIES,SELECTION AND USE, (VCHA/Wiley-VCH, 2002); S.M. Berge, et al., "Pharmaceutical Salts," Journal ofPharmaceutical Sciences, Vol. 66, No. 1, January 1977. Предпочтительной солью является гидрохлоридная соль. Соединения формулы I и их соли можно получать в виде фармацевтических композиций для системного введения. Указанные фармацевтические композиции для применения у человека и млекопитающих, отличных от человека, и способы их получения известны в данной области техники. См., например, REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY, (A. Gennaro, et al., eds., 19th ed.,Mack Publishing Co., 1995). В состав, содержащий соединение формулы I или его соль, можно включать дополнительные активные ингредиенты. Носитель используют в настоящем изобретении для описания любого ингредиента, отличного от активного(ых) компонента(ов), содержащегося(ихся) в составе. Выбор носителя в большой степени зависит от таких факторов, как конкретный способ введения, действие носителя на растворимость и стабильность и природа лекарственной формы. Соединения согласно настоящему изобретению можно получать при помощи описанных далее способов, а также при помощи способов, описанных в Selnick, H.С.; Bourgeois, M.L.; Butcher, J.W.; Radzilowski, E.M. Tetrahedron Lett, 1993, 34, 2043; Alvarado, С.; Guzman, A.; Diaz, E.; Patino. R.I. Мех. Chem.Res. Dev. 2002, 6, 729; и Mohacsi, E.; O'Brien, J.P.; Blount, J. F. J.Heterocycl. Chem. 1990, 27, 1623. В изобретении предложен фармацевтический состав, содержащий соединение формулы I или его фармацевтически приемлемую соль, и один или более фармацевтически приемлемых носителей. Фармацевтический состав может дополнительно содержать по меньшей мере один дополнительный активный ингредиент. Фармацевтический состав может представлять собой фармацевтический состав для введения человеку или фармацевтический состав для использования в ветеринарии. В изобретении предложен способ снятия боли у млекопитающего, нуждающегося в этом, включающий введение эффективного количества соединения формулы I или его фармацевтически приемлемой соли указанному млекопитающему. Способ может дополнительно включать введение по меньшей мере одного другого активного ингредиента указанному млекопитающему. Млекопитающее может представлять собой человека или млекопитающее, отличное от человека, кроме того, может представлять собой комнатное животное, такое как собака или кошка. На схемах А-С, в примерах получения и/или в примерах 1-76 проиллюстрированы способы получения соединений формулы Ia Смесь бицикло[3.2.1]октан-3-она (5,2 г, 41,9 ммоль), (НСНО)n (1,51 г, 50,3 ммоль), гидрохлорида диметиламина (3,42 г, 41,9 ммоль) и 0,5 мл конц. HCl в MeCN (50 мл) перемешивали при 80 С в течение 2 ч. После удаления растворителя в вакууме растворяли остаток в Н 2 О (20 мл) и промывали EtOAc (20 мл 3). Подщелачивали водный раствор при помощи NaOH до рН 10. Полученную водную смесь экстрагировали EtOAc (60 мл 3). Объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением неочищенного 2 диметиламинометилбицикло[3.2.1]октан-3-она в виде коричневой маслянистой жидкости (5,9 г, выход: 78,7%). МС (m/z): 182 (М+1). Пример 2. Синтез 2-диметиламинометил-3-(3-метоксифенил)бицикло[3.2.1]октан-3-ола Раствор t-BuLi (19,2 мл, 25,0 ммоль) в гексане при помощи шприца добавляли по каплям в раствор 1-бром-3-метоксибензола (3,74 г, 20,0 ммоль) в ТГФ (60 мл) при -78 С в атмосфере N2. После перемешивания при -78 С в течение 1 ч добавляли по каплям раствор 2-диметиламинометилбицикло[3.2.1]октан-3 она (1,81 г, 10,0 ммоль) в ТГФ (10 мл) в реакционную смесь и дополнительно перемешивали полученную смесь при -78 С в течение 1 ч. Гасили реакцию насыщенным водным раствором NH4Cl (20 мл) Экстрагировали водную смесь EtOAc (50 мл 3). Объединенные органические слои промывали солевым раствором (15 мл), сушили над Na2SO4, фильтровали и концентрировали в вакууме. Очищали остаток путем хроматографии на силикагеле (CH2Cl2:МеОН=30:1) с получением 2-диметиламинометил-3-(3 метоксифенил)бицикло[3.2.1]октан-3-ола в виде белого твердого вещества (1,49 г, выход: 51%). МС (m/z): 290 (М+1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 2. Добавляли Н 2 О (100 мг, 5,56 ммоль) и TMSCl (361 мг, 3,34 ммоль) в раствор 2-диметиламинометил 3-(3-метоксифенил)бицикло[3.2.1]октан-3-ола (877 мг, 3,03 ммоль) в 2-бутаноне (60 мл). Перемешивали смесь при температуре окружающей среды в течение 12 ч. Концентрировали смесь в вакууме с получением гидрохлорида 2-диметиламинометил-3-(3-метоксифенил)бицикло[3.2.1]октан-3-ола в виде белого твердого вещества (986 мг, выход: 100%). 1H ЯМР (400 МГц, D2O)7,23-7,27 (t, J=16,4, 1H), 7,00-7,02 (d, J=8,0, 1H), 6,95-6,96 (t, J=4,0, 1H),6,78-6,80 (d, J=10,4, 1H), 3,71 (s, 3H), 3,05-3,19 (m, 1H), 2,52-2,58 (m, 4H), 2,14-2,26 (m, 4H), 2,09-2,14 (m,2H), 2,05-2,06 (d, J=2,4, 1H), 1,89-1,92 (m, 1H), 1,78-1,80 (m, 1H), 1,51-1,68 (m, 4H), 1,40-1,52 (m, 1H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 14. Добавляли TBSCl (3,37 г, 22,37 ммоль) и имидазол (1,9 г, 27,96 ммоль) в раствор 3-бром-4 фторфенола (3,56 г, 18,64 ммоль) в CH2Cl2 (60 мл). Перемешивали раствор при температуре окружающей среды в течение 3 ч. Гасили реакцию водой (30 мл). Экстрагировали водный слой CH2Cl2 (30 мл 3). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4, концентрировали в вакууме. Остаток очищали путем хроматографии на силикагеле (петролейный эфир) с получением (3 бром-4-фторфенокси)-трет-бутилдиметилсилана в виде бесцветной маслянистой жидкости (5,81 г, 99%). МС (m/z): 303 (М-1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере получения 26. каплям при помощи шприца в реакционный раствор. После перемешивания при -78 С в течение 1 ч добавляли по каплям раствор 2-диметиламинометилбицикло[3.2.1]октан-3-она (2,87 г, 15,86 ммоль) в ТГФ(1,5 мл) в реакционную смесь и дополнительно перемешивали смесь при -78 С в течение 1 ч. Гасили реакцию 60 мл разбавленной HCl (2 н.) и перемешивали при температуре окружающей среды в течение 2 ч. Подщелачивали полученную смесь при помощи K2CO3 до рН 9 и экстрагировали EtOAc (100 мл 3). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4, фильтровали и концентрировали в вакууме. Очищали остаток путем хроматографии на силикагеле (градиент от CH2Cl2 доCH2Cl2:MeOH=10:1) с получением 2-диметиламинометил-3-(2-фтор-5 гидроксифенил)бицикло[3.2.1]октан-3-ола в виде белого твердого вещества (2,38 г, выход: 51,2%). МС (m/z): 294 (М+1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 39. Добавляли Н 2 О (175,1 мг, 9,73 ммоль) и TMSCl (1,057 г, 9,73 ммоль) в раствор 2 диметиламинометил-3-(2-фтор-5-гидроксифенил)бицикло[3.2.1]октан-3-ола (2,38 г, 8,11 ммоль) в 2 бутаноне (60 мл). Перемешивали реакционную смесь при температуре окружающей среды в течение 3 ч. После удаления растворителя путем выпаривания промывали остаток EtOAc с получением гидрохлорида 2-диметиламинометил-3-(2-фтор-5-гидроксифенил)бицикло[3.2.1]октан-3-ола в виде белого твердого вещества (2,23 г, выход: 83,5%). 1H ЯМР (400 МГц, D2O)6,89-6,93 (m, 2H), 6,66-6,70 (m, 1H), 3,10-3,14 (m, 1H), 2,59-2,65 (m, 4H),2,42-2,44 (d, J=8,0, 1H), 2,36-2,41 (d, J=20,0, 3 Н), 2,30-2,33 (d, J=12,0, 2H), 2,18 (s, 1H), 1,89-1,95 (m, 1H),1,74-1,78 (m, 1H), 1,51-1,67 (m, 4H), 1,47-1,50 (m, 1H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 52.(587 мг, 2,0 ммоль), 2,2-диметилпропионилхлорида (361,5 мг, 3,0 ммоль) и триэтиламина (606 мг, 6,0 ммоль) в CH2Cl2 (60 мл) при температуре окружающей среды в течение 12 ч. Концентрировали смесь в вакууме и очищали остаток путем препаративной ТСХ с получением 3-(2-диметиламинометил-3 гидроксибицикло[3.2.1]окт-3-ил)-4-фторфенилового эфира 2,2-диметилпропановой кислоты (368 мг, выход: 48,8%). МС (m/z): 378 (М+1). 1 Н ЯМР (400 МГц, метанол-d4)7,29-7,32 (d, J1=6,8, J2=2,8, 1H), 7,14-7,19 (d, J1=11,6, J2=8,8, 1H),7,01-7,05 (m, 1H), 3,19-3,25 (m, 1H), 2,64-2,67 (d, J=13,6, 1H), 2,51 (s, 6H), 2,46-2,48 (m, 2H), 2,36-2,40 (m,2H), 2,25-2,30 (m, 1H), 1,99-2,06 (m, 1H), 1,78-1,85 (m, 4H), 1,61-1,65 (m, 1H), 1,36 (s, 9H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 65. Добавляли Н 2 О (9 мг, 0,5 ммоль) и TMSCl (43 мг, 0,397 ммоль) в раствор 3-(2-диметиламинометил 3-гидроксибицикло[3.2.1]окт-3-ил)-4-фторфенилового эфира 2,2-диметилпропановой кислоты (150 мг,0,397 ммоль) в 2-бутаноне (50 мл). Перемешивали реакционную смесь при 0 С в течение 2 ч. Выпаривали смесь в вакууме с получением гидрохлорида 3-(2-диметиламинометил-3-гидроксибицикло[3.2.1]окт 3-ил)-4-фторфенилового эфира 2,2-диметилпропановой кислоты в виде белого твердого вещества (164 мг, выход: 100%). 1H ЯМР (400 МГц, метанол-d4)7,30-7,32 (d, J1=6,8, J2=2,8, 1H), 7,15-7,20 (d, J1=11,6, J2=8,8, 1H),7,03-7,06 (m, 1H), 3,28-3,31 (m, 1H), 2,77-2,81 (m, 4H), 2,37-2,52 (m, 7H), 2,27 (m, 1H), 2,03 (m, 1H), 1,791,86 (m, 4H), 1,63-1,65 (m, 1H), 1,38 (s, 9 Н). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 71. На схемах D и Е и в примерах 77-113 проиллюстрированы способы получения соединений приведенной ниже формулы(5,0 г,29,1 ммоль) в раствор 2-диметиламинометил-3-(3 гидроксифенил)бицикло[3.2.1]октан-3-ола (4,8 г, 17,5 ммоль) в толуоле (150 мл). Кипятили реакционную смесь с обратным холодильником в течение 2 ч, а затем реакцию гасили путем добавления насыщенного водного K2CO3 (20 мл). Экстрагировали водный слой EtOAc (60 мл 3). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4 и выпаривали в вакууме. Очищали остаток путем препаративной ВЭЖХ с получением 3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенола в виде белого твердого вещества (2,27 г, 50,2%). МС (m/z): 258 (М+1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 77. Добавляли Н 2 О (392 мг, 21,8 ммоль) и TMSCl (1,4 г, 12,9 ммоль) в раствор 3-(4 диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенола (2,8 г, 10,9 ммоль) в 2-бутаноне (200 мл). Перемешивали реакционную смесь при температуре окружающей среды в течение 12 ч. Собирали осадок пу- 17024101 тем фильтрования и промывали EtOAc (30 мл 2), сушили в вакууме с получением гидрохлорида 3-(4 диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенола в виде белого твердого вещества (2,41 г, выход: 75,5%). 1H ЯМР (400 МГц, D2O)7,20-7,24 (t, J=15,6, 1H), 6,76-6,81 (m, 2 Н), 6,72 (s, 1H), 6,15 (d, J=6,4, 1H),3,58-3,61 (d, J=12,8, 1H), 3,08-3,14 (t, J=26,0, 1H), 2,89-2,92 (m, 1H), 2,88 (s, 3 Н), 2,76 (s, 3 Н), 2,56 (m, 1H),2,45 (m, 1H), 1,72-1,83 (m, 6H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 91.CH2Cl2 (40 мл) при температуре окружающей среды в течение 12 ч. Концентрировали смесь в вакууме и очищали остаток путем препаративной ТСХ с получением 3-(4-диметиламинометилбицикло[3.2.1]окт-2 ен-3-ил)фенилового эфира 2,2-диметилпропановой кислоты в виде белого твердого вещества (232 мг,выход: 87,5%). МС (m/z): 342 (М+1%). 1H ЯМР (400 МГц, метанол-d4)7,29-7,32 (t, J=15,6 Гц, 1H), 7,06-7,08 (d, J=7,6, 1H), 6,88-6,90 (d,J1=8,0, J2=1,6, 1H), 6,84-6,85 (t, J=3,6, 1H), 6,05-6,07 (d, J=6,8, 1H), 3,22-3,32 (m, 1H), 2,52-2,60 (m, 1H),2,62-2,63 (m, 1H), 2,37-2,41 (m, 1H), 2,17 (s, 6H), 2,07-2,14 (m, 1H), 1,71-1,85 (m, 6H), 1,37 (s, 9H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 105.(197 мг, 0,58 ммоль) в 2-бутаноне (70 мл). Перемешивали реакционную смесь при температуре окружающей среды в течение 2 ч. Выпаривали смесь в вакууме с получением гидрохлорида 3-(4- 21024101 диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенилового эфира 2,2-диметилпропановой кислоты в виде белого твердого вещества (219 мг, выход: 100%). 1(m, 2H), 6,21-6,23 (d, J=6,8, 1H), 3,68-3,71 (d, J=12,0, 1H), 3,16-3,23 (t, J=25,6, 1H), 2,99-3,00 (m, 1H), 2,882,92 (d, J=14,8, 6H), 2,65 (m, 1H), 2,60 (m, 1H), 1,95-1,98 (m, 1H), 1,82-1,86 (m, 5H), 1,37 (s, 9H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 111. На схемах F и G и в примерах получения и/или примерах 114-140 проиллюстрированы способы получения соединений формулы Ic Добавляли Pd/C (80 мг) в раствор 3-(4-диметиламинометилбицикло[3.2.1]окт-2-ен-3-ил)фенола (250 мг, 0,97 ммоль) в МеОН (40 мл). Затем перемешивали смесь при 25 С в течение 12 ч при 45 psi H2. После фильтрования концентрировали раствор в вакууме с получением 3-(2 диметиламинометилбицикло[3.2.1]окт-3-ил)фенола в виде белого твердого вещества (252 мг, выход: 100%). МС (m/z): 260 (М+1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 114. Добавляли Н 2 О (70 мг, 3,89 ммоль) и TMSCl (126 мг, 1,17 ммоль) в раствор 3-(2 диметиламинометилбицикло[3.2.1]окт-3-ил)фенола (252 мг, 0,97 ммоль) в 2-бутаноне (30 мл). Затем перемешивали реакционную смесь при температуре окружающей среды в течение 12 ч. Выпаривали смесь в вакууме с получением гидрохлорида 3-(2-диметиламинометилбицикло[3.2.1]окт-3-ил)фенола в виде белого твердого вещества (286 мг, выход: 99,8%). 1H ЯМР (400 МГц, D2O)7,04-7,07 (t, J=10,4, 1H), 6,58-6,72 (m, 3 Н), 2,80-2,91 (m, 1H), 2,52-2,54 (m,3 Н), 2,44-2,48 (m, 3 Н), 2,33-2,41 (m, 1H), 2,20-2,29 (m, 1H), 2,11 (s, 1H), 1,99 (s, 2H), 1,36-1,47 (m, 8H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 122.CH2Cl2 (40 мл) при температуре окружающей среды в течение 12 ч. Концентрировали смесь при пониженном давлении и очищали остаток путем препаративной ТСХ с получением 3-(2 диметиламинометилбицикло[3.2.1]окт-3-ил)фенилового эфира 2,2-диметилпропановой кислоты в виде белого твердого вещества (217 мг, выход: 81,9%). МС (m/z): 344 (М+1). 1H ЯМР (400 МГц, метанол-d4)7,36-7,40 (t, J=13,6, 1H), 7,19-7,21 (d, J=7,2, 1H), 7,03 (s, 1H), 6,926,94 (d, J=8,0, 1H), 2,97-3,03 (t, J=23,6, 1H), 2,49-2,68 (m, 6H), 2,40-2,44 (d, J=13,2, 1H), 2,35 (s, 2H), 2,172,21 (m, 2H), 1,60-1,84 (m, 8H), 1,37 (s, 9H). Следующие соединения получали по существу при помощи способа, приведенного в примере 130. Добавляли Н 2 О (9 мг, 0,5 ммоль) и TMSCl (39 мг, 0,357 ммоль) в раствор 3-(2 диметиламинометилбицикло[3.2.1]окт-3-ил)фенилового эфира 2,2-диметилпропановой кислоты (102 мг,0,297 ммоль) в 2-бутаноне (50 мл). Затем перемешивали реакционную смесь при температуре окружающей среды в течение 4 ч. Выпаривали смесь в вакууме с получением гидрохлорида 3-(2 диметиламинометилбицикло[3.2.1]окт-3-ил)фенилового эфира 2,2-диметилпропановой кислоты в виде белого твердого вещества (112 мг, выход: 100%). 1H ЯМР (400 МГц, метанол-d4)7,38-7,42 (t, J=15,6, 1H), 7,20-7,22 (d, J=7,6, 1H), 7,05 (s, 1H), 6,946,96 (m, 1H), 3,08-3,14 (m, 1H), 2,79 (s, 3 Н), 2,66 (s, 3 Н), 2,53-2,57 (m, 2H), 2,36 (s, 2H), 2,23 (m, 1H), 1,611,85 (m, 8H), 1,39 (s, 9H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 135. На схемах H-J и в примерах получения и/или в примерах 147-164 проиллюстрированы способы получения соединений формулы Id, приведенной ниже. Добавляли йодид триметилсульфоксония (126,3 г, 0,572 моль) в суспензию гидрида натрия (22,9 г,60% дисперсия в масле, 0,572 моль) в сухом ДМСО (550 мл) при температуре окружающей среды в течение 10 мин. Перемешивали смесь в течение 1 ч, а затем добавляли по каплям раствор циклогекс-2-енона(51,2 г, 0,52 моль) в сухом ДМСО (100 мл) в реакционную смесь. Дополнительно перемешивали реакционную смесь при 50 С в течение 2 ч. Выливали реакционную смесь в ледяную воду и экстрагировали водную смесь CH2Cl2 (300 мл 3). Объединенные органические слои промывали солевым раствором, сушили над MgSO4, концентрировали в вакууме. Очищали остаток путем перегонки (55-60 С, 5 мм рт. ст.) с получением бицикло[4.1.0]гептан-2-она в виде бесцветной маслянистой жидкости (38,45 г, 66,6%). МС (m/z): 109 (М-1). Следующее соединение можно получать по существу при помощи способа, приведенного в примере получения 141. Добавляли по каплям бицикло[4.1.0]гептан-2-он (43,3 г, 0,393 моль) в сухом ТГФ (50 мл) в растворLDA (237 мл, 0,472 моль) в ТГФ (500 мл). Перемешивали реакционную смесь в течение 30 мин, а затем добавляли по каплям TMSCl (64,2 г, 0,59 моль) в реакционную смесь. Дополнительно перемешивали полученный раствор в течение 1 ч. Выливали смесь в ледяную воду (92 мл) и экстрагировали водную смесьEtOAc (100 мл 3). Объединенные органические слои промывали солевым раствором, сушили надMgSO4, фильтровали и концентрировали в вакууме с получением (бицикло[4.1.0]гепт-2-ен-2 илокси)триметилсилана (68,0 г, 95,0%) в виде желтоватой маслянистой жидкости.MC (m/z): 181 (М-1). Следующее соединение можно получать по существу при помощи способа, приведенного в примере получения 143. Добавляли (бицикло[4.1.0]гепт-2-ен-2-илокси)триметилсилан (72,9 г, 0,40 моль) в охлажденную суспензию хлорида N,N-диметилметилениминия (48,6 г, 0,52 моль) в CH2Cl2 (400 мл) при 0 С. После перемешивания в течение ночи при температуре окружающей среды разбавляли реакционную смесь 2 н.HCl (200 мл). После удаления органических слоев промывали водный слой EtOAc (50 мл 3), а затем подщелачивали при помощи NaOH до рН 10. Экстрагировали полученную смесь EtOAc (100 мл 4). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4, фильтровали и концентрировали в вакууме. Очищали остаток путем перегонки (80-85 С, 5 мм рт.ст.) с получением 3-диметиламинометилбицикло[4.1.0]гептан-2-она (16,0 г, 24,0%) в виде бесцветной маслянистой жидкости. МС (m/z): 168 (М+1). Следующее соединение можно получать по существу при помощи способа, приведенного в примере получения 145. Добавляли раствор t-BuLi (5,8 мл, 8,68 ммоль) при помощи шприца в раствор 3-бромфенола (752 мг, 4,34 ммоль) в ТГФ (60 мл) при -78 С в атмосфере N2. После перемешивания при -78 С в течение 1 ч добавляли раствор 3-диметиламинометилбицикло[4.1.0]гептан-2-она (300 мг, 2,17 ммоль) в ТГФ (2 мл) в реакционную смесь и дополнительно перемешивали реакционную смесь при -78 С в течение 2 ч. Гасили реакцию насыщенным раствором NH4Cl (30 мл). Экстрагировали полученную водную смесь EtOAc (60 мл 3). Объединенные органические слои промывали солевым раствором (30 мл), сушили над Na2SO4,фильтровали и концентрировали в вакууме. Очищали остаток путем препаративной ВЭЖХ с получением 3-диметиламинометил-2-(3-гидроксифенил)бицикло[4.1.0]гептан-2-ола в виде белого твердого вещества(73 мг, выход: 12,9%). МС (m/z): 262 (М+1). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 147. Добавляли Н 2 О (10 мг, 0,560 ммоль) и TMSCl (33 мг, 0,308 ммоль) в раствор 3-диметиламинометил 2-(3-гидроксифенил)бицикло[4.1.0]гептан-2-ола (73 мг, 0,280 ммоль) в 2-бутаноне (10 мл). Затем перемешивали смесь при комнатной температуре в течение 2 ч. Выпаривали смесь в вакууме с получением гидрохлорида 3-диметиламинометил-2-(3-гидроксифенил)бицикло[4.1.0]гептан-2-ола в виде белого твердого вещества (83 мг, выход: 100%). 1H ЯМР (400 МГц, метанол-d4)7,21-7,25 (t, J=16,0, 1H), 7,17-7,18 (t, J=4,4, 1H), 7,11-7,13 (m, 1H),6,76-6,79 (d, J=10,0, 1H), 3,23-3,25 (m, 1H), 2,68-2,69 (m, 7H), 2,14-2,17 (m, 1H), 2,04-2,09 (m, 1H), 1,761,81 (m, 1H), 1,62-1,64 (m, 1H), 1,47-1,49 (m, 1H), 1,11-1,16 (m, 1H), 0,93-1,05 (m, 1H), 0,73-0,84 (m, 1H),0,50-0,53 (m, 1H). Следующие соединения можно получать по существу при помощи способа, приведенного в примере 153.
МПК / Метки
МПК: C07C 217/54
Метки: анальгезирующими, терапии, обладающие, соединения, составы, применение, свойствами, содержащие
Код ссылки
<a href="https://eas.patents.su/30-24101-soedineniya-obladayushhie-analgeziruyushhimi-svojjstvami-soderzhashhie-ih-sostavy-i-ih-primenenie-v-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения, обладающие анальгезирующими свойствами, содержащие их составы и их применение в терапии</a>