Производные изохинолинона в качестве антагонистов nk3
Номер патента: 21581
Опубликовано: 30.07.2015
Авторы: Симонсен Клаус Бек, Нильсен Серен Меллер, Ханжин Николай, Юль Карстен
Формула / Реферат
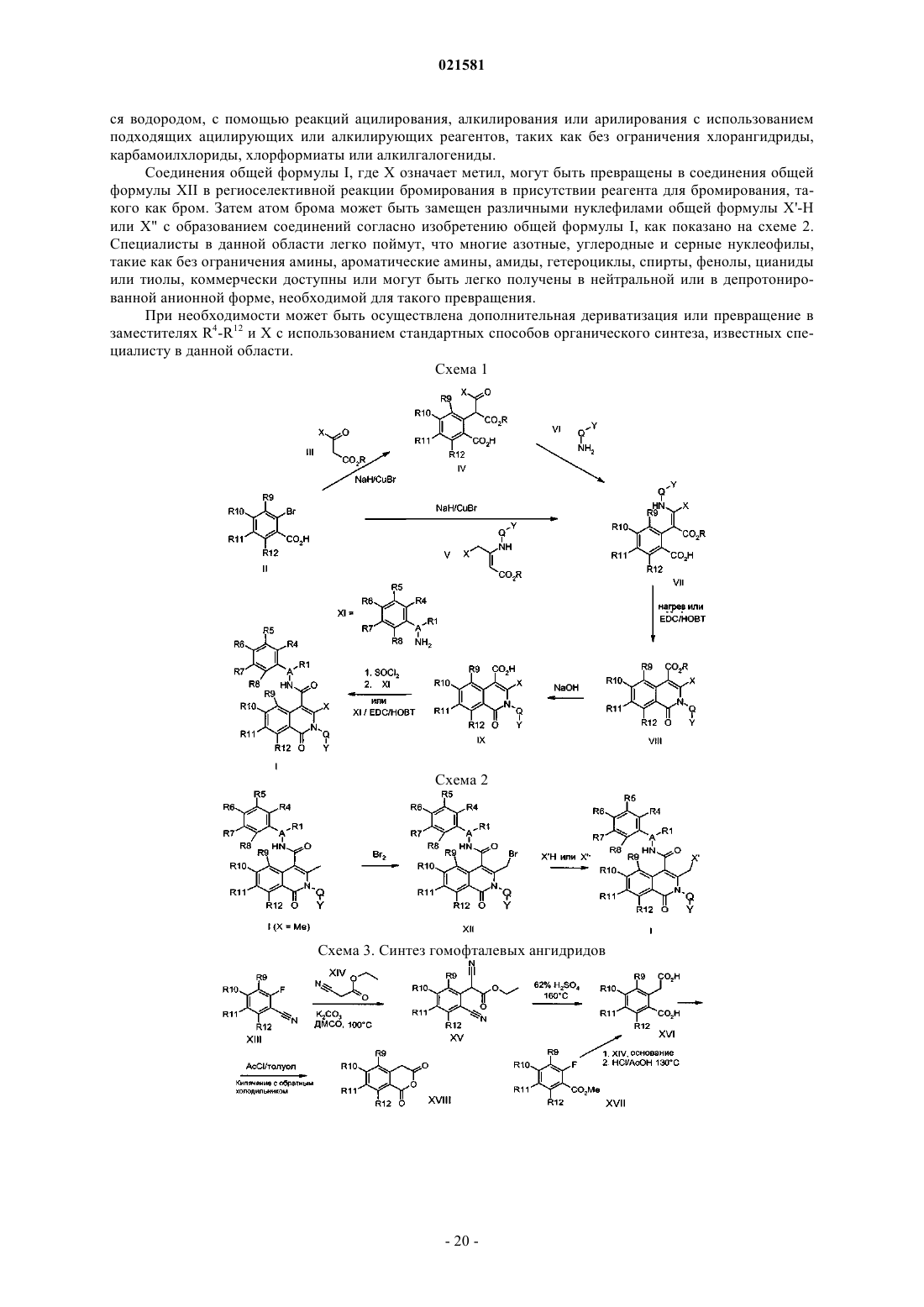
1. Соединение формулы I
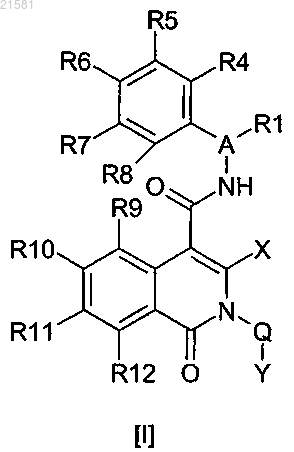
где А означает СН;
каждый R1 означает водород, С1-6-алкил;
X означает водород, C1-6-алкил, необязательно замещенный галогеном или -CRaRb-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, одним из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из C1-6-алкила или (=О);
каждый из Ra и Rb означает водород;
Q означает связь, -СН2-, -NH- или -О-;
Y означает C1-6-алкил, С2-6-алкенил или С2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, С1-6-алкоксигруппы, цианогруппы, -S-С1-6-алкила и моноциклического насыщенного остатка, имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может быть атомом N, а остальные атомами С; или
Y может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из C1-6-алкила, (=O), -С(О)-C1-6-алкила;
каждый из R4-R8 и R9-R12 независимо означает водород, галоген, гидроксигруппу;
при условии, что указанное соединение отличается от (1-фенилэтил)амида 2-метил-1-оксо-1,2-дигидроизохинолин-4-карбоновой кислоты;
или его фармацевтически приемлемые соли.
2. Соединение по п.1, где R1 означает C1-6-алкил.
3. Соединение по п.2, где R1 означает этил.
4. Соединение по любому из пп.1-3, где X означает Н, метил, необязательно замещенный F, или -СН2-Х', где X' означает моноциклический насыщенный остаток, выбранный из пиперазинила и пирролидинила, при этом указанный моноциклический остаток может быть замещен одним или несколькими заместителями W, где W выбран из C1-6-алкила и (=O).
5. Соединение по любому из пп.1-4, где Q означает -СН2- и Y означает С1-4-алкил, С2-4-алкенил или С2-4-алкинил, и в котором Р выбран из галогена, гидроксила, -S-СН3 и цианогруппы.
6. Соединение по любому из пп.1-4, где Q означает -СН2- и Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и в котором моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, при этом Z выбран из C1-6-алкила, (=O), -С(О)-О1-6-алкила.
7. Соединение по любому из пп.1-4, где Q означает -NH- и Y означает C1-6-алкил, в котором Р означает галоген, или в котором Y означает моноциклический остаток, имеющий 4, 5 или 6 атомов в кольце, и такие атомы в кольце выбраны из С.
8. Соединение по любому из пп.1-4, где Q означает -O- и Y означает C1-4-алкил.
9. Соединение по любому из пп.1-4, где Q означает связь и Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом 1 из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и в котором моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из C1-6-алкила, (=O).
10. Соединение по любому из пп.1-9, где каждый из R4-R8 независимо означает водород или галоген.
11. Соединение по п.10, где R7 означает галоген и R4, R5 и R8 означают водород.
12. Соединение по п.10, где все R4-R8 означают водород.
13. Соединение по любому из пп.1-12, где каждый из R9-R12 независимо означает водород или галоген.
14. Соединение по п.13, где R12 означает галоген и R9-R11 означают водород.
15. Соединение по п.13, где все R9-R12 означают водород.
16. Соединение по п.1 формулы I'
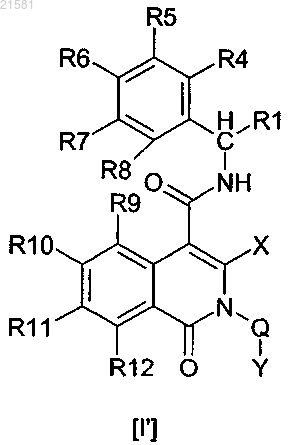
где R1 означает C1-6-алкил;
X означает водород, C1-6-алкил, необязательно замещенный F или -CRaRb-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из C1-6-алкила или (=O);
каждый из Ra и Rb означает водород;
Q означает связь, -СН2-, -NH- или -О-;
Y означает С1-6-алкил, С2-6-алкенил или С2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, С1-6-алкоксигруппы, цианогруппы, -S-C1-6-алкила и моноциклического насыщенного остатка, имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может представлять собой атом N, а остальные являются атомами С; или альтернативно Y может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из С1-6-алкила, (=O), -С(О)-O-C1-6-алкила;
каждый из R4-R8 и R9-R12 независимо означает водород, галоген;
или его фармацевтически приемлемые соли.
17. Соединение по п.16, где R1 означает этил;
X означает C1-6-алкил, необязательно замещенный F или -СН2-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и в котором один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из C1-6-алкила или (=O);
Q означает -СН2- или -NH-;
Y означает С1-6-алкил, С2-6-алкенил или С2-6-алкинил, все из которых необязательно имеют в качестве заместителей до трех атомов галогенов, или альтернативно Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и такой моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, при этом Z выбран из C1-6-алкила;
каждый из R4-R8 и R9-R12 независимо означает водород, галоген.
18. Соединение по п.17, в котором каждый из R4-R8 и R9-R12 независимо означает водород или галоген.
19. Соединение по п.18, где R7 означает галоген, R5, R6 и R8 означают водород.
20. Соединение по п.16, где R1 означает этил;
X означает C1-6-алкил, необязательно замещенный F или -СН2-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и в котором один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, который выбран из пиперазинила и пирролидинила, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из C1-6-алкила или (=O);
Q означает -СН2- или -NH-;
Y означает С1-4-алкил, С2-4-алкенил или С2-4-алкинил, все из которых необязательно имеют в качестве заместителей до трех атомов галогенов;
каждый из R4-R8 и R9-R12 независимо означает водород или галоген.
21. Соединение по п.20, где R7 и R12 каждый независимо означают галоген, и R4-R6, R8 и R9-R11 означают водород.
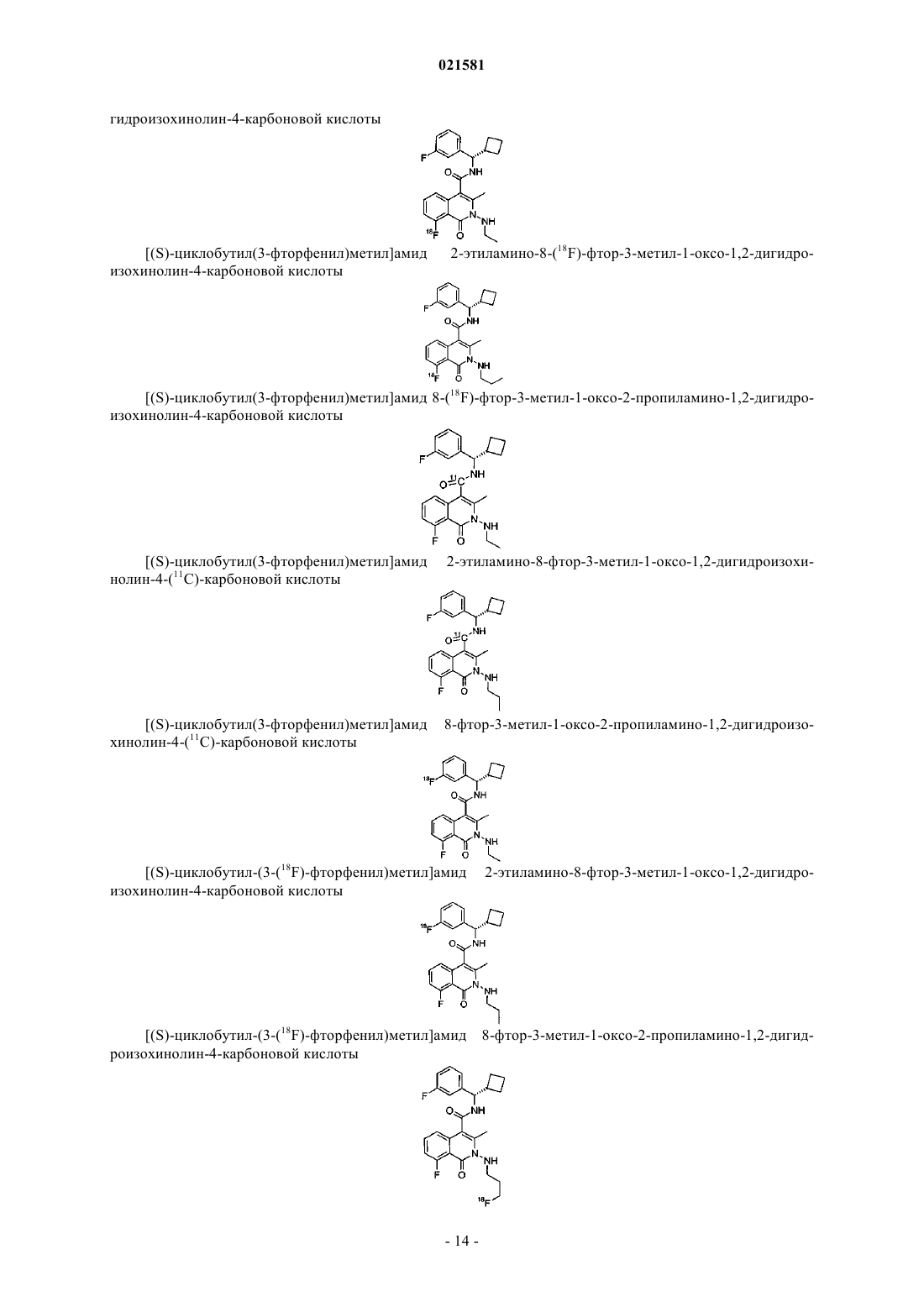
22. Соединение по п.1, выбранное из группы, включающей










или его фармацевтически приемлемые соли.
23. Фармацевтическая композиция, обладающая свойствами антагониста NK3, содержащая соединение по любому из пп.1-22 в сочетании с одним или несколькими фармацевтически приемлемыми носителями или эксципиентами.
24. Применение соединения по любому из пп.1-22 для получения лекарственного средства для лечения заболевания, выбранного из психоза; шизофрении; шизофреноподобного расстройства; шизоаффективного расстройства; бредового расстройства; кратковременного психотического расстройства; индуцированного психотического расстройства; психотического расстройства вследствие общего состояния здоровья; индуцированного веществом или лекарственным средством психотического расстройства (кокаин, спирт, амфетамин и т.д.); шизоидного расстройства личности; шизотипического расстройства личности; психоза или шизофрении, ассоциированной с глубокой депрессией, биполярным расстройством, болезнью Альцгеймера или болезнью Паркинсона; глубокой депрессии; генерализованного тревожного расстройства; биполярного расстройства (поддерживающее лечение, предотвращение рецидивов и стабилизация); мании; гипоманиакального состояния; когнитивного нарушения; ADHD; ожирения; снижения аппетита; болезни Альцгеймера; болезни Паркинсона; боли; судорог; кашля; астмы; гиперчувствительности дыхательных путей; гиперчувствительности микрососудов; бронхоконстрикции; хронического обструктивного легочного заболевания; недержания мочи; воспаления кишечника; синдрома воспаленной кишки; PTDS; деменции и ажитации и делирия в пожилом возрасте.
25. Применение по п.24, в котором указанным заболеванием является шизофрения.
26. Применение по п.25, в котором лечению подвергают позитивные, негативные и/или когнитивные симптомы.
Текст
X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, одним из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из С 1-6-алкила или (=O); каждый из Ra и Rb означает водород; Q означает связь, -СН 2-, -NH- или -O-; Y означает C1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, C1-6-алкоксигруппы, цианогруппы, -S-C1-6-алкила и моноциклического насыщенного остатка, имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может быть атомом N, а остальные атомами С; или Y может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителямиZ, где Z выбран из C1-6-алкила, (=O), -С(О)-C1-6-алкила; каждый из R4-R8 и R9-R12 независимо означает водород, галоген,гидроксигруппу; при условии, что указанное соединение отличается от (1-фенилэтил)амида 2-метил-1-оксо-1,2 дигидроизохинолин-4-карбоновой кислоты; и их фармацевтически приемлемым солям. Изобретение также относится к фармацевтическим композициям, обладающим антагонистической активностью в отношении рецептора NK3,содержащим указанные соединения, и к применению указанных соединений для получения лекарственного средства для лечения психического заболевания. Ханжин Николай, Юль Карстен, Нильсен Серен Меллер, Симонсен Клаус Бек (DK) Область техники, к которой относится изобретение Настоящее изобретение относится к соединениям, применимым для терапии, в частности для лечения психического заболевания, к композициям, содержащим указанные соединения, и к способам лечения заболеваний, включающим введение указанных соединений. Уровень техники Одобренные в настоящее время антипсихотические лекарственные средства обладают общим свойством, а именно снижают передачу сигнала допамином в головном мозге. Указанное влияние достигается либо посредством антагонистического, либо частичного агонистического эффекта на рецептор допамина D2. Антипсихотические средства первого поколения (также называемые типичными) часто ассоциированы с экстрапирамидальными побочными эффектами, и по этой причине применение таких средств сокращено. Антипсихотические средства второго поколения или атипичные антипсихотические средства в добавление к аффинности к рецептору D2 обладают аффинностью к рецептору серотонина 2 А (5-НТ 2 А). Некоторые атипичные антипсихотические средства дополнительно обладают аффинностью к рецепторам 5-НТ 2 с, 5-НТ 6 или 5-НТ 7. Атипичные антипсихотические средства вызывают меньше экстрапирамидальных побочных эффектов, но их применение сдерживают эффекты, связанные с увеличением массы, и QTc-эффекты. Примерами атипичных средств являются клозапин, оланзапин и рисперидон. Совсем недавно рецепторы нейрокинина были предложены в качестве мишеней в случае заболеваний ЦНС (Albert, Expert Opin. Ther. Patents, 14, 1421-1433, 2004). Нейрокинины (или тахикинины) представляют собой семейство нейропептидов, которое включает субстанцию Р (SP), нейрокинин A (NKA) и нейрокинин В (NKB). Биологические эффекты указанных веществ, главным образом, проявляются посредством связывания и активации трех рецепторов нейрокининов NK1, NK2 и NK3. Хотя вероятно имеет место некоторая перекрестная реактивность, SP обладает самой высокой аффинностью и, как полагают, является эндогенным лигандом для NK1. Подобным образом, полагают, что NKA является эндогенным лигандом для NK2, и полагают, что NKB является эндогенным лигандом для NK3.NK3 главным образом экспрессируется в центральных областях, включая области коры головного мозга, такие как лобная кора, теменная кора и кора поясной извилины; ядра миндалевидного тела, такие как базальное, центральное и латеральное ядра; гиппокамп; и структуры среднего мозга, такие как вентральная область покрышки, компактная часть черной субстанции (substantia nigra pars compacta) и дорсальные ядра шва (Spooren et al., Nature Reviews, 4, 967-975, 2005). Рецептор NK3 экспрессируется на допаминергических нейронах, и Spooren с соавторами предположили, что антипсихотические эффекты антагонистов NK3 опосредованы ингибированием допаминового тонуса, в частности, рецептора D2, в сочетании с уменьшением серотонинергического тонуса, в частности, рецептора 5-HT2A. Два структурно различных антагониста NK3, а именно талнетант и осанетант, были подвергнуты клиническому испытанию в отношении антипсихотических и, в частности, противошизофренических эффектов. Осанетант превосходил плацебо в клинических испытаниях, в частности в отношении позитивных симптомов психоза, т.е. бреда, галлюцинаций и паранойи (Am. J. Psychiatry, 161, 2004, 975-984). Подобным образом, в клинических испытаниях было показано, что талнетант улучшает когнитивное поведение у шизофреников (Curr. Opion. Invest. Drug, 6, 717-721, 2005). Однако применение обоих соединений сдерживается плохими фармакокинетическими и фармакодинамическими свойствами, включая плохую растворимость, плохую биодоступность, относительно высокий клиренс и плохое проникновение через гематоэнцефалический барьер (Nature reviews, 4, 967-975, 2005). Такие результаты подтверждают представление о том, что рецептор NK3 является многообещающей мишенью для лечения, например, психического заболевания, однако подчеркивают необходимость в идентификации соединений с соответствующими фармакокинетическими и фармакодинамическими свойствами. В WO 95/32948 описан ряд производных хинолина, включая талнетант, в качестве антагонистов-1 021581 и указано, что такие соединения являются антагонистами NK3; и в публикациях WO 2006/050991 иWO 2006/050992 раскрыты дополнительные производные хинолинкарбоксамидов и указано, что такие производные являются антагонистами NK3. В WO 2005/014575 описаны соединения формулы где R означает N-содержащие гетероциклы, т.е. пиразолил, триазолил и тетразолил. В публикации (см. Ind. J. Chem. Section В, 18 В, 304-306, 1979) описано исследование синтеза соединений со следующей центральной структурой Поставщик химических соединений Ambinter предлагает соединение структуры с химическим названием (1-фенилэтил)амид 2-метил-1-оксо-1,2-дигидроизохинолин-4-карбоновой кислоты. Сущность изобретения Авторы настоящего изобретения неожиданно обнаружили, что некоторые производные изохинолинона являются сильными антагонистами NK3, которые как таковые могут быть использованы, например,для лечения психоза. Соответственно, в одном варианте изобретение относится к соединениям формулыX означает водород, С 1-6-алкил, необязательно замещенный галогеном или -CRaRb-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, одним из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W,где W выбран из C1-6-алкила или (=O); каждый из Ra и Rb означает водород;Y означает С 1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, C1-6-алкоксигруппы, цианогруппы, -S-C1-6-алкила и моноциклического насыщенного остатка,имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может быть атомом N, а остальные атомами С; илиY может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из C1-6-алкила, (=O), -С(О)-С 1-6-алкила; каждый из R4-R8 и R9-R12 независимо означает водород, галоген, гидроксигруппу;-2 021581 при условии, что указанное соединение отличается от (1-фенилэтил)амида 2-метил-1-оксо-1,2-дигидроизохинолин-4-карбоновой кислоты; и их фармацевтически приемлемым солям. В одном варианте изобретение относится к фармацевтической композиции, содержащей соединения формулы I и фармацевтически приемлемые соли в сочетании с одним или несколькими фармацевтически приемлемыми носителями или эксципиентами. В одном варианте изобретение относится к применению соединения формулы I и фармацевтически приемлемых солей для получения лекарственных средств. В одном варианте изобретение относится к соединению формулы I и фармацевтически приемлемым солям для применения в лечении заболеваний. Определения В контексте настоящего описания подразумевается, что алкил означает неразветвленный, разветвленный и/или циклический насыщенный углеводород. В частности, термин C1-6-алкил предназначен для обозначения такого углеводорода, имеющего 1, 2, 3, 4, 5 или 6 атомов углерода. Примерами C1-6 алкила являются метил, этил, пропил, бутил, пентил, гексил, циклопропил, циклобутил, циклопентил,циклогексил, 2-метилпропил, трет-бутил и циклопропилметил. В контексте настоящего описания термин алкенил предназначен для обозначения неароматического, неразветвленного, разветвленного и/или циклического углеводорода, содержащего по меньшей мере одну углерод-углеродную двойную связь. В частности, термин С 2-6-алкенил предназначен для обозначения такого углеводорода, имеющего 2, 3, 4, 5 или 6 атомов углерода. Примерами С 2-6-алкенила являются этенил, 1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил, 3-бутенил и циклогексенил. В контексте настоящего описания термин алкинил предназначен для обозначения неароматического, неразветвленного, разветвленного и/или циклического углеводорода, содержащего по меньшей мере одну углерод-углеродную тройную связь и необязательно также одну или несколько углеродуглеродных двойных связей. В частности, термин С 2-6-алкинил предназначен для обозначения такого углеводорода, имеющего 2, 3, 4, 5 или 6 атомов углерода. Примерами С 2-6-алкинила являются этинил, 1 пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил и 5-бут-1-ен-3-инил. В контексте настоящего описания термин галоген предназначен для обозначения представителей 7-й группы Периодической системы, например, фтора, хлора, брома и йода. В контексте настоящего описания термин алкокси- предназначен для обозначения остатка формулы -OR', где R' означает алкил, который определен выше. В частности, термин C1-6-алкокси- предназначен для обозначения такого остатка, где алкильная часть имеет 1, 2, 3, 4, 5 или 6 атомов углерода. В контексте настоящего описания галогеналкил предназначен для обозначения алкила, который определен выше, замещенного одним или несколькими галогенами. В частности, галоген-С 1-6-алкил предназначен для обозначения остатка, где алкильная часть имеет 1, 2, 3, 4, 5 или 6 атомов углерода. Одним из примеров галогеналкила является трифторметил. В контексте настоящего описания фармацевтически приемлемые соли включают фармацевтически приемлемые кислотно-аддитивные соли, фармацевтически приемлемые соли металлов, соли аммония и алкилированного аммония. Кислотно-аддитивные соли включают соли неорганических кислот, а также органических кислот. Примерами подходящих неорганических солей являются хлористо-водородная, бромистоводородная, йодисто-водородная, фосфорная, серная, сульфаминовая, азотная кислоты и тому подобные. Примерами подходящих органических кислот являются муравьиная, уксусная, трихлоруксусная,трифторуксусная, пропионовая, бензойная, коричная, лимонная, фумаровая, гликолевая, итаконовая, молочная, метансульфоновая, малеиновая, яблочная, малоновая, миндальная, щавелевая, пикриновая, пировиноградная, салициловая, янтарная, метансульфоновая, этансульфоновая, винная, аскорбиновая, памовая, бисметиленсалициловая, этандисульфоновая, глюконовая, цитраконовая, аспарагиновая, стеариновая, пальмитиновая, EDTA, гликолевая, п-аминобензойная, глутаминовая, бензолсульфоновая, птолуолсульфоновая кислоты, теофиллинуксусные кислоты, а также 8-галогентеофиллины, например 8 бромтеофиллин и тому подобные. Другими примерами фармацевтически приемлемых неорганических или органических кислотно-аддитивных солей являются фармацевтически приемлемые соли (см. перечисленные в публикации J. Pharm. Sci. 1977, 66, 2, которая включена в настоящее описание в виде ссылки). Примеры солей металлов включают соли лития, натрия, калия, магния и тому подобные. Примеры солей аммония и алкилированного аммония включают соли аммония, метил-, диметил-,триметил-, этил-, гидроксиэтил-, диэтил-, н-бутил-, втор-бутил-, трет-бутил-, тетраметиламмония и тому подобные. В контексте настоящего описания термин атом в кольце предназначен для обозначения атомов,составляющих кольцо, и атомы в кольце выбраны из С, N, О и S. В качестве примера бензол и толуол имеют по 6 атомов углерода в качестве атомов в кольце, тогда как пиридин имеет 5 атомов углерода и 1 атом азота в качестве атомов в кольце.-3 021581 В контексте настоящего описания термин моноциклический остаток предназначен для обозначения кольца, образованного структурой, содержащей только одно кольцо. В контексте настоящего описания термин терапевтически эффективное количество соединения означает количество, достаточное для излечения, облегчения или частичной задержки клинических проявлений данного заболевания и его осложнений при терапевтическом вмешательстве, включающем введение указанного соединения. Количество, достаточное для осуществления указанного эффекта, определяют как терапевтически эффективное количество. Эффективные количества для каждой цели будут зависеть от тяжести заболевания или нарушения, а также массы и общего состояния субъекта. Будет понятно, что определение соответствующей дозы можно осуществить с использованием обычного экспериментирования, путем конструирования матрицы значений и тестирования разных точек на матрице,что относится к среднему уровню компетентности опытного врача. В контексте настоящего описания термин лечение и процесс лечения означает терапию и уход за пациентом в целях борьбы с состоянием, таким как заболевание или расстройство. Подразумевается,что термин охватывает полный спектр лечения данного состояния, от которого страдает пациент, например введение активного соединения, чтобы облегчить симптомы или осложнения, замедлить прогрессирование заболевания, расстройства или состояния, ослабить или облегчить симптомы и осложнения и/или излечить или устранить заболевание, расстройство или состояние, а также для профилактики состояния, при этом профилактику понимают как лечение и уход за пациентом в целях борьбы с заболеванием, состоянием или расстройством, которые включают введение активных соединений для предотвращения появления симптомов или осложнений. Однако профилактическое (превентивное) и терапевтическое (радикальное) лечение представляют собой два аспекта изобретения. Пациентом, подвергаемым лечению, предпочтительно является млекопитающее, в частности человек. В контексте настоящего описания термин занятость в связывании означает фракцию сайтов связывания мишени, занятых конкретным соединением. В контексте настоящего описания термин лигандPET означает высоко аффинный лиганд для соответствующей мишени с хорошим распределением в соответствующем компартменте, в контексте настоящего описания в ЦНС. Указанный лиганд радиоактивно метят короткоживущим радиоактивным индикаторным изотопом, предпочтительно 11 С или 18F,который подвергается позитронному распаду. В контексте настоящего описания термин фракция, не содержащая плазмы означает фракцию соединения в плазме крови, которая не связана с белками плазмы. В контексте настоящего описания термин гематоэнцефалический барьер (или ВВВ) означает физиологический барьер, образованный слоем эндотелиальных клеток. Указанный барьер предотвращает проникновение некоторых веществ, таких как некоторые лекарственные средства, в ткань головного мозга. В контексте настоящего описания, Р-gp (Р-гликопротеид) означает переносчик оттока, локализованный в ГЭБ. Другие названия P-gp: MDR1 и АВСВ 1. Подробное описание изобретения В одном варианте изобретение относится к соединениям формулы IX означает водород, С 1-6-алкил, необязательно замещенный галогеном или -CRaRb-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, одним из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W,где W выбран из С 1-6-алкила или (=O); каждый из Ra и Rb означает водород;Y означает С 1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, C1-6-алкоксигруппы, цианогруппы, -S-C1-6-алкила и моноциклического насыщенного остатка,имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может быть атомом N, а остальные атомами С; илиY может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из C1-6-алкила, (=O), -С(О)-C1-6-алкила; каждый из R4-R8 и R9-R12 независимо означает водород, галоген, гидроксигруппу; при условии, что указанное соединение отличается от (1-фенилэтил)амида 2-метил-1-оксо-1,2 дигидроизохинолин-4-карбоновой кислоты; и их фармацевтически приемлемым солям (т.е. соединениям согласно настоящему изобретению). Примерами таких моноциклических насыщенных остатков, имеющих 5-6 атомов в кольце, один из которых является атомом N, и где один или два дополнительных атома в кольце могут представлять собой гетероатом, выбранный из N, О, S, являются пиперазинил, пирролидинил, имидазолидинил, пирразолидинил, пиперидил, морфолинил и тиоморфолинил. Примеры такого моноциклического насыщенного остатка, имеющего 5-6 атомов в кольце, один из которых может быть атомом N, а остальные представляют собой атомы С, включают циклопропил, циклогексил, пирролидинил и пиперидил. Примеры такого моноциклического насыщенного остатка, имеющего 4-6 атомов в кольце, где 1 из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С,включают циклопропил, циклогексил, пирролидинил, пиперидил, тетрагидрофуранил и тетрагидропиранил. В одном варианте R1 означает С 1-6-алкил, в частности этил, циклопропил или циклобутил. В одном варианте X означает Н, метил, необязательно замещенный F или -СН 2-Х', где X' означает моноциклический насыщенный остаток, выбранный из пиперазинила и пирролидинила, при этом указанный моноциклический остаток может быть замещен одним или несколькими заместителями W, где W выбран из C1-6-алкила и (=O). В одном варианте Q означает -СН 2-, и Y означает C1-4-алкил, С 2-4-алкенил или С 2-4-алкинил, где Р выбран из галогена, гидроксила, -S-СН 3 и цианогруппы. Конкретные примеры C1-4-алкила включают метил, этилпропил, циклопропил, циклобутил, 2-метилпропил и трет-бутил. Конкретные примеры С 2-4 алкенила включают этенил, 1-пропенил и 2-пропенил. Конкретные примеры С 2-4-алкинила включают этинил, 1-пропенил и 2-пропенил. В одном варианте Q означает -СН 2-, и Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, где 1 из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и такой моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из С 1-6-алкила, (=O), С(О)Н, -С(О)-O-C1-6-алкила,галогена, C1-6-алкоксигруппы, С 1-6-гидроксиалкила и гидроксигруппы. В одном варианте Q означает -NH-, и Y означает С 1-6-алкил, при этом Р означает галоген, или альтернативно Y означает моноциклический остаток, имеющий 4, 5 или 6 атомов в кольце, и такие атомы в кольце выбраны из С. Конкретными примерами Y являются метил, этил, пропил, 1-метилэтил, 2 метилпропил и бутил. В одном варианте Q означает -O-, и Y означает С 1-4-алкил. Конкретные примеры C1-4-алкила включают метил, этил, пропил, циклопропил, циклобутил, 2-метилпропил и трет-бутил. В одном варианте Q означает связь, и Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные представляют собой атомы С, и такой моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из C1-6-алкила, (=О), галогена и гидроксигруппы. В одном варианте каждый из R4-R8 независимо означает водород или галоген; в частности, R7 означает галоген, и R4, R5 и R8 означает водород. В одном варианте все радикалы R4-R8 представляют собой водород. В одном варианте каждый из R9-R12 независимо означает водород или галоген; в частности R12 означает галоген и R9-R11 означают водород. В одном варианте все радикалы R9-R12 представляют собой водород. В одном варианте соединения согласно изобретению дополнительно определяют формулой I', приведенной нижеX означает водород, C1-6-алкил, необязательно замещенный F или -CRaRb-X', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и где один дополнительный атом в кольце может представлять собой гетероатом, выбранный из N, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из С 1-6-алкила или (=O); каждый из Ra и Rb означает водород;Y означает С 1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, при этом указанный алкил, алкенил или алкинил может быть замещен одним или несколькими заместителями Р, где Р выбран из галогена, гидроксигруппы, C1-6-алкоксигруппы, цианогруппы, -S-C1-6-алкила и моноциклического насыщенного остатка,имеющего 5-6 атомов в кольце, при этом один из атомов в кольце может представлять собой атом N, а остальные являются атомами С; или альтернативно Y может означать моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом один из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и при этом моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из С 1-6-алкила, (=O), -С(О)-O-C1-6 алкила; каждый из R4-R8 и R9-R12 независимо означает водород, галоген; и их фармацевтически приемлемые соли. В одном варианте, имеющем отношение к формуле I', R1 означает этил, циклопропил или циклобутил; X означает C1-6-алкил, необязательно замещенный F, или -СН 2-Х', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и где один или два дополнительных атома в кольце могут представлять собой гетероатомы, выбранные из N, О и S, который выбран из пиперазинила и пирролидинила, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, где W выбран из C1-6-алкила или (=O); Q означает -СН 2 или -NH-; Y означает C1-6-алкил, С 2-6-алкенил или С 2-6-алкинил, которые все необязательно могут быть иметь в качестве заместителей до трех атомов галогенов, или альтернативно Y означает моноциклический насыщенный остаток, имеющий 4-6 атомов в кольце, при этом 1 из указанных атомов в кольце может быть выбран из N и О, а остальные являются атомами С, и такой моноциклический насыщенный остаток может быть замещен одним или несколькими заместителями Z, где Z выбран из С 1-6-алкила; и каждый из R4-R8 и R9-R12 независимо означает водород, галоген, C1-6-алкоксигруппу или C1-6-галогеналкил, в частности каждый из R4-R8 и R9-R12 независимо означает водород или галоген. В следующем варианте в рамках настоящего варианта R7 означает галоген, R5, R6 и R8 означают водород. В одном варианте, имеющем отношение к формуле I', R1 означает этил, циклопропил или циклобутил; X означает C1-6-алкил, необязательно замещенный F, или -СН 2-Х', где X' означает моноциклический насыщенный остаток, имеющий 5-6 атомов в кольце, один из которых является атомом N, и где один или два дополнительных атома в кольце могут представлять собой гетероатомы, выбранные из N, О и S, который выбран из пиперазинила и пирролидинила, и такое моноциклическое кольцо может быть замещено одним или несколькими заместителями W, при этом W выбран из C1-6-алкила или (=O); Q означает-СН 2- или -NH-; Y означает C1-4-алкил, С 2-4-алкенил или С 2-4-алкинил, которые все необязательно могут иметь в качестве заместителей до трех атомов галогенов; каждый из R4-R8 и R9-R12 независимо означает водород или галоген, в частности R7 и R12 каждый независимо означают галоген, a R4-R6, R8 и R9-R11 означает водород. Альтернативно R7 означает галоген,и R4-R8 и R9-R11 означают водород. Конкретные примеры Y в виде C1-4-алкила включают метил, этил,пропил, циклопропил, циклобутил, 2-метилпропил и трет-бутил; конкретные примеры Y в виде С 2-4 алкенила включают этенил, 1-пропенил и 2-пропенил; конкретные примеры Y в виде С 2-4-алкинила включают этинил, 1-пропенил и 2-пропенил. В одном варианте, имеющем отношение к формуле I', R1 означает этил, циклопропил или циклобутил; X означает C1-6-алкил, необязательно замещенный F; Q означает -NH-; Y означает C1-4-алкил, который необязательно может иметь в качестве заместителей до трех атомов галогенов; каждый из R4-R8 иR9-R12 независимо означает водород или галоген, в частности R7 означает галоген, и R4-R6, R8 и R9-R11 означают водород. Конкретные примеры Y в виде C1-4-алкила включают метил, этил, пропил, циклопропил, циклобутил, 2-метилпропил и трет-бутил. В одном варианте изобретение относится к соединениям, выбранным из следующего списка: Кроме того, соединения согласно изобретению могут существовать в несольватированной форме, а также в сольватированной форме, при этом молекулы растворителя выбраны из фармацевтически приемлемых растворителей, таких как вода, этанол и тому подобные. В общем, такие сольватированные формы считаются эквивалентными несольватированным формам в целях настоящего изобретения. Соединения согласно настоящему изобретению могут иметь один или несколько асимметричных центров, и подразумевается, что любые оптические изомеры (т.е. энантиомеры или диастереомеры) в форме отдельных, очищенных или частично очищенных оптических изомеров и любых их смесей, включая рацемические смеси, т.е. смесь стереоизомеров, входят в объем изобретения. В частности, когда А означает СН или CR1, А может быть асимметричным центром, приводящим к двум оптическим изомерам, R-формы и S-формы. В одном варианте соединения согласно настоящему изобретению имеют Sформу. В конкретном варианте соединения согласно настоящему изобретению имеют следующую абсолютную конфигурацию при А, при этом А означает СН В данном контексте подразумевают, что если конкретно указана энантиомерная форма, то соединение находится в энантиомерном избытке, например, по существу, в чистой моноэнантиомерной форме. Соответственно, один вариант осуществления изобретения относится к соединению согласно изобретению, имеющему избыток энантиомера, составляющий по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 96%, предпочтительно по меньшей мере 98%. Рацемические формы могут быть разделены на оптические антиподы известными способами, например, с помощью разделения диастереомерных солей соединения, образованных с оптически активной кислотой, и высвобождения оптически активного аминного соединения обработкой основанием. Другой способ разделения рацематов на оптические антиподы основан на хроматографии оптически активной матрицы. Соединения согласно настоящему изобретению также могут быть разделены путем образования диастереомерных производных. Можно использовать дополнительные способы разделения оптических изомеров, известные специалистам в данной области. Таким способы включают способы, описанные в публикации J. Jaques, A. Collet and S. Wilen (Enantiomers, Racemates, and Resolutions, John Wileyand Sons, New York (1981. Оптически активные соединения также могут быть получены из оптически активных исходных веществ. Кроме того, когда в молекуле присутствует двойная связь или полностью или частично насыщенная циклическая система, могут быть образованы геометрические изомеры. Подразумевается, что любые геометрические изомеры в виде отдельных, очищенных или частично очищенных геометрических изомеров или в виде их смесей входят в объем изобретения. Подобным образом, молекулы, имеющие связь с ограниченным вращением, могут образовывать геометрические изомеры. Также подразумевается, что такие геометрические изомеры входят в объем настоящего изобретения. Кроме того, некоторые из соединений согласно настоящему изобретению могут существовать в разных таутомерных формах и подразумевается, что любые таутомерные формы, которые соединения способны образовывать, входят в объем настоящего изобретения. Антагонисты рецептора NK3 вовлечены в различные заболевания кроме психоза и шизофрении, об- 11021581 суждаемых выше. Langlois с соавторами (J. Pharm. Exp. Ther., 299, 712-717, 2001) пришли к выводу, что антагонисты NK3 могут быть применимы в общем при заболеваниях ЦНС, и в частности при состояниях тревожности и депрессии. Yip с соавторами (Br. J. Phar., 122, 715-722, 1997) дополнительно показали участие антагонистов NK3 в различных функциях головного мозга, таких как обработка информации в коре головного мозга, обучение и память, нейроэндокринная и поведенческая регуляция. Дополнительные исследования показали, что рецепторы NKB и NK3 вовлечены в состояние боли и что антагонистыNK3 оказывают действие при воспалении кишечника, и пришли к выводу, что такие антагонисты можно применять при лечении синдрома раздраженной кишки (IBS). Кроме того, антагонисты NK3, как было показано в моделях in vivo, применимы для лечения заболеваний, связанных с дыхательными путями,таких как астма, гиперчувствительность дыхательных путей, кашель и бронхиальная рестрикция (Daoui,Am. J. Respir. Crit. Care Med., 158, 42-48, 1998). Maubach с соавторами (Neurosci., 83, 1047-1062, 1998) показали, что агонист NKB и NK3 сенктид увеличивает частоту и продолжительность эпилептиформных разрядов, и, следовательно, предположительно такие антагонисты NK3 обладают способностью к противосудорожному действию. Наконец, Kernel с соавторами (J. Neurosci., 22, 1929-1936, 2002) предлагают применение антагонистов NK3 для лечения болезни Паркинсона. Соответственно, клинические, доклинические исследования in vivo и in vitro свидетельствуют, что антагонисты рецептора NK3 важны для лечения или профилактики различных расстройств, включая психоз, шизофрению, депрессию, тревожность, когнитивное нарушение, ожирение, болезнь Альцгеймера, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей, гиперчувствительность микрососудов, бронхоконстрикцию, воспаление кишечника, синдром воспаленной кишки, PTSD, деменцию и ажитацию и делирий в пожилом возрасте. Шизофрению делят на подгруппы. Параноидный тип характеризуется бредом и галлюцинациями и отсутствием расстройства мышления, дезорганизованного поведения и аффективной тупости. Дезорганизованный тип, который также называют гебефренной шизофренией согласно ICD, при котором вместе присутствуют расстройство мышления и эффект уплощения эмоций. Кататонический тип, при котором явно выражены психомоторные расстройства, и симптомы могут включать кататонический ступор и восковую гибкость. Недифференцированный тип, при котором имеют место психотические симптомы,но не удовлетворяются критерии параноидного, дезорганизованного или кататонического типов. Симптомы шизофрении обычно проявляются сами по себе в трех широких категориях, т.е. позитивные, негативные и когнитивные симптомы. Позитивными симптомами являются симптомы, которые представляют собой избыток нормальных переживаний, например, галлюцинации и бред. Негативными симптомами являются симптомы, при которых пациент страдает от отсутствия нормальных переживаний, например, ангедония и недостаток социального взаимодействия. Когнитивные симптомы относятся к когнитивному нарушению у шизофреников, такому как отсутствие устойчивого внимания и недостаточность функции принятия решений. Современные антипсихотические средства довольно успешны при лечении позитивных симптомов, но дают менее хорошие результаты в случае негативных и когнитивных симптомов. Напротив, клинически было показано, что антагонисты NK3 улучшают как позитивные, так и негативные симптомы у шизофреников (Am. J. Psychiatry, 161, 975-984, 204), и согласно приведенному выше обсуждению также ожидается, что они оказывают влияние на когнитивные симптомы. Когнитивное нарушение включает снижение когнитивных функций или когнитивных доменов, например, рабочей памяти, внимания и вигильности, вербального научения и памяти, визуального научения и памяти, логического мышления и решения проблем, например, организующей функции, скорости обработки информации и/или социальных когнитивных функций. В частности, когнитивное нарушение может означать дефицит внимания, дезорганизованное мышление, замедленное мышление, затрудненное понимание, плохое концентрирование внимания, нарушение процесса решения проблем, плохую память,затруднения в выражении мыслей и/или затруднения в интегрировании мыслей, чувств и поведения или затруднения в торможении неуместных мыслей. Способы визуализации, такие как позитронно-эмиссионная томография (ПЭТ), стали важными методиками, применяемыми при клинической разработке лекарственных средств. Соединения с высокой аффинностью к важной мишени, меченые короткоживущими радионуклидами, вводят, например, внутривенно животным, таким как человек, для измерений с помощью PET. Обычная методика заключается в исследовании ингибирования сигнала меченого соединения (РЕТ-лиганда) немеченым тестируемым соединением. При этом возможно определение корреляции между концентрацией тестируемого соединения в плазме и занятостью в рассматриваемой мишени. Такая информации особенно важная для определения дозы при клинической разработке лекарственных средств. Эффективное количество РЕТлиганда представляетсобой количество, достаточное для получения специфичного сигнала для рассматриваемой мишени. Специфичный сигнал представляет собой разницу между сигналом, получаемым в случае связанного с рецептором РЕТ-лиганда отдельно, и сигналом, получаемым в случае связанного с рецептором РЕТ-лиганда в присутствии тестируемого соединения, связывающегося с рассматриваемой- 12021581 мишенью. Предпочтительно соединение, используемое при лечении заболевания ЦНС, способно проникать в головной мозг в достаточном количестве с подходящей скоростью, т.е. соединение должно обладать свойствами, позволяющими ему проникать через гематоэнцефалический барьер. Способность соединения проникать через гематоэнцефалический барьер отчасти основана на физико-химических свойствах, которые влияют на пассивный транспорт через слой клеток. Другим фактором,влияющим на проницаемость через ВВВ, является отток, например, Р-gp-переносчиком, локализованным в клеточном слое, который предотвращает проникновение некоторых соединений в головной мозг. Кроме того, чтобы минимизировать периферические побочные эффекты, требуется высокое соотношение между стационарной концентрацией в головном мозге и плазме, чтобы добиться высокой активности ЦНС при сохранении минимальных количеств соединения в плазме. Для достижения указанной цели обязательно, чтобы некоторая доля соединения не была связана с белками плазмы, т.е. полезной является большая свободная от плазмы доля. Соединения согласно настоящему изобретению, в частности 2-алкиламиноизохинолины (т.е. соединения согласно настоящему изобретению, где Q означает NH, например, где Q означает NH; Y означает необязательно замещенный C1-6-алкил; Х означает С 1-6-алкил; R4-R12 означает Н или галоген; и А означает СН), как было показано, обладают превосходной проницаемостью через ВВВ. Это можно объяснить тем фактом, что в общем такие соединения обладают преимуществом благодаря высокой пассивной проницаемости, а также отсутствию или низкой аффинности по отношению к P-gp-переносчику. Кроме того,высокая свободная от плазмы доля является общим признаком таких соединений, как показано в примерах. В одном варианте изобретение относится к соединениям, применимым в качестве РЕТ-лигандов,т.е. соединениям, определяемым формулой I', где каждый С может представлять собой изотоп 11 С и каждый F может представлять собой изотоп 18F, при этом указанное соединение содержит по меньшей мере один из указанных изотопов; и к их фармацевтически приемлемым солям. В одном варианте настоящее изобретение относится к радиоактивно меченым соединениям формулы I', в частности выбранным из приведенного ниже списка[(S)-циклопропил(3-(18F)-фторфенил)метил]амид 8-фтор-3-метил-1-оксо-2-пропиламино-1,2-дигидроизохинолин-4-карбоновой кислоты. В одном варианте настоящее изобретение относится к способу лечения заболевания, выбранного из психоза; шизофрении; шизофреноподобного расстройства; шизоаффективного расстройства; бредового расстройства; кратковременного психотического расстройства; индуцированного психотического расстройства; психотического расстройства вследствие общего состояния здоровья; индуцированного веществом или лекарственным средством психотического расстройства (кокаин, спирт, амфетамин и т.д.); шизоидного расстройства личности; шизотипического расстройства личности; психоза или шизофрении,ассоциированной с глубокой депрессией, биполярным расстройством, болезнью Альцгеймера или болезнью Паркинсона; глубокой депрессии; генерализованного тревожного расстройства; биполярного расстройства (поддерживающее лечение, предотвращение рецидивов и стабилизация); мании; гипоманиакального состояния; когнитивного нарушения; ADHD; ожирения; снижения аппетита; болезни Альцгеймера; болезни Паркинсона; боли; судорог; кашля; астмы; гиперчувствительности дыхательных путей; гиперчувствительности микрососудов; бронхоконстрикции; хронического обструктивного легочного заболевания; недержания мочи; воспаления кишечника; синдрома воспаленной кишки; PTDS; деменции и ажитации и делирия в пожилом возрасте, при этом способ включает введение терапевтически эффективного количества соединения согласно настоящему изобретению пациенту, нуждающемуся в таком лечении. В одном варианте настоящее изобретение относится к способу лечения шизофрении, при этом способ включает введение терапевтически эффективного количества соединения согласно настоящему изобретению пациенту, нуждающемуся в таком лечении. В частности, указанное лечение включает лечение позитивных, негативных и/или когнитивных симптомов шизофрении. В одном варианте настоящее изобретение относится к способу лечения когнитивного нарушения,при этом способ включает введение терапевтически эффективного количества соединения согласно настоящему изобретению пациенту, нуждающемуся в таком лечении. В частности, указанное когнитивное нарушение проявляется в виде снижения рабочей памяти, внимания и вигильности, вербального обучения и памяти, визуального обучения и памяти, логического мышления и решения проблем, например,организующей функции, скорости обработки информации и/или социальных когнитивных функций. Антипсихотический эффект типичных и атипичных антипсихотических средств, в частности антагонистов D2, проявляется посредством ингибирования постсинаптических рецепторов D2. Однако пресинаптические ауторецепторы D2 также испытывают воздействие при введении таких соединений, приводя к повышению доли работающих допаминовых нейронов, что фактически противодействует антипсихотическим эффектам. Повышенная доля работающих нейронов сохраняется вплоть до блокирования эффекта пресинаптических ауторецепторов (деполяризационный блок), обычно примерно через 3 недели хронического лечения типичными или атипичными антипсихотическими средствами. Такая модель объясняет задержку вплоть до 3 недель клинического эффекта, обычно наблюдаемую вначале лечения антагонистом D2. Антагонисты NK3, по-видимому, ингибируют повышение активности допаминовых нейронов, опосредованное пресинаптическими ауторецепторами D2, вызванное антагонистами D2, поэтому ожидается, что комбинированное введение антагонистов NK3 (например, соединений согласно настоящему изобретению) и антагонистов D2 приведет к более быстрому проявлению клинического эффекта. Кроме того, известно, что антагонисты D2 увеличивают уровни пролактина, что может приводить к серьезным побочным эффектам, таким как остеопороз. Известно, что агонисты NK3 приводят к увеличению уровня пролактина, из чего можно заключить, что антагонист NK3 будет снижать повышенный уровень пролактина, т.е. приводить к нормализации уровня пролактина. Таким образом, комбинированное- 15021581 применение антагонистов NK3 (например, соединений согласно настоящему изобретению) и антагонистов D2 может решить некоторые проблемы безопасности, ассоциированные с введением антагонистовD2. Подобным образом, антагонисты NK3 (например, соединения согласно настоящему изобретению) можно вводить вместе с антагонистами/обратными агонистами/негативными модуляторами/частичными агонистами одной или нескольких мишеней: рецептора допамина D2, рецептора допамина D3, рецептора допамина D4, фосфодиэстеразы PDE10, рецептора серотонина 5-НТ 1 А, рецептора серотонина 5-НТ 2 А,рецептора серотонина 5-НТ 6, адренергического рецептора альфа 2, каннабиноидного рецептора типа 1,рецептора гистамина Н 3, циклооксигеназ, натриевых каналов или переносчик глицина GlyT1; или с агонистами/позитивными модуляторами/частичными агонистами одной или нескольких мишеней; рецептора серотонина 5-НТ 2 С, KCNQ-каналов, рецептора NMDA, рецептора АМРА, никотинового рецептора альфа-7, мускаринового рецептора M1, мускаринового рецептора М 4, метаботропного рецептора глутамата mGluR2, метаботропного рецептора глутамата mGluR5, рецептора допамина D1 или рецептора допамина D5. Такое комбинированное введение соединений согласно настоящему изобретению и других антипсихотических соединений может быть последовательным или одновременным. Примерами антагонистов или частичных агонистов D2 являются галоперидол, хлорпромазин, сульпирид, рисперидон, зипрасидон, оланзапин, кветиапин, клозапин и арипипразол. В одном варианте соединение согласно настоящему изобретению вводят в количестве примерно от 0,001 мг/кг массы тела до примерно 100 мг/кг массы тела в сутки. В частности, ежедневные дозы могут быть в диапазоне от 0,01 мг/кг массы тела до примерно 50 мг/кг массы тела в сутки. Точные дозы будут зависеть от частоты и способа введения, пола, возраста, массы и общего состояния субъекта, подвергаемого лечению, природы и тяжести состояния, подвергаемого лечению, любых сопутствующих заболеваний, подвергаемых лечению, требуемого эффекта лечения и других факторов, известных специалистам в данной области. Типичная пероральная доза для взрослых будет в диапазоне 1-1000 мг/сутки соединения согласно настоящему изобретению, например 1-500 мг/сутки, например 1-100 мг/сутки или 1-50 мг/сутки. В одном варианте настоящее изобретение относится к применению соединений согласно настоящему изобретению в производстве лекарственного средства для лечения заболевания, выбранного из психоза/шизофрении; шизофреноподобного расстройства; шизоаффективного расстройства; бредового расстройства; кратковременного психотического расстройства; индуцированного психотического расстройства; психотического расстройства вследствие общего состояния здоровья; индуцированного веществом или лекарственным средством психотического расстройства (кокаин, спирт, амфетамин и т.д.); шизоидного расстройства личности; шизотипического расстройства личности; психоза или шизофрении,ассоциированной с глубокой депрессией, биполярным расстройством, болезнью Альцгеймера или болезнью Паркинсона; глубокой депрессии; генерализованного тревожного расстройства; биполярного расстройства (поддерживающее лечение, предотвращение рецидивов и стабилизация); мании; гипоманиакального состояния; когнитивного нарушения; ADHD; ожирения; снижения аппетита; болезни Алыдгеймера; болезни Паркинсона; боли; судорог; кашля; астмы; гиперчувствительности дыхательных путей; гиперчувствительности микрососудов; бронхоконстрикции; хронического обструктивного легочного заболевания; недержания мочи; воспаления кишечника; синдрома воспаленной кишки; PTDS; деменции и ажитации и делирия в пожилом возрасте. В одном варианте настоящее изобретение относится к применению соединения согласно настоящему изобретению в производстве лекарственного средства для лечения шизофрении. В частности, указанное лечение включает лечение позитивных, негативных и/или когнитивных симптомов шизофрении. В одном варианте настоящее изобретение относится к применению соединения согласно настоящему изобретению в производстве лекарственного средства для лечения когнитивного нарушения. В частности, указанное когнитивное нарушение проявляется в виде снижения рабочей памяти, внимания и вигильности, вербального обучения и памяти, визуального обучения и памяти, логического мышления и решения проблем, например, организующей функции, скорости обработки информации и/или социальных когнитивных функций. В одном варианте настоящее изобретение относится к соединению согласно настоящему изобретению для применения при лечении заболевания, выбранного из психоза; шизофрении; шизофреноподобного расстройства; шизоаффективного расстройства; бредового расстройства; кратковременного психотического расстройства; индуцированного психотического расстройства; психотического расстройства вследствие общего состояния здоровья; индуцированного веществом или лекарственным средством психотического расстройства (кокаин, спирт, амфетамин и т.д.); шизоидного расстройства личности; шизотипического расстройства личности; психоза или шизофрении, ассоциированной с глубокой депрессией,биполярным расстройством, болезнью Альцгеймера или болезнью Паркинсона; глубокой депрессии; генерализованного тревожного расстройства; биполярного расстройства (поддерживающее лечение, предотвращение рецидивов и стабилизация); мании; гипоманиакального состояния; когнитивного нарушения; ADHD; ожирения; снижения аппетита; болезни Альцгеймера; болезни Паркинсона; боли; судорог; кашля; астмы; гиперчувствительности дыхательных путей; гиперчувствительности микрососудов; брон- 16021581 хоконстрикции; хронического обструктивного легочного заболевания; недержания мочи; воспаления кишечника; синдрома воспаленной кишки; PTDS; деменции и ажитации и делирия в пожилом возрасте. В одном варианте настоящее изобретение относится к соединению согласно настоящему изобретению для применения при лечении шизофрении. В частности, указанное лечение включает лечение позитивных, негативных и/или когнитивных симптомов шизофрении. В одном варианте настоящее изобретение относится к соединению согласно настоящему изобретению для применения при лечении когнитивного нарушения. В частности, указанное когнитивное нарушение проявляется в виде снижения рабочей памяти, внимания и вигильности, вербального обучения и памяти, визуального обучения и памяти, логического мышления и решения проблем, например, организующей функции, скорости обработки информации и/или социальных когнитивных функций. Соединения согласно настоящему изобретению можно вводить отдельно в виде чистого соединения или в сочетании с фармацевтически приемлемыми носителями или эксципиентами, в любой однократной или многократных дозах. Фармацевтические композиции согласно изобретению могут быть приготовлены с фармацевтически приемлемыми носителями или разбавителями, а также любыми другими известными адъювантами и эксципиентами согласно обычным способам, таким как способы, описанные вRemington (The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA,1995). Фармацевтические композиции могут быть специально приготовлены для введения любым подходящим путем, таким как пероральный, ректальный, назальный, легочный, местный (включая буккальный и подъязычный), трансдермальный, интрацистернальный, внутрибрюшинный, вагинальный и парентеральный (включая подкожный, внутримышечный, интратекальный, внутривенный и интрадермальный) путь, при этом предпочтительным является пероральный путь. Будет понятно, что предпочтительный путь будет зависеть от общего состояния и возраста субъекта, подвергаемого лечению, природы состояния, подвергаемого лечению, и выбранного активного ингредиента. Фармацевтические композиции для перорального введения включают твердые дозированные формы, такие как капсулы, таблетки, драже, пилюли, лепешки, порошки и гранулы. В соответствующих случаях они могут быть приготовлены с покрытиями. Жидкие дозированные формы для перорального введения включают растворы, эмульсии, суспензии, сиропы и эликсиры. Фармацевтические композиции для парентерального введения включают стерильные водные и неводные инъекционные растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки для перерастворения в виде стерильных инъекционных растворов или дисперсий перед применением. Другие подходящие формы введения включают суппозитории, спреи, мази, кремы, гели, средства для ингаляции, кожные пластыри, имплантаты и т.д. Для удобства соединения согласно изобретению вводят в стандартной лекарственной форме, содержащей указанные соединения в количестве примерно от 0,1 до 500 мг, например 1, 5, 10, 50, 100, 150,200 или 250 мг соединения согласно настоящему изобретению. В случае парентеральных путей, таких как внутривенное, интратекальное, внутримышечное и подобное введение, обычно дозы являются такими, что они составляют примерно половину дозы, используемой для перорального введения. В случае парентерального введения можно использовать растворы соединения согласно изобретению в стерильном водном растворе, водном растворе пропиленгликоля, водном растворе витамина Е или кунжутном или арахисовом масле. Такие водные растворы при необходимости должны быть соответствующим образом забуферены, и жидкий разбавитель сначала делают изотоничным с использованием достаточного количества раствора соли или глюкозы. Водные растворы особенно подходят для внутривенного, внутримышечного, подкожного и внутрибрюшинного введения. Используемые стерильные водные среды легко могут быть получены стандартными способами, известными специалистам в данной области. Подходящие фармацевтические носители включают инертные твердые разбавители или наполнители, стерильный водный раствор и различные органические растворители. Примерами твердых носителей являются лактоза, каолин, сахароза, циклодекстрин, тальк, желатин, агар, пектин, аравийская камедь,стеарат магния, стеариновая кислота и простые низшие алкиловые эфиры целлюлозы. Примерами жидких носителей являются сироп, арахисовое масло, оливковое масло, фосфолипиды, жирные кислоты,амины жирных кислот, полиоксиэтилен и вода. Фармацевтические композиции, образованные в результате объединения соединения согласно изобретению и фармацевтически приемлемых носителей, затем легко вводят в различных дозированных формах, подходящих для указанных путей введения. Препараты согласно настоящему изобретению, подходящие для перорального введения, могут быть представлены в виде дискретных единиц, таких как капсулы или таблетки, каждая из которых содержит предварительно определяемое количество активного ингредиента и которая может включать подходящий эксципиент. Кроме того, перорально принимаемые препараты могут быть в форме порошка или гранул, раствора или суспензии в водной или неводной жидкости или жидкой эмульсии типа масло в- 17021581 воде или вода в масле. Если для перорального введения используют твердый носитель, то препарат может представлять собой таблетку, например, быть помещенным в твердую желатиновую капсулу, в форме порошка или пилюли или в форме пастилки или лепешки. Количество твердого носителя может варьировать, но обычно будет составлять примерно от 25 мг до примерно 1 г. Если используют жидкий носитель, то препарат может быть в форме сиропа, эмульсии, мягкой желатиновой капсулы или стерильной инъекционной жидкости, такой как водная или неводная жидкая суспензия или раствор. Таблетки могут быть приготовлены смешиванием активного ингредиента с обычными адъювантами и/или разбавителями с последующим прессованием смеси в обычной таблеточной машине. Примерами адъювантов или разбавителей являются: кукурузный крахмал, картофельный крахмал, тальк, стеарат магния, желатин, лактоза, камеди и тому подобное. Могут быть использованы любые другие адъюванты или добавки, обычно применяемые для таких целей, такие как красители, корригенты, консерванты и т.д., при условии, что они совместимы с активными ингредиентами. В одном варианте изобретение относится к фармацевтической композиции, содержащей соединение согласно настоящему изобретению вместе со вторым антипсихотическим средством. В одном варианте указанное второе антипсихотическое средство выбрано из антагонистов/обратных агонистов/негативных модуляторов/частичных агонистов мишеней: рецептора допамина D2, рецептора допамина D3, рецептора допамина D4, фосфодиэстеразы PDE10, рецептора серотонина 5-HT1A, рецептора серотонина 5-НТ 2 А, рецептора серотонина 5-НТ 6, адренергического рецептора альфа 2, каннабиноидного рецептора типа 1, рецептора гистамина Н 3, циклооксигеназ, натриевых каналов или переносчика глицина GlyT1; или из агонистов/позитивных модуляторов/частичных агонистов мишеней: рецептора серотонина 5-НТ 2 С, KCNQ-каналов, рецептора NMDA, рецептора АМРА, никотинового рецептора альфа-7, мускаринового рецептора M1, мускаринового рецептора М 4, метаботропного рецептора глутамата mGluR2,метаботропного рецептора глутамата mGluR5, рецептора допамина D1 или рецептора допамина D5. Конкретными примерами таких антипсихотических средств являются галоперидол, хлорпромазин, сульпирид, рисперидон, зипрасидон, оланзапин, кветиапин, клозапин и арипопразол. В одном варианте изобретение относится к фармацевтическому набору, включающему емкость, содержащую соединение согласно настоящему изобретению, и отдельную емкость, содержащую антипсихотическое лекарственное средство, такое как типичные антипсихотические средства, антипичные антипсихотические средства, антагонисты/обратные агонисты/негативные модуляторы/частичные агонисты одной или нескольких мишеней: рецептора допамина D2, рецептора допамина D3, рецептора допаминаD4, фосфодиэстеразы PDE10, рецептора серотонина 5-HT1A, рецептора серотонина 5-НТ 2 А, рецептора серотонина 5-НТ 6, адренергического рецептора альфа 2, каннабиноидного рецептора типа 1, рецептора гистамина Н 3, циклооксигеназ, натриевых каналов или переносчика глицина GlyT1; или агонисты/позитивные модуляторы/частичные агонисты одной или нескольких мишеней: рецептора серотонина 5-НТ 2 с/KCNQ-каналов, рецептора NMDA, рецептора АМРА, никотинового рецептора альфа-7, мускаринового рецептора M1, мускаринового рецептора М 4, метаботропного рецептора глутамата mGluR2, метаботропного рецептора глутамата mGluR5, рецептора допамина D1 или рецептора допамина D5. Конкретными примерами таких антипсихотических средств являются галоперидол, хлорпромазин,сульпирид, рисперидон, зипрасидон, оланзапин, кветиапин, клозапин и арипопразол. Все ссылки, включая публикации, заявки на выдачу патентов и патенты, цитированные в настоящем описании, включены в настоящее описание в виде ссылки в полном объеме и в такой степени, как в случае, когда отдельно и специально указано, что каждая публикация включена в виде ссылки и в полном объеме (в максимальной степени, разрешенной законом), независимо от любого отдельно указанного включения конкретных документов в различных местах настоящего описания. Следует понимать, что использование терминов в единственном числе и сходных указаний в контексте описания изобретения охватывает как формы единственного числа, так и формы множественного числа, если в описании не оговорено особо или ясно не отрицается контекстом. Например, фразу соединение следует понимать как указание на различные соединения согласно изобретению или конкретно описанные аспекты, если не указано иное. Если не оговорено особо, все точные значения, указанные в описании, являются типичными представителями соответствующих приближенных значений (например, можно считать, что все точные приведенные в качестве примеров значения, указанные в связи с конкретным фактором или измерением,также представляют соответствующее приближенное измерение, определяемое в соответствующих случаях термином примерно). Предполагается, что приведенное в настоящей публикации описание любого аспекта или аспекта изобретения с использованием таких терминов, как содержащий, имеющий, включающий или имеющий в своем составе, по отношению к элементу или элементам обеспечивает сходный аспект или аспект изобретения, который состоит из, по существу, состоит из или по существу, включает данный конкретный элемент или элементы, если не указано иное или ясно не исключено контекстом (на- 18021581 пример, следует понимать, что композиция, описанная в настоящей публикации как содержащая конкретный элемент, также описывает композицию, состоящую из данного элемента, если не указано иное или ясное не исключено контекстом). Пути синтеза Соединения согласно настоящему изобретению общей формулы I, где R1-R12, А, X, Q и Y имеют значения, которые определены выше, могут быть получены способами, описанными на следующих далее схемах реакций и в примерах. В описанных способах можно использовать варианты или модификации,которые известны химикам-специалистам в данной области или которые могут быть очевидны для специалиста в данной области. Кроме того, другие способы получения соединений согласно изобретению будут легко понятны специалисту в данной области в свете приведенных ниже схем реакций и примеров. В промежуточных соединениях общих формул II - XXXI R1-R12, А, X, Q и Y имеют значения, которые определены для формулы I. В случае соединений, которые могут существовать в виде смеси или равновесия между двумя или более таутомерами, только один таутомер представлен на схемах, хотя он может быть не самым стабильным таутомером. В случае соединений, которые могут существовать в формах энантиомеров, стереоизомеров или геометрических изомеров, указана их геометрическая конфигурация; в противном случае структура означает смесь стереоизомеров. Такие соединения включают без ограничения сложные 1,3 кетоэфиры или енамины общих формул IV и VII, которые могут существовать в равновесии между кетоили енольными формами, и последние также могут существовать в изомерных Z- и Е-формах, которые хорошо известны химикам-специалистам в данной области. Такие соединения также включают соединения согласно настоящему изобретению общей формулы I, которые могут существовать в виде смеси атропизомеров вследствие ограниченного вращения вокруг одинарной углерод-углеродной связи, подобно атропизомеризму в орто-, орто'-двузамещенных биарильных соединениях, также хорошо известных специалисту в данной области. Исходные вещества общих формул II, III, VI, XI, XX и XXI либо получают из коммерческих источников, которые суммированы в табл. 2, либо они могут быть легко получены стандартными способами или с использованием модификаций таких способов, описанных в литературе. 2-Бромбензойные кислоты общей формулы II связывают со сложными кетоэфирами общей формулы III в присутствии сильного основания, такого как гидрид натрия, и меди или солей меди, таких как бромид меди (I), в подходящем растворителе, таком как 1,4-диоксан, ацетонитрил, или избытка указанных выше сложных кетоэфиров при подходящей температуре, такой как температура образования флегмы или 70 С, с образованием соединений общей формулы IV (схема 1). Такая реакция арилирования хорошо известна в общем как катализируемая медью реакция сочетания Ульмана (см. S.V. Ley, A.W. Thomas Angew. Chem. Int. Ed. 2003,42, 5400). Также в данном конкретном случае, когда в реакцию сочетания вовлечены активированные соединения метилена, такие как соединения общей формулы IV, в присутствии меди или солей меди,реакция известна как реакция Хартли (W.R.H. Hurtley, J. Chem. Soc. 1929, 1870). Затем полученные соединения общей формулы IV конденсируют с аминосоединениями общей формулы VI в присутствии или в отсутствие подходящего растворителя в условиях нагревания с образованием изохинолинонов общей формулы VIII через промежуточное образование енаминов общей формулы VII, которые обычно не отделяют от реакционной смеси. Альтернативно, енамины общей формулыVII могут быть получены из аминосоединений общей формулы VI в присутствии подходящего дегидратирующего реагента, такого как тетраэтоксисилан в условиях нагревания или при температуре окружающей среды в присутствии каталитического количества кислоты, такой как уксусная кислота. Затем может быть осуществлена реакция циклизации с образованием изохинолинонов общей формулы VIII в условиях нагревания, как указано выше, или при температуре окружающей среды в присутствии подходящего связывающего реагента, такого как EDC/HOBT (схема 1). Кроме того, изохинолиноны общей формулы VIII могут быть получены непосредственно из исходных 2-бромбензойных кислот общей формулы II и депротонированных енаминов общей формулы V модифицированным одностадийным способом, включающим реакцию Хартли, осуществляемую при 70 С,с образованием соединений общей формулы VII и последующей циклизацией, осуществляемой при более высокой температуре. Енамины общей формулы V легко получают из сложных кетоэфиров III и аминосоединений VI в условиях, описанных выше для получения енаминов общей формулы VII (схема 1). Соединения общей формулы VIII легко гидролизуются до кислот общей формулы IX в условиях,используемых для гидролиза сложных эфиров, хорошо известных химикам, специалистам в данной области. Наконец, последующее связывание с аминами (А=С) или гидразинами (A=N) общей формулы XI приводит к образованию соединений согласно изобретению общей формулы I (схема 1). Такие реакции связывания обычно осуществляют посредством активации кислоты с использованием подходящего связывающего или активирующего реагента, такого как без ограничения тионилхлорид, с образованием соответствующего хлорангидрида или в присутствии EDC/HOBT. Гидразиды общей формулы I (A=N), гдеR1=H, могут быть превращены в двузамещенные гидразиды такой же общей формулы, где R1 не являет- 19021581 ся водородом, с помощью реакций ацилирования, алкилирования или арилирования с использованием подходящих ацилирующих или алкилирующих реагентов, таких как без ограничения хлорангидриды,карбамоилхлориды, хлорформиаты или алкилгалогениды. Соединения общей формулы I, где X означает метил, могут быть превращены в соединения общей формулы XII в региоселективной реакции бромирования в присутствии реагента для бромирования, такого как бром. Затем атом брома может быть замещен различными нуклефилами общей формулы X'-Н или X" с образованием соединений согласно изобретению общей формулы I, как показано на схеме 2. Специалисты в данной области легко поймут, что многие азотные, углеродные и серные нуклеофилы,такие как без ограничения амины, ароматические амины, амиды, гетероциклы, спирты, фенолы, цианиды или тиолы, коммерчески доступны или могут быть легко получены в нейтральной или в депротонированной анионной форме, необходимой для такого превращения. При необходимости может быть осуществлена дополнительная дериватизация или превращение в заместителях R4-R12 и X с использованием стандартных способов органического синтеза, известных специалисту в данной области. Схема 1 Альтернативно соединения общей формулы I могут быть получены, исходя из замещенных гомофталевых ангидридов общей формулы XVIII, как показано на схеме 4. Гомофталевые ангидриды либо коммерчески доступны, либо могут быть получены, как показано на схеме 3, исходя из соответствующих фторбензонитрилов или фторбензоатов общей формулы XIII и XVII, соответственно. Они подвергаются реакции ароматического нуклеофильного замещения с использованием этилцианоацетата XIV в присутствии основания, такого как карбонат калия или карбонат цезия в условиях нагревания в подходящем растворителе, таком как диметилсульфоксид. Продукты связывания гидролизуют в присутствии сильных кислот, таких как серная или хлористо-водородная кислоты, в воде в условиях нагревания с образованием дикислот общей формулы XVI. Наконец, дикислоты превращают в гомофталевые ангидриды общей формулы XVIII в присутствии дегидратирующего реагента, такого как без ограничения ацетилхлорид без растворителя или в подходящем растворителе, таком как толуол, в условиях нагревания, таких как кипячение с обратным холодильником. Гомофталевые ангидриды общей формулы XVIII могут быть региоселективно превращены в амиды кислот общей формулы XIX при комнатной температуре или в условиях нагревания в подходящем растворителе, таком как ацетонитрил. Затем их можно обработать подходящими ангидридами кислот или хлорангидридами общей формулы XX и XXI соответственно, в отсутствие или присутствии основания,такого как триэтиламин и DMAP, в подходящем растворителе, обычно в ацетонитриле, при комнатной температуре или в условиях умеренного нагревания (Т +100 С). Такое превращение сначала дает промежуточные кетенаминали общей формулы XXII, которые подвергаются дальнейшей реакции ацилирования с образованием кетенаминалей общей формулы XXIII. Дополнительное нагревание при более высокой температуре, такой как +150 С, приводит к перегруппировке с образованием амидов общей формулы XIV. Соединения общей формулы XXIII и XXIV могут быть легко гидролизованы при температуре окружающей среды с использованием подходящего основания, такого как гидроксид натрия в водном метаноле или водном тетрагидрофуране в качестве растворителя. Полученные кетокислоты общей формулы XXV или кетенаминали общей формулы XXIII превращают в конечные соединения согласно изобретению общей формулы I в результате конденсации с аминосоединениями общей формулы VI в таких же условиях, которые описаны выше для конденсации с кетокислотами общей формулы IV. В некоторых случаях такая конденсация может быть осуществлена с аминосоединениями, несущими защитные группы на дополнительном атоме азота, присутствующем в молекуле (схема 7). Затем защитную группу удаляют, и такой атом азота может быть дополнительно дериватизован, например, посредством восстановительного алкилирования, как показано на схеме 7. Альтернативно амиды кислот общей формулы XIX могут быть превращены непосредственно в соединения согласно изобретению общей формулы I путем конденсации с подходящими имидоилхлоридами общей формулы XXVII, которые легко могут быть получены из соответствующего амида общей формулы XXVI и которые легко получают хорошо известным сочетанием между аминосоединениями общей формулы VI и соответствующими карбоновыми кислотами или их ангидридами или хлорангидридами общей формулы XX и XXI, соответственно. В дополнение к описанным выше способам можно использовать реакцию карбонилирования, в частности трехкомпонентное сочетание арилгалогенида, оксида углерода и нуклеофила, такого как амин или спирт (Schoenberg, A.; Bartoletti, L; Heck, R.F.J. Org. Chem. 1974, 39, 3318; Schoenberg, A.; Heck,R.F.J. Org. Chem. 1974, 39, 3327), на ключевой стадии, как показано на схеме 5. Таким образом, дикислоты общей формулы XVI превращают в кетокислоты общей формулы XXVIII в ходе одностадийной реакции ацилирования-декарбоксилирования в уксусном ангидриде (в случае уксусного ангидрида заместитель X является Me) и в присутствии пиридина с последующей конденсацией с аминосоединениями общей формулы VI с образованием изохинолинонов формулы XXIX. Их региоселективно бромируют Nбромсукцинимидом с образованием бромидов общей формулы XXX. Реакция аминокарбонилирования с- 22021581 использованием бромидов общей формулы XXX в присутствии аминов общей формулы XI в атмосфере оксида углерода, ускоряемая катализатором, например, ацетатом палладия - ксантфосом (Kranenburg, М.;van der Burgt, Y.E.M.; Kamer, P.C.J.; van Leeuwen, P.W.N. M. Organometallics 1995, 14, 3081) приводит к образованию соединений согласно изобретению общей формулы I, где X означает Me. Альтернативно,реакция карбонилирования в присутствии спиртов, таких как бензиловый спирт, в таких же условиях приводит к образованию сложных бензиловых эфиров общей формулы XXXI, которые легко превращают в кислоты общей формулы IX в катализируемой палладием реакции гидрирования с последующей конденсацией с аминами общей формулы XI, как описано выше (см. схему I). Альтернативно, гомофталевые ангидриды общей формулы XVIII превращают в еноловые эфиры общей формулы XXXII при кипячении с обратным холодильником в сложных ортоэфирах, таких как триэтилортоацетат или триметилортоформиат. В зависимости от заместителя X (Х=Ме или Н) и аминосоединения общей формулы VI взаимодействие с VI в условиях нагревания в подходящем растворителе,таком как этанол или ацетонитрил, может давать либо кислоты общей формулы IX, либо декарбоксилированные соединения общей формулы XXIX. Последние могут быть превращены в кислоты общей формулы IX, как описано выше (схема 5), в реакциях бромирования и карбонилирования. Также, как описано выше, кислоты общей формулы IX легко превращают в соединения согласно изобретению. Схема 8 где один или несколько из R4-R12 представляют собой удаляемую группу (LG), такую как без ограничения фторид, хлорид, бромид, нитрогруппа, третичный амин или йодарен. Меченые фтором-18 соединения формулы 1 а могут быть получены замещением удаляемой группы(LG) анионами фторида-18, как показано на схеме 8. Схема 9 где LG означает удаляемую группу, такую как без ограничения хлорид, бромид или трифторметилсульфонат, и R30 означает С 2-4-алкил, где один атом углерода представляет собой изотоп 11 С, или С 2-4 алкил замещен 1-2 изотопами 18F. Меченые изотопами соединения формулы Ib могут быть получены в результате взаимодействия соединений формулы XXXIV с мечеными изотопами алкилирующими реагентами, такими как соединения формулы Q, которые показаны на схеме 9. Схема 10 где LG означает удаляемую группу, такую как без ограничения хлорид, бромид или трифторметилсульфонат. Меченые фтором-18 соединения формулы Ic могут быть получены в результате замещения удаляемой группы (LG) анионами фторид-18, как показано на схеме 10. Меченые углеродом-11 соединения формулы Ie могут быть получены в результате реакции аминокарбонилирования с использованием бромидов общей формулы XXX в присутствии аминов общей формулы XI в атмосфере оксида углерода-11, ускоряемой катализатором, например, ацетатом палладия, как показано на схеме 11. Примеры Аналитическая ЖХ-МС, способ А (используемый в большинстве случаев, если не указано иное). Данные получали, используя аналитическую ЖХ/МС-систему Sciex API 150EX, оборудованную одинарным квадрупольным масс-спектрометром Applied Biosystems API150EX и источником ионов, образуемых при фотоионизации при атмосферном давлении (APPI), насосами для ЖХ Shimadzu LC10ADvp (3 Х),матричным фотодиодным детектором Shimadzu SPD-M20A, низкотемпературным испарительным детектором светорассеяния (ELSD) SEDERE Sedex 85, системным контроллером Shimadzu CBM-20A, автоматическим пробоотборником Gilson 215 и дегазатором Gilson 864, управляемую компьютерной программой Analyst. Колонка: колонка С 18 Waters Symmetry 304,6 мм с размером частиц 3,5 мкм; вводимый объем: 15 мкл; температура колонки: 60 С; система растворителей: А=вода/трифторуксусная кислота(100:0,05) и В=вода/ацетонитрил/трифторуксусная кислота (5:95:0,035); способ: элюирование линейным градиентом с использованием 10-100% В в течение 2,4 мин, затем с использованием 10% В в течение 0,4 мин, при скорости потока 3,3 мл/мин. Время удержания (tR) выражено в минутах на основе регистрации в УФ при 254 нм. Аналитическая ЖХ-МС, способ В. Данные получали, используя аналитическую ЖХ/МС-системуSciex API300, оборудованную тройным квадрупольным масс-спектрометром Applied Biosystems API300 с источником ионов, образуемых при фотоионизации при атмосферном давлении (APPI), насосами для ЖХ Shimadzu LC10ADvp (3 Х), матричным фотодиодным детектором Shimadzu SPD-M20A, низкотемпературным испарительным детектором светорассеяния (ELSD) Polymer Labs PL-ELS 2100, системным контроллером Shimadzu SCL10A VP, автоматическим пробоотборником Gilson 215 и дегазатором Gilson 864, управляемую компьютерной программой Analyst. Колонка: колонка С 18 Symmetry, 3,5 мкм, 4,630 мм, 304,6; вводимый объем: 5 мкл; температура колонки: 60 С; система растворителей: А=вода/трифторуксусная кислота (100:0,05) и В=вода/ацетонитрил/трифторуксусная кислота(5:95:0,035); способ: элюирование линейным градиентом с использованием 10-100% В в течение 1,45 мин, затем с использованием 10% В в течение 0,55 мин, при скорости потока 5,5 мл/мин Время удержания (tR) выражено в минутах на основе регистрации в УФ при 254 нм. Аналитическая ЖХ-МС, способ С. Такие же условия, как при аналитической ЖХ-МС в способе А,но со следующими модификациями: растворитель В: метанол с 0,035% ТФУ; расход: 3,0 мл/мин; градиент: 0,01 мин 17% В (об./об.); 0,27 мин 28% В; 0,53 мин 39% В; 0,80 мин 50% В; 1,07 мин 59% В; 1,34 мин 68% В; 1,60 мин 78% В; 1,87 мин 86% В; 2,14 мин 93% В; 2,38 мин 100% В; 2,40 мин 17% В; 2,80 мин 17% В. Очистку препаративной ЖХ-МС осуществляли с использованием такой же системы Sciex API 150EX, оборудованной насосами Gilson 333 и 334, насосом Shimadzu LC10ADvp, УФ-детектором GilsonUV/VIS 155, автоматическим пробоотборником Gilson 233XL, коллектором фракций Gilson FC204, системным интерфейсом Gilson 506 С, дегазатором Gilson 864, разделителем потока DIY (примерно 1:1000) и точным разделителем потока для ЖХ Packings (1:10000, 140 мл/мин). МС и коллектором фракций управляли с помощью компьютерной программы Masschrom (Macintosh PC), системой ЖХ управляли с использованием компьютерной программы Unipoint. В случае небольшого масштаба (20 мг) фракции после очистки собирали во флаконе объемом 4 мл, используя колонку Symmetry С 18, 5 мкм, 1050 мм,вводимый объем 0-300 мкл, расход 5,7 мл/мин и продолжительность 8 мин. ЖХ-МС высокого разрешения осуществляли на приборе Bruker Daltonics micrOTOF с источником ионов типа электроспрея и времяпролетным масс-детектором. 1 Н-ЯМР-спектры регистрировали при 500,13 МГц на приборе Bruker Avance DRX-500 при Т=303,3 13 К. С-ЯМР и 19F-ЯМР регистрировали на том же самом приборе. 1 Н-ЯМР-спектры при различных температурах регистрировали при 250 МГц на приборе Bruker Avance DPX-250. Дейтерированный диметилсульфоксид (ДМСО-d6, 99,8%D) использовали в качестве растворителя, если не указано иное. Тетраметилсилан использовали в качестве внутреннего стандарта, если не указано иное. Значения химических сдвигов выражены в значениях м.д. относительно тетраметилсилана, если не указано иное. Следующие сокращения или их сочетания используют для обозначения сложности сигналов ЯМР: с = синглет, d = дублет, t = триплет, к = квартет, квин = квинтет, г = гептет, дд = двойной дублет, ддд = двойной двойной дублет, дт = двойной триплет, дкв = двойной квартет, тт = триплет триплетов, м = мультиплет и уш. = уширенный или уширенный синглет. Эксперименты, в которых использовали микроволновое излучение, осуществляли в герметичных реакционных флаконах или реакторах, используя синтезатор Emrys или оптимизатор Emrys EXP PersonalChemistry или устройство Milestone Microsynth, Milestone. Когда реакционную смесь нагревали в микроволновом приборе, ее охлаждали до 25 С перед следующей стадией способа. Получение промежуточных продуктов Синтез гомофталевых ангидридов общей формулы XVIII Этиловый эфир циано(2-циано-3-фторфенил)уксусной кислоты Смесь этилового эфира цианоуксусной кислоты (26,7 мл, 251 ммоль), 2,6-дифторбензонитрила (33,2 г, 239 ммоль) и карбоната калия (82,5 г, 597 ммоль) в диметилсульфоксиде (120 мл) перемешивали при+55 С в течение 16 ч и вливали в смесь лед-вода (около 400 мл). Смесь осторожно (выделение СО 2) подкисляли концентрированным водным раствором HCl и экстрагировали этилацетатом (600 мл). Органическую фазу промывали насыщенным раствором соли (100 мл) и упаривали, получая 55,1 г бледно-желтого твердого вещества, которое использовали на следующей стадии без дополнительной очистки. 1 Н ЯМР 2-Карбоксиметил-6-фторбензойная кислота Смесь 62% серной кислоты (2:1 концентрированная H2SO4 в воде, 400 мл) и этилового эфира циано(2-циано-3-фторфенил)уксусной кислоты (52,0 г, 224 ммоль) перемешивали при +150 С в течение ночи (16 ч). Реакционную смесь вливали в лед (около 500 г) и при охлаждении добавляли 10,8 N водный раствор NaOH (500 мл). Смесь экстрагировали этилацетатом (3500 мл) и объединенный органический раствор промывали насыщенным раствором соли, сушили над MgSO4 и упаривали, получая 40,28 г сырого продукта, который использовали на следующей стадии без дополнительной очистки. Аналитический образец получали перекристаллизацией из смеси толуол-этилацетат. 1 Н ЯМР (500 МГц, ДМСО-d6): 3,4 8-Фторизохроман-1,3-дион 2-Карбоксиметил-6-фторбензойную кислоту (130 мг, 0,65 ммоль) в ацетилхлориде (2 мл) нагревали,используя микроволновое излучение, при 150 С в течение 10 мин, затем концентрировали в вакууме,получая указанный в заголовке продукт (120 мг, выход 100%). Соединение является гигроскопичным и медленно разлагается снова до исходной дикислоты во влагосодержащих растворителях или во влажной- 25021581 атмосфере. 1 Н ЯМР (500 МГц, ДМСО-d6): 4,29 (с, 2 Н), 7,27 (д, J=7,8 Гц, 1 Н), 7,34 (дд, J=8,5 Гц, J=11 Гц,1 Н), 7,76 (дт, J=5,3 Гц, J=8 Гц, 1 Н). Следующие гомофталевые ангидриды получали аналогично с использованием описанного выше 3 стадийного способа из соответствующих фторбензонитрилов и этилцианоацетата 8-Йодизохроман-1,3-дион Синтез хиральных и рацемических аминов общей формулы XI(S)-(-)-2-Метил-2-пропансульфинамид Указанное в заголовке хиральное вспомогательное вещество получали согласно способу, описанному для (R)-(+)-энантиомера (см. публикации D.J. Weix and J. A. Ellman Organic Syntheses 2005, 82, 157). 1-Циклопропилметилиденамид (S)-2-метил-2-пропансульфиновой кислоты Указанное в заголовке соединение получали согласно общему способу (см. G. Liu, D.A. Cogan, T.D.(35,0 г, 0,5 моль), 1-циклопропилметилиденамида 2-метил-2-пропансульфиновой кислоты (30 г, 0,25 моль) и безводного CuSO4 (120 г, 0,75 моль) в CH2Cl2 (1500 мл) перемешивали при комнатной температуре в течение ночи. Реакционную смесь фильтровали и упаривали, получая указанное в заголовке соединение (39 г, выход 95%), которое использовали на следующей стадии без дополнительной очистки.[(S)-Циклопропил (3-фторфенил)метил]амид (S)-2-метил-2-пропансульфиновой кислоты и [(R)циклопропил (3-фторфенил)метил]амид (S)-2-метил-2-пропансульфиновой кислоты Указанные в заголовке соединения получали согласно общему способу, описанному для 1,2 стереоселективного присоединения металлоорганических реагентов к сульфинилиминам (см. публикации D.A. Cogan, G. Liu, J.A. Ellman, Tetrahedron 1999, 55, 8883). Способ А. К безводному хлориду лития (1,7 г, 40 ммоль) добавляли ТГФ (20 мл) в атмосфере азота с последующим медленным добавлением i-PrMgCl (22 мл, 2 М в ТГФ) и полученную смесь перемешивали при комнатной температуре в течение ночи. Полученный раствор i-PrMgCl-LiCl по каплям добавляли к перемешиваемому раствору 1-бром-3-фторбензол (5,6 г, 33 ммоль) в ТГФ (25 мл) при 0 С и перемешивание продолжали в течение 2 ч. Полученный реагент Гриньяра добавляли к раствору 1-циклопропилметилиденамида (S)-2-метил-2-пропансульфиновой кислоты (2,5 г, 14 ммоль) в CH2Cl2 (60 мл) при -48 С. Смесь перемешивали при -48 С в течение 5 ч и затем при комнатной температуре в течение ночи. Реакционную смесь гасили добавлением насыщенного водного раствора NH4Cl (50 мл) и экстрагировалиCH2Cl2 (3100 мл). Объединенный органический раствор сушили (Na2SO4) и упаривали, получая неочищенную смесь, которую очищали хроматографией на колонке с силикагелем (EtOAc/петролейный эфир=1/10). Полученную смесь диастереоизомеров разделяли, используя SFC, получая указанный в заго- 26021581 ловке (S,S)-изомер в качестве основного продукта (1,5 г, выход 37,5%) и указанный в заголовке (S,R)изомер (0,16 г, выход: 4,0%). Способ В. Альтернативно к суспензии Mg (13,4 г, 0,55 моль) в 50 мл безводного ТГФ при 50 С по каплям добавляли раствор 1-бром-3-фторбензола (89,0 г, 0,50 моль). Смесь перемешивали в течение 2 ч при +50 С и затем ее по каплям добавляли к раствору 1-циклопропил-метилиденамида (S)-2-метил-2 пропансульфиновой кислоты (78,0 г, 0,46 моль) в 100 мл ТГФ при 50-60 С и перемешивали в течение 2 ч. Смесь гасили насыщенным водным раствором NH4Cl (100 мл), водой (300 мл), фильтровали и твердое вещество и фильтрат экстрагировали горячим этилацетатом (600 мл) и упаривали в вакууме. Остаток кристаллизовали из смеси этилацетата и петролейного эфира (1:1, 200 мл) при -20 С, получая 80 г указанного в заголовке (S,S)-изомера в виде белого порошка, выход 66%, ee 100% согласно хиральной ВЭЖХ. 1 Н ЯМР (CDCl3, 400 МГц, ТМС=0 м.д.): 7,34-7,28 (м, 1 Н), 7,16-7,12 (м, 2 Н), 7,00-6,96 (м, 1 Н),3,68 (дд, J=8,8 Гц, 3,2 Гц, 1 Н), 3,52 (с, 1 Н), 1,42 (с, 9 Н), 1,15-1,08 (м, 1 Н), 0,84-0,75 (м, 1 Н), 0,69-0,61 (м,1 Н), 0,55-0,46 (м, 1 Н), 0,28-0,21 (м, 1 Н). Гидрохлорид (S)-(+)-С-[С-циклопропил-С-(3-фторфенил)]метиламина К насыщенному раствору HCl в безводном диоксане (400 мл) при 0 С добавляли [(S)-циклопропил(3-фторфенил)метил]амид (S)-2-метил-2-пропансульфиновой кислоты (80 г, 0,3 моль). После перемешивания при комнатной температуре в течение 1 ч реакционную смесь упаривали в вакууме. Остаток промывали безводным эфиром (2100 мл) и сушили в вакууме, получая 56 г указанного в заголовке соединения в виде белого твердого вещества, выход 93%, ее 100% согласно хиральной ВЭЖХ. []20, D= Гидрохлорид (R)-(-)-С-[С-циклопропил-С-(3-фторфенил)]метиламина Указанное в заголовке соединение получали согласно описанному выше идентичному способу из[(R)-циклопропил(3-фторфенил)метил]амида (S)-2-метил-2-пропансульфиновой кислоты (0,16 г, 0,6 ммоль), получая 0,116 г указанного в заголовке соединения в виде белого твердого вещества, []20, D=49,18 (с=10 мг/мл, СН 3 ОН), ее 100%. 1H-ЯМР (CD3OD, 400 МГц, TMS=0): идентичный с (S)энантиомером. Следующие энантиомерно чистые гидрохлориды аминов получали аналогично, используя трехстадийный способ, начиная с конденсации соответствующего альдегида с хиральным вспомогательным веществом, стереоселективного присоединения реагентов Гриньяра, при этом смесь диастереоизомеров разделяли либо перекристаллизацией, либо хроматографией (SFC или колонка) и основной (S,S)диастереоизомер, наконец, превращали в хиральный амин, используя HCl. Синтез амидов кислот общей формулы XIX 2-[S)-1-Фенилпропилкарбамоил)метил]бензойная кислота Смесь гомофталевого ангидрида (810 мг, 5 ммоль) и (S)-(-)-1-фенилпропиламина (676 мг, 5 ммоль) в ацетонитриле (15 мл) нагревали под действием микроволнового излучения при +150 С в течение 15 мин. Белый преципитат собирали фильтрованием, промывали гептаном и сушили в вакууме, получая чистое указанное в заголовке соединение с выходом 72% (1,065 г). Альтернативно к перемешиваемому раствору гомофталевого ангидрида (16,214 г, 0,1 моль) в ацетонитриле (100 мл) по каплям добавляли (S)(-)-1-фенилпропиламин (13,83 г, 0,102 моль) (экзотермическая реакция) и полученную реакционную смесь кипятили с обратным холодильником в течение 5 мин. Смеси давали возможность остыть и продукт выделяли фильтрованием, как указано выше, получая 23,4 г бесцветного твердого вещества, выход 79%. ЖХ-МС (m/z) 298,5 (МН+); tR=1,11. 1 Н ЯМР (500 МГц, ДМСО-d6): 0,84 (т, J=7,3 Гц, 3 Н), 1,67 (квинтет, J=7,3 Гц, 2 Н), 3,85 (д системы АВ, J=15,1 Гц, 1 Н), 3,95 (д системы АВ, J=15,1 Гц, 1 Н), 4,66 (кв, J=7,6 Гц, 1 Н), 7,2 (неразрешенный, м, 1 Н), 7,25-7,34 (м, 5 Н), 7,45 (т, J=7,3 Гц, 1 Н), 7,8 (д, J=7,8 Гц, 1 Н), 8,39(уш., д, J=7,7 Гц, 1 Н, NH). Следующие соединения получали аналогично из соответствующих гомофталевых ангидридов и аминов общей формулы XVIII и XI, соответственно. Реакции обычно осуществляли при комнатной температуре и продукты выделяли экстракцией или фильтрованием и использовали на следующих стадиях без дополнительной очистки.
МПК / Метки
МПК: C07D 217/26, C07D 407/04, A61P 25/18, A61K 31/472, C07D 401/06, C07D 403/06
Метки: антагонистов, изохинолинона, качестве, производные
Код ссылки
<a href="https://eas.patents.su/30-21581-proizvodnye-izohinolinona-v-kachestve-antagonistov-nk3.html" rel="bookmark" title="База патентов Евразийского Союза">Производные изохинолинона в качестве антагонистов nk3</a>
Предыдущий патент: Применение антитела, специфичного к рецептору fgf-r4
Следующий патент: Способ получения жидкости для подземного ремонта скважин и способ подземного ремонта скважины
Случайный патент: Средство фиксации горлышка пробки незаполняемого повторно типа