Терапевтическое применение производных хиназолиндиона при сердечно-сосудистых заболеваниях
Номер патента: 20984
Опубликовано: 31.03.2015
Авторы: Нав Жан-Франсуа, Марсиньяк Жильбер, Вивьяни Фабрис, Жаниак Филип
Формула / Реферат
1. Применение соединения, соответствующего общей формуле (I)
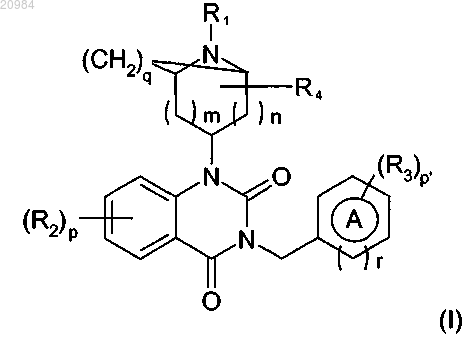
где А представляет собой арил, выбранный из фенила и нафтила, или гетероарил, выбранный из пиридила, пиразолила, пиримидинила, 1,2,4-оксадиазолила, индолила, хинолинила, бензофурила, бензотиазолила, тиено[2,3-b]пиридила, имидазо[1,2-а]пиридила, 1,3-бензодиоксолила и 1,5-бензодиоксепинила;
R1 представляет собой
атом водорода;
-C(O)R, где R означает атом водорода, (C1-С6)алкоксигруппу, (С3-С6)циклоалкил или (C1-C6)алкил, причем указанный алкил при необходимости имеет такие заместители, как одна или несколько гидроксигрупп; бензилоксигруппа;
(C1-C6)алкил;
R2 представляет собой
атом водорода;
атом галогена;
цианогруппу;
нитрогруппу;
(C1-C6)алкил, имеющий при необходимости в качестве заместителя -NH2 или -NHC(O)Rb, где Rb имеет значения, определенные далее;
-ORa, где Ra представляет собой атом водорода; (C1-C6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов или одну или несколько цианогрупп;
R3 представляет собой
атом водорода;
атом галогена;
гидроксигруппу;
цианогруппу;
-SCF3;
нитрогруппу;
-S(О)0-2-алкил, -S(О)0-2-гетероциклоалкил, где гетероциклоалкил представляет собой морфолинил, -O-SO2-арил, где арил представляет собой фенил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;
арил, представляющий собой фенил, или гетероарил, выбранный из пиридила, 1,2,4-оксадиазолила, тиенила, 1,2,4-триазолила, пиразолила, тиазолила, бензимидазолила, бензотиенила, и, кроме того, имеющий при необходимости в качестве заместителей (C1-C6)алкил или один или несколько атомов галогенов;
гетероциклоалкил, выбранный из пирролидинила и морфолинила, имеющий при необходимости в качестве заместителя (C1-C6)алкил;
(C1-С6)алкил, имеющий при необходимости такие заместители, как один или несколько атомов галогенов; гетероарил, выбранный из пиразолила и 1,2,4-триазолила; гетероциклоалкил, выбранный из пирролидинила, пиперидинила, морфолинила и пиперазинила, имеющий при необходимости в качестве заместителя CO(O)Ra или (C1-C6)алкил, где Ra имеет значения, определенные ранее;
-C(O)NRbRc, где Rb и Rc имеют значения, определенные далее;
-C(O)ORc или -O-C(O)ORc, где Rc имеет значения, определенные далее;
(C1-C6)алкоксигруппу, имеющую при необходимости следующие заместители: (С3-С6)циклоалкил; гетероциклоалкил, представляющий собой пирролидинил; моноциклический гетероарил, представляющий собой пиримидинил; одна или несколько гидроксигрупп; -C(O)ORc, где Rc имеет значения, определенные далее; -C(O)NRbRc, где Rb и Rc имеют значения, определенные далее, и/или арил, представляющий собой фенил;
-NH-CO-арил, где арил представляет собой фенил, при необходимости имеющий в качестве заместителей один или несколько атомов галогенов;
R4 представляет собой атом водорода;
Rb представляет собой
атом водорода;
(С1-С6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов, одну или несколько гидроксигрупп, цианогруппу, аминогруппу, гетероциклоалкил, представляющий собой морфолинил, (С1-С6)алкоксигруппу;
(С1-С6)алкоксигруппу;
арил, представляющий собой фенил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;
Rc представляет собой атом водорода или (C1-C6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;
или Rb и Rc совместно с атомом азота, с которым они связаны, образуют полициклический гетероарил, представляющий собой 2,3-дигидро-1Н-индолил, или гетероциклоалкил, представляющий собой пиперидинил;
m и n независимо друг от друга имеют значения 0, 1 или 2 при условии, что m+n≤3;
р и р' независимо друг от друга имеют значения 1, 2 или 3 при условии, что в случае, когда р больше или равно 2, группы R2 присоединены к разным атомам углерода и могут отличаться друг от друга, а в случае, когда р' больше или равно 2, группы R3 присоединены к разным атомам углерода и могут отличаться друг от друга;
q имеет значения 0 или 2 при условии, что в случае, когда q равно 0, азотсодержащий гетероцикл, связанный с атомом азота, находящимся в положении 1 ядра 2,4-диоксо-1,2,3,4-тетрагидрохиназолина, не является мостиковым и соответствует формуле
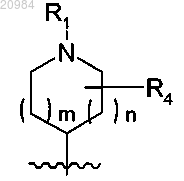
где R1, R4, m и n имеют значения, определенные ранее;
r имеет значение 0 или 1;
в виде основания или кислотно-аддитивной соли;
для получения лекарственного средства, предназначенного для лечения по меньшей мере одного сердечно-сосудистого заболевания и/или профилактики возникновения по меньшей мере одного сердечно-сосудистого заболевания.
2. Применение по п.1, отличающееся тем, что сердечно-сосудистое заболевание выбрано из таких заболеваний, как (i) коронарные болезни, (ii) болезни сердечной мышцы, (iii) болезни сердечных клапанов, (iv) болезни перикарда, (v) нарушения сердечного ритма и внутрисердечной проводимости и (vi) болезни сосудов.
3. Применение по любому из пп.1 или 2, отличающееся тем, что сердечно-сосудистое заболевание выбрано из таких заболеваний, как инфаркт миокарда, в частности нарушения сократительной функции сердца, вызываемые инфарктом миокарда, заболевания, связанные с нарушениями реперфузии сердечной мышцы и/или скелетных мышц, легочная гипертензия, фиброз печени, артериальный рестеноз после осуществления ангиопластики необязательно с установкой стента, атеросклероз и его осложнения, сердечная недостаточность, дилатационные кардиопатии и миокардиты вирусного и/или бактериального происхождения.
4. Применение по любому из пп.1-3, отличающееся тем, что А представляет собой фенил или пиридил.
5. Применение по любому из пп.1-4, отличающееся тем, что q равно 0, a m и n по отдельности равны 1.
6. Применение по любому из пп.1-5, отличающееся тем, что R2 представляет собой (C1-C6)алкил, предпочтительно метил, имеющий в качестве заместителя -NH-C(O)Rb, где Rb имеет значения, определенные в п.1.
7. Применение по любому из пп.1-5, отличающееся тем, что R2 представляет собой -ORa, где Ra имеет значения, определенные в п.1.
8. Применение по любому из пп.1-5, отличающееся тем, что R2 представляет собой атом галогена, или цианогруппу, или атом водорода, или гидроксил, или (С1-С6)алкил, имеющий при необходимости в качестве заместителя -NH2 или -NHC(O)Rb, где Rb имеет значения, определенные в п.1.
9. Применение по любому из пп.1-5, отличающееся тем, что А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0, n и m по отдельности равны 1, a R2 представляет собой -ORa, где Ra имеет значения, определенные в п.1.
10. Применение по любому из пп.1-5, отличающееся тем, что А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0, n и m по отдельности равны 1, р равно 1, a R2 представляет собой метил, имеющий в качестве заместителя -NH-CO-Rb, где Rb имеет значения, определенные в п.1.
11. Применение по любому из пп.1-5, отличающееся тем, что А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0, n и m по отдельности равны 1, р равно 2, одна из групп R2 представляет собой -ORa, где Ra имеет значения, определенные в п.1, а другая группа R2 представляет собой атом галогена.
12. Применение по любому из пп.1-11, отличающееся тем, что R2 находится в положении 6 ядра 2,4-диоксо-1,2,3,4-тетрагидрохиназолина и, кроме того, в положении 7 ядра 2,4-диоксо-1,2,3,4-тетрагидрохиназолина может находиться группа R2, являющаяся идентичной или отличающейся от ранее упомянутой группы R2, причем соединение формулы (I) находится в виде основания, гидрата, сольвата, изомеров или их смесей.
13. Применение по любому из пп.1-3, отличающееся тем, что соединение формулы (I) выбрано из следующих соединений:

















в виде основания или кислотно-аддитивной соли.
Текст
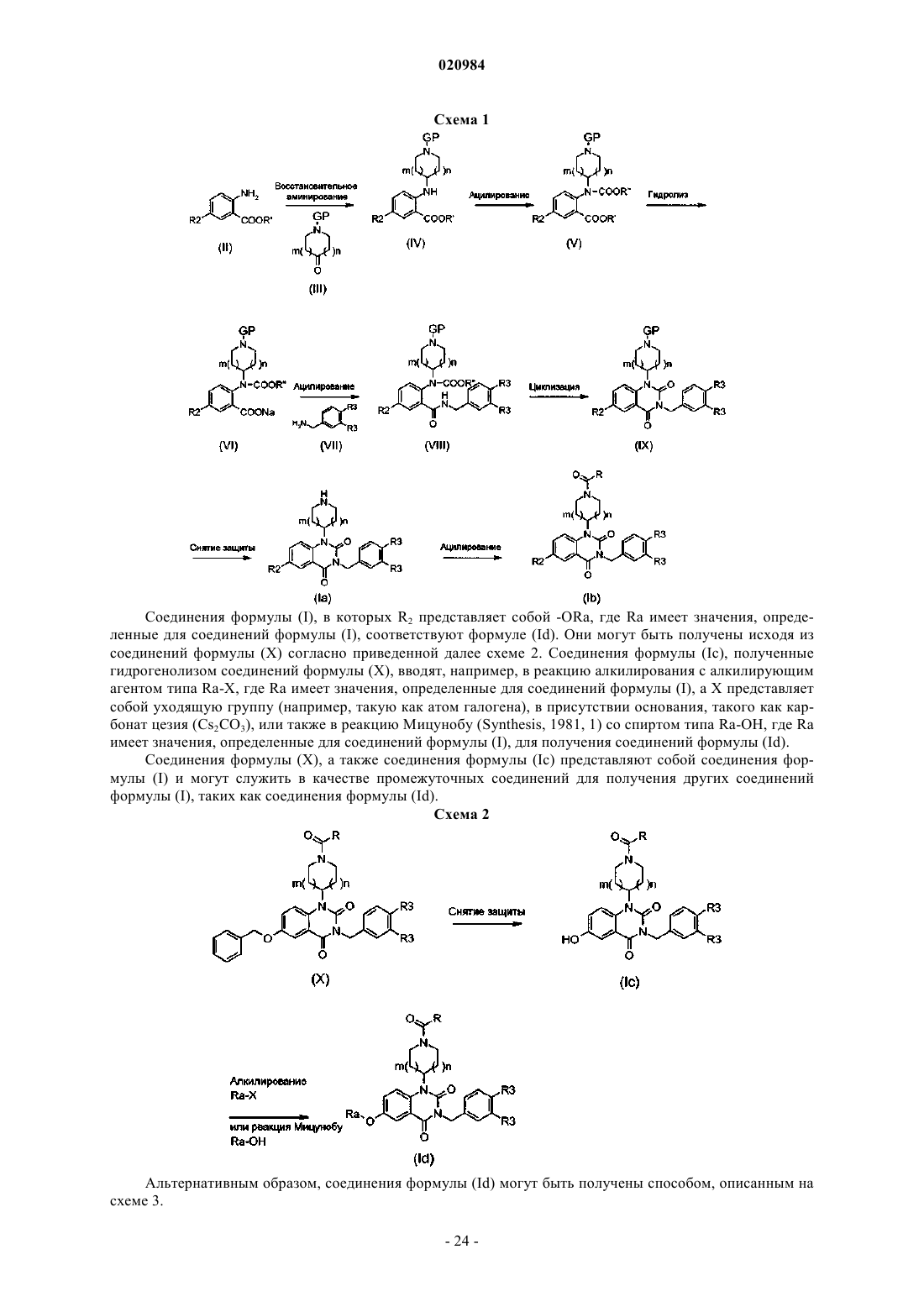
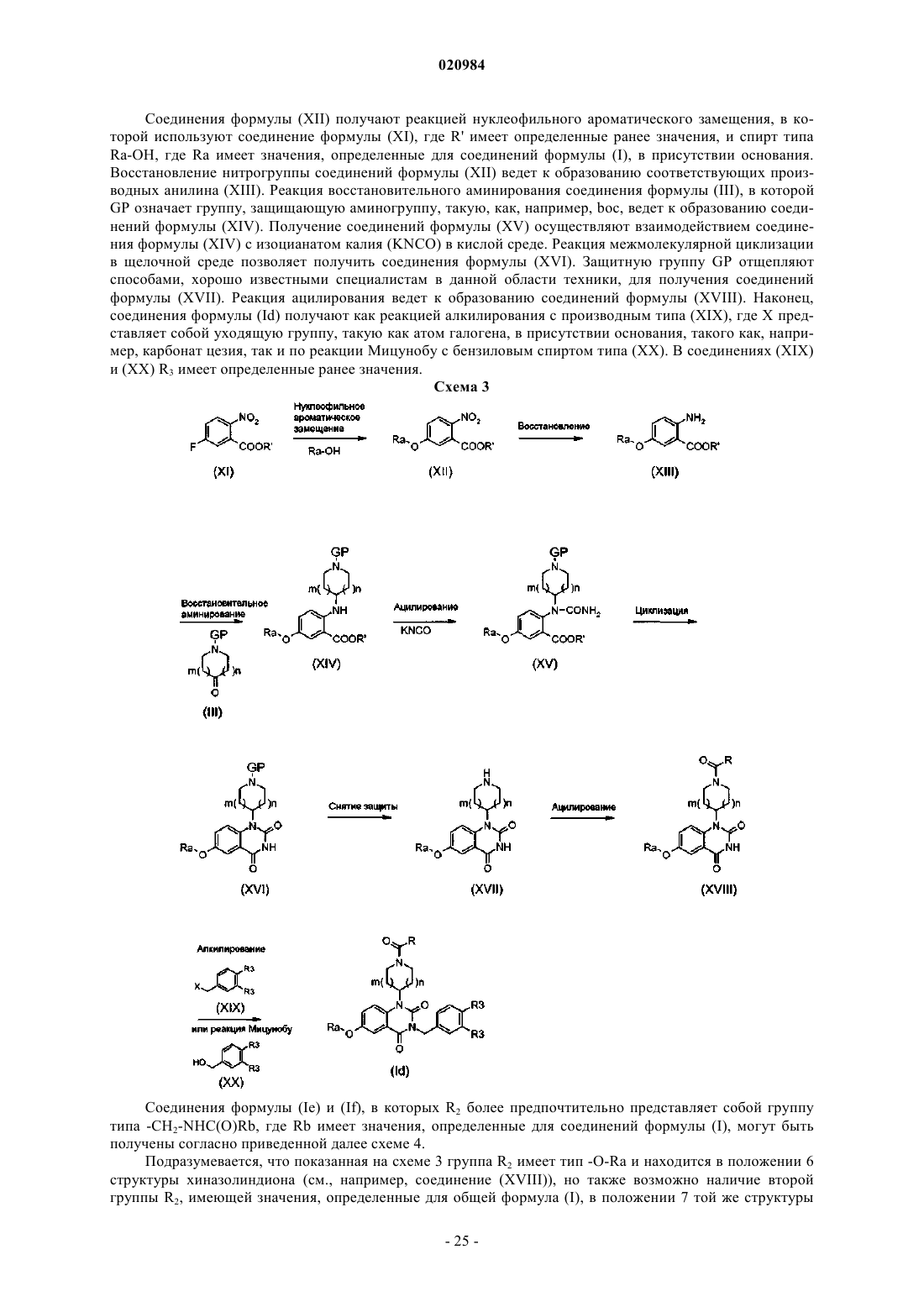
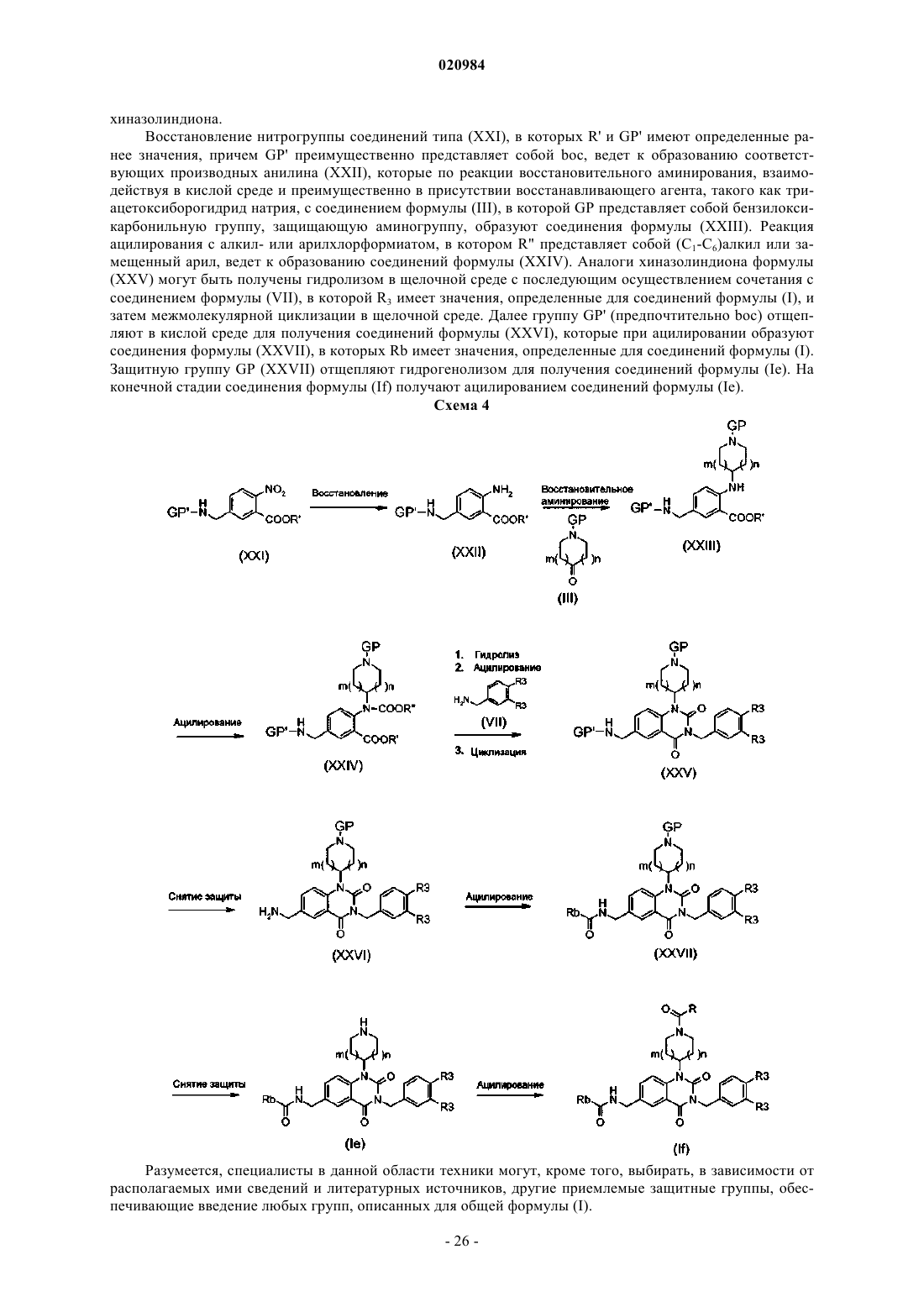
ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ ХИНАЗОЛИНДИОНА ПРИ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЯХ Изобретение относится к применению соединений формулы (I) в виде основания, гидрата, сольвата или их смесей в качестве лекарственных средств или для получения лекарственных средств, предназначенных для лечения по меньшей мере одного сердечно-сосудистого заболевания и/или профилактики появления по меньшей мере одного сердечно-сосудистого заболевания. Изобретение относится к применению производных хиназолиндиона в качестве лекарственных средств или для получения лекарственных средств, предназначенных для лечения и/или профилактики по меньшей мере одного сердечно-сосудистого заболевания. Изобретение более предпочтительно относится к применению производных хиназолиндиона, способных действовать в качестве ингибиторов фосфодиэстеразы 7 (PDE7), и также некоторых из таких производных, способных также действовать в качестве ингибиторов фосфодиэстеразы 8 (PDE8), причем не исключается, что одни и те же производные хиназолиндиона могут быть также способными действовать через другие биологические/биохимические пути на сердечно-сосудистую систему с целью лечения одного или нескольких сердечно-сосудистых заболеваний и/или профилактики появления таких заболеваний. Фосфодиэстеразы (PDE) представляют собой внутриклеточные ферменты, ответственные за гидролиз вторичных информационных АМРс (циклический аденозин-3',5'-монофосфат) и GMPc (циклический гуанозин-3',5'-монофосфат) до неактивных нуклеотид-5'-монофосфатов. АМРс и GMPc играют существенную роль в путях клеточной сигнализации и участвуют в большом числе физиологических процессов. Ингибирование фосфодиэстеразы выражается в увеличении внутриклеточных концентраций АМРс и GMPc, вызывающих специфическую активацию путей фосфорилирования, вовлеченных в различные функциональные ответы. Увеличение внутриклеточных концентраций АМРс и GMPc посредством селективных ингибиторов фосфодиэстераз представляется многообещающим подходом для лечения различных заболеваний (Bender et Beavo, Pharmacol. Rev. (2006), 58, 488-520). Таким образом, ингибиторы фосфодиэстераз представляют интерес в качестве терапевтических средств и фармакологических препаратов. К настоящему времени идентифицированы одиннадцать групп фосфодиэстераз. Они отличаются своей первичной структурой, специфичностью к субстрату и чувствительностью в отношении различных специфических эффекторов и ингибиторов PDE. Каждая группа включает в себя один или несколько генов, которые экспрессируются в различных тканях в виде вариантов сплайсинга (Bender et Beavo, Pharmacol. Rev. (2006), 58, 488-520; Lugnier, Pharmacol. Therapeut. (2006), 109, 366-398).PDE4, 7 и 8 специфически гидролизуют АМРс, a PDE5, 6 и 9 гидролизуют GMPc. Группа PDE7 представлена изоформами PDE7A и PDE7B, происходящими от двух различных генов.(1997), 272, 16152-16157; Wang et al., Biochem. Biophys. Res. Commun. (2000), 276, 1271-1277) и PDE7B человека (Sasaki et al., Biochem. Biophys. Res. Commun. (2000), 271, 575-583; Gardner et al., Biochem. Biophys. Res. Commun. (2000), 272, 186-192) селективно гидролизуют АМРс с константами Михаэлиса (Km) в интервале от 0,1 до 0,2 мкМ и от 0,13 до 0,2 мкМ соответственно. Каталитическая часть PDE7B приблизительно на 67% гомологична каталитической части PDE7A. Для PDE7A известны три варианта сплайсинга. PDE7A1 и PDE7A3 экспрессируются главным образом в клетках иммунной системы и легких, тогда как PDE7A2 экспрессируется предпочтительно в клетках скелетных мышц, сердца и почек. Для PDE7B недавно были идентифицированы также три варианта(Giembycz et Smith, Drugs Future (2006), 31, 207-229). Профили распределения PDE7A и PDE7B в тканях очень сильно отличаются, приводя к предположению, что эти две изоформы обладают отличающимися функциями в физиологическом отношении.PDE7A в значительном количестве экспрессируется в кроветворных клетках, в клетках легких, плаценты,селезенки, скелетных мышц, сердца, клетках Лейдига, собирательных трубочках почек и надпочечников. Большая экспрессия PDE7B обнаруживается в поджелудочной железе, сердце, щитовидной железе и скелетных мышцах (Giembycz et Smith, Drugs Future (2006), 31, 207-229; Wang et al., Biochem. Biophys. Res.Commun. (2000), 276, 1271-1277). В некоторых тканях наблюдается совместная экспрессия информационных ДНК (иРНК (RNAm PDE7A и PDE7B. Это относится к остеобластам (Ahlstrom et al., Cell. Mol.Biol. Lett. (2005), 10, 305-319) и некоторым зонам головного мозга, таким как ряд зон коры, зубчатая извилина, большая часть компонентов обонятельной системы, стриатум, большинство ядер таламуса и пирамидальные клетки гиппокампа (Miro et al., Synapse (2001), 40, 201-214; Reyes-Irisarri et al., Neuroscience(2005), 132, 1173-1185). В отличие от этого в некоторых зонах головного мозга экспрессируется только одна их двух изоформ. Так, например, в большинстве ядер ствола мозга содержатся только иРНКPDE7A. Аналогичным образом, иРНК PDE7B содержатся в больших концентрациях в прилегающем и заднем ядрах блуждающего нерва, тогда как иРНК PDE7A там не обнаруживаются (Miro et al., Synapse(2001), 40, 201-214; Reyes-Irisarri et al., Neuroscience (2005), 132, 1173-1185). Настоящее изобретение предпочтительно относится к терапевтическому применению производных хиназолиндиона, которые могут представлять собой мощные ингибиторы PDE7 или PDE7 и PDE8 в зависимости от вида производных или которые могут действовать через другие биологические пути. Настоящее изобретение относится к соединению, соответствующему приведенной далее формуле где А представляет собой арил или гетероарил;R1 представляет собой атом водорода;-C(O)R, где R означает атом водорода, (С 1-С 6)алкоксигруппу, арил, (С 3-С 6)циклоалкил или (C1 С 6)алкил, причем данный алкил при необходимости имеет такие заместители, как одна или несколько гидроксигрупп; бензилоксигруппа; (C1-С 6)алкоксигруппа, имеющая при необходимости в качестве заместителя арил, или (С 3-С 6)циклоалкил;(C1-C6)алкил, имеющий при необходимости заместители;R2 представляет собой атом водорода; атом галогена; цианогруппу; нитрогруппу;(C1-C6)алкил, имеющий при необходимости в качестве заместителя -NH2 или -NHC(O)Rb, где Rb имеет значения, определенные далее;-ORa, где Ra представляет собой атом водорода; (C1-C6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов, одну или несколько гидроксигрупп, арил и/или одну или несколько цианогрупп; (C2-С 6)алкинил; арил;R3 представляет собой атом водорода; атом галогена; гидроксигруппу; цианогруппу;-S(О)0-2-алкил, -S(О)0-2-гетероциклоалкил, -О-SO2-арил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;-алкиламиноалкил или -циклоалкиламиноалкил, каждый из которых при необходимости имеет заместители при концевом алкиле; сульфонамидную группу, имеющую при необходимости заместители; арил или гетероарил, являющийся моноциклическим или полициклическим и, кроме того, имеющий при необходимости в качестве заместителей (C1-C6)алкил, один или несколько атомов галогенов или(C1-C6)алкоксигруппу; гетероциклоалкил, имеющий при необходимости в качестве заместителя (C1-C6)алкил;(C1-С 6)алкил, имеющий при необходимости такие заместители, как один или несколько атомов галогенов; арил, который может иметь в качестве заместителей один или несколько атомов галогенов или одну или несколько гидроксигрупп; гетероарил; одна или несколько гидроксигрупп, которые могут иметь в качестве заместителей арил, в свою очередь, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов, или гетероциклоалкил, имеющий при необходимости в качестве заместителя CO(O)Ra или (C1-C6)алкил, где Ra имеет значения, определенные ранее;(C1-C6)алкоксигруппу, имеющую при необходимости такие заместители, как аминоалкил; аминоциклоалкил; циклоалкил; гетероциклоалкил; моноциклический или полициклический гетероарил; одна или несколько гидроксигрупп; один или несколько атомов галогенов; (C1-C6)алкоксигруппа; -C(O)ORc,где Rc имеет значения, определенные далее; -C(O)NRbRc, где Rb и Rc имеют значения, определенные далее, и/или арил, в свою очередь, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов, цианогруппу, (C1-C6)алкоксигруппу, -О-галогеналкил и/или галогеналкил;-О-циклоалкил, -О-арил или -О-гетероциклоалкил, каждый из которых при необходимости имеет такие заместители, как арил, в свою очередь, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов или (C1-C6)алкил; один или несколько атомов галогенов, и/или (C1C6)алкил, который, в свою очередь, может иметь в качестве заместителя арил;-NH-CO-NH-арил, -NH-CO-NH-гетероарил или -NH-CO-NH-(C1-С 6)алкил, причем каждый из них при необходимости имеет в качестве заместителей один или несколько атомов галогенов, цианогруппу,нитрогруппу, одну или несколько гидроксигрупп или (C1-C6)алкоксигруппу;-N-(C1-C6)алкил, причем (C1-C6)алкил может иметь в качестве заместителей один или несколько арилов, имеющих при необходимости в качестве заместителей один или несколько атомов галогенов и/или групп SO2;-NH-CO-арил, -NH-CO-гетероарил, причем каждый из них при необходимости имеет в качестве заместителей один или несколько атомов галогенов; или R3 образует с группой А полициклический гетероарил, имеющий при необходимости в качестве заместителя (С 1-С 6)алкоксигруппу, (C1-C6)алкил, имеющий при необходимости в качестве заместителя арил, который, в свою очередь, может иметь в качестве заместителей один или несколько атомов галогенов;R4 представляет собой атом водорода или (C1-C6)алкил;Rb представляет собой атом водорода;(C1-C6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов, одну или несколько гидроксигрупп, цианогруппу, аминогруппу, гетероциклоалкил, (C1 С 6)алкоксигруппу или арил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;(C1-С 6)алкоксигруппу; арил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов;Rc представляет собой атом водорода или (C1-C6)алкил, имеющий при необходимости в качестве заместителей один или несколько атомов галогенов; или Rb и Rc совместно с атомом азота, с которым они связаны, образуют полициклический гетероарил или гетероциклоалкил;m и n независимо друг от друга имеют значения 0, 1 или 2 при условии, что m+n3; р и р' независимо друг от друга имеют значения 1, 2 или 3 при условии, что в случае, когда р больше или равно 2, группы R2 присоединены к разным атомам углерода и могут отличаться друг от друга, а в случае, когда р' больше или равно 2, группы R3 присоединены к разным атомам углерода и могут отличаться друг от друга;q имеет значения 0 или 2 при условии, что в случае, когда q=0, азотсодержащий гетероцикл, связанный с атомом азотом, находящимся в положении 1 ядра 2,4-диоксо-1,2,3,4-тетрагидрохиназолина, не является мостиковым и соответствует формулеr имеет значение 0 или 1; в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения по меньшей мере одного сердечно-сосудистого заболевания и/или профилактики появления по меньшей мере одного сердечно-сосудистого заболевания. Соединения общей формулы (I) могут содержать один или несколько асимметрических атомов углерода. Таким образом, они могут существовать в форме энантиомеров или диастереоизомеров. Такие энантиомеры, диастереоизомеры, а также их смеси, включая рацемические смеси, составляют часть настоящего изобретения. Благодаря своей структуре соединения общей формулы (I) могут существовать также в виде изомеров типа ротамеров или атропоизомеров. Соединения формулы (I) могут существовать также в виде оснований или кислотно-аддитивных солей. Такие аддитивные соли составляют часть настоящего изобретения. Эти соли предпочтительно получают с фармацевтически приемлемыми кислотами, однако и соли других кислот, которые могут быть использованы, например, для очистки или разделения соединений общей формулы (I), также составляют часть настоящего изобретения. Соединения общей формулы (I) могут также находиться в кристаллическом, аморфном или маслоподобном состоянии, причем такие формы составляют часть настоящего изобретения. Соединения общей формулы (I) могут, кроме того, находиться в виде гидратов или сольватов, а именно, в виде ассоциаций или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты и сольваты также составляют часть настоящего изобретения. По настоящему изобретению N-оксиды соединений, содержащих аминогруппу, также составляют часть настоящего изобретения. Соединения формулы (I) по настоящему изобретению включают в себя также соединения, в которых один или несколько атомов водорода, углерода или галогенов, в частности хлора или фтора, замещены их радиоактивными изотопами, например тритием, замещающим водород, или углеродом 14, замещающим углерод 12. Такие меченые соединения являются полезными при исследованиях метаболизма или фармакокинетики, в биологических и фармакологических испытаниях в качестве препаратов. В рамках настоящего изобретения принято, что численные индексы в выражении (C1-C6) определяют возможное число атомов углерода, содержащихся в цепи или цикле. Таким образом, например, (C1-C6) означает углеродную цепь, которая может содержать от 1 до 6 атомов углерода. Аналогичным образом, например, (C1-C5) означает углеродную цепь, которая может содержать от 1 до 5 атомов углерода, или же (С 3-С 6) может означать насыщенный углеродный цикл, который может содержать от 3 до 6 атомов углерода; алкоксигруппа представляет собой -О-алкил с линейной или разветвленной насыщенной алифатической цепью; алкинил представляет собой линейную или разветвленную моно- или полиненасыщенную алифатическую группу, содержащую, например, одну или две ненасыщенные тройные связи. Например, (С 2 С 6)алкинил может представлять собой этинил, пропинил и т.д.; алкил представляет собой линейную или разветвленную насыщенную алифатическую группу; например, (C1-C6)алкил представляет собой линейную или разветвленную углеродную цепь, содержащую от 1 до 6 атомов углерода, в частности метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил,трет-бутил, пентил; аминоалкил представляет собой -NH(C1-C6)алкил или также -NC1-C6)алкил)2; арил представляет собой моноциклическую ароматическую систему, имеющую при необходимости заместители и содержащую в цикле от 5 до 14 членов и предпочтительно от 5 до 10 членов. В качестве примеров моноциклических арилов можно назвать фенил или нафтил; арил может иметь заместители,которые могут представлять собой, например, один или несколько атомов галогенов, гидрокси-, циано-,трифторметилтио-, нитрогруппу, алкил, алкокси-, алкилтиогруппу, метилсульфонил, алкиламиноалкил или алкиламиноциклоалкил, имеющий при необходимости заместители, алкиламиноалкокси- или циклоалкиламиноалкоксигруппу или сульфонамидную группу; полициклический арил представляет собой полициклическую ароматическую систему, имеющую при необходимости заместители, содержащую в цикле от 5 до 14 членов и предпочтительно от 5 до 10 членов и включающую в себя от 2 до 10 циклов, из которых по меньшей мере один из циклов является ароматическим. В качестве примеров полициклических арилов можно назвать ацеантрилен, антрацен,азулен, коронен, рубицен, нафталин; полициклический арил может иметь заместители, которые могут представлять собой, например, один или несколько атомов галогенов, гидрокси-, циано-, трифторметилтио-, нитрогруппу, алкил, алкокси-, алкилтиогруппу, метилсульфонил, алкиламиноалкил или алкиламиноциклоалкил, имеющий при необходимости заместители, алкиламиноалкокси- или циклоалкиламиноалкоксигруппу или сульфонамидную группу; мостиковый цикл представляет собой бициклическую структуру, которая содержит согласно настоящему изобретению атом азота и в которой по меньшей мере 2 атома углерода соединены простой связью или углеродной цепью, которая может содержать 2 атома углерода. В качестве примера такой цикл соответствует формуле где q=1 или 2, а другие группы и индексы имеют определенные ранее значения; циклоалкил представляет собой насыщенный алифатический цикл, содержащий от 3 до 8 атомов углерода. В качестве примеров можно назвать циклопропил, метилциклопропил, циклобутил, циклопентил, циклогексил; галоген представляет собой фтор, хлор, бром или йод; галогеналкил представляет собой (C1-C6)алкил, имеющий в качестве заместителей от одного до трех атомов галогенов; гетероарил представляет собой моноциклическую ароматическую систему, содержащую от 5 до 14 членов и предпочтительно от 5 до 10 членов и включающий в себя от одного до нескольких гетероатомов, таких как атомы азота, кислорода или серы. Атомы азота могут находиться в структуре N-оксидов. Например, моноциклический гетероцикл может представлять собой пиран, пиразин, пиразол, пиридазин,пиридин, пиримидин, пиррол, изотиазол, изоксазол, фуран, имидазол, морфолин, тиофен, пиперазин,диазетидин, дигидропирролидин, пиперидин, азепин и т.п.; бициклический гетероцикл может представ-4 020984 лять собой изохинолин, птеридин, хроман и т.п.; трициклический гетероцикл может представлять собой фенантролин, ксантен и т.п.; полициклический гетероарил представляет собой полициклическую ароматическую систему, которая при необходимости имеет заместители, содержит в цикле от 5 до 14 членов и предпочтительно от 5 до 10 членов, включает в себя от 2 до 10 циклов, содержит, кроме того, от одного до нескольких гетероатомов, таких как атомы азота, кислорода или серы, по меньшей мере в одном из циклов и в которой по меньшей мере один из циклов является ароматическим. В качестве примеров полициклических гетероарилов можно назвать индол, бензофуран, бензимидазол, бензотиофен, бензотриазол, бензотиазол, бензоксазол, хинолин, изохинолин, индазол, хиназолин, фталазин, хиноксалин, нафтиридин, 2,3-дигидро 1 Н-индол, 2,3-дигидробензофуран, 2,3-дигидроинден, тетрагидрохинолин, тетрагидроизохинолин, тетрагидроизохиназолин; гетероциклоалкил представляет собой насыщенный цикл, имеющий при необходимости заместители, содержащий от 3 до 8 атомов и включающий в себя от одного до нескольких гетероатомов, таких, как атомы азота, кислорода или серы, по меньшей мере в одном из циклов или несколько гетероатомов, являющихся одинаковыми или различающимися между собой. Например, гетероциклоалкил может представлять собой пирролидин, морфолин, пиперазин, диазетидин, дигидропирролидин, пиперидин, пиперадин, азепан, имидазолидин, тиоморфолин, тетрагидропиран, тетрагидротиопиран, пиперазин, диазепан и т.п.; гидроксигруппа представляет собой группу -OH; нитрогруппа представляет собой группу -NO2; оксогруппа представляет собой -C(О)-; сульфонамидная группа представляет собой группу, соответствующую формуле SO2-N-алкил илиSO2-N-циклоалкил, причем алкил и циклоалкил имеют определенные ранее значения; трифторметилтиогруппа соответствует формуле -S-CF3. Кроме того, в настоящем описании принято, что в случае, когда атом или группа имеет или при необходимости может иметь один или несколько заместителей в виде определенных групп или атомов,заместители могут быть одинаковыми или различающимися между собой и при необходимости могут быть связаны с одним и тем же атомом или с разными атомами. Среди соединений, являющихся объектами настоящего изобретения, можно назвать группу соединений формулы (I), в которой А представляет собой арил, предпочтительно фенил, или гетероарил,предпочтительно пиридил, а все другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений формулы (I), в которой q=0, m и n по отдельности равны 1, а все другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений формулы (I), в которой R2 представляет собой (C1-C6)алкил, предпочтительно метил, имеющий в качестве заместителя-NHC(O)Rb, причем Rb и другие заместители и индексы имеют значения, определенные для соединений общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений общей формулы(I), в которой R2 представляет собой -ORa, причем Ra и все другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений общей формулы(I), в которой R2 представляет собой атом галогена, или цианогруппу, или атом водорода, или гидроксил,или (C1-C6)алкил, имеющий при необходимости в качестве заместителя -NH2 или -NHC(O)Rb, причем Rb и другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений общей формулы(I), в которой А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0,n и m по отдельности равны 1, R2 представляет собой -ORa, причем Ra и другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений общей формулы(I), в которой А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0,n и m по отдельности равны 1, р равно 2, одна из групп R2 представляет собой -ORa, а другая группа R2 представляет собой атом галогена, причем Ra и другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. Среди соединений по настоящему изобретению можно назвать группу соединений общей формулы(I), в которой А означает фенил, R1 означает -C(O)R, где R представляет собой атом водорода, q равно 0,n и m по отдельности равны 1, р=1, R2 означает метил, имеющий в качестве заместителя -NH-CO-Rb,причем Rb и другие заместители и индексы имеют значения, определенные для общей формулы (I), определенной ранее. В соединениях формулы (I) группа R2 предпочтительно находится в положении 6 ядра 2,4-диоксо-5 020984 1,2,3,4-тетрагидрохиназолина. В соединениях формулы (I) в положении 7 ядра 2,4-диоксо-1,2,3,4 тетрагидрохиназолина также может находиться группа R2. Группы R2 в положении 6 и 7 могут быть одинаковыми или различающимися. В соединениях формулы (I) p предпочтительно равно 1 или 2. Соединения общей формулы (I) могут находиться в виде оснований, гидратов, сольватов, изомеров или их смесей. В предпочтительном варианте в случае, когда p'=2, обе группы R3 находятся в положении 3 и 4 ядра и могут отличаться друг от друга. Комбинации групп соединений по настоящему изобретению, упомянутых ранее, также составляют часть настоящего изобретения. В качестве примеров предпочтительных соединений по настоящему изобретению можно назвать следующие соединения: Соединения по настоящему изобретению могут быть получены способами, поясненными на приведенных далее схемах 1-4. В последующем тексте под уходящей группой понимают группу, которая может быть легко замещена посредством разрыва гетеролитической связи с уходом электронной пары. Такая группа также может быть легко замещена другой группой, например по реакции замещения. Такими уходящими группами являются, например, галогены или активированная гидроксигруппа, такая как мезилатная, тозилатная,трифлатная и т.д. Примеры уходящих групп, а также информация по их получению приведены в "Advanced Organic Chemistry", J. March, 3rd Edition, Wiley Interscience, p. 310-316. Под защитной группой PG понимают группу, препятствующую проявлению реакционной способности функциональной группы или реакционного центра во время химической реакции, которая может затрагивать их, и позволяющую воспроизводить исходную молекулу после ее отщепления способами,известными специалистам в данной области техники. Под группой, временно защищающей амины или спирты, понимают защитные группы, такие как группы, описанные в Protective Groups in Organic Synthesis, Greene T.W. et Wuts P.G.M., Ed. Willey Intersciences, 1999, и в Protecting Groups, Kocienski P.J., 1994, Georg Thieme Verlag. В качестве временных защитных групп можно назвать, например, группы, защищающие амины, такие, как бензильные, карбаматные группы (такие как трет-бутилоксикарбонильная группа, отщепляемая в кислой среде, бензилоксикарбонильная группа, отщепляемая гидрогенолизом); группы, временно защищающие карбоновые кислоты, такие, как группы алкиловых сложных эфиров (такие как метиловые,этиловые или трет-бутиловые группы, гидролизуемые в щелочной или кислой среде) и гидрогенолизуемые группы бензиловых сложных эфиров; группы, временно защищающие спирты или фенолы, такие,как группы тетрагидропираниловых, метилоксиметиловых или метилэтоксиметиловых, трет-бутиловых и бензиловых простых эфиров; группы, временно защищающие карбонильные производные, такие, как группы линейных или циклических ацеталей, такие как, например, 1,3-диоксан-2-ил или 1,3-диоксолан 2-ил; также можно сослаться на хорошо известные общие способы, описанные в издании "ProtectiveGroups", упомянутом ранее. В зависимости от случая специалисты в данной области техники могут выбирать приемлемые защитные группы. Соединения формулы (I) могут содержать группы-предшественники других функциональных групп, получаемых в дальнейшем осуществлением одной или нескольких других стадий. Указанные на приведенных далее общих схемах синтеза исходные вещества и реактивы, способы получения которых не описаны, имеются в продаже или описаны в литературе, или могут быть получены способами, описанными в данном тексте или известными специалистам в данной области техники. Чистые энантиомеры соединений по настоящему изобретению могут быть получены исходя из энантиомерно чистых предшественников или хроматографией на хиральных фазах, или, в случае, когда соединения содержат кислотные группы или аминогруппы, селективной кристаллизацией диастереоизомерных солей, получаемых взаимодействием соединений (I) с хиральными аминами или кислотами соответственно. Соединения общей формулы (I) могут быть получены согласно приведенным далее схемам 1-4. Из соображений наглядности принято, что группа R4 представляет собой атом водорода, р и р' равны 1 и 2 соответственно, а группы R2 и R3 зафиксированы соответственно указанному на схемах. Однако подразумевается, что R4 может иметь значения, определенные для общей формулы (I), R2 и R3 могут находиться в положениях, указанных для общей формулы (I), a p и р' могут иметь значения, определенные для общей формулы (I). Пути синтеза, описанные далее, служат только для пояснения и ни в коем случае не являются ограничительными. Специалисты в данной области техники смогут без затруднений применять приведенные далее указания в отношении соединений формулы (I), в которых R, R1, R2, R3, R4, Ra, Rb, Rc, m, n, p, p' иq имеют значения, определенные для общей формулы (I). Согласно схеме 1 соединение формулы (IV) получают по реакции восстановительного аминирования, приводя во взаимодействие соединение формулы (II), в которой R' представляет собой (C1-C6)алкил,a R2 имеет значения, определенные для соединений формулы (I), с соединением формулы (III) в кислой среде и в присутствии восстанавливающего агента, такого как триацетоксиборогидрид натрия. ГруппаGP соединения формулы (III) представляет собой группу, которая защищает аминогруппу и преимущественно может представлять собой трет-бутилоксикарбонил (boc). Затем полученное таким образом соединение формулы (IV) ацилируют способами, хорошо известными специалистам в данной области техники, алкил- или арилхлорформиатом для получения соединения формулы (V), в которой R" представляет собой (C1-C6)алкил или замещенный арил. Реакция гидролиза в щелочной среде позволяет получить соединения формулы (VI), которые при реакции сочетания с соединением формулы (VII), в которой R3 имеют значения, определенные для соединений формулы (I), образуют соединения формулы (VIII). Реакция межмолекулярной циклизации в щелочной среде позволяет получить производные хиназолиндиона формулы (IX). Затем группу GP, защищающую аминогруппу, отщепляют, например, в кислой среде в случае, когда GP представляет собой boc, для получения соединений формулы (Ia), которые по реакции ацилирования образуют соединения формулы (Ib). Соединения формулы (Ia) представляют собой соединения формулы (I) и могут служить в качестве промежуточных соединений для получения других соединений формулы (I), таких как соединения формулы (Ib). Соединения формулы (I), в которых R2 представляет собой -ORa, где Ra имеет значения, определенные для соединений формулы (I), соответствуют формуле (Id). Они могут быть получены исходя из соединений формулы (X) согласно приведенной далее схеме 2. Соединения формулы (Ic), полученные гидрогенолизом соединений формулы (X), вводят, например, в реакцию алкилирования с алкилирующим агентом типа Ra-X, где Ra имеет значения, определенные для соединений формулы (I), а X представляет собой уходящую группу (например, такую как атом галогена), в присутствии основания, такого как карбонат цезия (Cs2CO3), или также в реакцию Мицунобу (Synthesis, 1981, 1) со спиртом типа Ra-OH, где Ra имеет значения, определенные для соединений формулы (I), для получения соединений формулы (Id). Соединения формулы (X), а также соединения формулы (Ic) представляют собой соединения формулы (I) и могут служить в качестве промежуточных соединений для получения других соединений формулы (I), таких как соединения формулы (Id). Схема 2 Альтернативным образом, соединения формулы (Id) могут быть получены способом, описанным на схеме 3. Соединения формулы (XII) получают реакцией нуклеофильного ароматического замещения, в которой используют соединение формулы (XI), где R' имеет определенные ранее значения, и спирт типаRa-OH, где Ra имеет значения, определенные для соединений формулы (I), в присутствии основания. Восстановление нитрогруппы соединений формулы (XII) ведет к образованию соответствующих производных анилина (XIII). Реакция восстановительного аминирования соединения формулы (III), в которойGP означает группу, защищающую аминогруппу, такую, как, например, boc, ведет к образованию соединений формулы (XIV). Получение соединений формулы (XV) осуществляют взаимодействием соединения формулы (XIV) с изоцианатом калия (KNCO) в кислой среде. Реакция межмолекулярной циклизации в щелочной среде позволяет получить соединения формулы (XVI). Защитную группу GP отщепляют способами, хорошо известными специалистам в данной области техники, для получения соединений формулы (XVII). Реакция ацилирования ведет к образованию соединений формулы (XVIII). Наконец,соединения формулы (Id) получают как реакцией алкилирования с производным типа (XIX), где X представляет собой уходящую группу, такую как атом галогена, в присутствии основания, такого как, например, карбонат цезия, так и по реакции Мицунобу с бензиловым спиртом типа (XX). В соединениях (XIX) и (XX) R3 имеет определенные ранее значения. Схема 3 Соединения формулы (Ie) и (If), в которых R2 более предпочтительно представляет собой группу типа -CH2-NHC(О)Rb, где Rb имеет значения, определенные для соединений формулы (I), могут быть получены согласно приведенной далее схеме 4. Подразумевается, что показанная на схеме 3 группа R2 имеет тип -O-Ra и находится в положении 6 структуры хиназолиндиона (см., например, соединение (XVIII, но также возможно наличие второй группы R2, имеющей значения, определенные для общей формула (I), в положении 7 той же структуры хиназолиндиона. Восстановление нитрогруппы соединений типа (XXI), в которых R' и GP' имеют определенные ранее значения, причем GP' преимущественно представляет собой boc, ведет к образованию соответствующих производных анилина (XXII), которые по реакции восстановительного аминирования, взаимодействуя в кислой среде и преимущественно в присутствии восстанавливающего агента, такого как триацетоксиборогидрид натрия, с соединением формулы (III), в которой GP представляет собой бензилоксикарбонильную группу, защищающую аминогруппу, образуют соединения формулы (XXIII). Реакция ацилирования с алкил- или арилхлорформиатом, в котором R" представляет собой (C1-C6)алкил или замещенный арил, ведет к образованию соединений формулы (XXIV). Аналоги хиназолиндиона формулы(XXV) могут быть получены гидролизом в щелочной среде с последующим осуществлением сочетания с соединением формулы (VII), в которой R3 имеет значения, определенные для соединений формулы (I), и затем межмолекулярной циклизации в щелочной среде. Далее группу GP' (предпочтительно boc) отщепляют в кислой среде для получения соединений формулы (XXVI), которые при ацилировании образуют соединения формулы (XXVII), в которых Rb имеет значения, определенные для соединений формулы (I). Защитную группу GP (XXVII) отщепляют гидрогенолизом для получения соединений формулы (Ie). На конечной стадии соединения формулы (If) получают ацилированием соединений формулы (Ie). Схема 4 Разумеется, специалисты в данной области техники могут, кроме того, выбирать, в зависимости от располагаемых ими сведений и литературных источников, другие приемлемые защитные группы, обеспечивающие введение любых групп, описанных для общей формулы (I). В случае, когда соединение формулы (I) содержит мостиковый цикл, оно может быть получено произвольным образом по одному из путей синтеза, описанных ранее. В приведенных далее методиках и примерах описано получение некоторых соединений по настоящему изобретению. Эти методики и примеры не являются ограничительными и приведены только для пояснения настоящего изобретения. В приведенных далее методиках и примерах: масс-спектры записаны на квадрупольном спектрометре типа Platform LCZ (WATERS) или типа ZQ 4000 (WATERS) в режиме положительной ионизации электрораспылением; спектры ЯМР (ядерного магнитного резонанса) записаны на спектрометре с фурьепреобразованием (BRUKER) при температуре 300 К (с подавлением протонов, способных к обмену); с (с) - синглет; д (d) - дублет; м (m) - мультиплет; ушир. (br) - уширенный пик (широкий пик); т (t) - триплет; кв (q) - квартет; ДМСО-d6 (DMSO-d6) - дейтерированный диметилсульфоксид;CDCl3 - дейтерированный хлороформ. Смеси растворителей количественно охарактеризованы объемными соотношениями. Спектры ЯМР и масс-спектры подтверждают структуры соединений, полученных согласно приведенным далее примерам. В приведенных далее примерах использованы следующие сокращения:NEt3 - триэтиламин; ТФУ (TFA) - трифторуксусная кислота. Примеры В приведенных далее примерах описано получение некоторых соединений по настоящему изобретению. Данные примеры не являются ограничительными и приведены только для пояснения настоящего изобретения. Номера соединений в приведенных примерах соответствуют номерам в таблице, приведенной далее для пояснения химической структуры и физических свойств некоторых соединений по настоящему изобретению. Пример 1. Соединение 6. ПолучениеNaBH(OAc)3 в 10 мл АсОН. Такой же синтез повторяют с 2 другими порциями по 2 г метил-2-амино-5(бензилокси)бензоата. Объединяют 3 фракции реакционной смеси. Растворяют их в AcOEt. Органическую фракцию промывают водой, насыщенным раствором NH4Cl, насыщенным раствором NaHCO3, сушат над Na2SO4, фильтруют и растворитель выпаривают при пониженном давлении. Остаток хроматографируют на силикагеле, элюируя смесью AcOEt/гептан (от 5/95 до 30/70 об./об.), с получением 10,2 г требуемого соединения. Стадия 1.2. 1,1-Диметилэтил-4-[4-(бензилокси)-2-(метоксикарбонил)фенил][(2-метилпропокси)карбонил]аминопиперидин-1-карбоксилат Микроволновым излучением в течение 30 мин при 80 С нагревают смесь 2 г 1,1-диметилэтил-4-[4(бензилокси)-2-(метоксикарбонил)фенил]аминопиперидин-1-карбоксилата, полученного на стадии 1.1,0,87 мл DIEA, 1,78 мл IBCF и 1 г NaOH в 10 мл ДХЭ. Такой же синтез повторяют с 4 другими порциями по 2 г 1,1-диметилэтил-4-[4-(бензилокси)-2-(метоксикарбонил)фенил]аминопиперидин-1 карбоксилата. Объединяют 5 фракций реакционной смеси. Растворяют в AcOEt, фильтруют и фильтрат упаривают при пониженном давлении. Остаток хроматографируют на силикагеле, элюируя смесью AcOEt/гептан (от 10/90 до 50/50 об./об.), с получением 9,3 г требуемого соединения. Стадия 1.3. Натриевая соль 5-(бензилокси)-2-(1-[(1,1-диметилэтокси)карбонил]пиперидин-4-ил[(2 метилпропокси)карбонил]амино)бензойной кислоты В течение 3 ч при 100 С нагревают смесь 9,3 г 1,1-диметилэтил-4-[4-(бензилокси)-2(метоксикарбонил)фенил][(2-метилпропокси)карбонил]аминопиперидин-1-карбоксилата, полученного на стадии 1.2, 34,4 мл 2 н. раствора NaOH в 57 мл МеОН. Раствор упаривают при пониженном давлении и прибавляют ДХМ. Сушат над Na2SO4, фильтруют и растворитель выпаривают при пониженном давлении с получением 8,7 г требуемого соединения. В течение 15 мин при Ткомн перемешивают смесь 6 г натриевой соли 5-(бензилокси)-2-(1-[(1,1 диметилэтокси)карбонил]пиперидин-4-ил[(2-метилпропокси)карбонил]амино)бензойной кислоты, полученной на стадии 1.3, и 4,42 г DIEA в 250 мл ДМФА. Прибавляют 6,48 г HBTU и перемешивают в течение 30 мин. Прибавляют 2,48 г вератриламина и реакционную смесь перемешивают в течение 48 ч. Смесь упаривают при пониженном давлении, остаток растворяют в AcOEt, промывают насыщенным раствором NH4Cl, насыщенным раствором NaHCO3, сушат над Na2SO4, фильтруют и растворитель выпаривают при пониженном давлении. Остаток хроматографируют на силикагеле, элюируя смесью Микроволновым излучением в течение 30 мин при 110 С нагревают смесь 2,5 г 1,1-диметилэтил-4[4-(бензилокси)-2-[(3,4-диметоксибензил)карбамоил]фенил(изобутоксикарбонил)амино]пиперидин-1 карбоксилата, полученного на стадии 1.4, и 7,4 г NaOH в 18,5 мл ДХЭ. Такой же синтез повторяют с 2 другими порциями по 2,5 г 1,1-диметилэтил-4-[4-(бензилокси)-2-[(3,4-диметоксибензил)карбамоил]фенил(изобутоксикарбонил)амино]пиперидин-1-карбоксилата. Объединяют 3 фракции реакционной смеси. Растворяют в ДХМ, промывают водой, сушат над Na2SO4, фильтруют и растворитель выпаривают при пониженном давлении с получением 6,6 г требуемого соединения. Стадия 1.6. 6-(Бензилокси)-3-(3,4-диметоксибензил)-1-пиперидин-4-илхиназолин-2,4(1 Н,3 Н)-дион В течение 2 ч при Ткомн перемешивают смесь 3,5 г 1,1-диметилэтил-4-[6-(бензилокси)-3-(3,4 диметоксибензил)-2,4-диоксо-3,4-дигидрохиназолин-1(2 Н)-ил]пиперидин-1-карбоксилата, полученного на стадии 1.5, и 25 мл ТФУ в 50 мл ДХМ. Смесь нейтрализуют посредством K2CO3. Затем смесь фильтруют и фильтрат упаривают при пониженном давлении. Растворяют в ДХМ, промывают насыщенным раствором NaHCO3 и затем 8%-м раствором NaOH. Сушат над Na2SO4, фильтруют и растворитель выпаривают при пониженном давлении с получением 2,67 г требуемого соединения.
МПК / Метки
МПК: A61K 31/517, A61K 9/00, A61P 9/00
Метки: производных, терапевтическое, применение, заболеваниях, хиназолиндиона, сердечно-сосудистых
Код ссылки
<a href="https://eas.patents.su/30-20984-terapevticheskoe-primenenie-proizvodnyh-hinazolindiona-pri-serdechno-sosudistyh-zabolevaniyah.html" rel="bookmark" title="База патентов Евразийского Союза">Терапевтическое применение производных хиназолиндиона при сердечно-сосудистых заболеваниях</a>
Предыдущий патент: Газовыделяющие композиции, уменьшающие вязкость нефти, для возбуждения продуктивного пласта нефтяного коллектора
Следующий патент: Тостер с фиксатором нагревательных пластин в заданных положениях
Случайный патент: Композиции, предназначенные для хранения эритроцитов