Конъюгаты цитотоксинов
Номер патента: 19962
Опубликовано: 30.07.2014
Авторы: Пассмор Дэвид Б., Чэнь Лян, Чжан Цян, Герлавэ Винсен, Суфи Билал, Гангвар Санджив
Формула / Реферат
1. Соединение формулы
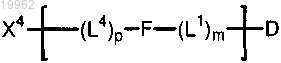
в которой m равно 0;
F представляет собой линкер, содержащий структуру
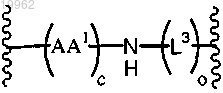
где (АА1)с представляет собой пептидную последовательность, выбранную из группы, состоящей из Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID NO: 1), β-Ala-Leu-Ala-Leu (SEQ ID NO: 2) и Gly-Phe-Leu-Gly (SEQ ID NO: 3);
L3 представляет собой спейсерную группу формулы
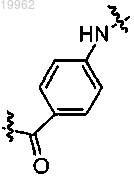
карбоксильная группа L3 образует амидную связь с боковой функциональной аминогруппой D;
о равно 1;
L4 представляет собой линкерную группу, где L4 содержит
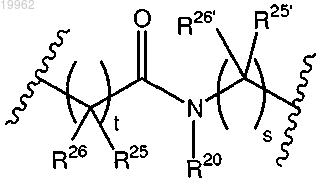
непосредственно присоединенный к N-концу (АА1)c,
где R20 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;
каждый из R25, R25', R26 и R26' независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;
s и t независимо равны целым числам от 1 до 6;
р представляет собой 1;
X4 представляет собой группу, выбранную из R29, COOR29, C(O)NR29 и C(O)NNR29, где R29 представляет собой группу, выбранную из замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного гетероарила, N-гидроксисукцинимидных эфиров, малеимидов;
D содержит структуру
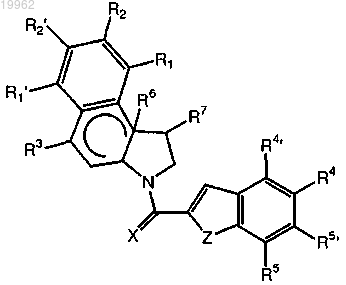
где X представляет собой О;
Z представляет собой NR23;
R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;
R1 представляет собой Н, замещенный или незамещенный низший алкил, C(O)R8 или CO2R8, где R8 представляет собой группу, выбранную из NR9R10 и OR9, где R9 и R10 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила и замещенного или незамещенного гетероалкила;
R1' представляет собой Н, замещенный или незамещенный низший алкил или C(O)R8, где R8 представляет собой группу, выбранную из NR9R10 и OR9, где R9 и R10 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила и замещенного или незамещенного гетероалкила;
R2 представляет собой Н, или замещенный или незамещенный низший алкил, или незамещенный гетероалкил, или циано- или алкоксигруппу;
R2' представляет собой Н, или замещенный или незамещенный низший алкил, или незамещенный гетероалкил;
R3 представляет собой группу, выбранную из группы, состоящей из (=O), SR11, NHR11 и OR11, где R11 представляет собой группу, выбранную из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, монофосфатов, дифосфатов, трифосфатов, сульфонатов, ацила, C(O)R12R13, C(O)OR12, C(O)NR12R13, P(O)(OR12)2, С(O)CHR12R13, SR12 и SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, где R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;
R4, R4', R5 и R5' представляют собой группы, независимо выбранные из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NHC(O)R15, ОС(О)NR15R16, ОС(О)OR15, C(O)R15, SR15, OR15, CR15=NR16 и О(СН2)nN(CH3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп;
n равно целому числу от 1 до 20;
R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила;
R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;
R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;
R7 представляет собой СН2-Х1 или -СН2-, присоединенные в указанном циклопропильном кольце к R6, где X1 представляет собой уходящую группу;
по меньшей мере один из R4, R4', R5, R5', R15 или R16 связывает указанное лекарственное средство с F;
или его фармацевтически приемлемая соль,
где алкил обозначает углеводородный радикал с неразветвленной или разветвленной цепью, содержащий от 1 до 10 атомов углерода;
низший алкил обозначает углеводородный радикал с неразветвленной или разветвленной цепью, содержащий от 1 до 6 атомов углерода;
гетероалкил обозначает углеводородный радикал с неразветвленной или разветвленной цепью, содержащий от 1 до 10 атомов углерода и как минимум один гетероатом, выбранный из группы, состоящей из О, N, Si и S, где атомы азота, углерода и серы необязательно могут быть окисленными и гетероатом азота необязательно может быть четвертичным;
ацил обозначает группу, присоединенную к и занимающую валентность карбонильного атома углерода, которая прямо или косвенно присоединена к полициклическому ядру;
арил обозначает замещенный или незамещенный полиненасыщенный, ароматический, углеводородный заместитель, который может представлять собой одинарное кольцо или несколько колец, конденсированных или связанных ковалентной связью;
гетероарил обозначает арильную группу, которая содержит от 1 до 4 гетероатомов, выбранных из N, О и S, где атомы азота, углерода и серы необязательно окислены и атом(ы) азота необязательно являет(ют)ся четвертичным(и);
гетероциклоалкил обозначает циклические версии замещенного или незамещенного алкила и замещенного или незамещенного гетероалкила;
заместитель представляет собой одну или несколько разнообразных групп, выбранных из OR', =O, =NR', =N-OR', -NR'R", -SR', -галогена, -SiR'R"R"', -OC(O)R', -C(O)R', -CO2R', -CONR'R", -OC(O)NR'R",
-NR"C(O)R', -NR'-C(O)NR"R"', -NR"C(O)2R', -NR-C(NR'R"R'")=NR"", -NR-C(NR'R")=NR'", -S(O)R', -S(O)2R', -S(O)2NR'R", -NRSO2R', -CN и -NO2, где каждый из R', R", R"' и R"" независимо обозначает водород, замещенные или незамещенные гетероалкильные, замещенные или незамещенные арильные, замещенные или незамещенные алкильные, алкокси или тиоалкокси или арилалкильные группы.
2. Соединение по п.1, отличающееся тем, что (АА1)c представляет собой Val-Cit или Val-Lys.
3. Соединение по п.1, отличающееся тем, что R25, R25', R26 и R26' независимо представляют собой Н или низший алкил.
4. Соединение по п.1, отличающееся тем, что s и t независимо представляют собой 1 или 2.
5. Соединение по п.1, отличающееся тем, что R20 представляет собой Н или низший алкил.
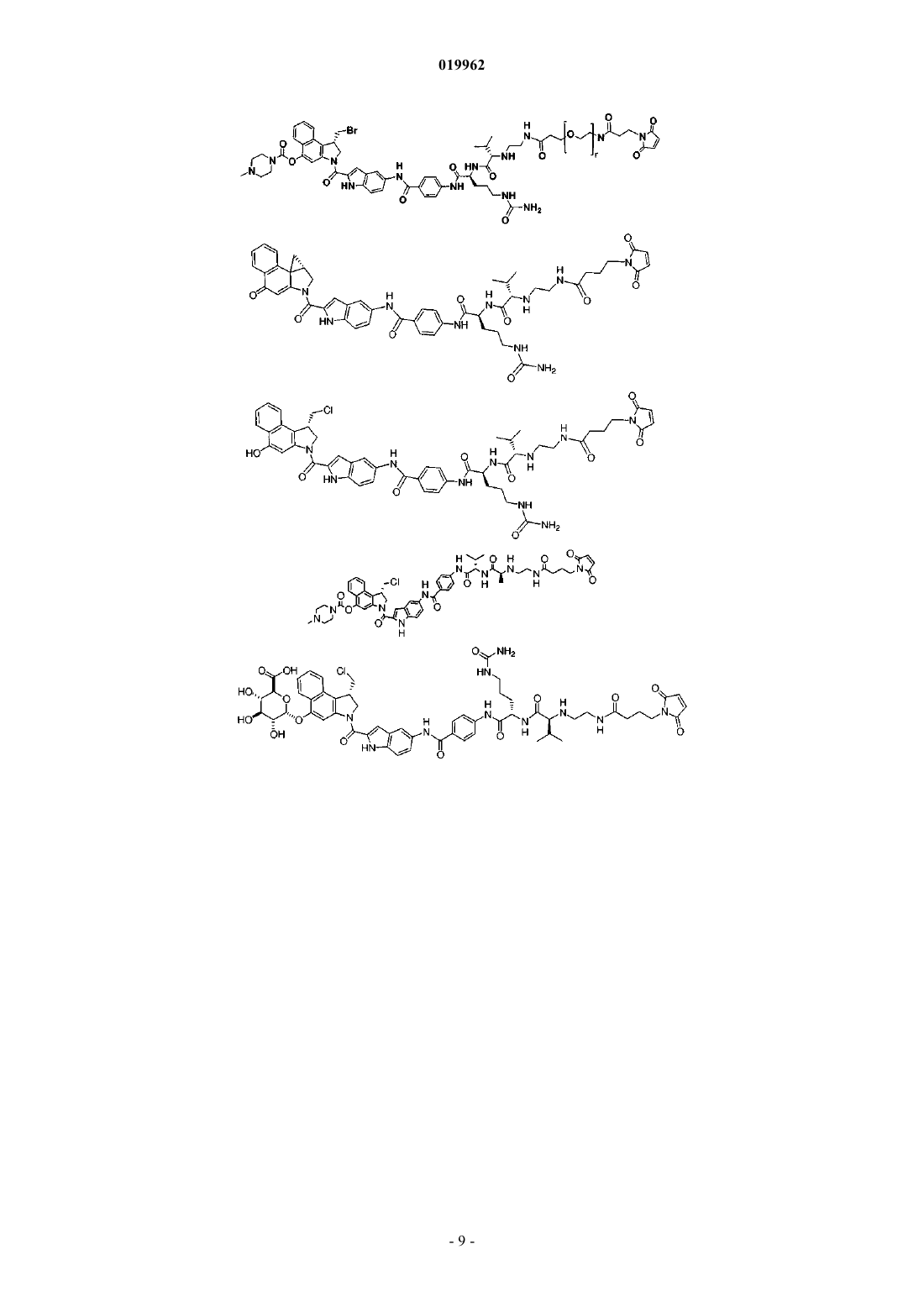
6. Соединение по п.1, выбранное из
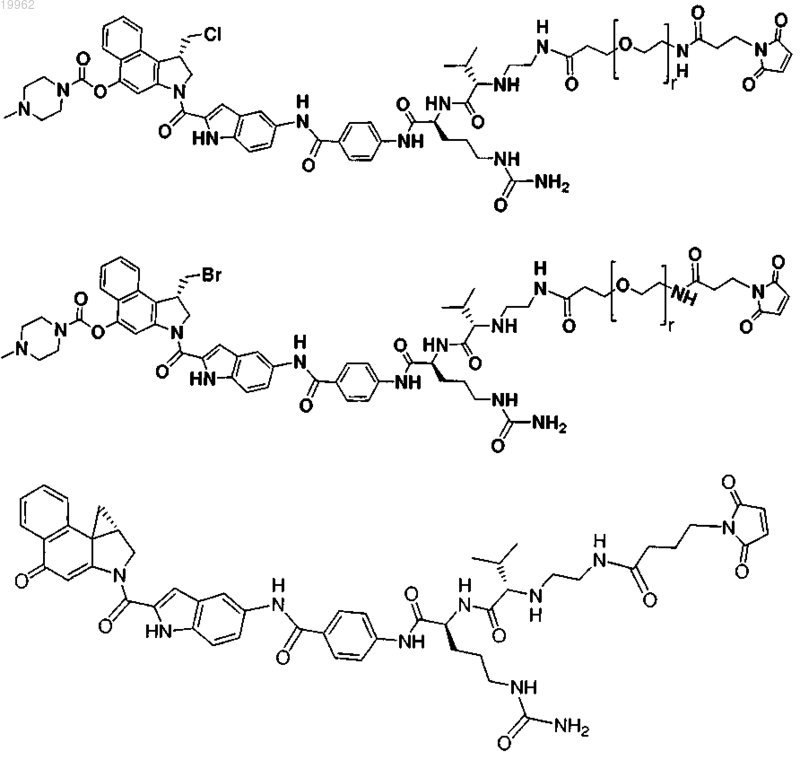
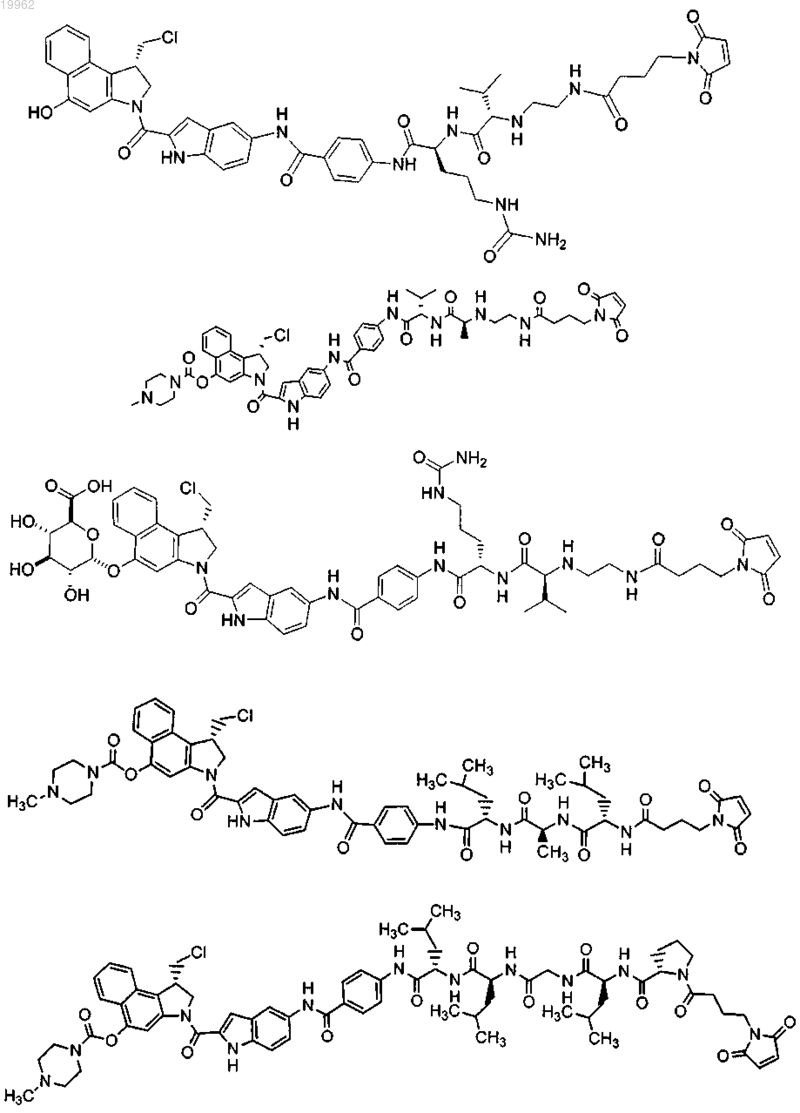
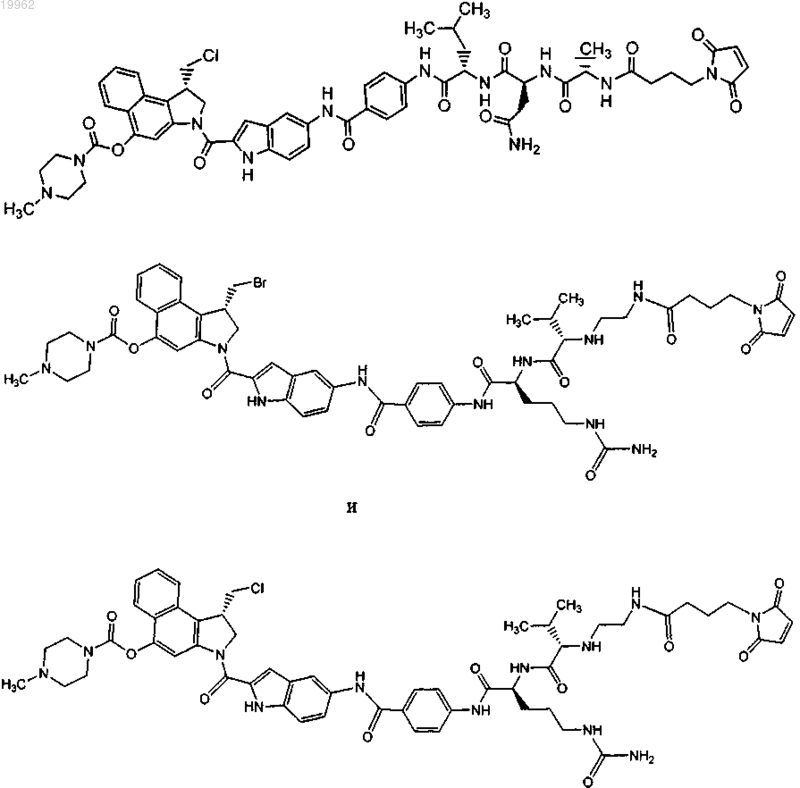
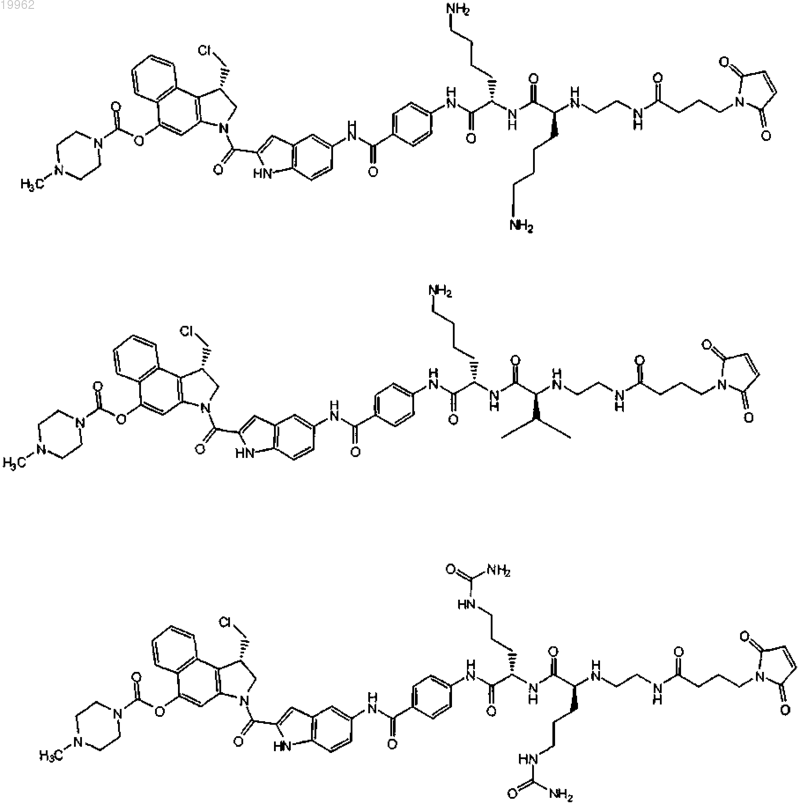
где r равно целому числу от 0 до 24.
7. Соединение по п.1, отличающееся тем, что R29 выбирают из группы, состоящей из N-гидроксисукцинимидных эфиров и малеимидов.
Текст
X4, L4, p, F, L1, D, m определены в формуле изобретения. Указанные конъюгаты могут быть избирательно доставлены к целевому месту действия в активной форме, после чего расщепляются для высвобождения активного лекарственного средства. Перекрестная ссылка на родственные заявки Заявка на данное изобретения испрашивает приоритет предварительной патентной заявки США 60/882461, поданной 28 декабря 2006 г., и предварительной патентной заявки США 60/991300, поданной 30 ноября 2007 г., преимущества которых, таким образом, заявляются в соответствии со Сводом законов США 35119, и раскрытие которых включено в данное описание путем ссылки во всей его полноте. Область изобретения В настоящем изобретении предлагаются линкеры и расщепляемые субстраты, которые присоединены к лекарственному средству и лиганду и расщепляются in vivo. Линкеры и расщепляемые субстраты применяются в существующих пролекарствах и конъюгатах цитотоксинов по изобретению, а также в качестве других диагностических и терапевтических фрагментов. Предпосылки изобретения Многие терапевтические средства, в частности те, которые являются особенно эффективными в химиотерапии рака, часто проявляют острую токсичность in vivo, особенно токсичность в отношении костного мозга и слизистых оболочек, а также хроническую сердечную и неврологическую токсичность. Такая высокая токсичность может ограничить их применение. Разработка более безопасных и более специфических терапевтических средств, особенно противоопухолевых средств, желательна с точки зрения повышения эффективности против клеток опухоли, а также уменьшения частоты и тяжести побочных эффектов таких средств (токсичность, разрушение не опухолевых клеток и т.п.). Другое затруднение в случае существующих терапевтических средств состоит в их субоптимальной стабильности в плазме. Добавление функциональных групп для стабилизации таких соединений приводило к существенному снижению активности. Соответственно, желательно идентифицировать пути стабилизации соединений при сохранении приемлемых уровней терапевтической активности. Хотя поиск более селективных цитотоксических средств ведется чрезвычайно активно в течение многих десятилетий, ограничивающая дозу токсичность (т.е. нежелательная активность цитотоксинов в нормальных тканях) представляет собой одну из основных причин неуспешной терапии рака. Например,известно, что СС-1065 и дуокармицины являются чрезвычайно мощными цитотоксинами. СС-1065 был изначально выделен из Streptomyces zelensis в 1981 г. компанией Upjohn (Hanka et al.,J. Antibiot. 31: 1211 (1978); Martin et al., J. Antibiot. 33: 902 (1980); Martin et al., J. Antibiot. 34: 1119(1981, было обнаружено, что он обладает мощной противоопухолевой и противомикробной активностью как in vitro, так и в экспериментах на животных (Li et al., Cancer Res. 42: 999 (1982. СС-1065 связывается с двухцепочечной B-DNA в пределах незначительного желобка (Swenson et al., Cancer Res. 42: 2821 (1982 с предпочтительной последовательностью 5'-d(A/GNTTA)-3' и 5'-d(AAAAA)-3' и алкилирует положение N3 3'-аденина расположенной слева частью молекулы CPI (Hurley et al., Science 226: 843(1984. Несмотря на мощную и противоопухолевую активность с широким спектром действия, СС-1065 не может применяться у человека, поскольку вызывает отсроченную гибель экспериментальных животных. Многие аналоги и производные СС-1065 и дуокармицинов известны из уровня техники. Исследования структуры, способов синтеза и свойств многих соединений были рассмотрены, например, Boger etal., Angew. Chem. Int. Ed. Engl. 35: 1438 (1996) и Boger et al., Chem. Rev. 97: 787 (1997). Группой в Kyowa Hakko Kogya Co., Ltd. был получен целый ряд производных СС-1065. См., например, патенты США 5101038, 5641780, 5187186, 5070092, 5703080, 5070092, 5641780, 5101038,5084468 и опубликованную заявку РСТ WO 96/10405, а также опубликованную европейскую заявку 0537575 А 1. Компания Upjohn (Pharmacia Upjohn) также активно действует в направлении получения производных СС-1065. См., например, патенты США 5739350, 4978757, 5332837 и 4912227. Исследования также фокусируются на разработке новых терапевтических средств, которые существуют в форме пролекарств, соединений, способных к превращению в лекарства (терапевтически активные соединения) in vivo при определенных химических или ферментных модификациях их структуры. Для целей уменьшения токсичности такое превращение предпочтительно ограничивается местом действия или целевой тканью вместо кровеносной системы или не целевой ткани. Однако даже пролекарства создают проблемы, поскольку многие характеризуются низкой стабильностью в крови и сыворотке, в результате присутствия ферментов, которые разлагают или активизируют пролекарства до того, как пролекарства достигнут целевых участков в пределах организма больного. В Bristol-Myers Squibb описаны конкретные, расщепляемые лизосомальными ферментами конъюгаты противоопухолевых лекарственных средств. См., например, патент США 6214345. В указанном патенте предлагается аминобензилоксикарбонил. В Seattle Genetics были опубликованы патентные заявки США 2003/0096743 и 2003/0130189, в которых описаны п-аминобензиловые эфиры в средствах доставки лекарственных средств. Линкеры, описанные в указанных заявках, ограничиваются композициями аминобензиловых эфиров. Другими группами также описаны линкеры. См., например, de Groot et al., J. Med. Chem. 42, 5277WO 02/083180; Carl et al., J. Med. Chem. Lett. 24, 479, (1981); Dubowchik et al., BioorgMed. Chem. Lett. 8, 3347 (1998). Такие линкеры включают спейсер аминобензилового эфира, удлиненный электронный каскад и системы циклизации спейсера, циклизацию элиминационных спейсеров, таких какw-аминоаминокарбонилы и линкер п-аминобензилоксикарбонил. Стабильность цитотоксических лекарственных средств, в том числе стабильность in vivo, попрежнему представляет собой важную проблему, требующую решения. Кроме того, токсичность многих соединений делает их менее применимыми, таким образом, необходимы композиции, которые уменьшают токсичность лекарственного средства, например образование расщепляемого пролекарства. Таким образом, несмотря на успехи в данной области, продолжает существовать потребность в разработке усовершенствованных терапевтических средств для лечения млекопитающих, в частности человека, более конкретно, цитотоксинов, которые проявляют высокую специфичность действия, сниженную токсичность и улучшенную стабильность в крови относительно известных соединений сходной структуры. Данное изобретение направленно на удовлетворение перечисленных потребностей. Краткое описание изобретения Данное изобретение относится к конъюгатам "лекарственное средство-лиганд", где лекарственное средство и лиганд связаны через пептидил или другой линкер, и к конъюгатам "лекарственное средстворасщепляемый ферментом субстрат". Указанные конъюгаты представляют собой мощные цитотоксины,которые могут быть избирательно доставлены к целевому месту действия в активной форме, после чего расщепляются для высвобождения активного лекарственного средства. Один из вариантов представляет собой соединение формулы в которой L1 представляет собой самоуничтожающийся линкер;m равно целому числу 0, 1, 2, 3, 4, 5 или 6; где АА 1 представляет одну или несколько групп, независимо выбранных из группы, состоящей из природных аминокислот и неприродных -аминокислот; с равно целому числу от 1 до 20;L2 представляет собой самоуничтожающийся линкер и содержит где каждый из R17, R18 и R19 независимо выбирают из Н, замещенного или незамещенного алкила,замещенного или незамещенного гетероалкила и замещенного или незамещенного арила,и w равно целому числу от 0 до 4; о равно 1;L4 представляет собой линкерную группу; р представляет собой 0 или 1;X4 представляет собой группу, выбранную из группы, состоящей из защищенных реакционноспособных функциональных групп, незащищенных реакционноспособных функциональных групп, определяемых меток и направляющих агентов; и где кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп; Е и G представляют собой группы, независимо выбранные из Н, замещенного или незамещенного-2 019962 алкила, замещенного или незамещенного гетероалкила, гетероатома, одинарной связи; или Е и G соединены с образованием кольцевой системы, выбранной из замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;R3 представляет собой OR11, где R11 представляет собой группу, выбранную из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, монофосфатов, дифосфатов, трифосфатов, сульфонатов, ацила, C(O)R12R13, С(О)OR12, C(O)NR12R13,P(O)(OR12)2, С(О)CHR12R13, SR12 и SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R4, R4', R5 и R5' представляют собой группы, независимо выбранные из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, ОС(О)OR15, C(O)R15, SR15, OR15, CR15=NR16 и О(СН 2)nN(СН 3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп;n равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;R7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6R , где X1 представляет собой уходящую группу,R11 связывает указанное лекарственное средство с L1, если он присутствует, или с F; или его фармацевтически приемлемая соль. Другой вариант представляет собой соединение формулы в которой L1 представляет собой самоуничтожающийся линкер;m равно целому числу 0, 1, 2, 3, 4, 5 или 6; где АА 1 представляет одну или несколько групп, независимо выбранных из группы, состоящей из природных аминокислот и неприродных -аминокислот; с равно целому числу от 1 до 20;L2 представляет собой самоуничтожающийся линкер; о равно 0 или 1;L4 представляет собой линкерную группу; р представляет собой 0 или 1;X представляет собой группу, выбранную из группы, состоящей из защищенных реакционноспособных функциональных групп, незащищенных реакционноспособных функциональных групп, определяемых меток и направляющих агентов; и где кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп; Е и G представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, гетероатома, одинарной связи; или Е и G соединены с образованием кольцевой системы, выбранной из замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, где R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы,содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R4, R4', R5 и R5' представляют собой группы, независимо выбранные из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, OC(O)OR15, C(O)R15, SR15, OR15, CR15=NR16 иO(CH2)nN(CH3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп,n равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов; как минимум один из R4, R4', R5 и R5' связывает указанное лекарственное средство с L1, если он присутствует, или с F и содержит где v равно целому числу от 1 до 6; каждый из R27, R27', R28 и R28' независимо выбирают из Н, замещенного или незамещенного алкила,замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца; иR7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6X1 представляет собой уходящую группу; или его фармацевтически приемлемая соль. Другой вариант представляет собой соединение формулы-4 019962 в которой L1 представляет собой самоуничтожающийся линкер;m равно целому числу 0, 1, 2, 3, 4, 5 или 6; где АА 1 представляет одну или несколько групп, независимо выбранных из группы, состоящей из природных аминокислот и неприродных -аминокислот; с равно целому числу от 1 до 20;L3 представляет собой спейсерную группу, включающую первичный или вторичный амин, или функциональную карбоксильную группу, где, если L3 присутствует, m равно 0 и амин L3 образует амидную связь с боковой функциональной карбоксильной группой D или карбоксильная группа L3 образует амидную связь с боковой функциональной аминогруппой D; о равно 0 или 1;L4 представляет собой линкерную группу, где L4 содержитR20 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила; каждый из R25, R25', R26 и R26' независимо выбирают из Н, замещенного или незамещенного алкила,замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;s и t независимо равны целым числам от 1 до 6; р представляет собой 1;X4 представляет собой группу, выбранную из группы, состоящей из защищенных реакционноспособных функциональных групп, незащищенных реакционноспособных функциональных групп, определяемых меток и направляющих агентов; и где кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп; Е и G представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, гетероатома, одинарной связи; или Е и G соединены с образованием кольцевой системы, выбранной из замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, где R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы,содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R4, R4', R5 и R5' представляют собой группы, независимо выбранные из группы, состоящей из Н, за-5 019962 мещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, OC(O)OR15, C(O)R15, SR15, OR15, CR15=NR16 и О(СН 2)nN(CH3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп,n равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;R7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6X1 представляет собой уходящую группу,как минимум один из R4, R4', R5, R5', R15 или R16 связывает указанное лекарственное средство с L1,если он присутствует, или с F; или его фармацевтически приемлемая соль. Дополнительный вариант представляет собой соединение, имеющее следующую структуру: в которой L1 представляет собой самоуничтожающийся спейсер;m равно целому числу 0, 1, 2, 3, 4, 5 или 6;X2 представляет собой расщепляемый субстрат; где кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп; Е и G представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, гетероатома, одинарной связи; или Е и G соединены с образованием кольцевой системы, выбранной из замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, где R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы,содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;R7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6X1 представляет собой уходящую группу;R4, R4', R5 и R5' представляют собой группы, независимо выбранные из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гете-6 019962 роарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, OC(O)OR15, C(O)R15, SR15, OR15, CR15=NR16 и О(СН 2)nN(CH3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп,n равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов; как минимум один из группы R4, R4', R5 и R5' связывает указанное лекарственное средство с L1, если он присутствует, или с X2 и выбирают из группы, состоящей из где R30, R30', R31 и R31' независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила; иv равно целому числу от 1 до 6; или его фармацевтически приемлемая соль. Другой вариант представляет собой соединение, имеющее следующую структуру: в которой кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп;Z и X независимо представляют собой группы, выбранные из О, S и NR23;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;SiR12R13R14, где R12, R13 и R14 представляют собой группы, независимо выбранные из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и замещенного или незамещенного арила, где R12 и R13, вместе с атомом азота или углерода, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы,содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;R7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6R , где X1 представляет собой уходящую группу;R5, R5' и R32 представляют собой группы, независимо выбранные из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоал-7 019962 кила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, OC(O)OR15, C(O)R15, SR15, OR15, CR15=NR16 иn равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов; или его фармацевтически приемлемая соль. Дополнительный вариант представляет собой соединение, имеющее следующую структуру: в которой кольцевая система А представляет собой группу, выбранную из замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклоалкильных групп;Z и X независимо представляют собой группы, выбранные из О, S и NR23;R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила;R4, R4', R5, R5' и R33 представляют собой группы, независимо выбранные из группы, состоящей из Н,замещенного алкила, незамещенного алкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR15R16, NC(O)R15, ОС(О)NR15R16, OC(O)OR15, C(O)R15, SR15, OR15, CR15=NR16 и О(СН 2)nN(CH3)2, или члены любой смежной пары, состоящей из R4, R4', R5 и R5', вместе с атомами углерода, к которым они присоединены, соединены с образованием замещенной или незамещенной циклоалкильной или гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп;n равно целому числу от 1 до 20;R15 и R16 независимо выбирают из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклоалкила и замещенного или незамещенного пептидила, где R15 и R16 вместе с атомом азота, к которому они присоединены, необязательно соединены с образованием замещенной или незамещенной гетероциклоалкильной кольцевой системы, содержащей от 4 до 6 групп, необязательно содержащей два или несколько гетероатомов,R33 содержит одну или несколько расщепляемых групп;R6 представляет собой одинарную связь, которая присутствует или отсутствует, и, если она присутствует, R6 и R7 соединены с образованием циклопропильного кольца;R7 представляет собой СН 2-Х 1 или -СН 2-, присоединенные в указанном циклопропильном кольце к 6R , где X1 представляет собой уходящую группу; или его фармацевтически приемлемая соль. Другой вариант представляет собой соединение, выбранное из где r равно целому числу от 0 до 24. Любое из этих соединений может использоваться в качестве или для формирования конъюгатов"лекарственное средство-лиганд". В другом аспекте изобретение относится к фармацевтическим препаратам. Такие препараты обычно содержат соединение-конъюгат по изобретению и фармацевтически приемлемый носитель. Еще в одном аспекте изобретение относится к способам применения соединений-конъюгатов по изобретению. Например, в изобретении предлагается способ уничтожения клеток, в котором конъюгатное соединение по изобретению вводят в клетку в количестве, достаточном, чтобы вызвать гибель клетки. В предпочтительном варианте клетка представляет собой опухолевую клетку. В другом варианте изобретения предлагается способ задержки или остановки роста опухоли у млекопитающего субъекта,где соединение-конъюгат по изобретению вводят субъекту в количестве, достаточном, чтобы замедлить или остановить рост опухоли. Другие аспекты, преимущества и объекты изобретения станут понятными из обзора детального описания ниже. Краткое описание чертежей Не ограничивающие и не исчерпывающие варианты настоящего изобретения описаны со ссылкой на следующие фигуры. Номера на фигурах обозначают сходные части на всех фигурах, если не указано иное. Для лучшего понимания настоящего изобретения будет приведена ссылка на подробное описание ниже, которое следует трактовать в связи с приложенными фигурами, где: фиг. 1-3 представляют графики среднего объема опухоли, медианного объема опухоли и медианы% изменения массы тела соответственно по отношению к показателям дней после введения дозы в первом исследовании in vivo; фиг. 4-6 представляют графики среднего объема опухоли, медианного объема опухоли и медианы% изменения массы тела соответственно по отношению к показателям дней после введения дозы во втором исследовании in vivo; фиг. 7 содержит логистические кривые, аппроксимированные для различных конъюгатов антителотоксин и полученные значения ЕС 50, в клетках LNCaP и 786-O; фиг. 8 показывает графики среднего объема опухоли по отношению к показателям дней после введения дозы для третьего исследования in vivo; фиг. 9 показывает графики медианного изменения массы тела по отношению к показателям дней после введения дозы для третьего исследования in vivo; фиг. 10 показывает графики среднего объема опухоли по отношению к показателям дней после вве- 11019962 дения дозы для четвертого исследования in vivo; фиг. 11 показывает графики медианного изменения массы тела по отношению к показателям дней после введения дозы для четвертого исследования in vivo; фиг. 12 показывает график среднего объема опухоли по отношению к показателям дней после введения дозы для пятого исследования in vivo; фиг. 13 показывает график среднего объема опухоли по отношению к показателям дней после введения дозы для шестого исследования in vivo; фиг. 14 показывает график среднего объема опухоли по отношению к показателям дней после введения дозы для седьмого исследования in vivo; фиг. 15 показывает график среднего объема опухоли по отношению к показателям дней после введения дозы для восьмого исследования in vivo; фиг. 16 показывает график среднего объема опухоли по отношению к показателям дней после введения дозы для девятого исследования in vivo. Подробное описание изобретения Сокращения В изобретении приняты следующие обозначения и сокращения:N-(диметиламино)-1 Н-1,2,3-триазоло[4,5-b]пиридин-1-ил]метилен]-Nметилметанаминия гексафторфосфат N-оксид; символ "Е" представляет собой ферментно расщепляемую группу;"ГОБТ" (НОВТ) - N-гидроксибензотриазол; символ "Q" представляет собой терапевтическое средство, диагностическое средство или определяемую метку. Определения Если не указано иное, все технические и научные термины, используемые в данном описании, в целом имеют такое же значение, какое им обычно придает средний специалист в области, к которой относится данное изобретение. В целом, номенклатура, используемая в данном описании, и лабораторные методики в области культивировании клеток, молекулярной генетике, органической химии и химии нуклеиновых кислот, а также гибридизации, описанные ниже, хорошо известны и обычно применяются в уровне техники. Стандартные методы применяются для синтеза нуклеиновых кислот и пептидов. В общем, ферментные реакции и стадии очистки выполняются в соответствии со спецификациями производителей. Методы и методики, в общем, выполняются в соответствии с обычными методами из уровня техники и различными источниками общего характера (в общем см. Sambrook et al. Molecular Cloning: ALaboratory Manual, 2nd ed. (1989), Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., которое включено в данное описание путем ссылки), приведенными в данном документе. Номенклатура, используемая в данном описании и описании лабораторных методик в области аналитической химии и органического синтеза, приведенных ниже, хорошо известна и обычно применяется в уровне техники. Стандартные методы или их модификации применяются для химического синтеза и химических анализов.- 12019962 Термин "терапевтическое средство" обозначает соединение, которое в терапевтически эффективном количестве осуществляет желательное терапевтическое действие на млекопитающее. Для лечения раковых новообразований желательно, чтобы терапевтическое средство также обладало способностью входить в клетку-мишень. Термин "цитотоксин" обозначает терапевтическое средство, оказывающее желательное воздействие, т.е. цитотоксическое действие на раковые клетки. "Цитотоксическое" означает, что средство останавливает рост или вызывает гибель клеток. Модельные цитотоксины включают, например, не ограничиваясь ими, комбретастатин, дуокармицины, противоопухолевые антибиотики СС-1065, антрациклины и родственные соединения. Другие цитотоксины включают микотоксины, рицин и его аналоги, калихеамицины, доксирубицин и мейтанзиноиды. Термин "пролекарство" и термин "конъюгат лекарственного средства" применяются в данном описании равнозначным образом. Оба термина обозначают соединение, в форме конъюгата относительно безобидное для клеток, которое выборочно разлагается до фармакологически активной формы в определенных условиях, например ферменты, расположенные в пределах или поблизости клеток-мишеней. Термин "маркер" обозначает соединение, пригодное для характеристики опухолей или другого медицинского состояния, например диагностики, контроля прогрессирования опухоли и анализа факторов,выделяемых клетками опухоли. Маркеры рассматриваются как подмножество "диагностических средств". Термин "селективный" при использовании в связи с ферментным расщеплением означает, что скорость расщепления линкерного фрагмента превышает скорость расщепления пептида со случайной последовательностью аминокислот. Термины "направляющая группа" и "направляющее средство" обозначают фрагмент, который(1) способен направлять соединение, к которому он присоединен (например, терапевтическое средство или маркер), к клетке-мишени, например к определенному виду опухолевых клеток; или (2) предпочтительно активизируется в целевой ткани, например опухолевой. Нацеливающая группа или направляющее средство может представлять собой низкомолекулярное соединение, которое включает соединения как не пептидной, так и пептидной природы. Нацеливающая группа также может представлять собой макромолекулу, что включает сахариды, лектины, рецепторы, лиганд для рецепторов, белки, например альбумин телячьей сыворотки, антитела и т.д. В предпочтительном варианте настоящего изобретения направляющая группа представляет собой антитело или фрагмент антитела, более предпочтительно моноклональное антитело или фрагмент моноклонального антитела. Термин "саморазрушающийся спейсер" обозначает бифункциональный химический фрагмент, способный ковалентно связывать два химических фрагмента в молекулу из 3 частей с обычной стабильностью. Саморазрушающийся спейсер способен самопроизвольно отделяться от второго фрагмента, если расщепляется связь с первым фрагментом. Термин "определяемая метка" обозначает фрагмент, проявляющий определяемое физическое или химическое свойство. Термин "расщепляемая группа" обозначает нестабильный in vivo фрагмент. Предпочтительно "расщепляемая группа" позволяет активацию маркера или терапевтического средства путем отщепления маркера или средства от остальной части конъюгата. Функционально определенный, линкер предпочтительно расщепляется in vivo биологическим окружением. Расщепление может быть результатом какоголибо процесса, например, не ограничиваясь ими, ферментного, восстановительного, рН и т.п. Предпочтительно расщепляемая группа выбрана таким образом, что активация происходит в целевом местоположении воздействия, которое может представлять собой участок в клетках- или тканях-мишенях или около них (например, клетки карциномы), или, например, на участке терапевтического воздействия или активности маркера. Такое расщепление может быть ферментным, и примеры расщепляемых ферментами групп включают природные аминокислоты или пептидные последовательности, которые заканчиваются природной аминокислотой, и присоединены к карбоксильному концу линкера. Хотя степень увеличения скорости расщепления не критична для изобретения, предпочтительными примерами расщепляемых линкеров являются такие, в которых как минимум около 10% расщепляемых групп расщепляются в кровотоке в пределах 24 ч после введения, наиболее предпочтительно как минимум около 35%. Термин "лиганд" подразумевает любую молекулу, которая специфично связывается или вступает в реакцию образования ассоциатов или комплексов с рецептором, субстратом, антигенным детерминантом или другим сайтом связывания на клетке- или ткани-мишени. Примеры лигандов включают антитела и их фрагменты (например, моноклональное антитело или его фрагмент), ферменты (например, фибринолитические ферменты), модификаторы биологического ответа (например, интерлейкины, интерфероны,эритропоэтин или колониестимулирующие факторы), пептидные гормоны, а также их антигенсвязывающие фрагменты. Термин "реакция циклизации", используемый в связи с циклизацией пептида, гидразина или дисульфидного линкера, указывает на циклизацию линкера в кольцо и инициирует разделение комплекса"лекарственное средство-лиганд". Его скорость может быть измерена ex situ, и процесс завершается с образованием как минимум 90, 95 или 100% продукта.- 13019962 Термины "полипептид", "пептид" и "белок" используются в данном описании равнозначным образом для обозначения полимера из остатков аминокислот. Термины применяются к аминокислотным полимерам, в которых один или несколько остатков аминокислоты представляет собой искусственный химический миметик соответствующей природной аминокислоты, а также к полимерам природных аминокислот и полимеру не встречающихся в природе аминокислот. Эти термины также включают термин"антитело". Термин "аминокислота" обозначает аминокислоты природного и синтетического происхождения, а также аналоги аминокислот и миметики аминокислот, которые функционируют сходным образом с аминокислотами природного происхождения. Природные аминокислоты представляют собой аминокислоты,кодируемые генетическим кодом, а также аминокислоты, впоследствии модифицированные, например гидроксипролин, -карбоксиглутамат и О-фосфосерин. Аналоги аминокислот обозначают соединения с такой же базовой химической структурой, как у природных аминокислот, т.е. -атом углерода, связанный с атомом водорода, карбоксильной группой, аминогруппой и группой R, например гомосерин, норлейцин, метионин сульфоксид, метионин метилсульфоний. В таких аналогах модифицированы группы R(например, норлейцин) или модифицированы скелеты пептида, но сохранена такая же базовая химическая структура, как в природных аминокислотах. Одной из подходящих аминокислот является, в частности, цитруллин, представляющий собой прекурсор аргинина и участвующий в образовании мочевины в печени. Миметики аминокислот обозначают химические соединения со структурой, отличной от общей химической структуры аминокислоты, но с функцией подобной природной аминокислоте. Термин "не встречающаяся в природе аминокислота" обозначает стереохимическую форму "D" 20 природных аминокислот, описанных выше. Кроме того, следует понимать, что термин "не встречающаяся в природе аминокислота" включает гомологи природных аминокислот и синтетически измененные формы природных аминокислот. Синтетически измененные формы включают, не ограничиваясь ими, аминокислоты с укороченными или удлиненными на 1-2 атома углерода алкиленовыми цепями, аминокислоты, содержащие необязательно замещенные арильные группы, и аминокислоты, содержащие галогенированные группы, предпочтительно галогенированные алкильные и арильные группы. При присоединении к линкеру или конъюгату по изобретению, аминокислота находится в форме "аминокислоты боковой цепи",где группа карбоновой кислоты в аминокислоте заменена кетогруппой [С(O)]. Таким образом, например,аланиновая боковая цепь представляет собой -C(O)-CH(NH2)-CH3 и т.д. Аминокислоты и пептиды могут быть защищены блокирующими группами. Блокирующая группа представляет собой атом или химический фрагмент, который защищает N-конец аминокислоты или пептида от нежелательных реакций и может использоваться в ходе синтеза конъюгата "лекарственное средство-лиганд". Он должен оставаться присоединенным к N-концу в ходе синтеза и может быть удален после завершения синтеза конъюгата лекарственного средства химическими или другими средствами,которые обеспечивают его селективное удаление. Блокирующие группы, подходящие для защитыN-конца, хорошо известны из уровня техники в области химии пептидов. Примеры блокирующих групп включают, не ограничиваясь ими, водород, D-аминокислоту и карбобензоксихлорид (Cbz)."Нуклеиновая кислота" обозначает дезоксинуклеотиды или рибонуклеотиды и их полимеры в одноцепочечной или двухцепочечной форме. Этот термин включает нуклеиновые кислоты, содержащие известные нуклеотидные аналоги или модифицированные остатки оснований скелета или связи, которые являются синтетическими, природными и неприродными, обладающие сходными свойствами связывания с эталонной нуклеиновой кислотой, которые метаболизируются до некоторой степени сходным образом с эталонными нуклеотидами. Примеры таких аналогов включают, не ограничиваясь ими, фосфортиоаты, фосфорамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метилрибонуклеотиды,пептид-нуклеиновые кислоты (ПНК). Если не указано иное, конкретная последовательность нуклеиновой кислоты также в неявной форме включает ее консервативно модифицированные варианты (например, замены с вырождением кодонов) и комплементарные последовательности, а также явно указанную последовательность. Конкретно, замены с вырождением кодонов могут быть осуществлены генерацией последовательностей, в которых третье положение одного или несколько выбранных (или всех) кодонов замещено остатками смешанных оснований и/или дезоксиинозина (Batzer et al., Nucleic Acid Res. 19: 5081 (1991); Ohtsuka et al., J. Biol. Chem. 260: 2605-2608 (1985); Rossolini et al., Mol. Cell. Probes 8: 91-98 (1994. Термин "нуклеиновая кислота" используется равнозначным образом с терминами "ген", "кДНК", "мРНК", "олигонуклеотид" и "полинуклеотид". Обозначение, используемое как связь или показанное перпендикулярно к связи, указывает точку, в которой показанный фрагмент присоединен к остатку молекулы, твердой подложке и т.п. Термин "алкил", отдельно или как часть другого заместителя, обозначает, если не указано иное, углеводородный радикал с неразветвленной или разветвленной цепью, или циклический, или их комбинацию, который может быть полностью насыщенным, моно- или полиненасыщенным, и может включать ди- и поливалентные радикалы, содержащие указанное количество атомов углерода (т.е. C1-C10 подразумевает от 1 до 10 атомов углерода). Примеры насыщенных углеводородных радикалов включают, не ог- 14019962 раничиваясь ими, такие группы, как метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, изобутил,втор-бутил, циклогексил, (циклогексил)метил, циклопропилметил, гомологи и изомеры, например н-пентил, н-гексил, н-гептил, н-октил и т.п. Ненасыщенная алкильная группа - это группа, содержащая одну или несколько двойных или тройных связей. Примеры ненасыщенных алкильных групп включают,не ограничиваясь ими, винил, 2-пропенил, кротил, 2-изопентенил, 2-(6 утадиенил), 2,4-пентадиенил,3-(1,4-пентадиенил), этинил, 1- и 3-пропинил, 3-бутинил, а также их и высшие гомологи и изомеры. Термин "алкил", если не указано иное, также предназначен включать производные алкила, определенные более подробно ниже, такие как "гетероалкил". Алкильные группы, которые ограничены углеводородными группами, носят название "гомоалкил". Термин "алкилен", отдельно или как часть другого заместителя, подразумевает двухвалентный радикал, происходящий от алкана, например, не ограничиваясь им, -CH2CH2CH2CH2-, и дополнительно включает группы, описанные ниже как "гетероалкилен". Обычно алкильная (или алкиленовая) группа будет содержать от 1 до 24 атомов углерода, причем группы, содержащие 10 или меньше атомов углерода, в настоящем изобретении предпочтительны. "Низший алкил" или "низший алкилен" - это алкильная или алкиленовая группа с более короткий цепью, в общем содержащая 8 или меньше атомов углерода. Термин "гетероалкил", отдельно или в комбинации с другим термином, обозначает, если не указано иное, стабильный углеводородный радикал с неразветвленной или разветвленной цепью, или циклический, или их комбинацию, содержащий указанное количество атомов углерода и как минимум один, гетероатом, выбранный из группы, состоящей из О, N, Si и S, где атомы азота, углерода и серы необязательно могут быть окисленными, и гетероатом азота необязательно может быть четвертичным. Гетероатом(ы) О, N, S и Si могут размещаться в любом внутреннем положении гетероалкильной группы или в положении, в котором алкильная группа присоединена к остальной части молекулы. Примеры включают,не ограничиваясь ими, -CH2-CH2-O-CH3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3,-CH2-CH2, -S(O)-CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -Si(CH3)3, -CH2-CH=N-OCH3 и-CH=CH-N(СН 3)-СН 3. До двух гетероатомов могут быть размещены последовательно, например,-CH2-NH-OCH3 и -CH2-O-Si(CH3)3. Также термин "гетероалкилен", отдельно или как часть другого заместителя, подразумевает двухвалентный радикал, происходящий от гетероалкила, например, не ограничиваясь ими, -CH2-CH2-S-CH2-СН 2- и -CH2-S-CH2-CH2-NH-CH2-. В случае гетероалкиленовых групп, гетероатомы также могут занимать один оба конца цепи (например, алкиленокси, алкилендиокси, алкиленамино, алкилендиамино и т.п.). Термины "гетероалкил" и "гетероалкилен" включают поли(этиленгликоль) и его производные (см., например, Shearwater Polymers Catalog, 2001). Кроме того, для мостиковых алкиленовых и гетероалкиленовых групп, направление, в котором записана формула мостиковой группы, не подразумевает никакой конкретной ориентации мостиковой группы. Например, формула C(O)2R' представляет как -C(O)2R'-, так и -R'C(O)2. Термин "низший" в сочетании с терминами "алкил" или "гетероалкил" обозначает фрагмент, содержащий от 1 до 6 атомов углерода. Термины "алкокси", "алкиламино", "алкилсульфонил" и "алкилтио" (или тиоалкокси) используются в их обычном значении и обозначают алкильные группы, присоединенные к остатку молекулы через кислородный атом, аминогруппу, группу SO2 или атом серы соответственно. Термин "арилсульфонил" обозначает арильную группу, присоединенную к остальной части молекулы через группу SO2, и термин "сульфгидрильный" обозначает группу SH. В целом, "ацильный заместитель" также выбирается из группы, указанной выше. В данном описании термин "ацильный заместитель" обозначает группы, присоединенные к и занимающие валентность карбонильного атома углерода, который прямо или косвенно присоединен к полициклическому ядру соединений по настоящему изобретению. Термины "циклоалкил" и "гетероциклоалкил", отдельно или в комбинации с другими терминами,обозначают, если не указано иное, циклические версии замещенного или незамещенного "алкила" и замещенного или незамещенного "гетероалкила" соответственно. Дополнительно, в случае гетероциклоалкила гетероатом может занять положение, в котором гетероцикл присоединен к остатку молекулы. Примеры циклоалкила включают, не ограничиваясь ими, циклопентил, циклогексил, 1-циклогексенил,3-циклогексенил, циклогептил и т.п. Примеры гетероциклоалкила включают, не ограничиваясь ими,1-(1,2,5,6-тетрагидропиридил), 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-морфолинил,3-морфолинил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидротиен-2-ил, тетрагидротиен-3-ил,1-пиперазинил, 2-пиперазинил и т.п. Атомы гетероатомов и углерода в циклических структурах необязательно окислены. Термин "галоген", отдельно или как часть другого заместителя, обозначают, если не указано иное,атом фтора, хлора, брома или йода. Дополнительно, такие термины, как "галогеналкил" предназначены включать моногалогеналкил и полигалогеналкил. Например, "галоген(C1-C4)алкил" предназначен включать, не ограничиваясь ими, трифторметил, 2,2,2-трифторэтил, 4-хлорбутил, 3-бромпропил и т.п. Термин "арил" обозначает, если не указано иное, замещенный или незамещенный полиненасыщенный, ароматический, углеводородный заместитель, который может представлять собой одинарное кольцо или несколько колец (предпочтительно от 1 до 3 колец), конденсированных или связанных ковалент- 15019962 ной связью. Термин "гетероарил" обозначает арильные группы (или кольца), которые содержат от 1 до 4 гетероатомов, выбранных из N, О и S, где атомы азота, углерода и серы необязательно окислены, и атом(ы) азота необязательно являются четвертичными. Гетероарильная группа может быть присоединена к остатку молекулы через гетероатом. Не ограничивающие примеры арильных и гетероарильных групп включают фенил, 1-нафтил, 2-нафтил, 4-бифенил,1-пирролил, 2-пирролил, 3-пирролил, 3-пиразолил, 2-имидазолил, 4-имидазолил, пиразинил, 2-оксазолил,4-оксазолил, 2-фенил-4-оксазолил, 5-оксазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил,2-тиазолил, 4-тиазолил, 5-тиазолил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 2-пиридил, 3-пиридил,4-пиридил, 2-пиримидил, 4-пиримидил, 5-бензотиазолил, пуринил, 2-бензимидазолил, 5-индолил,1-изохинолил, 5-изохинолил, 2-хиноксалинил, 5-хиноксалинил, 3-хинолил и 6-хинолил. Заместители для каждой из вышеуказанных арильных и гетероарильных кольцевых систем выбирают из группы приемлемых заместителей, описанной ниже. "Арил" и "гетероарил" также включают системы колец, где одно или несколько неароматических колец в системе конденсированы или другим способом связаны с арильной или гетероарильной системой. Для краткости, термин "арил" при использовании в комбинации с другими терминами (например,арилокси, арилтиокси, арилалкил) включает как арильные, так и гетероарильные кольца, как определено выше. Таким образом, термин "арилалкил" предназначен включать те радикалы, в которых арильная группа присоединена к алкильной группе (например, бензил, фенэтил, пиридилметил и т.п.), включая те алкильные группы, в которых атом углерода (например, метиленовой группы) заменен, например, атомом кислорода (например, феноксиметил, 2-пиридилоксиметил, 3-(1-нафтилокси)пропил и т.п.). Каждый из упомянутых выше терминов (например, "алкил", "гетероалкил", "арил" и "гетероарил") включает как замещенные, так и незамещенные формы указанного радикала. Предпочтительные заместители для каждого вида радикала приведены ниже. Заместители для алкильных и гетероалкильных радикалов (включая группы, которые часто называют алкиленом, алкенилом, петероалкиленом, гетероалкенилом, алкинилом, циклоалкилом, гетероциклоалкилом, циклоалкенилом и гетероциклоалкенилом) в целом носят название "заместители алкила" и"заместители гетероалкила" соответственно, и они могут представлять собой одну или несколько разнообразных групп, выбранных из, но не ограничиваясь ими, OR', =O, =NR', =N-OR', -NR'R", -SR', -галоген,-SiR'R"R"', -OC(O)R', -C(O)R', -CO2R', -CONR'R", -ОС(O)NR'R", -NR"C(O)R', -NR'-C(O)NR"R"',-NR"C(O)2R', -NR-C(NR'R"R'")=NR, -NR-C(NR'R")=NR"', -S(O)R', -S(O)2R', -S(O)2NR'R", -NRSO2R', -CN и -NO2 в количестве от нуля до (2m'+1), где m' равно общему количеству атомов углерода в таком радикале. Каждый из R', R", R"' и R предпочтительно независимо обозначает водород, замещенные или незамещенные гетероалкильные, замещенные или незамещенные арильные, например арильные, замещенные 1-3 атомами галогена, замещенные или незамещенные алкильные, алкокси или тиоалкокси группы,или арилалкильные группы. Если соединение по изобретению содержит более чем одну группу R, например, каждая из групп R независимо выбирается из групп R', R", R'" и R, если присутствует более чем одна из этих групп. Если R' и R" присоединены к одному и тому же атому азота, они могут быть соединены с атомом азота с образованием 5-, 6-, или 7-членного кольца. Например, -NR'R" предназначен включать, не ограничиваясь ими, 1-пирролидинил и 4-морфолинил. На основе приведенного обсуждения заместителей, специалисту в данной области будет понятно, что термин "алкил" предназначен включать группы, в том числе атомы углерода, связанные с группами, кроме атомов водорода, например галогеналкил (например, -CF3 и -CH2CF3) и ацил (например, -C(O)CH3, -C(O)CF3, -C(O)CH2OCH3 и т.п.). Подобно заместителям, описанным для алкильного радикала, заместители арила и заместители гетероарила, в целом, носят название "заместителей арила" и "заместителей гетероарила" соответственно и варьируют и выбирают из, например, галогена, -OR', =O, =NR', =N-OR', -NR'R", -SR', -галогена,-SiR'R"R"', -OC(O)R', -C(O)R', -CO2R', -CONR'R", -ОС(O)NR'R", -NR"C(O)R', -NR'-C(O)NR"R"',-NR"C(O)2R', -NR-C(NR'R")=NR'", -S(O)R', -S(O)2R', -S(O)2NR'R", -NRSO2R', -CN и -NO2, -R', -N3,-CH(Ph)2, фтор(С 1-С 4)алкокси и фтор(C1-C4)алкил в количестве от нуля до общего количества открытых валентностей на системе ароматических колец; где R', R", R"' и R предпочтительно независимо выбирают из водорода, (C1-C8)алкила и гетероалкила, незамещенного арила и гетероарила, (незамещенный арил)-(С 1-C4)алкила и (незамещенный арил)окси(C1-C4)алкил. Если соединение по изобретению содержит более чем одну группу R, например, каждая из групп R выбирается независимо из групп R', R", R'" иR, если присутствует более чем одна из этих групп. Два из заместителей арила при смежных атомах арильного или гетероарильного кольца могут быть необязательно заменены на заместитель формулы -Т-С(О)-(CRR')q-U-, где Т и U независимо представляют собой -NR-, -O-, -CRR'- или одинарную связь и q равно целому числу от 0 до 3. Альтернативно, два из заместителей при смежных атомах арильного или гетероарильного кольца могут быть необязательно заменены на заместитель формулы -А-(СН 2)r-В-, где А и В независимо представляют собой -CRR'-, -O-,-NR-, -S-, -S(O)-, -S(O)2-, -S(O)2NR'- или одинарную связь и r равно целому числу от 1 до 4. Одна из одинарных связей образованного таким образом нового кольца может быть необязательно заменена двойной связью. Альтернативно, два из заместителей при смежных атомах арильного или гетероарильного кольца могут быть необязательно заменены заместителем формулы -(CRR')s-X-(CR"R'")d-, где s и d независимо- 16019962 равны целым числам от 0 до 3 и X представляет собой -O-, -NR'-, -S-, -S(O)-, -S(O)2-или -S(O)2NR'-. Заместители R, R', R" и R'" предпочтительно независимо выбираются из водорода и замещенного или незамещенного (C1-C6)алкила. В данном описании термин "дифосфат" включает, не ограничиваясь им, эфир фосфорной кислоты,содержащей две фосфатные группы. Термин "трифосфат" включает, не ограничиваясь им, эфир фосфорной кислоты, содержащей три фосфатные группы. Например, конкретные лекарственные средства, содержащие дифосфат или трифосфат, включают В данном описании термин "гетероатом" включает кислород (О), азот (N), серу (S) и кремний (Si). Обозначение "R" - это общее сокращение, которое представляет группу заместителя, которую выбирают из замещенных или незамещенных алкильных, замещенных или незамещенных гетероалкильных, замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных и замещенных или незамещенных гетероциклильных групп. Термин "фармацевтически приемлемый носитель" в данном описании обозначает фармацевтически приемлемый материал, композицию или носитель, такой как жидкий или твердый наполнитель, разбавитель, вспомогательное вещество, растворитель или инкапсулирующий материал, принимающий участие в переноске или транспорте химического средства. Фармацевтически приемлемые носители включают фармацевтически приемлемые соли, где термин"фармацевтически приемлемые соли" включает соли активных соединений с относительно нетоксичными кислотами или основаниями, в зависимости от конкретных заместителей, содержащихся в соединениях, описанных в данном описании. Если соединения по настоящему изобретению содержат относительно кислую функциональную группу, основно-аддитивные соли могут быть получены путем обеспечения контакта нейтральной формы таких соединений с достаточным количеством желательного основания, в не разведенном виде или в подходящем инертном растворителе. Примеры фармацевтически приемлемых основно-аддитивных солей включают соли натрия, калия, кальция, аммония, органических аминов или магния, и подобные соли. Если соединения по настоящему изобретению содержат относительно основную функциональную группу, кислотно-аддитивные соли могут быть получены путем обеспечения контакта нейтральной формы таких соединений с достаточным количеством желательной кислоты, в не разведенном виде или в подходящем инертном растворителе. Примеры фармацевтически приемлемых кислотно-аддитивных солей включают полученные из неорганических кислот, таких как хлористоводородная, бромоводородная, азотная, угольная, одноосновная соль угольной кислоты, фосфорный,одноосновная соль фосфорной кислоты, двухосновная соль фосфорной кислоты, серная, одноосновная соль серной кислоты, йодоводородная или фосфористые кислоты и т.п., а также соли, полученные из относительно нетоксичных органических кислот, таких как уксусная, пропионовая, изомасляная, яблочная, малоновая, бензойная, янтарная, суберовая, фумаровая, молочная, манделовая, фталевая, бензолсульфоновая, п-толилсульфоновая, лимонная, винная, метансульфоновая и т.п. Также включены соли аминокислот, такие как аргинат и т.п., и соли органических кислот, таких как глюкуроновая или галактуроновая кислота и т.п. [см., например, Berge et al., "Pharmaceutical Salts", Journal of PharmaceuticalScience, 1977, 66, 1-19). Некоторые конкретные соединения по настоящему изобретению содержат как основные, так и кислотные функциональные группы, которые позволяют соединениям превращаться как в основно-аддитивные, так и в кислотно-аддитивные соли. Нейтральные формы соединений предпочтительно регенерируют, обеспечивая контакт соли с основанием или кислотой и выделяя исходное соединение в обычной форме. Форма исходного соединения отличается от различных солевых форм некоторыми физическими свойствами, такими как растворимость в полярных растворителях, но в других отношениях соли равноценны форме исходного соединения для целей настоящего изобретения. В дополнение к солевым формам настоящее изобретение обеспечивает соединения, которые находятся в форме пролекарства. Пролекарства соединений, описанных в данном описании, представляют- 17019962 собой соединения, которые легко подвергаются химическим изменениям в физиологических условиях,чтобы обеспечить соединения по настоящему изобретению. Дополнительно, пролекарства могут быть превращены в соединения по настоящему изобретению химическими или биохимическими методами в окружении ex vivo. Например, пролекарства могут быть медленно превращены в соединения по настоящему изобретению при помещении в резервуаре трансдермального пластыря с подходящим ферментным или химическим реактивом. Некоторые соединения по настоящему изобретению могут существовать в не сольватированных формах, а также в сольватированных формах, в том числе в гидратированных формах. В целом, сольватированные формы равноценны не сольватированным формам и находятся в пределах контекста настоящего изобретения. Некоторые соединения по настоящему изобретению могут существовать в многочисленных кристаллических или аморфных формах. В целом, все физические формы равноценны с точки зрения применения, предусмотренного настоящим изобретением, и находятся в пределах контекста настоящего изобретения. Некоторые соединения по настоящему изобретению содержат асимметрические атомы углерода(оптические центры) или двойные связи; рацематы, диастереомеры, геометрические изомеры и отдельные изомеры находятся в пределах контекста настоящего изобретения. Соединения по настоящему изобретению могут также содержать неприродные пропорции атомных изотопов для одного или несколько атомов, из которых состоят такие соединения. Например, соединения могут содержать метку в виде радиоактивного изотопа, такого как тритий (3 Н), йод-125 (125I) или углерод-14 (14 С). Все изотопные вариации соединений по настоящему изобретению, радиоактивный или нет,находятся в пределах контекста настоящего изобретения. Термин "присоединяющий фрагмент" или "фрагмент для присоединения направляющей группы" обозначает фрагмент, который позволяет присоединение направляющей группы к линкеру. Типичные присоединяющие группы включают, для иллюстрации и, не ограничиваясь ими, алкил, аминоалкил, аминокарбонилалкил, карбоксиалкил, гидроксиалкил, алкилмалеимид, алкил-N-гидроксилсукцинимид, поли(этиленгликоль)-малеимид и поли(этиленгликоль)-N-гидроксисукцинимид, все из которых могут быть дополнительно замещены. Линкер может также содержать присоединяющий фрагмент, фактически присоединенный к направляющей группе. В данном описании термин "уходящая группа" обозначает часть субстрата, которая отщепляется от субстрата в ходе реакции. Термин "антитело" в данном описании включает антитела целиком и любой антигенсвязывающий фрагмент (т.е. "антигенсвязывающая часть") или их одинарные цепи. "Антитело" обозначает гликопротеин, содержащий как минимум две тяжелые (Н) цепи и две легкие (L) цепи, соединенные между собой дисульфидными связями, или его антигенсвязывающую часть. Каждая тяжелая цепь состоит из вариабельного участка тяжелой цепи (VH) и константного участка тяжелой цепи. Константный участок тяжелой цепи состоит из трех доменов, СН 1, СН 2 и CH3 и может принадлежать к мю, дельта, гамма, альфа или эпсилон изотипу. Каждая легкая цепь состоит из вариабельного участка легкой цепи (VL) и константного участка легкой цепи. Константный участок легкой цепи состоит из одного домена, CL, который может принадлежать к каппа или лямбда изотипу. Участки VH и VL могут быть дополнительно подразделены на участки гипервариабельности, которые носят название определяющих комплементарность участков(CDR), перемежающиеся более консервативными участками, которые носят название каркасных участков (FR). Каждый VH и VL состоит из трех CDR и четырех FR, организованных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные участки тяжелых и легких цепей содержат связывающий домен, который взаимодействует с антигеном. Константные участки антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, в том числе различными клетками иммунной системы (например, эффекторными клетками), и первым компонентом (Clq) классической системы комплемента. Термины "фрагмент антитела" или "антигенсвязывающая часть" антитела (или просто "часть антитела") в данном описании обозначают один или несколько фрагментов антитела, которые сохраняют способность специфично связываться с антигеном. Показано, что антигенсвязывающая функция антитела может выполняться фрагментами полноразмерного антитела. Примеры связывающих фрагментов в пределах терминов "фрагмент антитела" или "антигенсвязывающая часть" антитела, включают (i) Fab фрагмент, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) фрагмент F(ab')2, двухвалентный фрагмент, включающий два фрагмента Fab, связанных дисульфидным мостиком в шарнирном участке; (iii) фрагмент Fd, состоящий из доменов VH и CH1; (iv) фрагмент Fv, состоящий из доменов VL иVH одного плеча антитела, (v) фрагмент dAb (Ward et al. (1989), Nature, 341:544-546), который состоит из домена VH; и (vi) изолированный участок, определяющий комплементарность (CDR). Кроме того, хотя два домена фрагмента Fv, VL и VH, кодируют отдельные гены, они могут быть соединены, с использованием рекомбинантных методов, синтетическим линкером, который дает им возможность существовать в виде одноцепочечного белка, в котором пара участков VL и VH образуют одновалентные молекулы (известные как одноцепочечный Fv (scFv); см., например, Bird et al. (1988), Science, 242: 423-426 and Hustonet al. (1988), Proc. Natl. Acad. Sci. USA 85: 5879-5883J. Такие одноцепочечные антитела также находятся в- 18019962 пределах термина "антигенсвязывающая часть" антитела. Такие фрагменты антитела получают, используя обычные методы, известные специалисту в данной области, и проводят скрининг фрагментов в такой же форме, как и для интактных антител. Термин "моноклональное антитело" в данном описании обозначает препарат молекул антитела одинакового молекулярного состава. Композиция моноклонального антитела демонстрирует одинаковую специфичность связывания и сродство в отношении конкретного эпитопа. Для получения моноклональных или поликлональных антител может применяться любая техника,известная из уровня техники (см., например, KohlerMilstein, Nature 256: 495-497 (1975); Kozbor et al.,Immunology Today 4: 72 (1983); Cole et al., p. 77-96 в Monoclonal Antibodies and Cancer Therapy, Alan R.Liss, Inc. (1985. Методы продуцирования поликлональных антител известны специалисту в данной области. Инбредный штамм мышей (например, мыши BALB/C) или кроликов иммунизируют белком, используя стандартный адъювант, такой как адъювант Фрейнда, и стандартный протокол иммунизации. Иммунный ответ животного на иммуногенный препарат контролируют, отбирая тестовые образцы крови и определяя титр реактивности бета-субъединиц. Если получены подходящие высокие титры антител к иммуногену, кровь животного собирают и готовят антисыворотки. Дальнейшее фракционирование антисывороток для обогащения антителами, реакционноспособными в отношении белка, может быть осуществлено при желании. Моноклональные антитела могут быть получены различными методами, знакомыми специалистам в данной области. Если коротко, клетки селезенки животного, иммунизированного целевым антигеном,делают бессмертными, обычно путем слияния с клеткой миеломы (см. KohlerMilstein, Eur. J. Immunol. 6: 511-519 (1976. Альтернативные методы получения бессмертных клеток включают трансформацию с помощью вируса Эпштейна-Барр, онкогенов или ретровирусов или другие методы, хорошо известные из уровня техники. В предпочтительном варианте антитело представляет собой химерное или гуманизированное антитело. Химерные или гуманизированные антитела по настоящему изобретению могут быть получены на основании последовательности мышиного моноклонального антитела. ДНК, кодирующая тяжелые и легкие цепи иммуноглобулинов, может быть получена из целевой мышиной гибридомы и сконструирована таким образом, чтобы содержать последовательности не мышиного (например, человеческого) иммуноглобулина, с использованием стандартных методов молекулярной биологии. Например, чтобы создать химерное антитело, мышиные вариабельные участки могут быть присоединены к человеческим константным участкам, с использованием методов, известных из уровня техники (см. например, патент США 4816567, выданный Cabilly et al.,). Для создания гуманизированного антитела, мышиные участкиCDR могут быть вставлены в человеческую структуру с использованием методов, известных из уровня техники (см., например, патент США 5225539, выданный Winter, и патенты США 5530101; 5585089; 5693762 и 6180370, выданные Queen et al.). В другом предпочтительном варианте антитело представляет собой человеческое антитело. Такие человеческие антитела могут генерироваться путем иммунизации трансгенных или трансхромосомных мышей, у которых эндогенные гены иммуноглобулина мыши инактивированы, и введены экзогенные гены человеческого иммуноглобулина. Такие мыши известны из уровня техники (см., например, патенты США 5545806; 5569825; 5625126; 5633425; 5789650; 5877397; 5661016; 5814318; 5874299; и 5770429; выданные Lonberg и Kay; патенты США 5939598; 6075181; 6114598; 6150584 и 6162963, выданные Kucherlapati et al.; и РСТ публикацию WO 02/43478, Ishida et al.) Человеческие антитела также могут быть получены с использованием методов показа фага для скрининга библиотек человеческих генов иммуноглобулина. Такие методы дисплея фага для выделения человеческих антител также известны из уровня техники (см., например, патенты США 5223409; 5403484 и 5571698, выданные Ladner et al.; патенты США 5427908 и 5580717, выданные Dower et al.; патенты США 5969108 и 6172197, выданные McCafferty"Твердая подложка" в данном описании обозначает материал, который является в существенной мере нерастворимым в выбранной системе растворителей или который может быть легко отделен (например, осаждением) от выбранной системы растворителей, в которой он растворим. Твердые подложки,подходящие для практики данного изобретения, могут содержать группы, которые активируются или способны к активации, чтобы позволить выбранным молекулам присоединиться к твердой подложке. Твердая подложка также может представлять собой субстрат, например микрочип, пластину или лунку, с которой связывается отдельное или несколько соединений по изобретению."Реакционноспособная функциональная группа" в данном описании обозначает группы, в том числе, но не ограничиваясь ими, олефины, ацетилены, спирты, фенолы, простые эфиры, оксиды, галогениды, альдегиды, кетоны, карбоновые кислоты, сложные эфиры, амиды, цианаты, изоцианаты, тиоцианаты,изотиоцианаты, амины, гидразины, гидразоны, гидразиды, диазо, диазоний, нитро, нитрилы, меркаптаны,сульфиды, дисульфиды, сульфоксиды, сульфоны, сульфоновые кислоты, сульфиновые кислоты, ацетали,кетали, ангидриды, сульфаты, сульфеновые кислоты, изонитрилы, амидины, имиды, имидаты, нитроны,гидроксиламины, оксимы, гидроксамовые кислоты, тиогидроксамовые кислоты, аллены, ортоэфиры,- 19019962 сульфиты, енамины, инамины, производные мочевины, псевдомочевины, семикарбазиды, карбодиимиды, карбаматы, имины, азиды, азосоединения, азоксисоединения и нитрозосоединения. Реакционноспособные функциональные группы также включают группы, используемые для получения биоконъюгатов,например N-гидроксисукцинимидные эфиры, малеимиды и т.п. (см., например, Hermanson, BioconjugateTechniques, Academic press, San Diego, 1996). Способы получения каждой из указанных функциональных групп хорошо известны в данной области, и их применение или модификация для конкретной цели находятся в пределах квалификации специалиста в данной области (см., например, Sandier and Karo, eds.Organic Functional Group Preparations, Academic Press, San Diego, 1989). Реакционноспособные функциональные группы могут быть защищенными или незащищенными. Соединения по изобретению получают в виде одинарного изомера (например, энантиомер, цистранс, изомер положения, диастереомер) или смеси изомеров. В предпочтительном варианте соединения получают как в существенной мере одинарный изомер. Способы получения в существенной мере изомерно чистых соединений известны из уровня техники. Например, энантиомерно обогащенные смеси и чистые энантиомерные соединения могут быть получены с использованием синтетических промежуточных соединений, которые являются энантиомерно чистыми, в комбинации с реакциями, которые оставляют стереохимию хирального центра неизменной или приводят к ее полной инверсии. Альтернативно,конечный продукт или промежуточные соединения вдоль пути синтеза могут быть разделены на одинарные стереоизомеры. Способы инверсии или сохранения конфигурации специфического стереоцентра и способы разделения смесей стереоизомеров хорошо известны из уровня техники, и навык выбора подходящего способа для конкретной специфической ситуации находится в пределах квалификации специалиста в данной области. См. для общей информации Furniss et al. (eds.), Vogel's Encyclopedia of PracticalChem. Res. 23: 128 (1990). Линкеры. Настоящее изобретение предусматривает конъюгаты "лекарственное средство-лиганд", где лекарственное средство связано с лигандом через химический линкер. В некоторых вариантах линкер представляет собой пептидильный линкер и изображается в данном описании как (L4)p-F-(L1)m. Другие линкеры включают гидразиновые и дисульфидные линкеры и изображаются в данном описании как (L4)р-Н-(L1)m или (L4)p-J-(L1)m соответственно. В добавление к линкерам, присоединенным к лекарственному средству,в настоящем изобретении также предлагаются расщепляемые плечи линкера, подходящие для прикрепления, по существу, к любым видам молекул. Примером аспекта плеча линкера по изобретению в данном описании является ссылка на их прикрепление к терапевтическому фрагменту. Однако специалисту в данной области будет понятно, что линкеры могут быть присоединены к различным видам молекул, в том числе, не ограничиваясь ими, диагностическим средствам, аналитическим средствам, биологическим молекулам, направляющим агентам, определяемым меткам и т.п. Использование пептидильных и других линкеров в конъюгатах "лекарственное средство-лиганд" описано во Временных патентных заявках США, серийные номера 60/295196; 60/295259; 60/295342; 60/304908; 60/572667; 60/661174; 60/669871; 60/720499; 60/730804; и 60/735657 и патентных заявках США, серийные номера 10/160972; 10/161234; 11/134685; 11/134826; и 11/398854, в патенте США 6989452 и патентной заявке РСТ под номером PCT/US2006/37793, все из которых включены в данное описание путем ссылки. В одном аспекте настоящее изобретение относится к линкерам, пригодным для присоединения направляющих групп к терапевтическим средствам и маркерам. В другом аспекте изобретения предлагаются линкеры, которые придают стабильность соединениям, уменьшают их токсичность in vivo или оказывают другое благоприятное воздействие на их фармакокинетику, биодоступность и/или фармакодинамику. В общем, предпочтительно в таких вариантах, линкер расщепляется, высвобождая активное лекарственное средство, как только лекарственное средство доставлено к месту его действия. Таким образом, в одном варианте изобретения линкеры по изобретению не оставляют следов своего присутствия, таким образом, что после удаления с терапевтического средства или маркера (например, в ходе активации) следов присутствия линкера не остается. В другом варианте изобретения линкеры характеризуются их способностью расщепляться на участке в непосредственной близости или около клетки-мишени, например в месте терапевтического действия или активности маркера. Такое расщепление может быть ферментным по своей природе. Такой признак помогает уменьшить системную активацию терапевтического средства или маркера, уменьшая токсичность и системные побочные эффекты. Предпочтительные расщепляемые группы для расщепления ферментами включают пептидные связи, эфирные связи и дисульфидные связи. В других вариантах линкеры чувствительны к рН и расщепляются при изменении рН. Важный аспект настоящего изобретения представляет собой способность управлять скоростью, с которой расщепляются линкеры. Часто желателен линкер, который расщепляется быстро. В некоторых вариантах, однако, линкер, который расщепляется медленнее, может быть предпочтительным. Например,в препарате с замедленным высвобождением или в препарате с быстрым и медленным высвобождением компонента может быть полезно обеспечить линкер, который расщепляется медленнее. В WO 02/096910- 20019962 предлагается несколько конкретных комплексов "лекарственное средство-лиганд", содержащих гидразиновый линкер. Однако отсутствует возможность "настроить" композицию линкера в зависимости от необходимой скорости циклизации, и в описанных конкретных соединениях лиганд отщепляется от лекарственного средства с более медленной скоростью, чем предпочтительная для многих конъюгатов" лекарственное средство-линкер". И наоборот, гидразиновые линкеры по настоящему изобретению предусматривают интервал значений скорости циклизации, от очень быстрой до очень медленной, таким образом позволяя выбрать конкретный гидразиновый линкер, основываясь на желательной скорости циклизации. Например, очень быстрая циклизация может быть достигнута с помощью гидразиновых линкеров, которые образуют одинарное 5-членное кольцо при расщеплении. Предпочтительные значения скорости циклизации для целенаправленной доставки цитотоксического средства к клеткам достигаются с использованием гидразиновых линкеров, которые при расщеплении образуют два 5-членных кольца или одинарное 6-членное кольцо из линкера, содержащего две метильных группы в геминальном положении (присоединенные к одному и тому же атому). Показано, что влияние гем-диметила ускоряет скорость реакции циклизации по сравнению с одинарным 6-членным кольцом без двух метильных групп в геминальном положении. Это происходит в результате уменьшенного натяжения в кольце. Иногда, однако, заместители могут замедлять реакцию вместо ее ускорения. Часто причины замедления могут быть выявлены в стерических помехах. Как показано в примере 2.4, замена гем-диметила позволяет реакции циклизации протекать намного быстрее по сравнению с соединением, где углерод в геминальном положении представляет собой СН 2. Важно отметить, однако, что в некоторых вариантах линкер, который расщепляется медленнее, может быть предпочтительным. Например, в препарате с замедленным высвобождением или в препарате как с быстрым, так и медленным высвобождением компонента, может быть полезно обеспечить линкер,который расщепляется медленнее. В некоторых вариантах медленная скорость циклизации достигается использованием гидразиновых линкеров, которые при расщеплении образуют одинарное 6-членное кольцо, без гем-диметильного замещения, или одинарное 7-членное кольцо. Линкеры также служат целям стабилизации терапевтического средства или маркера против деградации при нахождении в кровотоке. Этот признак обеспечивает существенное преимущество, поскольку такая стабилизация приводит к увеличению периода полувыведения из кровотока присоединенного средства или маркера. Линкер также служит целям аттенуации активности присоединенного средства или маркера, таким образом, что конъюгат проявляет относительно доброкачественные свойства при нахождении в кровотоке и оказывает желательный эффект, например токсический, после активации на участке целевого воздействия. Для конъюгатов терапевтического средства такой признак линкера служит целям улучшения терапевтического индекса средства. Стабилизирующие группы предпочтительно выбирают таким образом, чтобы ограничить клиренс и метаболизм терапевтического средства или маркера ферментами, которые могут присутствовать в крови или не целевой ткани и, кроме того, выбирают таким образом, чтобы ограничить транспорт средства или маркера в клетки. Стабилизирующие группы служат целям блокирования разложения средства или маркера и могут также действовать для обеспечения других физических характеристик средства или маркера. Стабилизирующая группа также может улучшать стабильность средства или маркера в процессе хранения в форме препарата или субстанции. В идеале, стабилизирующая группа пригодна для стабилизации терапевтического средства или маркера, если она служит целям защиты средства или маркера от разложения, что проверяется в процессе хранения средства или маркера в крови человека при 37 С на протяжении 2 ч, причем расщепление средства или маркера ферментами, присутствующими в крови человека в заданных условиях испытания составляет менее 20%, предпочтительно менее 10%, более предпочтительно менее 5% и даже более предпочтительно менее 2%. Настоящее изобретение также относится к конъюгатам, содержащим такие линкеры. Более конкретно, изобретение относится к пролекарствам, которые могут применяться для лечения заболевания,особенно для химиотерапии рака. Конкретно, использование линкеров, описанных в данном описании,предусматривают пролекарства, которые демонстрируют высокую избирательность действия, сниженную токсичность и улучшенную стабильность в крови в сравнении с пролекарством подобной структуры. Линкеры по настоящему изобретению, описанные в данном документе, могут присутствовать в разнообразных положениях в пределах цитотоксического конъюгата. Таким образом, предлагается линкер, который может содержать любую из многочисленных групп как часть цепи, которая будет расщепляться in vivo, например в кровотоке со скоростью, которая превышает скорость для конструкций, где такие группы отсутствуют. Также предлагаются конъюгаты плеч линкера с терапевтическими и диагностическими средствами. Линкеры пригодны для образования пролекарственных аналогов терапевтических средств и обратного присоединения терапевтического или диагностического средства к направляющему агенту, определяемой метке или твердой подложке. Линкеры могут быть инкорпорированы в комплексы, которые включают цитотоксины по изобретению.- 21019962 В дополнение к расщепляемой пептидной, гидразиновой или дисульфидной группе, одна или несколько линкерных саморазрушающихся групп L1 необязательно вводится между цитотоксином и направляющим агентом. Такие линкерные группы могут также быть описаны как спейсерные группы и содержат как минимум две реакционноспособные функциональные группы. Обычно одна функциональная химическая группа спейсерного фрагмента связывается с функциональной химической группой терапевтического средства, например цитотоксина, в то время как другая функциональная химическая группа спейсерного фрагмента используется для образования связи с функциональной химической группой направляющего агента или расщепляемого линкера. Примеры химических функциональных групп спейсерного фрагмента включают гидрокси, меркапто, карбонильные, карбокси-, амино-, кето- и меркаптогруппы. Саморазрушающиеся линкеры, представленные L1, в общем представляют собой замещенную или незамещенную алкильную, замещенную или незамещенную арильную, замещенную или незамещенную гетероарильную или замещенную или незамещенную гетероалкильную группу. В одном из вариантов алкильные или арильные группы могут содержать от 1 до 20 атомов углерода. Они также могут содержать полиэтиленгликольный фрагмент. Примеры спейсерной группы включают, например, 6-аминогексанол, 6-меркаптогексанол,10-гидроксидекановую кислоту, глицин и другие аминокислоты, 1,6-гександиол, -аланин,2-аминоэтанол, цистеамин (2-аминоэтантиол), 5-аминопентановую кислоту, 6-аминогексановую кислоту,3-малеимидобензойную кислоту, фталид, -замещенные фталиды, карбонильную группу, эфиры аминаля, нуклеиновые кислоты, пептиды и т.п. Спейсер может служить для введения дополнительной молекулярной массы и химической функциональной группы в комплекс "цитотоксин-направляющий агент". В целом, дополнительная масса и функциональная группа будут влиять на период полувыведения из сыворотки и другие свойства комплекса. Таким образом, путем тщательного выбора спейсерных групп, могут быть получены комплексы цитотоксина с интервалом значений периода полувыведения из сыворотки. Спейсер(ы), размещенный(е) в непосредственной близости от фрагмента лекарственного средства,также обозначают как (L1)m, где m равно целому числу, выбранному из 0, 1, 2, 3, 4, 5 и 6. Если присутствует несколько спейсеров L1, могут применяться одинаковые или разные спейсеры. L1 может представлять собой любую саморазрушающуюся группу.L4 представляет собой линкерный фрагмент, который предпочтительно обеспечивает повышенную растворимость или снижение агрегационных свойств конъюгата, в котором используется линкер, который содержит фрагмент или изменяет скорость гидролиза конъюгата. Линкер L4 не должен быть саморазрушающимся. В одном из вариантов фрагмент L4 представляет собой замещенный алкил, незамещенный алкил, замещенный арил, незамещенный арил, замещенный гетероалкил или незамещенный гетероалкил, каждый из которых может быть неразветвленным, разветвленным или циклическим. Заместители могут представлять собой, например, низший (С 1-С 6)алкил, алкокси, алкилтио, алкиламино или диалкиламино. В некоторых вариантах L4 включает нециклический фрагмент. В другом варианте L4 включает любой положительно или отрицательно заряженный аминокислотный полимер, такой как полилизин или полиаргинин. L4 может включать такой полимер, как фрагмент полиэтиленгликоля. Дополнительно, линкер L4 может включать, например, как компонент полимера, так и низкомолекулярный химический фрагмент. В предпочтительном варианте L4 включает фрагмент полиэтиленгликоля (ПЭГ). Длина фрагмента ПЭГ L4 может составлять от 1 до 50 единиц. Предпочтительно длина ПЭГ будет составлять 1-12 повторяющихся единиц, более предпочтительно 3-12 повторяющихся единиц, более предпочтительно 2-6 повторяющихся единиц или даже более предпочтительно 3-5 повторяющихся единиц, и наиболее предпочтительно 4 повторяющиеся единицы. L4 может состоять исключительно из фрагмента ПЭГ, или может также содержать дополнительный замещенный или незамещенный алкил или гетероалкил. Полезно включить ПЭГ как часть фрагмента L4, чтобы увеличить растворимость комплекса в воде. Дополнительно, фрагмент ПЭГ уменьшает степень агрегации, которая может возникать в ходе конъюгации лекарственного средства с антителом. В некоторых вариантах L4 включаетR20 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила. Каждый из R25, R25', R26 и R26' независимо выбирают из Н, замещенного или незамещенного алкила,замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила и замещенного или незамещенного гетероциклоалкила и s и t независи- 22019962 мо равны целым числам от 1 до 6. Предпочтительно R20, R25, R25', R26 и R26' являются гидрофобными. В некоторых вариантах R20 представляет собой Н или алкил (предпочтительно незамещенный низший алкил). В некоторых вариантах R25, R25, R26 и R26' независимо представляют собой Н или алкил (предпочтительно незамещенный С 1-С 4-алкил). В некоторых вариантах R25, R25', R26 и R26' все представляют собой Н. В некоторых вариантах t равно 1 и s равно 1 или 2. Пептидные линкеры (F). Как обсуждалось выше, пептидильные линкеры по изобретению могут быть представлены общей формулой: (L4)p-F-(L1)m, где F представляет часть линкера, включающую пептидильный фрагмент. В одном из вариантов часть F необязательно включает дополнительный саморазрушающийся линкер(ы), L2, и карбонильную группу. В другом варианте часть F включает аминогруппу и необязательную спейсерную группу(ы) L3. Соответственно, в одном из вариантов конъюгат включает пептидильный линкер, содержащий структуру формулы (4) В данном варианте L1 представляет собой саморазрушающийся линкер, как изложено выше, и L4 является фрагментом, который предпочтительно обеспечивает повышенную растворимость или сниженные агрегационные свойства, или изменяет скорость гидролиза, как изложено выше. L2 представляет саморазрушающийся линкер(ы). Кроме того, m равно 0, 1, 2, 3, 4, 5 или 6 и о и р независимо равны 0 или 1. АА 1 представляет одну или несколько природных аминокислот и/или неприродные -аминокислоты; с равно целому числу в интервале от 1 до 20. В некоторых вариантах с равно 2-5 или с равно 2 или 3. В описанных выше пептидных линкерах по изобретению формулы (4) АА 1 связан на аминоконце непосредственно с L4 или, если L4 отсутствует, непосредственно с группой X4 (т.е. направляющим агентом, определяемой меткой, защищенной реакционноспособной функциональной группой или незащищенной реакционноспособной функциональной группой). В некоторых вариантах, если L4 присутствует,L4 не включает карбоксильную группу ацила, непосредственно присоединенную к N-концу (АА 1)с. Таким образом, в таких вариантах карбоксильный фрагмент ацила не обязательно расположен непосредственно между L4 или X4 и АА 1, как это необходимо для пептидных линкеров в соответствии с патентом США 6214345. В другом варианте конъюгат, содержащий пептидильный линкер, включает структуру формулы (5): В данном варианте L4 представляет собой фрагмент, который предпочтительно обеспечивает повышенную растворимость или сниженные агрегационные свойства или изменяет скорость гидролиза, как изложено выше; L3 представляет собой спейсерную группу, включающую первичный или вторичный амин или карбоксильную функциональную группу, и амин L3 образует амидную связь с боковой карбоксильной функциональной группой D, или карбоксильная группа L3 образует амидную связь с боковой функциональной группой амина D; о и р независимо равны 0 или 1. АА 1 представляет одну или несколько природных аминокислот и/или не встречающихся в природе -аминокислот; с равно целому числу от 1 и 20. В данном варианте L1 отсутствует (т.е. m равно 0, представляет собой общую формулу). В пептидных линкерах по изобретению описанной выше формулы (5) АА 1 связан на N-конце непосредственно с L4 или, если L4 отсутствует, непосредственно с группой X4 (т.е. направляющим агентом,определяемой меткой, защищенной реакционноспособной функциональной группой или незащищенной реакционноспособной функциональной группой). В некоторых вариантах, если L4 присутствует, L4 не включает карбоксильную ацильную группу, непосредственно присоединенную к N-концу (АА 1)с. Таким образом, в таких вариантах карбоксильный фрагмент ацила не обязательно расположен непосредственно между L4 или X4 и АА 1, как это необходимо для пептидных линкеров в соответствии с патентом США 6214345. Саморазрушающийся линкер L2. Саморазрушающийся линкер L2 представляет собой бифункциональный химический фрагмент,способный ковалентно связывать вместе два отстоящих друг от друга химических фрагмента в молекулу из 3 частей с обычной стабильностью, высвобождая один из указанных размещенных химических фрагментов молекулы из 3 частей с помощью ферментного расщепления; причем после указанного ферментного расщепления происходит самопроизвольное отщепление от остальной части молекулы, для высвобождения второго из указанных размещенных химических фрагментов. В соответствии с настоящим изобретением саморазрушающийся спейсер ковалентно присоединен одним своим концом к пептидному- 23019962 фрагменту и ковалентно связан другим своим концом с химически реакционноспособным сайтом фрагмента лекарственного средства, дериватизация которого подавляет фармакологическую активность, таким образом, чтобы расположить в пространстве и ковалентно связать вместе пептидный фрагмент и фрагмент лекарственного средства в молекулу из 3 частей, стабильную и фармакологически инертную в отсутствие целевого фермента, но которая расщепляется под действием такого целевого фермента в месте связи, ковалентно связывающей спейсерный фрагмент и пептидный фрагмент, для высвобождения таким образом пептидного фрагмента из молекулы из 3 частей. Такое ферментное расщепление, в свою очередь, активизирует саморазрушающийся элемент спейсерного фрагмента и инициирует самопроизвольное расщепление связи, ковалентно связывающей спейсерный фрагмент с фрагментом лекарственного средства, чтобы таким образом осуществить высвобождение лекарственного средства в фармакологически активной форме. Саморазрушающийся линкер L2 может представлять собой любую саморазрушающуюся группу. Предпочтительно L2 представляет собой замещенный алкил, незамещенный алкил, замещенный гетероалкил, незамещенный гетероалкил, незамещенный гетероциклоалкил, замещенный гетероциклоалкил,замещенный и незамещенный арил, а также замещенный и незамещенный гетероарил. Один из особенно предпочтительных саморазрушающихся спейсеров L2 может быть представлен формулой (6) Ароматическое кольцо аминобензильной группы может быть замещено одной или несколькими группами "K". Группа "K" представляет собой заместитель на ароматическом кольце, на который заменен водород, в противном случае присоединенный к одному из 4 незамещенных атомов углерода, которые представляют собой часть структуры кольца. Группа "K" может представлять собой одинарный атом, такой как галоген, или может представлять собой многоатомную группу, такую как алкил, гетероалкил, амино, нитро, гидрокси, алкокси, галогеналкил и циано. Каждый K независимо выбирают из группы, состоящей из замещенного алкила, незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2,NR21R22, NR21COR22, OCONR21R22, OCOR21 и OR21, где R21 и R22 независимо выбирают из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила и незамещенного гетероциклоалкила. Примеры заместителейK включают, не ограничиваясь ими, F, Cl, Br, I, NO2, ОН, ОСН 3, NHCOCH3, N(CH3)2, NHCOCF3 и метил. Для "Ka" а равно целому числу 0, 1, 2, 3 или 4. В одном из предпочтительных вариантов а равно 0. Эфирный атом кислорода показанной выше структуры соединен с карбонильной группой. Линия между функциональной группой NR24 и ароматическим кольцом показывает, что аминная функциональная группа может быть связана с любым из 5 атомов углерода, которые формируют кольцо и не замещены группой -CH2-O-. Предпочтительно функциональная группа NR24 фрагмента X ковалентно связана с ароматическим кольцом в пара-положении по отношению к группе -СН 2-О-. R24 представляет собой группу, выбранную из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила и незамещенного гетероалкила. В конкретном варианте R24 представляет собой водород. В одном варианте изобретения предлагается пептидный линкер формулы (4) выше, где F включает структуру где R24 выбирают из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила и незамещенного гетероалкила. Каждый K представляет собой член, независимо выбранный из группы, состоящей из замещенного алкила, незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, замещенного арила, незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила, галогена, NO2, NR21R22, NR21COR22, OCONR21R22,OCOR21 и OR21, где R21 и R22 независимо выбирают из группы, состоящей из Н, замещенного алкила,незамещенного алкила, замещенного гетероалкила, незамещенного гетероалкила, замещенного арила,незамещенного арила, замещенного гетероарила, незамещенного гетероарила, замещенного гетероциклоалкила, незамещенного гетероциклоалкила; а равно целому числу 0, 1, 2, 3 или 4. В другом варианте пептидный линкер формулы (4) выше включает -F-(L1)m-, содержащий структу где каждый из R24 представляет собой член, независимо выбранный из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила и незамещенного гетероалкила. В некоторых вариантах саморазрушающийся спейсер L1 или L2 включает где каждый из R17, R18 и R19 независимо выбирают из Н, замещенного или незамещенного алкила,замещенного или незамещенного гетероалкила и замещенного или незамещенного арила иw равно целому числу от 0 до 4. В некоторых вариантах R17 и R18 независимо представляют собой Н или алкил (предпочтительно незамещенный C1-4 алкил). Предпочтительно R17 и R18 представляют собой C1-4 алкил, такой как метил или этил. В некоторых вариантах w равно 0. Без желания привязываться к какой-либо конкретной теории, экспериментально было обнаружено, что циклизация такого конкретного саморазрушающегося спейсера происходит относительно быстро. В некоторых вариантах L1 или L2 включает Спейсерная группа L3. Спейсерная группа L3 отличается тем, что включает первичный или вторичный амин или карбоксильную функциональную группу, и амин группы L3 образует амидную связь с боковой карбоксильной функциональной группой D, или карбоксильная группа L3 образует амидную связь с боковой функциональной аминогруппой D. L3 выбирают из группы, состоящей из замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила или замещенного или незамещенного гетероциклоалкила. В предпочтительном варианте L3 включает ароматическую группу. Более предпочтительно L3 включает группу бензойной кислоты, анилиновую группу или индольную группу. Не ограничивающие примеры структур,которые могут служить в качестве спейсера -L3-NH- включают следующие структуры: где Z представляет собой группу, выбранную из О, S и NR23, R23 представляет собой группу, вы- 25019962 бранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила. При расщеплении линкера по изобретению, содержащего L3, фрагмент L3 остается присоединенным к лекарственному средству D. Соответственно, фрагмент L3 выбирают таким образом, что его присутствие в присоединенном к D виде существенно не изменяет активности D. В другом варианте часть лекарственного средства D сама по себе функционирует как спейсер L3. Например, в одном из вариантов лекарственное средство D представляет собой производное дуокармицина, в котором фрагмент лекарственного средства функционирует как спейсер L3. Не ограничивающие примеры таких вариантов включают такие, в которых NH2-(L3)-D имеет структуру, выбранную из группы, состоящей из в которой Z представляет собой группу, выбранную из О, S и NR23, где R23 представляет собой группу, выбранную из Н, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила и ацила; и группа NH2 на каждой структуре реагирует с (АА 1)c с образованием -(AA1)c-NH-. Пептидная последовательность АА 1. Группа АА 1 представляет одинарную аминокислоту или несколько аминокислот, соединенных между собой амидными связями. Аминокислоты могут являться природными аминокислотами и/или неприродными -аминокислотами. Пептидная последовательность (АА 1)c с функциональной точки зрения представляет собой остаток амидирования одинарной аминокислоты (если с=1) или нескольких аминокислот, соединенных вместе амидными связями. Пептид по настоящему изобретению выбирают таким образом, чтобы направить катализируемое ферментами расщепление пептида ферментом на целевой участок в биологической системе. Например, для конъюгатов, которые нацеливают на клетку с помощью направляющих средств, и которые затем захватываются клеткой, выбирают пептид, который расщепляется одной или несколькими лизосомальными протеазами таким образом, что пептид расщепляется внутриклеточно в пределах лизосомы. Количество аминокислот в пределах пептида может варьировать от 1 до 20; но более предпочтительно будет составлять 2-8 аминокислот, 2-6 аминокислот или 2, 3 или 4 аминокислоты, включающие(АА 1)c. Пептидные последовательности, чувствительные к расщеплению конкретными ферментами или классами ферментов, хорошо известны из уровня техники. Многие пептидные последовательности, которые расщепляются ферментами в сыворотке, печени,кишечнике и т.п., известны из уровня техники. Пример последовательности пептида по изобретению включает пептидную последовательность, которая расщепляется протеазой. Фокус нижеследующего обсуждения применения чувствительной к действию протеаз последовательности предназначен для ясности иллюстрации и не предназначен для ограничения контекста настоящего изобретения. Если фермент, который расщепляет пептид, представляет собой протеазу, в целом линкер включает пептид, содержащий последовательность распознавания расщепления для протеазы. Последовательность распознавания расщепления для протеазы представляет собой определенную последовательность аминокислот, которая распознается протеазой в ходе протеолитического расщепления. Множество сайтов расщепления протеазой известны из уровня техники, и эти и другие сайты расщепления могут входить вAlzheimer's Disease, ed. Masters et al. p. 190-198 (1994). Аминокислоты пептидной последовательности (АА 1)c выбирают на основании их чувствительности к селективному ферментному расщеплению специфическими молекулами, такими как связанная с опухолью протеаза. Используемые аминокислоты могут быть природными или неприродными аминокислотами. Они могут находиться в L- или D-конфигурации. В одном из вариантов используются как минимум три различные аминокислоты. В другом варианте используются только две аминокислоты. В предпочтительном варианте пептидную последовательность (АА 1)c выбирают на основании ее способности расщепляться лизосомальными протеазами, не ограничивающие примеры которых включают катепсины В, С, D, H, L и S. Предпочтительно пептидная последовательность (АА 1)c способна расщепляться катепсином В in vitro, что может быть проверено с использованием испытаний на расщепление протеазой in vitro, известных из уровня техники. В другом варианте пептидную последовательность (АА 1)c выбирают на основании ее способности расщепляться связанной с опухолью протеазой, такой как протеаза, найденная во внеклеточном пространстве в непосредственной близости от опухолевых клеток, не ограничивающие примеры которой включают тимет олигопептидазу (ТОП) и CD10. Способность пептида расщепляться ТОП или CD10 можно проверить с помощью испытаний на расщепление протеазой in vitro, известных из уровня техники. Подходящие, но не ограничивающие, примеры пептидных последовательностей, пригодных для использования в конъюгатах по изобретению включают Val-Cit, Cit-Cit, Val-Lys, Phe-Lys, Lys-Lys,Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys,D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID NO: 1),-Ala-Leu-Ala-Leu (SEQ ID NO: 2), Gly-Phe-Leu-Gly (SEQ ID NO: 3), Val-Ala, Leu-Leu-Gly-Leu(SEQ ID NO: 14), Leu-Asn-Ala и Lys-Leu-Val. Предпочтительные пептидные последовательности - Val-Cit и Val-Lys. В другом варианте аминокислоту, расположенную непосредственно около фрагмента лекарственного средства, выбирают из группы, состоящей из Ala, Asn, Asp, Cit, Cys, Gln, Glu, Gly, Ile, Leu, Lys, Met,Phe, Pro, Ser, Thr, Trp, Tyr и Val. Еще в одном варианте аминокислоту, расположенную непосредственно около фрагмента лекарственного средства, выбирают из группы, состоящей из: Ala, Asn, Asp, Cys, Gln,Glu, Gly, Ile, Leu, Met, Phe, Pro, Ser, Thr, Trp, Tyr и Val. Протеазы принимают участие в образовании метастазов рака. Увеличенный синтез протеазы урокиназы коррелировал с увеличенной способностью к образованию метастазов при многих видах рака. Урокиназа активизирует плазмин из плазминогена, который находится повсеместно во внеклеточном пространстве, и его активация может вызвать разложение белков во внеклеточном матриксе, через которые происходит инвазия опухолевых клеток. Плазмин может также активизировать коллагеназу, таким образом способствуя разложению коллагена в базальной мембране, окружающей капилляры и лимфатическую систему, таким образом позволяя инвазию клеток опухоли в ткани-мишени (Dano, et al. Adv.Cancer. Res., 44: 139 (1985. Таким образом, в пределах контекста настоящего изобретения находится использование в качестве линкера пептидной последовательности, которая расщепляется урокиназой. В изобретении также предлагается использование пептидных последовательностей, чувствительных к расщеплению триптазами. Тучные клетки человека экспрессируют как минимум четыре различных триптазы, обозначенные , I, II и III. Эти ферменты не контролируются ингибиторами протеиназы плазмы крови и расщепляют только несколько физиологических субстратов in vitro. Триптазное семейство сериновых протеаз принимает участие в различных аллергических и воспалительных заболеваниях, вовлекающих тучные клетки вследствие повышенных уровней триптаз, найденных в биологических жидкостях больных такими расстройствами. Однако точная роль триптазы в патофизиологии заболеваний нуждается в прояснении. Контекст биологических функций и соответствующих физиологических последствий триптазы в существенной мере определяется их специфичностью в отношении субстрата. Триптаза представляет собой мощный активатор проурокиназного активатора плазминогена(uPA), проферментной формы протеазы, связанной с метастазированием и инвазией опухолей. Активация каскада плазминогена, приводящая к уничтожению внеклеточной матрицы для экстравазации и миграции клеток может быть функцией активации триптазой проурокиназного активатора плазминогена в последовательности Р 4-Р 1 Pro-Arg-Phe-Lys (SEQ ID NO: 4) (Stack, et al., Journal of Biological Chemistry 269 (13): 9416-9419 (1994. Вазоактивный кишечный пептид, нейропептид, который принимает участие в регулировании проницаемости сосудов, также расщепляется триптазой, прежде всего в последовательности Thr-Arg-Leu-Arg (SEQ ID NO: 5) (Tam, et al., Am. J. Respir. Cell Mol. Biol. 3: 27-32 (1990. Связанный с G-протеином рецептор PAR-2 может расщепляться и активизироваться триптазой в последова- 27019962 тельности Ser-Lys-Gly-Arg (SEQ ID NO: 6), чтобы управлять размножением фибробластов, тогда как активизированный тромбином рецептор PAR-1 инактивируется триптазой в последовательностиPro-Asn-Asp-Lys (SEQ ID NO: 7) (Molino et al., Journal of Biological Chemistry, 272(7): 4043-4049 (1997. Взятые вместе, эти доказательства наводят на предположение о центральной роли триптазы в ремоделировании тканей как последствии заболевания. Это согласуется с глубокими изменениями, наблюдаемыми при нескольких расстройствах, опосредованных тучными клетками. Одним из отличительных признаков хронической астмы и других дыхательных болезней длительного течения является фиброз и утолщение базальных тканей, которые могут быть результатом активации триптазой ее физиологических мишеней. Подобным образом, серия отчетов продемонстрировала связь ангиогенеза с плотностью тучных клеток, активностью триптазы и неблагоприятным прогнозом при различных видах рака (Coussens etal., Genes and Development, 13(11): 1382-97 (1999; Takanami et al., Cancer, 88(12): 2686-92 (2000); TothJakatics et al., Human Pathology, 31(8): 955-960 (2000); Ribatti et al., International Journal of Cancer, 85(2): 171-5 (2000. Из уровня техники известны методы оценки того, расщепляет ли конкретная протеаза выбранную пептидную последовательность. Например, использование флюорогенных пептидных субстратов 7-амино-4-метилкумарина (АМК) представляет собой широко распространенный метод определения специфичности протеаз (Zimmerman, M., et al. (1977), Analytical Biochemistry, 78:47-51). Специфическое расщепление анилидной связи высвобождает уходящую флюорогенную группу АМК, что позволяет несложно определить скорость расщепления для индивидуальных субстратов. Позже массивы (Lee, D., etal. (1999), Bioorganic and Medicinal Chemistry Letters, 9: 1667-72) и библиотеки позиционного сканирования (Rano, Т.A., et al. (1997), Chemistry and Biology, 4: 149-55) библиотек пептидного субстрата АМК использовали для быстрого построения профиля N-концевой специфичности протеаз путем отбора образцов широкого спектра субстратов в единичном эксперименте. Таким образом, специалист в данной области может легко оценить массив пептидных последовательностей с целью определения их пригодности для настоящего изобретения без излишнего экспериментирования. Конъюгат "лекарственное средство-лиганд" по настоящему изобретению может необязательно содержать два или несколько линкеров. Такие линкеры могут быть одинаковыми или разными. Например,пептидильный линкер может использоваться для соединения лекарственного средства с лигандом, и второй пептидильный линкер может присоединить диагностическое средство к комплексу. Другие виды применения дополнительных линкеров включают присоединение аналитических средств, биомолекул,направляющих агентов и определяемых меток к комплексу "лекарственное средство-лиганд". Также в пределах контекста настоящего изобретения находятся соединения по изобретению, которые являются разновидностями поли- или мультивалентных молекул, в том числе, например, таких молекул, как димеры, тримеры, тетрамеры и высшие гомологи соединений по изобретению или их реакционноспособных аналогов. Поли- и мультивалентные формы могут быть собраны из одинарных молекул или нескольких видов молекул по изобретению. Например, димерная конструкция может быть "гомодимерной" или "гетеродимерной". Кроме того, поли- и мультивалентные конструкции, в которых соединение по изобретению или его реакционноспособный аналог присоединен к олигомерной или полимерной структуре (например, полилизин, декстран, гидроксиэтилкрахмал и т.п.) находятся в пределах контекста настоящего изобретения. Структура предпочтительно является полифункциональной (т.е. содержит массив реакционноспособных сайтов для присоединения соединений по изобретению). Кроме того, могут быть образованы производные структуры с одинарными молекулами по изобретению или нескольких видов молекул по изобретению. Кроме того, настоящее изобретение включает соединения, в которые введены функциональные группы, с образованием соединений, обладающих повышенной растворимостью в воде по сравнению с аналогичными соединениями, которые не содержат таких функциональных групп. Таким образом, любой из заместителей, описанных в данном описании, может быть заменен аналогичным радикалом, который повышает растворимость в воде. Например, в пределах контекста изобретения находится замена гидроксильной группы на диол, амина на четверичный амин, гидроксиамин или подобный фрагмент с большей растворимостью в воде. В предпочтительном варианте дополнительная растворимость в воде обеспечивается заменой на сайте, несущественном для активности по направлению к каналу ионов соединений,описанных в данном изобретении, фрагментом, который увеличивает растворимость в воде исходных соединений. Способы повышения растворимости в воде органических соединений известны из уровня техники. Такие методы включают, не ограничиваясь ими, введение функциональных групп в органическое ядро с постоянно заряженным фрагментом, например четвертичного аммония, или группа, которая является заряженной при физиологически уместных значениях рН, например карбоновая кислота, амин. Другие способы включают присоединение к органическому ядру гидроксил- или аминосодержащих групп, таких как спирты, полиолы, полиэфиры и т.п. Характерные примеры включают, не ограничиваясь ими, полилизин, полиэтиленимин, поли(этиленгликоль) и поли(пропиленгликоль). Подходящие химические методы введения функциональных групп и стратегии для таких соединений известны из уровня техники. См., например, Dunn, R.L., et al., Eds. Polymeric Drugs and Drug Delivery Systems, ACS- 28019962 Гидразиновые линкеры (Н). Во втором варианте конъюгат по изобретению включает гидразиновый саморазрушающийся линкер, где структура конъюгата является следующей: где D, L1, L4 и X4 являются такими, как определено выше и дополнительно описано в данном документе; и Н представляет собой линкер, содержащий структуру где n1 равно целому числу от 1 до 10;n2 равно 0, 1 или 2; каждый из R24 представляет собой член, независимо выбранный из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила и незамещенного гетероалкила; иI представляет собой связь (т.е., связь между атомом углерода скелета и смежным атомом азота),или: где R представляет собой Me или СН 2-СН 2-NMe2. В одном из вариантов замещение в фенильном кольце представляет собой пара-замещение. В предпочтительных вариантах n1 равно 2, 3 или 4 или n1=3. В предпочтительных вариантах n2=1. В предпочтительных вариантах I представляет собой связь (т.е. связь между атомом углерода скелета и смежным атомом азота). В одном аспекте гидразиновый линкер, Н, при расщеплении может образовывать 6-членный саморазрушающийся линкер, например, если n3=0 и n4=2. В другом аспекте гидразиновый линкер, Н, при расщеплении может образовывать два 5-членных саморазрушающихся линкера. В других аспектах Н образует 5-членный саморазрушающийся линкер, Н образует 7-членный саморазрушающийся линкер, или Н при расщеплении образует 5-членный саморазрушающийся линкер и 6-членный саморазрушающийся линкер. На скорость расщепления влияет размер кольца, образованного при расщеплении. Таким образом, в зависимости от желательной скорости расщепления, может быть выбран подходящий размер кольца, которое будет образовываться при расщеплении. 5-Членные гидразиновые линкеры. В одном из вариантов гидразиновый линкер включает 5-членный гидразиновый линкер, где Н включает структуру: В предпочтительном варианте n1 равно 2, 3 или 4. В другом предпочтительном варианте n1=3. В описанной выше структуре каждый из R24 представляет собой член, независимо выбранный из группы, состоящей из Н, замещенного алкила, незамещенного алкила, замещенного гетероалкила и незамещенного гетероалкила. В одном из вариантов каждый из R24 независимо представляет собой Н илиC1-C6 алкил. В другом варианте каждый из R24 независимо представляет собой Н или C1-C3 алкил, более предпочтительно Н или СН 3. В другом варианте как минимум один R24 представляет собой метильную группу. В другом варианте каждый из R24 представляет собой Н. Каждый R24 выбирают таким образом,чтобы адаптировать стерические эффекты соединения, а также для изменения растворимости.
МПК / Метки
МПК: C07D 403/14, A61K 47/48, A61P 35/00, C07D 487/04, A61K 49/00
Метки: цитотоксинов, конъюгаты
Код ссылки
<a href="https://eas.patents.su/30-19962-konyugaty-citotoksinov.html" rel="bookmark" title="База патентов Евразийского Союза">Конъюгаты цитотоксинов</a>
Предыдущий патент: Антагонисты киназы
Случайный патент: Производные n-(1h-индолил)-1н-индол-2-карбоксамидов, их получение и их применение в терапии