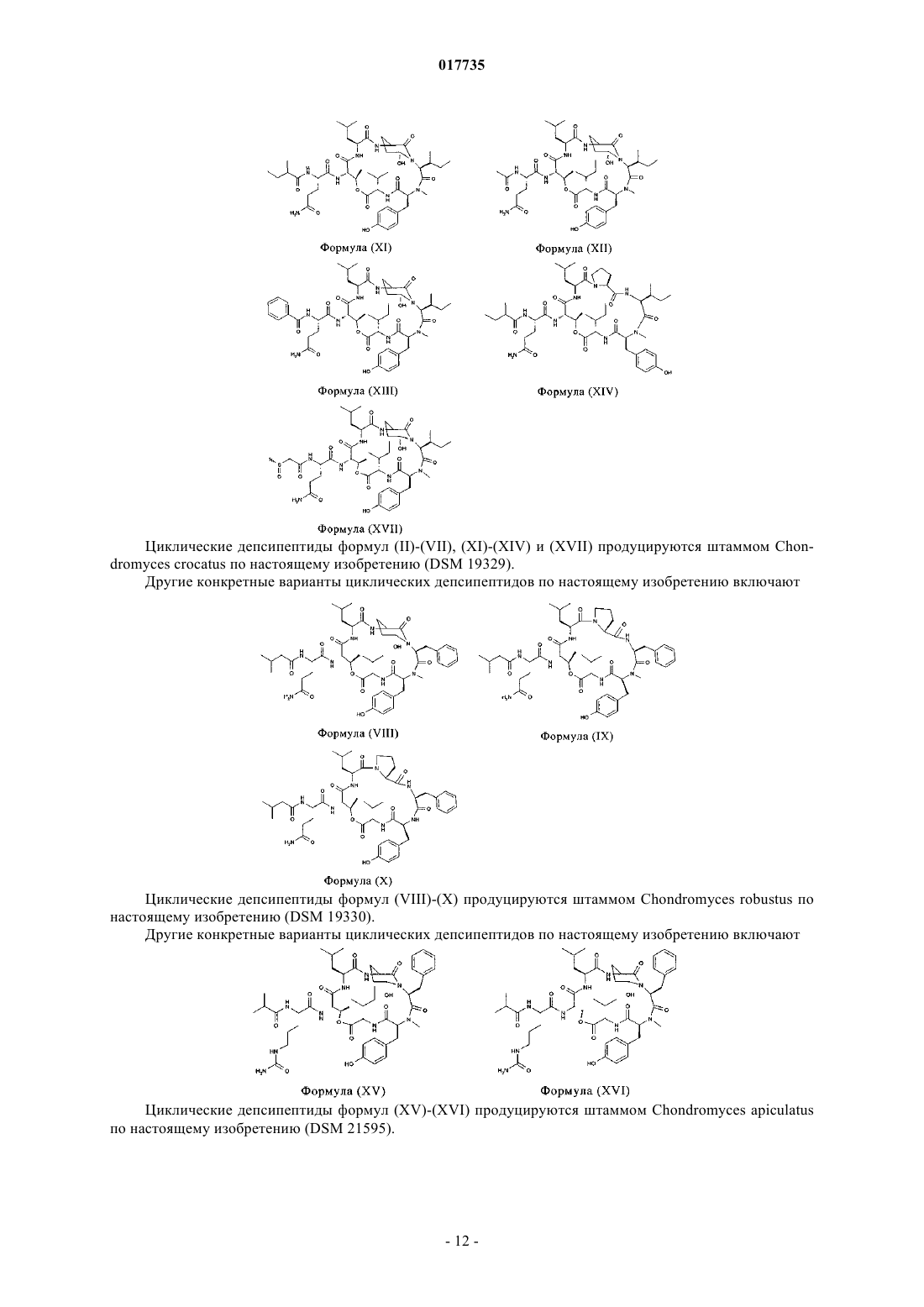
Циклические депсипептиды
Номер патента: 17735
Опубликовано: 28.02.2013
Авторы: Крастель Филипп, Лихти Бригитта-Мария, Майнгасснер Йозеф Готтфрид, Шрайнер Эрвин Пол, Шмитт Эстер
Формула / Реферат
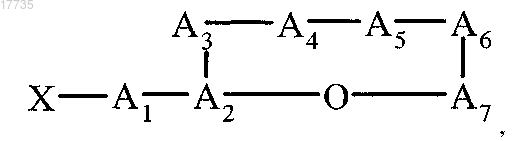
1. Циклический депсипептид, характеризующийся формулой (I)
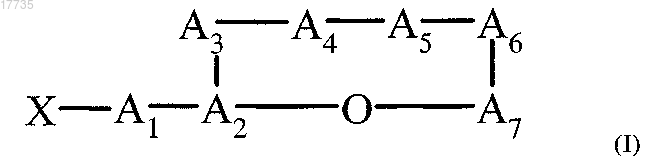
где сложноэфирная связь образуется между карбоксигруппой А7 и гидроксигруппой A2,
где ацильный остаток X обозначает CH3CH2CH(CH3)CO или (CH3)2CHCO,
A1 обозначает глутамин, глутаминовую кислоту или их производные,
A2 обозначает треонин,
A3 обозначает лейцин,
A4 обозначает Ahp, 3-аминопиперидин-2-он, пролин, 5-гидроксипролин или его производное,
А5 обозначает изолейцин,
A6 обозначает тирозин, N-Me-тирозин или его производное,
А7 обозначает изолейцин или валин, предпочтительно изолейцин, или
его фармацевтически приемлемая соль.
2. Депсипептид по п.1, где атом азота амидной связи между А5 и A6 замещен метилом, а группа ОН в остатке тирозина обозначает OR, где R выбирают из группы, включающей водород, С1-С12алкил, C2-С12алкенил, С2-С12алкинил, галоген(C1-C12)алкил, галоген(C2-C12)алкенил, галоген(C2-C12)алкинил, C1-С12алкоксикарбонил, С1-С12алкоксикарбонил(C1-C12)алкил, C1-С12алкиламинокарбонил, незамещенный или дополнительно замещенный арилом, арилалкилом, арилалкенилом или арилалкинилом, гетероциклилом и гетероциклилалкилом.
3. Циклический депсипептид по любому из предшествующих пунктов, где A1 обозначает глутаминовую кислоту или ее производное и указанный депсипептид выбирают из нитрила глутамина, сложного эфира глутаминовой кислоты, такого как С1-С12алкиловый эфир (например, метиловый эфир глутаминовой кислоты) или С6-С24ариловый эфир (например, фениловый или бензиловый эфир глутаминовой кислоты).
4. Депсипептид по п.1, который обозначает соединение формулы А или В
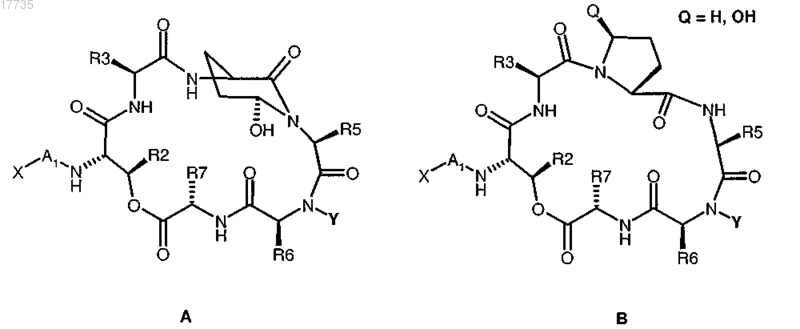
где X и A1 имеют значения, определенные в п.1, и где
R2 обозначает боковую цепь треонина,
R3 обозначает боковую цепь лейцина,
R5 обозначает боковую цепь изолейцина,
R6 обозначает боковую цепь тирозина, необязательно модифицированного, прежде всего необязательно модифицированного по гидроксильной группе, по п.2,
R7 обозначает боковую цепь изолейцина или валина, прежде всего R7 обозначает боковую цепь изолейцина,
Y обозначает водород или метил, прежде всего Y обозначает метил.
5. Циклический депсипептид по п.4, где X обозначает (CH3)2CHCO.
6. Циклический депсипептид по п.4, где R7 обозначает боковую цепь изолейцина.
7. Циклический депсипептид по любому из предшествующих пунктов, где A1, A2, A3, A5, A6 и А7 обозначают L-аминокислоты.
8. Циклический депсипептид по любому из предшествующих пунктов, где А4 обозначает (3S,6R)-Ahp.
9. Циклический депсипептид по любому из предшествующих пунктов, выбранный из
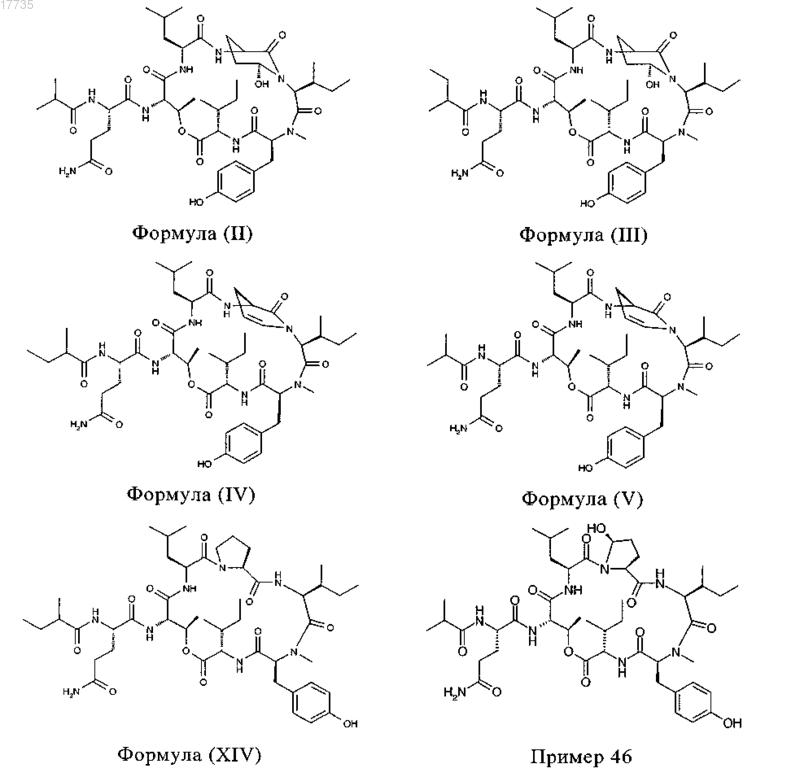
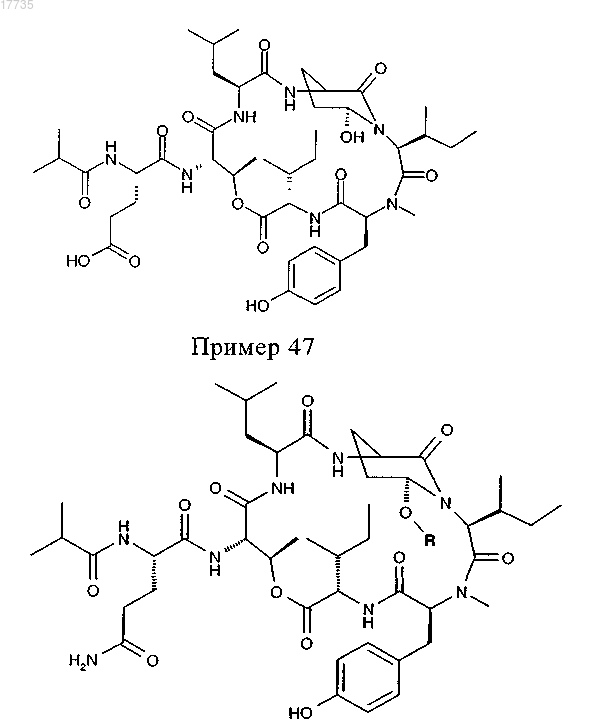
где R выбирают из следующих групп:


где R и R2 выбирают из следующих групп:
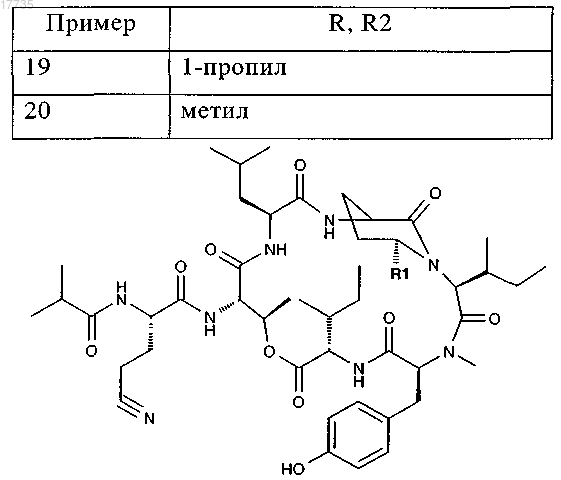
где R1 выбирают из следующих групп:
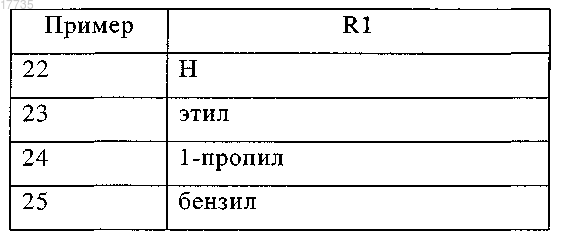
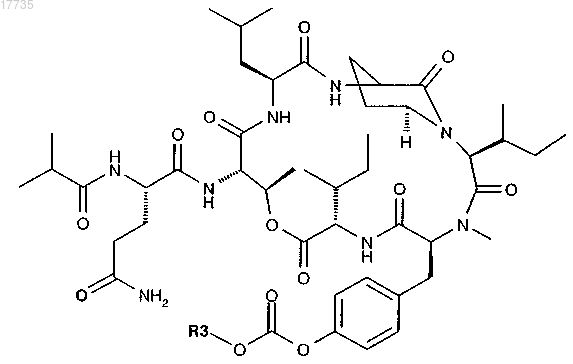
где R3 выбирают из следующих групп:
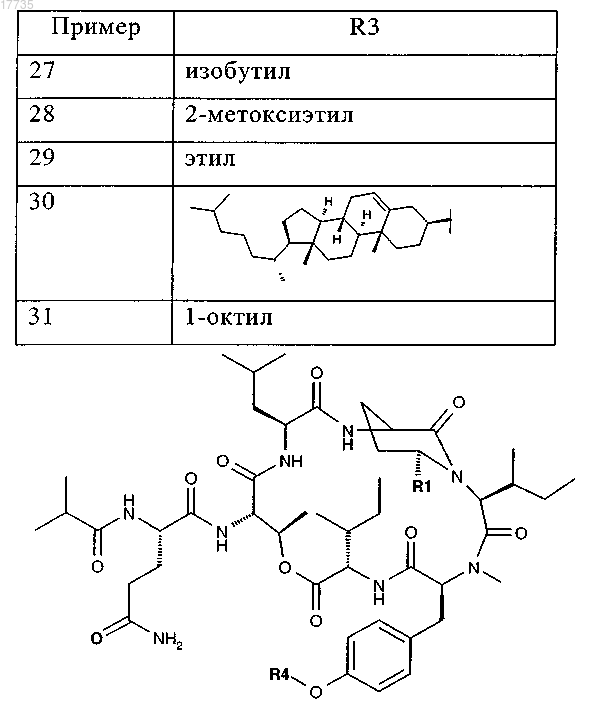
где R1 и R4 выбирают из следующих групп:

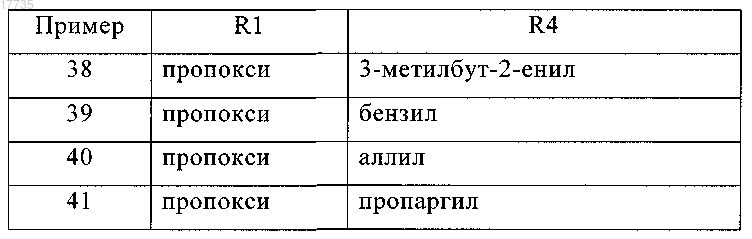
10. Фармацевтическая композиция, обладающая ингибирующей активностью калликреин-7, включающая терапевтически эффективное количество циклического депсипептида по любому из предшествующих пунктов в смеси с фармацевтически приемлемым носителем и/или ингредиентом.
11. Применение циклического депсипептида по любому из пп.1-9 для получения лекарственного средства, предназначенного для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников, муковисцидоз (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых, хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза или астмы.
12. Способ лечения субъекта, страдающего от воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников, муковисцидоз (MB), хроническое обструктивное заболевание легких (ХОЗЛ), фиброз легких, респираторный дистресс-синдром взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника, псориаз, астма, и указанный способ заключается во введении указанному субъекту терапевтически эффективного количества циклического депсипептида по любому из пп.1-9.
13. Способ лечения субъекта по п.12, где субъект страдает от келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников.
14. Способ лечения субъекта по п.13, где субъект страдает от келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, такой как старческая кожа.
15. Способ лечения субъекта по п.12, где субъект страдает от муковисцидоза (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых, хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, астмы.
16. Применение циклического депсипептида по любому из пп.1-9 для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или от других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников, муковисцидоз (MB), хроническое обструктивное заболевание легких (ХОЗЛ), фиброз легких, респираторный дистресс-синдром взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника, псориаз и астма.
17. Применение по п.16 для лечения келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников.
18. Применение по п.17 для лечения келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа.
19. Применение по п.16 для лечения муковисцидоза (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых, хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, астмы.
20. Способ по пп.12-15, где лечение проводят местным или системным способом, в виде кремов, мазей и суппозиториев, или пероральным, или подкожным, или внутривенным способом или ингаляцией, соответственно.
21. Применение по пп.16-19, где лечение проводят местным или системным способом, в виде кремов, мазей и суппозиториев, или пероральным, или подкожным, или внутривенным способом или ингаляцией, соответственно.
22. Способ продуцирования циклического депсипептида или его производного по любому из пп.1-9, который заключается в культивировании штамма Chondromyces, его вариантов или мутантных форм в пригодной среде и, необязательно, химической модификацией полученного таким образом циклического депсипептида.
23. Способ продуцирования циклического депсипептида или его производного по любому из пп.1-9, который заключается в экспрессии генов биосинтеза штамма Chondromyces, его вариантов или мутантных форм в гетерологическом микробном штамме-хозяине и, необязательно, химической модификацией полученного таким образом циклического депсипептида.
24. Способ по п.22 или 23, где штамм обозначает Chondromyces crocatus (DSM 19329).
25. Выделенный штамм микроорганизма Chondromyces, продуцирующий циклический депсипептид или его производное по любому из пп.1-9, депонированный в коллекции DSM под номером DSM 19329.
26. Циклический депсипептид или его производное, продуцированный выделенным штаммом микроорганизма Chondromyces по п.25 или полученный способом по пп.22, 23.
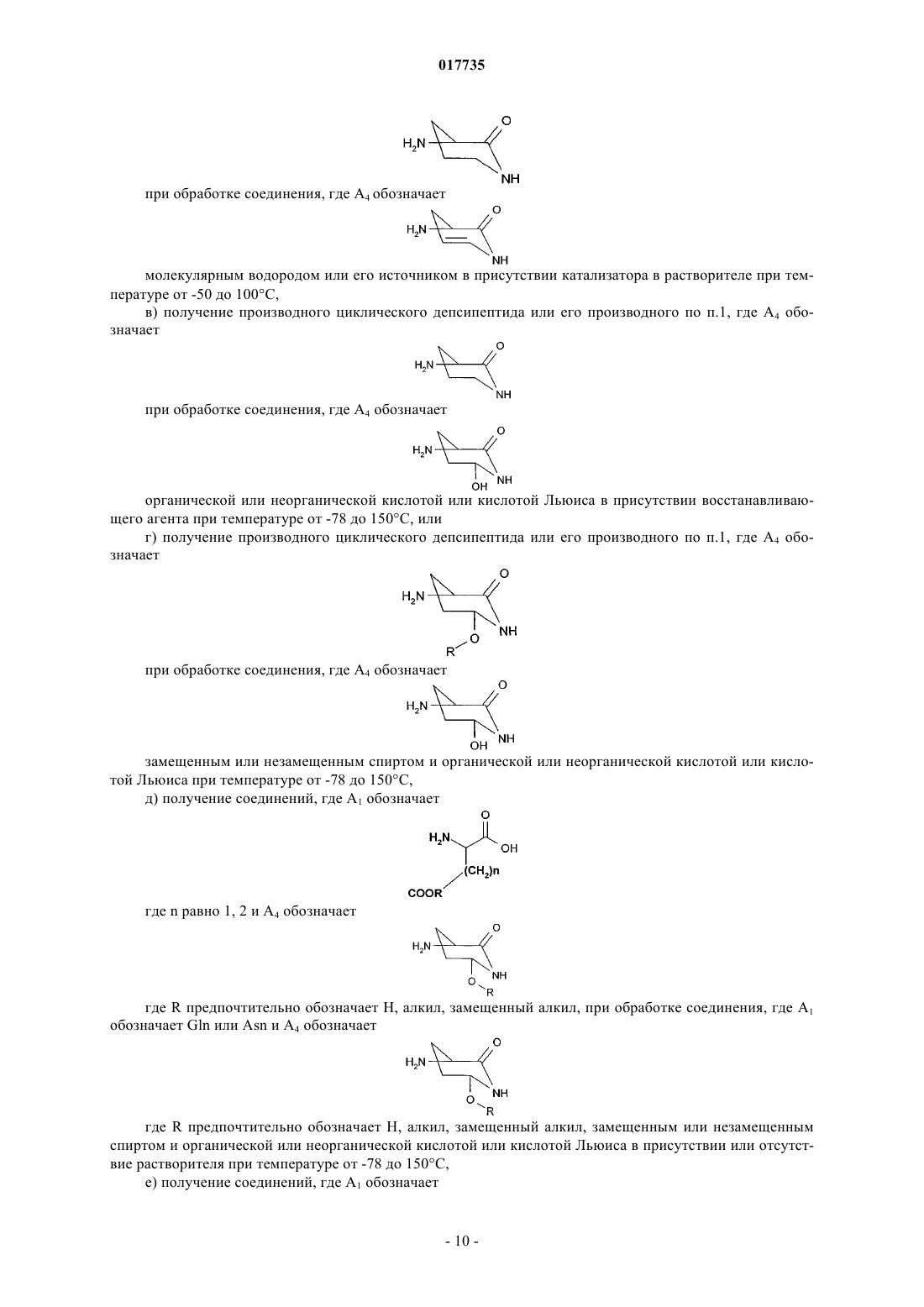
27. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
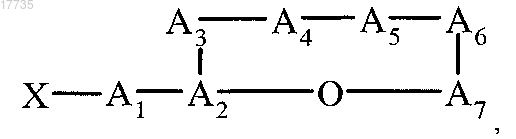
где A1-A3, А5-А7, X указаны в п.1, а А4 обозначает
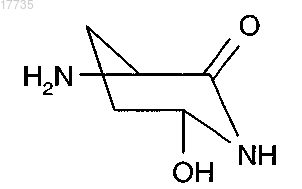
органической или неорганической кислотой или кислотой Льюиса при температуре от -78 до 150°C, с получением соединения формулы (I)
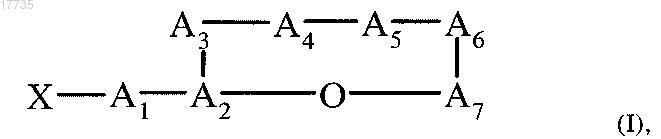
где А4 обозначает
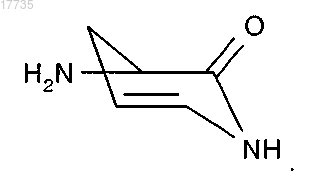
28. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
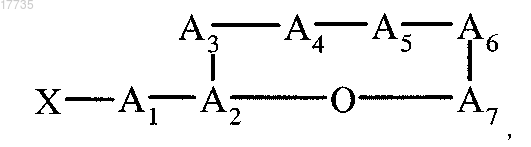
где A1-A3, A5-A7, X указаны в п.1, а А4 обозначает
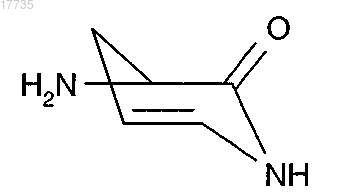
молекулярным водородом или его источником в присутствии катализатора в растворителе при температуре от -50 до 100°C, с получением соединения формулы (I)
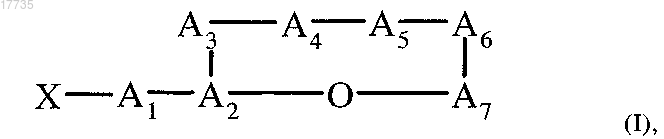
где А4 обозначает
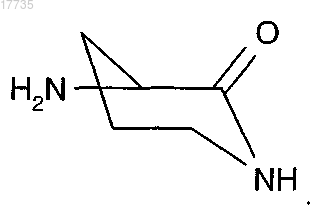
29. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
где A1-A3, A5-A7, X указаны в п.1, а A4 обозначает
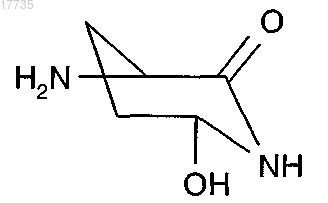
органической или неорганической кислотой или кислотой Льюиса в присутствии восстанавливающего агента при температуре от -78 до 150°C, с получением соединения формулы (I)
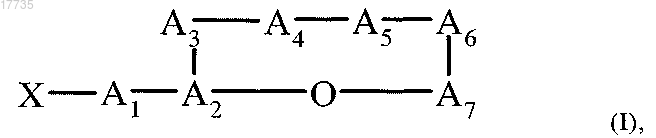
где A4 обозначает
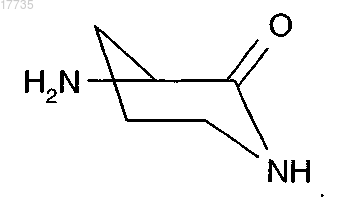
30. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
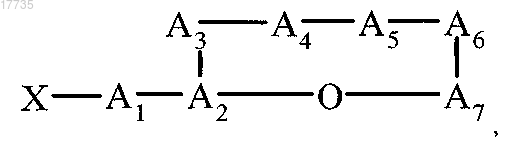
где A1-A3, A5-A7, X указаны в п.1, а A4 обозначает
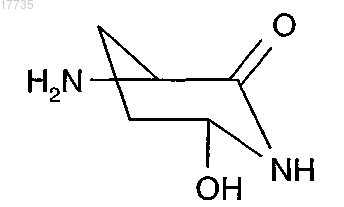
замещенным или незамещенным спиртом и органической или неорганической кислотой или кислотой Льюиса при температуре от -78 до 150°C, с получением соединения формулы (I)
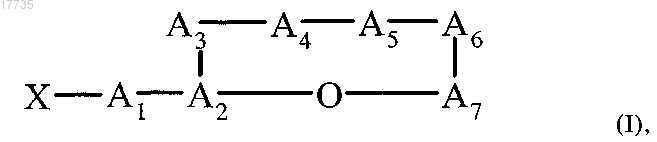
где A4 обозначает

31. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
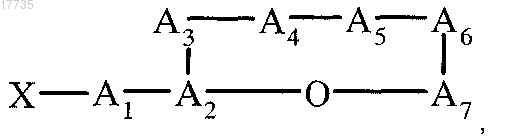
где A2-A3, A5-A7, X указаны в п.1, a A1 обозначает Gln или Asn и A4 обозначает
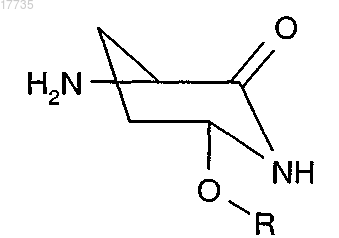
где R предпочтительно обозначает H, алкил, замещенный алкил, замещенным или незамещенным спиртом и органической или неорганической кислотой или кислотой Льюиса в присутствии или в отсутствие растворителя при температуре от -78 до 150°C, с получением соединения формулы (I)

где A1 обозначает
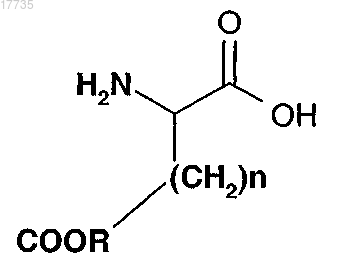
где n равно 2 и A4 обозначает
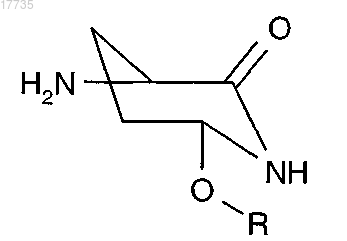
где R предпочтительно обозначает H, алкил, замещенный алкил.
32. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
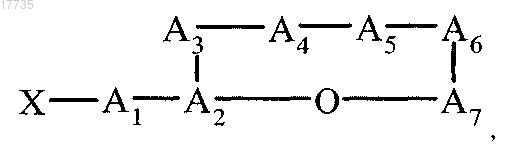
где A2-A3, A5-A7, X указаны в п.1, a A1 обозначает Gln или Asn и A4 обозначает
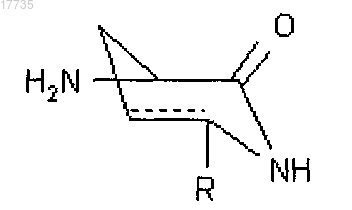
дегидратирующим агентом в присутствии или отсутствие растворителя при температуре от -78 до 150°C, с получением соединения формулы (I)
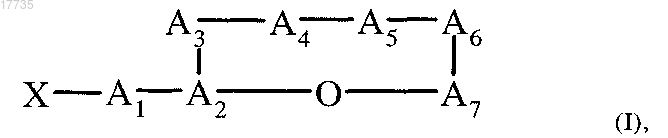
где A1 обозначает
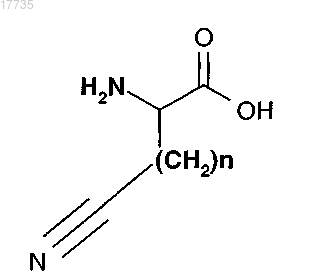
где R предпочтительно обозначает H, OH, O-алкил, замещенный О-алкил, O-ацил.
33. Способ получения производного циклического депсипептида, характеризующийся формулой (I) по п.1, который включает обработку соединения
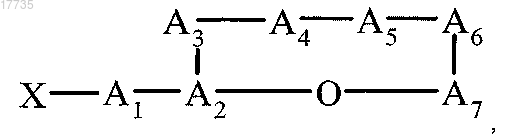
где A1-A3, A5, A7, X указаны в п.1, а А4 обозначает
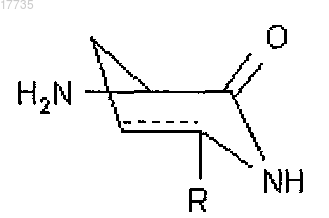
и A6 обозначает Tyr,
алкилирующим агентом или ацилирующим агентом в присутствии или в отсутствие растворителя при температуре от -78 до 150°C, с получением соединения формулы (I)
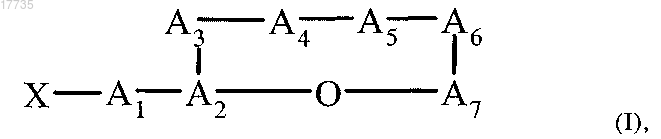
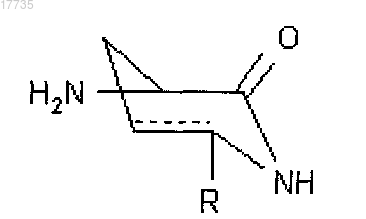
где A4 обозначает
и A6 обозначает
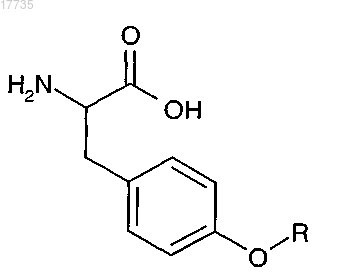
где R предпочтительно обозначает алкил, замещенный алкил, ацил, алкоксикарбонил.
Текст
Крастель Филипп (DE), Лихти Бригитта-Мария (CH), Майнгасснер Йозеф Готтфрид (AT), Шмитт Эстер(DE), Шрайнер Эрвин Пол (AT) Веселицкая И.А., Пивницкая Н.Н.,Кузенкова Н.В., Веселицкий М.Б.,Каксис Р.А., Комарова О.М., Белоусов Ю.В. (RU) Изобретение относится к циклическим депсипептидам или их производным формулы (I) и их применению, например, в качестве ингибиторов калликреина 7 или эластазы нейтрофилов человека. 017735 Область изобретения Настоящее изобретение относится к циклическим депсипептидам или к их производным. Предпосылки создания изобретения Калликреин 7 является сериновой протеазой S1, относится к семейству генов калликреина и проявляет химотрипсиноподобную активность. Калликреин 7 человека (K7 ч, KLK7 или фермент химотрипсинового типа из рогового слоя (ХРС), Swissprot P49862) играет важную роль в физиологии кожи (1, 2, 3). В основном он экспрессируется в коже, и как недавно было установлено, играет важную роль в физиологии кожи. К 7 ч принимает участие в деградации межклеточных связующих структур ороговевшего плоского эпителия в процессе отшелушивания клеток кожи. Процесс отшелушивания строго регулируется и находится в неустойчивом равновесии с продуцированием de novo корнеоцитов, чтобы поддерживать постоянную толщину рогового слоя, который является внешним слоем кожи и принимает основное участие в функционировании барьера кожи. В связи с этим было установлено, что К 7 ч расщепляет корнеодесмосомальные белки - корнеодесмозин и десмоколлин 1 (4, 5, 6). Деградация корнеодесмосом необходима для отшелушивания. Кроме того, недавно было установлено, что фермент К 7 ч расщепляет два деградирующих липиды ферментаглюкоцереброзидазу и кислую сфингомиелиназу (7). Оба деградирующих липиды фермента секретируются совместно с их субстратами - глюкозилцерамидами и сфингомиелином, и расщепляют эти полярные предшественники липидов с образованием более неполярных продуктов, например, церамидов, которые затем встраиваются во внеклеточную многослойную мембрану. Структура многослойной мембраны играет важную роль в функционировании клеточного барьера. И наконец было установлено, что К 7 ч активирует предшественник интерлейкина-1 (ИЛ-1), при этом образуется его активная форма in vitro (8). Так как кератиноциты экспрессируют ИЛ-1, но не активную форму специфического ИЛ-1 конвертирующего фермента (ИКФ или каспаза 1), можно предположить,что активация ИЛ-1 в эпидермисе человека происходит под действием другой протеазы, предположительно фермента К 7 ч. Недавно была установлена взаимосвязь повышенной активности К 7 ч с воспалительными заболеваниями кожи, такими как атопический дерматит, псориаз или синдром Незертона. Такая повышенная активность может привести к неконтролируемой деградации корнеодесмом, что в свою очередь может привести к разрегулированному отшелушиванию, повышенной деградации расщепляющих липиды ферментов и повреждению структуры многослойной мембраны или неконтролируемой активации провоспалительного цитокина ИЛ-1. В результате нарушается функционирование клеточного барьера и развивается воспаление (см. также WO-A-2004/108139). В связи с тем, что активность К 7 ч контролируется на нескольких уровнях, повышенную активность К 7 ч при воспалительных заболеваниях кожи могут вызывать различные факторы. Во-первых, на количество экспрессированной протеазы могут влиять генетические факторы. Например, в качестве такой генетической связи недавно был выявлен полиморфизм 3'-UTR(3'-нетранслируемая область) в гене К 7 ч (9). Авторы предполагают, что описанная вставка из 4 п.о. в 3'-UTR гена К 7 ч стабилизирует мРНК К 7 ч, что приводит к сверхэкспрессии К 7 ч. Во-вторых, так как К 7 ч секретируется из многослойных тел в межклеточное пространство рогового слоя в виде профермента и не способен самоактивироваться, то для его активации требуется другая протеаза, например, К 5 ч (5). Неконтролируемая активность такого активирующегося фермента может привести к сверхэкспрессии К 7 ч. В-третьих, активированный К 7 ч можно ингибировать природными ингибиторами, такими как LEKTI, ALP или элафин (10, 11), сниженный уровень экспрессии таких ингибиторов или их отсутствие может привести в повышенной активности К 7 ч. Недавно было установлено, что мутации в гене spink5, кодирующем LEKTI, являются причиной развития синдрома Незертона (12), а одноточечная мутация в гене связана с атопическим дерматитом (13, 14). И наконец, другим уровнем контроля активности К 7 ч является pH. pH-Оптимум К 7 ч находится в интервале от нейтрального до слабо щелочного pH (2), а градиент pH по направлению от внутреннего до внешнего слоев кожи составляет от нейтрального до кислого pH. Факторы окружающей среды, такие как мыло,могут привести к повышению pH во внешних слоях рогового слоя до pH-оптимума К 7 ч, и тем самым повысить активность К 7 ч. Гипотеза о взаимосвязи увеличения активности К 7 ч с заболеваниями кожи, вызванными повреждением барьера кожи, включающими воспалительные и гиперпролиферативные заболевания кожи, подтверждается следующими данными. Во-первых, у пациентов с синдромом Незертона наблюдается зависимое от фенотипа увеличение активности сериновых протеаз, снижение количества корнеодесмосом,снижение уровня расщепляющих липиды ферментов глюкоцереброзидазы и кислой сфингомиелиназы, и нарушенная функция барьера кожи (15, 16). Во-вторых, у трансгенных мышей со сверхэкспрессией К 7 ч наблюдается фенотип кожи, аналогичный фенотипу пациентов с атопическим дерматитом (17, 18,19). В-третьих, установлено, что у пациентов с атопическим дерматитом кожи и псориазом наблюдаются повышенные уровни К 7 ч (17, 20). Более того, повышенная активность К 7 и связанная с этим дисфункция эпителиального барьера могут играть важную роль в патологии других эпителиальных заболеваний, таких как воспалительное заболевание кишечника и болезнь Крона. Следовательно, К 7 ч можно рассматривать как потенциальную мишень для лечения заболеваний,-1 017735 связанных с эпителиальной дисфункцией, таких как воспалительные и/или гиперпролиферативные заболевания, и зудящих заболеваний кожи, таких как атопический дерматит, псориаз, синдром Незертона,или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как воспалительное заболевание кишечника и болезнь Крона, и таким образом существует необходимость в разработке специфических модуляторов (агонистов или ингибиторов) К 7 ч. Эластаза нейтрофилов человека (НЭч, известная также под названием эластаза лейкоцитов, ЛЭч) относится к семейству сериновых протеаз типа химотрипсина. pH-Оптимум ее каталитической активности составляет приблизительно 7, а каталитический участок включает три образующих водородные связи аминокислотных остатка: His57, Asp102 и Ser195 (нумерация соответствует последовательности химотрипсина), которые образуют так называемую каталитическую триаду. Фермент состоит из одной полипептидной цепи, включающей 218 аминокислотных остатка и четыре дисульфидных связи. Гомология последовательности с другими эластинолитическими или не-эластинолитическими сериновыми протеиназами составляет от 30 до 40%. НЭч предпочтительно расщепляет окисленную цепь В инсулина, содержащую остаток валина в положении P1, но также расщепляет связи, содержащие остатки аланина, серина или цистеина в положении P1. НЭч локализована в азурофильных гранулах полиморфноядерных лейкоцитов (ПМЯЛ), которые характеризуются достаточной высокой концентрацией НЭч (3 мкг фермента/10 клеток). Основная физиологическая функция фермента заключается в расщеплении бактерий и иммунокомплексов, он также принимает участие в защитном механизме организма-хозяина. НЭч способствует также миграции нейтрофилов из крови в различные ткани, такие как дыхательные пути, в ответ на факторы хемотаксиса. НЭч принимает также участие в ранозаживлении, регенерации ткани и апоптозе ПМЯЛ. Наряду с эластином (высоко эластичный и высокогидрофобный компонент соединительной ткани легких, артерий, кожи и связок), НЭч расщепляет множество белков, проявляющих важную биологическую функцию, включая коллагены различного типа, мембранные белки и протеогликаны хрящевых тканей. НЭч косвенно способствует деградации белков внеклеточного матрикса за счет активации проколлагеназы, простромелизина и прожелатиназы. НЭч инактивирует также ряд эндогенных ингибиторов протеиназ, таких как а 2-антиплазмин, 1-антихимотрипсин, антитромбин и тканевой ингибитор металлопротеиназ. В легочной системе активность внеклеточной эластазы строго контролируется ингибитором 1 протеаз (1P1), ответственным за защиту нижних дыхательных путей от эластолитической деградации, в то время как секреторный ингибитор протеиназы лейкоцитов в основном защищает верхние дыхательные пути. В ряде патофизиологических состояний легких, например, при эмфиземе легких, хроническом бронхите и муковисцидозе, эндогенные ингибиторы эластаз неэффективны в регуляции активности НЭч. Предполагается, что НЭч является первичным источником повреждения тканей, связанного с воспалительными заболеваниями, таким как энфизема легких, респираторный дистресс-синдром взрослых(РДСВ), хронический бронхит, хроническая обструктивная болезнь легких (ХОБЛ), легочная гипертензия, и с другими воспалительными заболеваниями, такими как легочная дисплазия у недоношенных новорожденных. НЭч принимает участие в патогенезе повышенной и аномальной секреции дыхательных путей, обычно связанной с воспалительными заболеваниями дыхательных путей. Таким образом, бронхоальвеолярная промывная жидкость (БАПЖ), полученная от пациентов с диагнозом хронического бронхита и муковисцидоза, характеризуется повышенной активностью НЭч. Более того, полагают, что избыточная эластаза принимает участие не только в развитии указанных хронических воспалительных заболеваний, но и острых воспалительных заболеваний, таких как ХОБЛ и септический шок. Следовательно, НЭч можно рассматривать как потенциальную мишень для лечения заболеваний,связанных с активностью НЭч, таких как воспалительные заболевания, такие как энфизема легких, респираторный дистресс-синдром взрослых (РДСВ), хронический бронхит, хроническая обструктивная болезнь легких (ХОБЛ), легочная гипертензия, и другие воспалительные заболевания, а также легочная дисплазия у недоношенных новорожденных, и заболевания, связанные с повышенной и аномальной секрецией дыхательных путей, а также острые воспалительные заболевания. Таким образом существует необходимость в разработке специфических модуляторов (агонистов или ингибиторов) НЭч. Лечение можно проводить местным или системным способом, например, с использованием кремов,мазей и суппозиториев, или подкожным или внутривенным способом или ингаляцией, соответственно. Род Chondromyces относится к семейству Polyangiaceae, принадлежащему к порядку Myxococcales класса дельта-протеобактерий. Бактерии порядка Myxococcales, также называемые миксобактериями,являются грамотрицательными бактериями палочковидной формы и обладают двумя выраженными отличиями от большинства других бактерий. Они закрепляются и начинают расти на твердых поверхностях, используя механизм активного перемещения и агрегирования для формирования плодовых тел при наступлении голодания (Kaiser (2003 В настоящем изобретении предлагаются циклические депсипептиды, продуцируемые штаммом Chondromyces и способные специфически модулировать калликреин 7.-2 017735 Краткое описание сущности изобретения В одном объекте настоящего изобретения предлагаются циклические депсипептиды или их производные формулы (I) где сложноэфирная связь расположена между карбоксигруппой A7 и гидроксигруппой A2, где X и A1 каждый независимо являются необязательными, и где X обозначает любой химический остаток, A1 обозначает стандартную аминокислоту, которая не является аспарагиновой кислотой, или производное указанной стандартной аминокислоты, A2 обозначает треонин или серии, A3 обозначает неосновную аминокислоту или ее неосновное производное, A4 обозначает Ahp, дегидро-AHP, пролин или его производное, A5 обозначает изолейцин или валин, A6 обозначает тирозин или его производное, A7 обозначает лейцин,изолейцин или валин. В другом варианте циклические депсипептиды или их производные характеризуются формулой (I')R2 обозначает H или метил,R3 обозначает боковую цепь неосновной аминокислоты или ее неосновное производное,R5 обозначает боковую цепь изолейцина или валина,R6 обозначает боковую цепь тирозина или его производного,R7 обозначает боковую цепь лейцина, изолейцина или валина,Y обозначает водород или метил,и где Ahp замещен остатками дегидро-AHP, Ahp-I, Ahp-II, пролина или его производного. Настоящее изобретение также относится к фармацевтически приемлемым солям указанных циклических депсипептидов или их производных. В циклических депсипептидах по настоящему изобретению X обозначает H или ацил, например,CH3CH2CH(CH3)CO, (CH3)2CHCH2CO или (CH3)2CHCO. В циклических депсипептидах A1 обозначает глутамин, глутаминовую кислоту или ее производное,например нитрил глутамина или сложный эфир глутаминовой кислоты. В циклических депсипептидах A2 обозначает треонин или его производное. В циклических депсипептидах A3 обозначает лейцин. В циклических депсипептидах A6 обозначает тирозин. В некоторых вариантах циклических депсипептидов А 4 обозначает производные 3-аминопиперидин-2-она, Ahp, Ahp-I или Ahp-II. В некоторых вариантах циклических депсипептидов или их производных X обозначает(CH3)2CHCO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, A4 обозначает Ahp или его производное, А 5 обозначает изолейцин или валин,A6 обозначает тирозин или его производное, A7 обозначает изолейцин или валин. В других вариантах циклических депсипептидов или их производных X обозначаетCH3CH2CH(CH3)CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает Ahp или его производное, A5 обозначает изолейцин, A6 обозначает тирозин или его производное и А 7 обозначает изолейцин. В некоторых вариантах циклических депсипептидов или их производных X обозначаетCH3CH2CH(CH3)CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает дегидро-AHP или его производное, А 5 обозначает изолейцин, A6 обозначает тирозин или его производное и А 7 обозначает изолейцин. В других вариантах циклических депсипептидов или их производных X обозначает(CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, A4 обозначает дегидро-AHP, Ahp или его производное, A5 обозначает изолейцин, A6 обозначает тирозин или его производное и A7 обозначает изолейцин. Настоящее изобретение также относится к циклическим депсипептидам или их производным, формулы (I) где сложноэфирная связь расположена между карбоксигруппой А 7 и гидроксигруппой A2, где X-3 017735 обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, A4 обозначает Ahp или пролин или его производное, A5 обозначает фенилаланин, A6 обозначает тирозин или его производное и А 7 обозначает валин. В конкретных вариантах X обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, A4 обозначает Ahp или его производное, A5 обозначает фенилаланин, A6 обозначает тирозин или его производное и A7 обозначает валин. В других вариантах X обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, A4 обозначает пролин или его производное, A5 обозначает фенилаланин, A6 обозначает тирозин или его производное и A7 обозначает валин. В этих вариантах атом азота амидной связи между A5 и A6 замещен метилом. В циклическом депсипептиде или его производном A1, A2, A3, A5, A6 и A7 обозначают Lаминокислоты. Кроме того A4 обозначает (3S,6R)-Ahp. Настоящее изобретение также относится к применению указанных выше депсипептидов и их производных в качестве лекарственных средств, например, для лечения рака, прежде всего рака яичников,или для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха,неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников, муковисцидоз (MB), хроническое обструктивное заболевание легких (ХОЗЛ), фиброз легких, респираторный дистресс-синдром взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника, псориаз, астма. В одном варианте настоящего изобретения предлагается также применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак,прежде всего рак яичников. В другом варианте настоящего изобретения также предлагается применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения муковисцидоза (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых, хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, астмы. В еще одном варианте настоящего изобретения также предлагается применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы,гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри,синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста. Настоящее изобретение также включает способы продуцирования циклического депсипептида или его производного, например, при культивировании штамма Chondromyces, его вариантов или мутантных форм, в пригодной среде, и необязательно химической модификации полученного таким образом циклического депсипептида, или при экспрессии генов биосинтеза штамма Chondromyces, его вариантов или мутантных форм, в гетерологическом микробном штамме-хозяине, и необязательно химической модификации полученного таким образом циклического депсипептида. Указанные способы осуществляют с использованием штаммов Chondromyces crocatus (DSM 19329) или Chondromyces robustus (DSM 19330) или Chondromyces apiculatus (DSM 21595). Настоящее изобретение также относится к выделенному микроорганизму Chondromyces, продуцирующему циклический депсипептид или его производное, депонированному в коллекции DSM под номером DSM 19329 или DSM 19330 или DSM 21595, и к циклическому депсипептиду или его производному, продуцированному выделенным микроорганизмом Chondromyces. Описание фигур Фиг. 1 - 1 Н ЯМР спектр соединения формулы (II) (600 МГц, ДМСО-d6). Фиг. 2 - 13 С ЯМР спектр соединения формулы (II) (150 МГц, ДМСО-d6). Фиг. 3 - 1 Н ЯМР спектр соединения формулы (VIII) (600 МГц, ДМСО-d6). Фиг. 4 - 13 С ЯМР спектр соединения формулы (VIII) (150 МГц, ДМСО-d6). Фиг. 5 - 1 Н ЯМР спектр производного циклического депсипептида формулы (II), где Ahp превращают в 3-аминопиперидин-2-он (пример 4).-4 017735 Фиг. 6 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 5 (500 МГц, ДМСО-d6). Фиг. 7 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 19 (500 МГц, ДМСО-d6). Фиг. 8 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 21 (500 МГц, ДМСО-d6). Фиг. 9 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 26 (500 МГц, ДМСО-d6). Фиг. 10 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 32 (500 МГц, ДМСО-d6). Фиг. 11 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 44 (500 МГц, ДМСО-d6). Фиг. 12 - 1 Н ЯМР спектр производного циклического депсипептида, полученного в примере 45 (500 МГц, ДМСО-d6). Подробное описание изобретения Как описано выше в данном контексте и в пунктах формулы изобретения, в одном объекте настоящего изобретения предлагаются циклические депсипептиды или их производные формулы (I) где сложноэфирная связь расположена между карбоксигруппой А 7 и гидроксигруппой A2, где X иA1 каждый независимо являются необязательными, и где X обозначает любой химический остаток, A1 обозначает стандартную аминокислоту, которая не является аспарагиновой кислотой, A2 обозначает треонин или серии, A3 обозначает неосновную стандартную аминокислоту или ее неосновное производное,А 4 обозначает Ahp, дегидро-AHP, пролин или его производное, A5 обозначает изолейцин или валин, A6 обозначает тирозин или его производное, A7 обозначает лейцин, изолейцин или валин. В другом варианте циклические депсипептиды или их производные характеризуются формулой (I')R2 обозначает боковую цепь треонина или серина,R3 обозначает боковую цепь неосновной аминокислоты или ее неосновное производное,R5 обозначает боковую цепь изолейцина или валина,R6 обозначает боковую цепь тирозина или его производного,R7 обозначает боковую цепь лейцина, изолейцина или валина,Y обозначает водород или метил,и где Ahp замещен остатками дегидро-AHP, Ahp-I, Ahp-II, пролина или его производного. Настоящее изобретение также относится к фармацевтически приемлемым солям указанных циклических депсипептидов или их производных. В циклических депсипептидах или их производных атом азота в амидной связи между А 5 и A6 замещен метилом. В циклических депсипептидах по настоящему изобретению X обозначает H или ацил, напримерCH3CH2CH(CH3)CO, (CH3)2CHCH2CO или (CH3)2CHCO. В циклических депсипептидах A1 обозначает глутамин, глутаминовую кислоту или ее производное. В циклических депсипептидах А 2 обозначает треонин. В циклических депсипептидах А 3 обозначает лейцин. В циклических депсипептидах A6 обозначает тирозин или его производное. В некоторых вариантах циклических депсипептидов А 4 обозначает производные 3 аминопиперидин-2-она, Ahp, Ahp-I или Ahp-II. В некоторых вариантах циклического депсипептида или его производного X обозначает(CH3)2CHCO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает Ahp или его производное, А 5 обозначает изолейцин или валин,A6 обозначает тирозин или его производное, А 7 обозначает изолейцин или валин. В других вариантах циклического депсипептида или его производного X обозначаетCH3CH2CH(CH3)CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает Ahp или его производное, А 5 обозначает изолейцин, A6-5 017735 обозначает тирозин или его производное и А 7 обозначает изолейцин. В некоторых вариантах циклического депсипептида или его производного X обозначаетCH3CH2CH(CH3)CO, А 1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает дегидро-AHP или его производное, А 5 обозначает изолейцин, A6 обозначает тирозин или его производное и А 7 обозначает изолейцин. В других вариантах циклического депсипептида или его производного X обозначает(CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает дегидро-AHP или его производное, А 5 обозначает изолейцин, A6 обозначает тирозин или его производное и А 7 обозначает изолейцин. Настоящее изобретение кроме того относится к циклическим депсипептидам или их производным формулы (I) где сложноэфирная связь расположена между карбоксигруппой А 7 и гидроксигруппой A2, где X обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает Ahp или пролин или его производное, А 5 обозначает фенилаланин, A6 обозначает тирозин или его производное и А 7 обозначает валин. В конкретных вариантах X обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает Ahp или его производное, А 5 обозначает фенилаланин, A6 обозначает тирозин или его производное и А 7 обозначает валин. В других вариантах X обозначает (CH3)2CHCH2CO, A1 обозначает глутамин, глутаминовую кислоту или ее производное, A2 обозначает треонин, A3 обозначает лейцин, А 4 обозначает пролин или его производное, А 5 обозначает фенилаланин, A6 обозначает тирозин или его производное и А 7 обозначает валин. В указанных вариантах атом азота в амидной связи между А 5 и A6 замещен метилом. В циклическом депсипептиде или его производном A1, A2, A3, A5, A6 и А 7 обозначают Lаминокислоты. Кроме того А 4 обозначает (3S,6R)-Ahp. А 5 обозначает изолейцин, фенилаланин или валин. А 5 обозначает прежде всего изолейцин или валин, предпочтительно изолейцин. В другом варианте А 5 обозначает фенилаланин, прежде всего если А 4 не обозначает Ahp, и остальные остатки имеют значения, как определено в п.1. Еще в одном варианте А 4 обозначает 5-гидроксипролин и А 5 обозначает изолейцин, а остальные остатки имеют значения, как определено в п.1. В другом варианте А 4 обозначает Ahp и А 5 обозначает изолейцин, а остальные остатки имеют значения, как определено в п.1. Еще в одном варианте А 4 обозначает AhpI и А 5 обозначает изолейцин, а остальные остатки имеют значения, как определено в п.1. В другом варианте А 4 обозначает Ahp-II и А 5 обозначает изолейцин, а остальные остатки имеют значения, как определено в п.1. Еще в одном варианте А 4 обозначает Ahp, A5 и А 7 обозначают изолейцин, а остальные остатки имеют значения, как определено в п.1. В другом варианте А 4 обозначает Ahp-I, A5 и А 7 обозначают изолейцин, а остальные остатки имеют значения, как определено в п.1. Еще в одном варианте А 4 обозначает Ahp-II, A5 и А 7 обозначают изолейцин, а остальные остатки имеют значения, как определено в п.1. В другом варианте А 4 обозначает 5-гидроксипролин, А 5 и А 7 обозначают изолейцин, а остальные остатки имеют значения, как определено в п.1. Как указано в данном контексте, A1 обозначает глутамин, глутаминовую кислоту, орнитин или производное глутамина, такое как, например, нитрил глутамина, сложный эфир глутаминовой кислоты, такой как С 1-С 12 алкиловый эфир (например, метиловый эфир глутаминовой кислоты) или такой как C6-C24 ариловый эфир (например, фениловый или бензиловый эфир глутаминовой кислоты). Настоящее изобретение также относится к применению указанных выше циклических депсипептидов или их производных в качестве лекарственных средств, например, для лечения рака, прежде всего рака яичников, или для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз,синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний, связанных с дисфункцией эпителиального барьера, таких как воспалительное заболевание кишечника и болезнь Крона, а также панкреатит. В одном варианте настоящего изобретения также предлагается применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, ги-6 017735 пертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак,прежде всего рак яичников. В одном варианте настоящего изобретения также предлагается применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения муковисцидоза (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых, хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, астмы. В другом варианте настоящего изобретения также предлагается применение указанных выше депсипептидов и их производных в качестве лекарственных средств, предназначенных для лечения воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста. Настоящее изобретение также включает способы продуцирования циклического депсипептида или его производного, например, при культивировании штамма Chondromyces, его вариантов или мутантных форм, в пригодной среде, и необязательно способы химической модификации полученного таким образом циклического депсипептида, или при экспрессии генов биосинтеза штамма Chondromyces, его вариантов или мутантных форм, в гетерологическом микробном штамме-хозяине, и необязательно способы химической модификации полученного таким образом циклического депсипептида. Указанные способы осуществляют с использованием штамма Chondromyces crocatus (DSM 19329) или Chondromyces robustus (DSM 19330) или Chondromyces apiculatus (DSM 21595). Настоящее изобретение также относится к выделенному микроорганизму Chondromyces, продуцирующему циклический депсипептид или его производное, депонированному в коллекции DSM под номером DSM 19329 или DSM 19330 или DSM 21595, и к циклическому депсипептиду или его производному, продуцированному выделенным микроорганизмом Chondromyces. Настоящее изобретение включает циклический депсипептид или его производное формулы (I) где сложноэфирная связь образуется между карбоксигруппой А 7 и гидроксигруппой A2,где X и A1 каждый независимо является необязательным, и гдеX обозначает H или группу, аминомодифицирующую группу, и ее обычно выбирают из арилкарбонила или ацила,A1 обозначает глутамин, орнитин, глутаминовую кислоту или ее производное,A2 обозначает треонин или серии,A3 обозначает лейцин,A4 обозначает Ahp, 3-аминопиперидин-2-он, дегидро-AHP, Ahp-I, Ahp-II, пролин, 5-гидроксипролин или его производное, причем участок присоединения A3 к A5 включает атом азота и карбоксильный атом кислорода (за счет замены атома водорода на связь) в составе пролина и 5-гидроксипролина, гдеAhp, 3-аминопиперидин-2-он, дегидро-AHP, Ahp-I и Ahp-II имеют значения, определенные ниже, и где участок присоединения A3 к A5 включает атомы азота указанных соединений (за счет замены атома водорода на связь) где X обозначает O или связь, и R обозначает органический остаток или радикал, как определено в-7 017735 п.3,A5 обозначает изолейцин, фенилаланин или валин,A6 обозначает тирозин, N-Me-тирозин или его производное,A7 обозначает лейцин, изолейцин или валин, или их фармацевтически приемлемую соль. Депсипептид по п.1, где X обозначает CH3CH2CH(CH3)CO, (CH3)2CHCH2CO, (CH3)2CHCO, CH3CO или фенил-CO. Депсипептид по п.1, где атом азота амидной связи между А 5 и A6 замещен метилом и где группа OH в остатке тирозина обозначает OR, где R выбирают из группы, включающей водород, С 1-С 12 алкил, C2-C12 алкенил, С 2-С 12 алкинил, галоген(C1-C12)алкил, галоген(C2-C12)алкенил, галоген(C2-C12)алкинил, C1-C12 алкоксикарбонил, С 1-С 12 алкоксикарбонил(C1-C12)алкил, С 1-С 12 алкиламинокарбонил, незамещенный или дополнительно замещенный арилом, арилалкилом, арилалкенилом или арилалкинилом, гетероциклилом и гетероциклилалкилом. Депсипептид по п.1, где A4 обозначает производные 3-аминопиперидин-2-она: Ahp, Ahp-I или AhpII, где R выбирают из группы, включающей С 1-С 12 алкил, С 2-С 12 алкенил, С 2-С 12 алкинил, галоген(C1-C12) алкил, С 1-С 12 алкокси(C1-C12)алкил, С 1-С 12 алкокси(C1-C12)алкокси(C1-C12)алкил, гидрокси(C1-C12)алкил,фенил и фенил(C1-C6)алкил. Депсипептид по п.1, где ацильный остаток X обозначает CH3CH2CH(CH3)CO или (CH3)2CHCO,A1 обозначает глутамин, глутаминовую кислоту или ее производное,A2 обозначает треонин,A3 обозначает лейцин,A4 обозначает Ahp, 3-аминопиперидин-2-он, пролин, 5-гидроксипролин или его производное,A5 обозначает изолейцин,A6 обозначает тирозин, N-Me-тирозин или его производное,A7 обозначает изолейцин или валин, предпочтительно изолейцин. Депсипептид по любому из предшествующих пунктов, где А 4 обозначает Ahp, Ahp-I, 3 аминопиперидин-2-он, пролин или 5-гидроксипролин, предпочтительно Ahp, Ahp-I, 3-аминопиперидин 2-он, или 5-гидроксипролин, также предпочтительно Ahp, Ahp-I или 5-гидроксипролин, более предпочтительно Ahp. Депсипептид по п.1, который обозначает соединение формулы А или ВR2 обозначает боковую цепь треонина или серина,R3 обозначает боковую цепь лейцина,R5 обозначает боковую цепь изолейцина или валина, прежде всего R5 обозначает боковую цепь изолейцина,R6 обозначает боковую цепь тирозина, необязательно модифицированного, прежде всего необязательно модифицированного по гидроксильной группе, как определено в п.3,R7 обозначает боковую цепь лейцина, изолейцина или валина, прежде всего R7 обозначает боковую цепь изолейцина,Y обозначает водород или метил, прежде всего Y обозначает метил. Циклический депсипептид по любому из предшествующих пунктов, где A1, A2, A3, A5, A6 и А 7 обозначают L-аминокислоты. Циклический депсипептид по любому из предшествующих пунктов, где А 4 обозначает (3S,6R)-Ahp. Циклический депсипептид по любому из предшествующих пунктов, где A1 обозначает глутамин,орнитин или производное глутамина, как описано в любом из примеров в настоящем описании, и указанный депсипептид, например, выбирают из нитрила глутамина, сложного эфира глутаминовой кислоты, такого как С 1-С 12 алкиловый эфир (например, метиловый эфир глутаминовой кислоты) или C6-C24 ариловый эфир (например, фениловый или бензиловый эфир глутаминовой кислоты). Фармацевтическая композиция, включающая циклический депсипептид по любому из предшествующих пунктов в смеси с фармацевтически приемлемым носителем и/или ингредиентом. Циклический депсипептид по любому из предшествующих пунктов для применения в качестве лекарственного препарата, прежде всего для применения, как описано в пунктах, относящихся к способам лечения пациента, таких как пп.13-15, и применение указанных депсипептидов для получения лекарст-8 017735 венного средства, предназначенного для лечения заболевания или нарушения, как описано в указанных пунктах, относящихся к способам лечения. Способ лечения субъекта, страдающего от воспалительных и/или гиперпролиферативных и зудящих кожных заболеваний, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или от других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников, муковисцидоз (MB), хроническое обструктивное заболевание легких (ХОЗЛ), фиброз легких, респираторный дистресс-синдром взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника, псориаз, астма, и указанный способ заключается во введении указанному субъекту терапевтически эффективного количества циклического депсипептида или его производного по любому из пп.1-10. Способ лечения субъекта по п.13, где субъект страдает от келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний, связанных с дисфункцией эпителиального барьера, таких как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников. Способ лечения субъекта по п.14, где субъект страдает от келоидных рубцов, гипертрофических рубцов, угрей, атопического дерматита, псориаза, пустулезного псориаза, розовых угрей, синдрома Незертона или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также других заболеваний, связанных с дисфункцией эпителиального барьера, таких как старческая кожа. Способ лечения субъекта по п.13, где субъект страдает от муковисцидоза (MB), хронического обструктивного заболевания легких (ХОЗЛ), фиброза легких, респираторного дистресс-синдрома взрослых,хронического бронхита, наследственной эмфиземы, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, астмы. Способ продуцирования циклического депсипептида или его производного по любому из пп.1-10,который заключается в культивировании штамма Chondromyces, его вариантов или мутантных форм в пригодной среде, и необязательно способ химической модификации полученного таким образом циклического депсипептида. Способ продуцирования циклического депсипептида или его производного по любому из пп.1-10,который заключается в экспрессии генов биосинтеза штамма Chondromyces, его вариантов или мутантных форм, в гетерологическом микробном штамме-хозяине, и необязательно способ химической модификации полученного таким образом циклического депсипептида. Способ по п.17 или 18, где штамм обозначает Chondromyces crocatus (DSM 19329) или Chondromyces robustus (DSM 19330) или Chondromyces apiculatus (DSM 21595). Выделенный микроорганизм Chondromyces, продуцирующий циклический депсипептид или его производное по любому из п.п.1-10, депонированный в коллекции DSM под номером DSM 19329 илиDSM 19330 или DSM 21595. Циклический депсипептид или его производное, продуцированный выделенным микроорганизмомChondromyces по п.20 или полученный способом по пп.17-18. Способ получения производного циклического депсипептида или его производного по п.1, который включает следующие варианты: а) получение производного циклического депсипептида или его производного по п.1, где А 4 обозначает органической или неорганической кислотой или кислотой Льюиса при температуре от -78 до 150C,б) получение производного циклического депсипептида или его производного по п.1, где А 4 обозначает молекулярным водородом или его источником в присутствии катализатора в растворителе при температуре от -50 до 100C,в) получение производного циклического депсипептида или его производного по п.1, где A4 обозначает органической или неорганической кислотой или кислотой Льюиса в присутствии восстанавливающего агента при температуре от -78 до 150C, или г) получение производного циклического депсипептида или его производного по п.1, где A4 обозначает замещенным или незамещенным спиртом и органической или неорганической кислотой или кислотой Льюиса при температуре от -78 до 150C,д) получение соединений, где A1 обозначает где R предпочтительно обозначает H, алкил, замещенный алкил, замещенным или незамещенным спиртом и органической или неорганической кислотой или кислотой Льюиса в присутствии или отсутствие растворителя при температуре от -78 до 150C,е) получение соединений, где A1 обозначает дегидратирующим агентом в присутствии или отсутствие растворителя при температуре от -78 до 150C,ж) получение соединений, где A4 обозначает и A6 обозначает Tyr, алкилирующим агентом или ацилирующим агентом в присутствии или отсутствие растворителя при температуре от -78 до 150C. Циклический депсипептид или его производное или его фармацевтически приемлемая соль, прежде всего и как описано в данном контексте и/или в примерах. Конкретные варианты циклических депсипептидов по настоящему изобретению включают Циклические депсипептиды формул (II)-(VII), (XI)-(XIV) и (XVII) продуцируются штаммом Chondromyces crocatus по настоящему изобретению (DSM 19329). Другие конкретные варианты циклических депсипептидов по настоящему изобретению включают Циклические депсипептиды формул (VIII)-(X) продуцируются штаммом Chondromyces robustus по настоящему изобретению (DSM 19330). Другие конкретные варианты циклических депсипептидов по настоящему изобретению включают Циклические депсипептиды формул (XV)-(XVI) продуцируются штаммом Chondromyces apiculatus по настоящему изобретению (DSM 21595).DSMZ - немецкая коллекция микроорганизмов и культуральных клеток; К 7 ч - калликреин 7 человека; ЖХВР - жидкостная хроматография высокого разрешения;pO2 - парциальное давление кислорода в питательной среде (100% насыщение воздухом); об./об./мин скорость аэрации (объем воздуха/объем культуральной среды/мин. Термин "химический остаток" обозначает любую органическую или неорганическую группу. "Химический остаток" включает, не ограничиваясь только ими, замещенную или незамещенную алифатическую группу, например, С 1-С 3 алкил, С 1-С 6 алкил или С 1-С 12 алкил, замещенный или незамещенный арил,замещенный или незамещенный арилалкил, замещенный или незамещенный гетероарил или галоген. Например, остаток, как определено в пунктах формулы, обозначает любые химические группы, описанные ниже в данном контексте. Термин "химический остаток" включает, не ограничиваясь только ими, аминокислоты, пептиды,полипептиды, белки и т.п. Примеры неорганических остатков обозначают, например, галогены, такие как Br или Cl. Термин "алифатическая группа" обозначает неароматический остаток, который содержит любую комбинацию атомов углерода, атомов водорода, атомов галогена, кислорода, азота или других атомов, и необязательно содержит одну или более ненасыщенных связей, например, двойные и/или тройные связи. Алифатическая группа является прямой, разветвленной или циклической структурой, предпочтительно содержит от приблизительно 1 до приблизительно 24 атомов углерода, более предпочтительно содержит от приблизительно 1 до приблизительно 12 атомов углерода. Кроме алифатических углеводородных групп алифатические группы включают, например, полиалкоксиалкилы, такие как полиалкиленгликоли,полиамины и полиимины. Указанные алифатические группы могут содержать заместители. Термины "С 1-С 3 алкил, С 1-С 6 алкил или С 1-С 12 алкил", использованные в данном контексте, обозначают насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от одного до трех, от одного до шести или от одного до двенадцати атомов углерода, соответственно. Примеры C1 С 3 алкильных радикалов включают метил, этил, пропил и изопропил, примеры С 1-С 6 алкильных радикалов включают, не ограничиваясь только ими, метил, этил, пропил, изопропил, н-бутил, трет-бутил, вторбутил, н-пентил, неопентил и н-гексил, а примеры С 1-С 12 алкильных радикалов включают, не ограничиваясь только ими, этил, пропил, изопропил, гексил, гептил, октил, нонил, децил, ундецил, додецил и т.п. Термин "замещенный алкил", использованный в данном контексте, обозначает алкил, такой как C1 С 12 алкил или С 1-С 6 алкил, замещенный одним, двумя, тремя или более алифатическими заместителями. Пригодные алифатические заместители включают, не ограничиваясь только ими, -F, -Cl, -Br, -I, -OH, защищенную гидроксигруппу, алифатические простые эфиры, ароматические простые эфиры, оксогруппу,-NO2, -CN, -С 1-С 12 алкил, необязательно замещенный галогеном (такой как пергалогеналкилы), -C2-C12 алкенил, необязательно замещенный галогеном, -С 2-С 12 алкинил, необязательно замещенный галогеном,-NH2, защищенную аминогруппу, -NH-C1-С 12 алкил, -NH-С 2-С 12 алкенил, -NH-C2-С 12 алкинил, -NH-C3 С 12 ииклоалкил,-NH-арил,-NH-гетероарил,-NH-гетероциклоалкил,-диалкиламиногруппу,-диариламиногруппу, -дигетероариламиногруппу, -O-С 1-С 12 алкил, -O-C2-С 12 алкенил, -O-C2-С 12 алкинил,-O-C3-С 12 циклоалкил, -O-арил, -O-гетероарил, -O-гетероциклоалкил, -C(O)-C1-С 12 алкил, -C(O)-C2 С 12 алкенил, -C(O)-C2-С 12 алкинил, -C(O)-C3-С 12 циклоалкил, -C(O)-арил, -C(O)-гетероарил, -C(O)гетероциклоалкил, -CONH2, -CONH-C1-С 12 алкил, -CONH-C2-С 12 алкенил, -CONH-C2-С 12 алкинил, -CONHC3-С 12 циклоалкил, -CONH-арил, -CONH-гетероарил, -CONH-гетероциклоалкил, -CO2-C1-С 12 алкил, -CO2C2-С 12 алкенил, -CO2-C2-С 12 алкинил, -CO2-C3-С 12 циклоалкил, -CO2-арил, -CO2-гетероарил, -CO2 гетероциклоалкил, -OCO2-C1-С 12 алкил, -OCO2-C2-С 12 алкенил, -OCO2-C2-С 12 алкинил, -OCO2-C3 С 12 циклоалкил, -OCO2-арил, -OCO2-гетероарил, -OCO2-гетероциклоалкил, -OCONH2, -OCONH-C1 С 12 алкил, -OCONH-C2-С 12 алкенил, -OCONH-C2-С 12 алкинил, -OCONH-C3-С 12 циклоалкил, -OCONH-арил,-OCONH-гетероарил, -OCONH-гетероциклоалкил, NHC(O)-C1-С 12 алкил, -NHC(O)-C2-С 12 алкенил,-NHC(O)-C2-С 12 алкинил, -NHC(O)-C3-С 12 циклоалкил, -NHC(O)-арил, -NHC(O)-гетероарил, -NHC(O)гетероциклоалкил, -NHCO2-C1-С 12 алкил, -NHCO2-C2-С 12 алкенил, -NHCO2-C2-С 12 алкинил, -NHCO2-C3 С 12 циклоалкил, -NHCO2-арил, -NHCO2-гетероарил, -NHCO2-гетероциклоалкил, NHC(O)NH2, NHC(O)NHC1-С 12 алкил, -NHC(O)NH-C2-С 12 алкенил, -NHC(O)NH-C2-С 12 алкинил, -NHC(O)NH-C3-С 12 циклоалкил,-NHC(O)NH-арил, -NHC(O)NH-гетероарил, -NHC(O)NH-гетероциклоалкил, NHC(S)NR2, NHC(S)NH-C1 С 12 алкил, -NHC(S)NH-C2-С 12 алкенил, -NHC(S)NH-C2-С 12 алкинил, -NHC(S)NH-C3-С 12 циклоалкил,-NHC(S)NH-арил, -NHC(S)NH-гетероарил, -NHC(S)NH-гетероциклоалкил, NHC(NH)NH2, NHC(NH)NHC1-С 12 алкил,-NHC(NH)NH-C2-С 12 алкенил,-NHC(NH)NH-C2-С 12 алкинил,-NHC(NH)NH-C3 С 12 циклоалкил,-NHC(NH)NH-арил,-NHC(NH)NH-гетероарил,-NHC(NH)NH-гетероциклоалкил,NHC(NH)-C1-С 12 алкил, -NHC(NH)-C2-С 12 алкенил, -NHC(NH)-C2-С 12 алкинил, -NHC(NH)-С 3-С 12 циклоалкил, -NHC(NH)-арил, -NHC(NH)-гетероарил, -NHC(NH)-гетероциклоалкил, C(NR)NH-C1-С 12 алкил,-C(NH)NH-C2-С 12 алкинил, -C(NR)NH-C2-С 12 алкинил, -C(NH)NH-С 3-С 12 циклоалкил, -C(NH)NH-арил,-C(NH)NH-гетероарил, -C(NH)NH-гетероциклоалкил, -S(O)-C1-С 12 алкил, -S(O)-C2-С 12 алкенил, -S(O)-C2- 13017735 С 12 алкинил, -S(O)-C3-С 12 циклоалкил, -S(O)-арил, -S(O)-гетероарил, -S(O)-гетероциклоалкил, -SO2NH2,-SO2NH-C1-С 12 алкил, -SO2NH-C2-С 12 алкенил, -SO2NH-C2-С 12 алкинил, -SO2NH-C3-С 12 циклоалкил,-SO2NH-арил, -SO2NH-гетероарил, -SO2NH-гетероциклоалкил, -NHSO2-C1-С 12 алкил, -NHSO2-C2-С 12 алкенил, -NHSO2-C2-С 12 алкинил, -NHSO2-C3-С 12 циклоалкил, -NHSO2-арил, -NHSO2-гетероарил, -NHSO2 гетероциклоалкил, -CH2NH2, -CH2SO2CH3, -арил, -арилалкил, -гетероарил, -гетероарилалкил, -гетероциклоалкил, -C3-С 12 циклоалкил, полиалкоксиалкил, полиалкоксигруппу, -метоксиметоксигруппу,-метоксиэтоксигруппу, -SH, -S-C1-С 12 алкил, -S-C2-С 12 алкенил, -S-C2-С 12 алкинил, -S-C3-С 12 циклоалкил,-S-арил, -S-гетероарил, -S-гетероциклоалкил или метилтиометил. Следует понимать, что указанные арилы, гетероарилы, алкилы и т.п. дополнительно замещены. Термины "C2-С 12 алкенил" или "C2-С 6 алкенил", использованные в данном контексте, обозначают одновалентную группу, полученную из углеводородного остатка, содержащего от двух до двенадцати или от двух до шести атомов углерода и по крайней мере одну углерод-углеродную двойную связь за счет удаления одного атома водорода. Алкенильные группы включают, не ограничиваясь только ими,например, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил, алкадиены и т.п. Термин "замещенный алкенил", использованный в данном контексте, обозначает группы "C2 С 12 алкенил" или "С 2-С 6 алкенил", как определено выше, замещенные одним, двумя, тремя или более алифатическими заместителями. Термины "C2-С 12 алкинил" или "С 2-С 6 алкинил", использованные в данном контексте, обозначают одновалентную группу, полученную из углеводородного остатка, содержащего от двух до двенадцати или от двух до шести атомов углерода и по крайней мере одну углерод-углеродную тройную связь за счет удаления одного атома водорода. Примеры алкенильных групп включают, не ограничиваясь только ими, например, этинил, 1-пропинил, 1-бутинил и т.п. Термин "замещенный алкинил, использованный в данном контексте, обозначает группы "C2 С 12 алкинил" или "C2-С 6 алкинил", как определено выше, замещенные одним, двумя, тремя или более алифатическими заместителями. Термин "C1-С 6 алкоксигруппа", использованный в данном контексте, обозначает группу C1-С 6 алкил,как определено выше, присоединенную к остальному фрагменту молекулы через атом кислорода. Примеры C1-С 6 алкоксигруппы включают, не ограничиваясь только ими, метокси, этокси, пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, н-пентокси, неопентокси и н-гексокси. Термин "галоген", использованный в данном контексте, обозначает атом, выбранный из фтора, хлора, брома и иода. Термин "арил", использованный в данном контексте, обозначает моно- или бициклическую карбоциклическую циклическую систему, содержащую один или два ароматических цикла, и включает, не ограничиваясь только ими, фенил, нафтил, тетрагидронафтил, инданил, иденил и т.п. Термин "замещенный арил", использованный в данном контексте, обозначает арильную группу, как определено выше, замещенную одним, двумя, тремя или более ароматическими заместителями. Ароматические заместители включают, не ограничиваясь только ими, -F, -Cl, -Br, -I, -OH, защищенную гидроксигруппу, алифатические простые эфиры, ароматические простые эфиры, оксогруппу,-NO2, -CN, -C1-С 12 алкил, необязательно замещенный галогеном (такой как пергалогеналкил), -C2-С 12 алкенил, необязательно замещенный галогеном, -C2-С 12 алкинил, необязательно замещенный галогеном,-NH2, защищенную аминогруппу, -NH-C1-С 12 алкил, -NH-C2-С 12 алкенил, -NH-C2-С 12 алкинил, -NH-C3 С 12 циклоалкил, -NH-арил, -NH-гетероарил, -NH-гетероциклоалкил, -диалкиламиногруппу, -диариламиногруппу, -дигетероариламиногруппу, -O-C1-С 12 алкил, -O-C2-С 12 алкенил, -O-C2-С 12 алкинил, -O-C3 С 12 циклоалкил, -O-арил, -O-гетероарил, -O-гетероциклоалкил, -C(O)-C1-С 12 алкил, -C(O)-C2-С 12 алкенил,-C(O)-C2-С 12 алкинил, -C(O)-C3-С 12 циклоалкил, -C(O)-арил, -C(O)-гетероарил, -C(O)-гетероциклоалкил,-CONH2, -CONH-C1-С 12 алкил, -CONH-C2-С 12 алкенил, -CONH-C2-С 12 алкинил, -CONH-C3-С 12 циклоалкил,-CONH-арил, -CONH-гетероарил, -CONH-гетероциклоалкил, -CO2-C1-С 12 алкил, -CO2-C2-С 12 алкенил,-CO2-C2-С 12 алкинил, -CO2-C3-С 12 циклоалкил, -CO2-арил, -CO2-гетероарил, -CO2-гетероциклоалкил,-OCO2-C1-С 12 алкил, -OCO2-C2-С 12 алкенил, -OCO2-C2-С 12 алкинил, -OCO2-C3-С 12 циклоалкил, -OCO2-арил,-OCO2-гетероарил, -OCO2-гетероциклоалкил, -OCONH2, -OCONH-C1-С 12 алкил, -OCONH-C2-С 12 алкенил,-OCONH-C2-С 12 алкинил, -OCONH-С 3-С 12 циклоалкил, -OCONH-арил, -OCONH-гетероарил, -OCONHгетероциклоалкил, -NHC(O)-C1-С 12 алкил, -NHC(O)-C2-С 12 алкенил, -NHC(O)-C2-С 12 алкинил, -NHC(O)-C3 С 12 циклоалкил, -NHC(O)-арил, -NHC(O)-гетероарил, -NHC(O)-гетероциклоалкил, -NHCO2-C1-С 12 алкил,-NHCO2-C2-С 12 алкенил, -NHCO2-C2-С 12 алкинил, -NHCO2-C3-С 12 циклоалкил, -NHCO2-арил, -NHCO2 гетероарил, -NHCO2-гетероциклоалкил, NHC(O)NH2, NHC(O)NH-C1-С 12 алкил, -NHC(O)NH-C2 С 12 алкенил, -NHC(O)NH-C2-С 12 алкинил, -NHC(O)NH-С 3-С 12 циклоалкил, -NHC(O)NH-арил, -NHC(O)NHгетероарил, -NHC(O)NH-гетероциклоалкил, NHC(S)NH2, NHC(S)NH-C1-С 12 алкил, -NHC(S)NH-C2 С 12 алкинил, -NHC(S)NH-C2-С 12 алкинил, -NHC(S)NH-С 3-С 12 циклоалкил, -NHC(S)NH-арил, -NHC(S)NHгетероарил, -NHC(S)NH-гетероциклоалкил, NHC(NH)NH2, NHC(NH)NH-C1-С 12 алкил, -NHC(NH)NH-C2 С 12 алкенил,-NHC(NH)NH-C2-С 12 алкинил,-NHC(NH)NH-C3-С 12 циклоалкил,-NHC(NH)NH-арил,-NHC(NH)NH-гетероарил,-NHC(NH)NH-гетероциклоалкил, NHC(NH)-C1-С 12 алкил, -NHC(NH)-C2-C12 алкенил, -NHC(NH)-C2-С 12 алкинил, -NHC(NH)-С 3-С 12 циклоалкил, -NHC(NH)-арил, -NHC(NH)- 14017735 гетероарил, -NHC(NH)-гетероциклоалкил, -C(NH)NH-C1-С 12 алкил, -C(NH)NH-C2-С 12 алкенил, -C(NH)NHC2-С 12 алкинил, -C(NH)NH-C3-С 12 циклоалкил, -C(NH)NH-арил, -C(NH)NH-гетероарил, -C(NH)NHгетероциклоалкил, -S(O)-C1-С 12 алкил, -S(O)-C2-С 12 алкенил, -S(O)-C2-С 12 алкинил, -S(O)-C3-C12 циклоалкил, -S(O)-арил, -S(O)-гетероарил, -S(O)-гетероциклоалкил, -SO2NH2, -SO2NH-C1-С 12 алкил, -SO2NH-C2 С 12 алкенил, -SO2NH-C2-С 12 алкинил, -SO2NH-C3-С 12 циклоалкил, -SO2NH-арил, -SO2NH-гетероарил,-SO2NH-гетероциклоалкил, -NHSO2-C1-С 12 алкил, -NHSO2-С 2-С 12 алкенил, -NHSO2-C2-С 12 алкинил,-NHSO2-C3-С 12 циклоалкил, -NHSO2-арил, -NHSO2-гетероарил, -NHSO2-гетероциклоалкил, -CH2NH2,-CH2SO2CH3, -арил, -арилалкил, -гетероарил, -гетероарилалкил, -гетероциклоалкил, -C3-С 12 циклоалкил,полиалкоксиалкил, полиалкоксигруппу, -метоксиметоксигруппу, -метоксиэтоксигруппу, -SH, -S-C1-C12 алкил, -S-C2-С 12 алкенил, -S-C2-С 12 алкинил, -S-C3-С 12 циклоалкил, -S-арил, -S-гетероарил, -S-гетероциклоалкил или метилтиометил. Следует понимать, что указанные арилы, гетероарилы, алкилы и т.п. дополнительно замещены. Термин "арилалкил", использованый в данном контексте, обозначает арильную группу, присоединенную к остальному фрагменту молекулы через C1-С 3 алкил или C1-С 6 алкил. Примеры арилалкила включают, не ограничиваясь только ими, бензил, фенетил и т.п. Термин "замещенный арилалкил", использованный в данном контексте, обозначает арилалкильную группу, как определено выше, замещенную одним, двумя, тремя или более ароматическими заместителями. Термин "гетероарил", использованный в данном контексте, обозначает моно-, би- или трициклический ароматический радикал или цикл, содержащий от пяти до десяти атомов в цикле, из которых по крайней мере один атом в цикле выбирают из S, O и N, ноль, один или два атома в цикле обозначают дополнительные гетероатомы, независимо выбранные из S, O и N, а остальные атомы в цикле обозначают углерод, причем любой атом N или S, содержащийся в цикле, необязательно находится в окисленном состоянии. Гетероарил включает, не ограничиваясь только ими, пиридинил, пиразинил, пиримидинил,пирролил, пиразолил, имидазолил, тиазолил, оксазолил, изоксазолил, тиадиазолил, оксадиазолил, тиофенил, фуранил, хинолинил, изохинолинил, бензимидазолил, бензооксазолил, хиноксалинил и т.п. Гетероароматический цикл связан с остальным фрагментом молекулы через атом углерода или гетероатом. Термин "замещенный гетероарил", использованный в данном контексте, обозначает гетероарильную группу, как определено выше, замещенную одним, двумя, тремя или четырьмя ароматическими заместителями. Термин "C3-С 12 циклоалкил", использованный в данном контексте, обозначает одновалентную группу, полученную из моноциклического или бициклического насыщенного карбоциклического соединения за счет удаления одного атома водорода. Примеры включают, не ограничиваясь только ими, циклопропил, циклобутил, циклопентил, циклогексил, бицикло[2.2.1]гептил и бицикло[2.2.2]октил. Термин "замещенный C3-С 12 циклоалкил", использованный в данном контексте, обозначает C3-C12 циклоалкильную группу, как определено выше, замещенную одним, двумя, тремя или более алифатическими заместителями. Термин "гетероциклоалкил", использованный в данном контексте, обозначает неароматический 5-,6- или 7-членный цикл, или би- или трициклическую конденсированную систему, где (1) каждый цикл содержит от одного до трех гетероатомов, независимо выбранных из кислорода, серы и азота, (2) каждый 5-членный цикл не содержит двойных связей или содержит 1 двойную связь, а каждый 6-членный цикл не содержит двойных связей или содержит 1 или 2 двойных связей, (3) гетероатомы азота и серы необязательно находятся в окисленном состоянии, (4) гетероатом азота необязательно является четвертичным,(5) любой из указанных выше циклов конденсирован с бензольным циклом, и (6) остальные атомы в цикле обозначают атомы углерода, которые необязательно замещены оксогруппой. Примеры гетероциклоалкильных групп включают, не ограничиваясь только ими, [1.3]диоксолан, пирролидинил, пиразолинил, пиразолидинил, имидазолинил, имидазолидинил, пиперидинил, пиперазинил, оксазолидинил, изоксазолидинил, морфолинил, тиазолидинил, изотиазолидинил, хиноксалинил, пиридазинонил и тетрагидрофурил. Термин "замещенный гетероциклоалкил", использованный в данном контексте, обозначает гетероциклоалкильную группу, как определено выше, замещенную одним, двумя, тремя или более алифатическими заместителями. Термин "гетероарилалкил", использованный в данном контексте, обозначает гетероарилалкильную группу, присоединенную к остальному фрагменту молекулы через C1-С 3 алкил или C1-С 6 алкил. Примеры гетероарилалкила включают, не ограничиваясь только ими, пиридинилметил, пиримидинилэтил и т.п. Термин "замещенный гетероарилалкил", использованный в данном контексте, обозначает гетероарилалкильную группу, как определено выше, замещенную одним, двумя, тремя или более ароматическими заместителями. Термин "C1-С 3 алкиламиногруппа", использованный в данном контексте, обозначает одну или двеC1-С 3 алкильных групп, как определено выше, присоединенных к остальному фрагменту молекулы через атом азота. Примеры C1-С 3 алкиламиногрупп включают, не ограничиваясь только ими, метиламиногруппу, диметиламиногруппу, этиламиногруппу, диэтиламиногруппу и пропиламиногруппу. Термин "алки- 15017735 ламиногруппа" обозначает группу формулы -NH(C1-С 3 алкил), где C1-С 12 алкил имеет значение, как определено ранее. Термин "диалкиламиногруппа" обозначает группу формулы -N(C1-С 12 алкил)(C1-С 12 алкил), гдеC1-С 12 алкил имеет значение, как определено ранее. Примеры диалкиламиногрупп включают, не ограничиваясь только ими, диметиламиногруппу, диэтиламиногруппу, метилэтиламиногруппу, пиперидино и т.п. Термин "алкоксикарбонил" обозначает сложноэфирную группу, например, алкоксигруппу, присоединенную к остальному фрагменту молекулы через карбонильную группу, такую как метоксикарбонил,этоксикарбонил и т.п. Термин "карбоксальдегид", использованный в данном контексте, обозначает группу формулы-C(O)NH(C1-С 12 алкил) или -C(O)N(C1-С 12 алкил)(C1-С 12 алкил), -C(O)NH2, -NHC(O)(C1-С 12 алкил), -N(С 1 С 12 алкил)C(O)(C1-С 12 алкил) и т.п. Термин "гидроксизащитная группа", использованный в данном контексте, обозначает химически лабильный остаток, который защищает гидроксильную группу от нежелательных реакций в ходе синтеза. После проведения указанного синтеза гидроксизащитную группу, описанную в данном контексте,можно селективно удалить. Гидроксизащитные группы описаны в книге Т. Н. Green и P.G.M. Wuts, Protective Groups in Organic Synthesis, 3-е изд., John WileySons, New York, (1999). Примеры гидроксизащитных групп включают бензилоксикарбонил, 4-нитробензилоксикарбонил, 4-бромбензилоксикарбонил,4-метоксибензилоксикарбонил, метоксикарбонил, трет-бутоксикарбонил, изопропоксикарбонил, дифенилметоксикарбонил, 2,2,2-трихлорэтоксикарбонил, 2-(триметилсилил)этоксикарбонил, 2-фурфурилоксикарбонил, аллилоксикарбонил, ацетил, формил, хлорацетил, трифторацетил, метоксиацетил, феноксиацетил, бензоил, метил, трет-бутил, 2,2,2-трихлорэтил, 2-триметилсилилэтиловый эфир, 1,1-диметил-2 пропенил, 3-метил-3-бутенил, аллил, бензил, пара-метоксибензилдифенилметил, трифенилметил(тритил), тетрагидрофурил, метоксиметил, метилтиометил, бензилоксиметил, 2,2,2-трихлорэтоксиметил,2-(триметилсилил)этоксиметил, метансульфонил, пара-толуолсульфонил, триметилсилил, триэтилсилил,триизопропилсилил и т.п. Предпочтительными гидроксизащитными группами являются ацетил (Ас или C(O)CH3), бензоил (Bn или -C(O)C6H5) и триметилсилил (TMS или -Si(CH3)3). Термин "защищенная гидроксигруппа", использованный в данном контексте, обозначает гидроксигруппу, защищенную защитной группой, как определено выше, включая, например, бензоил, ацетил,триметилсилил, триэтилсилил, метоксиметил. Термин "аминозащитная группа", использованный в данном контексте, обозначает химически лабильный остаток, который защищает аминогруппу от нежелательных реакций в ходе синтеза. После проведения указанного синтеза аминозащитную группу, как описано в данном контексте, можно селективно удалить. Аминозащитные группы описаны в книге Т. Н. Green и P.G.M. Wuts, Protective Groups in OrganicSynthesis, 3-е изд., John WileySons, New York, (1999). Примеры аминозащитных групп включают, не ограничиваясь только ими, трет-бутоксикарбонил, 9-флуоренилметоксикарбонил, бензилоксикарбонил и т.п. Термин "защищенная аминогруппа" использованный в данном контексте, обозначает аминогруппу,защищенную защитной группой, как определено выше. Термин "ацил" обозначает кислотный остаток, включая, не ограничиваясь только ими, остатки карбоновых кислот, карбаминовых кислот, угольных кислот, сульфоновых кислот и фосфорных кислот. Примеры включают алифатические карбонилы, ароматические карбонилы, алифатические сульфонилы,ароматические сульфонилы, алифатические сульфинилы, ароматические сульфинилы, алифатические сульфамилы, ароматические сульфамилы, ароматические фосфаты и алифатические фосфаты. Термин "аминокислота" обозначает молекулу, которая содержит аминогруппу и карбоксильную группу, общей формулы NH2CHRCOOH. Термин "аминокислота" включает стандартные аминокислоты и нестандартные аминокислоты. Термин "стандартная аминокислота" обозначает аланин, аргинин, аспарагин, аспарагиновую кислоту, цистеин, глутаминовую кислоту, глутамин, глицин, гистидин, изолейцин, лейцин, лизин, метионин,фенилаланин, пролин, серии, треонин, триптофан, тирозин и валин. Термин "стандартная аминокислота, которая не является аспарагиновой кислотой" обозначает аминокислоту, которую выбирают из группы, включающей аланин, аргинин, аспарагин, цистеин, глутаминовую кислоту, глутамин, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин,серии, треонин, триптофан, тирозин и валин. В случае глутамина или глутаминовой кислоты производное обозначает, например, нитрил или сложный эфир, такой как, например, нитрил глутамина, сложный эфир глутаминовой кислоты. Термин "нестандартная аминокислота" обозначает аминокислоты (молекулу, которая содержит аминогруппу и карбоксильную группу), которые не относятся к стандартным аминокислотам. Примеры- 16017735 нестандартных аминокислот обозначают селеноцистеин (входит в состав некоторых белков и кодируется кодоном УГА), пирролизин (который используется некоторыми метанобразующими бактериями, продуцирующими метан, входит в состав ферментов и кодируется кодоном УАГ), лантионин, 2-аминоизомасляную кислоту, дегидроаланин, 3-амино-6-гидрокси-2-пиперидон, -аминомасляную кислоту, орнитин, цитруллин, гомоцистеин, допамин или гидроксипролин. Термин "неосновная стандартная аминокислота" обозначает аланин, аспарагин, аспарагиновую кислоту, цистеин, глутаминовую кислоту, глутамин, глицин, изолейцин, лейцин, метионин, фенилаланин,пролин, серии, треонин, триптофан, тирозин и валин. Термин "Ahp" (3-амино-6-гидроксипиперидин-2-он) обозначает нестандартную аминокислоту, входящую в состав, например, цианобактерий. Термин "производные Ahp" включает, не ограничиваясь только ими, 3-амино-3,4-дигидро-1H-пиридин-2-он (дегидро-AHP), 3-аминопиперидин-2-он и производные АНР и простых и сложных эфиров. Предпочтительно производные Ahp обозначают 3 аминопиперидин-2-он, или Ahp-I или Ahp-II, как показано ниже, где R выбирают из группы, включающей C1-С 12 алкил, C2-С 12 алкенил, C2-С 12 алкинил, галоген(C1-C12)алкил, C1-С 12 алкокси(C1-C12)алкил, C1-С 12 алкокси(C1-C12)алкокси(C1-C12)алкил, гидрокси(C1-C12)алкил, фенил и фенил(C1-C6)алкил. Различные члены указанного семейства нестандартных аминокислот обозначают: Производное пролина включает, например, 5-гидроксипролин. Термин "производные аминокислот" включает, не ограничиваясь только ими, O-алкил, O-арил, Oацил, S-алкил, S-арил, S-S-алкил, алкоксикарбонил, O-карбонилалкоксигруппу, карбонат, Oкарбониларилоксигруппу, O-карбонилалкиламиногруппу, O-карбонилариламиногруппу, N-алкил, Nдиалкил, N-триалкиламмоний, N-ацил, N-карбонилалкоксигруппу, N-карбониларилоксигруппу, Nкарбонилалкиламиногруппу, N-карбонилариламиногруппу, N-сульфонилалкил или N-сульфониларил. Термин "производные неосновных стандартных аминокислот" включает, не ограничиваясь только ими, O-алкил, O-арил, O-ацил, S-алкил, S-арил, S-S-алкил, алкоксикарбонил, O-карбонилалкоксигруппу,карбонат, O-карбониларилоксигруппу, O-карбонилалкиламиногруппу, O-карбонилариламиногруппу, Nалкил, N-диалкил, N-триалкиламмоний, N-ацил, N-карбонилалкоксигруппу, N-карбониларилоксигруппу,N-карбонилалкиламиногруппу, N-карбонилариламиногруппу, N-сульфонилалкил или N-сульфониларил. Термин "производное тирозина" включает, не ограничиваясь только ими, O-алкил, O-арил, Oгетероарил, O-ацил, O-PO3H и O-SO3H, а также галогенированные в орто- или мета-положении производные. Группа ОН в составе тирозина может обозначать OR, где R выбирают из группы, включающей водород, C1-С 12 алкил, C2-С 12 алкенил, C2-С 12 алкинил, галоген(C1-C12)алкил, галоген(C2-C12)алкенил, галоген(C2-C12)алкинил, C1-С 12 алкоксикарбонил, C1-С 12 алкоксикарбонил(C1-C12)алкил, C1-С 12 алкиламинокарбонил, незамещенный или дополнительно замещенный арилом, арилалкилом, арилалкенилом или арилалкинилом, гетероциклилом и гетероциклилалкилом. Термин "производное депсипептида" включает, не ограничиваясь только ими, модифицированные депсипептиды, как описано в данном контексте, и более подробно ниже в разделе "Примеры". Указанные производные можно получить по известным методикам. Настоящее изобретение также относится к фармацевтически приемлемым солям и производным соединений по настоящему изобретению, а также к способам получения указанных соединений. Один способ получения соединения заключается в культивировании штамма Chondromyces, его вариантов или- 17017735 мутантных форм в пригодных условиях, предпочтительно по методике ферментации, описанной ниже."Соли" соединений по настоящему изобретению, содержащих по крайней мере одну солеобразующую группу, получают по стандартным методикам. Например, соли соединений по настоящему изобретению, содержащих кислотные группы, получают при обработке указанных соединений соединениями металлов, такими как соли щелочных металлов пригодных органических карбоновых кислот, например,натриевая соль 2-этилгексановой кислоты, органическими соединениями щелочных или щелочноземельных металлов, такими как соответствующие гидроксиды, карбонаты или гидрокарбонаты, такие как гидроксид, карбонат или идрокарбонат натрия или калия, соответствующими соединениями кальция или аммония или пригодным органическим амином, предпочтительно в стехиометрическом количестве или в присутствии небольшого избытка солеобразующего агента. Кислотно-аддитивные соли соединений по настоящему изобретению получают по стандартным методикам, например, при обработке указанных соединений кислотой или ионно-обменным реагентом. Внутренние соли соединений по настоящему изобретению, содержащих кислотную и основную солеобразующие группы, например, свободную карбоксильную группу и свободную аминогруппу, получают, например, при нейтрализации солей, таких как кислотно-аддитивные соли, до рН, соответствующего электрической точке, например, слабыми основаниями или при обработке ионообменниками. Соли можно превратить в свободные соединения по стандартным методикам, например, соли металлов и аммония при обработке пригодными кислотами, а кислотно-аддитивные соли, например, при обработке пригодным основанием. Смеси изомеров, полученные по настоящему изобретению, можно разделить на индивидуальные изомеры известными способами, например, диастереоизомеры при распределении в многофазных смесях растворителей, при перекристаллизации и/или хроматографией, например, на силикагеле, или жидкостной хроматографией среднего давления на обращено-фазовой колонке, а рацематы разделяют, например,при образовании солей с оптически чистыми солеобразующими реагентами и разделением полученной таким образом смеси диастереоизомеров, например, фракционной кристаллизацией или хроматографией на колонках с оптически активными материалами. Промежуточные и конечные продукты можно обрабатывать и/или очищать по стандартным методикам, например, методами хроматографии, распределения, (пере-)кристаллизации и т.п. Циклические депсипептиды по настоящему изобретению ингибируют химотрипсин-подобные протеазы. Примеры химотрипсин-подобных протеаз включают эластазы и калликреин 7. Прежде всего циклические депсипептиды по настоящему изобретению являются эффективными ингибиторами калликреина 7. Термин "ингибитор" обозначает циклический депсипептид, который ингибирует ферментативную реакцию, при этом мерой ингибирования является величина IC50, составляющая менее 100 мкМ, например, 50 мкМ, 30 мкМ, 20 мкМ или 10 мкМ. Прежде всего предпочтительны циклические депсипептиды,характеризующиеся величиной IC50 менее 30 мкМ для калликреина 7 человека, например, циклические депсипептиды, характеризующиеся величиной IC50 менее 10 мкМ, 1 мкМ, 100 нМ, 50 нМ, 40 нМ, 40 нМ,30 нМ, 20 нМ, 10 нМ или менее. Например, величина IC50 для соединений, описанных в примерах 5, 19 и 33, составляет 0,009 мкМ, 0,007 мкМ, 0,005 мкМ, соответственно. Величину IC50 для калликреина 7 человека можно определять с использованием субстрата с гашением флуоресценции Ac-Glu-Asp(EDANS)Lys-Pro-Ile-Leu-PheArg-Leu-Gly-Lys(DABCYL)-Glu-NH2 (гдеобозначает расщепляемую связь по данным МС) фирмы Biosyntan (Берлин, Германия). Ферментативную реакцию проводили в 50 мМ натрийцитратном буферном растворе, pH 5,6, содержащем 150 мМ NaCl и 0,05% (мас./об.) CHAPS. ВеличинуIC50 определяли при комнатной температуре в 384-луночном планшете. Конечный объем реакционной смеси для анализа во всех лунках составлял 30 мкл. Исследуемые соединения растворяли в 90% (об./об.) ДМСО/вода и разбавляли в воде (содержащей 0,05% (мас./об.) CHAPS) в 3 раза, при этом получали требуемые 11 конечных концентраций соединения: 0,3 нМ, 1 нМ, 3 нМ, 10 нМ, 30 нМ, 100 нМ, 300 нМ, 1 мкМ, 3 мкМ, 10 мкМ и 30 мкМ. Для анализа в каждую лунку добавляли 10 мкл смеси вода/CHAPS (+ исследуемое соединение), затем 10 мкл раствора протеазы (разбавленный буферным раствором для анализа 1,5). Концентрация протеазы в конечном растворе для анализа составляла 0,2 нМ (концентрацию фермента определяли методом Бредфорд). После инкубации при комнатной температуре в течение 1 ч реакцию инициировали при добавлении 10 мкл раствора субстрата (субстрат растворяли в буферном растворе для анализа 1,5, конечная концентрация 2 мкМ). Действие соединения на ферментативную активность оценивали с использованием графиков зависимости ингибирования в % от концентрации ингибитора и по двум значениям, первое значение регистрировали непосредственно после добавления субстрата(t=0) и второе значение через 1 ч (t=60 мин). Величину IC50 рассчитывали методом нелинейного регрессионного анализа с использованием программного обеспечения (XLfit, версия. 4.0 ID Business SolutionLtd., Guildford, Surrey, Великобритания). Термины "заболевания" и "нарушения", которые поддаются лечению или профилактике циклическими депсипептидами, включают заболевания, связанные с химотрипсин-подобными протеазами, более предпочтительно, заболевания, связанные с активностью эластазы или калликреина 7. Предпочтительны- 18017735 также заболевания, связанные с эластазой нейтрофилов человека. Заболевания и нарушения, которые поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению,включают боль, острое воспаление, хроническое воспаление, артрит, воспаленные суставы, бурсит, остеоартрит, ревматоидный артрит, юношеский ревматоидный артрит, септический артрит, фибромиалгию,системную красную волчанку, флебит, тендинит, высыпания, псориаз, угри, экзему, лицевую себорейную экзему, экзему рук, лица или шеи, инфекции крайней плоти, дерматомикоз стопы, свищевые инфекции, инфицированные топические язвы, пупочные инфекции у новорожденных, зуд, связанный с морщинами, шрамами, келоидными рубцами, фурункулами, бородавками и с аллергией, геморрой, раны, раневые инфекции, раны от ожогов, грибковые инфекции и иммунные нарушения, включая аутоиммунные заболевания. Предпочтительные заболевания, которые поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают хроническое обструктивное заболевание легких (включая легочную эмфизему и хронический бронхит), хроническую и острую интерстициальную пневмонию, идиопатическую интерстициальную пневмонию (ИИП), диффузный глубокий бронхит, муковисцидоз легких, острое повреждение легких (ОПЛ)/острый респираторный дистресс-синдром(ОРДС), бронхоэктаз, астму, панкреатит, нефрит, гепатит (печеночная недостаточность), хронический ревматоидный артрит, артросклероз, остеоартрит, псориаз, парадонтоз, атеросклероз, отторжение трансплантата, повреждение тканей при ишемии/реперфузии, шок, сепсис, коагулопатию, включая рассеянную внутрисосудистую коагуляцию (РВК) и тромбоз глубоких вен, конъюктивит, кератит, язву роговицы, болезнь Крона, системную красную волчанку. Более предпочтительные заболевания, которые поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают "эпителиальную дисфункцию" или "эпителиальное заболевание", которое включает, не ограничиваясь только ими, воспалительные и/или гиперпролиферативные и зудящие кожные заболевания, такие как келоидные рубцы, гипертрофические шрамы, угри, атопический дерматит, псориаз, синдром Незертона или другие зудящие дерматозы, такие как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как воспалительное заболевание кишечника и болезнь Крона, муковисцидоз, хроническое обструктивное заболевание легких (ХОЗЛ), легочный фиброз, респираторный дистресс синдром у взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника,псориаз, астму. В другом предпочтительном варианте циклические депсипептиды по настоящему изобретению можно использовать для лечения рака, прежде всего рака яичников. Заболевания и нарушения, которые поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают воспалительные и/или гиперпролиферативные и зудящие кожные заболевания, такие как келоидные рубцы, гипертрофические шрамы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона или другие зудящие дерматозы, такие как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников,муковисцидоз, хроническое обструктивное заболевание легких (ХОЗЛ), легочный фиброз, респираторный дистресс-синдром у взрослых, хронический бронхит, наследственная эмфизема, ревматоидный артрит, воспалительное заболевание кишечника, псориаз и астму. Заболевания и нарушения, которые более предпочтительно поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают келоидные рубцы, гипертрофические шрамы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона или другие зудящие дерматозы, такие как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как старческая кожа, воспалительное заболевание кишечника и болезнь Крона, а также панкреатит или рак, прежде всего рак яичников. Предпочтительные заболевания и нарушения, которые поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают муковисцидоз, хроническое обструктивное заболевание легких (ХОЗЛ), легочный фиброз, респираторный дистресс-синдром у взрослых, хронический бронхит, наследственную эмфизему, ревматоидный артрит, воспалительное заболевание кишечника, псориаз и астму. Заболевания и нарушения, которые даже более предпочтительно поддаются лечению или профилактике циклическими депсипептидами по настоящему изобретению, включают келоидные рубцы, гипертрофические шрамы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона или другие зудящие дерматозы, такие как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как старческая кожа. Калликреин 7 человека (К 7 ч) является ферментом, который проявляет активность сериновой протеазы и локализован в коже человека. Впервые он был описан как фермент химотрипсинового типа из рогового слоя (ХРС), который может играть роль в отшелушивании рогового слоя за счет расщепления белков рогового слоя (например, корнеодесмозин и плакоглобин). Роговой слой является внешним слоем- 19017735 эпидермиса, формирующим барьер, и состоит из ороговевших эпителиальных клеток, окруженных высокоорганизованными липидами. Он непрерывно образуется в результате эпидермальной дифференциации,а постоянная толщина рогового слоя в нормальном эпидермисе поддерживается за счет равновесия между пролиферацией кератиноцитов и отшелушиванием. Повышенная экспрессия ХРС при воспалительном заболевании кожи может иметь этиологическое значение (Hansson и др. (2002. Было установлено, что у трансгенных мышей с экспрессией калликреина 7 человека эпидермальными кератиноцитами развиваются патологические изменения кожи с повышенной толщиной эпидермиса, гиперкератозом, воспалением кожи и тяжелым пруритом. Была установлена генетическая взаимосвязь между вставкой из 4 п.о.(ААСС) в 3'-UTR-фрагменте (3'-нетранслируемая область) гена химотрипсиноподобного фермента рогового слоя и атопическим дерматитом (Vasilopoulos и др. (2004, что свидетельствует о важной роли фермента в развитии атопического дерматита. Атопическим дерматитом является заболевание, при котором наблюдается повреждение барьера кожи и которое поражает 15-20% детей. Калликреин 7 является сериновой протеазой S1, относится к семейству генов калликреина и проявляет химотрипсиноподобную активность. Калликреин 7 человека (К 7 ч, KLK7 или фермент химотрипсинового типа из рогового слоя (ХРС), Svvissprot P49862) играет важную роль в физиологии кожи (1, 2, 3). В основном он экспрессируется в коже и, как было установлено, играет важную роль в физиологии кожи. К 7 ч принимает участие в деградации межклеточных связующих структур ороговевшего плоского эпителия в процессе отшелушивания клеток кожи. Процесс отшелушивания строго регулируется и находится в неустойчивом равновесии с продуцированием de novo корнеоцитов, чтобы поддерживать постоянную толщину рогового слоя, который является внешним слоем кожи и который принимает основное участие в функционировании барьера кожи. В связи с этим было установлено, что К 7 ч расщепляет корнеодесмосомальные белки - корнеодесмозин и десмоколлин 1 (4, 5, 6). Деградация корнеодесмосом необходима для отшелушивания. Кроме того, недавно было установлено, что фермент К 7 ч расщепляет два деградирующих липиды фермента глюкоцереброзидазу и кислую сфингомиелиназу (7). Оба деградирующих липиды фермента секретируются совместно с их субстратами - глюкозилцерамидами и сфингомиелином- и расщепляют эти полярные предшественники липидов с образованием более неполярных продуктов,например, церамидов, которые затем встраиваются во внеклеточную многослойную мембрану. Структура многослойной мембраны играет важную роль в функционировании клеточного барьера. И наконец было установлено, что К 7 ч активирует предшественник интерлейкина-1 (ИЛ-1), при этом образуется его активная форма in vitro (8). Так как кератиноциты экспрессируют ИЛ-1, но не активную форму специфического ИЛ-1 конвертирующего фермента (ИКФ или каспаза 1), можно предположить, что активация ИЛ-1 в эпидермисе человека происходит под действием другой протеазы, предположительно фермента К 7 ч. Недавно была установлена взаимосвязь повышенной активности К 7 ч с воспалительными заболеваниями кожи, такими как атопический дерматит, псориаз или синдром Незертона. Такая повышенная активность может привести к неконтролируемой деградации корнеодесмом, что в свою очередь может привести к разрегулированному отшелушиванию, повышенной деградации расщепляющих липиды ферментов и повреждению структуры многослойной мембраны или неконтролируемой активации провоспалительного цитокина ИЛ-1. В результате нарушается фукционирование клеточного барьера и развивается воспаление (см. также WO-A-2004/108139). В связи с тем, что активность К 7 ч контролируется на нескольких уровнях, повышенную активность К 7 ч при воспалительных заболеваниях кожи могут вызывать различные факторы. Во-первых, на количество экспрессированной протеазы могут влиять генетические факторы. Например, в качестве такой генетической связи недавно был выявлен полиморфизм 3'-UTR(3'-нетранслируемая область) в гене К 7 ч (9). Авторы предполагают, что описанная вставка из 4 п.о. в 3'-UTR-фрагменте гена К 7 ч стабилизирует мРНК К 7 ч, что приводит к сверхэкспрессии К 7 ч. Во-вторых, так как К 7 ч секретируется из многослойных тел в межклеточное пространство рогового слоя в виде профермента и не способен самоактивироваться,то для его активации требуется другая протеаза, например, К 5 ч (5). Неконтролируемая активность такого активирующегося фермента может привести к сверхэкспрессии К 7 ч. В-третьих, активированный К 7 ч можно ингибировать природными ингибиторами, такими как LEKTI, ALP или элафин (10, 11). сниженный уровень экспрессии таких ингибиторов или их отсутствие может привести в повышенной активности К 7 ч. Недавно было установлено, что мутации в гене spink5, кодирующем LEKTI, являются причиной развития синдрома Незертона (12), а одноточечная мутация в гене связана с атопическим дерматитом(13, 14). И наконец, другим уровнем контроля активности К 7 ч является pH. pH-Оптимум К 7 ч находится в интервале от нейтрального до слабо щелочного pH (2), а градиент pH по направлению от внутреннего до внешнего слоев кожи составляет от нейтрального до кислого pH. Факторы окружающей среды, такие как мыло, могут привести к повышению pH во внешних слоях рогового слоя до pH-оптимума К 7 ч, и тем самым повысить активность К 7 ч. Повышенная активность К 7 ч связана с заболеваниями кожи, вызванными повреждением барьера кожи, включающими воспалительные и гиперпролиферативные заболевания кожи. Во-первых, у пациентов с синдромом Незертона наблюдается зависимое от фенотипа увеличение активности сериновых про- 20017735 теаз, снижение количества корнеодесмосом, снижение уровня расщепляющих липиды ферментов - глюкоцереброзидазы и кислой сфингомиелиназы, и нарушенная функция барьера кожи (15, 16). Вовторых, у трансгенных мышей со сверхэкспрессией К 7 ч наблюдается фенотип кожи, аналогичный фенотипу пациентов с атопическим дерматитом (17, 18, 19). В-третьих, установлено, что у пациентов с атопическим дерматитом кожи и псориазом наблюдаются повышенные уровни К 7 ч (17, 20). Более того, повышенная активность К 7 и связанная с этим дисфункция эпителиального барьера могут играть важную роль в патологии других эпителиальных заболеваний, таких как воспалительное заболевание кишечника и болезнь Крона. Следовательно, К 7 ч можно рассматривать как потенциальную мишень для лечения заболеваний,связанных с эпителиальной дисфункцией, таких как воспалительные и/или гиперпролиферативные заболевания, и зудящих заболеваний кожи, таких как келоидные рубцы, гипертрофические рубцы, угри, атопический дерматит, псориаз, пустулезный псориаз, розовые угри, синдром Незертона, или других зудящих дерматозов, таких как узелковая почесуха, неспецифический зуд у людей пожилого возраста, а также другие заболевания, связанные с дисфункцией эпителиального барьера, такие как воспалительное заболевание кишечника и болезнь Крона, а также панктеатит или рак, прежде всего рак яичников, и таким образом существует необходимость в разработке специфических модуляторов (агонистов или ингибиторов) К 7 ч. Эластаза нейтрофилов человека (НЭч, известная также под названием эластаза лейкоцитов, ЛЭч) относится к семейству сериновых протеаз типа химотрипсина. pH-Оптимум ее каталитической активности составляет приблизительно 7, а каталитический участок включает три образующих водородные связи аминокислотных остатка: His57, Asp102 и Ser195 (нумерация соответствует последовательности химотрипсина), которые образуют так называемую каталитическую триаду. Фермент состоит из одной полипептидной цепи, включающей 218 аминокислотных остатка и четыре дисульфидных связи. Гомология последовательности с другими эластинолитическими или неэластинолитическими сериновыми протеиназами составляет от 30 до 40%. НЭч предпочтительно расщепляет окисленную цепь В инсулина, содержащую остаток валина в положении P1, но также расщепляет связи, содержащие остатки аланина, серина или цистеина в положении P1. НЭч локализована в азурофильных гранулах полиморфноядерных лейкоцитов (ПМЯЛ), которые характеризуются достаточной высокой концентрацией НЭч (3 мкг фермента/10 клеток). Основная физиологическая функция фермента заключается в расщеплении бактерий и иммунных комплексов, он также принимает участие в защитном механизме организма-хозяина. НЭч способствует также миграции нейтрофилов из крови в различные ткани, такие как дыхательные пути, в ответ на факторы хемотаксиса. НЭч принимает также участие в ранозаживлении, регенерации ткани и апоптозе ПМЯЛ. Наряду с эластином (высоко эластичный и высоко гидрофобный компонент соединительной ткани легких, артерий, кожи и связок), НЭч расщепляет множество белков, проявляющих важную биологическую функцию, включая коллагены различного типа, мембранные белки и протеогликаны хрящевых тканей. НЭч косвенно способствует деградации белков внеклеточного матрикса за счет активации проколлагеназы, простромелизина и прожелатиназы. НЭч инактивирует также ряд эндогенных ингибиторов протеиназ, таких как а 2-антиплазмин, 1-антихимотрипсин, антитромбин и тканевой ингибитор металлопротеиназ. В легочной системе активность внеклеточной эластазы строго контролируется ингибитором 1 протеаз (11), ответственным за защиту нижних дыхательных путей от эластолитической деградации, в то время как секреторный ингибитор протеиназы лейкоцитов в основном защищает верхние дыхательные пути. В рядепатофизиологических состояний легких, например, при эмфиземе легких, хроническом бронхите и муковисцидозе, эндогенные ингибиторы эластаз неэффективны в регуляции активности НЭч. Предполагается, что НЭч является первичным источником повреждения тканей, связанного с воспалительными заболеваниями, таким как энфизема легких, респираторный дистресс-синдром взрослых(РДСВ), хронический бронхит, хроническая обструктивная болезнь легких (ХОБЛ), легочная гипертензия, и с другими воспалительными заболеваниями, такими как легочная дисплазия у недоношенных новорожденных. НЭч принимает участие в патогенезе повышенной и аномальной секреции дыхательных путей, обычно связанной с воспалительными заболеваниями дыхательных путей. Таким образом, бронхоальвеолярная промывная жидкость (БАПЖ), полученная от пациентов с диагнозом хронического бронхита и муковисцидоза, характеризуется повышенной активностью НЭч. Более того, полагают, что избыточная эластаза принимает участие не только в развитии указанных хронических воспалительных заболеваний, но и острых воспалительных заболеваний, таких как ХОБЛ и септический шок. Следовательно, НЭч можно рассматривать как потенциальную мишень для лечения заболеваний,связанных с активностью НЭч, таких как воспалительные заболевания, такие как энфизема легких, респираторный дистресс-синдром взрослых (РДСВ), хронический бронхит, хроническая обструктивная болезнь легких (ХОБЛ), легочная гипертензия, и другие воспалительные заболевания, а также легочная дисплазия у недоношенных новорожденных, и заболевания, связанные с повышенной и аномальной секрецией дыхательных путей, а также острые воспалительные заболевания. Таким образом существует не- 21017735 обходимость в разработке специфических модуляторов (агонистов или ингибиторов) НЭч. Лечение можно проводить местным или системным способом, например, с использованием кремов,мазей и суппозиториев, или подкожным или внутривенным способом или ингаляцией, соответственно. В одном объекте депсипептиды по настоящему изобретению получают при культивировании штамма Chondromyces crocatus, депонированного в коллекции DSM 24 апреля 2007 г. под номером DSM 19329, или штамма Chondromyces robustus депонированного в коллекции DSM 24 апреля 2007 г. под номером DSM 19330, или штамма Chondromyces apiculatus, депонированного в коллекции DSM 23 июня 2007 г. под номером DSM 21595. Депонирование штаммов проводили согласно инструкциям Будапештского международного соглашения по индентификации и депонированию микроорганизмов для оформления патентов. Депонированные штаммы безоговорочно и без ограничения доступны для использования после публикации патента. Депонированные штаммы представлены только для ознакомления специалистов в данной области техники и депонирование не требуется для применения указанных штаммов на практике. Следует понимать, что настоящее изобретение не ограничивается культивированием конкретных штаммов Chondromyces crocatus, Chondromyces robustus и Chondromyces apiculatus. Напротив, в настоящее изобретение включено культивирование других организмов, способных продуцировать депсипептиды, таких как мутантные формы или варианты штаммов, которые можно получить из организма по известным методикам, таким как облучение рентгеновскими лучами, в УФ-свете, обработка химическими мутагенами, действие фагов, селекция с использованием антибиотиков и т.п. Депсипептиды по настоящему изобретению можно получить в результате биосинтеза различных микроорганизмов, которые могут синтезировать соединения по настоящему изобретению и которые включают, но не ограничиваясь только ими, бактерии порядка Myxococcales, так называемые миксобактерии. Примеры членов, принадлежащих к роду миксобактерий, включают, но не ограничиваясь только ими, Chondromyces, Sorangium, Polyangium, Byssophaga, Haploangium, Jahnia, Nannocystis, Koffleria,Myxococcus, Corallococcus, Cystobacter, Archangium, Stigmatella, Hyalangium, Melittangium, Pyxicoccus. Таксономия миксобактерий является сложной системой и описана в книге Garrity G.M., Bell J.Y., LilburnT.G., Taxonomic outline of the prokaryotes, Bergey's manual of systematic bacteriology, 2-е изд., вып.5.0 (май 2004), http://141.150.157.80/bergeysoutline/main.htm). Соединения формул (I-XVII) получают в ходе аэробной ферментации в пригодной среде в контролируемых условиях при высеивании культур Chondromyces crocatus, Chondromyces robustus и Chondromyces apiculatus. Пригодной средой является предпочтительно водная среда, содержащая источники ассимилируемых углерода, азота и неорганических солей. Пригодные среды включают, но не ограничиваясь только ими, питательные среды, описанные ниже в примерах 1 и 2. Ферментацию проводили в течение от приблизительно 3 до приблизительно 20 сут при температуре от приблизительно 10C до приблизительно 40C, однако оптимальные результаты можно получить предпочтительно в ходе ферментации при приблизительно 30C. Величина pH питательной среды в ходе ферментации составляет от приблизительно 6,0 до приблизительно 9,0. Культуральную среду, засеянную продуцирующими депсипептиды микроорганизмами, можно инкубировать в аэробных условиях, с использованием, например, ротационной качалки или ферментера с мешалкой. Аэрацию можно осуществлять при продувке засеянной культуральной жидкости воздухом,кислородом или соответствующей газообразной смесью в ходе инкубации. Как только образуется достаточное количество депсипептидов, их можно концентрировать и выделять стандартными методами, например, с использованием экстракции, хроматографии, осаждения или кристаллизации, и/или по описанным в данном контексте методикам. Например, при экстракции культуральную жидкость смешивают с пригодным органическим растворителем, таким как н-бутанол, этилацетат, циклогексан, н-гексан, толуол, н-бутилацетат или 4-метил-2-пентанон, с последующим перемешиванием, при этом получают депсипептиды в органическом растворителе, который удаляют при пониженном давлении. Полученный остаток можно необязательно растворить, например, в воде, этаноле, метаноле или их смеси, и повторно экстрагировать пригодным органическим растворителем, таким как гексан, четыреххлористый углерод, дихлорметан или их смесь. После удаления растворителя соединения можно дополнительно очищать с использованием хроматографических методов. Пример носителей для хроматографии включает стационарные фазы, такие как силикагель или оксид алюминия, а в качестве элюента можно использовать органические растворители или их смеси, включая простые эфиры, кетоны, сложные эфиры, галогенированные углеводороды или спирты, или с использованием обращено-фазовой хроматографии на модифицированном силикагеле, содержащем различные функциональные группы, а в качестве элюента можно использовать органические растворители или их водные смеси, такие как ацетонитрил, метанол или тетрагидрофуран при различном pH. Другой пример включает распределительную хроматографию, например,в режиме твердое вещество-жидкость или жидкость-жидкость. Можно также использовать гельфильтрафию, например, на сефадексе LH-20 (Sigma-Aldrich), а в качестве элюента использовать различные растворители, предпочтительно спирты. Как известно в данной области техники, процессы продуцирования, а также выделения и очистки- 22017735 можно контролировать рядом аналитических методов, включая биоанализ, ТСХ, ЖХВР или их комбинацию, с использованием различных методов детекции, в случае ТСХ обычно используют облучение в УФсвете, проявление парами иода или распыление окрашивающими реагентами, в случае ЖХВР обычно используют УФ-свет, методы МС или светорассеяния. Например, в случае ЖХВР используют обращенофазовую колонку с модифицированным силикагелем, а в качестве элюента - линейный градиент полярного смешивающегося с водой растворителя в воде при определенном значении pH с использованием УФ-детектора при различных длинах волн, а также МС-детектора. Полученные в ходе биосинтеза микроорганизмов депсипептиды необязательно можно модифицировать статистическим или направленным методом, при этом получают производные или структурные аналоги указанных соединений Такие производные или структурные аналоги обладают аналогичной функциональной активностью и включены в объем настоящего изобретения. Депсипептиды можно необязательно модифицировать по известным методикам или как описано в данном контексте. Например, производные депсипептидов по настоящему изобретению можно получить при модификации циклических депсипептидов формулы указанная модификация включает а) получение соединения, где А 4 обозначает органической или неорганической кислотой, например, трифторуксусной кислотой, серной кислотой, хлористо-водородной кислотой или кислотой Льюиса, например, эфиратом нитрофторида бора, в растворителе, например, в дихлорметане, ТГФ или в отсутствие растворителя, при температуре от -78C до 150C, предпочтительно от -30C до КТ,б) получение соединения, где А 4 обозначает молекулярным водородом или его источником, например, циклогексеном, формиатом аммония, в присутствии катализатора, например, палладия, в растворителе, например, 2-пропаноле при температуре от -50 до 100C, предпочтительно при КТ,в) получение соединения, где А 4 обозначает органической или неорганической кислотой, например, серной кислотой, хлористо-водородной кислотой или кислотой Льюиса, например, эфиратом трифторида бора, в присутствии восстанавливающего агента, например, триэтилсилана, в присутствии растворителя, например, дихлорметана, ТГФ или в отсутствие растворителя, при температуре от -78 до 150C, предпочтительно от -50C до КТ,г) получение соединения, где А 4 обозначает замещенным или незамещенным спиртом и органической или неорганической кислотой, например,трифторуксусной кислотой, серной кислотой, хлористоводородной кислотой или кислотой Льюиса, например, солями металла в растворителе, например, в замещенном или незамещенном спирте, ТГФ, дихлорметане, предпочтительно в замещенном или незамещенном спирте или в отсутствие растворителя при температуре от -78 до 150C, предпочтительно от -30 до 50C,д) получение соединений, где А 1 обозначает где R предпочтительно обозначает H, алкил, замещенный алкил, замещенным или незамещенным спиртом и органической или неорганической кислотой, например, трифторуксусной кислотой, серной кислотой, хлористо-водородной кислотой или кислотой Льюиса, например, эфиратом трифторида бора в растворителе, например, в замещенном или незамещенном спирте, ТГФ, дихлорметане, предпочтительно в замещенном или незамещенном спирте или в отсутствие растворителя при температуре от -78C до 150C, предпочтительно от -30C до КТ,е) получение соединений, где А 1 обозначает дегидратирующим агентом, например, ангидридом трифторуксусной кислоты в присутствии основания, например, диизопропилэтиламина (DIPEA), в растворителе, например, дихлорметане или в отсут- 24017735 ствие растворителя при температуре от -78C до 150C, предпочтительно от -30C до КТ,ж) получение соединений, где А 4 обозначает и A6 обозначает Tyr, алкилирующим агентом, например, метилиодидом, бензилбромидом, пропаргилбромидом, или ацилирующим агентом, например, этилхлорформиатом или алкил- или арилизоцианатом, в присутствии основания, например, карбоната натрия, в растворителе, например, ДМФА, или в отсутствие растворителя при температуре от -78 до 150C, предпочтительно от -30C до КТ, предпочтительно при обработке ультразвуком. Если не указано иное, следует понимать, что все перечисленные в настоящем описании и формуле изобретения числа, относящиеся к количеству ингредиентов, свойствам, таким как молекулярная масса,условия реакции, величины IC50 и т.п., во всех случаях можно изменять в соответствии с термином "приблизительно". В связи с этим, если не указано прямо противоположное, числовые параметры, указанные в настоящем описании и прилагаемой формуле изобретения, являются приблизительными. По крайней мере и не ограничивая предел применения принципов эквивалентов к объему формулы изобретения, каждый числовой параметр представлен в виде значащей цифры с учетом обычных методов округления. Несмотря на то, что числовые диапазоны и параметры, представляющие широкий объем изобретения,являются приблизительными, числовые значения, указанные в примерах, таблицах и фигурах, представлены по возможности в виде более точных значений. Представляется очевидным, что любые числовые значения включают определенные ошибки, которые наблюдаются в результате изменений условий экспериментов, испытаний соединений, статистического анализа и т.п. Если не указано иное, все технические и научные термины, использованные в настоящем контексте,имеют стандартные значения, известные в данной области техники, к которой принадлежит настоящее изобретение. Хотя на практике или при испытаниях соединений по настоящему изобретению можно использовать аналогичные или эквивалентные методы и материалы, пригодные методы и материалы описаны ниже. Все публикации, заявки и патенты или другие ссылки, перечисленные в данном контексте,включены в данное описание в качестве ссылок. В случае конфликта, основанием является настоящее описание, включая определения терминов. Кроме того, материалы, методы и примеры представлены только для иллюстрации изобретения и не ограничивают его объем. Примеры Пример 1. Получение соединений. Пример 1.1. Получение соединений формул (II)-(VII), (XI)-(XIV) и (XVII). Штамм. Штамм был однозначно отнесен к виду Chondromyces, основываясь на морфологических признаках плодовых тел, а также на части последовательности гена 16S-PHK. C.crocatus относят к первой группе биологического риска по классификации DSMZ (DSMZ (2007. Род Chondromyces относится к семейству Polyangiaceae, принадлежащему к порядку Myxococcales класса дельта-протеабактерии. Бактерии порядка Myxococcales, также называемые миксобактериями, являются грамотрицательными бактериями палочковидной формы и обладают двумя выраженными отличиями от большинства других бактерий. Они закрепляются и начинают расти на твердых поверхностях, используя механизм активного перемещения и агрегирования для формирования плодовых тел при наступлении голодания (Kaiser (2003. Штамм Chondromyces crocatus по настоящему изобретению был депонирован в коллекции DSMZ под номером 19329. Штамм Chondromyces crocatus относится к нежизнеспособной культуре и его нельзя культивировать в виде чистой культуры без сопутствующего штамма. Сопутствующий штамм можно получить и поддерживать в виде чистой культуры при высеивании штрихом полоски совместной культуры, исполь- 25017735 зуя в качестве посевного погруженную культуру с агаровой средой (среда LB). Аналогичные результаты получены учеными из г. Рейгенбах (Jacobi и др. (1996), Jacobi и др. (1997. На основании частичной последовательности ДНК гена 16S-рРНК сопутствующего штамма по настоящему изобретению для штамма Chondromyces crocatus, Bosea thiooxidans из подкласса Rhizobiales наибольшая степень гомологии наблюдается с последовательностью ДНК в составе альфа-протеобактерий. Гомология фрагмента 16SpPHK, содержащего 424 п.о., составляет приблизительно 98% по сравнению с последовательностью штамма AF508112 (В.thiooxidans) из генофонда. В. Htiooxidans выделяли из твердых образцов, которые собирали на различных сельскохозяйственных полях в округе Калькутты, Индия. Этот штамм окисляет восстановленные неорганические серосодержащие соединения в присутствии некоторых органических субстратов и был описан в качестве нового вида и нового рода 1996 году (Das и др. (1996. Филогенетическое древо, построенное исходя из последовательности 16S-PHK всех пяти описанных видов родаBosea, показывает, что сопутствующий штамм Bosea, выделенного из С.crocatus, занимает особое положение. Культивирование. Культивирование штамма проводили в ферментере объемом 100 л по следующей методике. Сначала 5 мл (10%) жидкой культуры штамма Chondromyces crocatus высеивали в 50 мл среды MD1 (состав описан в статье Bode и др. (2003), табл. 6) в качалочных колбах с отбойниками объемом 200 мл. После инкубации в течение 11 сут при 30C на ротационной качалке при 120 об/мин первую промежуточную культуру высевали по 10 мл (10%) в среде MD1 (5x100 мл) в пяти качалочных колбах с отбойниками объемом 500 мл. После инкубации в течение 7 сут при 30C на ротационной качалке при 120 об/мин вторую промежуточную культуру высевали по 25 мл (5%) в среде MD1 (19x500 мл) в качалочных колбах с отбойниками объемом 2 л. После инкубации в течение 6 сут при 30C на ротационной качалке при 150 об/мин вторую промежуточную культуру (9,5 л, 9,5%) использовали для высеивания в среду POL1 (100 л) (состав описан в статье Kunze и др. (1995), табл. 7). Полученную основную культуру (100 л) загружали в стандартный стальной ферментер объемом 100 л. Температуру поддерживали при 30C, аэрацию проводили со скоростью 20 л/мин (0,2 об.воздуха/ об.культуры/мин) и перемешивали при 50 об/мин. В ферментере поддерживали избыточное давление 0,5 бар. Величину pH в культуре поддерживали в диапазоне 6,9-7,1 при добавлении 3 н. H2SO4 или 3 н. NaOH. После достижения лаг-фазы через приблизительно 1 сут потребление кислорода увеличивалось через приблизительно 4 сут, что указывало на экспоненциальный рост культуры. В течение последних 2 сут потребление кислорода в некоторой степени снижалось, что указывало на стационарную фазу культуры. Через 7 сут титр циклического депсипептида формулы II составлял 5,3 мг/л, полученную культуральную жидкость собирали. Экстракция. Всю культуральную жидкость переносили в стальной сосуд объемом 1600 л и декантировали в течение 1 ч. Влажный клеточный осадок (200 г) собирали со дна сосуда фильтрованием через бумажный фильтр. Клеточный осадок экстрагировали 3 раза в течение 30 мин по 10 л этилацетата. Затем остаточную воду отделяли от фазы растворителя. Фазу растворителя промывали водой (5 л) и упаривали, при этом получали сухой экстракт, так называемый "клеточный экстракт". Фильтрат культуральной жидкости экстрагировали этилацетатом (200 л). Смесь выдерживали в течение 2 ч, органическую фазу отделяли, промывали водой (20 л) и упаривали, при этом получали сухой экстракт, так называемый "экстракт из культурального фильтрата". Выделение соединения. Экстракт из культурального фильтрата (4,4 г) растворяли в метаноле (80 мл). Нерастворимые ингредиенты удаляли при центрифугировании и супернатант упаривали досуха, при этом получали сухой экстракт (3,3 г). Экстракт растворяли в МеОН (7,5 мл), ДМСО (3 мл) и дихлорметане (0,5 мл) и очищали обращенно-фазовой хроматографией (Waters Sunfire RP18, 10 мкл, 30150 мм), элюент: 0,01% муравьиная кислота (растворитель A1 и ацетонитрил, содержащий 0,1% муравьиной кислоты (растворитель В),скорость потока 50 мл/мин. Градиент описан в табл.1. При очистке проводили 7 циклов хроматографии. Собранные фракции после каждого цикла анализировали методом ЖХВР, фракции, содержащие циклический депсипептид по настоящему изобретению, объединяли и упаривали в вакууме досуха, при этом получали 134 мг циклического депсипептида формулы II, чистота 97% и 80 мг, чистота 90%.- 26017735 Таблица 1. Градиент ЖХВР, очистка циклического депсипептида формулы II. Клеточный экстракт (6,67 г) растворяли в дихлорметане/метаноле, 4:1. Раствор фильтровали и фильтрат пропускали через диатомовую землю (2 г диатомовой земли/1 г экстракта, Isolute, International Sorbent Technology Ltd., Hengoed Mid Glam, Великобритания), затем упаривали. Твердый остаток наносили на колонку с силикагелем (418 см, 90 г силикагеля 40-63) и проводили элюцию в градиенте циклогексана, этилацетата и метанола. Градиент описан в табл.2, скорость потока 28 мл/мин. Собирали фракции объемом по 28 мл. Фракции объединяли согласно пикам поглощения в УФ, получали 12 фракций (A-L). Фракции, содержащие депсипептиды (H-J) по настоящему изобретению, затем очищали обращенно-фазовой хроматографией. Хроматографию и обработку фракций проводили аналогично тому,как описано для экстракта культурального фильтрата, при этом получали циклический депсипептид формулы II (46,1 мг), циклический депсипептид формулы III (17,9 мг) и смесь депсипептидов формулы(VI) и (VII) (6,1 мг, 1:1). Структуру соединений (VI) и (VII) подтверждали по данным МС с высоким разрешением и при сравнении спектров Н-ЯМР смеси соединений (VI) и (VII) со спектрами Н-ЯМР соединения (II). Было установлено, что другие циклические депсипептиды формулы II содержатся в клеточном экстракте в более низких концентрациях. Из смеси этих других циклических депсипептидов выделяли соединения формул (IV), (V) и (XI)-(XV) и (XVII). Характеристика соединени. Физические данные соединения формулы II. ИК (таблетка KBr): 3337, 3297, 3062, 2966, 2936, 2877, 1736, 1659, 1533, 1519, 1464, 1445, 1410,1385, 1368, 1249, 1232, 1205, 989, 832 см-1. МС (FT, 9.4 Т АРЕХ-III): найд. 951,5165, рассч. для C46H72N8O12+Na: 951,5162. 1 Н ЯМР (600 МГц, d6-ДМСО) H: -0,10 (3H, d, J 7,0 Гц), 0,65 (4H, m), 0,78 (3H, d, J 7,0 ГЦ), 0,82 (3H,t, J 7,2 Гц), 0,85 (3H, d, J 7,0 Гц), 0,89 (3H, d, J 7,0 Гц), 1,02 (1H, m), 1,03 (6H, 2d, J 7,0 Гц), 1,10 (1H, m),1,21 (3H, d, J 7,0 Гц), 1,25 (1H, m), 1,40 (1H, m), 1,52 (1H, m), 1,76 (6H, m), 1,84 (1H, m), 1,93 (1H, m), 2,15(1H, d, J 9,5 Гц), 4,71 (1H, m), 4,94 (1H, s), 5,06 (1H, m), 5,49 (1H, m), 6,08 (1H, d, J 2,2 Гц), 6,65 (2H, d, J 8,4), 6,74 (1H, s), 7,00 (2H, d, J 8,4 Гц), 7,27 (1H, s), 7,36 (1H, d, J 9,5 Гц), 7,66 (1H, d, J 10,2 Гц), 7,74 (1H,d, J 8,8 Гц), 8,02 (1H, d, J 8,1 Гц), 8,43 (1H, d, J 8,1 Гц), 9,19 (1H, s). 13 С-ЯМР (150 МГц, d6-ДМСО) C: 10,35 CH3, 11,22 CH3, 13,79 CH3, 16,00 CH3, 17,63 CH3, 19,49 2CH3, 20,83 CH3, 21,72 CH2, 23,30 CH3, 23,70 CH2, 24,16 CH, 24,41 CH2, 27,35 CH2, 29,74 CH2, 30,07 CH3,31,44 CH2, 33,13 CH, 33,19 CH2, 33,68 CH, 37,39 CH, 39,05 CH2, 48,75 CH, 50,59 CH, 52,01 CH, 54,11 CH,54,65 CH, 55,24 CH, 60,60 CH, 71,86 CH, 73,89 CH, 115,28 2CH, 127,31 Cq, 130,35 2xCH, 156,25 Cq,169,09 Cq, 169,25 Cq, 169,34 Cq, 169,74 Cq, 170,60 Cq, 172,41 Cq, 172,52 Cq, 173,78 Cq, 176,32 Cq. Физические данные соединения формулы III. МС (FT, 9.4 Т APEX-III): найд.: 965,5318, рассч. для C47H74N8O12+Na: 965,5318. 1H-ЯМР (600 МГц, d6-ДМСО) H: -0,10 (3H, d, J 7,0 Гц), 0,64 (4H, m), 0,78 (3H,d, J 7,0 Гц), 0,82 (3H,t, J 7,0 Гц), 0,83 (3H, t, J 7,3 Гц), 0,85 (3H, d, J 7,0 Гц), 0,89 (3H, d, J 7,0 Гц), 1,01 (3H, d, J 7,1 Гц), 1,04 (1H,m), 1,10 (1H, m), 1,21 (3H, d, J 7,0 Гц), 1,25 (1H, m), 1,32 (1H, m), 1,40 (1H, m), 1,53 (2 Н, m), 1,77 (6H, m),1,84 (1H, m), 1,92 (1H, m), 2,12 (1H, m), 2,16 (1H, m), 2,28 (1H, m), 2,59 (1H, m), 2,68 (1H, m), 2,72 (3H, s),- 27017735 3,17 (1H, m), 4,32 (1H, m), 4,38 (1H, m), 4,43 (1H, d, J 10,2 Гц), 4,46 (1H, m), 4,63 (1H, d, J 9,5 Гц), 4,71 (1H,m), 4,94 (1H, m), 5,06 (1H, m), 5,49 (1H, m), 6,11 (1H, ушир.s), 6,65 (2 Н, d, J 8,8 Гц), 6,73 (1H, s), 7,00 (2 Н,d, J 8,8 Гц), 7,27 (1H, s), 7,37 (1H, d, J 9,5 Гц), 7,66 (1H, d, J 10,2 Гц), 7,75 (1H, d, J 9,7 Гц), 8,07 (1H, d, J 8,1 Гц), 8,45 (1H, d, J 8,8 Гц), 9,24 (1H, ушир.) Физические данные соединения формулы IV. МС (FT, 9.4 Т APEX-III): найд.: 947,5196, рассч. для C47H72N8O11+Na: 947,5213. 1 Н ЯМР (600 МГц, d6-ДМСО) H: 0,08 (3H, d, J 7,0 Гц), 0,68 (3H, t, J 7,2 Гц), 0,71 (3H, d, J 7,0 Гц),0,78 (3H, d, J 7,0 Гц), 0,83 (3H, t, J 7,3 Гц), 0,84 (1H, m), 0,87 (3H, t, J 7,2 Гц), 0,88 (3H, d, J 7,0 Гц), 0,99(3H, d, J 7,1 Гц), 1,08 (1H, m), 1,17 (3H, d, J 6,7 Гц), 1,18 (1H, m), 1,31 (2 Н, m), 1,43 (1H, m), 1,51 (1H, m),1,54 (1H, m), 1,76 (2 Н, m), 1,90 (1H, m), 1,94 (1H, m), 2,01 (1H, m), 2,10 (1H, m), 2,16 (1H, m), 2,26 (1H, m),2,46 (2 Н, m), 2,73 (1H, m), 2,74 (3H, s), 3,19 (1H, m), 4,34 (1H, m), 4,36 (1H, m), 4,51 (1H, m), 4,55 (1H, m),4,66 (1H, d, J 10,0 Гц), 4,79 (1H, d, J 11,0 Гц), 5,19 (1H, m), 5,28 (1H, m), 5,44 (1H, m), 6,25 (1H, d, J 7,3 Гц),6,33 (1H, d, J 8,8 Гц), 6,68 (2H, d, J 8,8 Гц), 6,75 (1H, s), 7,04 (2H, d, J 8,8 Гц), 7,28 (1H, s), 7,32 (1H, d, J 8,8 Гц), 7,91 (1H, d, J 9,5 Гц), 8,05 (1H, d, J 8,1 Гц), 8,57 (1H, d, J 8,9 Гц), 9,38 (1H, ушир.) Физические данные соединения формулы V. МС (FT, 9.4 Т APEX-III): найд.: 933,5053, рассч. для C46H70N8O11+Na: 953,5056 1 Н ЯМР (600 МГц, d6-ДМСО) H: 0,08 (3H, d, J 7,0 Гц), 0,68 (3H, t, J 7,2 Гц), 0,71 (3H, d, J 7,0 Гц),0,79 (3H, d, J 7,0 Гц), 0,83 (1H, m), 0,88 (3H, t, J 7,2 Гц), 0,89 (3H, d, J 7,0 Гц), 1,01 (3H, d, J 7,0 Гц), 1,03(3H, d, J 7,0 Гц) 1,08 (1H, m), 1,17 (3H, d, J 6,7 Гц), 1,20 (1H, m), 1,31 (1H, m), 1,42 (1H, m), 1,54 (1H, m),1,74 (2 Н, m), 1,91 (2 Н, m), 2,02 (1H, m), 2,10 (1H, m), 2,15 (1H, m), 2,46 (3H, m), 2,75 (3H, s), 2,76 (1H, m),3,19 (1H, m), 4,32 (1H, m), 4,34 (1H, m), 4,51 (1H, m), 4,55 (1H, m), 4,66 (1H, d, J 9,5 Гц), 4,79 (1H, d, J 11,0 Гц), 5,19 (1H, m), 5,28 (1H, m), 5,43 (1H, m), 6,25 (1H, d, J 7,0 Гц), 6,33 (1H, d, J 8,5 Гц), 6,68 (2 Н, d, J 8,8 Гц), 6,75 (1H, s), 7,04 (2 Н, d, J 8,8 Гц), 7,28 (1H, s), 7,31 (1H, d, J 8,8 Гц), 7,90 (1H, d, J 9,5 Гц), 7,99 (1H, d,J 8,1 Гц), 8,52 (1H, d, J 8,8 Гц), 9,30 (1H, ушир.) Физические данные соединения формулы XI. МС (ESI): положит.иониз.: m/z 951,5 (M+Na), отриц.иониз.: m/z 927,5 (М-Н), ММ моноизотопа 928,5, C46H72N8O12 1 Н ЯМР (600 МГц, d6-ДМСО) H: -0,11 (3H, d, J 6,6 Гц), 0,64 (4H, m), 0,77 (3H,d, J 6,6 Гц), 0,83 (3H,m), 0,85 (3H, m), 0,87 (3H, m), 0,89 (3H, m), 1,01 (3H, m), 1,10 (1H, m), 1,21 (3H, d, J 5,9 Гц), 1,32 (1H, m),1,40 (1H, m), 1,52 (2 Н, m), 1,75 (5 Н, m), 1,84 (1H, m), 1,91 (1H, m), 2,05 (1H, m), 2,15 (2 Н, m), 2,27 (1H, m),2,59 (1H, m), 2,68 (1H, m), 2,73 (3H, s), 3,16 (1H, m), 4,31 (1H, m), 4,37 (1H, m), 4,43 (1H, m), 4,45 (1H, m),4,63 (1H, d, J 8,8 Гц), 4,69 (1H, m), 4,94 (1H, m), 5,05 (1H, m), 5,50 (1H, m), 6,15 (1H, ушир.s), 6,65 (2 Н, d, J 8,1 Гц), 6,75 (1H, s), 7,00 (2 Н, d, J 8,1 Гц), 7,29 (1H, s), 7,37 (1H, d, J 9,5 Гц), 7,64 (1H, d, J 9,5 Гц), 7,78 (1H,d, J 8,8 Гц), 8,09 (1H, d, J 8,1 Гц), 8,49 (1H, d, J 9,5 Гц), (OH группа тирозина не детектируется). Физические данные соединения формулы XII. МС (ESI): положит.иониз.: m/z 923,5 (M+Na), отриц.иониз.: m/z 899,5 (М-Н), ММ моноизотопа 900,5, C44H68N8O12 1 Н ЯМР (500 МГц, d6-ДМСО) H: -0,11 (3H, d, J 6,4 Гц), 0,63 (4H, m), 0,75 (3H, d, J 6,4 Гц), 0,83 (6H,d, J 7,0 Гц), 0,87 (3H, d, J 6,4 Гц), 1,03 (1H, m), 1,10 (1H, m), 1,20 (3H, d, J 6,4 Гц), 1,25 (1H, m), 1,38 (1H,m), 1,50 (1H, m), 1,73 (1H, m), 1,75 (2 Н, m), 1,77 (1H, m), 1,79 (3H, m), 1,85 (3H, s), 1,85 (1H, m), 2,12 (1H,m), 2,16 (1H, m), 2,55 (1H, m), 2,67 (1H, m), 2,70 (3H, s), 3,13 (1H, m), 4,30 (1H, m), 4,40 (1H, m), 4,43 (2 Н,m), 4,59 (1H, d, J 9,5 Гц), 4,71 (1H, m), 4,92 (1H, m), 5,02 (1H, m), 5,46 (1H, m), 6,08 (1H, ушир.s), 6,62 (2 Н,d, J 8,5 Гц), 6,71 (1H, s), 6,97 (2 Н, d, J 8,5 Гц), 7,22 (1H, s), 7,34 (1H, d, J 9,2 Гц), 7,64 (1H, d, J 9,5 Гц), 7,93(1H, d, J 9,2 Гц), 8,06 (1H, d, J 7,6 Гц), 8,39 (1H, d, J 8,5 Гц), 9,06 (1H, ушир.s). Физические данные соединения формулы XIII. МС (FT, 9.4 Т APEX-III): найд.: 961,5039, рассч. для C49H70N8O12+Na: 985,5005 1(2 Н, d, J 8,5 Гц), 7,33 (1H, s), 7,35 (1H, d, J 9,2 Гц), 7,46 (2 Н, t, J 7,3 Гц), 7,53 (1H, t, J 7,3 Гц), 7,66 (1H, d, J 9,5 Гц), 7,88 (2 Н, d, J 7,3 Гц), 7,95 (1H, d, J 9,5 Гц), 8,46 (1H, d, J 8,5 Гц), 8,71 (1H, d, J 7,3 Гц); (ОН-группа тирозина не детектируется). Физические данные соединения формулы XIV. МС (ESI): положит.иониз.: m/z 927,5 (М+Н), отриц.иониз.: m/z 925,5 (М-Н), ММ моноизотопа 926,5,C47H74N8O11 1 Н ЯМР (500 МГц, d6-ДМСО) H: 0,00 (1H, m), 0,48 (3H, t, J 7,5 Гц), 0,70 (3H,d, J 7,0 Гц), 0,73 (3H, t,J 7,0 Гц), 0,76 (3H, d, J 7,3 Гц), 0,79 (3H, t, J 7,3 Гц), 0,83 (6H, d, J 6,4 Гц), 0,89 (1H, m), 0,95 (1H, m), 0,98(3H, d, J 7,0 Гц), 1,04 (3H, d, J 6,1 Гц), 1,09 (1H, m), 1,17 (1H, m), 1,28 (1H, m), 1,31 (1H, m), 1,36 (1H, m),1,38 (1H, m), 1,55 (1H, m), 1,61 (1H, m), 1,68 (1H, m), 1,79 (1H, m), 1,82 (1H, m), 1,95 (2H, m), 2,15 (3H, m),- 28017735 2,25 (1H, m), 2,66 (3H, s), 2,76 (1H, m), 3,14 (1H, m), 3,40 (1H, m), 3,42 (1H, m), 4,33 (1H, m), 4,36 (1H, m),4,45 (2H, m), 4,55 (2H, m), 4,69 (1H, m), 5,06 (1H, m), 6,63 (2H, d, J 8,2 Гц), 6,71 (1H, ушир.s), 7,01 (2H, d, J 8,2 Гц), 7,27 (1H, ушир.s), 7,36 (1H, d, J 9,5 Гц), 8,00 (1H, d, J 9,5 Гц), 8,17 (1H, d, J 4,00 Гц), 8,22 (1H, d, J 7,3 Гц), 8,53 (1H, d, J 9,5 Гц), 9,14 (1H, ушир.s) Физические данные соединения формулы XVII. МС (ESI): положит.иониз.: m/z 985,4 (M+Na), отриц.иониз.: m/z 961,5 (М-Н), ММ моноизотопа 962,5, C45H70N8O13S. 1 Н ЯМР (600 МГц, d6-ДМСО) H: совпадения величины химических сдвигов не наблюдаются (смесь двух диастереомеров, структуру подтверждали при сравнении с другими родственными соединениями,например, соединением (II). Пример 1.2. Получение соединений формул VIII, IX, X. Штамм. Штамм был однозначно отнесен к виду Chondromyces robustus, основываясь на морфологических признаках плодовых тел, а также на части последовательности гена 16S-PHK. C.robustus относят к первой группе биологического риска по классификации DSMZ (DSMZ (2007. Род Chondromyces относится к семейству Polyangiaceae, принадлежащему к порядку Myxococcales класса дельта-протеабактерии. Бактерии порядка Myxococcales, также называемые миксобактериями, являются грамотрицательными бактериями палочковидной формы и обладают двумя выраженными отличиями от большинства других бактерий. Они закрепляются и начинают расти на твердых поверхностях, используя механизм активного перемещения и агрегирования для формирования плодовых тел при наступлении голодания (Kaiser (2003. Штамм Chondromyces robustus по настоящему изобретению был депонирован в коллекции DSMZ под номером 19330. Культивирование. Культивирование штамма проводили в ферментере объемом 100 л по следующей методике. Сначала 20 мл (20%) жидкой культуры штамма Chondromyces robustus высеивали в среде MD1 (6100 мл) (состав описан в статье Bode и др. (2003), табл. 6) в качалочных колбах с отбойниками объемом 500 мл. После инкубации в течение 1 сут при 30C на ротационной качалке при 120 об/мин первую промежуточную культуру высевали по 100 мл (25%) в среде MD1 (6400 мл) в качалочных колбах с отбойниками объемом 2 л. После инкубации в течение 3 сут при 30C на ротационной качалке при 120 об/мин вторую промежуточную культуру высевали в среде MD1 (19500 мл) в качалочных колбах с отбойниками объемом 20 л. Температуру поддерживали при 30C, аэрацию проводили со скоростью 20 л/мин (1,0 об.воздуха/об.культуры/мин) и перемешивали при 80 об/мин. В ферментере поддерживали избыточное давление 0,5 бар. Хотя pH культуральной жидкости не контролировали, pH в культуре незначительно изменялся от pH 6,95 в начале культивирования до pH 6,88 в день 7. После инкубации в течение 7 сут всю вторую промежуточную культуру (18 л, 20%) использовали для высеивания в среду POL1 (90 л) (состав описан в статье Kunze и др. (1995, исходный объем 108 л. Полученную основную культуру загружали в стандартный стальной ферментер объемом 100 л. Температуру поддерживали при 30C, аэрацию проводили со скоростью 30 л/мин (0,3 об.воздуха/об.культуры/ мин) и перемешивали при 50 об/мин и затем через 4 сут со скоростью 80 об/мин. В ферментере поддерживали избыточное давление 0,5 бар. Величину pH в культуре поддерживали в диапазоне 6,8-7,2 при добавлении 3 н. H2SO4 или 1,5 н. NaOH. Через 14 сут титр циклического депсипептида составлял 3 мг/л,полученную культурную жидкость собирали. Экстракция. Всю культуральную жидкость переносили в стальной сосуд объемом 1600 л и декантировали в течение 1 ч. Влажный клеточный осадок (приблизительно 200 г) собирали со дна сосуда фильтрованием через бумажный фильтр. Клеточный осадок экстрагировали 3 раза в течение 30 мин по 10 л этилацетата. Затем остаточную воду отделяли от фазы растворителя. Фазу растворителя промывали водой (5 л) и упаривали, при этом получали сухой экстракт, так называемый "клеточный экстракт". Фильтрат культуральной жидкости экстрагировали этилацетатом (200 л). Смесь выдерживали в течение 2 ч, органическую фазу отделяли, промывали водой (20 л) и упаривали, при этом получали сухой экстракт (12,5 г), так называемый "экстракт из культурального фильтрата". Выделение соединения. Каждый экстракт (из мицелия и культурального фильтрата) растворяли в дихлорметане/метаноле,4:1. Раствор фильтровали и фильтрат пропускали через диатомовую землю (2 г диатомовой земли/1 г экстракта, Isolute, International Sorbent Technology Ltd., Hengoed Mid Glam, Великобритания), затем упаривали. Твердый остаток наносили на колонку с силикагелем (418 см, 100 г силикагеля 40-63) и проводили элюцию в градиенте циклогексана, этилацетата и метанола. Градиент описан в табл.4, скорость потока 28 мл/мин. Собирали фракции объемом 28 мл. Фракции объединяли согласно пикам поглощения в УФ. Фракции, содержащие циклический депсипептид (H-J) по настоящему изобретению, затем очищали обращенно-фазовой хроматографией (Waters Sunfire RP18, 10 мкл, 30150 мм), элюент: 0,01% муравьиная кислота (растворитель A1 и ацетонитрил, содержащий 0,1% муравьиной кислоты (растворитель
МПК / Метки
МПК: A61K 38/15, C07K 11/02
Метки: депсипептиды, циклические
Код ссылки
<a href="https://eas.patents.su/30-17735-ciklicheskie-depsipeptidy.html" rel="bookmark" title="База патентов Евразийского Союза">Циклические депсипептиды</a>
Предыдущий патент: Способ и устройство для заканчивания, добычи и нагнетания
Следующий патент: Соединения 4-пиридинона и их применение для лечения рака
Случайный патент: Способ удаления so2 и co2 из газовых потоков