Лечение инфекционных заболеваний
Формула / Реферат
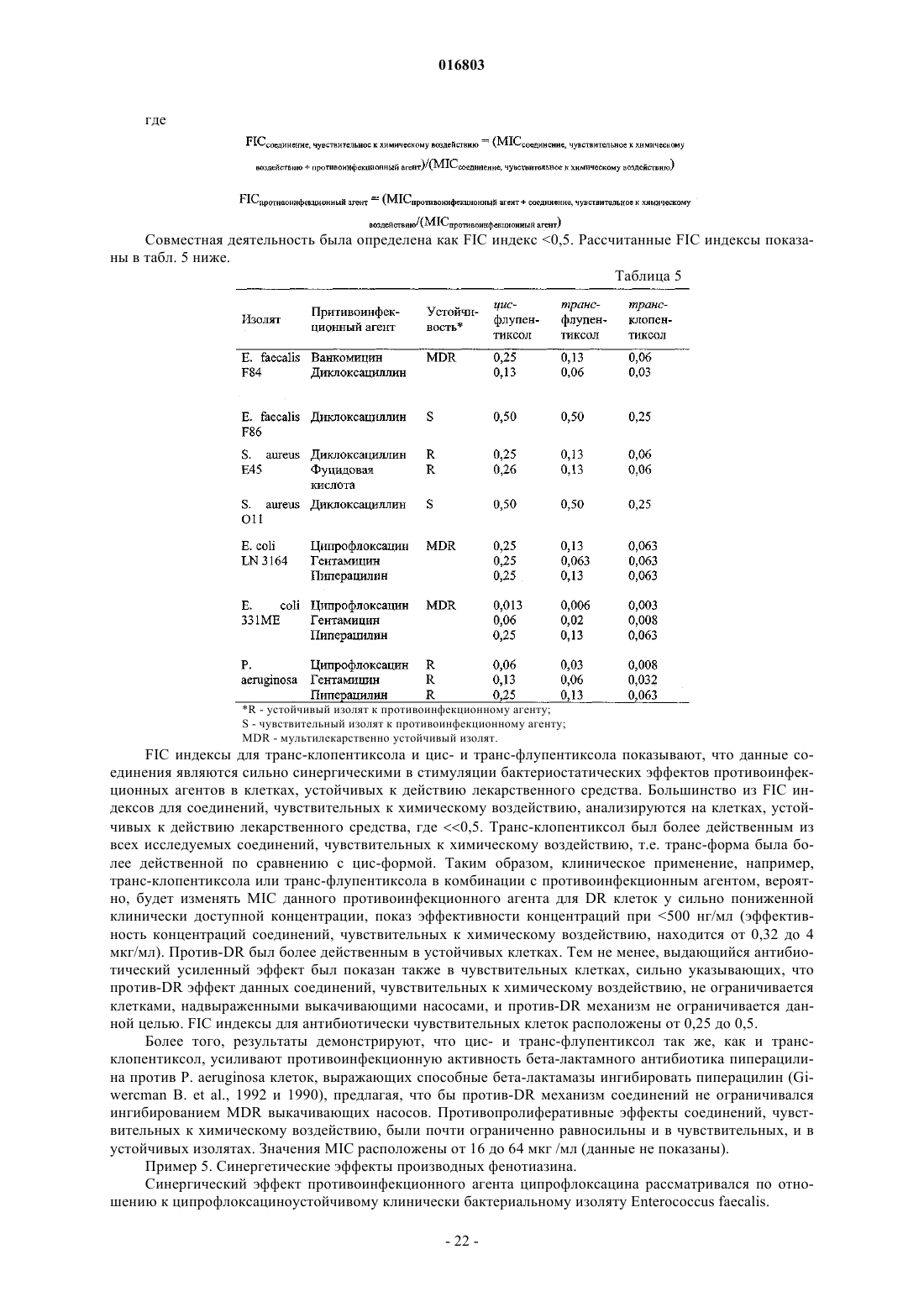
1. Применение клинически релевантного количества соединения, чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови соединения, чувствительного к химическому воздействию, менее чем 8,0 мг/л, общей формулы (I)
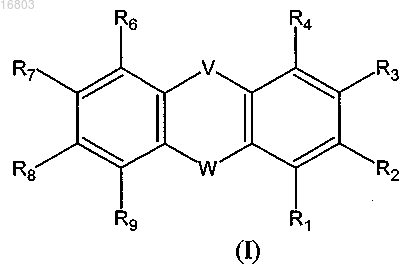
где V выбран из группы, состоящей из S, SO2 и SO;
W представляет собой C=CH-(CHX)m-N(R10)(R11);
m представляет собой целое число от 1 до 5;
каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро, метила, этила, н-пропила, изопропила, метокси, этокси, н-пропокси и изопропокси;
R2 выбран из группы, состоящей из F, Cl, Br, I, CH2Y, CHY2 и CY3, где Y представляет собой атом галогена;
R1, R3, R4, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, C1-6-алкила и С1-6-алкокси;
R10 и R11 вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероарил или гетероциклил;
или его соли для изготовления медикамента для лечения или профилактики инфекционного заболевания в комбинации с противоинфекционным агентом;
где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus, штаммов SA-1199, SA-1199В, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068.
2. Применение по п.1, где R2 выбран из группы, состоящей из F, Cl, CF3 и CCl3.
3. Применение по п.2, где R2 представляет собой Cl или CF3.
4. Применение по любому из предыдущих пунктов, где R1, R3, R4, R6, R7, R8 и R9 представляют собой водород.
5. Применение по любому из предыдущих пунктов, где V представляет собой S или SO.
6. Применение по п.5, где V представляет собой S.
7. Применение по любому из предыдущих пунктов, где m равно 2 или 3.
8. Применение по п.7, где m равно 2.
9. Применение по п.8, где W представляет собой С=СН-(СН2)2-N(R10)(R11), a R10 и R11, как определены в п.1.
10. Применение по любому из предыдущих пунктов, где R10 и R11 вместе с атомом азота, к которому они присоединены, образуют гетероциклил.
11. Применение по п.10, где указанный гетероциклил выбран из группы, состоящей из 2-пирролинила, 3-пирролинила, пирролидинила, 2-имидазолинила, имидазолидинила, 2-пиразолинила, 3-пиразолинила, пиразолидинила, пиперидинила, морфолинила, тиоморфолинила и пиперазинила.
12. Применение по п.11, где указанный гетероциклил представляет собой пиперидинил или пиперазинил.
13. Применение по п.12, где указанный гетероциклил представляет собой пиперазинил.
14. Применение по п.13, где указанный пиперазинил является замещенным в 4-положении.
15. Применение по п.13 или 14, где указанный пиперазинил замещен группой С1-6-алкила.
16. Применение по п.15, где указанный C1-6-алкил выбран из группы, состоящей из -СН3, -СН2ОН, -СН2-СН3 и -СН2-СН2ОН.
17. Применение по п.16, где указанный C1-6-алкил представляет собой -СН3 или -СН2-СН2ОН.
18. Применение по п.17, где указанный С1-6-алкил представляет собой -СН2-СН2ОН.
19. Применение по любому из пп.15-18, где указанный C1-6-алкил находится в 4-положении.
20. Применение по п.13, где указанный пиперазинил является незамещенным.
21. Применение по любому из предыдущих пунктов, где указанная С=СН-(CHX)m-N(R10)(R11) группа находится в транс-конфигурации.
22. Применение по любому из пп.1-19, где указанное соединение выбрано из группы, состоящей из транс-флупентиксола, цис-флупентиксола, транс-клопентиксола и цис-клопентиксола.
23. Применение по п.22, где указанное соединение представляет собой транс-флупентиксол или транс-клопентиксол.
24. Применение по п.23, где указанное соединение представляет собой транс-клопентиксол.
25. Применение по любому из предыдущих пунктов, где указанное устойчивое состояние концентрации в сыворотке крови находится в интервале от 0,01 мкг/л до менее чем 8,0 мг/л.
26. Применение по любому из предыдущих пунктов, где указанный инфекционный агент является мультилекарственно устойчивым.
27. Применение соединения по любому из пп.1-24 для изготовления медикамента для предупреждения развития устойчивости у инфекционного агента, выбранного из группы, состоящей из бактерии, вируса и грибка.
28. Применение по п.27 для предупреждения мультилекарственной устойчивости у инфекционного агента, выбранного из группы, состоящей из бактерии, вируса и грибка.
29. Способ лечения или предупреждения инфекционного заболевания у пациента, причем указанный способ включает введение указанному пациенту клинически релевантного количества соединения, чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови менее чем 8,0 мг/л, общей формулы (I)
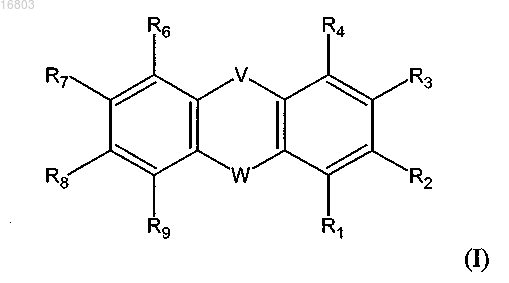
где V выбран из группы, состоящей из S, SO2, SO;
W представляет собой C=CH-(CHX)m-N(R10)(R11);
m представляет собой целое число от 1 до 5;
каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро, изопропила, метокси, этокси, н-пропокси и изопропокси;
R2 является выбранным из группы, состоящей из F, Cl, Br, I, CH2Y, CHY2 и CY3, где Y представляет собой атом галогена;
R1, R3, R4, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, С1-6-алкила и С1-6-алкокси;
R10 и R11 вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероарил или гетероциклил;
или его соли в комбинации с противоинфекционным агентом;
где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus штаммов SA-1199, SA-1199В, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068.
30. Способ по п.29, где указанное соединение представляет собой соединение, как определено в одном из пп.2-24.
31. Способ по п.29 или 30, где указанное соединение вводят для обеспечения указанного устойчивого состояния концентрации в сыворотке крови в интервале от 0,01 мкг/л до менее чем 8,0 мг/л.
32. Способ по любому из пп.29-31, где указанный инфекционный агент является мультилекарственно устойчивым.
33. Набор, включающий первую единицу дозировки, содержащую клинически релевантное количество соединения, чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови менее чем 8,0 мг/л, как определено в одном из пп.1-24, и дополнительно единицу дозировки, включающую противоинфекционный агент, для лечения или профилактики инфекционного заболевания в комбинации с противоинфекционным агентом; где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus штаммов SA-1199, SA-1199B, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068.
34. Набор по п.33 для применения в качестве медикамента.
Текст
(71)(73) Заявитель и патентовладелец: БКГ ФАРМА АПС (DK)(57) Данное изобретение направлено на применение соединений, чувствительных к химическому воздействию, в частности производных тиоксантена и производных фенотиазина, для лечения или профилактики инфекционных заболеваний в комбинации с противоинфекционным агентом, где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка. 016803 Область изобретения Данное изобретение направлено на применение соединений, чувствительных к химическому воздействию, в частности производных тиоксантена и производных фенотиазина, для лечения инфекционных заболеваний в комбинации с противоинфекционным агентом. Предпосылки изобретения Устойчивость к химиотерапии является общей клинической проблемой у пациентов с инфекционными заболеваниями. При лечении инфекций часто наблюдалась невосприимчивость к различным лекарственным средствам, которые имели различные структуры и функции, у целевых для данного лекарственного средства прокариотических или эукариотических клеток микроорганизмов. Данное явление было названо мультилекарственной устойчивостью (MDR). Организмы, от бактерии до человека, обладают трансмембранными переносчиками, которые придают устойчивость к токсичным соединениям. Подчеркивая их биологическое значение, прокариотические и эукариотические белки переноса многих лекарственных средств очень похожи по структуре и функции. К тому же, другие виды важных механизмов устойчивости в комбинации с выкачивающими насосами могут взаимодействовать, таким образом обеспечивая повышение высоких уровней устойчивости. Существует насущная необходимость в лекарственных средствах, которые могут ингибировать (реверсировать) или устранить механизмы устойчивости и улучшить эффективность обычно применяемых противоинфекционных агентов. Степень множественной противомикробной устойчивости бактерии, которая вызывает инфекции, в больницах/блоках интенсивной терапии, повышается, и нахождение микроорганизмов, невосприимчивых к более чем 10 различных антибиотиков, не редкость. Примеры такой устойчивой бактерии включают метицилиноустойчивую и метицилинованкомизиноустойчивую Staphylococcus aureus; ванкомизиноустойчивые энтерококки, такие как Enterococcus faecalis и Enterococcus faecium; пенициллиноустойчивую Streptococcus pneumoniae, цефалоспорин- и хинолиноустойчивые грамотрицательные палочки (колиформы), такие как Е. coli, виды Salmonella, Klebsiella pneumoniae, виды Pseudomonas и виды Enterobacter. Позднее, появились грамотрицательные и грамположительные бациллы, устойчивые ко всем антибиотикам. Скорость появления данного множества, устойчивого к антибиотику, не была отражена той же скоростью развития новых антибиотиков и, таким образом, возможно, что пациенты с серьезными инфекциями в будущем не будут поддаваться лечению доступными в настоящее время противоинфекционными агентами. В нескольких международных докладах были выделены потенциальные проблемы, связанные с появлением противомикробной устойчивости во многих областях медицины, а также были подчеркнуты трудности в отношении пациентов с инфекциями, вызванными данными микроорганизмами. Несмотря на то что большинство сложнейших микроорганизмов находится в больницах, штаммы мультилекарственно устойчивой бактерии, такие как Streptococcus pneumoniae и Mycobacterium tuberculosis, также вызваны серьезными внебольничными инфекциями. Широкая распространенность лекарственно-устойчивой Streptococcus pneumoniae повысилась 60-кратно с 1980 на 51 и на 8% изолированного демонстрационного интермедиата или устойчивости высокого уровня к пенициллину или цефалоспоринам третьего поколения соответственно. Таким образом, пневмококковая пневмония становится более сложной в лечении противоинфекционными агентами первого уровня. Устойчивая бактерия из больниц может попасть в общество через пациентов, выпущенных для продолжительного лечения дома, унесенная с ними, например мультилекарственно устойчивая Staphylococcus aureus и ванкомизиноустойчивые энтерококки. Механизмы устойчивости в бактерии могут быть опосредованы или через хромосомы, или через плазмиды. Изучения появления устойчивости показывают, что устойчивость в бактерии может возникать на этапах, проходящих от низшего уровня до высшего уровня, если плазмида не будет приобретенной, на которой развитая устойчивость уже присутствует. Например, исходный пенициллиноустойчивый пневмококк появляется со слегка пониженной восприимчивостью к антибиотику, но со временем выявляет устойчивость высокого уровня. Пенициллиновая и тетрациклиновая устойчивость из гонококков появляется подобным образом. Также наблюдалась полная устойчивость Е. coli, когда для достижения клинически релевантного уровня устойчивости требовались множественные этапы. Противоинфекционные агенты могут быть деактивизированы тремя основными механизмами: i) разрушение или модификация антибиотика (например, производством бета-лактамаз и аминогликозидоинактивных энзимов), ii) изменение целевого узла и iii) предотвращение доступа к цели (например, изменение проницаемости или истечения). Все три основных устойчивых механизма, по одному или в комбинации, являются клинически важными, ведущими к неудачному лечению. Тем не менее, в последнее время мультилекарственная устойчивость (MDR), связанная с оттоком, оценивается как существенный осложняющий фактор в химиотерапии бактериальных инфекций. Механизмы истечения, которые важны для устойчивости различных противоинфекционных агентов, являются, как правило, обнаруженными в широком ряду бактерии. Термин MDR системы относится к группе переносчиков, которые способны выталкивать широкий ряд совершенно различных субстратов. В то время как данный тип системы сначала был описан в эукариотических клетках в конце 1980-х, при-1 016803 сутствие MDR выкачивающих насосов в бактерии, показывающее устойчивость к нескольким лекарственным средствам, в большей степени было сообщено в литературе. Клеточные линии MDR в основном ассоциируются с пониженным накоплением лекарственного средства в результате ускоренного истечения так же, как и пониженное втекание химиотерапевтических лекарственных средств. Относительно выражения MDR выкачивающих насосов, после введения или из-за появления мутаций в их регулирующих элементах, является основным механизмом в приобретенной бактериальной устойчивости к множеству противоинфекционных агентов. Известны две главные группы систем истечения, специфические экспортеры и транспортеры, приводящие к мультилекарственной устойчивости(MDR). Системы MDR являются способными перемещать противоинфекционные агенты различных классов от бактериальной клетки и иногда играют роль во внутренней устойчивости некоторой бактерии к определенным противоинфекционным агентам. Их гены являются обычно расположенными в бактериальной хромосоме. Механизмы, сводящиеся к MDR, являются часто вызванными трансмембранными ксенобиотическими транспортными молекулами, принадлежащими надсемейству АТР-связывающей кассеты (ABC) транспортеров. MDR истечение главным образом установлено с устойчивостью к соединениям, таким как тетрациклины, фторхинолоны, макролиды, линкозамиды рифампицин, хлорфеникол и аминогликозиды. Напротив, кодирование генов для специфических систем истечения часто связано с подвижными генетическими элементами, которые могут легко обмениваться между бактерией. Специфические системы истечения главным образом устанавливаются с устойчивостью к соединениям, таким как макролиды, линкозамиды и/или стрептограмины, тетрациклины, так же, как и хлорамфеникол в грампозитивной и грамнегативной бактерии. Устойчивость к противовирусным агентам является мировой проблемой по отношению к различным вирусам, таким как ВИЧ у пациентов, больных СПИДом и вирус герпеса. Лекарственная устойчивость относится к хорошо известным мутациям в вирусе, но также может развиться на клеточном уровне человека. Было показано в уровне техники, что AZT (3'-азид-3'-деокситимидин) - устойчивый в ВИЧ-1,соответствует клеточному механизму для AZT-устойчивого. Клеточное истечение AZT необыкновенно повышается, ведущее к устойчивости. Таким образом, клеточный механизм истечения устойчивости является важным фактором, ограничивающим эффективность противовирусных химиотерапевтических агентов, которые применяются в лечении вирусоинфицированных пациентов, таких как ВИЧ инфицированных пациентов, и ингибирование подобных клеточных механизмов истечения будет менять устойчивость на обратное значение и усиливать эффект противовирусного соединения. Прокариотические и эукариотические транспортные белки многих лекарственных средств очень похожи по структуре и функции. Для эукариотических клеток выкачивающие насосы лекарственных средств рассматривались многими авторами как комплементарные системы детоксификации на основе энзимов. В прокариотических клетках несколько видов механизмов устойчивости в комбинации с выкачивающими насосами могут взаимодействовать, обусловлены на высоких уровнях устойчивости и терапевтической неспособности. Ингибирование механизмов устойчивости может восстанавливать активность противоинфекционных агентов, которые являются субстратами для данных механизмов. Недавняя демонстрация и объяснение явления образования устойчивости привели к поиску лекарственных средств, которые могли совершенствовать эффективность противоинфекционных агентов. Двумя потенциальными группами MDR ингибиторов являются фенотиазины и тиоксантены. Фенотиазины и тиоксантены применяются клинически как нейролептические и противорвотные агенты. Фенотиазины и структурно связанные антипсихотические агенты ингибируют несколько клеточных энзимов и блокируют функцию критических клеточных рецепторов. Экстрапирамидные побочные эффекты антипсихотической терапии объясняются связыванием допаминовых рецепторов. В основном данные экстрапирамидные побочные эффекты были доказаны для ограничения дозы в клинических испытаниях с применением фенотиазинов и тиоксантенов в непсихотических областях, таких как противораковое лечение. Фенотиазины и тиоксантены были показаны для ингибирования функции эукариотических MDR выкачивающих насосов и определенных прокариотических MDR выкачивающих насосов. Фенотиазины были показаны, что бы быть среди группы лекарственных средств, известных модифицированно-устойчивому одному или более противобактериальным агентам в определенной бактерии. Хотя механизм, которым фенотиазины и другие лекарственные средства модулируют MDR, еще не ясен,было предположено, что фармакологические свойства могут быть опосредованны хотя бы в части ингибирования выкачивающих насосов. Также, прометазин был признан как эффективный противоплазмидный агент в культурах, содержащих бактериальные виды, такие как Escherichia coli, Yersiniaenterocolitica, Staphylococcus aureus u Agrobacterium tumefaciens. Используемые концентрации, тем не менее, являются в целом выше клинически релевантных концентраций. Факт, что эффективные концентрации являются вышеприведенными клинически релевантными концентрациями, был подчеркнут Каацом и другими (2003). Хотя ингибирование выкачивающих насосов в определенных типах S. aureus выбранными фенотиазинами и двумя геометрическими стереоизомерами-2 016803 цис- и транс-флупентиксола были показаны, авторы все еще делают вывод, что "к сожалению, значенияIC50 ингибиторов для EtBr, акрифлавина и пиронина Y, истечение которых описано выше, используются в клинической практике". Фенотиазины и тиоксантены имеют умеренные, но широкие, противомикробные активности. MICs,в основном вышеописанные клинически релевантные концентрации, такие как минимум эффективных концентраций in vitro в порядке приблизительно от 20 мг/л до нескольких сотен мг/л и релевантные уровни в сыворотке крови приблизительно от 0,3 мкг/л до 0,5 мг/л (от 0,3 нг/мл до 0,5 мкг/мл). Тиоксантены демонстрируют геометрическую стереоизомерию. Cis и транс-формы предварительно были показаны, имеют приблизительную одинаковую умеренную противобактериальную действенность.MICs - в основном вышеописанные, клинически релевантные концентрации. В 1998 Кристиансен и другие предсказали синергический эффект между пенициллином и транс-клопентиксолом в изучении, применяя неустойчивый патогенный изолят мыши пневмонии стрептококка, высокочувствительного к пенициллину (MIC 0,02 мкг/мл пенициллина). Тем не менее, авторы не показали значительные различия значений MIC, применяя только пенициллин и пенициллин в комбинации с транс-клопентиксолом, и изучения концентрации/ответной реакции/времени корреляции не были выполнены, т.е. концентрация лекарственных средств в инфицированных мышах была неизвестна. Также ответная реакция инфекционной бактерии в мышах была не известна. Джонстон и другие показали в клинических испытаниях противопсихотического эффекта цисфлупентиксола в сравнении с транс-флупентиксолом в сравнении с лекарством для успокоения, что пока цис-флупентиксол был действенным нейролептически (особенно для "положительных" симптомов),транс-флупентиксол не имел активности как противопсихотический. С тех пор транс-флупентиксол является далеко меньшим действенным антагонистом допамина, и экстрапирамидные побочные эффекты,ассоциируемые с противопсихотической терапией, приписываются связывающему допаминовому рецептору, недостатки транс-флупентиксол - данные побочные эффекты. Видимый недостаток противопсихотической активности или экстрапирамидных побочных эффектов транс-форм, таких как транс-флупентиксол и транс-клопентиксол, делает их частично заманчивыми для применения как противоустойчивых агентов. Несколько производных фенотиазина и тиоксантена раскрыты в патенте США 6569853. Флупентиксол раскрыт в патенте Великобритании 925538 как применяемый в качестве транквилизатора, атарактик, противорвотное, антигистамин, антиспазматическое средство и депрессант главной нервной системы. Не было упоминаний о любой противоинфекционной или противоустойчивой активности. Несколько производных тиоксантена раскрыты в патенте Великобритании 863699 как транквилизаторы. Не было упоминаний о любой противоинфекционной или противоустойчивой активности. Из вышеописанного ясно, что повышение устойчивости к противоинфекционным агентам, таким как антибиотики, является главным препятствием лечения инфекций. Таким образом, это является крайней необходимостью для лекарственных средств, которые могут ингибировать или охватывать механизмы устойчивости и улучшить эффективность ныне доступных противоинфекционных агентов. Объектом данного изобретения является обеспечение соединений, чувствительных к химическому воздействию, способных сенсибилизировать устойчивость, включая мультилекарственную устойчивость,клеток или микроорганизмов к противоинфекционному агенту введением клинически релевантных количеств таких соединений, чувствительных к химическому воздействию пациенту, которому они нужны. Еще одним, но связанным, объектом изобретения является улучшение эффективности противоинфекционных агентов для лечения инфекционных заболеваний, в частности, когда такие инфекционные заболевания вызваны устойчивостью, включая мультилекарственную устойчивость микроорганизмов. Краткое изложение изобретения Как было понятно из вышеописанного, известный уровень техники до настоящего времени находил тиоксантены и фенотиазины неподходящими для лечения инфекционных заболеваний в комбинации с противоинфекционными агентами, с тех пор как необходимое терапевтическое количество таких соединений, чувствительных к химическому воздействию, будет вызывать тяжелые побочные эффекты. Изобретатель понимает, что предыдущие выводы в основном основывались на учениях, которые проводились на неприродной устойчивости или мультилекарственной устойчивости либо in vitro выбранных микроорганизмов. Таким образом, несмотря на сложившееся мнение в уровне техники, что концентрации тиоксантена и фенотиазина гораздо выше клинически релевантного уровня, необходимого для того, что бы побороть устойчивость или мультилекарственную устойчивость микроорганизмов, изобретатель решил изучить данный вопрос в дополнительных подробностях изучением эффекта таких соединений, чувствительных к химическому воздействию на клинически релевантную устойчивость и мультилекарственно устойчивые изоляты, применяя клинически релевантные количества соединений,чувствительных к химическому воздействию, которые описаны здесь. Неожиданно было обнаружено, что с применением клинически релевантных количеств соединений,чувствительных к химическому воздействию, описанных здесь, в комбинации с противоинфекционными агентами, эффективное подавление устойчивости и мультилекарственной устойчивости клинически ре-3 016803 левантных изолятов было достигнуто. Несмотря на то, чему до этого верили, данное неожиданное открытие открывает возможность эффективно побороть устойчивость и мультилекарственную устойчивость микроорганизмов комбинацией соединений, чувствительных к химическому воздействию, описанных здесь и обычно применяемых противоинфекционных агентов. Таким образом, с первого аспекта данное изобретение имеет отношение к применению соединения общей формулы (I) где V является выбранным из группы, состоящей из S, SO2, SO, О и NH;n представляет собой целое число от 2 до 6;m представляет собой целое число от 1 до 5; каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро,необязательно замещенного С 1-6-алкила и необязательно замещенного С 1-6-алкокси;R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, галогена,гидрокси, амино, нитро, необязательно замещенного C1-6-алкила, необязательно замещенного С 2-6 алкенила, необязательно замещенного С 2-6-алкинила и необязательно замещенного С 1-6-алкокси, необязательно замещенного С 2-6-алкенилокси, карбокси, необязательно замещенного С 1-6-алкоксикарбонила,необязательно замещенного С 1-6-алкилкарбонила, формила, необязательно замещенного С 1-6 алкилсульфониламина, необязательно замещенного арила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилокси, необязательно замещенного арилкарбонила, необязательно замещенного ариламина, арилсульфониламина, необязательно замещенного гетероарила, необязательно замещенного гетероарилоксикарбонила, необязательно замещенного гетероарилокси, необязательно замещенного гетероарилкарбонила, необязательно замещенного гетероариламина, гетероарилсульфониламина, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилоксикарбонила, необязательно замещенного гетероциклилокси, необязательно замещенного гетероциклилкарбонила, необязательно замещенного гетероциклиламина, гетероциклилсульфониламина, моно- и ди(С 1-6 алкил)амина, карбамоила, моно- и ди(С 1-6-алкил)аминокарбонила, амино-С 1-6-алкиламинокарбонила, монои ди(С 1-6-алкил)амино-С 1-6-алкиламинокарбонила,С 1-6-алкилкарбониламина,амино-С 1-6 алкилкарбониламина, моно- и ди(С 1-6-алкил)амино-С 1-6-алкилкарбониламина, амино-С 1-6-алкиламина,моно- и ди(С 1-6-алкил)амино-С 1-6-алкиламина, циано, гуанидино, карбамидо, С 1-6-алканоилокси, С 1-6 алкилсульфонила, С 1-6-алкилсульфинила, С 1-6-алкилсульфонилокси, аминосульфонила, моно- и ди(С 1-6 алкил)аминосульфонила и необязательно замещенного С 1-6-алкилтио; иR10 и R11 независимо выбраны из группы, состоящей из водорода, необязательно замещенного С 1-6 алкила, необязательно замещенного С 2-6-алкенила, необязательно замещенного С 2-6-алкинила, необязательно замещенного С 1-6-алкоксикарбонила, необязательно замещенного С 1-6-алкилкарбонила, необязательно замещенного арила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилкарбонила, необязательно замещенного гетероарила, необязательно замещенного гетероарилоксикарбонила, необязательно замещенного гетероарилкарбонила, аминокарбонила, моно- и ди(С 1-6 алкил)аминокарбонила; или R10 и R11 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный азотосодержащий гетероарил или необязательно замещенный гетероциклил; или метаболиту либо его соли для изготовления медикамента для лечения или профилактики инфекционного заболевания в комбинации с противоинфекционным агентом. Другой аспект данного изобретения будет виден из нижеописанного и приложенной формулы изобретения. Краткое описание чертежей Фиг. 1 показывает ряд столбцов, описывающих эффект соединений, чувствительных к химическому воздействию в отношении устойчивости к лекарственному средству и мультилекарственной устойчивости микроорганизмов (величины из табл. 1-4 ниже). Ось Y представляет коэффициент DR и определяется как коэффициент MIC одного противоинфекционного агента, разделенного MIC для противоинфекционного агента в присутствии соединения, чувствительного к химическому воздействию. Данный коэффициент показывает видимое увеличение в силе противоинфекционного агента, изготовленного индивидуально соединениями, чувствительными к химическому воздействию. Противоинфекционный агент: сопрофлоксацин. Соединения, чувствительные к химическому воздействию: 1) промазин; 2) 1 хлорпромазин; 3) хлорпромазин; 4) 7-гидроксихлорпромазин; 5) 7,8-дигидроксихлорпромазин; 6) тиоме-4 016803 тилпромазин; 7) трифторпромазин; 8) хлорпромазинсульфоксид; 9) десметилхлорпромазин; 10) перфеназин; 11) прохлорперазин; 12) флуфеназин; 13) трифлуперазин; 14) 2-хлор-10-(2 диметиламиноэтил)фенотиазин; 15) прометазин; 16) цис-флупентиксол; 17) транс-флупентиксол; 18) транс-клопентиксол. Фиг. 2 А и 2 В показывают ряд столбцов, описывающих сильный синергический эффект цисфлупентиксола, транс-флупентиксола и транс-клопентиксола на ципрофлоксацин, гентамицин и пиперацилин соответственно (величины из табл. 5 ниже). Проверенными микроорганизмами были Е. coli 331ME (фиг. 2 А) и P. aeruginosa 432b (фиг. 2 В). Ось Y представляет индекс частичной ингибиторной концентрации (FIC). Успешными совместными усилиями для FIC были определены индексы менее чем 0,5. Фиг. 3 показывает усиление эффекта ципрофлоксацина транс-клопентиксолом модели перитонита мыши. Фиг. 4 показывает уровни в сыворотке крови транс-клопентиксола в мышах после однократной дозы 0,3 мг на мышь. Детальное описание изобретения Определения В данном контексте термин "С 1-6-алкил" подразумевает линейную или разветвленную насыщенную углеводородную группу, которая имеет от одного до шести атомов углерода, таких как метил, этил, нпропил, изопропил, н-бутил, изобутил, сек-бутил, трет-бутил, н-пентил, изопентил, неопентил и нгексил. В данном контексте термин "С 3-6-циклоалкил" подразумевает трех -, четырех-, пяти- и шестичленные кольца, включающие только атомы углерода, тогда как термин "гетероциклил" означает трех-, четырех-, пяти- и шестичленные кольца, где атомы углерода вместе с гетероатомами от 1 до 3, составляющих указанное кольцо. Гетероатомы являются независимо выбранными из кислорода, серы и азота. С 3-6 циклоалкильные и гетероциклильные группы могут необязательно содержать одну или более ненасыщенных связей, расположенных, тем не менее, таким образом, что ароматическая -электронная система не возникает. Иллюстративные примеры "С 3-6-циклоалкила" являются углеродными циклами циклопропана, циклобутана, циклопентана, циклопентена, циклопентадина, циклогексана, циклогексена, 1,3 циклогексадиена и 1,4-циклогексадиена. Иллюстративные примеры "гетероциклилов" являются азотсодержащими гетероциклическими соединениями 2-пирролинил, 3-пирролинил, пирролидинил, 2-имидазолинил, имидазолидинил, 2 пиразолинил, 3-пиразолинил, пиразолидинил, пиперидинил, морфолинил, тиоморфолинил и пиперазинил. Соединение с гетероциклическим соединением может быть в положении гетероатома или через атом углерода гетероциклического соединения. В данном контексте термин "С 2-6-алкенил" означает линейную или разветвленную углеводородную группу, которая имеет от двух до шести атомов углерода и содержит одну или более двойных связей. Иллюстративные примеры групп С 2-6-алкенила включают аллил, гомоаллил, винил, кротил, бутенил,пентенил и гексенил. Иллюстративные примеры групп С 2-6-алкенила с более чем одной двойной связью включают бутадиенил, пентадиенил и гексадиенил. Положение двойной связи (связей) может быть в любом положении вдоль углеродной цепи. В данном контексте термин "С 2-6-алкинил" означает линейную или разветвленную углеводородную группу, содержащую от двух до шести атомов углерода, и содержит одну или более тройных связей. Иллюстративные примеры групп С 2-6-алкинила включают ацетилен, пропинил, бутинил, пентинил и гексинил. Положение тройной связи (связей) может быть в любом положении вдоль углеродной цепи. Более чем одна связь может быть ненасыщенной, так что "С 2-6-алкинил" представляет собой диин или ендиин,как известно из данного уровня техники. При использовании термина "C1-6-алкокси", подразумевается С 1-6-алкилокси, такие как метокси,этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, сек-бутокси, трет-бутокси, н-пентокси, изопентокси, неопентокси и н-гексокси. Термин "галоген" включает фтор, хлор, бром и йод. В данном контексте термин "арил" подразумевает карбоциклическое ароматическое кольцо или кольцевую систему. Более того, термин "арил" включает комбинированные кольцевые системы, где хотя бы два арильных кольца или хотя бы один арил и хотя бы один С 3-6-циклоалкил либо хотя бы один арил и хотя бы один гетероциклил участвуют хотя бы в одной химической связи. Иллюстративные примеры"арильных" колец включают нафталенил, фенантренил, антраценил, аценафтиленил, тетралинил, фторенил, инденил, индолил, кумаранил, хроманил, изохроманил и азуленеил. В данном контексте термин "гетероарил" подразумевает арильную группу, где один или более атомов углерода в ароматическом кольце были замещены одним или более гетероатомами, выбранными из группы, состоящей из азота, серы, фосфора и кислорода. Более того, в данном контексте термин "гетероарил" включает комбинированные кольцевые системы, где хотя бы одно арильное кольцо и хотя бы одно гетероарильное кольцо, хотя бы два гетероарила, хотя бы один гетероарил и хотя бы один гетероциклил или хотя бы один гетероарил и хотя бы один С 3-6-циклоалкил участвуют хотя бы в одной химиче-5 016803 ской связи. Иллюстративные примеры гетероарила включают фуранил, тиенил, пирролил, феноксазонил, оксазолил, тиазолил, изотиазолил, имидазолил, пиразолил, изоксазолил, оксадиазолил, фуразанил, триазолил,тиадиазолил, пиперидинил, пиридинил, пиридазинил, пиримидинил, пиразинил, пиразолил и триазинил,изоиндолил, индолинил, бензофуранил, бензотиофенил, бензопиразолил, индазолил, бензимидазолил,бензтиазолил, пуринил, хинолизинил, хинолинил, изохинолинил, циннолинил, фталазинил, хиназолинил,хиноксалинил, нафтиридинил, птеридинилтиенофуранил, карбазоил, акридинил, феназинил, фенотиазинил, феноксазинил и тиантренил. В данном контексте термин "необязательно замещенный" подразумевает, что группа в обсуждаемом вопросе может быть замещена один или несколько раз, например 1-5 раз, предпочтительно 1-3 раза,более предпочтительно 1-2 раза, одной или более группами, выбранными из группы, состоящей из С 1-6 алкила, С 1-6-алкокси, оксо (которая может быть представлена в таутомерической енольной форме), карбоксила, амино, гидрокси (который, когда присутствует в енольной системе, может быть представлен в таутомерической кетоформе), нитро, сульфоно, сульфанила, С 1-6-карбоксила, C1-6-алкоксикарбонила,С 1-6-алкилкарбонила, формила, арила, арилокси, арилоксикарбонила, арилкарбонила, гетероарила, амино,моно- и ди(С 1-6-алкил)амина, карбамоила, моно- и ди(С 1-6-алкил)аминокарбонила, амино-С 1-6 алкиламинокарбонила, моно- и ди(С 1-6-алкил)амино-С 1-6-алкиламинокарбонила, С 1-6-алкилкарбониламина, циано, гуанидино, карбамидо, С 1-6-алканоилокси, С 1-6-алкилсульфонилокси, дигалоген-С 1-6 алкила, тригалоген-С 1-6-алкила и галогена, где заместители арил и гетероарил могут сами быть замещены 1-3 раза С 1-6-алкилом, С 1-6-алкокси, нитро, циано, гидрокси, амино или галогеном. Вообще, вышеописанные заместители могут быть чувствительными к дальнейшим необязательным заместителям. Термин "инфекционный агент" подразумевает патогенные микроорганизмы, такие как бактерии,вирусы, грибок и внутри- или внеклеточные паразиты. В частном варианте изобретения термин "инфекционный агент" не означает агент, выбранный из группы, состоящей из Staphylococcus aureus штаммов АТСС 2593 и штаммов, произведенных из них, SA1199, SA-1199B, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068. В другом варианте изобретения термин "инфекционный агент" не означает Plasmodium falciparum. Аналогично, термин "инфекционное заболевание" употребляется относительно заболевания, вызванного инфекционным агентом. В данном контексте термин "противоинфекционный агент" объединяет соединения, такие как доступные с коммерческой точки зрения антибиотики, которые являются способными убить, ингибировать или иным способом замедлить рост инфекционного агента. Специфические примеры антибиотиков, обычно применяемых для лечения бактериальных и грибковых инфекций, включают, но не ограничиваются, аминогликозиды, такие как амиказин, гентамицин,канамицин, неомицин, нетилмицин, стрептомицин и тобрамицин; кабецефемы, такие как лоракарбеф; карбапенемы, такие как эртапенем, имипенем/циластанин и меропенем; цефалоспорины, такие как цефадроксил, цефазолин, цефалексин, цефаклор, цефамаедол, цефалексин, цефокситин, цефпрозил, цефуроксим, цефиксим, цефдинир, цефдиторен, цефопреазон, цефотаксим, цефподоксим, цефтиазидим, цефтибутен, цефтизоксим, цефтриаксон и цефепим; макролиды, такие как азитромицин, кларитромицин,диритромицин, эритромицин и тролеандомицин; монобактам; пенициллины, такие как амоксициллин,ампициллин, карбенициллин, клоксациллин, диклоксациллин, нафциллин, оксациллин, пенициллин G,пенициллин V, пиперацилин и тикарциллин; полипептиды, такие как бацитрацин, колистин и полимиксин В; хинолины, такие как ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, норфлоксацин, офлоксацин и тровафлоксацин; сульфонамиды, такие как мафенид,сульфацетамид, сульфаметизол, сульфасалазин, сульфисоксазол и триметопримсульфаметоксазол; тетрациклины, такие как демеклоциклин, доксициклин, миноциклин, окситетрациклин и тетрациклин. Специфические примеры противовирусных соединений, обычно применяемых для лечения вирусных инфекций, включают, но не ограничиваются, ацикловир, амантадин, цидофовир фамцикловир, фомивирсен, фоскарнет, ганцикловир, альфа интерферон, оцелтамивир, пенцикловир, рибавирин, римантадин, трифторидин, валацикловир, валганцикловир, видарабин и занамивир. Специфические примеры противогрибковых соединений, обычно применяемых для лечения тяжелых грибковых инфекций, включают, но не ограничиваются, амфотерицин В, каспофунгин, флюконазол,флюцитозин, итраконазол, кетоконазол и вориконазол. В данном контексте инфекционный агент указан для "устойчивости" или "лекарственной устойчивости", если инфекционный агент испытал изменение, которое уменьшает или устраняет эффективность противоинфекционного агента, который обычно применяется для лечения инфекций, вызванных инфекционным агентом. Аналогично, термин "лекарственная устойчивость" означает условие, при котором заболевание, например инфекционное заболевание, не отвечает терапевтическому агенту, такому как противоинфекционному агенту. Лекарственная устойчивость может быть наследственной, это означает,что заболевание никогда не отвечало терапевтическому агенту, или приобретенной, что означает, что заболевание прекращает реагирование на терапевтический агент, которому заболевание некогда отвечало.-6 016803 В данном контексте инфекционный агент указан для "мультилекарственной устойчивости", если инфекционный агент испытал изменение, которое уменьшает или устраняет эффективность двух или более противоинфекционных агентов, которые обычно применяются для лечения инфекций, вызванных инфекционным агентом. Аналогично, "мультилекарственная устойчивость" является типом лекарственной устойчивости, где заболевание, например инфекционное заболевание, является устойчивым к различным лекарственным средствам, таким как различные противоинфекционные агенты. Термин "клинически релевантное количество" подразумевает, что соединение, чувствительное к химическому воздействию, вводится пациенту в количестве, которое, с одной стороны, является способным уменьшать симптомы инфекционного заболевания или лечить инфекционное заболевание, которым пациент заболел, но, с другой стороны, не является токсичным для пациента и не приводит к неожиданным побочным эффектам. Как было определено выше, многие, если не все, соединения, чувствительные к химическому воздействию, описанные здесь, известно, вызывают тяжелые побочные эффекты у пациентов, когда вводятся в очень больших концентрациях, т.е. в количествах, которые не "клинически релевантные". В данном контексте термин "обычно происходящее" при применении в связи с термином "инфекционный агент", т.е. в связи с патогенными микроорганизмами, означает, что инфекционный агент, приводящий к началу инфекционного заболевания, это микроорганизм, который может быть обнаружен в природе, включая существование человека. Понятно, что инфекционные агенты, такие как лабораторные штаммы, полученные генной инженерией, или инфекционные агенты, которые другими способами были изменены и/или манипулированы вмешательством человека, не являются обоснованными для охватывания термина "обычно происходящее". Термин "сыворотка" применяется в своем обычном значении, т.е. как плазма крови без фибриногена и других коагулирующих факторов. Для лечения или предупреждения инфекционного заболевания соединения, чувствительные к химическому воздействию, раскрытые здесь, должны вводиться вместе с или в комбинации с противоинфекционным агентом. Когда в данном контексте используются термины "вместе с" и "в комбинации с",они не должны интерпретироваться в таком узком смысле, что соединение, чувствительное к химическому воздействию, и противоинфекционный агент должны обязательно вводиться одновременно и/или служить частью одной и той же фармацевтической композиции, несмотря на то, что это является одним вариантом данного изобретения. Таким образом, должно быть понятно, что термины "вместе с" и "в комбинации с" означают, что дозировка (включая форму дозировки) и частота введения каждого соединения, т.е. соединения, чувствительного к химическому воздействию, и противоинфекционного агента могут контролироваться индивидуально. Например, одно соединение может вводиться орально три раза в день на протяжении периода лечения, в то время как другое соединение может вводиться внутривенно один раз в день на протяжении периода лечения. Также одно соединение может вводиться каждый день в период лечения, а другое соединение может вводиться только раз или несколько дней в период лечения. Как объяснялось выше, соединение, чувствительное к химическому воздействию, и противоинфекционное соединение могут вводиться одновременно и они могут содержаться в той же фармацевтической композиции. Соответственно термины "вместе с" и "в комбинации с" означают, что соединение, чувствительное к химическому воздействию, вводится пациенту хотя бы один раз на протяжении периода лечения, и что противоинфекционный агент также вводится пациенту хотя бы один раз в период лечения. Здесь термин "устойчивое состояние концентрации в сыворотке крови" (соединения, чувствительного к химическому воздействию) определяется как значения, что повторяются с каждой дозой и представляют состояние равновесия между количеством введенного соединения, чувствительного к химическому воздействию, и количеством, удаленным в данный промежуток времени. В данном контексте термин "лечение" относится к введению лекарственного средства пациенту и включает: i) предупреждение инфекционного заболевания (т.е. вызванного клиническими симптомами не развитого инфекционного заболевания), ii) ингибирование инфекционного заболевания (т.е. задерживание развития клинических симптомов инфекционного заболевания) и iii) облегчение заболевания (т.е. вызванного возвращением клинических симптомов инфекционного заболевания) так же, как их комбинации. Термины "профилактика" или "профилактическое лечение" относятся к лечению пациента, который еще не инфицирован, но который может быть восприимчив или рискует получить инфекцию. Термин "пациент", применяемый здесь, означает живое позвоночное животное, например млекопитающее, такое как человек."Фармацевтически приемлемый "означает подходящий для применения млекопитающим, в частности подходящий для применения человеком. Когда здесь использовался термин "соединение, чувствительное к химическому воздействию", подразумевается агент, который изменяет устойчивость микроорганизмов или клеток для получения противоинфекционного агента. Таким образом, "соединение, чувствительное к химическому воздействию", применяемое здесь, сенсибилизирует устойчивость или устойчивость микроорганизмов или клеток к действию противоинфекционных агентов многих лекарственных средств.-7 016803 Соединения, чувствительные к химическому воздействию Относительно общей формулы (I), приведенной выше, заместители R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, галогена, гидрокси, амино, нитро, необязательно замещенного С 1-6-алкила, необязательно замещенного С 2-6-алкенила, необязательно замещенного С 2-6 алкинила и необязательно замещенного С 1-6-алкокси, необязательно замещенного С 2-6-алкенилокси, карбокси, необязательно замещенного С 1-6-алкоксикарбонила, необязательно замещенного С 1-6 алкилкарбонила, формила, необязательно замещенного С 1-6-алкилсульфониламина, необязательно замещенного арила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилокси,необязательно замещенного арилкарбонила, необязательно замещенного ариламина, арилсульфониламина, необязательно замещенного гетероарила, необязательно замещенного гетероарилоксикарбонила, необязательно замещенного гетероарилокси, необязательно замещенного гетероарилкарбонила, необязательно замещенного гетероариламина, гетероарилсульфониламина, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилоксикарбонила, необязательно замещенного гетероциклилокси, необязательно замещенного гетероциклилкарбонила, необязательно замещенного гетероциклиламина, гетероциклилсульфониламина, моно- и ди(С 1-6-алкил)амина, карбамоила, моно- и ди(С 1-6 алкил)аминокарбонила,амино-С 1-6-алкиламинокарбонила,монои ди(С 1-6-алкил)амино-С 1-6 алкиламинокарбонила, С 1-6-алкилкарбониламина, амино-С 1-6-алкилкарбониламина, моно- и ди(С 1-6 алкил)амино-С 1-6-алкилкарбониламина, амино-С 1-6-алкиламина, моно- и ди(С 1-6-алкил)амино-С 1-6 алкиламина, циано, гуанидино, карбамидо, С 1-6-алканоилокси, С 1-6-алкилсульфонила, С 1-6 алкилсульфинила, С 1-6-алкилсульфонилокси, аминосульфонила, моно- и ди(С 1-6-алкил)аминосульфонила и необязательно замещенного С 1-6-алкилтио. В предпочтительном варианте изобретения R2 заместитель является электронодонорной группой,такой как галоген, нитро или галогензамещенный С 1-6-алкил. Более предпочтительно R2 выбран из группы, состоящей из F, Cl, Br, I, CH2Y, CHY2 и CY3 (где Y представлен атомом галогена), такие как CH2Cl,CH2F, CHCl2, CHF2, CCl3 или CF3, в частности СС 13 или CF3. Более предпочтительно R2 представляет собой Cl или CF3. Заместители R1, R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода,необязательно замещенного С 1-6-алкила и необязательно замещенного C1-6-алкокси. Более предпочтительно все из R1, R3, R4, R5, R6, R7, R8 и R9 представляют собой водород. Соответственно в весьма предпочтительном варианте изобретения R2 представляет собой Cl илиCF3 и каждый из R1, R3, R4, R5, R6, R7, R8 и R9 представляют собой водород. Как упоминалось выше, V выбран из группы, состоящей из S, SO2, SO, О и NH, такие как S или SO. В весьма предпочтительном варианте изобретения V представляет собой S. Также понятно, в случае, когда W представляет собой H-(CHX)m-N(R10)(R11) и V представляет собой S, соединение, чувствительное к химическому воздействию, общей формулы (I) становится фенотиазином общей формулы (II) где n представляет собой целое число от 2 до 6, такое как 2, 3, 4, 5 или 6, и каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро, необязательно замещенного С 1-6-алкила и необязательно замещенного С 1-6-алкокси. R10 и R11, независимо выбранные из группы,состоящей из водорода, необязательно замещенного С 1-6-алкила, необязательно замещенного С 2-6 алкенила, необязательно замещенного С 2-6-алкинила, необязательно замещенного С 1-6-алкоксикарбонила,необязательно замещенного С 1-6-алкилкарбонила, необязательно замещенного арила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилкарбонила, необязательно замещенного гетероарила, необязательно замещенного гетероарилоксикарбонила, необязательно замещенного гетероарилкарбонила, аминокарбонила, моно- и ди(С 1-6-алкил)аминокарбонила; или R10 и R11 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный азотсодержащий гетероарил или необязательно замещенный гетероциклил. В предпочтительном варианте изобретения n представляет собой 2 или 3 и X представляет собой водород или СН 3. Таким образом, в предпочтительном варианте изобретения W представляет собой H(CH2)3-N(R10)(R11) или Н-СН 2-CH(CH3)-N(R10)(R11). В частности, структура, где W представляет собой Н(CH2)3-N(R10)(R11) является предпочтительной.-8 016803 В одном интересующем варианте изобретения R10 и R11, каждый независимо, выбраны из группы,состоящей из водорода и необязательно замещенного С 1-6-алкила. Согласно данному варианту является предпочтительным, что оба R10 и R11 представляют собой необязательно замещенный С 1-6-алкил. Более предпочтительно оба R10 и R11 представляют собой СН 3. В другом интересном варианте изобретения R10 и R11 вместе с атомом азота, к которому они присоединились, образуют необязательно замещенный гетероциклил, такой как необязательно замещенный 2-пирролинил, необязательно замещенный 3-пирролинил, необязательно замещенный пирролидинил,необязательно замещенный 2-имидазолинил, необязательно замещенный имидазолидинил, необязательно замещенный 2-пиразолинил, необязательно замещенный 3-пиразолинил, необязательно замещенный пиразолидинил, необязательно замещенный пиперидинил, необязательно замещенный морфолинил, необязательно замещенный тиоморфолинил или необязательно замещенный пиперазинил. Согласно данному варианту является предпочтительным, что R10 и R11 вместе с атомом азота, к которому они присоединились, образуют необязательно замещенный пиперидинил или необязательно замещенный пиперазинил, в частности необязательно замещенный пиперазинил. Пиперазинильное кольцо может быть незамещенным, но предпочтительно замещенное необязательно замещенной группой С 1-6-алкила, в частности в пара-положении, т.е. необязательно замещенная группа С 1-6-алкила является ковалентно присоединенной ко второму атому азота пиперазильного кольца. В весьма предпочтительном варианте изобретения необязательно замещенный С 1-6-алкил выбран из группы, состоящей из -СН 3, -СН 2 ОН, -СН 2-СН 3 и-СН 2-СН 2 ОН, такие как -СН 3 или -СН 2-СН 2 ОН, в частности -СН 2-СН 2 ОН. Специфические примеры вышеупомянутых фенотиазинов включают промазин, 1-хлорпромазин,хлорпромазин, 7-гидроксихлорпромазин, 7,8-дигидроксихлорпромазин, тиометилпромазин, трифторпромазин, десметилхлорпромазин, перфеназин, прохлорперазин и 2-хлор-10-(2-диметиламиноэтил)фенотиазин. Как также было понятно, в случае, когда W представляет собой С=СН-(СНХ)m-N(R10)(R11) и V представляет собой S, соединение, чувствительное к химическому воздействию, общей формулы (I) становиться тиоксантеном общей формулы (III) Тиоксантен общей формулы (III) дает начало цис- и транс-изомерии. В данном контексте соединения общей формулы (IIIa) находятся в цис-конфигурации, тогда как соединения общей формулы (IIIb) находятся в транс-конфигурации где m представляет собой целое число от 1 до 5, например 1, 2, 3, 4 или 5, и каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро, необязательно замещенного С 1-6-алкила и необязательно замещенного C1-6-алкокси. R10 и R11 независимо выбраны из группы, состоящей из водорода, необязательно замещенного С 1-6-алкила, необязательно замещенного С 2-6-алкенила,необязательно замещенного С 2-6-алкинила, необязательно замещенного С 1-6-алкоксикарбонила, необязательно замещенного С 1-6-алкилкарбонила, необязательно замещенного арила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилкарбонила, необязательно замещенного гетероарила, необязательно замещенного гетероарилоксикарбонила, необязательно замещенного гетероарилкарбонила, аминокарбонила, моно и ди(С 1-6-алкил)аминокарбонила; или R10 и R11 вместе с атомом азота, к которому они присоединились, образуя необязательно замещенный азотсодержащий гетероарил или необязательно замещенный гетероциклил. В основном предпочтительно то, что соединения общей формулы (III) имеют транс-конфигурацию,т.е. структура показана в основной формуле (IIIb). В предпочтительном варианте X представляет собой водород и m равно 2 или 3, в частности 3. Таким образом, в предпочтительном варианте изобретения W имел структуру C=CH-(CH2)2-N(R10)(R11). В одном интересном варианте изобретения R10 и R11, каждый независимо, выбраны из группы, состоящей из водорода и необязательно замещенного С 1-6-алкила. Согласно данному варианту является предпочтительным, что бы оба R10 и R11 представляли собой необязательно замещенный С 1-6-алкил. Более предпочтительно оба R10 и R11 представляли собой СН 3. В другом интересном варианте изобретения R10 и R11 вместе с атомом азота, к которому они присоединились, образуют необязательно замещенный гетероциклил, такой как необязательно замещенный 2-пирролинил, необязательно замещенный 3-пирролинил, необязательно замещенный пирролидинил,необязательно замещенный 2-имидазолинил, необязательно замещенный имидазолидинил, необязательно замещенный 2-пиразолинил, необязательно замещенный 3-пиразолинил, необязательно замещенный пиразолидинил, необязательно замещенный пиперидинил, необязательно замещенный морфолинил, необязательно замещенный тиоморфолинил или необязательно замещенный пиперазинил, согласно данному варианту является предпочтительным, чтобы R10 и R11 вместе с атомом азота, к которому они присоединились, образовали необязательно замещенный пиперидинил или необязательно замещенный пиперазинил, в частности необязательно замещенный пиперазинил. Пиперазинильное кольцо может быть незамещенным, но предпочтительно замещенным необязательно замещенной группой С 1-6-алкила, в частности в пара-положение, т.е. необязательно замещенная группа С 1-6-алкила ковалентно присоединена ко второму атому азота пиперазинильного кольца. В весьма предпочтительном варианте изобретения необязательно замещенный С 1-6-алкил выбран из группы, состоящей из -СН 3, -СН 2 ОН, -СН 2-СН 3 и СН 2 СН 2 ОН, таких как -СН 3 или -СН 2-СН 2 ОН, в частности -СН 2-СН 2 ОН. Специфические примеры вышеописанных фенотиазинов включают транс-флупентиксол, цисфлупентиксол, транс-клопентиксол и цис-клопентиксол. В частности, предпочтительными соединениями, чувствительными к химическому воздействию, для применения согласно изобретению являются- 10016803 транс-флупентиксол и транс-клопентиксол. Более предпочтительно является транс-клопентиксол. Как очевидно из формул, показанных здесь, и определений, соединенных с ними, определенные соединения, чувствительные к химическому воздействию, описанные здесь, являются хиральными. Более того, присутствие определенных ненасыщенных или циклических фрагментов или множества стереогенных атомов, обеспечивает существование диастереомерных форм некоторых соединений, чувствительных к химическому воздействию. Изобретение подразумевает включать все стереоизомеры, включая оптические изомеры и их смеси, так же, как и чистые, частично обогащенные или где релевантные, рацемические формы. В частности, многие из соединений, чувствительные к химическому воздействию,описанному здесь, могут быть в форме Е- или Z-стереоизомеров или смесей таких изомеров. К тому же, должно быть понятно, что соединения, чувствительные к химическому воздействию,описанные здесь, включают возможные его соли, фармацевтически приемлемые соли которых непременно являются особенно релевантными для терапевтических применений. Соли включают кислотноаддитивные соли и основные соли. Примерами кислотно-аддитивных солей являются гидрохлоридные соли, фумараты, оксалаты и т.д. Примерами основных солей являются соли, где (оставшийся) обратный ион выбран из щелочных металлов, таких как натрий и калий, щелочно-земельных металлов, таких как соли кальция, соли калия и ионы аммония (+N(R')4, где R' независимо представляет необязательно замещенный С 1-6-алкил, необязательно замещенный С 2-6-алкенил, необязательно замещенный арил или необязательно замещенный гетероарил). Фармацевтически приемлемыми солями являются, например, те,что описаны у Remington's - The Science and Practice of Pharmacy, 20th Ed. Alfonso R. Gennaro (Ed.), Lippincott, WilliamsWilkins; ISBN: 0683306472, 2000, и в Encyclopedia of Pharmaceutical Technology. Эффект соединений, чувствительных к химическому воздействию, для изменения на обратное лекарственной устойчивости или мультилекарственной устойчивости может исследоваться, как описано здесь, и эффективность соединения, чувствительного к химическому воздействию, в комбинации с выбранными противоинфекционными агентами против выбранных микроорганизмов может быть выражена как значение MIC, коэффициент лекарственной устойчивости и/или FIC индекс. Минимальная ингибиторная концентрация (MIC) определена как низшая ингибиторная концентрация, показывающая невидимое возрастание согласно рекомендации NCCLS. Коэффициент лекарственной устойчивости (DR) определен как коэффициент между значением MIC для одного противоинфекционного агента, отделенного MIC для противоинфекционного агента в присутствии соединения, чувствительного к химическому воздействию. Данный коэффициент представляет повышение в явной силе противоинфекционного агента, вызванной соединением, чувствительным к химическому воздействию, и может быть выражен как Индекс фракционной ингибиторной концентрации (FIC) может быть рассчитан для каждого противоинфекционного агента в отдельности и в комбинации с чувствительным к химическому воздействию согласно следующим формулам: где Синергические эффекты соединений, чувствительные к химическому воздействию, описанные здесь, т.е. их способность к противоположной лекарственной устойчивости или к мультилекарственной устойчивости в микроорганизме, могут оцениваться любым из способов, доступным специалисту в определенной области техники, включая оценивание in vitro, описанное в данных примерах. В предпочтительном варианте изобретения соединение, чувствительное к химическому воздействию, противоинфекционный агент и инфекционный агент (а следовательно, и лечение инфекционного заболевания) выражают индекс FIC не более чем 0,5, когда определен, как описано в данных примерах. Более предпочтительно индекс FIC не более чем 0,4, такой как не более чем 0,3, например не более чем 0,2. Даже более предпочтительно индекс FIC не более чем 0,1, такой как не более чем 0,075, не более чем 0,05 или даже не более чем 0,025. Как описано заранее, соединения, чувствительные к химическому воздействию, описанные здесь,обычно имеют высокое значение MIC. Для соединений, чувствительных к химическому воздействию,которые являются эффективными ингибиторами, это означает, что коэффициент становится близким к нулю, который по очереди означает, что Соответственно в другом предпочтительном варианте изобретения соединение, чувствительное к химическому воздействию, противоинфекционный агент и инфекционный агент (а следовательно, и лечение инфекционного заболевания) коэффициент DR равны по меньшей мере 2, как определено при описании в данных примерах. Более предпочтительно коэффициент DR по меньшей мере 5, такой как по меньшей мере 10, например, такой как по меньшей мере 20. Даже более предпочтительно значение MIC по меньшей мере 30, такой как по меньшей мере 50, по меньшей мере 75 или даже по меньшей мере 100. Терапия, фармацевтические композиции и дозировки Как объяснялось выше, соединения, чувствительные к химическому воздействию, описанные здесь,применимы к лечению инфекционных заболеваний в комбинации с противоинфекционным агентом. Таким образом, соединения, чувствительные к химическому воздействию, описанные здесь, могут применяться для изготовления медикамента для лечения инфекционного заболевания в комбинации с противоинфекционным агентом. К тому же, соединения, чувствительные к химическому воздействию, описанные здесь, применимы к профилактическому лечению инфекционных заболеваний в комбинации с противоинфекционным агентом. Это может быть частично релевантным в ситуациях, где человек имеет высокий риск получить инфекции, такие как иммунодепрессантные пациенты или пациенты, подвергающиеся хирургии. Таким образом, соединения, чувствительные к химическому воздействию, описанные здесь, также могут применяться для изготовления медикамента для профилактического лечения инфекционного заболевания в комбинации с противоинфекционным агентом. Также соединения, чувствительные к химическому воздействию, описанные здесь, могут применяться в комбинации с противоинфекционным агентом для изготовления медикамента для лечения или профилактики инфекционного заболевания. В дальнейшем аспекте данное изобретение направлено на соединения, чувствительные к химическому воздействию, описанные здесь, для применения в качестве медикаментов в комбинации с противоинфекционным агентом, или на соединения, чувствительные к химическому воздействию, описанные здесь, в комбинации с противоинфекционным агентом для применения в качестве медикаментов. В другом, но связанном аспекте соединения, чувствительные к химическому воздействию, описанные здесь, применяются для понижения устойчивости, в частности мультилекарственной устойчивости инфекционного агента. Таким образом, соединения, чувствительные к химическому воздействию, описанные здесь, могут применяться для изготовления медикамента для понижения устойчивости инфекционного агента против противоинфекционного агента. Во все еще другом, но еще связанном аспекте, соединения, чувствительные к химическому воздействию, описанные здесь, применяются для сенсибилизирования восприимчивости, устойчивости или мультилекарственной устойчивости клеток, предпочтительно устойчивости или мультилекарственной устойчивости клеток, более предпочтительно мультилекарственной устойчивости клеток к противоинфекционному агенту. Таким образом, соединения, чувствительные к химическому воздействию, описанные здесь, могут применяться для изготовления медикаментов для сенсибилизирования восприимчивых,устойчивых или мультилекарственно устойчивых клеток, предпочтительно устойчивых или мультилекарственно устойчивых клеток, более предпочтительно мультилекарственно устойчивых клеток к противоинфекционному агенту. Дальнейший аспект данного изобретения относится к способу лечения или предупреждения инфекционного заболевания у пациента, указанный способ включает введение указанному пациенту соединения, чувствительного к химическому воздействию, как описано здесь, в комбинации с противоинфекционным агентом. Дальнейший аспект данного изобретения относится к способу для понижения устойчивости, в частности мультилекарственной устойчивости, инфекционного агента. Даже дальнейший аспект данного изобретения относится к способу для сенсибилизирования восприимчивых, устойчивых или мультилекарственно устойчивых микроорганизмов или клеток, предпочтительно устойчивости или устойчивости микроорганизмов или клеток ко многим лекарственным средствам, более предпочтительно мультилекарственной устойчивости микроорганизмов или клеток к противоинфекционному агенту. Другой аспект данного изобретения относится к способу для предупреждения развития устойчивости или мультилекарственной устойчивости в инфекционном агенте, указанный способ включает введение пациенту соединения, чувствительного к химическому воздействию, как описано здесь. Дальнейший аспект изобретения относится к набору, включающему первую единицу дозировки,- 12016803 содержащую соединение, чувствительное к химическому воздействию, как описано здесь, и, кроме того,единицу дозировки, включающую противомикробный агент. Терапия. Как будет понятно из данного описания, инфекционное заболевание, которое лечится, это то, что обычно лечится при помощи противоинфекционного агента. Инфекционное заболевание, обычно вызванное инфекционным агентом, таким как бактерия, вирус, грибок или внутри- или внеклеточным паразитом. Инфекционный агент является типично в природе встречаемым, т.е. встречаемой в природе бактерии, встречаемого в природе вируса, встречаемого в природе грибка или встречаемого в природе внутри- или внеклеточного паразита. Более подробно, инфекционный агент может быть грамнегативной или грампозитивной бактерией. Специфические примеры включают грамнегативную бактерию рода, выбранную из группы, состоящей из Escherichia, Proteus, Salmonella, Klebsiella, Providencia, Enterobacter, Burkholderia, Pseudomonas, Acinetobacter, Aeromonas, Haemophilus, Yersinia, Neisseria, Erwinia, Rhodopseudomonas и Burkholderia. Специфические примеры грампозитивной бактерии включают бактерию из рода, выбранную из группы,состоящей из Lactobacillus, Azorhizobium, Streptococcus, Pediococcus, Photobacterium, Bacillus, Enterococcus, Staphylococcus, Clostridium, Butyrivibrio, Sphingomonas, Rhodococcus и Streptomyces. В других вариантах инфекционный агент представляет собой, например, род, выбранный из группы, состоящей из Methanobacierium, Sulfolobus, Archaeoglobu, Rhodobacter и Sinorhizobium. Во все еще других вариантах инфекционный агент представляет собой грибок, такой как из родаNeoformans; или из Genus Aspergillus, например A. fumingatus. В дополнительных вариантах инфекционный агент представляет собой вирус, такой как picornaviridae, reoviridae, orthomyxoviridae, paramyxoviridae, adenoviridae, coronaviridae, Human Immunedefiency Virus, hepatitisvira, herpesviridae, oncovira, cytomegalovira, papovaviridae или prions. Еще в других вариантах инфекционный агент представляет собой протозоа, такие как малярия или паразит криптоспоридии. В отдельном варианте изобретения инфекционный агент не штамм Staphylococcus aureus выбран из группы, состоящей из АТСС 2593 и штаммов, производных оттуда, SA-1199, SA-1199B, SA-K1712, SAK1748, SA 8325-4 и SA-K2068. В другом варианте изобретения инфекционный агент не Plasmodium falciparum. Токсичность и терапевтическая эффективность соединений, чувствительных к химическому воздействию, описанные здесь, могут быть определены стандартными фармацевтическими процедурами в клеточных культурах или подопытных животных, например, определением LD50 (смертельная доза для 50% населения) и ED50 (терапевтически эффективная доза у 50% населения). Коэффициент дозы между токсическими и терапевтическими эффектами представляет собой терапевтический индекс и это может быть представлено как коэффициент между LD50 и ED50 (LD50/ED50). Соединения, чувствительные к химическому воздействию, которые проявляют большие терапевтические индексы, являются предпочитаемыми. Данные, полученные из данных оценок клеточной культуры или изучений животного, могут применяться в составлении ряда дозировки для применения у человеческих пациентов. Дозировка таких соединений, чувствительных к химическому воздействию, лежит предпочтительно в пределах ряда переходящих концентраций, что включает ED50 с небольшой токсичностью или без нее. Дозировка может варьировать в пределах данного ряда в зависимости от примененной формы дозировки и пути утилизированного введения. Фармацевтические композиции. Соединения, чувствительные к химическому воздействию, описанные здесь, являются типично сформулированными в фармацевтическую композицию до применения в качестве лекарственной субстанции. Таким образом, в дальнейшем аспекте данное изобретение относится к фармацевтической композиции, включающей соединение, чувствительное к химическому воздействию, как описано здесь, и хотя бы один фармацевтически приемлемый носитель или наполнитель. Фармацевтическая композиция может содержать одно, два или более соединений, чувствительных к химическому воздействию, как описано здесь. В интересном варианте изобретения фармацевтическая композиция включает вдобавок к соединению, чувствительному к химическому воздействию, один или более противоинфекционного агента (агентов). Путь введения соединений, чувствительных к химическому воздействию, описанных здесь, может быть любым подходящим путем, который ведет к концентрации в крови или ткани, соответствующей клинически релевантной концентрации. Таким образом, например, следующие пути введения могут быть подходящими, хотя изобретение этим не ограничено: оральный путь, парентеральный путь, кожный путь, подкожный путь, носовой путь, местный путь, ректальный путь, вагинальный путь и глазной путь. Это должно быть ясно специалисту в данной области техники, что путь введения, частично зависимый от соединения, чувствительного к химическому воздействию, в данном частично выбор пути введения, зависит от физико-химических свойств соединения, чувствительного к химическому воздействию, вместе с- 13016803 возрастом и весом пациента и частично от заболевания или условия и серьезности того же. В общем, несмотря на это, оральный и парентеральный пути являются предпочитаемыми. Соединения, чувствительные к химическому воздействию, описанные здесь, могут содержаться в любом подходящем количестве в фармацевтической композиции и в основном содержатся в количестве приблизительно 0,1-95% веса от полного веса композиции. Композиция может находиться в форме дозировки в виде единичной дозированной лекарственной формы, которая подходит для орального, парентерального, ректального, кожного, подкожного, носового, местного, вагинального и/или глазного пути введения. Таким образом, композиция может быть в форме, например, таблеток, капсул, пилюль, порошков,гранул, суспензий, эмульсий, растворов, гелей, в том числе гидрогелей, паст, мазей, кремов, пластырей,дренчеров, подающих устройств, суппозиториев, клизм, инъекционных средств, имплантантов, спреев,аэрозолей и в другой подходящей форме. Фармацевтические композиции могут быть сформулированы согласно обычной фармацевтической практике, например, в "Remington's Pharmaceutical Sciences" и "Encyclopedia of PharmaceuticalTechnology", под редакцией Swarbrick, J.J.С. Boylan, Marcel Dekker, Inc., New York, 1988. Типично,соединения, чувствительные к химическому воздействию, описанные здесь, формулируются с (хотя бы) фармацевтически приемлемым носителем или наполнителем. Фармацевтически приемлемые носители или наполнители являются известными специалисту в данной области техники. Оральные составы. Фармацевтические композиции для орального применения включают таблетки, которые содержат соединение, чувствительное к химическому воздействию, как описано здесь, необязательно в комбинации с хотя бы одним противоинфекционным агентом, в примеси с не токсическими фармацевтически приемлемыми наполнителями. Данными наполнителями могут быть, например, инертные разбавители или заполнители, такие как сахароза, сорбит, сахар, маннитол, микрокристаллическая целлюлоза, крахмалы, включая картофельный крахмал, карбонат кальция, хлорид натрия, лактозу, фосфат кальция, сульфат кальция или фосфат натрия; гранулированные и распадающиеся агенты, например производные целлюлозы, включая микрокристаллическую целлюлозу, крахмалы, включая картофельный крахмал, кросскармелозы натрия, альгинаты или альгиновую кислоту; связывающие агенты, например сахарозу, глюкозу, сорбит, акацию, альгиновую кислоту, альгинат натрия, желатин, крахмал, пептизированный крахмал,микрокристаллическую целлюлозу, магния алюминия силикат, натрия карбоксиметилцеллюлозу, метилцеллюлозу, гидроксипропилметилцеллюлозу, этилцеллюлозу, поливинилпирролидон или полиэтиленгликоль; и смазывающие агенты, включая глиданты и антиадгезивы, например стеарат магния, стеарат цинка, стеариновую кислоту, кремнеземы, гидрогенизированные растительные масла или тальк. Другие фармацевтически приемлемые наполнители могут быть красителями, агентами, придающими запах, пластификаторами, гигроскопическими веществами, буферными агентами и другими. Таблетки могут быть непокрытыми или они могут быть покрыты известными технологиями, необязательно откладывая расщепление и абсорбцию в желудочно-кишечном тракте и, таким образом, обеспечивая продолжительное действие на протяжении длительного периода. Оболочка может быть приспособленной к высвобождению соединений, чувствительных к химическому воздействию в предопределенной модели, например, в порядке достижения контролированного высвобождения состава (как описано ниже) или это может быть приспособлено не к высвобождению активной лекарственной субстанции до/после прохождения в желудке (кишечная оболочка). Оболочка может быть сахарной оболочкой, пленочной оболочкой (например, размещенной на гидроксипропилметилцеллюлозе, метилцеллюлозе, метилгидроксиэтилцеллюлозе, гидроксипропилцеллюлозе, карбоксиметилцеллюлозе, сополимерах акрилата (Eudragit E), полиэтиленгликолях и/или поливинилпирролидоне) или кишечной оболочкой (например, размещенной на сополимере метакриловой кислоты (Eudragit L и S), ацетатфталате целлюлозы,фталате гидроксипропилметилцеллюлозы, ацетатсуккцинате гидроксипропилметилцеллюлозы, фталате поливинилацетата, шеллаке и/или этилцеллюлозе). Более того, время задержки материала, такого как, например, глицерилмоностеарат или глицерилдистеарат, может быть занято. К тому же, твердые таблетированные композиции, как упоминалось выше, могут быть оснащены оболочкой, приспособленной к защите композиции от нежелательных химических изменений, например химической деградации, до высвобождения соединения, чувствительного к химическому воздействию. Оболочка может быть использована на твердой форме дозировки подобным образом, как это описано в "Aqueous film coating" by James A. Seitz в "Encyclopedia of Pharmaceutical Technology", vol. 1, p. 337-349 под редакцией Swarbrick, J.J.С. Boylan, Marcel Dekker, Inc., New York, 1988. Составы для орального применения также могут быть представлены как жевательные таблетки или как твердые желатиновые капсулы, где активный ингредиент смешан с инертным твердым разбавителем,например картофельным крахмалом, лактозой, микрокристаллической целлюлозой, карбонатом кальция,фосфатом кальция или каолином, или как мягкие желатиновые капсулы, где активный ингредиент смешан с водной или масляной средой, например арахисовым маслом, жидким парафином или оливковым маслом.- 14016803 Порошки и гранулы могут быть приготовлены, применяя ингредиенты, упоминавшиеся выше под таблетками и капсулами определенным образом, применяя, например, смеситель, аппарат кипящего слоя или оборудование распылительной сушки. Контролируемое высвобождение композиций для орального применения может, например, быть создано для высвобождения активной лекарственной субстанции контролированием растворения и/или диффузией активной лекарственной субстанции. Растворение или диффузия контролируемого высвобождения может быть достигнута соответствующей оболочкой таблетки, капсулы, пилюли или гранулированного состава соединения, чувствительного к химическому воздействию, или объединением соединения, чувствительного к химическому воздействию, в данную, например, соответствующую матрицу. Контролируемое высвобождение оболочки может включать одну или несколько покрывающих субстанций, упоминавшихся выше, и/или, например, шеллак, пчелиный воск, гликовоск, касторный воск,карнаубский воск, стеариновый спирт, глицерил моностеарат, глицерил дистеарат, глицерол пальмитостеарат, этилцеллюлозу, акриловые смолы, DL-полимолочную кислоту, ацетатбутират целлюлозы, поливинилхлорид, поливинилацетат, винилпирролидон, полиэтилен, полиметакрилат, метилметакрилат, 2 гидроксиметакрилат, метакрилатные гидрогели, 1,3-бутиленгликоль, этиленгликоль метакрилат и/или полиэтиленгликоли. В контролируемом высвобождении матричного состава соединения, чувствительного к химическому воздействию, матричный материал может включать, например, гидратную метилцеллюлозу, карнаубский воск и стеариловый спирт, карбопол 934, силикон, глицерил тристеарат, метилакрилатметилметакрилат, поливинилхлорид, полиэтилен и/или галогенированный фторуглерод. Контролируемое высвобождение композиции соединений, чувствительных к химическому воздействию, описанных здесь, может также быть в форме плавучей таблетки или капсулы, т.е. таблетки или капсулы, которые при оральном введении плавают на поверхности желудочного содержимого определенный период времени. Плавучий таблетированный состав соединения, чувствительного к химическому воздействию, в данном может быть приготовлен гранулированием смеси соединения, чувствительного к химическому воздействию, наполнителей и 20-75% в/в гидроколлоидов, таких как гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза. Полученные гранулы могут потом быть сжаты в таблетки. При контакте с желудочным соком таблетка может образовывать существенный водонепроницаемый гелевый барьер вокруг своей поверхности. Данный гелевый барьер принимает участие в поддержании плотности менее чем один, таким образом, позволяя таблетке оставаться плавучей в желудочном соке. Текучие/жидкие композиции для орального применения. Порошки, дисперсные порошки или гранулы, подходящие для приготовления водной суспензии добавлением воды, также являются удобными формами дозировки. Состав в качестве суспензии, эмульсии или дисперсии обеспечивает активную субстанцию в примеси с дисперсионным или смоченным агентом,суспендированным агентом и/или одним или более предохранительным средством. Такие составы могут также подходить для применения в активных веществах для, например, слизистой оболочки, такой как желудочно-кишечной, щечной, носовой, ректальной или вагинальной слизистой оболочки, или для введения в целую или поврежденную кожу, или раны. Подходящие дисперсионные или смоченные агенты являются, например, природно встречающимися фосфатидами, например лецитин или соевый лецитин; конденсация продуктов этиленоксида с, например, жирной кислотой, длинной цепью алифатического спирта или частично с эфиром, производного жирных кислот и гексит или ангидрид гексита, например полиоксиэтилен стеарат, полиоксиэтилен сорбит моноолеат, полиоксиэтилен сорбитанмоноолеат и т.д. Подходящие суспендированные агенты являются, например, природно встречающимися камедями,такими как, например, камедь акации, ксантановая камедь или трагакантовая камедь; целлюлозами, такими как, например, натрия карбоксиметилцеллюлоза, микрокристаллическая целлюлоза (например,Avicel RC 591, метилцеллюлоза; альгинаты, такие как, например, альгинат натрия и т.д.). Подходящие примеры предохраняющих средств для применения в составах согласно изобретению являются парабенами, такими как метил или пропил р-гидроксибензоат и бензалконий хлорид. Ректальные и/или вагинальные составы. Для применения в ректальной или вагинальной слизистойоболочке подходящие составы для применения согласно изобретению включают суппозитории (эмульсионного или суспензионного типа),клизмы и ректальные желатиновые капсулы (растворы или суспензии). Предназначенные фармацевтически приемлемые основы суппозиторий включают масло какао, эстерифицированные жирные кислоты,глицеринизированный желатин и различные растворимые в воде или дисперсионные основы подобно полиэтиленгликолям и сложные эфиры жирной кислоты полиоксиэтиленсорбита. Различные аддитивы подобно, например, усиливающим агентам или поверхностно-активным веществам могут быть объединены. Носовые составы. Для применения в носовой слизистой оболочке носовые спреи и аэрозоли для ингаляции являются- 15016803 подходящими композициями для применения согласно изобретению. В типично носовом составе активное вещество находится в форме состава макрочастиц, необязательно распределенного в подходящем носителе. Фармацевтически приемлемые носители, наполнители и необязательно другие фармацевтически приемлемые материалы, находящиеся в композиции, такие как разбавители, усиливающие агенты,агенты, придающие запах, консерванты и т.д., являются выбранными согласно традиционной фармацевтической практики способом, который понятен специалистам в данной области фармацевтики. Носовое введение может быть использовано в тех случаях, где необходим непосредственный эффект, более того, после введения носового состава согласно изобретению активное вещество может быть адсорбировано на носовую слизистую оболочку. Адсорбция на слизистую оболочку предназначена для менее раздражающего эффекта, чем, например, в случае жидкого носителя, например, содержащего проницаемый усиливающий агент или использующий промотер. Местные составы. Для применения на коже составы согласно изобретению могут содержать условно нетоксичные фармацевтически приемлемые носители и наполнители, включая микросферы и липосомы. Составы включают кремы, мази, лосьоны, жидкие мази, гели, гидрогели, растворы, суспензии, палочки, спреи,пасты, пластыри и другие виды транстрансдермальных систем доставки лекарственных средств. Фармацевтически приемлемые наполнители могут включать эмульгирующие агенты, антиоксиданты, буферные агенты, консерванты, гигроскопические вещества, проницаемые усиливающие агенты, хелатные агенты, гелеобразующие агенты, мазевые основы, парфюмерные изделия и агенты, защищающие кожу. Примеры эмульгирующих агентов являются природно встречающимися камедями, например камедь акации или трагакантовая камедь, природно встречающиеся фосфатиды, например соевый лецитин и производные сорбитмоноолеата. Примерами антиоксидантов являются бутилированный гидроксианизол (ВНА), аскорбиновая кислота и ее производные, токоферол и его производные, бутилированный гидроксианизол и цистеин. Примерами консервантов являются парабены, такие как метил или пропил р-гидроксибензоат и бензалконий хлорид. Примерами гигроскопических веществ являются глицерин, пропиленгликоль, сорбит и мочевина. Примерами проницаемых усиливающих агентов являются пропиленгликоль, DMSO (диметилсульфоксид), триэтаноламин, N,Н-диметилацетамид, N,H-диметилформамид, 2-пирролидон и его производные, тетрагидрофурфуриловый спирт и Azone. Примерами хелатных агентов являются EDTA (этилендиаминтетраацетат), лимонная кислота и фосфорная кислота. Примерами других наполнителей являются съедобные масла, подобно миндальному маслу, касторовому маслу, маслу какао, кокосовому маслу, кукурузному маслу, хлопковому маслу, льняному маслу,оливковому маслу, пальмовому маслу, ореховому маслу, маковому маслу, рапсовому маслу, кунжутному маслу, соевому маслу, подсолнечному маслу и маслу чайного дерева; и полимеры, подобно кармелозе,кармелозе натрия, гидроксипропилметилцеллюлозе, гидроксиэтилцеллюлозе, гидроксипропилцеллюлозе, хитозану, пектину, ксантановой камеди, каррагенану, камеди плода рожкового дерева, камеди акации,желатину и альгинатам, примерами мазевых основ являются пчелиный воск, парафин, цетилпальмитат,растительные масла, сорбитные эфиры жирных кислот (Span), полиэтиленгликоли и продукты конденсации между сорбитными эфирами жирных кислот и этиленоксидом, например полиоксиэтилен сорбитанмоноолеат (Tween). Составы, упоминавшиеся выше для местного введения, могут также применяться для ран или они могут подходить для прямого применения или для введения в релевантное отверстие (отверстия) тела,например ректальное, уретральное, вагинальное или оральное отверстия. Состав может просто быть применен прямо на лечащийся участок, такой как, например, слизистая оболочка. Парентеральные составы. Фармацевтическая композиция также может быть введена парентерально при помощи инъекции,вливания или пересадкой (внутривенно, внутримышечно, внутрисуставно, подкожно или подобно) в формы дозировки, составы или, например, подходящие устройства доставки либо имплантанты, содержащие обычные, не токсические фармацевтически приемлемые носители и вспомогательные средства. Состав и приготовление подобных композиций хорошо известны специалистам в данной области техники фармацевтического состава. Специфические формулировки могут быть обнаружены в методическом пособии "Remington's Pharmaceutical Sciences". Композиции для парентерального применения могут находиться в виде единичной дозированной лекарственной формы, например в ампулах или в пузырьках, содержащих несколько дозировок и в которые может быть добавлен подходящий консервант (как описано ниже). Композиция может быть в форме раствора, суспензии, эмульсии, инфузийного устройства или устройства доставки для пересадки или она может находиться как сухой порошок для повторного растворения в воде или другом подходящем носителе до применения. Отдельно от соединений, чувствительных к химическому воздействию, описанному здесь, композиции могут включать подходящие парентерально принятые носители и/или наполнители или активное лекарственное вещество может быть объединено в микросферы, микрокапсулы, наноча- 16016803 стицы, липосомы или подобное для контролируемого высвобождения. Более того, композиция может, к тому же, обычно включать суспендирующие, растворяющие, стабилизирующие, рН-регулирующие агенты и/или диспергирующие агенты. В другом интересном варианте изобретения фармацевтическая композиция представляет собой твердую форму дозировки, такую как таблетка, приготовленную из материала макрочастиц, описанных вWO 03/004001 и WO 2004/062643. Как показано выше, фармацевтические композиции могут содержать соединение, чувствительное к химическому воздействию, в форме стерильной инъекции. Для приготовления подобной композиции соединение, чувствительное к химическому воздействию, растворяют или суспендируют в парентерально принятом жидком носителе. Между принятыми носителями и растворителями, что могут быть применены как вода, вода приспосабливается к подходящему рН добавлением соответственного количества гидрохлоридной кислоты, гидрохлорида натрия или подходящего буфера, 1,3-бутандиола, раствора Рингера и изотонического раствора хлорида натрия. Водный состав может также содержать один или более консервантов, например метил, этил или н-пропил р-гидроксибензоат. В случаях, где соединение, чувствительное к химическому воздействию, является только умеренно или трудно растворимым в воде, для увеличения растворения или растворимости агент может быть добавлен или растворитель может быть отделен от воды, включая 10-60% в/в пропиленгликоля или подобного. Дозировки. Как предварительно подробно обсуждалось, важным аспектом данного изобретения является осуществление соединений, чувствительных к химическому воздействию, описанных здесь, способных изменять устойчивость или мультилекарственную устойчивость, которые вводятся в клинически релевантных количествах, т.е. в количествах, достаточно малых во избежание тяжелых побочных эффектов,обычно ассоциирующихся с соединениями, чувствительными к химическому воздействию, описанных здесь. Будет понятно, что введенная дозировка будет зависеть от введенной формы (как будет описано ниже). Независимо от формы введения, соединение, чувствительное к химическому воздействию, должно быть введено в клинически релевантных количествах, т.е. в количествах, которые, с одной стороны,приводят в действие релевантный терапевтический эффект, но, с другой стороны, не дают тяжелые побочные эффекты. Предпочтительно соединение, чувствительное к химическому воздействию, как описано здесь, вводится в клинически релевантном количестве, приводящем к повышению устойчивого состояния концентрации в сыворотке крови менее чем 8,0 мг/л. Более предпочтительно соединение, чувствительное к химическому воздействию, вводится в клинически релевантном количестве, приводящем к повышению устойчивого состояния концентрации в сыворотке крови менее чем 7,0 мг/л, менее чем 6,0 мг/л, например, менее чем 5,0 мг/л. Даже более предпочтительно соединение, чувствительное к химическому воздействию, вводится в клинически релевантном количестве, приводящем к повышению устойчивого состояния концентрации в сыворотке крови менее чем 4,0 мг/л, менее чем 3,0 мг/л, например, менее чем 2,0 мг/л. Наиболее предпочтительно соединение, чувствительное к химическому воздействию, вводится в клинически релевантном количестве, приводящем к повышению устойчивого состояния концентрации в сыворотке крови менее чем 1,5 мг/л, например приблизительно 1,0 или приблизительно 0,5 мг/л. Другими словами, соединение, чувствительное к химическому воздействию, предпочтительно вводится в клинически релевантном количестве, приводящем к повышению устойчивого состояния концентрации в сыворотке крови в интервале от 0,01 мкг/л до менее чем 8,0 мг/л, в интервале от 0,02 мкг/л до 7,0 мг/л, например в интервале от 0,04 мкг/л до 6,0 мг/л. Более предпочтительно устойчивое состояние концентрации в сыворотке крови соединения, чувствительного к химическому воздействию, находится в интервале от 0,06 мкг/л до 5,0 мг/л, таком как в интервале от 0,08 мкг/л до 4,0 мг/л, например в интервале от 0,1 мкг/л до 3,0 мг/л. Даже более предпочтительно устойчивое состояние концентрации в сыворотке крови соединения, чувствительного к химическому воздействию, находится в интервале от 0,2 мкг/л до 2,0 мг/л, таком как в интервале от 0,4 мкг/л до 2,0 мг/л, например в интервале от 0,5 мкг/л до 2,0 мг/л. Все еще более предпочтительно устойчивое состояние концентрации в сыворотке крови соединения,чувствительного к химическому воздействию, находится в интервале от 0,6 мкг/л до 2,0 мг/л, такие как в интервале от 0,8 мкг/л до 2,0 мг/л, например в интервале от 0,9 мкг/л до 2,0 мг/л. Наиболее предпочтительно устойчивое состояние концентрации в сыворотке крови соединения, чувствительного к химическому воздействию, находится в интервале от 1,0 мкг/л до 2,0 мг/л, таком как в интервале от 1,5 мкг/л до 2,0 мг/л, например в интервале от 1,5 мкг/л до 1,5 мг/л. Соединение, чувствительное к химическому воздействию, предпочтительно вводится в количестве от 0,1 до 3000 мг на 1 день, такие как от 0,5 до 2000 мг на 1 день. Как будет понятно специалисту, актуальное количество, которое вводится inter alia будет зависеть от пути введения, т.е. вводится ли соединение, чувствительное к химическому воздействию, орально, внутривенно, внутримышечно и др. Для композиций, адаптированных для орального введения для системного применения, дозировкой является 0,1 мг-3 г на дозу, таком как 0,1-1000 мг, предпочтительно 1-600 мг, более предпочтительно 2400 мг, введенной 1-10 раз ежедневно, таком как 1-4 раза ежедневно, от 1 дня до 12 месяцев в зависимо- 17016803 сти от инфекционного заболевания, которое лечится. Дозированные формы композиций, которые вводятся ингаляцией, попадают в пределы тех же рядов. Для парентерального введения, в частности внутривенного введения, дозировка от приблизительно 0,1 до приблизительно 2000 мг на 1 день является удобной. Для внутривенного введения дозировка от приблизительно 0,1 до приблизительно 2000 мг на 1 день, которая вводится от 1 дня до 12 месяцев, является удобной. Для подкожного и местного введения дозировкой является 0,1 мг-5 г на дозу, введение 1-10 раз ежедневно от 1 дня до 12 месяцев. Для ректального введения дозировка является нормальной от 0,1 до 2000 мг на дозу, введение от 1 до 10 раз ежедневно от 1 дня до 12 месяцев. Вышеупомянутое устойчивое состояние концентрации в сыворотке крови и дозировки дает повышение желательных клинических эффектов и, в то же время, избегает тяжелых побочных эффектов,обычно ассоциируемых с соединениями, чувствительными к химическому воздействию, описанными здесь. Некоторые из соединений, чувствительные к химическому воздействию, описанные здесь, в частности соединения, чувствительные к химическому воздействию общей формулы (IIIb), могут, тем не менее, вводиться в больших количествах, таким образом давая увеличение устойчивому состоянию концентрации в сыворотке крови выше уровней, определенных выше. Это происходит в результате того, что данные соединения, чувствительные к химическому воздействию, вероятно, не показывают тяжелые побочные эффекты, даже когда вводятся в больших количествах. Изобретение, кроме того, иллюстрируется ниже, не ограничиваясь примерами. Материалы и способы Бактерия. Бактерия была субкультивирована на агаровых пластинках Мюллера-Хинтона и выращивалась в течение ночи при 37 С. Предварительно нагретый бульон Мюллера-Хинтона был привитый колониями из пластинки и выращивался приблизительно 3 ч до достижения фазы логарифмического роста культуры. Фаза логарифмического роста культуры бактерии была разбавлена свежей предварительно нагретой средой и приспособлена для определения Оптической Плотности (OD) при 600 нм с тем, чтобы получить заключительную анализируемую концентрацию 1104 бактерия/ мл среды.DR клетки были приблизительно в 10-100 раз более устойчивыми по сравнению с чувствительными клеточными линиями и поддерживают стабильный DR фенотип, который прорастает в среде, свободной от лекарственного средства. Исключением только был изолят Enterococcus faecalis F84. Данный штамм был культивирован в присутствии васкомицина при 4 мкг/мл с тем, чтобы удерживать значение MIC при 4 мкг/мл. Штаммы были получены из Института Сыворотки "Statens", Дания, Технического университета Дании и Министерства Клинической микробиологии, госпиталя в Санеборге, Дания. Изоляты. Е. coli, LN 3164. Acr AB-TolC MDR мутант, выбранный in vitro, устойчив к тетрациклину, беталактамам, фторхинолинам, хлорамфениколам и аминогликозидам. Е. coli 331 ME. In vivo-выбранные мультилекарственно устойчивые клинические изоляты Е. coli. Штаммы были изолированы от пациента с тяжелым циститом/уросепсисом. Устойчивость к тетрациклину, бета-лактамам, фторхинолинам, хлорамфениколам и аминогликозидам.P. aeruginosa 432b. Клинически мультилекарственно устойчивый изолят. Устойчив к тетрациклину,бета-лактамам, фторхинолинам и аминогликозидам. Производящий бета-лактамазу, изменяется в пенициллиновых связывающих белках и изменяется во внешних мембранных белках.Staphylococcus aureus O11. Клинический изолят устойчив к пеннициллину. Чувствительный к метициллину, тетрациклину, бета-лактамам, фторхинолинам, хлорамфениколу и аминогликозидам.Enterococcus faecalis, F84. Мультилекарственная устойчивость клинического изолята. Устойчив к ампициллину, ципрофлоксацину, гентамицину и понижает устойчивость к ванкомицину. Экспрессирующий цели предшествующей клеточной стенки как главный устойчивый механизм (экспрессия генаEnterococcus faecalis, F86. Чувствительный клинический изолят. Нет развития к устойчивости. Лекарственные средства. Лекарственные средства были растворены в небольших количествах воды или 1% DMSO (заключительная концентрация культуры DMSO менее чем 0,05% DMSO) до разбавления в среде. Растворы были недавно приготовленными для каждого эксперимента. Хлорпромазин, промазин, прометазин, прохлорперазин, трифторперазин, флуфеназин, тиоридазин,хлорпротиксен, транс-клопентиксол, цис- и транс-флупентиксол были получены от Н. Lundbeck (Копенгаген, Дания) и British Pharmacopoeia Commission Laboratory, Мидлсекс, Великобритания. 7 гидроксихлорпромазин, 7,8-дигидроксихлорпромазин, десметилхлорпромазина гидрохлорид, трифторпромазин, хлорпромазинсульфоксид, 1-хлорпромазин, фенотиазин, 2-хлор-10-(2-диметиламиноэтил)-,гидрохлорид были получены из Национального Института Психического Здоровья (США). Тиометил- 18016803 промазин был получен из Института Сыворотки "Statens" (Копенгаген, Дания). Перфеназин был получен от Сигмы (Копенгаген, Дания). Фуцидовая кислота была получена от Leo Pharma AS (Копенгаген, Дания), Азтреонам был получен от Bristol Meyers (Бромма, Швеция). Ванкомизин был получен от AlpharmaAS (Копенгаген, Дания). Ципрофлоксацин бал получен от 1 А Pharma (Копенгаген, Дания) и гентамицин был получен от Schering-Plough Europe (Брюссель, Бельгия). Эффект лекарственных средств на рост микробной клетки и DR. Клеточный рост проверяли, применяя MIC чувствительные тесты, с помощью метода микроразведений в жидкой питательной среде, согласно рекомендациям NCCLS (рекомендации NCCLS, Methods forDilution Antimicrobial Susceptibility Tests for Bacteria That Grow Aerobically; Approved Standard, Sixth Edition, vol. 23; Number 2). Применялись 100% бульон Мюллера-Хинтона и концентрация бактерий 1104/мл. Фаза логарифмического роста бактерии была разбавлена свежей предварительно нагретой средой и приспособлена для определения OD при 600 нм для получения заключительной концентрации 1104 бактерия/мл среды в каждой лунке. Каждое соединение, чувствительное к химическому воздействию, добавлялось в бактериальную культуру в лунки в двухкратных разбавлениях для получения окончательных концентраций, варьирующихся от 8 до 500 мкг/мл. Планшеты инкубировали при 37 С в течение 16 ч. Минимальная ингибиторная концентрация (MIC) определяется как низшая ингибиторная концентрация,показывающая не видимый рост согласно рекомендациям NCCLS. Эффекты соединений, чувствительных к химическому воздействию при DR, изучались микротитрационным анализом, описанным выше, вскрытием клеток до 0-64 мкг/мл противоинфекционным лекарственным средством при отсутствии или присутствии соединения, чувствительного к химическому воздействию. Каждый эксперимент повторялся по три раза. Значения MIC представляли средние значения двух разделенных экспериментов. Фаза логарифмического роста бактерии была разбавлена свежей предварительно нагретой средой и приспособлена для определения OD при 600 нм для получения заключительной концентрации 1104 бактерия/мл среды в каждой лунке. Соединение, чувствительное к химическому воздействию, добавлялось к бактериальной культуре в лунки для получения заключительных концентраций 1/4 соединения, чувствительного к химическим воздействиям значения MIC. Противоинфекционный агент добавлялся к бактериальной культуре в лунки в двоякие разбавители для получения заключительных концентраций, расположенных от 0 до 64 мкг/мл. Планшеты инкубировали при 37 С в течение 16 ч. DR коэффициент был определен как коэффициент между значением MIC только для противоинфекционного агента, разделенного MIC для противоинфекционного агента в присутствии соединения, чувствительного к химическому воздействию. Данный коэффициент представляет повышение видимой силы противоинфекционного агента, вызванной соединением, чувствительным к химическому воздействию, и может быть выражен как Примеры. Пример 1. Эффект модификации промазина. Табл. 1 показывает структуры, значения MIC и коэффициенты DR для ряда производных промазина, имеющих различные R1, R2, R7 и R8 заместители. Используемый противоинфекционный агент являлся ципрофлоксацином и бактериальный штамм являлся Е. coli, LN 3164. Соединения, чувствительные к химическому воздействию (промазин и его производные), имели следующую общую структуру:- 19016803 Полученные результаты собраны в табл. 1 ниже. Таблица 1 Как видно, незамещенное соединение, чувствительное к химическому воздействию (промазин), ингибирует рост клетки и сенсибилизирует мультилекарственную устойчивость Е. coli клеток к ципрофлоксацину 100% (DR коэффициент = 2). Тем не менее, введение атома хлора в положение 1 или 2 повышает действенность против лекарственной устойчивости. В частности, введение атома хлора в положение 2 имеет наибольший эффект и сенсибилизирует лекарственную устойчивость клеток на 220%. Подобно, введение группы CF3 в положение 2 также повышает действенность против роста клетки и лекарственной устойчивости. Окисление атома серы в кольце производит хлорпромазинсульфоксид, имеющий одинаковую активность против лекарственной устойчивости как хлорпромазин. Для исследования влияния ответвления амина соединения, чувствительные к химическому воздействию, имеющие следующие общие структуры, анализировались, как описано выше: Полученные результаты собраны в табл. 2 ниже. Таблица 2 Табл. 2 выше показывает, что фенотиазины, содержащие третичные амины (например, хлорпромазин) и вторичные амины (десметилхлорпромазин), обладают подобной активностью в ингибировании роста клетки (MICs 32 мкг/мл). Тем не менее, фенотиазины, содержащие третичные амины, такие как хлорпромазин, были более действенными антагонистами DR, чем со вторичными аминами, такими как десметилхлорпромазин, вырабатывающие кратное 1,6 повышение в против-DR активности. Другие изменения в типе аминогруппы также приводят к активности против-DR. Например, производные пиперазинила повышают действенность против DR. Таким образом, DR коэффициенты для соединений трифторперазина и флуфеназина были больше, чем трифторпромазина, соединения с идентичной моделью замещенного кольца, но обладающими алифатичным ответвлением. Подобные перфеназин и прохлорперазин были более действующими DR антагонистами, чем хлорпромазин. Данные серии экспериментов также указывают на важность замещения CF3 в положение 2 для противо-DR активности. Например, DR коэффициент для трифторперазина был больше, чем для прохлорперазина. Данные фенотиазины имеют идентичные структуры, кроме прошлой, имеющей CF3 группу вместо атома хлора в положение 2. Подобная взаимосвязь наблюдается при соединении флуфеназина с перфеназином. В заключении паразамещенный метил в пиперазинильном кольце будет более действенным, чем паразамещенный этанол, как наблюдается при соединении DR коэффициентов для прохлорперазина с перфеназином или трифторперазина с флуфеназином. Для определения влияния длины аминосодержащего ответвления соединения, чувствительные к химическому воздействию, имеющие следующие общие структуры, анализировались, как описано выше: Полученные результаты собраны в табл. 3 ниже. Таблица 3 Табл. 3 выше показывает эффект клеточного роста и DR ряда диметиламинофенотиазинов, у которых длина аминосодержащей боковой цепи варьировала. Как можно увидеть, изменение числа атомов углерода в алкильном мостике от двух до трех повышает против-DR эффекты данных соединений, чувствительных к химическому воздействию. Например, хлорпромазин имеет больший DR коэффициент,чем 2-хлор-10-(2-диметиламиноэтил)фенотиазин. Прометазин, который имеет изопропильное ответвление, был более действенным DR ингибитором по сравнению с промазином, у которого прямая триуглеродалкильная цепь. Пример 2. Эффект стереохимии. Для исследования влияния цис- и транс-стереохимии ряды тиоксантенов анализировались, как описано выше. Табл. 4 показывает значения MIC и DR коэффициенты для испытанных тиоксантенов. Таблица 4 Вышеописанные результаты демонстрируют, что стереоизомерические конфигурации необходимы для оптимальной активности против DR. Например, транс-флупентиксол более действенный против-DR агент, чем цис-форма соединения, и транс-клопентиксол был более действенным против-DR агентом. Таким образом, ориентация ответвлений амина в отношении к трициклическим центрам оказывается важным исследованием для против-DR активности. Пример 3. Эффект гидрофобности. Исследования, если различия в против-DR действенности у соединений, чувствительных к химическому воздействию с измененным ответвлением, были также обязаны изменениям в общей гидрофобности, октанол: буфер разделенных коэффициентов для каждого из лекарственных средств в табл. 1-4 был собран в свои DR коэффициенты. Ни одна статистически значимая корреляция не была обнаружена между гидрофобностью и против-DR активностью (р 0,5) (данные не показаны). Пример 4. Синергические эффекты производных тиоксантена. Синергический эффект транс-флупентиксола, цис-флупентиксола и транс-клопентиксола на различные противоинфекционные агенты рассматривался в отношении к чувствительной панели и устойчивым бактериальным изолятам, представляющим разные виды и устойчивые механизмы. Синергический эффект изучался комбинацией изучений методом "шахматной доски" раскрытых клеток до 0-64 мкг/мл противоинфекционного агента в отсутствие или присутствии трансфлупентиксола, цис-флупентиксола или транс-клопентиксола. Каждый эксперимент повторялся по три раза. Значения MIC представляют средние значения двух разделенных экспериментов. Фазу логарифмического роста культуры бактерии разбавили свежей предварительно нагретой средой и приспособили для определения OD при 600 нм для получения заключительной концентрации 1104 бактерия/мл среды в каждой лунке. Каждое соединение, чувствительное к химическому воздействию,добавлялось к бактериальной культуре в лунки в два раза разбавленные растворы для получения заключительных концентраций, расположенных от 0 до 8 мкг/мл. Противоинфекционный агент добавлялся к бактериальной культуре в лунки в два раза разбавленные растворы для получения заключительных концентраций, расположенных от 0 до 64 мкг/мл. Планшеты инкубировали 37 С в течение 16 ч. Лунки были определены визуально для роста. Фракционная Ингибиторная Концентрация (FIC) была рассчитана для каждого противоинфекционного агента отдельно и в комбинации с транс-флупентиксолом, цисфлупентиксолом или транс-клопентиксолом. Следующие формулы применялись для расчета индекса Совместная деятельность была определена как FIC индекс 0,5. Рассчитанные FIC индексы показаны в табл. 5 ниже. Таблица 5FIC индексы для транс-клопентиксола и цис- и транс-флупентиксола показывают, что данные соединения являются сильно синергическими в стимуляции бактериостатических эффектов противоинфекционных агентов в клетках, устойчивых к действию лекарственного средства. Большинство из FIC индексов для соединений, чувствительных к химическому воздействию, анализируются на клетках, устойчивых к действию лекарственного средства, где 0,5. Транс-клопентиксол был более действенным из всех исследуемых соединений, чувствительных к химическому воздействию, т.е. транс-форма была более действенной по сравнению с цис-формой. Таким образом, клиническое применение, например,транс-клопентиксола или транс-флупентиксола в комбинации с противоинфекционным агентом, вероятно, будет изменять MIC данного противоинфекционного агента для DR клеток у сильно пониженной клинически доступной концентрации, показ эффективности концентраций при 500 нг/мл (эффективность концентраций соединений, чувствительных к химическому воздействию, находится от 0,32 до 4 мкг/мл). Против-DR был более действенным в устойчивых клетках. Тем не менее, выдающийся антибиотический усиленный эффект был показан также в чувствительных клетках, сильно указывающих, что против-DR эффект данных соединений, чувствительных к химическому воздействию, не ограничивается клетками, надвыраженными выкачивающими насосами, и против-DR механизм не ограничивается данной целью. FIC индексы для антибиотически чувствительных клеток расположены от 0,25 до 0,5. Более того, результаты демонстрируют, что цис- и транс-флупентиксол так же, как и трансклопентиксол, усиливают противоинфекционную активность бета-лактамного антибиотика пиперацилина против P. aeruginosa клеток, выражающих способные бета-лактамазы ингибировать пиперацилин (Giwercman В. et al., 1992 и 1990), предлагая, что бы против-DR механизм соединений не ограничивался ингибированием MDR выкачивающих насосов. Противопролиферативные эффекты соединений, чувствительных к химическому воздействию, были почти ограниченно равносильны и в чувствительных, и в устойчивых изолятах. Значения MIC расположены от 16 до 64 мкг /мл (данные не показаны). Пример 5. Синергетические эффекты производных фенотиазина. Синергический эффект противоинфекционного агента ципрофлоксацина рассматривался по отношению к ципрофлоксациноустойчивому клинически бактериальному изоляту Enterococcus faecalis.- 22016803 Синергический эффект изучался комбинацией изучений методом "шахматной доски" раскрытых клеток 0-8 мкг/мл противоинфекционного агента в отсутствие или присутствии хлорпромазина, промазина или перфеназина. Каждый эксперимент повторялся по два раза. Значения MIC представляют собой средние значения двух разделенных экспериментов. Фазу логарифмического роста культуры бактерии разбавили свежей предварительно нагретой средой и приспособили для определения OD при 600 нм для получения заключительной концентрации 1104-5 бактерия/мл среды в каждой лунке. Каждое соединение, чувствительное к химическому воздействию, добавлялось к бактериальной культуре в лунки в два раза разбавленные растворы для получения заключительных концентраций, расположенных от 0 до 16 мкг/мл. Противоинфекционный агент добавлялся к бактериальной культуре в лунки в два раза разбавленные растворы для получения заключительных концентраций, расположенных от 0 до 16 мкг/мл. Планшеты инкубировали 37 С в течение 16 ч. Лунки были определены визуально для роста. Фракционная Ингибиторная Концентрация (FIC) была рассчитана для каждого противоинфекционного агента отдельно и в комбинации с хлорпромазином, промазином или перфеназином. Следующие формулы применялись для расчета индекса FIC: где Совместная деятельность была определена как FIC индекс 0,5. Рассчитанные FIC индексы показаны в табл. 6 ниже.FIC индексы для хлорпромазина, промазина или перфеназина показывают, что данные соединения являются сильно синергическими в стимуляции бактериостатических эффектов противоинфекционных агентов в клетках, устойчивых к действию лекарственного средства. Все FIC индексы для соединений,чувствительных к химическому воздействию, анализируются на клетках, устойчивых к действию лекарственного средства, где 0,5. Хлорпромазин, промазин или перфеназин были одинаковы относительно способности усиливать эффект ципрофлоксацина. Низшие эффективные концентрации улучшенных соединений были между 1 и 2 мкг/мл. Таким образом, клиническое применение, например, хлорпромазина,промазина или перфеназина в комбинации с противоинфекционным агентом, вероятно, будет изменятьMIC данного противоинфекционного агента для DR клеток у сильно пониженной клинически доступной концентрации, показ эффективности концентраций при 2 мкг/мл. Таблица 6 Пример 6. Развитие нечувствительности к соединениям, чувствительным к химическому воздействию. Одно возможное ограничение к комбинации противоинфекционного агента с ингибиторами устойчивости механизма (механизмов) является возможностью микроорганизмов развивать мутации, которые отдают нечувствительность ингибитору. Подобная ситуация наблюдалась для, например, бактерии, вируса, грибка и дрожжей. Эффект ингибиторов на скорость появления in vitro выбранного пошагово ципрофлоксацина, устойчивого к клиническому изоляту S. aureus O11 исследовался. Самопроизвольные мутанты получались 24 ч после выращивания S. aureus клеток на чашках Петри с LB-агаром, содержащих ципрофлоксацин при концентрации 1 мкг/мл (дважды MIC) в отсутствие или присутствии транс-клопентиксола при 1 мкг/мл. Частота отбора мутанта исследовалась 310-8 соединением количества колоний, которые растут на пластинках, содержащих противоинфекционный агент с количеством колоний, полученных при выращивании подходящих разбавителей в отсутствие противоинфекционных агентов. Вероятно, самым важным аспектом, когда оценка применения ингибиторов в клинике, является эффект данных ингибиторов на появление устойчивых мутантов. Важно, и как показано в табл. 7, проверенный ингибитор понижает частоту самопроизвольного появления устойчивости ципрофлоксацина 100 кратно или более. Данный внезапный эффект не мог быть приписан токсическому эффекту ингибитора с тех пор, как та же концентрация ингибитора, который был по меньшей мере 10-кратный, менее чем егоMIC для S. aureus, не задетый ни способностью образования колонии, ни размером колонии S. aureus клеток, выращенных при отсутствии ципрофлоксацина. В заключение, транс-клопентиксол, ингибиро- 23016803 ванный появлением устойчивости ципрофлоксацина в S. aureus. Таблица 7 Частота появления in vitro-выбранных вариантов S. aureus, устойчивых к 1 мкг ципрофлоксацина на 1 мл (дважды MIC для S. aureus штамма) или в отсутствие либо в присутствии ингибиторов. Пример 7. Усиленный эффект транс-клопентиксола в образце перитонита мыши. Бактерия. Применялся клинический изолят Enterococcus faecalis BG-029 из человеческой мочи. Данный штамм был устойчивым к ципрофлоксацину; MIC, 4 мкг/мл. MIC транс-клопентиксола был 6 мкг/мл.MICs исследовались микрорастворяющим исследованием согласно рекомендациям NCCLS. Животные. Для моделирования пневмонического перитонита мыши использовали женские особи мышей линииNMRI (возраст приблизительно от 6 до 8 недель; вес 302 г) (как описано ниже). Антибиотики. Ципрофлоксацин был получен от Bayer A/S, Lyngby, Дания, как раствор для вливания; 2 мг/мл транс-клопентиксол был получен как порошок, контрольное вещество от British Pharmacopoeia Commission Laboratory, Middlesex, United Kingdom. Фармакокинетические изучения транс-клопентиксола с мышами. Фармакокинетические изучения проводились с мышами линии NMRI. Концентрации в молочной сыворотке исследовались после введения одной дозы 0,3 мг на мышь. Лекарственное средство было введено подкожной инъекцией в область шеи в объеме 0,2 мл на дозу. За 1, 2, 4, 6 и 24 ч после инъекции образцы крови были получены от мышей в трех группах. После собирания кровь центрифугировали и сыворотку хранили при -80 С до анализирования жидкостной хроматографией высокого давления. Образец перитонита мыши. Бактериальные суспензии были приготовлены из свежих ночных культур (полученных из замороженных породных культур) на 5% крови агаровых пластин, как описано выше. Прививочный материал для образца перитонита мыши был приготовлен непосредственно до применения и был задан при 540 нм дающей плотности приблизительно 107 КОЕ/мл. Размер прививочного материала исследовался жизнеспособностью, считая на 5% крови агаровой пластины. Нейтропения внесена подготовкой мышей циклофосфамидом (6 мг ежедневно на протяжении трех дней). Мыши были впрыснуты интраперитонеально 0,5 мл суспензии энтерококка, получаемой в бактериемии в пределах 1 ч прививка. Антибиотическая терапия была включена после 1 ч после прививки. Ципрофлоксацин и транс-клопентиксол были введены подкожно в область шеи в объеме 0,1 мл на дозу. Пять мышей были в каждой группе, которая лечилась. Привитый необработанный контроль, мыши были включены во все испытания (способ связи: Erlandsdottir et al.; Antimicrob. Agents Chemother. 2001 Apr.; 45(4): 1078-85) Таблица 8 Лечение режимов инфекционных мышей Эффекты различного лечения образов жизни исследовались в течение 6 ч лечения определением бактериальных расчетов в жидкости брюшной полости. После уничтожения мышей брюшинные промывания были выполнены впрыскиванием 2 мл стерильного солевого раствора внутриперитонеально, потом массированием живота и потом открытием брюшины для сбора жидкости. Жидкости брюшной полости были непосредственно разбавлены 10 кратно в солевом растворе, откуда 20 мкл было подано в 5% крови агаровых пластинок в капельках с последующим покрытием колоний после выращивания в течение ночи при 35 С. Низшие обнаруженные- 24016803 уровни для бактериальных расчетов в крови и жидкости брюшной полости были 50 и 250 КОЕ/мл соответственно. Бактерицидные эффективности лечения жизненных образов в образцах мыши были подсчитаны вычитанием результатов для каждой лечимой мыши от средних результатов контроля мышей в конце терапии (6 ч). Р значение 0,05 было значительно обоснованным. Все статистические сравнения были двусторонними. Результаты. Сильная усиливающаяся активность транс-клопентиксола в брюшине мыши. Бактерицидная активность ципрофлоксацина и транс-клопентиксола, одних или в комбинации, в брюшине мыши показана на фиг. 3. Как видно, один ципрофлоксацин в субтерапевтической дозе не проявляет эффекта на инъекцию и устойчивая бактерия не уничтожена из брюшины мыши. Но когда мышей обрабатывали ципрофлоксацином и транс-клопентиксолом в комбинации, бактерия была уничтожена (р 0,05). Один транс-клопентиксол (ТС) не поражал бактерию согласно данной субтерапевтической дозе(значения сыворотки ТС в мышах являлись менее чем 300 нг/мл; это значительно ниже значения MIC 6 мкг ТС/мл, как видно из фиг. 4). Пример 8. Синергические эффекты производных тиоксантена на грибки. Синергический эффект транс-клопентиксола изучался комбинацией изучений методом "шахматной доски" раскрытых клеток 0-256 мкг/мл противоинфекционного агента в отсутствие или присутствии транс-клопентиксола (0-8 мкг/мл в двукратных разбавителях). Каждый эксперимент повторялся по три раза. Значения MIC представляют средние значения двух разделенных экспериментов. Грибковый штамм. Клинический изолят Candida albicans, устойчивый к флуконазолу, выделенный у пациента с кандидемией. Противогрибковый агент: флуконазол (Pfizer, Ballerup, Дания). Изоляты были субкультивированы в течение 24 ч на глюкозном агаре Сабуро до испытания на чувствительность. Оба микроразбавляемых испытания были выполнены согласно NCCLS документу М 27-А (Ref: National Commitee for Clinical Laboratory Standards. (1997). Reference Method for Broth Dilution AntifungalSusceptibility Testing of Yeasts: Approved Standard M27-A. NCCLS, Wayne, PA) Микротитрационные планшеты спектрофотометрически показывали при 530 нм, после смешивания лунок пипетированием ресуспендировали дрожжевые осадки. MIC определили как низшее лекарственное разбавление, получающееся в 80% роста ингибирования для флуконазола. Следующие пробные точки перелома были применены: восприимчивость флуконазола (S), MIC8 мкг/мл; восприимчивость зависимости от дозы (SDD), 8 мкг/млMIC64 мкг/мл; устойчивость (R), MIC64 мкг/мл. Фракциональная ингибиторная концентрация (FIC) была рассчитана только для противоинфекционного агента и в комбинации с транс-клопентиксолом. Следующие формулы применялись для расчета Совместная деятельность была определена как индекс FIC 0,5. Рассчитанный индекс FIC показан в табл. 9 ниже. Таблица 9 Индекс FIC для транс-клопентиксола показывает, что данное соединение является сильно синергическим в стимуляции противогрибкового эффекта противогрибковых агентов в лекарственноустойчивых клетках. Как видно, индекс FIC для соединений, чувствительных к химическому воздействию, анализируется на лекарственно-устойчивых клетках, является 0,5. Таким образом, клиническое применение, например, транс-клопентиксола в комбинации с противогрибковым агентом будет, вероятно, изменять MIC данного противогрибкового агента для DR клеток, хорошо пониженных клинически доступных концентрации, показывая эффективность концентрации при 3 мкг/мл.- 25016803 Пример 9. Усиленные эффекты производных тиоксантена на противовирусные соединения. Усиленный эффект транс-клопентиксола на противовирусные агенты изучался комбинацией изучений методом "шахматной доски" раскрытых ВИЧ инфицированных клеток до 0-3 мкМ противоинфекционного агента в отсутствие или присутствии транс-клопентиксола в концентрациях от 0 до 6 мкМ. Каждый эксперимент повторялся по три раза. Значения MIC представляют средние значения двух разделенных экспериментов. Способы. Вирусы и клетки. ВИЧ-1 штамм HTLV-IIIB распространен в Н 9 клетках при 37 С, 5% СО 2, применяя число оборотов в минуту 1640 с 10% термоинактивированной эмбриональной сыворотки теленка (FCS) и антибиотиков(среда для выращивания). Культурный супернатант отфильтровали (0,45 нм), отобрали аликвоту и хранили при -80 С до применения. ВИЧ-1 штамм был получен НИЗ исследования СПИДа и Связанной Программы. Соединения. Противовирусное лекарственное средство: AZT, (3'-азид-3'-деокситимидин), Glaxo Wellcome. Усиливающее соединение: транс-клопентиксол был получен как порошок относительно вещества из British Pharmacopoeia Commission Laboratory, Middlesex, United Kingdom. Ингибирование ВИЧ-1 репликации. Соединения рассматривались для возможной противовирусной активности против штамма IIIB ВИЧ-1, применяя МТ 4 клетки как целевые клетки. МТ 4 клетки были выращены с вирусом (0,005 MOI) и средой для выращивания, содержащей проверку разбавления соединения (соединений) для шести дней в соответствии с вирусинфицированными и неинфицированными контрольными культурами без добавления соединения. Выражение ВИЧ в культурах было косвенно квантифицированно, применяя МТТанализ, как предварительно описано. Соединения, посредничая менее чем на 30% понижения ВИЧ выражения, были обоснованы без биологической активности. Соединения испытывались соответственно для цитотоксического эффекта в неинфицированных МТ 4 культурах, содержащих проверку разбавления соединения, как описано выше. Культуры для проверки противовирусной активности и цитотоксического эффекта были подготовлены в тройном экземпляре, 200 мл на культуру в микротитрационных планшетах. 30% ингибирования роста клетки относительно контроля культур было значительно обоснованно. 50% ингибиторной концентрации было определено интерполяцией от частей процента ингибирования в сравнении с концентрацией соединения. ЕС 50 определена как эффективная концентрация, которая ингибирует 50% вирусной продукции,50% вирусной инфицированности или 50% вирусно-индуцированного цитопатического эффекта. СС 50 определена как ингибиторная концентрация, которая понижает клеточный рост или жизнеспособность инфекционных клеток на 50%. Результаты Как видно в табл. 10, комбинация транс-клопентиксола и AZT результируется в 10-кратном увеличении противовирусного эффекта AZT и таким образом может быть обоснованной для ингибирования устойчивости вирусных штаммов. Один транс-клопентиксол не имеет противовирусного или цитотического эффекта при используемой концентрации. Таблица 10 Усиливающий эффект транс-клопентиксола (ТС) на противовирусное соединение ЕС 50 определена как эффективная концентрация, которая ингибирует 50% вирусной продукции,50% вирусной инфицированности или 50% вирусно-индуцированного цитопатического эффекта. СС 50 определена как ингибиторная концентрация, которая понижает клеточный рост или жизнеспособность инфекционных клеток на 50%. Вирусное испытание относительным способом: Petersen L., Jorgensen P.T., Nielsen С., Hansen T.H.,Nielsen J., Pedersen E.B. Synthesis and Evaluation of Double-Prodrugs against HIV. Conjugation of D4T with 6-Benzyl-l-(ethoxymethyl)-5-isopropiluracil (MKC-442, Emivirine) Type Reverse Transcriptase Inhibitors viathe SATE Prodrug Approach. J. Med. Chem. 2005, 48, 1211-1220. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение клинически релевантного количества соединения, чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови соединения, чувствительного к химическому воздействию, менее чем 8,0 мг/л, общей формулы (I)m представляет собой целое число от 1 до 5; каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро,метила, этила, н-пропила, изопропила, метокси, этокси, н-пропокси и изопропокси;R2 выбран из группы, состоящей из F, Cl, Br, I, CH2Y, CHY2 и CY3, где Y представляет собой атом галогена;R1, R3, R4, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, C1-6-алкила и С 1-6 алкокси;R10 и R11 вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероарил или гетероциклил; или его соли для изготовления медикамента для лечения или профилактики инфекционного заболевания в комбинации с противоинфекционным агентом; где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus, штаммов SA-1199, SA-1199 В, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068. 2. Применение по п.1, где R2 выбран из группы, состоящей из F, Cl, CF3 и CCl3. 3. Применение по п.2, где R2 представляет собой Cl или CF3. 4. Применение по любому из предыдущих пунктов, где R1, R3, R4, R6, R7, R8 и R9 представляют собой водород. 5. Применение по любому из предыдущих пунктов, где V представляет собой S или SO. 6. Применение по п.5, где V представляет собой S. 7. Применение по любому из предыдущих пунктов, где m равно 2 или 3. 8. Применение по п.7, где m равно 2. 9. Применение по п.8, где W представляет собой С=СН-(СН 2)2-N(R10)(R11), a R10 и R11, как определены в п.1. 10. Применение по любому из предыдущих пунктов, где R10 и R11 вместе с атомом азота, к которому они присоединены, образуют гетероциклил. 11. Применение по п.10, где указанный гетероциклил выбран из группы, состоящей из 2 пирролинила, 3-пирролинила, пирролидинила, 2-имидазолинила, имидазолидинила, 2-пиразолинила, 3 пиразолинила, пиразолидинила, пиперидинила, морфолинила, тиоморфолинила и пиперазинила. 12. Применение по п.11, где указанный гетероциклил представляет собой пиперидинил или пиперазинил. 13. Применение по п.12, где указанный гетероциклил представляет собой пиперазинил. 14. Применение по п.13, где указанный пиперазинил является замещенным в 4-положении. 15. Применение по п.13 или 14, где указанный пиперазинил замещен группой С 1-6-алкила. 16. Применение по п.15, где указанный C1-6-алкил выбран из группы, состоящей из -СН 3, -СН 2 ОН, СН 2-СН 3 и -СН 2-СН 2 ОН. 17. Применение по п.16, где указанный C1-6-алкил представляет собой -СН 3 или -СН 2-СН 2 ОН. 18. Применение по п.17, где указанный С 1-6-алкил представляет собой -СН 2-СН 2 ОН. 19. Применение по любому из пп.15-18, где указанный C1-6-алкил находится в 4-положении. 20. Применение по п.13, где указанный пиперазинил является незамещенным. 21. Применение по любому из предыдущих пунктов, где указанная С=СН-(CHX)m-N(R10)(R11) группа находится в транс-конфигурации. 22. Применение по любому из пп.1-19, где указанное соединение выбрано из группы, состоящей из транс-флупентиксола, цис-флупентиксола, транс-клопентиксола и цис-клопентиксола. 23. Применение по п.22, где указанное соединение представляет собой транс-флупентиксол или транс-клопентиксол. 24. Применение по п.23, где указанное соединение представляет собой транс-клопентиксол. 25. Применение по любому из предыдущих пунктов, где указанное устойчивое состояние концентрации в сыворотке крови находится в интервале от 0,01 мкг/л до менее чем 8,0 мг/л. 26. Применение по любому из предыдущих пунктов, где указанный инфекционный агент является- 27016803 мультилекарственно устойчивым. 27. Применение соединения по любому из пп.1-24 для изготовления медикамента для предупреждения развития устойчивости у инфекционного агента, выбранного из группы, состоящей из бактерии,вируса и грибка. 28. Применение по п.27 для предупреждения мультилекарственной устойчивости у инфекционного агента, выбранного из группы, состоящей из бактерии, вируса и грибка. 29. Способ лечения или предупреждения инфекционного заболевания у пациента, причем указанный способ включает введение указанному пациенту клинически релевантного количества соединения,чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови менее чем 8,0 мг/л, общей формулы (I)m представляет собой целое число от 1 до 5; каждый X независимо выбран из группы, состоящей из водорода, галогена, гидрокси, амино, нитро,изопропила, метокси, этокси, н-пропокси и изопропокси;R2 является выбранным из группы, состоящей из F, Cl, Br, I, CH2Y, CHY2 и CY3, где Y представляет собой атом галогена;R1, R3, R4, R6, R7, R8 и R9 независимо выбраны из группы, состоящей из водорода, С 1-6-алкила и С 1-6 алкокси;R10 и R11 вместе с атомом азота, к которому они присоединены, образуют азотсодержащий гетероарил или гетероциклил; или его соли в комбинации с противоинфекционным агентом; где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus штаммов SA-1199, SA-1199 В, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068. 30. Способ по п.29, где указанное соединение представляет собой соединение, как определено в одном из пп.2-24. 31. Способ по п.29 или 30, где указанное соединение вводят для обеспечения указанного устойчивого состояния концентрации в сыворотке крови в интервале от 0,01 мкг/л до менее чем 8,0 мг/л. 32. Способ по любому из пп.29-31, где указанный инфекционный агент является мультилекарственно устойчивым. 33. Набор, включающий первую единицу дозировки, содержащую клинически релевантное количество соединения, чувствительного к химическому воздействию, приводящего к повышению устойчивого состояния концентрации в сыворотке крови менее чем 8,0 мг/л, как определено в одном из пп.1-24, и дополнительно единицу дозировки, включающую противоинфекционный агент, для лечения или профилактики инфекционного заболевания в комбинации с противоинфекционным агентом; где инфекционное заболевание вызвано инфекционным агентом, выбранным из группы, состоящей из вируса, бактерии и грибка, причем указанный инфекционный агент является устойчивым к лекарственному средству; и где указанный инфекционный агент не является выбранным из группы, состоящей из Staphylococcus aureus штаммов SA-1199, SA-1199B, SA-K1712, SA-K1748, SA 8325-4 и SA-K2068. 34. Набор по п.33 для применения в качестве медикамента.
МПК / Метки
МПК: A61P 33/00, A61P 31/00, A61K 45/06
Метки: заболеваний, инфекционных, лечение
Код ссылки
<a href="https://eas.patents.su/30-16803-lechenie-infekcionnyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Лечение инфекционных заболеваний</a>
Предыдущий патент: Многоступенчатый центробежный электронасос
Следующий патент: Циклические конструкты натрийуретических пептидов
Случайный патент: Применение бессывороточной культуральной среды, содержащей антиоксидант, для снижения окисления рекомбинантных гонадотропинов