Имидазольные соединения для лечения нейродегенеративных расстройств
Формула / Реферат
1. Соединение формулы I

где А отсутствует или выбран из
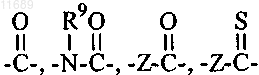
и SO2;
Z выбран из -СН2, -СН(ОН), групп -СН(С1-С6алкил), -СН(С1-С6алкокси), -CH(NR9R10),
-CH(CH2(OH)), -СН(СН(С1-С4алкил)(ОН)) и -СН(С(С1-С4алкил)(С1-С4алкил)(ОН));
R1 выбран из С1-С20алкила, С2-С20алкенила, С2-С20алкинила, C1-С20алкокси, С2-С20алкенокси, C1-С20 гидроксиалкила, С3-С8циклоалкила, групп бензо(С3-С8циклоалкил), бензо(С3-С8гетероциклоалкил), С4-С8циклоалкенила, (С5-С11)би- или трициклоалкила, бензо(С5-С11)би- или трициклоалкила, (С7-С11)би- или трициклоалкенила, 3-8-членного гетероциклоалкила, С6-С14арила и 5-14-членного гетероарила, где каждый атом водорода указанных алкила, алкенила, алкинила, алкокси и алкенокси возможно независимо заменен галогено и где указанные циклоалкил, бензо(С3-С8циклоалкил), циклоалкенил, 3-8-членный гетероциклоалкил, С6-С14арил и 5-14-членный гетероарил возможно независимо замещены заместителями в количестве от одного до четырех, независимо выбранными из C1-С10алкила, возможно замещенного атомами галогена в количестве от одного до трех, С1-С10алкокси, возможно замещенного атомами галогена в количестве от одного до трех, С1-С10гидроксиалкила, галогено, -ОН, -CN, -NR9R10, -C(=O)NR9R10,
-C(=O)R11, С3-С8циклоалкила и 3-8-членного гетероциклоалкила;
R2 выбран из Н, С1-С6алкила, С2-С6алкенила, С3-С8циклоалкила и С3-С8циклоалкенила, где R2 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С4алкила, возможно замещенного атомами галогена в количестве от одного до трех, С1-С4алкокси, возможно замещенного атомами галогена в количестве от одного до трех, галогено и -ОН;
или R1 и R2 вместе с группой А, когда она присутствует, и атомом азота, к которому присоединен R2, или R1 и R2 вместе с атомом азота, к которому присоединены R1 и R2, когда А отсутствует, возможно могут образовывать 4-8-членное кольцо;
R3 выбран из Н, C1-С6алкила, С2-С6алкенила, С2-С6алкинила, С3-С6циклоалкила, C5-С6циклоалкенила и 3-8-членного гетероциклоалкила, где каждый указанный алкил, алкенил, алкинил, циклоалкил, циклоалкенил и гетероциклоалкил возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С4алкокси, галогено, -ОН, групп -S(С1-С4)алкил, -О(С1-С4)алкил и 3-8-членного гетероциклоалкила;
R4 представляет собой Н, С1-С6алкил или галогено;
или R3 и R4 вместе с атомом углерода, к которому они присоединены, возможно могут образовывать группировку, выбранную из циклопропила, циклобутила, циклопентила, циклогексила, морфолино, пиперидино, пирролидино, тетрагидрофуранила и пергидро-2Н-пирана, где указанная группировка, образованная R3 и R4, возможно замещена заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, возможно замещенного атомами галогена в количестве от одного до трех, С1-С6алкокси, возможно замещенного атомами галогена в количестве от одного до трех, галогено, -ОН, -CN и аллила;
R6 выбран из Н, C1-С6алкила, С2-С6алкилена, С1-С6алкокси, галогено, -CN, С3-С12циклоалкила, С4-С12циклоалкенила, 5-10-членного гетероарила и С6-С10арила, где каждый указанный алкил, алкилен и алкокси из R6 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено и -CN, и где каждый указанный циклоалкил, циклоалкенил, гетероарил и арил из R6 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С4алкила, возможно замещенного атомами галогена в количестве от одного до трех, С1-С4 алкокси, возможно замещенного атомами галогена в количестве от одного до трех, галогено и -CN;
R7 выбран из Н, С1-С20алкила, C1-С20алкокси, С1-С20гидроксиалкила, С3-С12циклоалкила, С4-С12циклоалкенила, (С5-С20)би- или трициклоалкила, (С7-С20)би- или трициклоалкенила, 3-12-членного гетероциклоалкила, 7-20-членного гетероби- или гетеротрициклоалкила, С6-С14арила и 5-15-членного гетероарила, где R7 возможно независимо замещен заместителями в количестве от одного до четырех, независимо выбранными из C1-С20алкила, возможно замещенного атомами галогена в количестве от одного до трех, С1-С20алкокси, -ОН, -CN, -NO2, -NR9R10, -C(=O)NR9R10, -C(=O)R11, -C(=O)OR11, -S(O)nNR9R10,
-S(O)nR11, С3-С12циклоалкила, 4-12-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех, 4-12-членного гетероциклоалкокси, С6-С14арила, 5-15-членного гетероарила, С6-С12арилокси и 5-12-членного гетероарилокси;
или R6 и R7 вместе с атомами углерода и азота, к которым они соответственно присоединены, возможно могут образовывать 5-8-членное гетероциклоалкильное кольцо, 5-8-членное гетероциклоалкенильное кольцо или 6-8-членное гетероарильное кольцо, где каждое указанное гетероциклоалкильное, гетероциклоалкенильное и гетероарильное кольцо возможно независимо замещено заместителями в количестве от одного до трех, независимо выбранными из галогено, C1-С6алкила, возможно замещенного атомами галогена в количестве от одного до трех, C1-С6алкокси, возможно замещенного атомами галогена в количестве от одного до трех, C1-С6гидроксиалкила, -ОН, -(CH2)0-10NR9R10, -(CH2)0-10C(=O)NR9R10,
-SO2NR9R10 и С3-С12циклоалкила;
каждый из R9 и R10 независимо выбран из Н, С1-С10алкила, где каждый атом водорода указанного С1-С10алкила возможно независимо заменен атомом галогена, С2-С10алкенила, С2-С10алкинила, С1-С6алкокси, где каждый атом водорода указанного С1-С6алкокси возможно независимо заменен атомом галогена, С2-С6алкенокси, С2-С6алкинокси, -C(=O)R11, -S(O)nR11, С3-С8циклоалкила, С4-С8циклоалкениыр, (С5-С11)би- или трициклоалкила, (С7-С11)би- или трициклоалкенила, 3-8-членного гетероциклоалкила, С6-С14арила и 5-14-членного гетероарила, где каждый указанный алкил и алкокси возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено и -ОН, и где каждый указанный циклоалкил, циклоалкенил, би- или трициклоалкил, би- или трициклоалкенил, гетероциклоалкил, арил и гетероарил возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено, -ОН, C1-С6алкила, возможно независимо замещенного атомами галогена в количестве от одного до шести, С2-С6алкенила, С2-С6алкинила, C1-С6алкокси, С2-С6алкенокси, С2-С6алкинокси и С1-С6гидроксиалкила;
или NR9R10 может образовывать 4-7-членный гетероциклоалкил, где указанный гетероциклоалкил возможно включает 1-2 дополнительных гетероатома, независимо выбранных из N, О и S, и где указанный гетероциклоалкил возможно содержит двойные связи в количестве от одного до трех, и где указанный гетероциклоалкил возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, возможно замещенного атомами галогена в количестве от одного до шести, С2-С6алкенила, С2-С6алкинила, C1-С6алкокси, С2-С6алкенокси, С2-С6алкинокси, C1-С6гидроксиалкила, С2-С6гидроксиалкенила, С2-С6гидроксиалкинила, галогено, -ОН, -CN, -NO2, -C(=O)R11,
-C(=O)OR11, -S(O)nR11 и -S(O)nNR9R10;
R11 выбран из Н, С1-С8алкила, С3-С8циклоалкила, С4-С8циклоалкенила, (С5-С11)би- или трициклоалкила, -(С7-С11)би- или трициклоалкенила, 3-8-членного гетероциклоалкила, С6-С10арила и 5-14-членного гетероарила, где указанный алкил из R11 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из -ОН, -CN и С3-С8циклоалкила, и где каждый атом водорода указанного алкила возможно независимо заменен атомом галогена, и где каждый указанный циклоалкил, циклоалкенил, гетероциклоалкил, арил и гетероарил из R11 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено, С1-С8алкила, возможно замещенного атомами галогена в количестве от одного до трех, -ОН, -CN и С3-С8циклоалкила; и
n в каждом случае представляет собой целое число, независимо выбранное из 0, 1, 2 и 3;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где А отсутствует или представляет собой
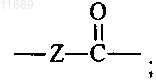
Z представляет собой -СН2, -СН(ОН) или -СН(С1-С6алкил); R1 представляет собой C1-С10алкил, С6-С10арил, 6-10-членный гетероарил или бензо(С5-С6циклоалкил), где когда R1 представляет собой С6-С10арил, С6-С10гетероарил или бензо(С5-С6циклоалкил), R1 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, галогено и ОН; R2 представляет собой Н или С1-С6алкил; R3 представляет собой Н, -CH2CH2SCH3, -О(С1-С4)алкил или С1-С6алкил; R4 представляет собой Н или С1-С6алкил; R6 представляет собой Н или С1-С6алкил; R7 представляет собой С1-С10алкил, С3-С8циклоалкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С8алкила, С1-С8алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех; и каждый из R9, R10 и R11 независимо выбран из Н и С1-С6алкила, где каждый атом водорода указанного С1-С6алкила возможно независимо заменен атомом галогена.
3. Соединение по п.2, где А отсутствует; R1 представляет собой бензо(С5-С6алкил), возможно замещенный заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, галогено и ОН; R2 представляет собой Н или С1-С6алкил; R3 представляет собой Н, -CH2CH2SCH3,
-СН2СН2ОСН3 или С1-С6алкил; R4 представляет собой Н или С1-С6алкил; R6 представляет собой Н или С1-С6алкил; R7 представляет собой С1-С10алкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С8алкокси, ОН, -NR9R10, -C(=O)NR9R10,
-C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила.
4. Соединение по п.3, где R7 возможно замещен -NR9R10, морфолино, пирролидинилом или пиперидинилом.
5. Соединение по п.3, где R4 представляет собой Н и R3 представляет собой метил, этил бутил, изобутил, пропил, изопропил, -CH2CH2SCH3 или -СН2СН2ОСН3.
6. Соединение по п.3, где R1 представляет собой 1,2,3,4-тетрагидронафталин или инданил, возможно замещенный атомами фтора или хлора в количестве от одного до трех.
7. Соединение по п.2, где А представляет собой 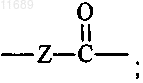 Z представляет собой -СН2, -СН(ОН) или -СН(С1-С6алкил); R1 представляет собой C1-С10алкил, С6-С10арил или 6-10-членный гетероарил, где указанные алкил, арил и гетероарил возможно независимо замещены заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, галогено и ОН; R2 представляет собой Н или С1-С6алкил; R3 представляет собой Н или С1-С6алкил; R4 представляет собой Н или С1-С6алкил; R6 представляет собой Н или C1-С6алкил; R7 представляет собой C1-С10алкил, С3-С8циклоалкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С8алкила, C1-С8алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11,
Z представляет собой -СН2, -СН(ОН) или -СН(С1-С6алкил); R1 представляет собой C1-С10алкил, С6-С10арил или 6-10-членный гетероарил, где указанные алкил, арил и гетероарил возможно независимо замещены заместителями в количестве от одного до трех, независимо выбранными из С1-С6алкила, галогено и ОН; R2 представляет собой Н или С1-С6алкил; R3 представляет собой Н или С1-С6алкил; R4 представляет собой Н или С1-С6алкил; R6 представляет собой Н или C1-С6алкил; R7 представляет собой C1-С10алкил, С3-С8циклоалкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С1-С8алкила, C1-С8алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11,
-C(=O)OR11 и 4-6-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех.
8. Соединение по п.7, где 4-10-членная гетероциклоалкильная группа из R7 представляет собой азетидинил, пирролидинил или пиперидинил; и 4-6-членный гетероциклоалкильэыщ заместитель R7 представляет собой морфолино, пирролидинил или пиперидинил.
9. Соединение по п.7, где R1 представляет собой арил, А представляет собой  Z представляет собой -СН2.
Z представляет собой -СН2.
10. Соединение по п.9, где R7 представляет собой C1-С6алкил, возможно замещенный -NR9R10, морфолино, пирролидинилом или пиперидинилом.
11. Соединение по п.1, выбранное из группы, состоящей из
метилового эфира 3-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил)масляной кислоты;
метилового эфира 3-{4-[2-(2-гидрокси-3-метилбутириламино)пентаноиламино]имидазол-1-ил}-3-метилмасляной кислоты;
метилового эфира 3-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил)-3-метилмасляной кислоты;
метилового эфира 3-{4-[2-(2-гидрокси-3,3-диметилбутириламино)пентаноиламино]имидазол-1-ил}-3-метилмасляной кислоты;
[1-(1-этилпропил)-1Н-имидазол-4-ил]амида 2-(2-гидрокси-3,3-диметилбутириламино)пентановой кислоты;
[1-(1-этилпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
1-(1-этилпропил)-1H-имидазоламида 2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентановой кислоты;
метилового эфира 2-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил)-2-метилпропионовой кислоты;
метилового эфира 2-(4-{2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентаноиламино}имидазол-1-ил)-2-метилпропионовой кислоты;
метилового эфира 2-{4-[2-(2-гидрокси-3,3-диметилбутириламино)пентаноиламино]имидазол-1-ил}-2-метилпропионовой кислоты;
метилового эфира 2-{4-[2-(2-гидрокси-3-метилбутириламино)пентаноиламино]имидазол-1-ил}-2-метилпропионовой кислоты;
метилового эфира 3-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пропиониламино}имидазол-1-ил)-3-метилмасляной кислоты;
метилового эфира 3-{4-[2-(2-гидрокси-3,3-диметилбутириламино)пропиониламино]имидазол-1-ил}-3-метилмасляной кислоты;
трет-бутилового эфира 4-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил) пиперидин-1-карбоновой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3-трифторметилфенил) ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]амида 2-[2-(3-трифторметоксифенил) ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентановой кислоты;
[1-(1-этилпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(4-фенилтиазол-2-ил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3-трифторметилфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(2-гидрокси-3-метилбутириламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]амида 2-(2-гидрокси-3,3-диметилбутириламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(2-гидрокси-3-метилбутириламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(2-гидрокси-3,3-диметилбутириламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]-4-метилпентановой кислоты;
2-[2-(3,5-дифторфенил)ацетиламино]-N-[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]пропионамида;
метилового эфира (4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил)уксусной кислоты;
метилового эфира 2-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}-2-метилимидазол-1-ил)-2-метилпропионовой кислоты;
[1-(2-метокси-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
метилового эфира 4-(4-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}имидазол-1-ил бензойной кислоты;
{1-[1-(2,2-диметилпропил)пирролидин-3-ил]-1H-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
метилового эфира 3-{4-[2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентаноиламино] имидазол-1-ил}масляной кислоты;
метилового эфира 2-{4-[2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентаноиламино] имидазол-1-ил}-2-метилпропионовой кислоты;
[1-(1-этилпропил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино) пентановой кислоты;
метилового эфира 3-{4-[2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентаноиламино] имидазол-1-ил}-3-метилмасляной кислоты;
[1-(2-изопропиламино-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-метиламиноэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(2-бензиламино-1,1-диметилэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[2-(2,2-диметилпропиламино)-1,1-диметилэтил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(2-диметиламино-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1,1-диметил-2-(1-фенилэтиламино)этил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-3-морфолин-4-илпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-3-пирролидин-1-илпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(5-хлориндан-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(индан-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6-фтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6-хлор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дихлор-1,2,3,4-тетрагидро-нафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(5,7-диметил-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6-изопропил-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(2-фторфенил)-1-метилэтиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[1-метил-2-(3-трифторметилфенил)этиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(5,7-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6-бром-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)этиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-1-метилэтиламино]пентановой кислоты;
[1-(1-этилпропил)-1Н-имидазол-4-ил]амшфр 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино) пентановой кислоты;
[1-(1,1-диметил-3-морфолин-4-илпропил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
{1-[1,1-диметил-2-(1-фенилэтиламино)этил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дихлор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)-4-метилпентановой кислоты;
2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)-N-[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]пропионамида;
[1-(2-диметиламино-1,1-диметилэтил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
метилового эфира 4-{4-[2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентаноиламино] имидазол-1-ил}бензойной кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,1-диметил-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6-изопропил-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(2-гидрокси-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(2-гидроксиэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(2-гидрокси-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(3-гидрокси-1,1-диметилпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(1-пиперидин-4-ил-1Н-имидазол-4-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1-метилпиперидин-4-ил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1-ацетилпиперидин-4-ил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(1-пиперидин-4-ил-1H-имидазол-4-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1-(3,3-диметилбутирил)пиперидин-4-ил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1-(3,3-диметилбутил)пиперидин-4-ил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1-(2,2-диметилпропил)пиперидин-4-ил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[6-(4-фторфенил)-1,2,3,4-тетрагидронафталин-2-иламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-ил)метиламино]пентановой кислоты;
[7-(2,2-диметилпропил)-5,5-диметил-5,6,7,8-тетрагидроимидазо[1,5-а]пиразин-1-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[2-(2,2-диметилпропиламино)-1,1-диметилэтил]-1Н-имидазол-4-ил}амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пиперидин-1-илэтил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(2-диметиламино-1,1-диметилэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
{1-[1,1-диметил-2-(2,2,2-трифторэтиламино)этил]-1Н-имидазол-4-ил}амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(3-гидроксициклобутил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
{1-[2-(2,6-диметилморфолин-4-ил)-1,1-диметилэтил]-1Н-имидазол-4-ил}амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
(1-{2-[(2,2-диметилпропил)метиламино]-1,1-диметилэтил}-1H-имидазол-4-ил)амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
{1-[1,1-диметил-2-(4-метилпиперазин-1-ил)этил]-1H-имидазол-4-ил}амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
[1-(2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[2-(2,2-диметилпропиламино)этил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[2-(4-метилпиперазин-1-ил)этил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино] пентановой кислоты;
[1-(2-гидрокси-1,1,2-триметилпропил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(3-гидрокси-1,1,3-триметилбутил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(2-этил-2-гидрокси-1,1-диметилбутил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(3-этил-3-гидрокси-1,1-диметилпентил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(1-трет-бутил-1Н-имидазол-4-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(1-трет-бутил-1Н-имидазол-4-ил)амида 2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]пентановой кислоты;
(1-трет-бутил-1Н-имидазол-4-ил)амида 2-(2-гидрокси-3,3-диметилбутириламино)пентановой кислоты;
(1-трет-бутил-1Н-имидазол-4-ил)амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты;
2-[2-(3,5-дифторфенил)-2-гидроксиацетиламино]-N-(1-изопропил-1Н-имидазол-4-ил)пропионамида;
(1-изопропил-1H-имидазол-4-ил)амида 2-(2-гидрокси-3,3-диметилбутириламино)пентановой кислоты;
{1-[2-(3-гидроксипирролидин-1-ил)-1,1-диметилэтил]-1H-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1-(2,2-диметилпропил)азетидин-3-ил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
{1-[1-(2,2-диметилпропионил)азетидин-3-ил]-1Н-имидазол-4-ил}амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(2-изопропокси-1,1-диметилэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидро-1,4-метанонафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-(5,7-дифторхроман-3-иламино) пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-(4,6-дифтортрицикло[6.2.2]додека-2(7),3,5-триен-9-иламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(нафталин-2-иламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1Н-имидазол-4-ил]амида 2-(хинолин-3-иламино)пентановой кислоты;
[1-(1,1-диметил-2-морфолин-4-илэтил)-1H-имидазол-4-ил]амида 2-(1-метил-1Н-индол-3-иламино) пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-2-трифторметил-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-2-фтор-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил) ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-2-фенил-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил) ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-5-фенил-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил) ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-5-трифторметил-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
метилового эфира 5-{2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламино}-3-(1,1-диметил-2-пирролидин-1-илэтил)-3Н-имидазол-4-карбоновой кислоты;
(6,6-диметил-5,6,7,8-тетрагидроимидазю[1,5-а]пиридин-1-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(6-метил-5,6,7,8-тетрагидроимидазо[1,2-а]пиридин-2-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(3,4-дигидро-2Н-имидазо[5,1-b][1,3]оксазин-8-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
(1Н-имидазо[1,2-а]пиридин-3-ил)амида 2-[2-(3,5-дифторфенил)ацетиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)этиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-2-гидроксиэтиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]амида 2-[2-(3,5-дифторфенил)-1-метилэтиламино]пентановой кислоты;
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(3,5-дифторбензиламино)пентановой кислоты;
[1-(1-диметиламинометилциклопентил)-1H-имидазол-4-ил]амида 2-(6,8-дифтор-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты и
[1-(1,1-диметил-2-пирролидин-1-илэтил)-1Н-имидазол-4-ил]амида 2-(6,8-дифтор-1-гидрокси-1,2,3,4-тетрагидронафталин-2-иламино)пентановой кислоты и их фармацевтически приемлемых солей.
12. Соединение по п.1, где стереохимия заместителей R3 и R4 представлена ниже:
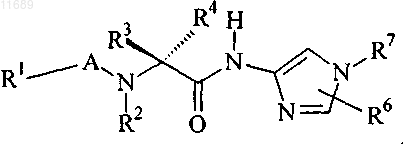
13. Соединение по п.12, где R4 и R2 представляют собой -Н.
14. Фармацевтическая композиция для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, содержащая соединение по п.1 в количестве, эффективном для ингибирования продукции Аb-пептида или лечения такого заболевания или состояния, и фармацевтически приемлемый носитель.
15. Способ ингибирования продукции Аb-пептида у млекопитающего, включающий введение указанному млекопитающему соединения по п.1 в количестве, эффективном для ингибирования Аb-продукции.
16. Способ лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, включающий введение указанному млекопитающему соединения по п.1 в количестве, эффективном для ингибирования Аb-продукции или лечения такого заболевания или состояния.
17. Способ лечения заболевания или состояния, связанного с продукцией Аb-пептида, у млекопитающего, включающий введение указанному млекопитающему (а) соединения по п.1; и (б) средства для улучшения памяти, антидепрессанта, анксиолитика, антипсихотического средства, средства от расстройства сна, противовоспалительного средства, антиоксиданта, модулятора холестерина, антагониста гистамина (Н2) или антигипертензивного средства; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния.
18. Способ лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, включающий введение указанному млекопитающему (а) соединения по п.1; и (б) средства для улучшения памяти, антидепрессанта, анксиолитика, антипсихотического средства, средства от расстройства сна, противовоспалительного средства, антиоксиданта, модулятора холестерина, антагониста гистамина (Н2) или антигипертензивного средства; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния.
19. Фармацевтическая композиция для лечения заболевания или состояния, связанного с модуляцией Notch-сигнального пути, содержащая соединение формулы I по п.1 или его фармацевтически приемлемые соли.
20. Композиция по п.19, где заболевание или состояние выбрано из группы, состоящей из рака, артериосклероза, диабетической ретинопатии, ревматоидного артрита, псориаза, воспалительного заболевания кишечника, воспаления, астмы, отторжения трансплантата, болезни "трансплантат против хозяина", аутоиммунного заболевания и отторжения ткани или органа.
21. Композиция по п.20, где заболевание или состояние выбрано из группы, состоящей из рака.
22. Способ лечения заболевания или состояния, выбранного из группы, состоящей из рака, артериосклероза, диабетической ретинопатии, ревматоидного артрита, псориаза, воспалительного заболевания кишечника, воспаления, астмы, отторжения трансплантата, болезни "трансплантат против хозяина", аутоиммунного заболевания и отторжения ткани или органа, включающий введение указанному млекопитающему соединения по п.1 в количестве, эффективном для модуляции Notch-сигнального пути или лечения такого заболевания или состояния.
Текст
011689 Перекрестная ссылка на родственную заявку. Настоящая заявка основана на заявке США 60/555,623, поданной 23 марта 2004. Область изобретения Настоящее изобретение относится к лечению нейродегенеративных и/или неврологических расстройств, таких как болезнь Альцгеймера, у млекопитающих, включая людей. Это изобретение также относится к ингибированию у млекопитающих, включая людей, продукции А-пептидов, которые могут способствовать формированию неврологических отложений амилоидного белка. Более конкретно, это изобретение относится к имидазольным соединениям, фармацевтическим композициям, содержащим такие соединения, и способам применения таких соединений, то есть для лечения нейродегенеративных и/или неврологических расстройств, таких как болезнь Альцгеймера, связанных с продукцией Апептида. Предшествующий уровень техники Деменция является результатом широкого множества типичных патологических процессов. Наиболее распространенные патологические процессы, вызывающие деменцию, представляют собой болезнь Альцгеймера (БА), церебральную амилоидную ангиопатию (ЦАА) и прионовые заболевания. БА поражает почти половину всех людей старше 85 лет, наиболее быстро растущую долю населения США. Ожидают, что количество пациентов с БА в США, по существу, вырастет от приблизительно 4 миллионов до приблизительно 14 миллионов к середине следующего века. Лечение БА обычно представляет собой помощь, обеспечиваемую членом семьи в уходе за больным. Было показано, что стимулирующие память упражнения, проводимые регулярно, замедляют, но не останавливают потерю памяти. Новые лекарства, например Aricept, предусматривают лечение БА. Признаком БА является накопление в головном мозге внеклеточных нерастворимых отложений, называемых амилоидными бляшками, и аномальных повреждений нейронов, называемых нейрофибриллярными клубками. Увеличенное формирование бляшек связано с увеличенным риском БА. Действительно, наличие амилоидных бляшек вместе с нейрофибриллярными клубками представляет собой основу для окончательного патологического диагноза БА. Основными компонентами амилоидных бляшек являются амилоидные А-пептиды, также называемые А-пептиды, которые состоят из нескольких белков, включающих 38, 40, 42 или 43 аминокислоты, обозначаемых соответственно как A1-38, A1-40, A1-42 и A1-43 пептиды. Полагают, что A-пептиды вызывают разрушение нервных клеток, частично из-за того, что являются токсичными в отношении нейронов in vitro и in vivo. А пептиды получаются из более крупных амилоидных белков предшественников (АРР белков),состоящих из четырех белков, содержащих 695, 714, 751 или 771 аминокислот(ы), обозначаемых соответственно как АРР 695, APP714, APP751 и АРР 771. Полагают, что протеазы продуцируют А пептиды путем расщепления специфических аминокислотных последовательностей в различных АРР белках. Протеазы названы "секретазами", поскольку А-пептиды, которые они продуцируют, секретируются клетками во внеклеточную среду. Каждая из этих секретаз названа в соответствии с расщеплением(ми), которые они осуществляют для продукции А-пептидов. Секретаза, образующая аминотерминальный конец Апептидов, названа бета-секретазой. Секретаза, образующая карбокситерминальный конец А-пептидов,названа гамма-секретазой. Это изобретение относится к новым соединениям, ингибирующим продукцию А-пептида, к фармацевтическим композициям, содержащим такие соединения, и к способам применения таких соединений для лечения нейродегенеративных и/или неврологических расстройств. Краткое изложение сущности изобретения Настоящее изобретение относится к соединениям формулы I где А отсутствует или выбран изR1 выбран из С 1-С 20 алкила, С 2-С 20 алкенила, С 2-С 20 алкинила, С 1-С 20 алкокси, С 2-С 20 алкенокси, С 1 С 20 гидроксиалкила, С 3-С 8 циклоалкила, групп бензо(С 3-С 8 циклоалкил), бензо(С 3-С 8 гетероциклоалкил),-1 011689 С 4-С 8 циклоалкенила, (С 5-С 11)би- или трициклоалкила, бензо(С 5-С 11)би- или трициклоалкила, (С 7-С 11)биили трициклоалкенила, 3-8-членного гетероциклоалкила, С 6-С 14 арила и 5-14-членного гетероарила, где каждый атом водорода указанных алкила, алкенила, алкинила, алкокси и алкенокси возможно независимо заменен галогено, и где указанные циклоалкил, бензо(С 3-С 8 циклоалкил), циклоалкенил, 3-8-членный гетероциклоалкил, С 6-С 14 арил и 5-14-членный гетероарил возможно независимо замещены заместителями в количестве от одного до четырех, независимо выбранными из C1-С 10 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1-С 10 алкокси, возможно замещенного атомами галогена в количестве от одного до трех, C1-С 10 гидроксиалкила, галогено, предпочтительно фторо, -ОН, -CN,-NR9R10, -C(=O)NR9R10, -C(=O)R11, С 3-С 8 циклоалкила и 3-8-членного гетероциклоалкила;R2 выбран из Н, C1-С 6 алкила, С 2-С 6 алкенила, С 3-С 8 циклоалкила и С 5-С 8 циклоалкенила, где R2 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 4 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1-С 4 алкокси,возможно замещенного атомами галогена в количестве от одного до трех, галогено и -ОН; или R1 и R2 вместе с группой А, когда она присутствует, и атомом азота, к которому присоединен 2R , или R1 и R2 вместе с атомом азота, к которому присоединены R1 и R2, когда А отсутствует, возможно могут образовывать 4-8-членное кольцо;R3 выбран из Н, С 1-С 6 алкила, С 2-С 6 алкенила, С 2-С 6 алкинила, С 3-С 6 циклоалкила, С 5-С 6 циклоалкенила и 3-8-членного гетероциклоалкила, где каждый указанный алкил, алкенил, алкинил, циклоалкил, циклоалкенил и гетероциклоалкил возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 4 алкокси, галогено, -ОН, группы -S(С 1-С 4)алкил и 3-8-членного гетероциклоалкила;R4 представляет собой Н, С 1-С 6 алкил или галогено; или R3 и R4 вместе с атомом углерода, к которому они присоединены, возможно могут образовывать группировку, выбранную из циклопропила, циклобутила, циклопентила, циклогексила, морфолино,пиперидино, пирролидино, тетрагидрофуранила и пергидро-2 Н-пирана, где указанная группировка, образованная R3 и R4, возможно замещена заместителями в количестве от одного до трех, независимо выбранными из С 1-С 6 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1 С 6 алкокси, возможно замещенного атомами галогена в количестве от одного до трех, галогено, -ОН, -CN и аллила;R6 выбран из Н, С 1-С 6 алкила, С 2-С 6 алкилена, С 1-С 6 алкокси, галогено, -CN, С 3-С 12 циклоалкила, С 4 С 12 циклоалкенила и С 6-С 10 арила, 5-10-членного гетероарила, где каждый указанный алкил, алкилен и алкокси из R6 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено и -CN, и где каждый указанный циклоалкил, циклоалкенил и арил и гетероарил из R6 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 4 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1 С 4 алкокси, возможно замещенного атомами галогена в количестве от одного до трех, галогено и -CN;R7 выбран из Н, С 1-С 20 алкила, С 1-С 20 алкокси, С 1-С 20 гидроксиалкила, С 3-С 12 циклоалкила, С 4-С 12 циклоалкенила, (С 5-С 20)би- или трициклоалкила, (С 7-С 20)би- или трициклоалкенила, 3-12-членного гетероциклоалкила, 7-20-членного гетероби- или гетеротрициклоалкила, С 6-С 14 арила и 5-15-членного гетероарила, где R7 возможно независимо замещен заместителями в количестве от одного до четырех, независимо выбранными из С 1-С 20 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1-С 20 алкокси, -ОН, -CN, -NO2, -NR9R10, -C(=O)NR9R10, -C(=O)R11, -C(=O)OR11, -S(O)nNR9R10,-S(O)nR11, С 3-С 12 циклоалкила, 4-12-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех, 4-12-членного гетероциклоалкокси, С 6-С 14 арила, 5-15 членного гетероарила, С 6-С 12 арилокси и 5-12-членного гетероарилокси; или R6 и R7 вместе с атомами углерода и азота, к которым они соответственно присоединены, возможно могут образовывать 5-8-членное гетероциклоалкильное кольцо, 5-8-членное гетероциклоалкенильное кольцо или 6-8-членное гетероарильное кольцо, где каждое указанное гетероциклоалкильное,гетероциклоалкенильное и гетероарильное кольцо возможно независимо замещено заместителями в количестве от одного до трех, независимо выбранными из галогено, С 1-С 6 алкила, возможно замещенного атомами галогена в количестве от одного до трех, С 1-С 6 алкокси, возможно замещенного атомами галогена в количестве от одного до трех, C1-С 6 гидроксиалкила, -ОН, -(CH2)0-10NR9R10, -(CH2)0-10C(=O)NR9R10,-SO2NR9R10 и С 3-С 12 циклоалкила; каждый из R9 и R10 независимо выбран из Н, С 1-С 10 алкила, где каждый атом водорода указанного С 1-С 10 алкила возможно независимо заменен атомом галогена, предпочтительно атомом фтора, С 2-С 10 алкенила, С 2-С 10 алкинила, С 1-С 6 алкокси, где каждый атом водорода указанного С 1-С 6 алкокси возможно независимо заменен атомом галогена, С 2-С 6 алкенокси, С 2-С 6 алкинокси, -C(=O)R11, -S(O)nR11, С 3-С 8 циклоалкила, С 4-С 8 циклоалкенила, (С 5-С 11)би- или трициклоалкила, (С 7-С 11)би- или трициклоалкенила, 3-8 членного гетероциклоалкила, С 6-С 14 арила и 5-14-членного гетероарила, где каждый указанный алкил и алкокси возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено и -ОН, и где каждый указанный циклоалкил, циклоалкенил, би- или трициклоалкил, би- или трициклоалкенил, гетероциклоалкил, арил и гетероарил возможно независимо замещен за-2 011689 местителями в количестве от одного до трех, независимо выбранными из галогено, -ОН, С 1-С 6 алкила,возможно независимо замещенного атомами галогена в количестве от одного до шести, С 2-С 6 алкенила,С 2-С 6 алкинила, С 1-С 6 алкокси, С 2-С 6 алкенокси, С 2-С 6 алкинокси и C1-С 6 гидроксиалкила; или NR9R10 может образовывать 4-7-членный гетероциклоалкил, где указанный гетероциклоалкил возможно включает 1-2 дополнительных гетероатома, независимо выбранных из N, О и S, и где указанный гетероциклоалкил возможно содержит двойные связи в количестве от одного до трех, и где указанный гетероциклоалкил возможно независимо замещен заместителями в количестве от одного до трех,независимо выбранными из С 1-С 6 алкила, возможно замещенного атомами галогена в количестве от одного до шести, С 2-С 6 алкенила, С 2-С 6 алкинила, С 1-С 6 алкокси, С 2-С 6 алкенокси, С 2-С 6 алкинокси, С 1-С 6 гидроксиалкила, С 2-С 6 гидроксиалкенила, С 2-С 6 гидроксиалкинила, галогено, -ОН, -CN, -NO2, -C(=O)R11,-C(=O)OR11, -S(O)nR11 и -S(O)nNR9R10;R11 выбран из Н, С 1-С 8 алкила, С 3-С 8 циклоалкила, С 4-С 8 циклоалкенила, (С 5-С 11)би- или трициклоалкила, -(С 7-С 11)би- или трициклоалкенила, 3-8-членного гетероциклоалкила, С 6-С 10 арила и 5-14-членного гетероарила, где указанный алкил из R11 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из -ОН, -CN и С 3-С 8 циклоалкила, и где каждый атом водорода указанного алкила возможно независимо заменен атомом галогена, предпочтительно атомом фтора, и где каждый указанный циклоалкил, циклоалкенил, гетероциклоалкил, арил и гетероарил из R11 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено, C1-С 8 алкила, возможно замещенного атомами галогена в количестве от одного до трех, -ОН, -CN и С 3-С 8 циклоалкила;n в каждом случае представляет собой целое число, независимо выбранное из 0, 1, 2 и 3; и фармацевтически приемлемым солям таких соединений. Соединения формулы I могут иметь оптические центры и поэтому могут существовать в различных энантиомерных и диастереоизомерных конфигурациях. Настоящее изобретение включает все энантиомеры, диастереоизомеры и другие стереоизомеры таких соединений формулы I, a также рацемические соединения и рацемические смеси, и другие смеси их стереоизомеров. Фармацевтически приемлемые соли соединений формулы I включают их соли присоединения кислоты и основные соли. Подходящие соли присоединения кислоты получают из кислот, которые образуют нетоксичные соли. Примеры включают соли ацетат, адипат, аспартат, бензоат, бесилат, бикарбонат/карбонат, бисульфат/ сульфат, борат, камсилат, цитрат, цикламат, эдисилат, эзилат, формиат, фумарат, глюцептат, глюконат,глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидройодид/йодид,изетионат, лактат, малат, малеат, малонат, манделаты, мезилат, метилсульфат, нафтилат, 2-напсилат, никотинат, нитрат, оротат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрофосфат, пироглутамат,салицилат, сахарат, стеарат, сукцинат, сульфонат, станнат, тартрат, тозилат, трифторацетат и ксинофоат,но не ограничиваются ими. Подходящие основные соли получают из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина,лизина, магния, меглумина, оламина, калия, натрия, трометамина и цинка, но не ограничиваются ими. Также могут быть получены гемисоли (hemisalts) кислот и оснований, например гемисульфат и гемикальциевая соли. Обзор подходящих солей смотри в Handbook of Pharmaceutical Salts: Properties, Selection, and Use byStahl and Wermuth (Wiley-VCH, 2002). Фармацевтически приемлемые соли соединений формулы I могут быть получены при помощи одного или более чем одного из трех способов:(1) путем взаимодействия соединения формулы I с желаемой кислотой или основанием;(2) путем удаления защитной группы, неустойчивой к кислоте или основанию, из подходящего предшественника соединения формулы I или путем раскрытия кольца подходящего циклического предшественника, например, лактона или лактама, с использованием желаемой кислоты или основания; или(3) путем превращения одной соли соединения формулы I в другую соль взаимодействием с соответствующей кислотой или основанием или при помощи подходящей ионообменной колонки. Все три реакции обычно проводят в растворе. Получающаяся в результате соль может выпадать в осадок или ее можно собрать фильтрованием, или можно выделить выпариванием растворителя. Степень ионизации получающейся в результате соли может изменяться от полностью ионизированной до почти неионизированной. Соединения по изобретению могут существовать в непрерывном ряде твердых состояний в диапазоне от полностью аморфного до полностью кристаллического. Термин "аморфный" относится к состоянию, при котором материал утрачивает дальний порядок на молекулярном уровне и в зависимости от температуры может проявлять физические свойства твердого вещества или жидкости. Обычно такие вещества не дают характерные картины дифракции рентгеновских лучей и, хотя демонстрируют свойства твердого вещества, формально в большей степени описываются как жидкость. При нагревании происходит изменение свойств от твердого вещества до жидкости, которое характеризуется изменением состоя-3 011689 ния, обычно второго рода ("стеклование"). Термин "кристаллический" относится к твердой фазе, в которой вещество имеет регулярным образом упорядоченную внутреннюю структуру на молекулярном уровне и дает характерную картину дифракции рентгеновских лучей с определенными пиками. Такие вещества при достаточном нагревании также будут проявлять свойства жидкости, но переход от твердого вещества к жидкости характеризуется фазовым переходом, обычно первого рода ("температура плавления"). Соединения по изобретению также могут существовать в несольватированной и сольватированной формах. Термин "сольват" используют здесь для описания молекулярного комплекса, включающего соединение по изобретению и одну или более чем одну молекулу фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют в том случае, когда указанный растворитель представляет собой воду. Принятая в настоящее время система классификации органических гидратов представляет собой такую систему, которая определяет гидраты с изолированным сайтом (isolated site), канальные гидраты или гидраты с координированным ионом металла - смотри Polymorphism in Pharmaceutical Solids by K. R.Morris (Ed. H. G. Brittain, Marcel Dekker, 1995). Гидраты с изолированным сайтом представляют собой гидраты, в которых молекулы воды изолированы от непосредственного контакта друг с другом промежуточными органическими молекулами. В канальных гидратах молекулы воды находятся в каналах решетки рядом с другими молекулами воды. В гидратах с координированным ионом металла молекулы воды связаны с ионом металла. В тех случаях, когда растворитель или вода связаны крепко, комплекс будет обладать хорошо определенной стереохимией, независимо от влажности. Однако когда растворитель или вода связаны слабо,как в канальных сольватах и гигроскопических соединениях, отношение вода/растворитель будет зависеть от влажности и условий сушки. В этих случаях нормальным будет отсутствие стехиометрии. Соединения по изобретению в подходящих условиях также могут существовать в мезоморфном состоянии (мезофаза или жидкий кристалл). Мезоморфное состояние является промежуточным между действительным кристаллическим состоянием и действительным жидким состоянием (или расплавленным,или раствором). Мезоморфизм, возникающий в результате изменения температуры, описан как "термотропный", а мезоморфизм, возникающий в результате добавления второго компонента, такого как вода или другой растворитель, описан как "лиотропный". Соединения, которые обладают потенциалом образовывать лиотропные мезофазы, описаны как "амфифильные", и состоят из молекул, несущих ионные(такие как -COO-Na+, -СОО-K+ или -SO3-Na+) или неионные (такие как -N-N+(CH3)3) полярные головные группы. Более подробную информацию смотри в Crystals and the Polarizing Microscope by N. H.Hartshome and A. Stuart, 4th Edition (Edward Arnold, 1970). В дальнейшем все ссылки на соединения формулы I включают ссылки на их соли, сольваты, многокомпонентные комплексы и жидкие кристаллы и на сольваты, многокомпонентные комплексы и жидкие кристаллы их солей. Соединения по изобретению включают соединения формулы I, как определено выше, в том числе все их полиморфы и формы кристалла, их пролекарства и изомеры (в том числе оптические, геометрические и таутомерные изомеры), как определено ниже, и изотопно-меченные соединения формулы I. Если не указано иначе, используемый здесь термин "А отсутствует" означает непосредственную связь между азотом и R1 (то есть, -N-R1). Если не указано иначе, используемый здесь термин "алкил" включает насыщенные одновалентные углеводородные радикалы, имеющие прямоцепочечные или разветвленные группировки. Примеры алкильных групп включают метил, этил, н-пропил, изопропил и тpeт-бутил, но не ограничиваются ими. Если не указано иначе, используемый здесь термин "алкенил" включает алкильные группировки,имеющие по меньшей мере одну углерод-углеродную двойную связь, где алкил является таким как определено выше. Примеры алкенила включают этенил и пропенил, но не ограничиваются ими. Если не указано иначе, используемый здесь термин "алкинил" включает алкильные группировки,имеющие по меньшей мере одну углерод-углеродную тройную связь, где алкил является таким как определено выше. Примеры алкинильных групп включают этинил и 2-пропинил, но не ограничиваются ими. Если не указано иначе, используемый здесь термин "алкокси" означает "алкил-О-", где "алкил" является таким как определено выше. Примеры "алкокси" групп включают метокси, этокси, пропокси, бутокси, пентокси и аллилокси, но не ограничиваются ими. Если не указано иначе, используемый здесь термин "алкенокси" означает "алкенил-О-", где "алкенил" является таким как определено выше. Если не указано иначе, используемый здесь термин "циклоалкил" включает неароматические насыщенные циклические алкильные группировки, где алкил является таким как определено выше. Примеры циклоалкила включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил, но не ограничиваются ими. Группы "бициклоалкил" и "трициклоалкил" представляют собой неароматические насыщенные карбоциклические группы, состоящие из двух или трех колец, соответственно, где указанные кольца имеют по меньшей мере один общий атом углерода. Если не указано иначе, для задач настоящего изобретения бициклоалкильные группы включают спирогруппы и конденсированные кольце-4 011689 вые группы. Примеры бициклоалкильных групп включают бицикло[3.1.0]гексил, бицикло[2.2.1]гепт-1 ил, норборнил, спиро[4.5]децил, спиро[4.4]нонил, спиро[4.3]октил и спиро[4.2]гептил, но не ограничиваются ими. Примером трициклоалкильной группы является адамантил. Другие циклоалкильные, бициклоалкильные и трициклоалкильные группы известны в области техники, и такие группы охвачены здесь определениями "циклоалкил", "бициклоалкил" и "трициклоалкил"."Циклоалкенил", "бициклоалкенил" и "трициклоалкенил" относятся к неароматическим карбоциклическим циклоалкильным, бициклоалкильным и трициклоалкильным группировкам, определенным выше, за исключением того, что содержат одну или более чем одну углерод-углеродную двойную связь,связывающую члены углеродного кольца ("эндоциклическая" двойная связь) и/или одну или более чем одну углерод-углеродную двойную связь, связывающую член углеродного кольца и соседний некольцевой углерод ("экзоциклическая" двойная связь). Примеры циклоалкенильных групп включают циклопентенил, циклобутенил и циклогексенил, но не ограничиваются ими, и неограничивающим примером бициклоалкенильной группы является норборненил. Другие циклоалкенильные, бициклоалкенильные и трициклоалкенильные группы известны в области техники, и такие группы включены здесь в определения "циклоалкенил", "бициклоалкенил" и "трициклоалкенил". Циклоалкильные, циклоалкенильные, бициклоалкильные и бициклоалкенильные группы также включают группы, которые замещены одной или более чем одной группировкой оксо. Примеры таких групп с группировками оксо представляют собой оксоциклопентил, оксоциклобутил, оксоциклопентенил и норкамфорил. Используемый здесь термин "бензоциклоалкил" включает, без ограничения, такие группировки, как тетрагидронафтил, инданил, 1,2-бензоциклогептанил и тому подобное. Если не указано иначе, используемый здесь термин "арил" включает органический радикал, являющийся производным ароматического углеводорода путем удаления одного атома водорода, такой как фенил, нафтил, инденил, инданил и флуоренил. "Арил" охватывает конденсированные кольцевые группы, где по меньшей мере одно кольцо является ароматическим. Если не указано иначе, используемые здесь термины "гетероциклический" и "гетероциклоалкил" относятся к неароматическим циклическим группам, содержащим один или более чем один гетероатом,предпочтительно от одного до четырех гетероатомов, каждый из которых выбран из О, S и N. "Гетеробициклоалкильные" группы представляют собой неароматические двухкольцевые циклические группы, где указанные кольца имеют общие один или два атома, и где по меньшей мере одно из колец содержит гетероатом (О, S или N). Гетеробициклоалкильные группы для задач настоящего изобретения, и если не указано иначе, включают спирогруппы и конденсированные кольцевые группы. "Гетеротрициклоалкильные" группы представляют собой неароматические трехкольцевые циклические группы, где указанные кольца конденсированы друг с другом или образуют спирогруппу (другими словами, по меньшей мере два указанных кольца имеют один или два общих атома, а третье кольцо имеет один или два общих атома по меньшей мере с одним из указанных двух колец). Гетеротрициклоалкильные группы соединений по настоящему изобретению могут включать один или более чем один гетероатом О, S и/или N. В одном из воплощений каждое кольцо в гетеробициклоалкиле или гетеротрициклоалкиле содержит до четырех гетероатомов (то есть, от нуля до четырех гетероатомов, при условии, что по меньшей мере одно кольцо содержит по меньшей мере один гетероатом). Гетероциклоалкильные, гетеробициклоалкильные и гетеротрициклоалкильные группы по настоящему изобретению также могут включать кольцевые системы,замещенные одной или более чем одной группировкой оксо. Гетероциклические группы, включающие гетеробициклические и гетеротрициклические группы, могут включать двойные или тройные связи, например, гетероциклоалкенил, гетеробициклоалкенил и гетеротрициклоалкенил. Примеры неароматических гетероциклических групп представляют собой азиридинил, азетидинил, пирролидинил, пиперидинил, азепинил, пиперазинил, 1,2,3,6-тетрагидропиридинил, оксиранил, оксетанил, тетрагидрофуранил,тетрагидротиенил, тетрагидропиранил, тетрагидротиопиранил, морфолино, тиоморфолино, тиоксанил,пирролинил, индолинил, 2 Н-пиранил, 4 Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, хинолизинил, хинуклидинил, 1,4-диоксаспиро[4.5] децил, 1,4-диоксаспиро[4.4]нонил, 1,4-диоксаспиро[4.3]октил и 1,4-диоксаспиро[4.2]гептил. Если не указано иначе, используемый здесь "гетероарил" относится к ароматическим группам, содержащим один или более чем один гетероатом (О, S или N), предпочтительно от одного до четырех гетероатомов. Мультициклическая группа, содержащая один или более чем один гетероатом, где по меньшей мере одно кольцо группы является ароматическим, представляет собой "гетероарильную" группу. Гетероарильные группы по этому изобретению также могут включать кольцевые системы, замещенные одной или более чем одной группировкой оксо. Примеры гетероарильных групп представляют собой пиридинил, пиридазинил, имидазолил, пиримидинил, пиразолил, триазолил, пиразинил, хинолил, изохинолил, 1,2,3,4-тетрагидрохинолил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, триазинил, 1,2,4-триазинил, 1,3,5-триазинил, изоиндолил, 1-оксоизоиндолил, пуринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотриазолил, бензотиазолил, бензок-5 011689 сазолил, хиназолинил, хиноксалинил, нафтиридинил, дигидрохинолил, тетрагидрохинолил, дигидроизохинолил, тетрагидроизохинолил, бензофурил, фуропиридинил, пиролопиримидинил и азаиндолил. Как понятно специалисту в данной области техники применение формулы I является удобным, и изобретение представляет и охватывает ниже каждый и все признаки, идентифицированные индивидуально и изложенные здесь. Таким образом, настоящее изобретение рассматривает каждый признак по отдельности и любую и все комбинации и перестановки признаков, подпадающих под формулу I. Вышеупомянутые группы, полученные из перечисленных выше соединений, могут быть присоединены по атому С или N, когда такое является возможным. Например, группа, полученная из пиррола,может представлять собой пиррол-1-ил (присоединение по N) или пиррол-3-ил (присоединение по С). Термины, относящиеся к группам, также охватывают все возможные таутомеры. Как указано, так называемые "пролекарства" соединений формулы I также находятся в объеме изобретения. Таким образом, некоторые производные соединений формулы I, которые сами могут обладать небольшой фармакологической активностью или не обладать ей, могут при введении в или на организм превращаться в соединения формулы I, обладающие желаемой активностью, например путем гидролитического расщепления. Такие производные названы "пролекарствами". Дополнительное описание применения пролекарств можно найти в Prodrugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T.Higuchi and W. Stella) и Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (Ed. E. B. Roche,American Pharmaceutical Association). Пролекарства по изобретению могут, например, быть получены путем замещения подходящих функциональных групп, присутствующих в соединениях формулы I, некоторыми группировками, которые известны специалистам в данной области техники как "прогруппировки", что описано, например вDesign of Prodrugs by H. Bundgaard (Elsevier, 1985). Некоторые примеры пролекарств по изобретению включают в себя случаи:(1) когда соединение формулы I содержит функциональную группу карбоновой кислоты (-COOH),ее сложный эфир, например, соединение, в котором атом водорода функциональной группы карбоновой кислоты соединения формулы (I) заменен (С 1-С 8)алкилом;(2) когда соединение формулы I содержит спиртовую функциональную группу (-ОН), ее простой эфир, например, соединение, в котором атом водорода спиртовой функциональной группы соединения формулы I заменен (С 1-С 6)алканоилоксиметилом; и(3) когда соединение формулы I содержит первичную или вторичную функциональную аминогруппу (-NH2 или -NHR, где R не равен Н), ее амид, например соединение, в котором в зависимости от обстоятельств один или оба атома водорода функциональной аминогруппы соединения формулы I заменен/заменены (С 1-С 10)алканоилом,но не ограничиваются ими. Дополнительные примеры заменяющих групп в соответствии с вышеупомянутыми примерами и примеры других типов пролекарств могут быть обнаружены в упомянутых выше ссылках. Кроме того, некоторые соединения формулы I сами могут действовать в качестве пролекарств других соединений формулы I. Кроме того, в объем изобретения включены метаболиты соединений формулы I, то есть, соединения, образующиеся in vivo при введении лекарства. Некоторые примеры метаболитов в соответствии с изобретением включают в себя случаи:(1) когда соединение формулы I содержит метильную группу, ее гидроксиметильное производное(2) когда соединение формулы I содержит алкоксигруппу, ее гидроксипроизводное (-OR - -ОН);(3) когда соединение формулы I содержит третичную аминогруппу, ее вторичное аминопроизводное (-NR1R2 - -NHR1 или -NHR2);(4) когда соединение формулы I содержит вторичную аминогруппу, ее первичное производное(5) когда соединение формулы I содержит фенильную группировку, ее фенольное производное(6) когда соединение формулы I содержит амидную группу, ее производное карбоновой кислоты(-CONH2 - СООН),но не ограничиваются ими. Соединения формулы I, содержащие один или более чем один асимметричный атом углерода, могут существовать в виде двух или более чем двух стереоизомеров. В тех случаях, когда соединение формулы I содержит алкенильную или алкениленовую группу, возможны геометрические цис/транс (илиZ/E) изомеры. В тех случаях, когда структурные изомеры взаимопревращаемы из-за низкого энергетического барьера, может возникать таутомерная изомерия ("таутомерия"). Она может принимать форму протонной таутомерии в соединениях формулы I, содержащих, например имино, кетогруппу или группу оксим, или так называемую валентную таутомерию в соединениях, содержащих ароматическую группировку. Отсюда следует, что одно соединение может демонстрировать более чем один тип изомерии. В объем настоящего изобретение включены все стереоизомеры, геометрические изомеры и тауто-6 011689 мерные формы соединений формулы I, включая соединения, демонстрирующие более чем один тип изомерии, и смеси одного или более чем одного из них. Также включены соли присоединения кислоты или основные соли, в которых противоион является оптически активным, например d-лактат или l-lysine, или рацемическим, например dl-тартрат или dl-аргинин. Цис/транс изомеры могут быть разделены при помощи обычных способов, хорошо известных специалистам в данной области техники, например, при помощи хроматографии и фракционной кристаллизации. Обычные способы получения/выделения индивидуальных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или расщепление рацемата (или рацемата соли или производного) с использованием, например хиральной жидкостной хроматографии высокого давления (ЖХВД). Альтернативно, рацемат (или рацемический предшественник) может быть подвергнут взаимодействию с подходящим оптически активным соединением, например, спиртом, или в случае, когда соединение формулы I содержит кислую или основную группировку, основанием или кислотой, такими как 1 фенилэтиламин или винная кислота. Получающаяся в результате диастереоизомерная смесь может быть разделена путем хроматографии и/или фракционной кристаллизации, и один или оба диастереоизомера могут быть превращены в соответствующие чистые энантиомер(ы) при помощи способов, хорошо известных специалистам в данной области техники. Хиральные соединения по изобретению (и их хиральные предшественники) могут быть получены в энантиомерно-обогащенной форме с использованием хроматографии, обычно ЖХВД, на асимметричной смоле с подвижной фазой, состоящей из углеводорода, обычно гептана или гексана, содержащего от 0 до 50% по объему изопропилового спирта, обычно от 2 до 20% и от 0 до 5% по объему алкиламина, обычно 0,1% диэтиламина. Концентрация элюата дает возможность получить обогащенную смесь. Когда какой-либо рацемат кристаллизуется, возможны кристаллы двух различных типов. Первый тип представляет собой рацемическое соединение (действительный рацемат), упомянутое выше, когда образуется одна гомогенная форма кристалла, содержащая оба энантиомера в эквимолярных количествах. Второй тип представляет собой рацемическую смесь или конгломерат, когда образуются две формы кристаллов в эквимолярных количествах, каждая из которых содержит единичный энантиомер. Несмотря на то, что обе кристаллические формы, присутствующие в рацемической смеси, обладают идентичными физическими свойствами, они могут обладать различными физическими свойствами по сравнению с действительным рацематом. Рацемические смеси могут быть разделены при помощи обычных способов, известных специалистам в данной области техники - смотри, например, Stereochemistry ofOrganic Compounds by E. L. Eliel и S. H. Wilen (Wiley, 1994). Настоящее изобретение включает все фармацевтически приемлемые соединения формулы I, меченные изотопом, где один или более чем один атом заменен атомами, имеющими тот же самый атомный номер, но атомную массу или массовое число, отличающееся от атомной массы или массового числа,преобладающих в природе. Примеры изотопов, подходящих для включения в соединения по изобретению, включают изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такой как 36Cl, фтора, такой как 18F,йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15 О, 17 О и 18 О, фосфора, такой как 32 Р, и серы, такой как 35S, но не ограничиваются ими. Некоторые соединения формулы I, меченные изотопом, например, соединения, включающие радиоактивный изотоп, полезны в исследованиях распределения лекарства и/или субстрата в тканях. Радиоактивные изотопы трития, т.е. 3 Н, и углерода-14, т.е. 14 С, особенно полезны для этой задачи с точки зрения легкости их включения и доступных средств обнаружения. Замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2 Н, может предоставить некоторые терапевтические преимущества, являющиеся результатом большей метаболической стабильности,например увеличенного периода полувыведения in vivo или уменьшенной потребности в дозах, и, следовательно, в некоторых случаях могут быть предпочтительными. Замещение позитронно-активными изотопами, такими как 11 С, 18F, 15O и 13N, может быть полезным в исследованиях путем позитрон-эмиссионной томографии (ПЭТ) для проверки "оккупации" рецептора субстратом. Соединения формулы I, меченные изотопом, обычно могут быть получены при помощи традиционных способов, известных специалистам в данной области техники, или при помощи способов, аналогичных описанным в сопутствующих примерах и получениях с использованием соответствующего реагента,меченного изотопом, вместо ранее используемого немеченого реагента. Фармацевтически приемлемые сольваты по изобретению включают сольваты, в которых растворитель кристаллизации может быть изотопно замещен, например D2O, d6-ацетон, d6-диметилсульфоксид(ДМСО). Кроме того, в объеме изобретения находятся промежуточные соединения формулы II, как определено выше, все их соли, сольваты и комплексы и все сольваты и комплексы их солей, как определено выше для соединений формулы I. Изобретение включает все полиморфы вышеупомянутых видов и их-7 011689 формы кристалла. При получении соединений формулы I по изобретению для специалистов в данной области техники является известным стандартный выбор формы соединения формулы II, которая обеспечивает лучшую комбинацию свойств для достижения этой цели. Такие свойства включают температуру плавления, растворимость, технологичность и выход промежуточной формы и вытекающая в результате легкость, с которым продукт может быть очищен при выделении, но не ограничиваются ими. Один из аспектов настоящего изобретения относится к соединениям формулы I, где А отсутствует или представляет собойZ представляет собой -СН 2, -СН(ОН) или -СН(С 1-С 6 алкил); R1 представляет собой С 1-С 10 алкил, С 6 С 10 арил, 6-10-членный гетероарил или бензо(С 5-С 6 циклоалкил), где, когда R1 представляет собой С 6 С 10 арил, С 6-С 10 гетероарил или бензо(С 5-С 6 циклоалкил), R1 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 6 алкила, галогено, предпочтительно фторо, и ОН; R2 представляет собой Н или С 1-С 6 алкил; R3 представляет собой Н, -CH2CH2SCH3 -О(С 1-С 4) алкил или С 1-С 6 алкил; R4 представляет собой Н или С 1-С 6 алкил; R6 представляет собой Н или С 1 С 6 алкил; R7 представляет собой С 1-С 10 алкил, С 3-С 8 циклоалкил или 4-10-членный гетероциклоалкил, гдеR7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 8 алкила, С 1-С 8 алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех; и каждый из R9, R10 и R11 независимо выбран из Н и С 1-С 6 алкила, где каждый атом водорода указанного С 1-С 6 алкила возможно независимо заменен атомом галогена, предпочтительно атомом фтора. В другом аспекте А отсутствует или представляет собойZ представляет собой -СН 2 или -СН(ОН); R1 представляет собой С 1-С 10 алкил, С 6-С 10 арил или бензо(С 5-С 6 циклоалкил), где, когда R1 представляет собой С 6-С 10 арил или бензо(С 5-С 6 циклоалкил), R1 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогено, предпочтительно фторо; R2 представляет собой Н или C1-С 6 алкил; R3 представляет собой Н или С 1-С 6 алкил; R4 представляет собой Н или C1-С 6 алкил; R6 представляет собой Н или С 1-С 6 алкил; R7 представляет собой С 1-С 10 алкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 8 алкила, С 1-С 8 алкокси,ОН, -NR9R10, -C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила, возможно замещенного группами ОН в количестве от одного до трех; и каждый из R9, R10 и R11 независимо выбран из Н и C1-С 6 алкила,где каждый атом водорода указанного C1-С 6 алкила возможно независимо заменен атомом галогена,предпочтительно атомом фтора. Еще один аспект настоящего изобретения относится к соединениям формулы I, где А отсутствует;R1 представляет собой бензо(С 5-С 6 алкил), возможно замещенный заместителями в количестве от одного до трех, независимо выбранными из C1-С 6 алкила, галогено, предпочтительно фторо, и ОН; R2 представляет собой Н или С 1-С 6 алкил; R3 представляет собой Н или С 1-С 6 алкил; R4 представляет собой Н или C1 С 6 алкил; R6 представляет собой Н или С 1-С 6 алкил; R7 представляет собой C1-С 10 алкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1 С 8 алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11 и -C(=O)OR11. В еще одном аспекте А отсутствует; R1 представляет собой бензо(С 5-С 6 алкил), возможно замещенный заместителями в количестве от одного до трех, независимо выбранными из галогено, предпочтительно фторо; R2 представляет собой Н или C1-С 6 алкил; R3 представляет собой Н, -CH2CH2SCH3, -О(С 1 С 4)алкил или C1-С 6 алкил; R4 представляет собой Н или C1-С 6 алкил; R6 представляет собой Н или С 1 С 6 алкил; R7 представляет собой С 1-С 10 алкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-С 8 алкокси, ОН, -NR9R10, -C(=O)NR9R10,-C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила. В еще одном аспекте R1 представляет собой 1,2,3,4-тетрагидронафталин или инданил, возможно замещенный атомами фтора или хлора в количестве от одного до трех. Еще один аспект настоящего изобретения относится к соединениям формулы I, где А представляет собойZ представляет собой -СН 2, -СН(ОН) или -СН(С 1-С 6 алкил); R1 представляет собой C1-С 10 алкил, С 6 С 10 арил или 6-10-членный гетероарил, где указанные алкил, арил и гетероарил возможно независимо замещены заместителями в количестве от одного до трех, независимо выбранными из С 1-С 6 алкила, галогено, предпочтительно фторо, и ОН; R2 представляет собой Н или С 1-С 6 алкил; R3 представляет собой Н-8 011689 или C1-С 6 алкил; R4 представляет собой Н или C1-С 6 алкил; R6 представляет собой Н или C1-С 6 алкил; R7 представляет собой C1-С 10 алкил, С 3-С 8 циклоалкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 8 алкила, С 1-С 8 алкокси, ОН, -NR9R10, -C(=O)NR9R10, -C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила, возможно замещенного группами ОН или галогено в количестве от одного до трех. В еще одном аспекте А представляет собойZ представляет собой -СН 2 или -СН(ОН); R1 представляет собой C1-С 10 алкил или С 6-С 10 арил, где указанные алкил и арил возможно независимо замещены заместителями в количестве от одного до трех,независимо выбранными из галогено, предпочтительно фторо; R2 представляет собой Н или С 1-С 6 алкил;R3 представляет собой Н или C1-С 6 алкил; R4 представляет собой Н или С 1-С 6 алкил; R6 представляет собой Н или С 1-С 6 алкил; R7 представляет собой C1-С 10 алкил или 4-10-членный гетероциклоалкил, где R7 возможно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из С 1-С 8 алкила, С 1-С 8 алкокси, ОН, -NR9R10, -C(=O)R11, -C(=O)OR11 и 4-6-членного гетероциклоалкила,возможно замещенного группами ОН в количестве от одного до трех. В еще одном аспекте 4-10-членная гетероциклоалкильная группа из R7 представляет собой азетидинил, пирролидинил или пиперидинил; и 4-6-членный гетероциклоалкильный заместитель R7 представляет собой морфолино, пирролидинил или пиперидинил. В еще одном аспекте -R7 представляет собой С 1-С 6 алкил, возможно замещенный -NR9R10, морфолино, пирролидинилом или пиперидинилом. В еще одном аспекте R4 представляет собой Н, и R3 представляет собой метил, этил, бутил, изобутил, пропил, изопропил, -CH2CH2SCH3 или -СН 2 СН 2 ОСН 3. В еще одном аспекте, где R1 представляет собой арил, А представляет собойZ представляет собой -СН 2, и R7 представляет собой С 1-С 6 алкил, возможно замещенный -NR9R10,морфолино, пирролидинилом или пиперидинилом. В еще одном аспекте соединение формулы I имеет следующую структуру, в которой стереохимия заместителей R3 и R4 представлена ниже: В еще одном аспекте в представленной выше стереохимической структуре R4 и R2 представляют собой водород. Конкретные воплощения настоящего изобретения включают следующие соединения формулы I, все их фармацевтически приемлемые соли, их комплексы и их производные, которые после введения превращаются в фармацевтически активное соединение: метиловый эфир 3-(4-2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламиноимидазол-1-ил)масляной кислоты; метиловый эфир 3-4-[2-(2-гидрокси-3-метилбутириламино)пентаноиламино]имидазол-1-ил-3 метилмасляной кислоты; метиловый эфир 3-(4-2-[2-(3,5-дифторфенил)ацетиламино]пентаноиламиноимидазол-1-ил)-3 метилмасляной кислоты; метиловый эфир 3-4-[2-(2-гидрокси-3,3-диметилбутириламино)пентаноиламино]имидазол-1-ил-3 метилмасляной кислоты;[1-(1,1-диметил-2-пирролидин-1-илэтил)-1H-имидазол-4-ил]амид 2-(6,8-дифтор-1-гидрокси-1,2,3,4 тетрагидронафталин-2-иламино)пентановой кислоты. Соединения формулы I по этому изобретению и их фармацевтически приемлемые соли обладают- 13011689 полезными фармацевтическими и медицинскими свойствами. Соединения формулы I и их фармацевтически приемлемые соли ингибируют продукцию А-пептида (таким образом, гамма-секретазную активность) у млекопитающих, включая людей. Следовательно, соединения формулы I и их фармацевтически приемлемые соли способны действовать в качестве терапевтических агентов при лечении нейродегенеративных и/или неврологических расстройств и заболеваний, специально перечисленных ниже, например болезни Альцгеймера, у страдающего от них млекопитающего, включая человека. Настоящее изобретение также относится к фармацевтической композиции для ингибирования продукции А-пептида у млекопитающего, в том числе человека, включающей соединение формулы I или его фармацевтически приемлемую соль в количестве, эффективном для ингибирования А-продукции, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающей соединение формулы I или его фармацевтически приемлемую соль в количестве, эффективном для ингибирования продукции А-пептида, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера и синдрома Дауна у млекопитающего, в том числе человека, включающей соединение формулы I или его фармацевтически приемлемую соль в количестве, эффективном для ингибирования продукции А-пептида, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающей соединение формулы I или его фармацевтически приемлемую соль в количестве, эффективном при лечении такого заболевания или состояния, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера и синдрома Дауна у млекопитающего, в том числе человека, включающей соединение формулы I или его фармацевтически приемлемую соль в количестве, эффективном при лечения такого заболевания или состояния, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу ингибирования продукции А-пептида у млекопитающего, в том числе человека, включающему введение указанному млекопитающему соединения формулы I или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования А-продукции. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного, когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему соединения формулы I или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования А-продукции. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из болезни Альцгеймера и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему соединения формулы I или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования А-продукции. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему соединения формулы I или его фармацевтически приемлемой соли в количестве, эффективном при лечении такого состояния. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из болезни Альцгеймера и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему соединения формулы I или его фармацевтически приемлемой соли в количестве, эффективном при лечении такого состояния. Соединения формулы I можно применять сами по себе или в комбинации с любым другим лекарством, включающим любое средство для улучшения памяти, например Aricept и/или Namenda, антидепрессант, например Zoloft, анксиолитик, антипсихотическое средство, например Geodon, средство отLipitor, Caduet и так далее, антагонист гистамина (Н 2), например Cimetadine, и антигипертензивное средство, например Norvasc, Caduet и так далее, но не ограничивающимся ими. Соответственно, настоящее изобретение также относится к следующим фармацевтическим композициям и способам лечения, включающим соединение формулы I в комбинации с другими лекарствами, такими как имеющие описанный выше тип. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, связанного с продукцией А-пептида у млекопитающего, в том числе человека, включающей (а) соединение формулы I или его фармацевтически приемлемую соль; (б) агент для улучшения памяти, например Aricept и/или Namenda, антидепрессант, например Zoloft, анксиолитик, антипсихотическое средство, например Geodon, средство от расстройства сна, противовоспалительное средство, например Celebrex, Bextra и так далее, антиоксидант, модулятор холестерина (например, агент,уменьшающий LDL или увеличивающий HDL), например Lipitor, Caduet и так далее, антагонист гистамина (Н 2), например Cimetadine, и антигипертензивное средство, например Norvasc, Caduet и так далее; и (в) фармацевтически приемлемый носитель; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающей (а) соединение формулы I или его фармацевтически приемлемую соль; (б) агент для улучшения памяти, например Aricept и/или Namenda, антидепрессант, например Zoloft, анксиолитик, антипсихотическое средство,например Geodon, средство от расстройства сна, противовоспалительное средство, напримерLDL или увеличивающий HDL), например Lipitor, Caduet и так далее, антагонист гистамина (Н 2),например Cimetadine, и антигипертензивное средство, например Norvasc, Caduet и так далее; и (в) фармацевтически приемлемый носитель; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Настоящее изобретение также относится к фармацевтической композиции для лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера и синдрома Дауна у млекопитающего, в том числе человека, включающей (а) соединение формулы I или его фармацевтически приемлемую соль; (б) агент для улучшения памяти, например Aricept и/или Namenda, антидепрессант, например Zoloft, анксиолитик, антипсихотическое средство, например Geodon, средство от расстройства сна, противовоспалительное средство, например Celebrex, Bextra и так далее, антиоксидант, модулятор холестерина (например, агент, уменьшающий LDL или увеличивающий HDL), напримерLipitor, Caduet и так далее, антагонист гистамина (Н 2), например Cimetadine, и антигипертензивное средство, например Norvasc, Caduet и так далее; и (в) фармацевтически приемлемый носитель; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Настоящее изобретение также относится к способу лечения заболевания или состояния, связанного с продукцией А-пептида у млекопитающего, в том числе человека, включающему введение указанному млекопитающему (а) соединения формулы I или его фармацевтически приемлемой соли; и (б) агента для улучшения памяти, например Aricept и/или Namenda, антидепрессанта, например Zoloft, анксиолитика, антипсихотического средства, например Geodon, средства от расстройства сна, противовоспалительного средства, например Celebrex, Bextra и так далее, антиоксиданта, модулятора холестеринаNorvasc, Caduet и так далее; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера, наследственной церебральной геморрагии с амилоидозом, церебральной амилоидной ангиопатии, прионопосредованного заболевания, миозита телец включений, удара, рассеянного склероза, травмы головы, умеренного когнитивного нарушения и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему (а) соединения Формулы I или его фармацевтически приемлемой соли; и (б) агента для улучшения памяти,например Aricept и/или Namenda, антидепрессанта, например Zoloft, анксиолитика, антипсихотического средства, например Geodon, средства от расстройства сна, противовоспалительного средства,- 15011689 например Celebrex, Bextra и так далее, антиоксиданта, модулятора холестерина (например, агента,уменьшающего LDL или увеличивающего HDL), например Lipitor, Caduet и так далее, антагониста гистамина (Н 2), например Cimetadine, и антигипертензивного средства, например Norvasc, Caduet и так далее; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Настоящее изобретение также относится к способу лечения заболевания или состояния, выбранного из группы, состоящей из болезни Альцгеймера и синдрома Дауна, у млекопитающего, в том числе человека, включающему введение указанному млекопитающему (а) соединения формулы I или его фармацевтически приемлемой соли; и (б) агента для улучшения памяти, например Aricept и/или Namenda, антидепрессанта, например Zoloft, анксиолитика, антипсихотического средства, например Geodon,средства от расстройства сна, противовоспалительного средства, например Celebrex, Bextra и так далее, антиоксиданта, модулятора холестерина (например, агента, уменьшающего LDL или увеличивающего HDL), например Lipitor, Caduet и так далее, антагониста гистамина (Н 2), например Cimetadine, и антигипертензивного средства, например Norvasc, Caduet и так далее; где упомянутые выше активные агенты (а) и (б) присутствуют в количествах, которые делают композицию эффективной при лечении такого заболевания или состояния. Соединения формулы I или любые комбинации, описанные в непосредственно предшествующих абзацах, возможно можно применять в сочетании с известным Р-гликопротеиновым ингибитором, таким как верапамил. Ссылки, сделанные здесь на заболевания и состояния, "связанные с продукцией А-пептида" относятся к заболеваниям или состояниям, которые вызваны, по меньшей мере частично, А-пептидом и/или его продукцией. Таким образом, А-пептиды представляет собой фактор, который способствует, не обязательно является единственным способствующим фактором, "заболеванию или состоянию, связанному с продукцией А-пептида". Соединения формулы I или их фармацевтически приемлемые соли также можно применять для модуляции или ингибирования Notch-сигнального пути в организмах, в том числе у людей.Notch-сигнальный путь представляет собой эволюционно консервативный механизм, используемый организмами от червей до людей, для регулирования предопределения ряда поколений различных клеток. Notch относится к семейству гомеотических генов, подобных эпидермальному фактору роста, которые кодируют трансмембранные белки с вариабельным количеством повторов, подобных эпидермальному фактору роста, во внеклеточном домене. Очевидность роли Notch-пути при заболевании людей возрастает. Еще не все компоненты пути идентифицированы, но среди идентифицированных до настоящего времени мутации, которые влияют на их взаимодействие друг с другом, могут приводить к множеству синдромов и патологических состояний. Например, Notch-передача сигнала обычно связана с определением судьбы клеток. Данные, чтоNotch-активация стимулирует рост капилляров, свидетельствуют о том, что Notch-рецепторы должны быть активированы для того, чтобы этот процесс мог происходить. Таким образом, Notch-модуляция представляет собой способ регулирования ангиогенеза. Конкретно, модуляцию Notch-передачи сигнала можно применять для модуляции ангиогенеза (например, путем блокирования Notch-передачи сигнала пути для блокирования ангиогенеза). Это ингибирование ангиогенеза in vivo можно применять в качестве терапевтического средства лечения множества заболеваний, включая рак, диабетическую ретинопатию, ревматоидный артрит, псориаз, воспалительное заболевание кишечника и атеросклероз, но не ограничиваясь ими.Nothc-путь также вовлечен в развитие и созревание Т-клеток, как описано Radtke, F. et al. в Immunity 10:547-558, 1999. Следовательно, соединения формулы I и их фармацевтически приемлемые соли представляют собой полезные кандидаты для модуляции иммунной системы, включающей лечение воспаления, астмы, отторжения трансплантата, болезни "трансплантат против хозяина", аутоиммунного заболевания и отторжения ткани или органа. Кроме того, множество исследований, опубликованных между 2002 и 2004, годами предоставили убедительное доказательство того, что Notch-передача сигнала часто увеличивается при различных опухолях у людей (включая опухоли молочной железы, предстательной железы, поджелудочной железы и Тклеточную острую лимфобластную лейкемию, но не ограничиваясь ими). В одном из ключевых исследований представлена сильная генетическая связь Notch-роли по отношению к важным типам опухолей. Конкретно, Weijzen et al. продемонстрировали, что Notch-передача сигнала поддерживает неопластический фенотип в клетках человека, трансформированных Ras (Weijzen et al., 2002, Nature Med 8: 979). Поскольку 30% злокачественностей человека могут нести активирующие мутации в по меньшей мере одной из трех изоформ Ras, это открытие увеличивает возможность того, что Notch-ингибиторы могут быть мощным дополнением к противораковой терапии. Данные другого исследования подтверждают центральную роль аберрантной Notch-передачи сигнала пути в патогенезе Т-клеточной острой лимфобластной лейкемии/лимфомы у человека (Pear et al., Current Opinion in Hematology (2004), 11(6), 426-433). Соответственно, соединения формулы I или их фармацевтически приемлемые соли можно приме- 16011689 нять для лечения заболевания или состояния, выбранного из группы, состоящей из рака, атеросклероза,диабетической ретинопатии, ревматоидного артрита, псориаза, воспалительного заболевания кишечника,астмы, отторжения трансплантата, болезни "трансплантат против хозяина", аутоиммунного заболевания и отторжения ткани или органа. Используемый здесь термин "лечение" относится к реверсированию, облегчению или ингибированию прогрессирования заболевания, расстройства или состояния, или одного или более чем одного симптома такого заболевания, расстройства или состояния, к которым такой термин применяется. Используемый здесь термин "лечение" также может относиться к уменьшению вероятности или степени возникновения заболевания, расстройства или состояния у млекопитающего по сравнению с не подвергнутой лечению контрольной популяцией или по сравнению с тем же самым млекопитающим перед лечением. Например, используемый здесь термин "лечение" может относиться к предотвращению заболевания,расстройства или состояния и может включать замедление или предотвращение начала заболевания, расстройства или состояния, или замедление или предотвращение симптомов, связанных с заболеванием,расстройством или состоянием. Используемый здесь термин "лечение" также может относиться к уменьшению тяжести заболевания, расстройства или состояния, или симптомов, связанных с таким заболеванием, расстройством или состоянием, перед тем, как млекопитающее начнет страдать от заболевания, расстройства или состояния. Такое предотвращение или уменьшение тяжести заболевания, расстройства или состояния "перед страданием" относится к введению композиции по настоящему изобретению, как описано здесь, субъекту, который на момент введения не страдает от заболевания, расстройства или состояния. Используемый здесь термин "лечение" также может относиться к предотвращению рецидива заболевания, расстройства или состояния, или одного или более чем одного симптома, связанного с таким заболеванием, расстройством или состоянием. Используемые здесь термины "лечение" и"терапевтически" относятся к акту лечения, определенного выше. Подробное описание изобретения Соединения формулы I и их фармацевтически приемлемые соли могут быть получены, как изображено на следующих схемах реакций и описано в обсуждении. Если не указано иначе, на следующих схемах реакций и в обсуждении R1, R2, R3, R4, R6, R7, R8, R9, R10, R11, A, Z и n являются такими, как определено выше. Соединения формулы I могут иметь асимметричные атомы углерода и поэтому могут существовать в виде рацемических смесей, диастереоизомеров или индивидуальных оптических изомеров. Разделение смеси изомеров соединений формулы I на отдельные изомеры может быть осуществлено в соответствии с общепринятыми способами, известными в области техники. Соединения формулы I могут быть получены при помощи способов, описанных ниже, вместе со способами синтеза, известными в области органической химии, или при помощи модификаций и вариантов получения производных, которые знакомы специалистам в данной области техники. Предпочтительные способы включают способы, описанные ниже, но не ограничиваются ими. Описанные ниже реакции проводят в растворителях, которые соответствуют используемым реагентам и материалам, и которые подходят для применения в описанных реакциях. Также следует понимать,что в приведенном ниже описании способов синтеза все условия реакции, действительные или предполагаемые, включающие выбор растворителя, температуру реакции, продолжительность реакции, давление в реакции и другие условия реакции (такие как безводные условия, в атмосфере аргона, в атмосфере азота и т.д.) и способы обработки представляют собой условия, которые являются стандартными для этой реакции, что будет легко установлено специалистами в данной области техники. Также могут быть использованы альтернативные способы. Соединения формулы II, где R7 содержит спиртовую группировку, могут быть окислены с использованием стандартного способа окисления, известного в области техники, такого как, например, с использованием реагентов Десс-Мартина, окисления Сверна или применения SO3-пиридина, CrO3, с получением соединения формулы II, где R7 содержит кетон или альдегид. Соединения формулы II, где R7 представляет собой кетон или альдегид, могут быть превращены в соответствующие соединения формулы II, где R7 представляет собой имин (взаимодействием с амином), олефин (путем реакции Виттига),спирт (путем реакции Гриньяра) или другое производное (при помощи стандартных реакций). Соединения формулы I по настоящему изобретению и их соли могут быть получены способом,включающим в себя взаимодействие соединения формулы II или взаимодействие соединения формулы IV где R1, R3, R4, R6, R7 и А являются такими, как определено выше, и L представляет собой гидроксигруппу или подходящую уходящую группу. Если желательно, 4-аминоимидазольное производное формулы I или синтетическое промежуточное соединение формулы IV может быть превращено в соль с использованием способов, известных специалистам в данной области техники. Примеры конкретных соединений формулы III и V, где L представляет собой гидроксигруппу или подходящую уходящую группу, представляют собой соединения, где L представляет собой атом галогена, такой как Cl, Вr или I, или A-L представляет собой алкиловый или ариловый эфир. Соединения формулы I могут быть получены взаимодействием соединения формулы II и карбоновой кислоты формулы III, или соединения формулы IV с соединением формулы V. Соединения формулыIV могут быть получены взаимодействием соединения формулы II с соединением формулы VI. Реакция между соединениями формулы II и соединениями формулы III, между соединениями формулы IV и соединениями формулы V, и между соединениями формулы II и соединениями формулы VI,может быть осуществлена с использованием стандартных способов. Например, если L представляет собой гидроксильную группу, то эти реакции можно проводить в присутствии агента сочетания или агента сочетания, связанного с полимером, такого как, например карбодиимид, то есть 1,3-дициклогексилкарбодиимид (DCC), 1,3-диизопропилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид(EDC), N-циклогексилкарбодиимид, или N'-метилполистирол, в присутствии или отсутствии 1 гидроксибензотриазола (HOBt), в подходящем растворителе, таком как, например один растворитель или комбинация нескольких растворителей, выбранных из дихлорметана (CH2Cl2), хлороформа (CHCl3), тетрагидрофурана (ТГФ), диэтилового эфира (Et2O), 1,4-диоксана, ацетонитрила (CH3CN), толуола, N,Nдиметилформамида (ДМФ) или диметилсульфоксида (ДМСО), при подходящей температуре, такой как приблизительно от -10 С до температуры дефлегмации, в течение подходящего периода времени, с контролем путем хроматографии или жидкостной хроматографии/масс-спектрометрии (ЖХ-МС). Альтернативный способ, где L представляет собой ОН, осуществляют путем превращения ОН в уходящую группу в результате взаимодействия с оксалилхлоридом, тионилхлоридом или смешанным ангидридом, с использованием алкилхлорформиата, такого как С 1-С 4 алкилхлорформиат, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин или диметиламинопиридин, в подходящем растворителе, таком как, например метиленхлорид, хлороформ, тетрагидрофуран (ТГФ), толуол, диэтиловый эфир, ацетонитрил, 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид (ДМСО), N-метилпирролидинон (NMP) или ксилол, при температуре приблизительно от -30 С до комнатной температуры. Альтернативно, аминоимидазольное сочетание может быть достигнуто следующим образом. Соединение формулы I может быть получено путем сочетания аминоимидазола II с III, где C(=O)L представляет собой сложный эфир, в присутствии триалкилалюминия, предпочтительно триметилалюминия,в подходящем растворителе, таком как метиленхлорид, ТГФ, диоксан, толуол, и т.д., при соответствующей температуре, такой как приблизительно от комнатной температуры до температуры дефлегмации,или в закрытом реакторе (таком как закрытая пробирка или завинчивающиеся виалы). Аналогично, соединение IV может быть получено путем взаимодействия аминоимидазола II, триметилалюминия и Nбутилоксикарбонила (N-Boc) из сложного эфира альфа-аминокислоты, с последующим удалением группы Boc с использованием стандартных способов. Защищенные аминосоединения формулы VI, где Р 1 представляет собой блокирующую группу, такую как группа N-Boc, могут быть получены с использованием способов, хорошо известных в литературе, например с использованием способов, описанных в книге Theodora W. Greene "Protective Groups inOrganic Synthesis". Соединения формулы IV могут быть получены с использованием способа, аналогичного приведенному выше: путем взаимодействия соединения формулы II с соединением формулы VI с последующим удалением блокировки группы Р 1. Снятие защиты может быть осуществлено хорошо из- 18011689 вестными способами, например, когда Р 1 представляет собой N-Boc, то удаление осуществляют любым из способов, хорошо известных в литературе, например HCl (г) в соответствующем растворителе, таком как 1,4-диоксан, диэтиловый эфир или трифторуксусная кислота в метиленхлориде. Известно и также может быть использовано множество других аминозащитных групп, таких как бензил или параметоксибензил, триметилсилил, трет-бутилдиметилсилил и т.д. Способы удаления блокировки таких групп хорошо известны в литературе и могут быть использованы. Соединения формулы II, III, IV, V и VI в некоторых случаях представляют собой известные соединения или могут быть получены в соответствии со способами, хорошо известными специалистам в данной области техники. Соединения формулы III и V, где L представляют собой уходящую группу, как определено выше,могут быть получены в соответствии с обычными способами из соответствующих карбоновых кислот формулы III, где X представляет собой гидрокси. Соединения формулы IV могут быть получены путем взаимодействия соединения формулы II с соединением формулы V с использованием известных способов. Сложноэфирная группа R7 в соединениях формулы I или II может быть превращена в соответствующий амид с использованием способа, похожего на способ для образования амидной связи, предпочтительно с использованием триметилалюминия в соответствующем растворителе или смеси растворителей, такой как ТГФ/толуол. Кетогруппа R7 в соединениях формулы I или II может быть превращена в соответствующий амин с использованием традиционного способа восстановительного аминирования путем взаимодействия такого кетона с соответствующим амином с кислым катализатором/ацетатом аммония/осушителями (такими как безводные Na2SO4 или MgSO4) или без них, и восстановителем, таким как триацетоксиборгидрид натрия, цианоборгидрид натрия или боргидрид натрия, или соответствующим связанным с полимеромNaBH4, связанным с полимером-NaBH3CN или связанным с полимером-NaB(OAc)3H, или любым восстановителем (например, гидрирование), известным в литературе для восстановления иминной связи до амина, в подходящем растворителе, таком как дихлорэтан, хлороформ, ТГФ, МеОН, этанол, изопропиловый спирт, трет-бутиловый спирт или толуол, при температуре приблизительно от комнатной температуры до температуры дефлегмации, предпочтительно приблизительно от комнатной температуры до 65 С. Соединения, где R6 представляет собой группу галогено, могут быть получены взаимодействием исходного вещества, где R6 представляет собой Н, с NBS (N-бромсукцинамидом), NCS (N-хлорсукцинамидом) или SO2Cl2, I2 в подходящем растворителе, таком как метиленхлорид, четыреххлористый углерод или хлороформ. Галогеногруппа затем может быть заменена другой группой с использованием способов, известных в области техники, таких как обмен галоген-металл с последующим гашением электрофилом или в типичных условиях сочетания Сузуки с использованием катализатора, такого как палладиевый комплекс, например тетракис(трифенилфосфин)палладий, с карбонатом натрия в качестве основания, в подходящем растворителе, таком как ТГФ, диметиловый эфир (ДМЭ) или этанол, и бороновой кислоты. 4-Аминоимидазол II может быть получен с использованием следующих способов, известных в химической литературе (например, Tetrahedron, 1995, 51, 2875-2894; J. Chem. Soc. Perkin, 1, 1987, 28192828; Bull. Chem. Soc. Fr., 1994, 131, 200-209; Tetrahedron Lett., 1996, 4423-4426; Tetrahedron, 1996, 37,4423-4426; Tetrahedron, 1994, 50, 5741-5752; Heterocycles, 1994, 37, 1511-1520; Tetrahedron Lett., 1999,1623-1626; Organic Lett., 2002, 4, 4133-4134; Organic Lett., 2000, 2, 1233-1236; J. Med. Chem., 1990, 33,1091-1097; или при помощи способов, описанных ниже. На схеме 1 представлены способы, подходящие для получения аминоимидазольных соединений формулы I. Со ссылкой на схему 1 обработка раствора 1,4-динитроимидазола (J. Phys. Chem. (1995) Vol. 99, pp. 5009-5015) в диметилсульфоксиде (ДМСО), в системе растворителей пиридин-вода, в воде, спирте или в системе растворителей спирт-вода, но предпочтительно в низшем спирте, таком как метанол, при температуре приблизительно от -20 до 50 С, предпочтительно приблизительно от -5 до 35 С, первичным алкил- или ариламином (NR9R10) позволяет получить 1-N-замещенные-4-нитроимидазолы формулы 2 А. 1,4-Динитроимидазол представляет собой высокоэнергетическое, полустабильное вещество, и все время,когда оно не используется, должно храниться в холодильнике. Термодинамические измерения продемонстрировали, что потенциально оно может образовывать достаточно энергии при 35 С в адиабатических условиях для сильного взрыва. Следует быть чрезвычайно внимательными все время при использовании этого вещества. Восстановление нитросоединения формулы 2 А до амина формулы 3 А может быть осуществлено путем воздействия на смесь соединения формулы 2 А и катализатора из благородного металла в растворителе, таком как этилацетат, тетрагидрофуран, диоксан или их смесь, атмосферы газообразного водорода при давлении приблизительно от 101 до 10100 кПа (от 1 до 100 атмосфер), где предпочтитель- 19011689 ное давление газообразного водорода составляет приблизительно от 101 до 1010 кПа (от одной до десяти атмосфер). Палладий представляет собой предпочтительный катализатор из благородного металла. Металл может быть легко суспендирован на инертном твердом носителе, таком как древесный уголь, и отфильтрован для получения амина формулы 3 А. Альтернативно, превращение нитрогруппы формулы 2 А в амин формулы 3 А может быть осуществлено путем воздействия на смесь соединения формулы 2 А смеси цинк/HCl или железо/HCl, или NaBH4/NiCl2, или NaBH2S3. Образовавшийся амин формулы 3 А сразу же подвергают взаимодействию с хлорангидридом, ангидридом кислоты или активированным производным карбоновой кислоты (определенным формулойIII), в присутствии основания, такого как триэтиламин, диизопропилэтиламин, пиридин или 2,6-лутидин,при температуре приблизительно от -78 до 40 С. Взаимодействие между соединениями формулы 3 А и соединениями формулы III может быть осуществлено с использованием стандартных способов. Например, если L формулы III представляет собой гидроксильную группу, то эти реакции можно проводить в присутствии агента сочетания или агента сочетания, связанного с полимером, такого как, например, карбодиимид, то есть 1,3-дициклогексилкарбодиимид (DCC), 1,3-диизопропилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид (EDC), N-циклогексилкарбодиимид или N'-метилполистирол, в присутствии или отсутствии HOBt, в подходящем растворителе, таком как, например один растворитель или комбинация нескольких растворителей, выбранных из дихлорметана (CH2Cl2), хлороформа (CHCl3), тетрагидрофурана (ТГФ), диэтилового эфира (Et2O), 1,4-диоксана, ацетонитрила (CH3CN), толуола, N,Nдиметилформамида (ДМФ) или диметилсульфоксида (ДМСО), при подходящей температуре, такой как приблизительно от -10 С до температуры дефлегмации, в течение подходящего периода времени, с контролем путем хроматографии или ЖХ-МС. Альтернативный способ, где L представляет собой ОН, осуществляют путем превращения ОН в уходящую группу в результате взаимодействия с оксалилхлоридом,тионилхлоридом или смешанным ангидридом, с использованием алкилхлорформиата, такого как С 1 С 4 алкилхлорформиат, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин,пиридин или диметиламинопиридин, в подходящем растворителе, таком как, например метиленхлорид,хлороформ, тетрагидрофуран (ТГФ), толуол, диэтиловый эфир, ацетонитрил, 1,4-диоксан, N,Nдиметилформамид, диметилсульфоксид (ДМСО), N-метилпирролидинон (NMP) или ксилол, при температуре приблизительно от -30 С до комнатной температуры. Альтернативно, аминоимидазольное сочетание может быть достигнуто следующим образом. Соединение формулы I может быть получено путем сочетания аминоимидазола 3 А с соединением формулыIII, где C(=О)L представляет собой сложный эфир, в присутствии триалкилалюминия, предпочтительно триметилалюминия, в подходящем растворителе, таком как метиленхлорид, ТГФ, диоксан, толуол и т.д.,при соответствующей температуре, такой как приблизительно от комнатной температуры до температуры дефлегмации, или в закрытом реакторе (таком как закрытая пробирка или завинчивающиеся виалы). Альтернативно, образовавшийся амин формулы 3 А сразу же подвергают взаимодействию с хлорангидридом, ангидридом кислоты или активированным производным карбоновой кислоты (определенным формулой IV) в присутствии основания, такого как триэтиламин, диизопропилэтиламин, пиридин или 2,6-лутидин, при температуре приблизительно от -78 до 40 С с получением соединения формулы 4 А. Взаимодействие между соединениями формулы 3 А и соединениями формулы IV может быть осуществлено с использованием стандартных способов. Например, если L формулы IV представляет собой гидроксильную группу, то эти реакции можно проводить в присутствии агента сочетания или агента сочетания, связанного с полимером, такого как, например карбодиимид, то есть 1,3-дициклогексилкарбодиимид (DCC), 1,3-диизопропилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид(EDC), N-циклогексилкарбодиимид или N'-метилполистирол, в присутствии или отсутствии HOBt, в подходящем растворителе, таком как, например один растворитель или комбинация нескольких растворителей, выбранных из дихлорметана (CH2Cl2), хлороформа (CHCl3), тетрагидрофурана (ТГФ), диэтилового эфира (Et2O), 1,4-диоксана, ацетонитрила (CH3CN), толуола, N,N-диметилформамида (ДМФ) или диметилсульфоксида (ДМСО), при подходящей температуре, такой как приблизительно от -10 С до температуры дефлегмации, в течение подходящего периода времени, с контролем путем хроматографии или ЖХ-МС. Альтернативный способ, где L представляет собой ОН, осуществляют путем превращения ОН в уходящую группу в результате взаимодействия с оксалилхлоридом, тионилхлоридом или смешанным ангидридом, с использованием алкилхлорформиата, такого как С 1-С 4 алкилхлорформиат, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин или диметиламинопиридин, в подходящем растворителе, таком как, например метиленхлорид, хлороформ, тетрагидрофуран (ТГФ),толуол, диэтиловый эфир, ацетонитрил, 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид(ДМСО), N-метилпирролидинон (NMP) или ксилол, при температуре приблизительно от -30 С до комнатной температуры. Альтернативно, аминоимидазольное сочетание может быть достигнуто следующим образом. Соединение формулы 4 А может быть получено путем сочетания аминоимидазола 3 А с соединением формулы IV, где C(=O)L представляет собой сложный эфир, в присутствии триалкилалюминия, предпочтительно триметилалюминия, в подходящем растворителе, таком как метиленхлорид, ТГФ, диоксан, толу- 20011689 ол, и т.д., при соответствующей температуре, такой как приблизительно от комнатной температуры до температуры дефлегмации, или в закрытом реакторе (таком как закрытая пробирка или завинчивающиеся виалы). Защищенные аминосоединения, определенные как PG, такие как соединение с группой Boc формулы IV, могут быть получены с использованием способов, хорошо известных в литературе, например с использованием способов, описанных в книге Theodora W. Greene "Protective Groups in OrganicSynthesis". Соединения, определенные формулой 5 А, могут быть получены из соединений формулы 4 А путем удаления блокировки группы PG. Снятие защиты может быть осуществлено хорошо известными способами, например, когда PG представляет собой N-Boc, то удаление осуществляют любым из способов,хорошо известных в литературе, например HCl (г) в соответствующем растворителе, таком как 1,4 диоксан, диэтиловый эфир или трифторуксусная кислота в метиленхлориде. Известно и также может быть использовано множество других аминозащитных групп, таких как бензил или пара-метокси-бензил,триметилсилил, трет-бутилдиметилсилил и т.д. Способы удаления блокировки таких групп хорошо известны в литературе и могут быть использованы. Соединения формулы I могут быть получены путем взаимодействия между соединениями формулы 5A и соединениями формулы V с использованием стандартных способов. Например, если L представляет собой гидроксильную группу, то эти реакции можно проводить в присутствии агента сочетания или агента сочетания, связанного с полимером, такого как, например, карбодиимид, то есть 1,3-дициклогексилкарбодиимид (DCC), 1,3-диизопропилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид (EDC), N-циклогексилкарбодиимид или N'-метилполистирол, в присутствии или отсутствииHOBt, в подходящем растворителе, таком как, например один растворитель или комбинация нескольких растворителей, выбранных из дихлорметана (CH2Cl2), хлороформа (CHCl3), тетрагидрофурана (ТГФ),диэтилового эфира (Et2O), 1,4-диоксана, ацетонитрила (CH3CN), толуола, N,N-диметилформамида(ДМФ) или диметилсульфоксида (ДМСО), при подходящей температуре, такой как приблизительно от-10 С до температуры дефлегмации, в течение подходящего периода времени, с контролем путем хроматографии или ЖХ-МС. Альтернативный способ, где L представляет собой ОН, осуществляют путем превращения ОН в уходящую группу в результате взаимодействия с оксалилхлоридом, тионилхлоридом или смешанным ангидридом, с использованием алкилхлорформиата, такого как С 1-С 4 алкилхлорформиат, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин или диметиламинопиридин, в подходящем растворителе, таком как, например метиленхлорид, хлороформ, тетрагидрофуран (ТГФ),толуол, диэтиловый эфир, ацетонитрил, 1,4-диоксан, N,N-диметилформамид; диметилсульфоксид(ДМСО), N-метилпирролидинон (NMP) или ксилол, при температуре приблизительно от -30 С до комнатной температуры. Соединение формулы I может быть получено путем сочетания аминоимидазола 5 А с V, где L представляет собой сложный эфир, в присутствии триалкилалюминия, предпочтительно триметилалюминия,в подходящем растворителе, таком как метиленхлорид, ТГФ, диоксан, толуол, и т.д., при соответствующей температуре, такой как приблизительно от комнатной температуры до температуры дефлегмации,или в закрытом реакторе (таком как закрытая пробирка или завинчивающиеся виалы). Альтернативно, соединения формулы I могут быть получены путем взаимодействия между соединениями формулы 5A и соединениями формулы V, где L представляет собой альдегид или кетон, с использованием традиционного способа восстановительного аминирования путем взаимодействия такого кетона с соответствующим амином 5 А с кислым катализатором/ацетатом аммония/осушителями (такими как безводные Na2SO4 или MgSO4) или без них, и восстановителем, таким как триацетоксиборгидрид натрия, цианоборгидрид натрия или боргидрид натрия, или соответствующим связанным с полимеромNaBH4, связанным с полимером-NaBH3CN или связанным с полимером-NaB(OAc)3H, или любым восстановителем (например, гидрирование), известным в литературе для восстановления иминной связи до амина, в подходящем растворителе, таким как дихлорэтан, хлороформ, ТГФ, МеОН, этанол, изопропиловый спирт, трет-бутиловый спирт или толуол, при температуре приблизительно от комнатной температуры до температуры дефлегмации, предпочтительно приблизительно от комнатной температуры до 65 С. На схеме 2 представлены дополнительные способы синтеза имидазольных соединений, определенных формулой 2 А. Обработка нитроимидазола 6 А основанием, таким как гидрид натрия, гидрид калия,алкиллитий, алкоксиды, в растворителе, таком как тетрагидрофуран, диметилформамид, метиленхлорид,простой эфир, предпочтительно диметилформамид, приблизительно от -60 до 40 С, где от -10 до 20 С является предпочтительным, с последующим добавлением R7-X, где X определен как Cl, Br, I, F, алкилсульфонат или арилсульфонат с последующим нагреванием реакционной смеси от 23 до 150 С, где 3080 С является предпочтительным, позволяет получить имидазолы формулы 2 А. Восстановление нитросоединения и реакцию сочетания проводят подобно описанному выше и используют для получения соединения формулы I. Схема 2 На схеме 3 представлены дополнительные способы синтеза нитроимидазольных соединений, определенных формулой 2 А. Ключевое исходное вещество для синтеза представляет собой соединение с двойной связью (соединение формулы 16 или 17), замещенное группой ER8 и группами в количестве от одного до трех, выбранными из R8, где ER8 определена как группа, отнимающая электроны, выбранная из C(=O)R9, C(=O)OR9, C(=O)NR9R10, S(=O)2R9, S(=O)2NR9R10, S(=O)2OR9, циано и гетероарила. Дополнительно, соединения формулы 16 или 17 могут быть определены следующим образом: где ER8 связана с одной из групп R8 или непосредственно с углерод-углеродной двойной связью с образованием кольца,и таким образом включают такие соединения, как 2-циклопентен-1-он и 2-циклогексен-1-он. Альтернативно, соединения формулы 17, где L определен как Cl, Br, I, OC(=O)R9 или OS(=O)2R9, могут быть использованы в качестве исходных веществ; примеры таких соединений представляют собой 3-хлор-1 циклопентанон, 3-ацетокси-1-циклобутанон. Таким образом, со ссылкой на схему 3, обработка 4 нитроимидазола 6 А основанием, таким как гидрид натрия, гидрид калия, карбонат цезия, 1,8 диазабицикло[5.4.0]ундец-7-ен (DBU) или хлорид тетраалкиламмония, где DBU представляет собой предпочтительное основание, промежуточными соединениями 16 или 17 в растворителе, таком как ацетонитрил, метиленхлорид, 1,2-дихлорэтан или хлороформ, где ацетонитрил представляет собой предпочтительный растворитель, при температуре приблизительно от -60 до 50 С, где предпочтительный диапазон представляет собой от -20 до 23 С, позволяет получить продукты присоединения формулы 2 А. Вос- 22011689 становление нитросоединения и сочетание с получением соединения формулы I осуществляют подобно описанному выше. Схема 3 На схеме 4 ниже представлены дополнительные способы синтеза аминоимидазольных соединений,определенных формулой 2 А. Обработка этил-2-изоциано-3-N,N-диметиламиноакрилата или бензил-2 изоциано-3-N,N-диметиламиноакрилата первичным амином, R7-NH2, в растворителе, таком как нбутанол, н-пропиловый спирт, i-пропиловый спирт или этанол, или при отсутствии растворителя, где предпочтительны н-пропиловый спирт или отсутствие растворителя, приблизительно от 23 до200 С, где предпочтительна температура приблизительно от 60 до 150 С, позволяет получить имидазолы формулы 18. Обработка сложного эфира 18 основанием, таким как гидроксид калия, гидроксид лития или гидроксид натрия, в растворителе, таком как тетрагидрофуран, вода, метанол, этанол, пропанол, где предпочтителен метанол, позволяет получить кислоту 19. Кислоту превращают в ацилазид 20 с использованием способов, известных специалистам в данной области техники, таких как обработка кислоты 19 тионилхлоридом или оксалилхлоридом при температуре от -20 до 50 С с последующим удалением оставшегося растворителя и гашения азидом натрия или калия в растворителе, таком как толуол, тетрагидрофуран,метиленхлорид, диоксан. Азид 20 подвергают перегруппировке Куртиуса до Boc 21 путем нагревания от 5-200 С в растворителе, таком как тpeт-бутиловый спирт, бензиловый спирт и этанол. Если используют трет-бутиловый спирт, то удаление защитной группы N-Boc может быть осуществлено с использованиемHCl или трифторуксусной кислоты в растворителе, таком как простой эфир, тетрагидрофуран, где предпочтителен HCl в метаноле, с получением желаемых аминоимидазольных соединений формулы 2 А. Если используют бензиловый спирт, то удаление защиты может быть осуществлено путем применения катализатора из благородного металла в растворителе, таком как этилацетат, тетрагидрофуран, диоксан или их смесь, и атмосферы газообразного водорода при давлении приблизительно от 101 до 10100 кПа (от 1 до 100 атм), где предпочтительное давление газообразного водорода составляет приблизительно от 101 до 1010 кПа (от одной до десяти атмосфер). Палладий представляет собой предпочтительный катализатор из благородного металла, который позволяет получить желаемые аминоимидазольные соединения формулы 2 А. Альтернативно, сложный эфир 18 может быть обработан гидразином в растворителе, таком как вода, при температуре от 50 до 200 С, где предпочтительна температура от 80 до 120 С, с получением гидразида 22. Гидразид 22 может быть превращен в ацилазид 20 с использованием трет-бутил нитрита в растворителе или комбинации растворителей, таких как простой эфир, метиленхлорид, дихлорэтан,хлороформ, где предпочтительна комбинация простой эфир/метиленхлорид, при температуре от -50 до 23 С, где предпочтительна температура от -30 до 10 С. Ацилазид затем превращают в аминоимидазольные соединения формулы 2 А в соответствии с описанным выше. Делают изменение до схемы 4. На схеме 5 ниже представлены дополнительные способы синтеза аминоимидазольных соединений,определенных формулой I. Обработка гидрохлорида N-O-диметилгидроксиламина триметилалюминием в 1,2-дихлорэтане с последующим добавлением сложного эфира 18, полученного как описано выше, и нагреванием при приблизительно от 30 до 80 С, где предпочтительно температура приблизительно 50 С,позволяет получить имидазол 23. Добавление металлоорганического реагента 24, где Z определен как галогенид лития, галогенид магния, галогенид калия, где предпочтителен галогенид лития, к раствору амида 23 в растворителе, таком как тетрагидрофуран, метиленхлорид или диэтиловый эфир, при температуре приблизительно от -78 до 30 С, где предпочтителен диапазон приблизительно от -20 до 0 С, позволяет получить 25. Добавление 25 к смеси гидрохлорида гидроксиламина и ацетата калия в низшем спиртовом растворителе, где предпочтителен этанол, приблизительно при 23 С, приводит к оксиму 26 в виде смеси изомеров. Обработка ацетонового раствора оксима 26 приблизительно при 0 С водным гидроксидом, а затем паратолуолсульфонилхлоридом приводит после экстракции к смеси О-сульфонильного соединения. Растворение неочищенного вещества в неполярном растворителе, таком как бензол,гексаны или толуол, где предпочтителен бензол, и нанесение на колонку с оксидом алюминия с последующим элюированием смесью хлороформ-метанол (приблизительно 10:1) приблизительно через пять минут позволяет получить соединение формулы I. Схема 5 На схеме 6 представлены способы, подходящие для получения аминоимидазольных соединений формулы I. Соединение формулы I, 27 может быть получено с использованием описанных выше способов. Превращение сложного эфира I, 27 в спирт соединений I, 28 может быть осуществлено путем обработки сложного эфира I, 27. Соединения формулы I, 28 могут быть окислены с использованием стандартного способа окисления, известного в области техники, такого как, например, с использованием реагентов Десс-Мартина, окисления Сверна или применения SO3-пиридина, CrO3, где предпочтительно окисление Сверна, с получением соединений, содержащих альдегид. Альдегид может быть превращен в соединения формулы I, 29 с использованием традиционного способа восстановительного аминирования путем взаимодействия альдегида с соответствующим амином 5 А с кислым катализатором/ацетатом аммония/осушителями (такими как безводные Na2SO4 или MgSO4) или без них, и восстановителем, таким как триацетоксиборгидрид натрия, цианоборгидрид натрия или боргидрид натрия, или соответствующим- 24011689 связанным с полимером-NaBH4, связанным с полимером-NaBH3CN или связанным с полимеромNaB(OAc)3H, или любым восстановителем (например гидрирование), известным в литературе для восстановления иминной связи до амина, в подходящем растворителе, таком как дихлорэтан, хлороформ,ТГФ, МеОН, этанол, изопропиловый спирт, трет-бутиловый спирт или толуол, при температуре приблизительно от комнатной температуры до температуры дефлегмации, предпочтительно приблизительно от комнатной температуры до 65 С. Альтернативно, спирт I, 28 может быть превращен в соответствующий алкил- или арилсульфонат путем обработки спирта алкил- или арилсульфонилхлоридом (где предпочтителен мезилхлорид) в растворителе, таком как метиленхлорид, тетрагидрофуран, толуол, где предпочтителен метиленхлорид, в присутствии амида, такого как триэтиламин, диизопропиламин, пиридин, 2,6 лутидин, где предпочтителен триэтиламин, при температуре от -50 до 23 С, где предпочтительна температура от 0 до 30 С. Арил- или алкилсульфонат затем подвергают взаимодействию с азидом щелочного металла (где предпочтителен азид натрия), в полярном растворителе, таком как диметилформамид, диметилсульфоксид, спирт, где предпочтителен этанол, с получением соединения, содержащего азид. Этот промежуточный азид может быть восстановлен путем воздействия на азид катализатора благородного металла, в растворителе, таком как этилацетат, тетрагидрофуран, диоксан или их смесь, и атмосферы газообразного водорода при давлении приблизительно от 101 до 10100 кПа (от 1 до 100 атмосфер), где предпочтительное давление газообразного водорода составляет приблизительно от 101 до 1010 кПа (от одной до десяти атмосфер). Палладий представляет собой предпочтительный катализатор из благородного металла, и реакция позволяет получить аминогруппу. Аминогруппа затем может быть превращена до соединений формулы I, 29 с использованием описанных выше условий восстановительного аминирования. Схема 6 Со ссылкой на схему 7 обработка раствора бромимидазола 30 основанием, таким как гидрид натрия, гидрид калия, гидрид лития, карбонат цезия, гидроксид натрия, гидроксид калия, гидроксид цезия,диизопропиламид лития, амид натрия, гексаметилдисилазид калия, гексаметилдисилазид натрия, третбутоксид натрия или трет-бутоксид калия, в реакционно-инертном растворителе, таком как тетрагидрофуран, 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид или толуол, при температуре приблизительно от -20 до 150 С, где предпочтительна температура от 20 до 100 С, в отсутствии или присутствии катализатора фазового переноса, такого как хлорид тетра-н-бутиламмония, бромид тетра-нбутиламмония, йодид тетра-н-бутиламмония, хлорид бензилтриметиламмония, бромид бензилтриметиламмония или фторид бензилтриметиламмония, с последующим добавлением алкил-, аллил- или бензилхлорида, бромида, йодида, алкилсульфоната, арилсульфоната или трифлата позволяет получать имидазолы 31. Обработка 1-замещенного-4-бромимидазола (31) промежуточным соединением формулы 32 илиPG-NH2 (где PG определен как (С=О)алкил или бензоил) и палладиевым катализатором, таким как ацетат палладия(II), димер хлорида аллилпалладия, трис(дибензилиденацетон)дипалладий(0), аддукт хлороформа и трис(дибензилиденацетон)дипалладия(0) или хлорид палладия(II), где предпочтительны ацетат- 25011689 палладия(II), трис(дибензилиденацетон)дипалладий(0) и аддукт хлороформа и трис(дибензилиденацетон) дипалладия(0), и фосфиновым лигандом, предпочтительно 9,9-диметил-4,5-бис(дифенилфосфино)ксантеном (XANTPHOS), и основанием, таким как карбонат цезия или фосфат калия (K3PO4), где предпочтителен фосфат калия, в реакционно-инертном растворителе, таком как толуол, 1,4-диоксан или тетрагидрофуран, при температуре приблизительно от 0 до 150 С, где предпочтительна температура от 20 до 110 С, позволяет получить продукт сочетания 1. Альтернативно, обработка 1-замещенного-4 бромимидазола (31) промежуточным соединением формулы 32 или PG-NH2 (где PG определен как(С=О)алкил или бензоил) и диамином, таким как 1,2-этилендиамин, N,N'-диметилэтилендиамин или цис 1,2-диаминоциклогексан, предпочтительно N,N'-диметилэтилендиамин, и хлоридом, бромидом или йодидом меди, предпочтительно йодидом меди, в присутствии небольшого количества воды, предпочтительно приблизительно от 1 до 4% воды, в реакционно-инертном растворителе, таком как 1,2 диметоксиэтан, диглим, трет-бутилметиловый эфир, тетрагидрофуран, бензол или толуол, предпочтительно толуол, при температуре приблизительно от 40 до 150 С, предпочтительно приблизительно от 80 до 120 С, приводит к получению соединения формулы I или соединений формулы 33. В случае соединения 33 оно может быть превращено в соединения формулы 2 А с использованием описанных выше стандартных способов. Схема 7 Исходные вещества, используемые в способах на вышеприведенных схемах, синтез которых не описан выше, имеются в продаже, известны в области техники или могут быть легко получены из известных соединений с использованием способов, которые понятны специалистам в данной области техники. Соединения формулы I и промежуточные соединения, представленные на вышеприведенных схемах реакций, могут быть выделены и очищены с использованием обычных способов, таких как перекристаллизация или хроматографическое разделение, такое как разделение на силикагеле с элюированием градиентом этилацетат/гексан, элюированием градиентом метиленхлорид/метанол или элюированием градиентом хлороформ/метанол. Альтернативно, может быть использован способ разделения путем обращенно-фазовой препаративной ЖХВД или хиральной ЖХВД. В каждой из реакций, обсуждавшихся или проиллюстрированных выше, если не указано иначе,давление не является критичным. Обычно приемлемы давления приблизительно от 50,5 до 505 кПа (от 0,5 до 5 атм); для удобства предпочтительно давление окружающей среды, то есть приблизительно 101 кПа (1 атмосфера). Соединение формулы I по настоящему изобретению или его фармацевтически приемлемую соль можно вводить млекопитающим пероральным, парентеральным (таким как подкожный, внутривенный,внутримышечный, интрастернальный путь и инфузия), ректальным, интраназальным, местным или трансдермальным (например, путем использования пластыря) путями. Вообще эти соединения наиболее желательно вводить в дозах, находящихся в диапазоне от приблизительно 0,1 мг до приблизительно 1000 мг в сутки, в разовой или разделенной дозах (то есть от 1 до 4 доз в сутки), хотя непременно возникнут вариации в зависимости от вида, массы, возраста и состояния пациента, которого лечат, а также конкретного выбранного пути введения. Однако наиболее желательно использовать уровень доз, находящихся в диапазоне от приблизительно 0,1 мг/кг до приблизительно 5 мг/кг массы организма в сутки, предпочтительно от приблизительно 0,1 мг/кг до приблизительно 100 мг/кг массы организма в сутки. Тем не менее,в зависимости от вида животного, которое лечат, и его индивидуальной реакции на указанное лекарство,а также в зависимости от типа выбранного фармацевтического препарата и периода времени и интервала,с которым осуществляют такое введение, могут возникать вариации. В некоторых случаях уровни доз ниже нижнего предела вышеупомянутого диапазона могут быть более чем достаточными, тогда как в других случаях могут быть использованы еще большие дозы без каких-либо вредных побочных эффектов, при условии, что такие более крупные дозы сначала разделяют на несколько небольших доз для введения в течение суток. Лечащим врачом, обладающим стандартными знаниями, могут быть сделаны ва- 26011689 риации, основанные на вышеупомянутом диапазоне. Соединение формулы I по настоящему изобретению можно вводить само по себе или в комбинации с фармацевтически приемлемыми носителями или разбавителями любым из ранее указанных путей, и такое введение может быть осуществлено в виде одной или множества доз. Подходящие фармацевтические носители включают твердые разбавители или наполнители, стерильные водные среды и различные нетоксичные органические растворители и так далее. Фармацевтические композиции, получаемые путем объединения соединения формулы I или его фармацевтически приемлемой соли с фармацевтически приемлемым инертным носителем, затем можно легко вводить во множестве лекарственных форм, таких как таблетки, капсулы, лепешки, пастилки, твердые леденцы, порошки, спреи, кремы, мази, суппозитории,желе, гели, пасты, лосьоны, мази, водные суспензии, инъецируемые растворы, эликсиры, сиропы и т.п. Кроме того, фармацевтические композиции для перорального введения могут быть подходящим образом подслащены и/или ароматизированы. Таблетки для перорального введения, содержащие различные эксципиенты, такие как микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, дикальция фосфат и глицин, могут быть использованы вместе с различными разрыхлителями, такими как крахмал (предпочтительно кукурузный,картофельный крахмал или тапиока), метилцеллюлоза, альгиновая кислота и некоторые сложные силикаты, вместе со связывающими веществами при гранулировании, такими как поливинилпирролидон,сахароза, желатин и гуммиарабик. Кроме того, часто для целей таблетирования полезны смазывающие вещества, такие как стеарат магния, лаурилсульфат натрия и тальк. В качестве наполнителей в желатиновых капсулах также могут быть использованы твердые композиции подобного типа. Предпочтительные вещества в этой связи включают лактозу или молочный сахар, а также высокомолекулярные полиэтиленгликоли. В тех случаях, когда для перорального введения желательны водные суспензии и/или эликсиры, активный ингредиент может быть объединен с различными подсластителями или корригентами,красящим материалом или красителями, и, если желательно, эмульгаторами и/или суспендирующими агентами, вместе с такими разбавителями, как вода, этанол, пропиленгликоль, глицерин и различные похожие их комбинации. Для парентерального введения могут быть использованы растворы, содержащие соединение Формулы I по настоящему изобретению или его фармацевтически приемлемую соль, в кунжутном или арахисовом масле, в водном пропиленгликоле или в стерильных водных растворах. Водные растворы при необходимости должны быть соответствующим образом забуферены (предпочтительно рН больше 8) и жидкий разбавитель сначала следует сделать изотоническим при помощи достаточного количества солевого раствора или глюкозы. Эти водные растворы являются подходящими для задач внутривенной инъекции. Масляные растворы подходят для задач внутриглазной, внутримышечной и подкожной инъекций. Приготовление всех этих растворов в стерильных условиях может быть легко осуществлено с использованием стандартных фармацевтических методик, хорошо известных специалистам в данной области техники. Соединения формулы I по настоящему изобретению полезны при ингибировании продукции Апептида (таким образом, гамма-секретазной активности) у млекопитающих, и, следовательно, они способны действовать в качестве терапевтических агентов при лечении вышеупомянутых расстройств и заболеваний у млекопитающего, страдающего от них. С использованием биологических анализов, известных специалистам в данной области техники, например анализов, описанных ниже, можно определить ингибирование продукции А-пептида для конкретного соединения формулы I. Активность соединений формулы I по настоящему изобретению в отношении ингибирования гамма-секретазной активности определяли в солюбилизированном мембранном препарате обычно в соответствии с описанием, приведенным в McLendon et al. Cell-free assays for -secretase activity, The FASEBJournal (Vol. 14, December 2000, pp. 2383-2386). С использованием такого анализа определили, что соединения по настоящему изобретению обладают активностью IC50 для ингибирования гамма-секретазной активности меньше чем приблизительно 100 мкмоль. Предпочтительными соединениями по настоящему изобретению являются соединения, которые, как определено, обладают активностью IC50 для ингибирования гамма-секретазной активности меньше чем приблизительно 1 мкмоль. Следующие примеры иллюстрируют настоящее изобретение. Однако следует понимать, что не подразумевается, что изобретение, полностью описанное здесь и изложенное в формуле изобретения, ограничено подробностями следующих примеров. Примеры. Общая методика А. Способ сочетания для образования амида а) Методика сочетания EDC/HOBt/триалкиламин. Смесь карбоновой кислоты (1,0 экв.), амина (1,0 экв.), HOBt (1,1-1,5 экв.), EDC (1,2-1,8 экв.) и триалкиламина (триэтиламина или диизопропилэтиламина) (3-6 экв.) в соответствующем растворителе или смеси растворителей, например метиленхлориде, дихлорэтане, ТГФ или ДМФ, перемешивали при комнатной температуре до образования продукта или исчезновения исходного вещества. Растворитель уда- 27011689 ляли при пониженном давлении, остаток переносили в этилацетат (или подобным образом выбранный растворитель, такой как метиленхлорид или хлороформ) и воду. Органический слой отделяли, промывали разбавленной HCl (если желаемый продукт содержит основную функциональную группу, промывку разбавленной HCl можно пропустить), рассолом и сушили над сульфатом натрия. Затем при пониженном давлении удаляли растворитель, получая продукт. б) Методика сочетания HATU/триалкиламин. Смесь карбоновой кислоты (1,0 экв.), амина (1,0 экв.), гексафторфосфата О-(7-азабензотриазол-1 ил)-N,N,N',N'-тетраметилурония (HATU) (1,1-1,5 экв.) и триалкиламина (триэтиламина или диизопропилэтиламина) (3-6 экв.) в соответствующем растворителе или смеси растворителей, например метиленхлориде, дихлорэтане, ТГФ или ДМФ, перемешивали при комнатной температуре до образования продукта или исчезновения исходного вещества. Растворитель удаляли при пониженном давлении, остаток переносили в этилацетат (или подобным образом выбранный растворитель, такой как метиленхлорид или хлороформ) и воду. Органический слой отделяли, промывали разбавленной HCl (если желаемый продукт содержит основную функциональную группу, промывку разбавленной HCl можно пропустить),рассолом и сушили над сульфатом натрия. Затем при пониженном давлении удаляли растворитель, получая продукт. в) Методика сочетания PyBOP/триалкиламин. Смесь карбоновой кислоты (1,0 экв.), амина (1,0 экв.), гексафторфосфата (бензотриазол-1 илокси)трипирролидинофосфония (РуВОР) (1,1-1,5 экв.) и триалкиламина (триэтиламина или диизопропилэтиламина) (3-6 экв.) в соответствующем растворителе или смеси растворителей, например метиленхлориде, дихлорэтане, ТГФ или ДМФ, перемешивали при комнатной температуре до образования продукта или исчезновения исходного вещества. Растворитель удаляли при пониженном давлении, остаток переносили в этилацетат (или подобным образом выбранный растворитель, такой как метиленхлорид или хлороформ) и воду. Органический слой отделяли, промывали разбавленной HCl (если желаемый продукт содержит основную функциональную группу, промывку разбавленной HCl можно пропустить), рассолом и сушили над сульфатом натрия. Затем при пониженном давлении удаляли растворитель, получая продукт. г) Методика сочетания HBTU/триалкиламин. Смесь карбоновой кислоты (1,0 экв.), амина (1,0 экв.), гексафторфосфата О-(бензотриазол-1-ил)N,N,N',N'-тетраметилурония (HBTU) (1,1-1,5 экв.), и триалкиламина (триэтиламина или диизопропилэтиламина) (3-6 экв.) в соответствующем растворителе или смеси растворителей, например метиленхлориде, дихлорэтане, ТГФ или ДМФ, перемешивали при комнатной температуре до образования продукта или исчезновения исходного вещества. Растворитель удаляли при пониженном давлении, остаток переносили в этилацетат (или подобным образом выбранный растворитель, такой как метиленхлорид или хлороформ) и воду. Органический слой отделяли, промывали разбавленной HCl (если желаемый продукт содержит основную функциональную группу, промывку разбавленной HCl можно пропустить), рассолом и сушили над сульфатом натрия. Затем при пониженном давлении удаляли растворитель, получая продукт. д) Методика хлоралкилформиатного сочетания. Смесь карбоновой кислоты (1 экв.) и триэтиламина (экв.) растворяли в соответствующем растворителе, таком как ДМФ, и охлаждали до -23 С. По каплям при перемешивании добавляли изобутилформиат (1 экв.). После перемешивания в течение некоторого времени (от 15 мин до 2 ч) добавляли 2 аминотиазол или амин (1 экв.) и перемешивание продолжали в течение еще 30 мин при -23 С. Затем смесь нагревали до комнатной температуры до образования амида (как правило, в течение ночи). Смесь гасили водой и рассолом и экстрагировали соответствующим растворителем, таким как этилацетат, метиленхлорид или хлороформ. Органический слой промывали разбавленным NaHSO4, NaHCO3 и рассолом, и при пониженном давлении удаляли растворитель, получая продукт. Может быть необходима очистка. е) Методика сочетания триметилалюминия. Смесь амина или аминотиазола (1-2 экв.), 2 М триметилалюминия готовили в соответствующем растворителе, таком как ТГФ, толуол, ксилол, метиленхлорид или дихлорэтан, или смеси растворителей,такой как ТГФ/толуол. Смесь перемешивали при комнатной температуре в течение периода времени от 15 мин до 2 ч, затем добавляли сложный эфир (1 экв.). Получающуюся в результате смесь перемешивали при температуре от комнатной температуры до температуры дефлегмации до образования продукта. Смесь осторожно гасили сегнетовой солью (солью Рошеля), экстрагировали соответствующим растворителем, таким как этилацетат или метиленхлорид, и фильтровали через целит. Органический слой промывали разбавленной HCl, нейтрализовали насыщенным бикарбонатом натрия и промывали рассолом. Органический слой отделяли, сушили и концентрировали с получением желаемого амида. Может быть необходима очистка. Общая методика Б. Способ восстановительного аминирования. а) Триацетоксиборгидрид натрия.- 28011689 Амин (1-4 экв.) в дихлорэтане или ТГФ добавляли к раствору кетона (1 экв.), NaBH(OAc)3 (1-3 экв.) и уксусной кислоты (1-3 экв.) в дихлорэтане или ТГФ. Смесь перемешивали при комнатной температуре до образования продукта или исчезновения исходного вещества. Смесь гасили разбавленным основанием, экстрагировали метиленхлоридом или другим соответствующим растворителем, таким как хлороформ или этилацетат. Органический слой отделяли, сушили и концентрировали с получением желаемого амида. Может быть необходима очистка. б) Цианоборгидрид натрия. Смесь кетона или альдегида (1 экв.), амина (1-20 экв.), цианоборгидрида натрия (1-5 экв.), уксусной кислоты (1-3 экв.), ацетата натрия (1-3 экв.), безводного сульфата натрия в дихлорэтане или ТГФ перемешивали при комнатной температуре до 60 С, предпочтительно нагревали при 35-50 С до образования продукта. Смесь гасили разбавленным основанием, экстрагировали метиленхлоридом или другим соответствующим растворителем, таким как хлороформ или этилацетат. Органический слой отделяли, сушили и концентрировали с получением желаемого амида. Может быть необходима очистка. в) Формиат калия и ацетат палладия. Раствор альдегида или кетона (1 экв.) и амина (1 экв.) в сухом ДМФ перемешивали при комнатной температуре в течение 4 ч в присутствии молекулярных сит. К получающейся в результате реакционной смеси добавляли формиат калия (2 экв.) и ацетат палладия (каталитическое количество, 0,02 экв.). Смесь нагревали при 40-60 С для завершения реакции (тонкослойная хроматография (ТСХ и после охлаждения ее разбавляли смесью лед-вода. Смесь экстрагировали соответствующим растворителем (таким как метиленхлорид, этилацетат или хлороформ). Органический слой отделяли, сушили и концентрировали с получением желаемого амида. Может быть необходима очистка. Общая методика В. Восстановление кетона или альдегида боргидридом натрия. Смесь альдегида или кетона (1 экв.) и боргидрида натрия (1-10 экв.) в соответствующем растворителе (метаноле или этаноле) перемешивали при температуре от 0 С до комнатной температуры в течение 10 мин для завершения реакции (ТСХ). Смесь концентрировали до небольшого объема, гасили водой,экстрагировали соответствующим растворителем (таким как метиленхлорид, этилацетат или хлороформ). Органический слой отделяли, сушили и концентрировали с получением желаемого амида. Может быть необходима очистка. Общая методика Г. Методика снятия N-трет-BOC защиты. К раствору N-трет-BOC соединения в 1,4-диоксане (0,03-0,09 М) добавляли 4 н. HCl в 1,4-диоксане или безводный газообразный HCl в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре в течение 1-24 ч до израсходования всего исходного материала (ТСХ). Раствор концентрировали и откачивали в вакууме. Конечную HCl соль соответствующего амина обычно использовали без дополнительной очистки. Общая методика Д. Присоединение конъюгата к нитроимидазолу. К суспензии 4-нитроимидазола (2,0 эквив.) в ацетонитриле добавляли DBU (1,0 эквив.), а затем енон (1,0 эквив.). Реакционную смесь нагревали в течение 12-24 ч, и в вакууме удаляли растворитель. Получающиеся в результате твердые частицы удаляли фильтрованием с метиленхлоридом, и образовавшееся масло концентрировали и очищали путем хроматографии на силикагеле с получением желаемого нитроимидазола. Общая методика Е. Алкилирование нитроимидазола. К суспензии 4-нитроимидазола (1,0 эквив.) в диметилформамиде при к.т. в атмосфере азота порциями добавляли гидрид натрия (1,2 эквив.). Реакционную смесь перемешивали в течение 15-30 мин. Затем добавляли соответствующий алкилгалогенид или алкилмезилат. Смесь перемешивали в течение 12-24 ч при 50 С, охлаждали до 0 С и гасили водой. Водный слой экстрагировали метиленхлоридом,сушили и очищали путем хроматографии на силикагеле с получением желаемого нитроимидазола. Общая методика Ж. Восстановление нитроимидазола. К раствору нитроимидазола (1,0 эквив.) в этилацетате добавляли палладий на угле (0,25% мас./мас.). Реакционную смесь гидрировали при 275790-413685 Па (40-60 фунт/кв.дюйм) в течение 2-6 ч и фильтровали над слоем целита с использованием этилацетата. Большую часть этилацетата удаляли в вакууме, и раствор амина в оставшемся этилацетате использовали без дополнительной очистки. Общая методика З. Восстановление нитроимидазол-сложного эфира с последующим восстановительным аминированием. К раствору метилового эфира 3-метил-3-(4-нитро-имидазол-1-ил)масляной кислоты (1,0 эквив.) в метиленхлориде по каплям при -78 С добавляли DIBAL (2 эквив.). Реакционную смесь перемешивали в течение 1 ч, гасили этилацетатом, извлекали из охлаждающей бани и перемешивали в течение 10 мин. К- 29011689 реакционной смеси добавляли воду и оставляли нагреваться до к.т. или перемешиваться в течение 1 ч. Реакционную смесь разбавляли метиленхлоридом, добавляли Na2SO4 и фильтровали через целит: Растворитель удаляли с получением 2-метил-2-(4-нитроимидазол-1-ил)пропионового альдегида, который использовали на следующей стадии без дополнительной очистки. К раствору 2-метил-2-(4-нитроимидазол-1-ил)пропионового альдегида (1 эквив.) в метиленхлориде добавляли соответствующий амин (2 эквив.) и молекулярные сита 4 А. Реакционную смесь перемешивали в течение 4-6 ч и добавляли соответствующий гидридный восстановитель, такой как триацетоксиборгидрид натрия (2 эквив.). Реакционную смесь перемешивали в течение 6-24 ч, гасили бикарбонатом натрия и водный слой экстрагировали метиленхлоридом. Растворитель удаляли, и остаток очищали путем хроматографии на силикагеле с получением желаемого нитроимидазола. Следующие соединения получали способами, аналогичными описанным выше для общей методики Д: Метиловый эфир 3-(4-нитроимидазол-1-ил)масляной кислоты. 4-Нитроимидазол подвергали взаимодействию с метил-3-метилакрилатом с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 1.62 (d, 3 Н, J=7.0 Гц), 2.81 (d, 2H, J=7.0 Гц), 3.66 (s,3H), 4.78 (m, 1 Н), 7.53 (d, 1H, J=1.6 Гц), 7.82 (d, 1H, J=1.6 Гц); МС m/z 214,1 (М+1). Метиловый эфир 3-метил-3-(4-нитроимидазол-1-ил)масляной кислоты. 4-Нитроимидазол подвергали взаимодействию с метил-3,3-диметилакрилатом с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 1.74 (s, 6H), 2.81 (s, 2H), 3.57 (s, 3 Н), 7.57 (d,1H, J=1.3 Гц), 7.90 (d, 1 Н, J=1.6 Гц); МС m/z 228,2 (М+1). Следующие соединения получали способами, аналогичными описанным выше для общей методики Е: Метиловый эфир 2-метил-2-(4-нитроимидазол-1-ил)пропионовой кислоты. 4-Нитроимидазол алкилировали метиловым эфиром 2-бром-2-метилпропионовой кислоты с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 1.89 (s, 6H), 3.78 (s, 3 Н), 7.59 (d,1H, J=1.7 Гц), 7.89 (s, 1H, J=1.7 Гц); МС 214,1 m/z (М+1). 1-(1-Этилпропил)-4-нитро-1H-имидазол. 4-Нитроимидазол алкилировали 3-бромпентаном с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 0.84-0.90 (m, 6H), 1.71-1.82 (m, 2 Н), 1.86-1.96 (m, 2 Н), 3.79 (р, 1 Н, J=4.8 Гц),7.41 (d, 1H, J=1.6 Гц), 7.73 (d, 1H, J=1.3 Гц); МС 184,2 m/z (M+1). Трет-бутиловый эфир 4-(4-нитроимидазол-1-ил)пиперидин-1-карбоновой кислоты. 4-Нитроимидазол алкилировали тpeт-бутиловым эфиром 4-метансульфонилоксипиперидин-1 карбоновой кислоты с получением указанного в заголовке соединения: 13 С ЯМР (100 МГц, CDCl3) 28.5,33.2, 42.7, 56.8, 80.7, 117.5, 134.4, 154.5; МС 297,1 m/z (M+1). Метиловый эфир (4-нитроимидазол-1-ил)уксусной кислоты. 4-Нитроимидазол алкилировали метиловым эфиром бромуксусной кислоты с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц) 3.82 (s, 1H), 4.80 (s, 2H), 7.47 (d, 1H, J=1.7 Гц), 7.84 (d, 1H,J=1.7 Гц); ГХ/МС m/z 185 (М). Метиловый эфир 2-метил-2-(2-метил-4-нитроимидазол-1-ил)пропионовой кислоты. 2-Метил-4-нитроимидазол алкилировали метиловым эфиром бромуксусной кислоты с получением указанного в заголовке соединения: МС m/z 228,2 (М+1). 1-(2-Метокси-1,1-диметилэтил)-4-нитро-1H-имидазол. Метиловый эфир 2-метил-2-(4-нитроимидазол-1-ил)пропионовой кислоты восстанавливали с использованием боргидрида натрия в метаноле, и образовавшийся спирт алкилировали метилйодидом с использованием гидрида натрия в качестве основания с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 1.53 (s, 6H), 3.25 (s, 3 Н), 3.38 (s, 2H), 7.53 (s, 1H), 7.88 (s,1H). Метиловый эфир 4-(4-нитроимидазол-1-ил)бензойной кислоты. 4-Нитроимидазол (1 эквив.) объединяли с 4-йодметилбензоатом (1,2 эквив.), карбонатом цезия (1,0 эквив.), трифлатом меди (I) (0,05 эквив.) в диметилформамиде (ДМФ) и нагревали в течение ночи при 100 С. Твердое вещество отфильтровывали и промывали метиленхлоридом, образовавшийся растворитель концентрировали и остаток очищали путем хроматографии на силикагеле с получением указанного в заголовке соединения: МС m/z 248,2 (М+1).(2,2-Диметилпропил)-[2-метил-2-(4-нитроимидазол-1-ил)пропил]амин обрабатывали формалином и муравьиной кислотой при 85 С в течение 5 ч, гасили водным бикарбонатом натрия, экстрагировали метиленхлоридом, сушили, концентрировали и образовавшийся остаток очищали путем хроматографии с получением указанного в заголовке соединения: 1 Н ЯМР (400 МГц, CDCl3) 0.74 (s, 9H), 1.52 (s, 6H), 2.2 (s,2H), 2.8 (s, 2H), 7.6 (s, 1H), 7.9 (s,1H);MC m/z 255,3 (М+1). Следующие соединения получали способами, аналогичными описанным выше для общей методики З. 4-[2-Метил-2-(4-нитроимидазол-1-ил)пропил]морфолин. 2-Метил-2-(4-нитроимидазол-1-ил)пропиональдегид подвергали взаимодействию с морфолином с
МПК / Метки
МПК: C07D 417/14, A61K 31/4164, A61P 25/28, C07D 233/88
Метки: лечения, расстройств, нейродегенеративных, имидазольные, соединения
Код ссылки
<a href="https://eas.patents.su/30-11689-imidazolnye-soedineniya-dlya-lecheniya-nejjrodegenerativnyh-rasstrojjstv.html" rel="bookmark" title="База патентов Евразийского Союза">Имидазольные соединения для лечения нейродегенеративных расстройств</a>
Предыдущий патент: Способ определения нарушений венозного кровотока, предназначенный для диагностики и лечения
Случайный патент: Способ индукции дифференцировки клеток


































