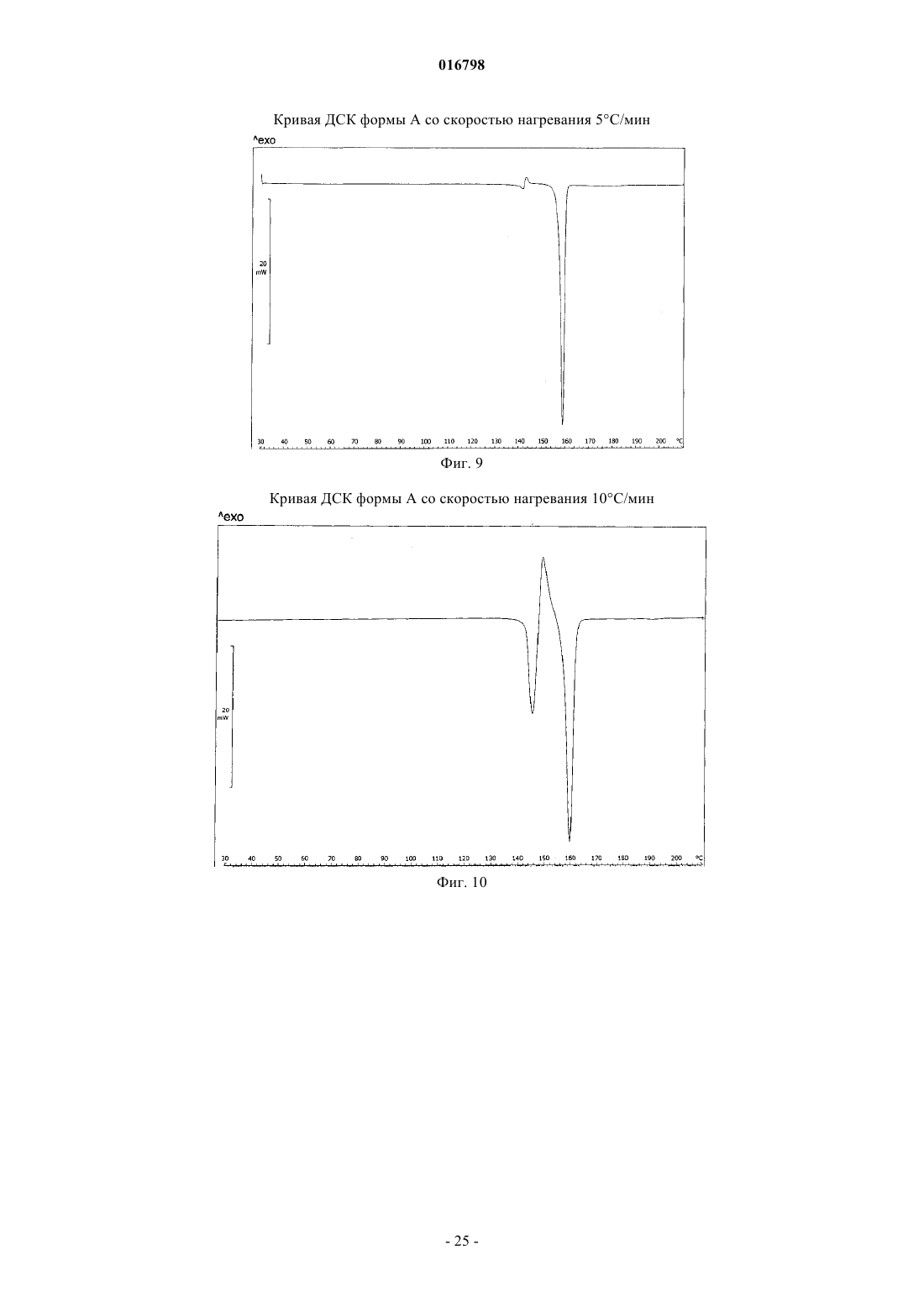
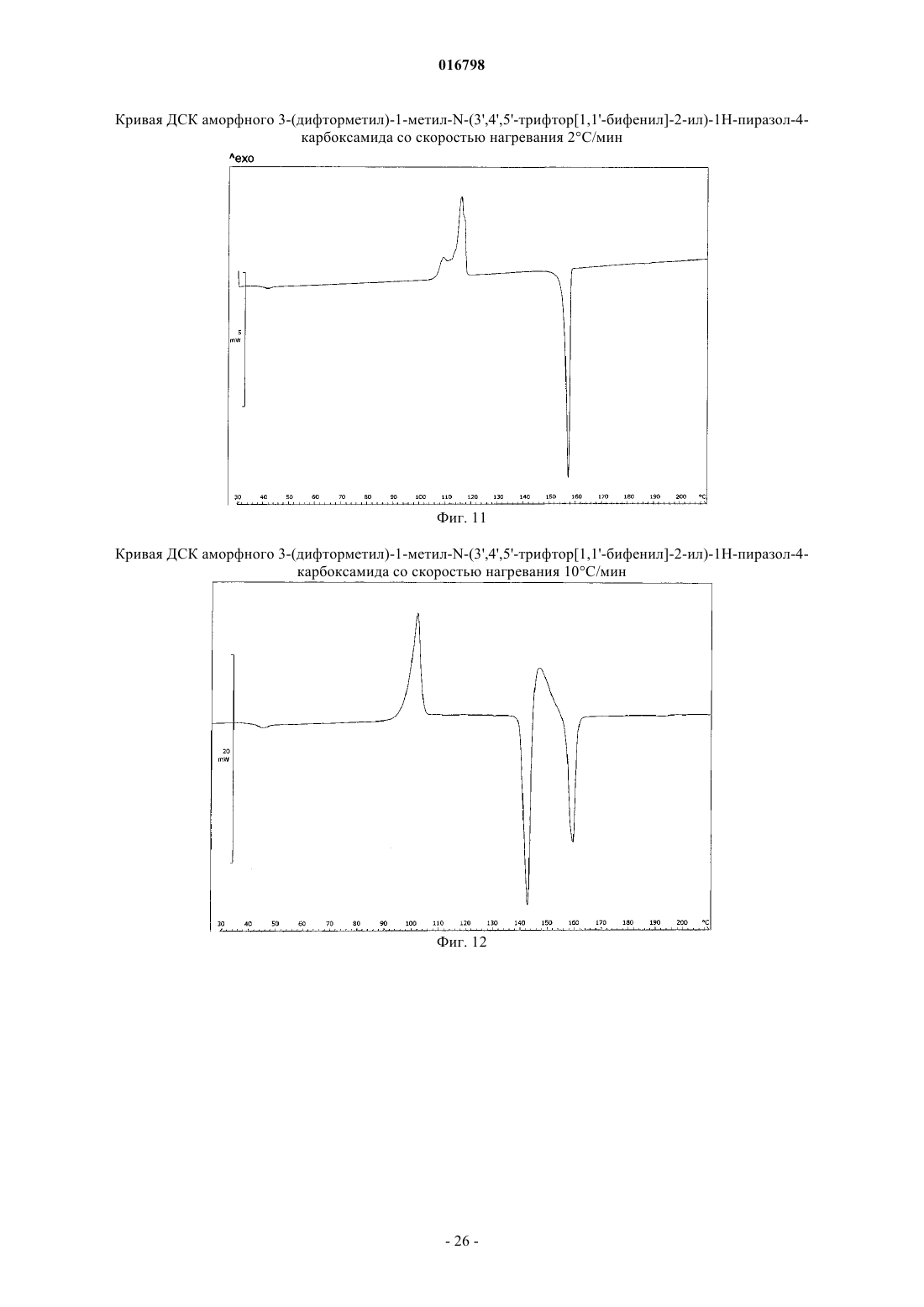
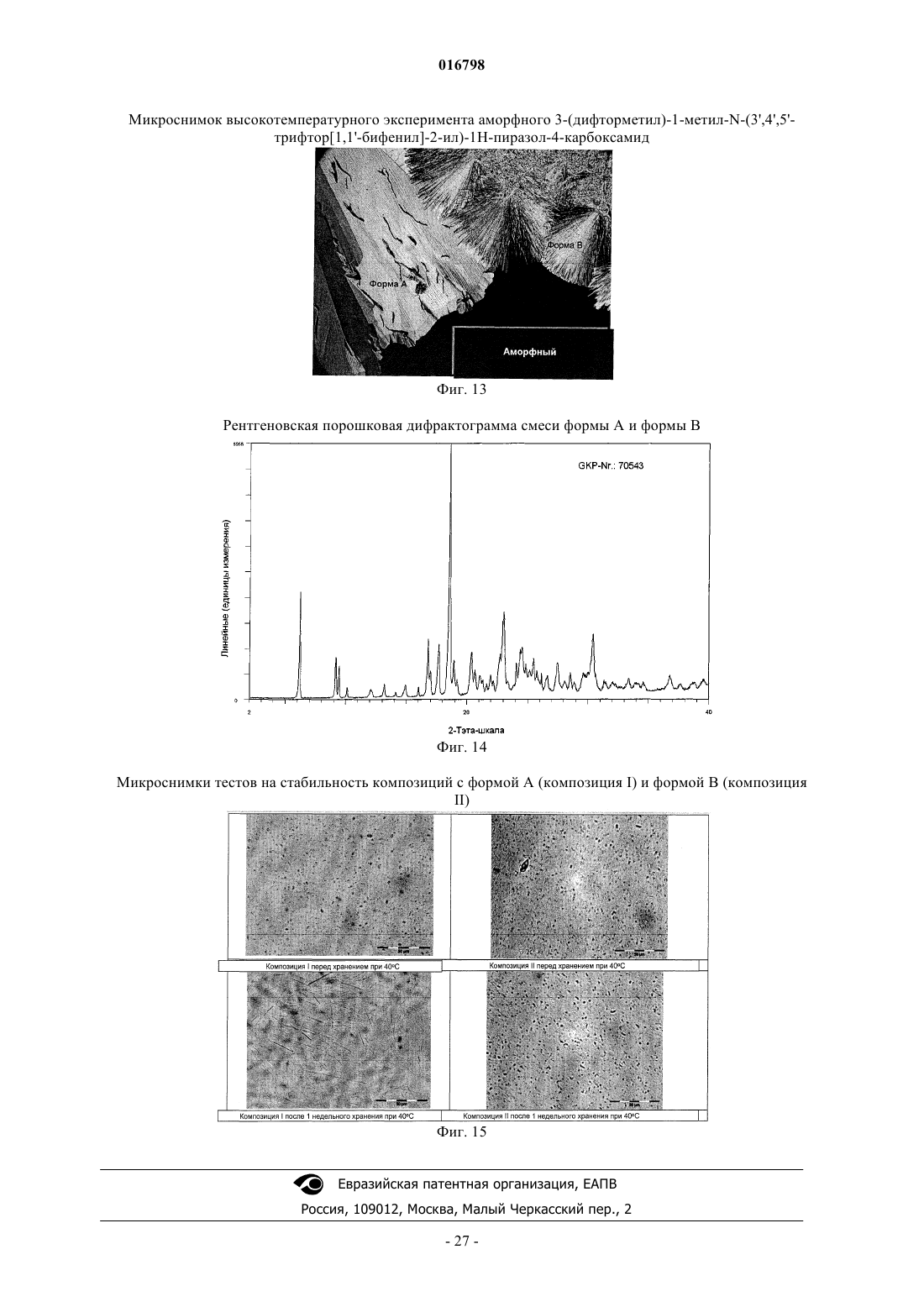
Новая кристаллическая форма 3-(дифторметил)-1-метил-n-(3′,4′,5′-трифтор[1,1'-бифенил]-2-ил)-1н-пиразол-4-карбоксамида
Номер патента: 16798
Опубликовано: 30.07.2012
Авторы: Шмидт Зебастиан Пер, Дилеман Цедрик, Сакселль Хейди Эмилия, Дитц Йохен
Формула / Реферат
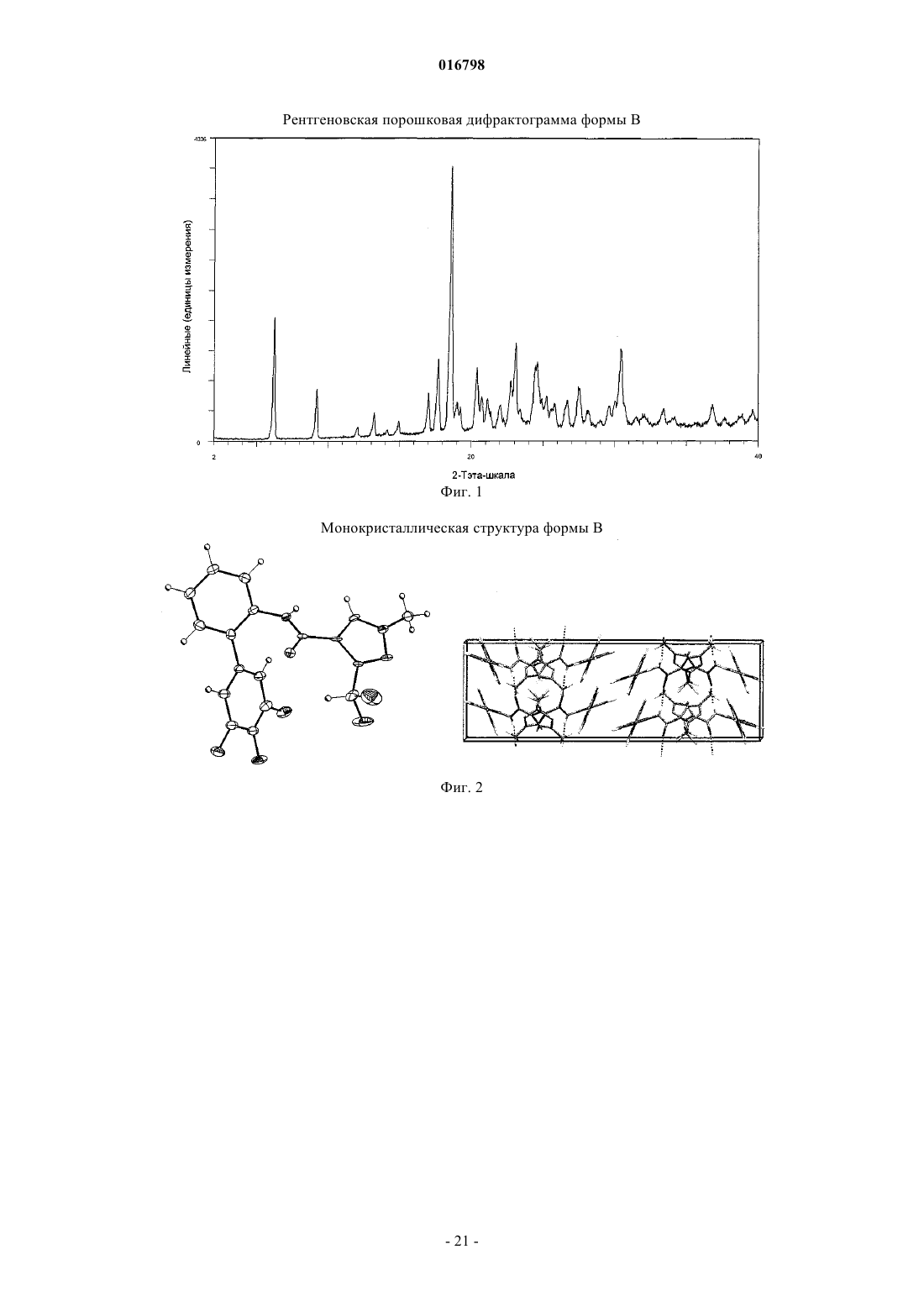
1. Кристаллическая форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, которая на диаграмме рентгеновской порошковой дифракции при 25°С и Cu-Kα излучении показывает по меньшей мере 3 из следующих характеристических пиков, выраженных в 2θ значениях: 6,2±0,2°, 9,2±0,2°, 13,2±0,2°, 14,9±0,2°, 17,7±0,2°, 18,6±0,2°, 23,1±0,2°, 27,6±0,2°, 30,5±0,2°.
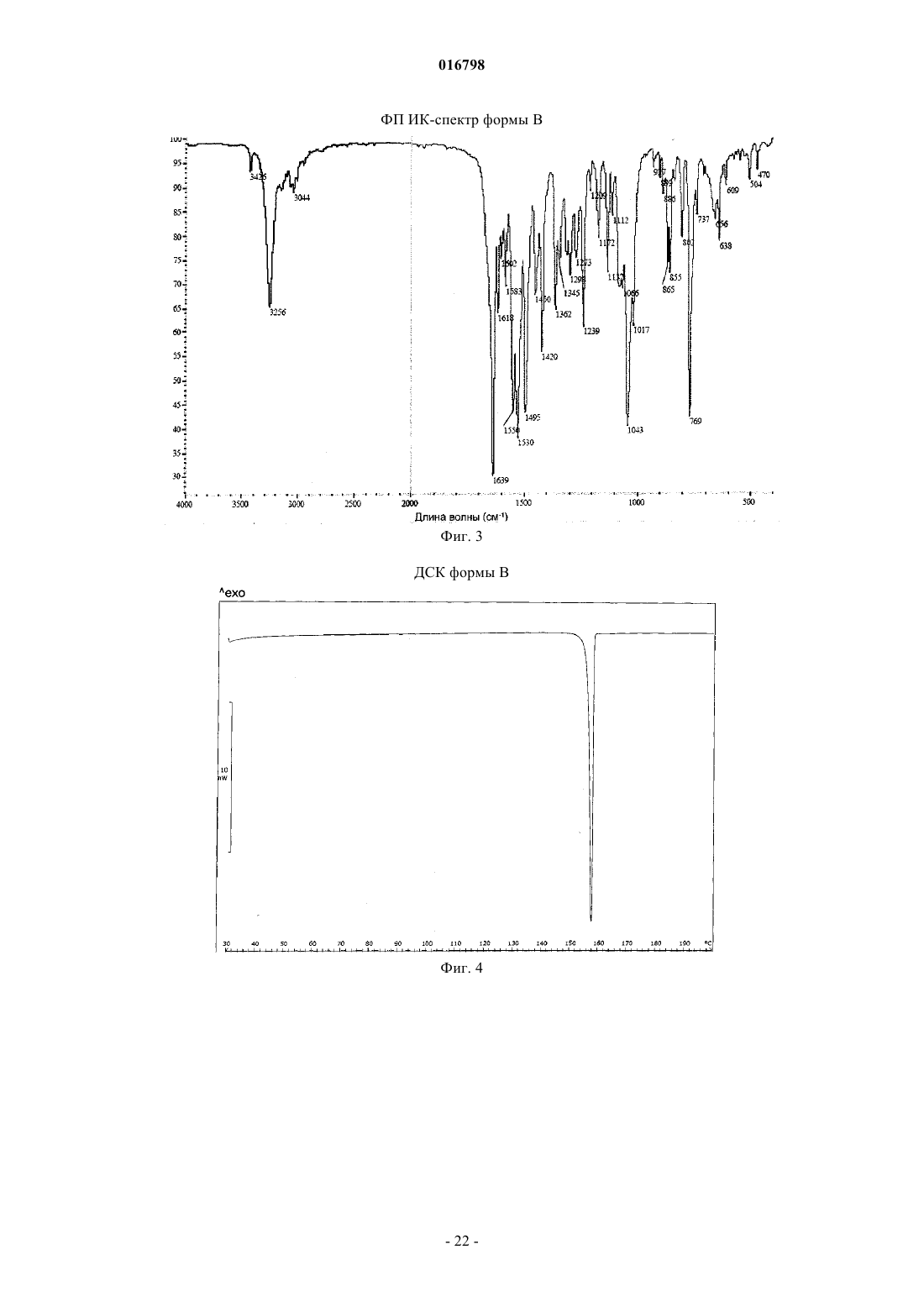
2. Кристаллическая форма В по п.1, имеющая характерные полосы поглощения в инфракрасном спектре с превращением Фурье на длинах волн 3256 и 1639 см-1.
3. Кристаллическая форма В по п.1 с содержанием 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамида по меньшей мере 94 мас.%.
4. 3-(Дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамид, состоящий по меньшей мере из 90 мас.% кристаллической формы В.
5. Способ получения кристаллической формы В по п.1, состоящий из:
i) получения раствора 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамида в органическом растворителе, который выбран из метанола, этанола, 2-пропанола, циклических эфиров, уксусной кислоты, апротонных растворителей и ароматических растворителей, при температуре от 50 до 130°С;
ii) охлаждения раствора со скоростью между 20 и 0,1°С/ч до температуры между 70 и -20°С;
iii) отделения формы В от маточного раствора.
6. Способ получения кристаллической формы В по п.1, состоящий из:
i) получения раствора 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамида в органическом растворителе, который выбран из метанола, этанола, 2-пропанола, циклических эфиров, уксусной кислоты, апротонных растворителей и ароматических растворителей, при температуре от 50 до 130°С;
ii) добавления в раствор уменьшающего коэффициент растворимости растворителя в течение от 40 мин до 2,5 ч;
iii) отделения формы В от маточного раствора.
7. Способ получения кристаллической формы В по п.1, включающий нагревание аморфной формы 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, его кристаллической формы А, смеси аморфной формы с формой А или смеси формы В с аморфной формой или формой А при температуре от 80 до 154°С.
8. Агент для защиты растений, содержащий 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамид, который состоит по меньшей мере из 90 мас.% кристаллической формы В по п.1 и одной или более добавок, типичных для получения составов агентов для защиты растений.
9. Агент для защиты растений по п.8 в форме водного концентрата суспензии.
10. Агент для защиты растений по п.8 в форме безводного концентрата суспензии.
11. Агент для защиты растений по п.8 в форме порошка или гранул, диспергируемых в воде.
12. Способ борьбы с нежелательным ростом растения, в котором 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Н-пиразол-4-карбоксамид, состоящий по меньшей мере из 90 мас.% кристаллической формы В по п.1, применяется на растениях, их месте распространения и/или на семенах.
Текст
НОВАЯ КРИСТАЛЛИЧЕСКАЯ ФОРМА 3-(ДИФТОРМЕТИЛ)-1-МЕТИЛ-N-(3',4',5'ТРИФТОР[1,1'-БИФЕНИЛ]-2-ИЛ)-1 Н-ПИРАЗОЛ-4-КАРБОКСАМИДА Настоящее изобретение касается новой кристаллической формы 3-(дифторметил)-1-метилN-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Изобретение также касается способа получения кристаллической формы и составов для защиты растений, которые содержат кристаллическую форму 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1H-пиразол-4-карбоксамида. Сакселль Хейди Эмилия, Шмидт Зебастиан Пер (DE), Дилеман Цедрик 016798 Область техники изобретения Настоящее изобретение относится к новой кристаллической форме 3-(дифторметил)-1-метил-N(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида. Изобретение также относится к способу получения этой кристаллической формы и композиций для защиты растений, содержащих эту кристаллическую форму 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида. Уровень техники изобретения 3-(Дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид представлен следующей формулой: 3-(Дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид и основной способ его получения известен из WO 2006/087343. Этот способ в результате дает соединение в виде аморфного твердого тела. 3-(Дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид также раскрыт в WO 2007/017416. Для производства активных веществ в промышленном масштабе, как и для композиций активных веществ, во многих случаях знание относительно возможного существования кристаллических модификаций (также описываемых в виде кристаллических форм или полиморфных) или сольватов рассматриваемого активного вещества и знание специфических свойств таких модификаций и способов их получения имеют решающее значение. Целый ряд активных веществ могут существовать в нескольких различных кристаллических, а также в аморфных модификациях. Термином, используемым в этих случаях, является полиморфизм. Полиморф представляет собой твердую, кристаллическую фазу соединения, которая характерна для разных полиморфных соединений, интересующих спецификой, плотностью и равномерным расположением молекул в твердой фазе. Несмотря на продолжающиеся усилия в главных исследовательских группах во всем мире возможные существования или свойства кристаллических модификаций, используемые в настоящий момент, не предсказуемы и не могут таким образом быть предвидены. Различные модификации одного и того же активного вещества могут обладать различными свойствами. К ним относятся растворимость, давления пара, скорости растворения, устойчивость к изменениям фаз в разных модификациях, устойчивость при измельчении, суспензионная стабильность, оптические и механические свойства, гигроскопичность, кристаллическая форма и размер, фильтруемость, плотность,температура плавления, устойчивость к разложению, цвет, а иногда и даже химическая активность или биологическая активность. Описание изобретения Собственные пробы заявителя преобразовать 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1H-пиразол-4-карбоксамид в твердую кристаллическую фазу путем кристаллизации сначала дали в результате аморфные продукты или кристаллические модификации, в дальнейшем именуемые как форма А, которые могли выполняться только с трудом и у которых стабильность композиции и устойчивость к фазовому превращению была неконтролируема и неудовлетворительна. В настоящее время неожиданно было обнаружено, что соответствующими способами одна ранее неизвестная кристаллическая, стабильная модификация 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1H-пиразол-4-карбоксамида, которая не показывает недостатков до сих пор известных аморфных соединений или кристаллической формы А, получена в высокой степени чистоты. Эта новая модификация описана далее как форма В. Кроме того, кристаллическая форма В изобретения проще в обращении, чем известный ранее аморфный 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид и его кристаллическая форма А, в первую очередь, поскольку в ходе ее специфического производства форма В получена в виде отдельных кристаллов или кристаллитов. По сравнению с аморфным соединением с кристаллической формой А или со смесями любых из этих форм форма В в чистом виде проявляет повышенную стабильность в связи с переходом в другую модификацию. Термин "форма В в чистом виде" следует понимать так, что пропорция исследуемого модифицированного по отношению к общему количеству 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида составляет по меньшей мере 90 мас.% и, в частности, по меньшей мере 95 мас.%. Таким образом, первый объект настоящего изобретения относится к кристаллической форме В 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Кроме того,объектом является 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамид, состоящий по крайней мере из 90 мас.% кристаллической формы В.-1 016798 Краткое описание фигур, используемых для пояснения изобретения Фиг. 1: рентгеновская порошковая дифрактограмма кристаллической формы В. Фиг. 2: рентгеновская структура монокристалла кристаллической формы В. Фиг. 3: спектр инфракрасной спектроскопии с Фурье-преобразованием кристаллической формы В. Фиг. 4: термограмма дифференциальной сканирующей калориметрии (ДСК) кристаллической формы В. Фиг. 5: рентгеновская порошковая дифрактограмма кристаллической формы А. Фиг. 6: рентгеновская структура монокристалла кристаллической формы А. Фиг. 7: спектр инфракрасной спектроскопии с Фурье-преобразованием кристаллической формы А. Фиг. 8-10 термограмма дифференциальной сканирующей калориметрии (ДСК) кристаллической формы А при тепловых режимах 2, 5 и 10 С/мин соответственно. Фиг. 11 и 12 термограмма дифференциальной сканирующей калориметрии (ДСК) аморфного 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида при тепловых режимах 2 и 10 С/мин соответственно. Фиг. 13: изображение высокотемпературной микроскопии преобразования аморфного 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида в кристаллические формы А и В (тепловой режим 5 С/мин). Фиг. 14: рентгеновская порошковая дифрактограмма смеси кристаллических форм А и В. Фиг. 15: микроснимки тестов композиций с кристаллической формой А (композиция I) и кристаллической формой В (композиция II). Подробное описание изобретения Кристаллическая форма В. Новая кристаллическая форма В согласно изобретению может быть идентифицирована путем рентгеновской порошковой дифрактометрии на основе ее фигуры дифракции. Таким образом, диаграмма рентгеновской порошковой дифракции (фиг. 1), записанная при помощи Cu-K излучения (1,54178) при 25 С, показывает по крайней мере 4, зачастую по меньшей мере 6, в частности по меньшей мере 8 и в особенности все отражения, приведенные в следующей таблице как 2 значения или как межплоскостные расстояния d. Таблица 1 Значения 2 и d-расстояний рентгеновской дифрактограммы кристаллической формы В Кристаллическая форма В имеет иглоподобную форму кристаллов. Параметры элементарной ячейки и структура кристалла могут быть определены путем измерения одной кристаллической структуры. Кристаллическая форма В показывает моноклинную кристаллическую систему с пространственной группой Pbca. Кристаллографические данные (измеренные при -173 С) и наиболее важные параметры приведены в табл. 2. Картина асимметричного узла и тип упаковки далее изображены на фиг. 2. Таблица 2 Кристаллографические данные и параметры кристаллической формы В-2 016798 Кроме того, как показано на фиг. 3, кристаллическая форма В также показывает инфракрасный(ИК) спектр с характерными пиками примерно в 1639 и 3256 см-1. Это пики вибрации карбонильной связи и вибрации N-H связи соответственно. Кроме того, как показано на фиг. 4, кристаллическая форма В показывает термограмму с характерным плавким эндотермом в районе 149 и 160 С. Температура плавления определяется как начало плавления эндотерма в измерении дифференциальной сканирующей калориметрии (фиг. 4), как правило, находится в диапазоне примерно от 155 до 158 С, в частности в диапазоне от 156 до 157 С. Значения, указанные здесь, относятся к значениям, определенным путем дифференциальной сканирующей калориметрии, ДСК (открытая алюминиевая чаша, скорость нагрева 2 К/мин). Удельная теплота плавления кристаллической формы В находится в диапазоне 90 Дж/г. Следует отметить, что в случае твердых форм 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1H-пиразол-4-карбоксамида, ДСК-измерения и особенно традиционные измерения температуры плавления не должны использоваться только в выявлении получаемых твердой формы или кристаллической модификации. А именно, в зависимости от скорости нагрева и других измерительных параметров, а также вычислительной техники для измерений, температура плавления и ДСК измерения аморфной формы и кристаллической формы А могут быть неправильно истолкованы, что приводит к ошибочному определению формы В. Получение кристаллической формы В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1 Н-пиразол-4-карбоксамида согласно изобретению осуществляется путем кристаллизации из раствора 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида в подходящем органическом растворителе. Подходящими растворителями для кристаллизации формы В являются спирты, такие как метанол, этанол и 2-пропанол, уксусная кислота, циклические эфиры, такие как тетрагидрофуран, апротонные растворители, такие как ацетонитрил, нитрометан, диметилсульфоксид, метилэтилкетон, диэтилкетон и метилизобутилкетон, а также ароматические растворители, как пиридин,1,2-дихлорбензол и толуол. Для этого первым этапом является i) получение раствора 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида в одном из вышеупомянутых органических растворителей, а затем на втором этапе ii) производится кристаллизация соединения. Концентрация 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида в растворе, используемая для кристаллизации, естественно, зависит от природы растворителя и температуры раствора и часто находится в диапазоне от 100 до 800 г/л. Подходящие условия могут определяться специалистом данной области в подобных экспериментах. Желательно, чтобы раствор, используемый для кристаллизации, содержал 3-(дифторметил)-1 метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид в чистоте по крайней мере 85%,часто не менее 90%, в частности по меньшей мере 95%, т.е. содержание органических примесей, которые не являются органическими растворителями, не более 15 мас.%, часто не более 10 мас.%, а в частности не более 5 мас.%, от растворенного 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Нпиразол-4-карбоксамида. Раствор, используемый для кристаллизации, предпочтительно существенно свободен от растворителей, помимо указанных выше. В связи с этим "существенно свободен" означает, что концентрация других растворителей в растворе, содержащем 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-дифенил]-2 ил)-1H-пиразол-4-карбоксамид не превышает 10 мас.%, часто 5 мас.%, от общего количества растворителя. Раствор 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида может, например, быть приготовлен следующими способами:(1) растворение 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида предпочтительно в форме, отличной от кристаллической формы В, в одном из вышеупомянутых органических растворителей или(2) получение 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида по химической реакции и перемещение из реакционной смеси, при необходимости, после удаления реагентов и/или побочных продуктов в подходящем органическом растворителе согласно изобретению. Для получения раствора может быть использована по сути любая известная форма 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Предпочтительно будет использоваться аморфный 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1H-пиразол-4-карбоксамид или смесь различных кристаллических модификаций или смесь аморфного и кристаллического 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида. Растворение 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида, как правило, осуществляется при температурах в диапазоне от 20 до 130 С. В предпочтительном варианте изобретения растворение 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1 Н-пиразол-4-карбоксамида осуществляется при повышенной температуре, в частности по меньшей-3 016798 мере 50 С, и, естественно, температура, используемая при растворении, не будет превышать температуру кипения растворителя. Растворение часто осуществляется при температурах в диапазоне от 50 до 130 С. Раствор 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида также может быть приготовлен перемещением реакционной смеси, полученной в результате химической реакции, которая содержит соединение, при необходимости, после удаления реагентов и/или побочных продуктов, в подходящем органическом растворителе согласно изобретению. Это может быть осуществлено таким образом, чтоб реакция осуществлялась в органическом растворителе или смеси растворителей, которая содержит, по крайней мере, частично предпочтительно по меньшей мере 50 мас.% подходящего растворителя для кристаллизации, при необходимости в течение проводимого действия избыточные реагенты и любые присутствующие катализаторы и любые присутствующие непригодные растворители удаляются. Получение раствора 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида по химической реакции подходящих прекурсоров этого соединения может быть осуществлено по аналогии со способами, которые описаны в существующем уровне техники, приведены в начале, к которым, таким образом, сделана полная ссылка. Кристаллизация формы В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Нпиразол-4-карбоксамида может быть осуществлена следующим образом, например: охлаждением раствора, который содержит растворенное соединение; путем добавления понижающего растворимость растворителя в раствор, который содержит растворенный 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид, в частности путем добавления неполярных органических растворителей или путем добавления воды; путем медленного концентрирования насыщенного раствора, который содержит растворенный 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид, и испарения растворителя при окружающем или пониженном давлении (от 1013 до 200 мбар), раствор перенасыщается по меньшей мере 10 мин, предпочтительно 30 мин до начала кристаллизации или путем сочетания вышеупомянутых действий. Кристаллизация, как правило, выполнена по крайней мере до выкристаллизации 80 мас.%, предпочтительно по крайней мере до 90 мас.% используемого 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенила]-2-ил)-1H-пиразол-4-карбоксамида. В режиме охлаждения кристаллизации начальная температура, как правило, находится в диапазоне между 50 и 130 С, предпочтительно между 80 и 110 С и в особенности между 75 и 90 С. Начальная температура не может быть выше, чем температура кипения растворителя. Конечная температура находится между 70 и -20 С, предпочтительно от 60 до 0 С и в особенности от 0 до 30 С. Скорость охлаждения в пределах 20 и 0,1 С/ч, предпочтительно от 15 до 2 С/ч и в особенности от 10 до 5 С/ч. Кристаллизация формы В может быть стимулирована или ускорена путем затравки зародышами кристаллов формы В, например добавив зародыши кристаллов формы В до или в ходе кристаллизации. Если зародыши кристаллов добавлены в процессе кристаллизации, их количество, как правило, составляет от 0,001 до 10 мас.%, часто от 0,005 до 5 мас.%, в частности от 0,01 до 1 мас.% и в особенности от 0,05 до 0,5 мас.% от растворенного карбоксамида. Если кристаллизация производится в присутствии зародышей кристаллов формы В, они желательно добавляются только при температуре, при которой достигается концентрация насыщения 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида в обсужденном растворителе, т.е. на уровне или ниже температуры, при которой растворенное количество 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида формирует насыщенный раствор в обсужденном растворителе. Специалист в данной области может определить температурную зависимость концентрации насыщения в растворителе при обычных экспериментах. С другой стороны, кристаллизация может также быть осуществлена путем добавления неполярных растворителей или путем добавления воды, например от 5 до 100 об.%, в частности от 20 до 80 об.% и в особенности от 30 до 60 об.% от объема полярных органических растворителей или смесей растворителей, используемых для растворения 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Нпиразол-4-карбоксамида. Добавление неполярных растворителей или добавление воды предпочтительно осуществлять на протяжении длительного периода времени, например за период от 30 мин до 3 ч, в частности за период от 40 мин до 2,5 ч. Часто это будет сделано таким образом, что неполярные растворители или вода добавляют до заметного начала кристаллизации и полученную таким образом смесь оставляют на время, в течение которого кристаллизация форма В продолжается. Если необходимо, то смесь может быть охлаждена для завершения кристаллизации. В частности, добавление неполярных растворителей или добавление воды и добавление зародышей кристаллов можно комбинировать. Добавление неполярных растворителей может быть осуществлено в форме чисто неполярных растворителей или в виде смеси неполярных растворителей с растворителем, используемым для растворения. Примерами неполярных растворителей являются алифатические и циклоалифатические углеводороды желательно с 5-10 атомами углерода, такие как пентан, гексан, циклопентан, циклогексан, изогексан,гептан, циклогептан, октан, декан или их смеси.-4 016798 Выделение формы В из продукта кристаллизации, т.е. выделение формы В из маточного раствора,осуществляется обычными методами выделения твердых компонентов из жидкостей, например путем фильтрации, центрифугирования или декантацией. Как правило, выделенное твердое тело промывают,например, растворителем, используемым для кристаллизации, водой или смесью органических растворителей, используемых для кристаллизации с водой. Промывание может быть осуществлено в один или несколько этапов, промывание водой зачастую применяется на последнем этапе промывания. Промывание обычно осуществляется при температуре ниже 30 С, зачастую ниже 25 С и, в частности, ниже 20 С для того, чтобы обеспечить как можно меньше потери ценного продукта. Далее, полученная кристаллическая форма В может быть высушена и затем предоставлена для дальнейшей обработки. Зачастую, однако, влажные активные веществ, полученные после промывания, в частности активные вещества, увлажненные водой, будут непосредственно представлены для дальнейшей обработки. В дополнение к кристаллизации из раствора форма В 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида также может быть достигнута исключительно путем нагревания аморфного соединения, его кристаллической формы А, смеси этих двух форм, а также смеси формы В с любыми или всеми ранее известными формами. Этот процесс осуществляется при температуре от 80 до 154 С, предпочтительно от 100 до 140 С и в особенности от 105 до 120 С по меньшей мере 30 мин, желательно около 1 ч. Давление реакции может быть примерно от нормального давления (1013 мбар) до 5 мбар. Предпочтительно выбрать давление от 1013 до 200 мбар, в особенности от 800 до 400 мбар. В этом случае фазовый переход занимает основное место путем сублимации, которой благоприятствует более низкое давление. С помощью кристаллизации согласно изобретению кристаллическая форма В получена с содержанием карбоксамида, как правило, по меньшей мере 90 мас.%, зачастую 94 мас.%, в частности по меньшей мере 96 мас.%. Содержание формы В от общего количества 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, как правило, не менее 90% и зачастую не менее 96%. Получение неочищенного 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Hпиразол-4-карбоксамида для производства кристаллической формы В может быть осуществлено способами, описанными в WO 2006/087343. Исходным материалом для получения кристаллической формы В может быть любая форма 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, в том числе аморфная форма, кристаллическая форма А и кристаллическая форма В. В связи с изучением и обнаружением на кристаллизации формы В аморфный 3-(дифторметил)-1 метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид и его кристаллическая форма А были охарактеризованы в деталях. В отличие от кристаллической формы В форма А и аморфный 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид не могут быть устойчиво сформулированы. Форма А. Кристаллическая форма 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Нпиразол-4-карбоксамида может быть определена рентгеновской порошковой дифрактометрией на основе фигуры дифракции (фиг. 5). Таким образом, диаграмма рентгеновской порошковой дифракции, записанная с помощью Cu-K излучения (1.54178 ) при 25 С, показывает по крайней мере 3, зачастую по меньшей мере 5 и в особенности все отражения, приведенные в следующей таблице как 2 значения или как межплоскостные расстояния d. Таблица 3 Значения 2 и d-расстояний рентгеновской дифрактограммы кристаллической формы А Кристаллическая форма А имеет блочную форму кристаллизации. Параметры элементарной ячейки и структура кристалла могут быть определены путем измерения одной кристаллической структуры. Форма А показывает моноклинную кристаллическую систему с пространственной группой Р 2(1)/с. Кристаллографические данные (измеренные при -173 С) и наиболее важные параметры приведены в табл. 4. Картина асимметричного узла и тип упаковки далее изображены на фиг. 6.-5 016798 Таблица 4 Кристаллографические данных и параметры кристаллической формы АZ - число молекул в элементарной ячейке. Кроме того, как показано на фиг. 7, форма А также показывает инфракрасный (ИК) спектр с характерными пиками примерно в 1659, 3138 и 3426 см-1. Это пики вибрации карбонильной связи (1659 см-1) и вибрации N-H связи (3138 и 3426 см-1) соответственно. Измерение температуры плавления формы А является сложным и очень легко завершается неправильно, как значение температуры плавления кристаллической формы В. Это связано с тем, что во время плавки блока в виде кристаллов формы А происходит фазовое превращение и ДСК (дифференциальная сканирующая калориметрия) измерение плавления эндотерма формы А легко маскируется под экзотерм,что связанно с фазовым превращением и кристаллизацией вновь выявленной формы В. Скорость нагрева является важнейшим параметром в таких методах и существенно различные ДСК следовые количества получаются при различных скоростях нагрева (см. фиг. 8-10). При очень низкой скорости нагрева(2 С/мин) плавление и фазовые превращения формы А в форму В не могут быть обнаружены и в основном изображен только пик плавления формы В. С более высокой скоростью нагрева (см. фиг. 9 и 10) плавление эндотерма формы А становится видимым и может быть ясно видно на фиг. 10 со скоростью нагрева 10 С/мин. На фиг. 10 плавление формы А прямо сопровождается кристаллизацией формы В и в конце плавлением формы В. Другие экспериментальные факторы, влияющие на качество ДСК измерений формы А, включают массу образца, размер частицы, присутствие примесей, форму кристаллических частиц и присутствие ядер или кристаллы-затравки различных полиморфов (см. также J. Bernstein, Polymorphism in Molecular Crystals, IUCR Monographs of crystallography, Oxford University Press, 2002, p. 104111). Форма А отображает термограмму с характерными пиками плавления в районе 138 и 145 С. Пик максимума обычно лежит в диапазоне от 142 до 144 С. Температура плавления, определяемая как начало пика плавления, как правило, лежит в диапазоне примерно от 142 до 144 С. Значения, указанные здесь,относятся к значениям, определяемым дифференциальной калориметрией (дифференциальная сканирующая калориметрия: ДСК, открытая алюминиевая чаша, скорость нагрева 10 К/мин). Кристаллическая форма А 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Hпиразол-4-карбоксамида может быть получена быстрым испарением с образованием кристаллов из растворителя такого, как дихлорметан, толуол и монохлорбензол, или быстрой кристаллизацией охлаждения тех же растворителей. Исходным материалом для подготовки формы А может быть любая форма 3-(дифторметил)-1 метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида, в том числе аморфная форма,кристаллическая форма А и кристаллическая форма В. Аморфные карбоксамиды. Аморфная форма 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида может быть охарактеризована, например, рентгеновской порошковой дифракцией. В рентгеновской порошковой дифрактограмме аморфная форма дает лишь фоновый сигнал без каких-либо значительных сигналов типичных для кристаллического материала. В другом аспекте, аморфная форма превращается при комнатной температуре медленно в кристаллическую форму А или обычно в смеси формы А и формы В. Превращение не может быть легко контролировано, но переход может быть направлен к форме В при помощи повышенных температур хранения. Фазовое превращение можно увидеть, например, при помощи ДСК измерения или под печью с микроскопом. Аморфная форма 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида может быть получена осаждением или выпариванием небеспримесного материала (чистотой менее 70%) или плавлением любой его кристаллической формы и охлаждением плавления до ком-6 016798 натной температуры. При нагревании аморфная форма кристаллизуется в форму А или форму В или в смеси этих двух форм. Превращение может быть ускорено путем нагревания или при повышенной степени влажности или при непосредственном контакте с растворителями. В типичных измерениях температура плавления превращения аморфной формы в одну из кристаллических форм А или В, или смеси этих двух форм, составляет от 95 до 130 (фиг. 10 и 11). Как и в случае ДСК измерения кристаллической формы А, ДСК измерения аморфной формы сильно зависит от параметров измерения. При скорости нагрева типичной для измерений температуры плавления (10 С/мин,см. фиг. 11) пики максимумов для процесса кристаллизации будут, например, около 115 С. В визуальных или автоматических измерениях температуры плавления эта точка может быть неверно истолкована, как температура плавления. Риску неправильного толкования весьма способствует тот факт, что аморфная форма 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида легко возгоняется при этой температуре, давая плавление как визуальный эффект. Это описание вместе с описанием температурного режима кристаллической формы А показывает,что тепловые методы и измерение точки плавления не могут быть использованы, чтобы убедительно показать фактически существующее изменение при комнатной температуре. Когда применяются тепловые методы в характеристике твердой фазы форм 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]2-ил)-1 Н-пиразол-4-карбоксамида, крайне важно использовать также сравнительный метод (например,порошковая дифракция или ФТ ИК-спектрометрия). Аморфная форма 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамид также может быть получена с помощью кристаллизации раствора, особенно если присутствуют примеси. Исходный материал, используемый для получения аморфной формы может быть любой формы 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, в том числе кристаллической формы А и кристаллической формы В, а также его аморфной формы. Смеси формы А и формы В с аморфным карбоксамидом. Кристаллическая форма В иногда фигурирует в смеси с формой А (фиг. 14). Однако названные смеси являются неблагоприятными для целей разработки. При использовании затравки с кристаллами формы В можно значительно способствовать формированию формы В, например, в толуоле. Подробное описание фигур Следующие фигуры и примеры служат для иллюстрации изобретения и не должны рассматриваться как ограничение. Фиг. 1 показывает характерную диаграмму рентгеновской порошковой дифракции кристаллической формы В. Диаграмма рентгеновской дифракции формы В была записана дифрактометром Bruker AXSCo.D-5000 в геометрии отражения в диапазоне от 2=2-40 с шириной шага 0,02 с применением Cu-K излучения (1,54178 ) при 25 С. Фиг. 2 показывает фигуру монокристаллической структуры формы В. Асимметричная единица изображена на левой стороне, упаковка кристалла - справа. Данные рентгеновской дифракции для кристаллической формы В собирались на синхротроне SLS (Villingen, Швейцария) на РХ Beamline. Структура была решена с применением прямых методов, улучшена и расширена с помощью метода Фурье с комплектом программного обеспечения SHELX (G.M. Sheldrick, SHELX-97, University of Goettingen, 1997). Фиг. 3 показывает ФТ ИК-спектр кристаллической формы В. Образец был приготовлен как KBrгранулы и спектр был записан в ФТ ИК-спектрометре (например, Nicolet Magna) в режиме передачи(Т=25 С, 32 сканирования, разрешающая способность 4 см-1). Фиг. 4 показывает ДСК кривую формы В с максимумом эндотерма плавления около 157 С, измеренного с помощью Mettler Co. Mettler Toledo ДСК 25 со скоростью нагрева 10 С/мин в диапазоне от 30 до 200 С. Образец весом от 5 до 10 мг. Фиг. 5 показывает диаграмму рентгеновской порошковой дифракции кристаллической формы А. Диаграмма рентгеновской дифракции формы А была записана дифрактометром Bruker AXS Co. D-5000 в геометрии отражения в диапазоне от 2=2-40 с шириной шага 0,02 с применением Cu-K излучения(1,54178 ) при 25 С. Фиг. 6 показывает фигуру монокристаллической структуры формы В. Асимметричная единица изображена на левой стороне и упаковка кристалла справа. Данные рентгеновской дифракции для кристаллической формы А собирались Bruker AXS CCD детектором, с применением граффитомонохроматизированного Cu-K излучения (1,54178 ). Структура была решена с помощью прямых методов, улучшена и расширена с помощью метода Фурье с комплектом программного обеспеченияSHELX (G.M. Sheldrick, SHELX-97, Университет Геттингена, 1997). Фиг. 7 показывает ФТ ИК-спектр кристаллической формы В. Образец был подготовлен как KBrгранулы и спектр был записан в ФТ ИК-спектрометре (например, Nicolet Magna) в режиме передачи(Т=25 С, 32 сканирования, разрешающая способность 4 см-1). Фиг. 8-10 показывают две существенно отличающиеся ДСК-кривые формы А. Фиг. 8 представляет измерение со скоростью нагрева 2 С/мин и показывает только плавление около 156 С. На этой диаграм-7 016798 ме плавление формы А фактически замаскировано с одновременной кристаллизацией формы В. Плавление формы А может, однако, быть уже обнаружено при 5 С/мин измерении (фиг. 9) и очень хорошо при 10 С/мин измерении (фиг. 10). Последние показывают эндотерму плавления около 145 С формы А, что сопровождается мгновенной кристаллизацией экзотерма до формы В и, наконец, с плавлением эндотерма формы В. ДСК-кривые были измерены с Mettler Co. Mettler Toledo ДСК 25 со скоростями нагрева 2, 5 и 10 К/мин в диапазоне от 30 до 200 С. Образцы весом от 5 до 10 мг. Фиг. 11 и 12 показывают ДСК-термограммы аморфного 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида со скоростями нагрева 2 и 10 К/мин соответственно. Фиг. 11 сначала показывает кристаллизацию экзотерма из аморфного соединения в кристаллическую форму А, форму В или смеси этих двух форм при около 100-120 С. Пик плавления формы А не наблюдается, в то время как пик плавления форма В присутствует. В связи с возможным фазовым превращением из кристаллической формы А в форму В и маскирующими эффектами при медленной скорости нагрева (см. описание фиг. 7 и 8) никакое заключение относительно наличия кристаллической формы не возможно только на основе этого измерения. На фиг. 12 (скорость нагрева 12 К/мин) может быть видна кристаллизация аморфной формы. После этого ДСК похож на форму А со скоростью нагрева 10 К/мин, давая первое плавление формы В, а затем кристаллизацию формы В и затем плавление формы В. ДСК-кривые были измерены Mettler Co. Mettler Toledo ДСК 25 со скоростью нагрева 10 К/мин в диапазоне от 25 до 140 С. Образцы весом от 5 до 10 мг. Фиг. 13 показывает диаграмму рентгеновской порошковой дифракции из смеси кристаллических форм А и В. Диаграмма рентгеновской дифракции смеси форм А и В были записаны дифрактометромBruker AXS Co. D-5000 в геометрии отражения в диапазоне от 2=2-40 с шириной шага излучения 0,02 с применением Cu-K излучения (1,54178 ) при 25 С. Фиг. 14 показывает изображение эксперимента нагревания с печью с микроскопом аморфного 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Этот эксперимент нагревания проводился на аморфной пленке (черная часть изображения) со скоростью нагрева 5 С/мин. Во время отображения температура была 115 С. Одновременная кристаллизация аморфной формы к форме А и форме В может быть хорошо видна. Измерения проводились на печи с микроскопомMettler. Фиг. 15 показывает микрофотографии тестов композиции с формой А (композиция I) и формой В(композиция II). Настоящее изобретение далее иллюстрируется следующими примерами. Пример 1. Получение кристаллической формы В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1 Н-пиразол-4-карбоксамида кристаллизацией из реакционной смеси. 9,55 кг 3',4',5'-трифтор[1,1'-бифенил]-2-иламина(I) растворяют в 51,4 кг толуола и добавляют 6 кг пиридина. Смесь перемешивают при 45 С и 8,3 кг 3-(дифторметил)-1-метил-1H-пиразол-4-карбонил хлорида(II) дозируют в течение 1 ч. В связи с экзотермической природой реакции температура повышена до 55 С. После реакции перемешивание продолжается в течение 1 ч при 55 С. Затем продолжалась тройная экстракция при температуре 85 С с 16 л соляной кислоты (5%), 14 л гидрокарбонат натрия (8%) и 14 л деионизированной воды. Полученный в результате чистый раствор охлаждают в толуоле от 85 С со скоростью 10 С/ч до 0 С. Около 75 С наблюдается первое помутнение, и при 75 и 73 С соответственно порция была затравлена 10 г 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Нпиразол-4-карбоксамида(III) каждая (98% форма В). Полученная в результате суспензия фильтруется при температуре 0 С в процессе фильтрации и осадок на фильтре промывают 10 кг толуола при 0 С. После высушивания в сушильной камере при температуре 80 С и 20 мбар в течение 12 ч, 13,5 кг 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида(III) 99,5% чистоты (ГХ, ВЭЖХ, ЯМР) были отделены. Используя порошковую дифрактометрию (ПРД) и инфракрасную спектрометрию преобразования Фурье твердого тела (ФТ-ИК) было доказано, что материал состоит на 98% из формы В. Пример 2. Получение кристаллической формы В кристаллизацией из органических растворителей с охлаждением. 615 г 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида растворяют при 85 С в 2,5 л кипящего толуола в испытательном сосуде. Раствор охлаждают от 85 до 25 С со скоростью нагрева 1 С/ч. Перемешивание не применяют. Длинные, как иглы, кристаллы (длина кристалла равна 1-2 см) были отделены декантацией. Измерения рентгеновской структуры монокристалла показали, что кристаллическая модификация была формы В. Пример 3. Получение формы В кристаллизацией из органических растворителей путем испарения. Насыщенный раствор около 1 г 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)1H-пиразол-4-карбоксамида (чистота 95%) в метаноле был приготовлен в испытательном сосуде близко-8 016798 точки кипения растворителя. Испытательный сосуд был помещен в комнатную температуру с проколотой крышкой, позволяя растворителю медленно испаряться. Таким образом, 3-(дифторметил)-1-метил-N(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид был получен в течение 2 недель в виде кристаллов, которые были отделены и проанализированы рентгеновской порошковой дифрактометрией(ПРК) и дифференциальной сканирующей калориметрией (ДСК). На основании характерных отображений была идентифицирована форма В. Тот же эксперимент, в результате которого была получена форма В, может быть повторен также и в этаноле, 2-пропаноле, уксусной кислоте, тетрагидрофуране, ацетонитриле, нитрометане, диметилсульфоксиде, метилэтилкетоне, метилизобутилкетоне, пиридине и толуоле. Пример 4. Получение формы В кристаллизацией из органических растворителей путем испарения. 1 г формы А растворяют в 20 мл ацетофенона при 100 С в круглой колбе. Растворитель выпаривали с применением потока азота на поверхности раствора. После всего растворитель выпаривали, кристаллический образец был проанализирован на соответствие форме В, порошковой дифрактометрией (ПРК). Тот же опыт может также осуществляться с 1,2-дихлорбензолом и диэтилкетоном. Пример 5. Получение чистой формы В нагреванием. 2 кг 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида,что согласно рентгеновской порошковой дифрактометрии содержит 10% формы А, нагревают в печи при температуре 115 С при 800 мбар в течение 16 ч. Полученное в результате твердое тело было проанализировано (с помощью ПРД и ДСК) на соответствие 98% чистой формы В. Пример 6. Получение чистой формы В нагреванием. 1 г чистой формы А нагревают в печи при температуре 110 С и нормальном давлении в течение 24 ч. Полученное в результате твердый продукт был проанализирован (с помощью рентгеновской дифракции и ДСК) на соответствие 98% чистой формы В. Сравнительный пример 7. Получение формы А кристаллизацией из толуола и монохлорбензола при пониженном давлении (не согласно изобретению). 5 г 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида(чистота 95%) растворяют в 50 мл монохлорбензола в круглодонной колбе при 100 С. Растворитель выпаривают при пониженном давлении стандартным лабораторным роторным испарителем при температуре 70 С. После всего растворитель был выпарен, полученное в результате твердый продукт проанализирован с помощью рентгеновской порошковой дифрактометрии (ПРК). На основании характерных отображений была идентифицирована форма А. Сравнительный пример 8. Получение формы А кристаллизацией из дихлорметана (не согласно изобретению). 200 мг формы А растворяют в 3 мл дихлорметана при около 35 С в небольшой стеклянной пробирке. Растворитель оставили до испарения при нормальном давлении при температуре 30 С. Эксперимент привел к получению блочных кристаллов, которые мы подтвердили рентгеновскими измерениями монокристала, что они имеют форму А. Сравнительный пример 9. Получение аморфного карбоксамида. Образец 1 г кристаллической формы А был помещен в печь в круглой колбе при температуре 160 С на 20 мин. Плавленый 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамид затем перемещен в комнатную температуру и оставлен для охлаждения. Полученный материал в виде аморфной пленки не давал дифракционной картины в измерении порошковой дифракции. Сравнительные эксперименты произведены как смеси форм А и В. Сравнительный пример 10. Насыщенный раствор около 300 мг 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2 ил)-1 Н-пиразол-4-карбоксамида (чистота 95%) в диэтиловом эфире был приготовлен при комнатной температуре. Растворитель оставили испарится при 30 С из открытой стеклянной пробирки. Полученный в результате кристаллический материал был проанализирован с помощью порошковой рентгеновской дифрактометрии на соответствие смеси формы А и В (см. Фигура 10 для характеристики ПРК). Сравнительный пример 11. Эксперимент, подобный на пример 10, был проведен с толуолом. Испарение растворителя заняло несколько дней, после чего твердый кристаллический образец был проанализирован. Согласно порошковой рентгеновской дифрактометрии в нем содержалась смесь формы А и В. Пример 12 и 13. Суспензионные примеры, подтверждающие стабильность формы В. Форма, о которой идет речь или смеси различных форм 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида были суспендированы в воде при 30 С. Смесь выдерживали при этой температуре и перемешивали магнитной мешалкой.-9 016798 Пример 12. После 1 дня в этих условиях аморфная форма была превращена (на основании ПРК анализа) в форму В. Пример 13. После 2 дней в этих условиях кристаллическая форма была превращена (на основании ПРК анализа) в форму В. Примеры 14 и 15. Примеры композиций, подтверждающие устойчивость кристаллической формы В. Устойчивость кристаллических форм была протестирована путем составления смеси формы А или формы В согласно примерам 1 и 2 и анализа стабильности композиции в форме седиментации, роста размера частиц и изменения в кристаллической модификации. Пример 14.SC состав, содержащий кристаллическую форму 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Был приготовлен SC состав I, имеющий композиции, изображенные в табл. 5. Таблица 5 Композиция SC состава I Оставшееся количество воды помещают в подходящий контейнер. Активный компонент, смачивающий агент, диспергатор, консервант, антифризный агент смешивают с водой. К этому приготовлению добавляют активный компонент и часть антипенообразователя. Затем смесь помещают в шаровую мельницу (такую как Dyno-Mill типа из Bachofen, Швейцария) с достаточной загрузкой слоя для обеспечения эффективной молотьбы. Охлаждающее устройство прикрепляется к борту мельницы для обеспечения надлежащего охлаждения устройства во время молотьбы. Молотьба останавливается, когда полученное распределение размера частиц соответствует требуемому (измерено с помощью Malvern Mastersizer 2000). К композиции добавляют оставшееся количество антипенообразователя, а также загуститель при перемешивании для обеспечения равномерного распределения компонентов. Пример 15.SC состав, содержащий кристаллическую форму В 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Подобный SC состав была приготовлен, как описано в примере 14, но используя форму В (состав Оценка составов. Полученные составы были оценены по их стабильности при хранении при температуре 40 С в течение одной недели. Микроизображения состава были взяты до и после хранения при температуре 40 С,чтобы показать изменения размера частиц. Дисперсионная стабильность была оценена, используя 2% раствор состава в воде в коническом цилиндре. Объем седиментации записан после 2 ч отстаивания. Осадок был собран и проанализирован с помощью ДСК и порошковой дифракционной дифрактометрии,чтобы охарактеризовать твердый осадок (давая тем самым подтверждение количеству осадка и кристал- 10016798 лическим изменениям, присутствующим в осаждении). Результаты, приведенные в табл. 7, а также на фиг. 15 наглядно демонстрируют, что состав примера 14 с формой А был нестабилен и значительно более осажден и вырос размер кристаллитов по сравнению с составом в примере 15 с формой В. В дальнейшем может быть показано путем ДСК и ПРД измерений, что приготовленная форма А,претерпевшая фазовое превращение, была преобразована в полной мере в игловидные кристаллы формы В. Переход из формы А в форму В привел к полной кристаллизации активного компонента в составе. Это на практике будет весьма неблагоприятным и будет причиной засорения выпускного отверстия во время применения и неоднородного распределения активного компонента в составе. Состав по примеру 15 с формой В в качестве исходного материала был, наоборот, стабильным в показателях седиментации, размера частиц, а также кристаллической модификации. Таблица 7 Аналитика составов% мас./мас. частиц менее 2 мкм. максимальный размер частиц. Фунгицидные составы и использование кристаллической формы В Так же как аморфный 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол 4-карбоксамид и его кристаллическая форма А форма В подходит в качестве фунгицида. Тем не менее,она превосходит его с точки зрения его обработки и особенно свойств состава. Таким образом, изобретение относится также к средствам защиты растений, содержащим кристаллическую форму В вместе с вспомогательными составами, обычными для составов средств защиты растений, в частности средства защиты растений в виде водных суспензионных концентратов (так называемые SC) или безводных суспензионных концентратов (так называемые OD), и средства защиты растений в виде порошка (так называемые WP) и гранул (так называемые WG), диспергируемых в воде. Изобретение также относится к способу борьбы с нежелательным ростом растений, который отличается тем, что кристаллическая форма В, предпочтительно приготовленная в виде подходящего активного вещества, применяется на растениях, их месте распространения и/или семенах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамид демонстрирует отличную активность против широкого спектра фитопатогенных грибков, в частности из класса Ascomycetes, Deuteromycetes, Basidiomycetes и Peronosporomycetes (син. Oomycetes) и несовершенные грибы. Некоторые из них являются систематически активными и могут быть использованы в защите урожая как лиственные фунгициды, как фунгициды для протравливания семян и грунтовые фунгициды. Форма В имеет особенно важное значение для борьбы с большим количеством грибов на различных сельскохозяйственных культурах, таких как пшеница, рожь, ячмень, тритикале, овес, рис, кукуруза, трава, бананы, хлопок, соя, кофе, сахарный тростник, виноград, плодовые и декоративные растения и овощей, таких как огурцы, фасоль, томаты, картофель, тыква, а также на семенах этих растений. Они также могут быть использованы в посевах, которые выносливы против нападения насекомых или грибков или гербицидов, появляющихся вследствие разведения, в том числе методов генной инженерии. Кроме того,они подходят для контроля видов Botryosphaeria, видов Cylindrocarpon, Eutypa lata, Neonectria liriodendri и Stereum hirsutum, которые поражают, в частности, древесину или корни винограда. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Alternaria на овощах, семенах рапса, сахарной свекле,фруктах, рисе, соевых бобах, на картофеле (например, A. solani или A. alternata) и помидорах (например,A. solani или А. alternata) и Alternaria ssp. (черный колос) на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Aphanomyces на сахарной свекле и овощах. Форма В 3(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида подходит для борьбы с видами Ascochyta на зерновых и овощах, например Ascochyta tritici (пятнистость листьев) на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Bipolaris и Drechslera на кукурузе (например, D. Maydis),зерновых, рисе и газонах. 2)- 11016798 Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Blumeria graminis (мучнистая роса) на зерновых (например,пшеница или ячмень). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Botrytis cinerea (серая плесень) на клубнике, овощах, цветах,винограде и пшенице (плесень на колосе). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для контроля Bremia lactucae на листьях зеленого салата. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Cercospora на кукурузе, рисе, сахарной свекле и, например,Cercospora sojina (пятнистость листьев) или Cercospora kikuchii (пятнистость листьев) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видом Cladosporium herbarum (черный колос) на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Cochliobolus на кукурузе, зерновых (например, Cochliobolussativus) и рисе (например, Cochliobolus miyabeanus). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Colletotricum на хлопке и, например, Colletotrichum truncatum (Antracnose) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видом corynespora cassiicola (пятнистость листьев) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видом Dematophora necatrix (гниль на корне/стебле) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Diaporthe phaseolorum (поражение стебля) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Drechslera, видами Pyrenophora на кукурузе, зерновых, рисе и газоне, на ячмене (например, D. teres) и пшенице (например, D. tritici-repentis). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Esca на винограде, вызванной Phaeoacremonium chlamydosporium,Ph Aleophilum и Formitipora punctata (син. Phellinus punctatus). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Elsinoe ampelina на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Epicoccum spp. (черный колос) на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Exserohilum на кукурузе. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Erysiphe cichoracearum и Sphae-rotheca fuliginea на огурцах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Fusarium и Verticillium на различных растениях, например, F.graminearum или F.culmorum (корневая гниль) на зерновых (например, пшенице или ячмене) или, например, F. oxysporum на помидорах и Fusarium solani (поражение стебля) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Gaeumanomyces graminis (черный корень) на зерновых культурах(например, пшенице или ячмене). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Gibberella на зерновых и рисе (например, Gibberella fujikuroi). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Glomerella cingulata на винограде и других растениях. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Grainstaining complex на рисе. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видом Guignardia budwelli на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Helminthosporium на кукурузе и рисе. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы Isariopsis clavispora на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Macrophomina phaseolina (гниль на корне/стебле) на соевых бобах.- 12016798 Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Michrodochium nivale (снежная плесень) на зерновых культурах (например, пшенице или ячмене). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Microsphaera Diffusa (мучнистая роса) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Mycosphaerella на зерновых, бананах и арахисе, такие как,например, М. graminicola на пшенице или М. fijiensis на бананах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Peronospora на капусте (например, P. brassicae), луковичных растениях (например, P. destructor) и, например, Peronospora manshurica (ложная мучнистая роса) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Phakopsara pachyrhizi (соевая ржавчина) и Phakopsara meibomiae(соевая ржавчина) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Phialophora gregata (поражение стебля) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Phomopsis на подсолнечниках, виноградах (например, P.viticola) и соевых бобах (например, Phomopsis Phaseoli). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамид подходит для борьбы с видами Phytophthora на различных растениях, например, P. capsici на сладком перце, Phytophthora megasperma (гниль на листе/стебле) на соевых бобах, Phytophthora infestans на картофеле и помидорах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Plasmopara viticola на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Podosphaera leucotricha на яблоках. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Pseudocercosporella herpotrichoides (глазковая пятнистость) на зерновых (пшеница или ячмень). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Pseudoperonospora на различных растениях, например, P. Cubensis на огурцах или P. humili на хмеле. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Pseudopezicula tracheiphilai на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Puccinia на различных растениях, например, P. triticina, P.striformins, P. hordei или P. graminis на зерновых (например, пшенице или ячмене), или на спарже (например, P. asparagi). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Pyricularia oryzae, Corticium sasakii, Sarocladium oryzae, S. attenuatum, Pyrenophora tritici-repentis (пятнистость листьев) на пшенице или Pyrenophora teres (сетчастая пятнистость) на ячмене. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида для борьбы с Entyloma oryzae на рисе. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Pyricularia grisea на газонах и зерновых. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видом Pythium spp. на газонах, рисе, кукурузе, пшенице, хлопке,рапсе, подсолнечниках, сахарной свекле, овощах и других растениях (например, P. ultiumum или P. aphanidermatum). Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Ramularia collo-cygni (Ramularia/солнечные ожоги/ физиологические пятна на листьях) на ячмене. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Rhizoctonia на хлопке, рисе, картофеле, газоне, кукурузе,рапсе, картофеле, сахарной свекле, овощах и различных растениях, например, Rhizoctonia solani (гниль на корне/стебле) на соевых бобах или Rhizoctonia cerealis (сильная глазковая пятнистость) на пшенице или ячмене. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Rhynchosporium secalis на ячмене (пятнистость листьев), ржи, три- 13016798 тикале. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Sclerotinia на рапсе и подсолнечниках и, например, Sclerotinia sclerotiorum (поражение стебля) или Sclerotinia rolfsii (поражение стебля) на соевых бобах. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Septoria Glycines (пятнистость листьев) на соевых бобах. В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 Форма карбоксамида подходит для борьбы с Septoria tritici (лиственный септорий) и Stagonospora nodorum на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Erysiphe (син. Uncinula) Necator на винограде. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Setospaeria на кукурузе и газоне. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с Sphacelotheca reilinia на кукурузе. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с Stagonospora nodorum (септорий колоса) на пшенице. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Thievaliopsis на соевых бобах и хлопке. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы с видами Tilletia на зерновых. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида подходит для борьбы Typhula incarnata (снежная гниль) на пшенице и ячмене. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Ustilago на зерновых, кукурузе (например, U. maydis) и сахарном тростнике. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида подходит для борьбы с видами Venturia (парша) на яблоках (например, V. Inaequalis) и груше. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида также подходит для борьбы с вредными грибками в защите материалов (например, древесины, бумаги, дисперсных красок, волокон или тканей) и в защите хранимой продукции. В защите древесины, особое внимание уделяется следующим вредным грибам: Ascomycetes, такие как Ophiostoma spp.,Ceratocystis spp., Aureobasidium pullulans, Sclerophoma spp., Chaetomium spp., Humicola spp., Petriella spp.,Trichurus spp.; Basidiomycetes, такие как Coniophora spp., Coriolus spp., Gloeophyllum spp., Lentinus spp.,Pleurotus spp., Poria spp., Serpula spp. и Tyromyces spp., Deuteromycetes, такие как Aspergillus spp.,Cladosporium spp., Penicillium spp., Trichoderma spp., Alternaria spp., Paecilomyces spp. и Zygomycetes, такие как Mucor spp., дополнительно в защите материалов от следующих дрожжей: Candida spp. и Saccharomyces cerevisae. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамид применяется путем обработки грибов или растений, семян или материалов для защиты от грибков или почвы фунгицидно эффективным количеством активного компонента. Применение может быть как до, так и после заражения материалов, растений и семян грибками. Соответственно, изобретение, кроме того, относится к способу борьбы с фитопатогенными грибами, в котором грибы или материалы, растения, грунт и семена с целью их защиты от поражения грибками обрабатывают эффективным количеством формы В 3-(дифторометил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида. Кроме того, изобретение относится к композиции для борьбы с фитопатогенными грибами, в состав которой входит форма В 3-(дифторометил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол 4-карбоксамида и по крайней мере один твердый или жидкий носитель. Фунгицидные композиции в основном содержат от 0,1 до 95 мас.%, предпочтительно от 0,5 до 90 мас.% активного компонента. При применении для защиты растений, нормами нанесения являются в зависимости от желаемого эффекта от 0,01 до 2,0 кг активного компонента на гектар. При обработке семян, необходимое количество активного компонента составляет, как правило, от 1 до 1000 г/100 кг семян, предпочтительно от 5 до 100 г/100 кг семян. При применении для защиты материалов или хранящихся продуктов, нормы нанесения активного компонента зависят от вида области нанесения и желаемого эффекта. Количества, как правило, применяемые для защиты материалов, составляют, например, от 0,001 г до 2 кг, предпочтительно от 0,005 до 1 кг активного компонента на кубический метр обрабатываемого материала. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4- 14016798 карбоксамида может быть преобразована в обычные составы, например, растворы, эмульсии, суспензии,дусты, порошки, пасты и гранулы. Форма применения зависит от конкретной цели, в каждом отдельном случае, она должна обеспечить хорошее и равномерное распределение соединения согласно изобретению. Составы приготавливают известным способом, например путем разбавления активного компонента растворителями и/или носителями, при желании использую эмульгаторы и диспергаторы. Подходящими растворителями/добавками для этой цели являются, главным образом: вода, ароматические растворители (например, продукты Solvesso, ксилол), парафины (например,фракции минерального масла), спирты (например, метанол, бутанол, пентанол, бензиловый спирт), кетоны (например, циклогексанон, гамма-бутиролактон), пирролидоны (N-метилпирролидон, Nоктилпирролидон), ацетаты (диацетат гликоль), гликоли, диметиламиды жирных кислот, жирные кислоты и сложные эфиры жирных кислот. В принципе, смеси растворителей также могут использоваться; носители, такие как грунтовые природные минералы (например, каолины, глины, тальк, мел) и измельченные синтетические минералы (например, мелкодисперсный кремнезем, силикаты); эмульгаторы такие как неионогенные и анионные эмульгаторы (например, полиоксиэтиленовые эфиры жирных спиртов, алкилсульфонаты и арилсульфонаты), и диспергаторы, такие как сульфитные щелоки лигносульфита и метилцеллюлоза. Подходящими для применения в качестве поверхностно-активных веществ являются щелочной металл, щелочно-земельный металл и соли аммония лигносульфоновой кислоты, нафталинсульфоновая кислота, фенолсульфоновая кислота, дибутилнафталинсульфоновая кислота, алкиларилсульфонаты, алкилсульфаты, алкилсульфонаты, сульфаты жирных спиртов, жирные кислоты и гликолевые эфиры сульфатированных жирных спиртов, кроме того конденсаты сульфированного нафталина и производные нафталина с формальдегидом, конденсаты нафталина или нафталинсульфоновой кислоты с фенолом и формальдегидом, эфир полиоксиэтилен октилфенила, этоксилированный изооктилфенол, октилфенол,нонилфенол, простые алкилфенилполигликолевые эфиры, простые эфиры трибутилфенилполигликоля,простой эфир тристеарилфенилполигликоля, алкиларилполиэфирные спирты, конденсаты спирта и жирного спирта этиленоксида, этоксилированное касторовое масло, полиоксиэтиленалкильные эфиры, этоксилированный полиоксипропилен, ацеталь лаурилового спирта полигликолиевого эфира, сложные эфиры сорбитола, сульфитные щелоки лигносульфита и метилцеллюлоза. Подходящими для получения непосредственно распыляемых растворов, эмульсий, паст или дисперсных масел являются фракции минеральных масел от средней до высокой температуры кипения, такие как керосин или дизельное топливо, кроме того, каменноугольные масла и масла растительного или животного происхождения, алифатические, циклические и ароматические углеводороды, например толуол, ксилол, парафин, тетрагидронафталин, алкилированные нафталины или их производные, метанол,этанол, пропанол, бутанол, циклогексанол, циклогексанон, изофорон, сильно полярные растворители,например диметилсульфоксид, N-метилпирролидон и вода. Порошки, материалы для разбрасывания по поверхности и поддающиеся распылению продукты могут быть приготовлены путем смешивания или одновременного измельчения активных веществ с твердым носителем. Гранулы, например покрытые гранулы, пропитанные гранулы и однородные гранулы, могут быть приготовлены путем связывания активных компонентов с твердыми носителями. Примерами твердых носителей являются минеральные земли, такие как силикагели, силикаты, тальк, каолин, аттапульгит,известняк, известь, мел, бол, лесс, глина, доломит, диатомовая земля, сульфат кальция, сульфат магния,оксид магния, земляные синтетические материалы, удобрения, такие как, например, сульфат аммония,фосфат аммония, аммиачная селитра, мочевины, а также продукты растительного происхождения, такие как зенрновая мука, мука древесной коры, древесная мука и мука ореховой скорлупы, целлюлозные порошки и другие твердые носители. В основном составы содержат от 0,01 до 95 мас.%, предпочтительно от 0,1 до 90 мас.% активного компонента. Активные компоненты применяются в чистоте от 90 до 100%,предпочтительно от 95 до 100% (по данным ЯМР спектра). Предпочтительное воплощение изобретения относится к жидким составам формы В. В добавок к активной фазе твердого вещества они имеют по крайней мере одну жидкую фазу, в которой 3-(дифторометил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид присутствует в форме В в виде высокодисперсных частиц. Возможной жидкой фазой в основном является вода и органические растворители, в которых форма В лишь незначительно растворима или нерастворима, например такие, в которых растворимость формы В при 25 С и 1013 мбар составляет не более 1 мас.%, в частности не более 0,1 мас.% и особенно не более 0,01 мас.%. Согласно первому предпочтительному воплощению жидкая фаза состоит из воды и водных растворителей, т.е. смесей растворителей, которые в добавок к воде также содержат до 20 мас.%, предпочтительно не более 10 мас.% от общего количества воды и растворителей, один или более органических растворителей смешивающихся с водой, например простые эфиры, смешивающиеся с водой, такие как тетрагидрофуран, метилгликоль, метилдигликоль, алканолы, такие как изопропанол или полиолы, такие как гликоль, глицерин, диэтиленгликоль, пропиленгликоль и т.п. Такие составы также упоминаются ниже- 15016798 как концентраты суспензий (SC). Такие концентраты суспензий содержат 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]2-ил)-1H-пиразол-4-карбоксамид как форму В в виде мелкодисперсных частиц, в которой частицы формы В присутствуют суспендированными в водной фазе. Размер частиц активного вещества, т.е. частиц,которые не превышают 90 мас.% активного вещества, обычно составляет меньше 30 мкм, в частности меньше 20 мкм. Преимущественно в SC согласно изобретению по крайней мере 40 мас.% и, в частности,по меньшей мере 60 мас.% частиц имеют диаметр меньше 2 мкм. В таких SC количество активного вещества, т.е. общее количество карбоксамида и других активных веществ в случае необходимости, как правило, находится в диапазоне от 10 до 70 мас.%, в частности в диапазоне от 20 до 50 мас.% от общей массы концентрата суспензии. В добавок к активному веществу водные концентраты суспензий обычно содержат поверхностноактивные вещества, а также при необходимости пеногасители, загустители (модификаторы реологии),антифризные агенты, стабилизаторы (биоциды), агенты для корректировки рН и предотвращающие слеживание агенты. Возможными поверхностно-активными веществами являются ранее называвшиеся поверхностноактивные вещества. Предпочтительно водные средства защиты растений согласно изобретению содержат по крайней мере один из ранее названных анионных поверхностно-активных веществ и при необходимости один или более неионогенных поверхностно-активных веществ, при необходимости в комбинации с защитным коллоидом. Количество поверхностно-активных веществ, как правило, составляет от 1 до 50 мас.%, в частности от 2 до 30 мас.% от общей массы водных SC согласно изобретению. Предпочтительно поверхностно-активные вещества содержат по крайней мере одно анионное поверхностноактивное вещество и по крайней мере одно неионогенное поверхностно-активное вещество, и пропорции анионного к неионогенному поверхностно-активному веществу, как правило, находятся в диапазоне от 10:1 до 1:10. Относительно природы и количества пеногасителей, загустителей, антифризных агентов и биоцидов применяется то же, что указано выше. В случае необходимости, водные SC согласно изобретению могут содержать буферы для регулировки рН. Примерами буферов являются соли щелочных металлов слабых неорганических и органических кислот, таких как, например, фосфорная кислота, борная кислота, уксусная кислота, пропионовая кислота, лимонная кислота, фумаровоя кислота, винная кислота, щавелевая кислота и янтарная кислота. Согласно первому предпочтительному воплощению жидкая фаза состоит из безводных органических растворителей, в которых растворимость формы В 3-(дифторометил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида при 25 С и 1013 мбар составляет не более 1 мас.%, в частности не более 0,1 мас.% и в особенности не более 0,01 мас.%. Они включают, в частности, алифатические и циклоалифатические углеводороды и масла, в частности, растительного происхождения, а также сложные эфиры С 1-С 4 алкила насыщенных или ненасыщенных жирных кислот или смесей жирных кислот, в частности сложные метиловые эфиры, например метилолеат, метилстеарат и сложный метиловый эфир рапсового масла, а также парафиновые минеральные масла и т.п. Соответственно, настоящее изобретение относится также к средствам защиты растений в форме безводного концентрата суспензии, который также будет ниже именоваться как ДМ (дисперсия в масле). Такие ДМ содержат форму В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида в виде мелкодисперсных частиц, где частицы формы В присутствуют суспендированными в безводной фазе. Размер частиц активного вещества, т.е. частиц которые не превышают 90 мас.% активного вещества, обычно составляет меньше 30 мкм, в частности меньше 20 мкм. Преимущественно, в безводных концентратах суспензий по меньшей мере 40 мас.% и, в частности, по меньшей мере 60 мас.% частиц имеют диаметр меньше 2 мкм. В таких ДМ количество активного вещества, т.е. общее количество карбоксамида и других активных веществ в случае необходимости, как правило, находится в диапазоне от 10 до 70 мас.%, в частности в диапазоне от 20 до 50 мас.%, от общей массы безводного концентрата суспензии. В добавок к активному веществу и жидкому носителю безводный концентрат суспензии обычно содержит поверхностно-активные вещества, а также при необходимости пеногасители, агенты для изменения реологии и стабилизаторы (биоциды). Возможными поверхностно-активными веществами являются ранее называвшиеся анионные и неионогенныеповерхностно-активные вещества. Количество поверхностно-активных веществ, как правило, будет составлять от 1 до 30 мас.%, в частности от 2 до 20 мас.% от общей массы безводного SC согласно изобретению. Предпочтительно поверхностно-активные вещества содержат по меньшей мере одно анионное поверхностно-активное вещество и по меньшей мере одно неионогенное поверхностноактивное вещество, и пропорция анионного к неионогенному поверхностно-активному веществу обычно находится в диапазоне от 10:1 до 1:10. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида согласно изобретению также может быть приготовлена как твердое вещество для защиты растений. К ним относятся порошок, рассеивающие и распыливающие агенты, а также диспергирующие- 16016798 в воде порошки и гранулы, например покрытые, пропитанные и однородные гранулы. Такие составы могут быть получены путем смешивания или одновременного измельчения формы В 3-(дифторометил)1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида с твердым носителем и при необходимости с другими добавками, в частности поверхностно-активными веществами. Гранулы могут быть получены путем связывания активных веществ на твердых носителях. Твердыми носителями являются минеральные земли, такие как кремниевая кислота, силикагель, силикаты, тальк, каолин, известняк,известь, мел, бол, лесс, глина, доломит, диатомовая земля, сульфат кальция и магния, оксид магния, измельченные пластмассы, удобрения, такие как сульфат аммония, фосфат аммония, аммиачная селитра,мочевина и продукты растительного происхождения, такие как злаковая мука, мука древесной коры,древесины и ореховой скорлупы, порошок целлюлозы или другие твердые носители. Твердые составы также могут быть произведены путем распылительной сушки, при необходимости в присутствии полимерного или неорганического вещества для сушки, а при необходимости в присутствии твердых носителей. Для получения твердых составов 3-(дифторометил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)1 Н-пиразол-4-карбоксамида формы В подходящими являются экструзионные процессы, грануляция в псевдоожиженном слое, грануляции распылением и подобные методы. Возможными поверхностно-активными веществами являются ранее называвшиеся поверхностноактивные вещества и защитные коллоиды. Количество поверхностно-активных веществ, как правило,будет составлять от 1 до 30 мас.%, в частности от 2 до 20 мас.% от общей массы твердого состава согласно изобретению. В таких твердых составах количество активного вещества, т.е. общее количество карбоксамида и других активных веществ в случае необходимости, как правило, находится в диапазоне от 10 до 70 мас.%, в частности в диапазоне от 20 до 50 мас.% от общей массы безводного концентрата суспензии. Следующие примеры приготовлений иллюстрируют приготовление таких препаратов.I. Диспергируемый в воде порошок. 20 мас.ч. формы В хорошо смешиваются с 3 мас.ч. натриевой соли диизобутилнафталинсульфоновой кислоты, с 17 мас.ч. натриевой соли лигнинсульфоновой кислоты из отработанного сульфитного щлока и с 60 мас.ч. порошкованого силикагеля и перемалывают в молотковой мельнице. Таким образом,получают диспергируемый в воде порошок, который содержит форму В.III. Безводный концентрат суспензии. 20 мас.ч. формы В тесно смешивают с 2 мас.ч. кальциевой соли додецинбензолсульфоновой кислоты, с 8 мас.ч. полигликолевого эфира жирного спирта, с 2 мас.ч. мочевино-формальдегидного конденсата натриевой соли фенолсульфокислоты и с 68 мас.ч. парафинового минерального масла. Получен стабильный, безводный концентрат суспензии формы В.IV. Безводный концентрат суспензии. 20 мас.ч. формы В размельчают до тонкоизмельченной суспензии активного вещества в перемешивающей шаровой мельнице с добавлением 10 мас.ч. диспергаторов и смачивающих агентов и 70 мас.ч. парафинового минерального масла. Получается стабильный, безводный концентрат суспензии формы В. При разведении в воде получается стабильная суспензия активного вещества. Содержание активного вещества в составе 20 мас.%.V. Водный концентрат суспензии. 10 мас.ч. формы В приготавливают в виде водного концентрата суспензии в растворе 17 мас.ч. поли(этиленгликоль)(пропиленгликоль) блок-сополимера, 2 мас.ч. формальдегидного конденсата фенолсульфоновой кислоты и около 1 мас.ч. других добавок (загустители, пеногасители) в смеси 7 мас.ч. пропиленгликоля и 63 мас.ч. воды.VI. Водный концентрат суспензии. 20 мас.ч. формы В размельчают до тонкоизмельченной суспензии активного вещества в перемешивающей шаровой мельнице с добавлением 10 мас.ч. диспергаторов и смачивающих агентов и 70 мас.ч. воды. При разведении в воде получается стабильная суспензия активного вещества. Содержание активного вещества в составе 20 мас.%.VII. Диспергируемые в воде и растворимые в воде гранулы. 50 мас.ч. формы В мелко измельчают с добавлением 50 мас.ч. диспергаторов и смачивающих агентов и приготавливают в виде диспергируемых в воде или растворимых в воде гранул с помощью промышленных устройств (например, экструзией, башней с распылительным орошением, кипящим слоем). При разведении в воде получается устойчивая дисперсия или раствор активного вещества. Состав содержит 50 мас.% активного вещества.VIII. Диспергируемые в воде и растворимые в воде порошки. 75 мас.ч. формы В измельчают в роторно-статорной мельнице с добавлением 25 мас.ч. диспергаторов и смачивающих агентов, а также силикагеля. При разведении в воде получается устойчивая дисперсия или раствор активного вещества. Содержание активного вещества в растворе составляет 75 мас.%.IX. Гелеобразные препараты. 20 мас.ч. формы В, 10 мас.ч. диспергатора, 1 мас.ч. гелеобразователя и 70 мас.ч. воды или органического растворителя перемешивают до тонкодисперсной суспензии в шаровой мельнице. При разведении в воде получается стабильная суспензия. Содержание активного вещества в составе 20 мас.%.X. Непосредственно используемые гранулы (GR, FG, GG, MG). 0,5 мас.ч. формы В мелко измельчают и комбинируют с 99,5 мас.ч. носителей. Подходящими способами здесь являются экструзия, распылительная сушка или кипящий слой. Получаются гранулы для непосредственного применения с содержанием активного вещества 0,5 мас.%. Суспензии (FS), дусты (DS), диспергируемые в воде и растворимые в воде порошки (WS, SS) обычно применяются для обработки семян. Такие составы могут быть применены к семенам в неразбавленном или, предпочтительно, в разбавленном виде. Применение может быть проведено еще до посева. Активные компоненты могут быть использованы как таковые, в форме их составов или в формах применения, приготовленных из них, например, в форме непосредственного распыляемых растворов,порошков, суспензии или дисперсий, эмульсий и масляных дисперсий, паст, дустовых продуктов, веществ для разбрасывания, или гранул, путем разбрызгивания, распыления, опыливания, разбрасывания или разливания. Используемые формы полностью зависят от предполагаемой цели; цель заключается в обеспечении в каждом конкретном случае лучшего возможного распределения активного вещества согласно изобретению. Используемые водные формы могут быть приготовлены из паст или смачиваемых порошков (распыляемые порошки, масляные дисперсии) путем добавления воды. Чтобы приготовить эмульсии, пасты или масляные дисперсии, вещества как таковые или растворенные в масле или растворителе, можно гомогенизировать в воде с помощью смачивателя, клеящего вещества, диспергатора или эмульгатора. Кроме того, можно приготовить концентрат, состоящий из активного вещества, смачивателя, клеящего вещества, диспергатора или эмульгатора и, при необходимости, растворителя или масла, и такие концентраты пригодны для разбавления водой. Концентрации активного компонента в готовых к использованию препаратах могут варьироваться в пределах относительно широких диапазонов. В основном, они составляют от 0,0001 до 10%, предпочтительно от 0,01 до 1%. Активный компонент может также быть успешно использован в ультромалообъемном способе(ULV), в котором можно применять составы, содержащие более 95 мас.% активного компонента, или даже применять активный компонент без присадок. Различные виды масел, смачивателей, вспомогательных агентов, гербицидов, фунгицидов, других пестицидов или бактерицидов могут быть добавлены к активному компоненту, в случае необходимости не непосредственно перед началом применения (резервуар смешивания). Эти составы могут быть смешаны с составами согласно изобретению в массовом соотношении от 1:100 до 100:1, предпочтительно от 1:10 до 10:1. Ниже приводятся особенно подходящие адъюванты в этом контексте: органически модифицированные полисилоксаны, например Break Thru S 240; алкоксилаты спирта, например Atplus 245, AtplusMBA 1303, Plurafac LF 300 и Lutensol ON 30; ЕО-РО блок-сополимеры, например Pluronic RPE 2035 и Genapol В; этоксилаты спирта, например Lutensol XP 80, натрия диоктилсульфосукцинат,например Leophen RA. Форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида в фунгицидной форме применения также может присутствовать вместе с другими активными компонентами, например с гербицидами, инсектицидами, регуляторами роста, фунгицидами, либо с удобрениями. При смешивании компонентов или составов содержащих их с одним или более активными компонентами, в частности фунгицидами, это во многих случаях позволяет, например, расширить спектр активности или предотвратить развитие резистентности. Во многих случаях получается синергический эффект. Настоящее изобретение также предусматривается сочетание формы В 3-(дифторометил)-1-метил-N(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида и по меньшей мере еще одного фунгицида, инсектицида, гербицида и/или активного компонента, регулирующего рост. Следующий перечень фунгицидов, с которыми вместе состав согласно изобретению может применяться, предназначен для иллюстрации возможных комбинаций, но не ограничиваться ими: стробилурины азоксистробин, димоксистробин, энестробурин, флуоксастробин, крезоксим-метил, метоминостробин, пикоксистробин, пираклостробин, трифлоксистробин, оризастробин, метил (2-хлоро-5-[1-(3 метилбензилоксиимино)этил]бензил)карбамат,метил(2-хлоро-5-[1-(6-метилпиридин-2-илметоксиимино)этил]бензил)карбамат, метил 2-(орто(2,5-диметилфенилоксиметилен)фенил)-3-метоксиакрилат; карбоксамиды карбоксанилиды: беналаксил, беноданил, боскалид, карбоксин, мепронил, фенфурам, фенгексамид,флутоланил, фураметпир, металаксил, офурас, оксадиксил, оксикарбоксин, пентиопирад, тифлузамид,- 18016798 тиадинил, N-(4'-бромобифенил-2-ил)-4-дифторметил-2-метилтиазол-5-карбоксамид, N-(4'-трифторметилбифенил-2-ил)-4-дифторметил-2-метилтиазол-5-карбоксамид,N-(4'-хлоро-3'-фторобифенил-2-ил)-4 дифторметил-2-метилтиазол-5-карбоксамид, N-(3',4'-дихлоро-4-фторобифенил-2-ил)-3-дифторметил-1 метилпиразол-4-карбоксамид, N-(3',4'-дихлоро-5-фторобифенил-2-ил)-3-дифторметил-1-метилпиразол-4 карбоксамид, N-(2-цианофенил)-3,4-дихлороизотиазол-5-карбоксамид; морфолиды карбоновой кислоты: диметоморф, флуморф; бензамиды: флуметовер, флуопиколид (пикобензамид), зоксамид; другие карбоксамиды: карпропамид, диклоцимет, мандипропамид, N-(2-(4-[3-(4-хлорофенил)проп 2-инилокси]-3-метоксифенил)этил)-2-метансульфониламин-3-метилбутирамид,N-(2-(4-[3-(4 хлорфенил)проп-2-инилокси]-3-метоксифенил)этил)-2-этансульфониламин-3-метилбутирамид; азолы триазолы: битертанол, бромуконазол, ципроконазол, дифеноконазол, диниконазол, энилконазол,эпоксиконазол, фенбуконазол, флузилазол, флуквинконазол, флутриафол, гексаконазол, имибенконазол,ипконазол, метконазол, миклобутанил, пенконазол, пропиконазол, протиоконазол, симеконазол, тебуконазол, тетраконазол, триадименол, триалмефон, тритиконазол; имидазолы: циазофамид, имазалил, пефуразоат, проклораз, трифлумизол; бензимидазолы: беномил, карбендазим, фуберидазол, тиабендазол; другие: этабоксам, этридиазол, химексазол; азотные гетероцикличные соединения пиридины: флуазинам, пирифенокс, 3-[5-(4-хлорфенил)-2,3-диметилизоксазолидин-3-ил]пиридин; пиримидины: бупиримат, ципродинил, феримзон, фенаримол, мепанипирим, нуаримол, пириметанил; пиперазины: трифорин; пирролы: флудиоксонил, фенпиклонил; морфолины: альдиморф, додеморф, фенпропиморф, тридеморф; дикарбоксимиды: ипродион, процимидон, винклозолин; другие: ацибензолар-S-метил, анилазин, каптан, каптафол, дазомет, дикломезин, феноксанил, фолпет, фенпропидин, фамоксадон, фенамидон, октилинон, пробеназол, проквиназид, пироквилон, квиноксифен, трициклазол, 5-хлоро-7-(4-метил-пиперидин-1-ил)-6-(2,4,6-трифторфенил)-[1,2,4]триазоло[1,5 а]пиримидин,6-(3,4-дихлорфенил)-5-метил-[1,2,4]триазоло[1,5-а]пиридин-7-иламин,6-(4-третбутилфенил)-5-метил-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин,5-метил-6-(3,5,5-триметилгексил)[1,2,4]триазоло[1,5-а]пиримидин-7-иламин, 5-метил-6-октил-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин,5-этил-6-октил-[1,2,4]триазоло[1,5-а]пиримидин-2,7-диамин,6-этил-5-октил-[1,2,4]триазоло[1,5 а]пиримидин-7-иламин,5-этил-6-октил-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин,5-этил-6-(3,5,5 триметилгексил)-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин,6-октил-5-пропил-[1,2,4]триазоло[1,5 а]пиримидин-7-иламин, 5-метоксиметил-6-октил-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин, 6-октил-5 трифторметил-[1,2,4]триазоло[1,5-а]пиримидин-7-иламин,5-трифторметил-6-(3,5,5-триметилгексил)[1,2,4]триазоло[1,5-а]пиримидин-7-иламин, 2-бутокси-6-иодо-3-пропилхромен-4-он, N,N-диметил-3-(3 бром-6-фторо-2-метилиндол-1-сульфонил)-[1,2,4]триазол-1-сульфонамид; карбаматы и дитиокарбаматы дитиокарбаматы: фербам, манкозеб, манеб, метирам, метам, пропинеб, тирам, зинеб, зирам; карбаматы: диетофенкарб, флубентиаваликарб, ипроваликарб, пропамокарб, метил 3-(4 хлорфенил)-3-(2-изопропоксикарбониламино-3-метилбутириламино)пропионат, 4-фторфенил N-(1-(1-(4 цианофенил)этансульфонил)бут-2-ил)карбамат; другие фунгициды гуанидины: додин, иминоктадин, гуазатин; антибиотики: касугамицин, полиоксинс, стрептомицин, валидамицин А; металлоорганические соединения: соли фентина; серосодержащие гетероциклические соединения: изопротиолан, дитианон; фосфороорганические соединения: эдифенфос, фосетил, фосетил-алюминий, ипробенфос, пиразофос, толклофос-метил, фосфорная кислота и ее соли; хлороорганические соединения: тиофанат-метил, хлороталонил, дихлофлуанид, толифлуанид, флусульфамид, фталид, гексахлоробензен, пенцикурон, квинтозен; производные нитрофенила: бинапакрил, динокап, динобутон; неорганические активные соединения: бордосская смесь, ацетат меди, гидроксид меди, оксихлорид меди, основный сульфат меди, сера; другие: спироксамин, цифлуфенамид, цимоксанил, метрафенон. Активные соединения, упомянутые выше, их приготовление и их действие против вредных грибов,как правило, известны (см.: http://www.hclrss.demon.co.uk/index.html); они являются коммерчески доступными. Соединения, названные согласно IUPAC, их получение и их фунгицидное действие также являются известными [см. ЕР-А 226917; ЕР-А 1028125; ЕР-А 1035122; ЕР-А 1201648; WO 98/46608;- 19016798 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Кристаллическая форма В 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1Hпиразол-4-карбоксамида, которая на диаграмме рентгеновской порошковой дифракции при 25 С и CuK излучении показывает по меньшей мере 3 из следующих характеристических пиков, выраженных в 2 значениях: 6,20,2, 9,20,2, 13,20,2, 14,90,2, 17,70,2, 18,60,2, 23,10,2, 27,60,2, 30,50,2. 2. Кристаллическая форма В по п.1, имеющая характерные полосы поглощения в инфракрасном спектре с превращением Фурье на длинах волн 3256 и 1639 см-1. 3. Кристаллическая форма В по п.1 с содержанием 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1 Н-пиразол-4-карбоксамида по меньшей мере 94 мас.%. 4. 3-(Дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид, состоящий по меньшей мере из 90 мас.% кристаллической формы В. 5. Способ получения кристаллической формы В по п.1, состоящий из:i) получения раствора 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол 4-карбоксамида в органическом растворителе, который выбран из метанола, этанола, 2-пропанола, циклических эфиров, уксусной кислоты, апротонных растворителей и ароматических растворителей, при температуре от 50 до 130 С;ii) охлаждения раствора со скоростью между 20 и 0,1 С/ч до температуры между 70 и -20 С;iii) отделения формы В от маточного раствора. 6. Способ получения кристаллической формы В по п.1, состоящий из:i) получения раствора 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол 4-карбоксамида в органическом растворителе, который выбран из метанола, этанола, 2-пропанола, циклических эфиров, уксусной кислоты, апротонных растворителей и ароматических растворителей, при температуре от 50 до 130 С;ii) добавления в раствор уменьшающего коэффициент растворимости растворителя в течение от 40 мин до 2,5 ч;iii) отделения формы В от маточного раствора. 7. Способ получения кристаллической формы В по п.1, включающий нагревание аморфной формы 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамида, его кристаллической формы А, смеси аморфной формы с формой А или смеси формы В с аморфной формой или формой А при температуре от 80 до 154 С. 8. Агент для защиты растений, содержащий 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид, который состоит по меньшей мере из 90 мас.% кристаллической формы В по п.1 и одной или более добавок, типичных для получения составов агентов для защиты растений. 9. Агент для защиты растений по п.8 в форме водного концентрата суспензии. 10. Агент для защиты растений по п.8 в форме безводного концентрата суспензии. 11. Агент для защиты растений по п.8 в форме порошка или гранул, диспергируемых в воде. 12. Способ борьбы с нежелательным ростом растения, в котором 3-(дифторметил)-1-метил-N(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4-карбоксамид, состоящий по меньшей мере из 90 мас.% кристаллической формы В по п.1, применяется на растениях, их месте распространения и/или на семенах.- 20016798 Рентгеновская порошковая дифрактограмма формы В Фиг. 1 Монокристаллическая структура формы В- 22016798 Рентгеновская порошковая дифрактограмма формы А Фиг. 5 Монокристаллическая структура формы А Фиг. 7 Кривая ДСК формы А со скоростью нагревания 2 С/мин- 24016798 Кривая ДСК формы А со скоростью нагревания 5 С/мин Фиг. 9 Кривая ДСК формы А со скоростью нагревания 10 С/мин- 25016798 Кривая ДСК аморфного 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4 карбоксамида со скоростью нагревания 2 С/мин Фиг. 11 Кривая ДСК аморфного 3-(дифторметил)-1-метил-N-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1 Н-пиразол-4 карбоксамида со скоростью нагревания 10 С/мин- 26016798 Микроснимок высокотемпературного эксперимента аморфного 3-(дифторметил)-1-метил-N-(3',4',5'трифтор[1,1'-бифенил]-2-ил)-1H-пиразол-4-карбоксамид Фиг. 13 Рентгеновская порошковая дифрактограмма смеси формы А и формы В Фиг. 14 Микроснимки тестов на стабильность композиций с формой А (композиция I) и формой В (композиция
МПК / Метки
МПК: A01N 43/56, C07D 231/14
Метки: форма, 3-(дифторметил)-1-метил-n-(3',4',5'-трифтор[1,1'-бифенил]-2-ил)-1н-пиразол-4-карбоксамида, кристаллическая, новая
Код ссылки
<a href="https://eas.patents.su/28-16798-novaya-kristallicheskaya-forma-3-diftormetil-1-metil-n-345-triftor11-bifenil-2-il-1n-pirazol-4-karboksamida.html" rel="bookmark" title="База патентов Евразийского Союза">Новая кристаллическая форма 3-(дифторметил)-1-метил-n-(3′,4′,5′-трифтор[1,1'-бифенил]-2-ил)-1н-пиразол-4-карбоксамида</a>
Предыдущий патент: Замороженное аэрированное кондитерское изделие и способ его получения
Следующий патент: Способ реконструкции систем теплогазоснабжения здания, сооружения
Случайный патент: Керамический анод и способ его изготовления