Индолы в качестве модуляторов никотинового рецептора ацетилхолина подтипа альфа-71
Номер патента: 18113
Опубликовано: 30.05.2013
Авторы: Диннелл Кевин, Маршалл Говард Роберт, Лайтфут Эндрю П.
Формула / Реферат
1. Соединение формулы (I) или его соль
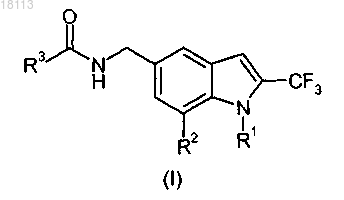
где R1 представляет собой водород или C1-3алкил;
R2 представляет собой водород, галоген или циано и
R3 представляет собой группу
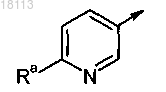
где Ra представляет собой галоген, C1-6алкил, C1-6алкокси, галогенС1-6алкил, галогенС1-6алкокси или циано.
2. Соединение по п.1 или его соль, где R1 представляет собой водород.
3. Соединение по любому предшествующему пункту или его соль, где R2 представляет собой водород.
4. Соединение, выбранное из
N-[(2-трифторметил-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида;
N-[(2-трифторметил-1H-индол-6-ил)метил]-5-(2,2,2-трифторэтокси)-3-пиридинкарбоксамида;
6-бром-N-{[2-(трифторметил)-1H-индол-5-ил]метил}-3-пиридинкарбоксамида;
6-циано-N-{[2-(трифторметил)-1H-индол-5-ил]метил}-3-пиридинкарбоксамида;
N-[(2-трифторметил-7-бром-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида;
N-[(2-трифторметил-7-циано-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида;
N-[(1-метил-2-трифторметилиндол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида
или их солей.
5. Соединение по любому предшествующему пункту, где соль соединения является фармацевтически приемлемой солью.
6. N-[(2-Трифторметил-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамид.
7. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли в качестве лекарственного средства.
8. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при лечении психотического расстройства.
9. Применение по п.8, где психотическим расстройством является шизофрения.
10. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при лечении когнитивного нарушения.
11. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения психотического расстройства.
12. Применение по п.11, где психотическим расстройством является шизофрения.
13. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения когнитивного нарушения.
14. Способ лечения психотического расстройства у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли.
15. Способ лечения шизофрении у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли.
16. Способ лечения когнитивного нарушения у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли.
17. Фармацевтическая композиция, содержащая а) соединение по любому из пп.1-6 или его фармацевтически приемлемую соль и b) один или несколько фармацевтически приемлемых носителей или эксципиентов.
Текст
ИНДОЛЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ НИКОТИНОВОГО РЕЦЕПТОРА АЦЕТИЛХОЛИНА ПОДТИПА АЛЬФА-71 Изобретение относится к модуляции никотинового рецептора 7 ацетилхолина (nAChR) соединением формулы (I) или его солью.(71)(73) Заявитель и патентовладелец: ГЛЭКСО ГРУП ЛИМИТЕД (GB) Данное изобретение относится к новым производным индола, обладающим активностью при модуляции никотинового рецептора 7 ацетилхолина (nAChR). Изобретение относится также к применению упомянутых производных при лечении заболеваний и состояний, опосредуемых модуляцией 7 nAChR. Кроме того, изобретение относится к композициям, содержащим упомянутые производные, и способам их получения. Нейротрансмиттер ацетилхолин (Ach) посредством связывания с холинергическими рецепторами вызывает открытие ионных каналов в организме млекопитающего. Центральная нервная система (ЦНС) содержит два типа рецептора ACh, мускариновые рецепторы и nAChR. nAChR являются открываемыми лигандом ионными каналами, содержащими пять субъединиц (для обзора см. Colquhon et al. (1997) Advances in Pharmacology 39, 191-220; Williams et al. (1994) Drug NewsPerspectives 7, 205-223; Doherty etal. (1995) Annual reports in Medicinal Chemistry 30, 41-50). Семейство генов nAChR можно разделить на две группы: гены, кодирующие -субъединицы, и гены, кодирующие -субъединицы (для обзора см.KarlinAkabas (1995) Neuron 15, 1231-1244, Sargent (1993) Annu. Rev. Neurosci. 16, 403-443). Три из субъединиц, 7, 8 и 9, могут образовывать функциональные рецепторы при экспрессии отдельно и могут образовывать гомоолигомерные рецепторы. Исследования показали, что нейронные никотиновые рецепторы играют важные роли в модуляции нейротрансмиссии, познавательной способности, "сенсорного гейтинга" (процесса, в котором мозг приспосабливается к ответу на стимул) и тревоги (Zarei et al. Neuroscience 1999, 88, 755-764, Frazier et al. J.Neurosci. 1998, 18, 8228-8235, Radcliffe et al. J. Neurosci. 1998, 18, 7075-7083, Minana et al. Neuropharmacology 1998, 37, 847-857, Albuquerque et al. Toxicol. Lett. 1998, 102-103, 211-218, Neubauer, et al. Neurology 1998, 51, 1608-1612, Stevens et al. Psychopharmacology 1998, 136, 320-327, Adler et al. Schizophrenia Bull. 1998, 24, 189-202.); поэтому существует интерес к применению соединений, которые модулируют эти рецепторы, для лечения заболеваний ЦНС. Роль рецепторов 7 в этиологии шизофрении была предположена исследованиями сцеплений генов(Freedman et al., Psychopharmacology (2004), 174(1), 54-64), демонстрирующими взаимосвязь между локусом 7 и дефицитом сенсорного гейтинга, который представляет собой основной эндофенотип шизофрении. Такие дефициты гейтинга у пациентов транзиторно реверсировались никотином с фармакологией,совместимой с действием посредством 7. Кроме того, на животных моделях повреждение холинергических афферентаций переднего мозга или фармакологическая блокада рецепторов 7 вызывает аналогичные дефициты сенсорного гейтинга, которые также являются очевидными у мышей инбредных линий,экспрессирующих пониженные уровни рецептора 7. Описано, что никотин нормализует дефициты как у поврежденных животных, так и у мышей инбредных линий, снова с фармакологией, совместимой с активностью у рецептора 7. Описано, что фармакологическая блокада рецепторов 7 ослабляет кратковременную рабочую память грызунов, тогда как активация рецептора, как описано, повышает действие в той же парадигме, тем самым вовлекая рецепторы 7 в качестве мишени для повышения познавательной способности. 7 nAChR характеризуются их быстрыми кинетиками активации и высокой проницаемости дляCa2+ по сравнению с другими подтипами (Delbono et al., J. Pharmacol. Exp. Ther. 1997, 280, 428-438) и проявляют быструю десенсибилизацию после воздействия на них агонистов (Castro et al., Neurosci. Lett. 1993, 164, 137-140, Couturier et al., Neuron 1990, 5, 847-856, Alkondon et al., J. Pharmacol. Exp. Ther. 1994,271, 494-506). Поэтому лечение агонистами 7 может быть проблематичным, поскольку как ацетилхолин, так и никотин, оба, проявляют активацию с последующим блокированием и/или десенсибилизацией рецептора, и поэтому постоянное лечение агонистом может вполне привести к явному антагонизму. Кроме того, обнаружено, что агонисты проявляют более высокую аффинность для десенсибилизированного состояния рецептора и поэтому могут опосредовать десенсибилизацию рецептора при концентрациях ниже пороговой величины для активации рецептора (Briggs and McKenna, Neuropharmacology 1998, 37,1095-1102). Эту проблему можно решить лечением позитивным аллостерическим модулятором (РАМ). РАМ повышают активацию 7 nAChR, опосредованную эндогенными или экзогенными агонистами без активации рецептора самих по себе, т.е. в отсутствие агониста. Описан ряд РАМ (Lightfoot et al., Progress inmedicinal chemistry 46:131-71, 2008). Согласно первому аспекту изобретение относится к соединению формулы (I) или его соли где R1 представляет собой водород или C1-3 алкил;R2 представляет собой водород, галоген или циано и где Ra представляет собой галоген, C1-6 алкил, C1-6 алкокси, галогенС 1-6 алкил, галогенС 1-6 алкокси,циано или диС 1-3 алкиламино. Применяемый в контексте заместитель C1-6 алкил является одновалентным радикалом, образованным удалением атома водорода у ациклического C1-6 алкана. Такие заместители C1-6 алкилы включают метил и этил и могут быть C1-6 алкилами с неразветвленной (т.е. н-пропил, н-бутил, н-пентил и н-гексил) или разветвленной цепью (например, изопропил, изобутил, втор-бутил, трет-бутил, изопентил и неопентил). Применяемый в контексте заместитель галоген относится к радикалам фтора, хлора, брома и иода. В варианте осуществления, если не указано иначе, любой заместитель галоген представляет собой хлор или бром. Применяемый в контексте заместитель галогенС 1-6 алкил представляет собой C1-6 алкильную группу,замещенную одним или несколькими галогенами, причем галогены могут быть одинаковыми или разными. Такие галогенС 1-6 алкильные заместители включают монофторметил, дифторметил, трифторметил и 1-хлор-2-фторэтил. Применяемый в контексте заместитель C1-6 алкокси представляет собой группу формулы "R-O-", гдеR представляет собой C1-6 алкил, который имеет указанные выше значения. Такие алкоксизаместители включают метокси и этокси и могут иметь неразветвленную цепь (т.е. н-пропокси, н-бутокси, н-пентокси и н-гексилокси) или разветвленную цепь (например, изопропокси, изобутокси, втор-бутокси, третбутокси, изопентокси и неопентокси). Применяемый в контексте заместитель галогенС 1-6 алкокси имеет формулу "Rx-O-", где Rx представляет собой галогенС 1-6 алкил, который имеет значения, указанные выше. Такие заместители галогенС 1-6 алкокси включают монофторметокси, дифторметокси, трифторметокси и 1-хлор-2-фторэтокси и могут иметь неразветвленную цепь или разветвленную цепь. В варианте осуществления R1 представляет собой водород. В варианте осуществления R2 представляет собой водород. В следующем варианте осуществления R1 и R2 представляют собой водород. В варианте осуществления Ra представляет собой бром, хлор, метил, метокси, этокси, трифторметил, трифторэтокси или циано. В следующем варианте осуществления Ra представляет собой бром, метил, метокси, этокси, трифторметил, трифторэтокси или циано. В следующем варианте осуществления Ra представляет собой трифторметил. В варианте осуществления соединение выбрано изN-[(1-метил-2-трифторметилиндол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида или их солей. В следующем варианте осуществления соединением является N-[(2-трифторметил-1H-индол-5 ил)метил]-6-(трифторметил)-3-пиридинкарбоксамид. Предполагается, что, как будет понятно, настоящее изобретение включает соединения, имеющие любую комбинацию вариантов осуществления, указанных в контексте ранее. Чтобы не было сомнения, если не указано иначе, термин "замещенный" означает замещенный одной или несколькими указанными группами. В случае, когда группы могут быть выбраны из ряда альтернативных групп, выбранные группы могут быть одинаковыми или разными. Чтобы не было сомнения, термин "независимо" означает, что когда более чем один заместитель выбран из ряда возможных заместителей, эти заместители могут быть одинаковыми или разными. Соединения формулы (I) могут образовывать фармацевтически приемлемые соли, например нетоксичные кислотно-аддитивные соли, образованные с неорганическими кислотами, такими как хлористоводородная, бромисто-водородная, иодисто-водородная, серная и фосфорная кислоты, с карбоновыми кислотами или с HCl, HBr, HI, сульфат или бисульфат, нитрат, фосфат или гидрофосфат, ацетат, бензоат,сукцинат, сахарат, фумарат, малеат, лактат, цитрат, тартрат, глюконат, камсилат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат. Для обзоров по подходящим фармацевтическим солям см. Berge et al., J. Pharm, Sci, 66, 1-19, 1977; P.L. Gould, International Journal of Pharmaceutics,33 (1986), 201-217 и Bighley et al., Encyclopedia of Pharmaceutical Technology, Marcel Dekker Inc, New В одном варианте осуществления солью соединения формулы (I) является фармацевтически приемлемая соль. В дальнейшем соединения формулы (I) и их фармацевтически приемлемые соли называют также"соединениями изобретения". Специалистам в данной области должно быть понятно, что некоторые защищенные производные соединений изобретения, которые можно получить перед конечной стадии удаления защиты, могут не обладать фармакологической активностью как таковой, но могут быть в некоторых случаях введены перорально или парентерально и после этого могут метаболизироваться в организме с образованием соединений, указанных в первом аспекте, которые являются фармакологически активными. Такие производные поэтому можно описывать как "пролекарства". Все защищенные производные и пролекарства соединений, указанных в первом аспекте, включены в объем изобретения. Примеры подходящих пролекарств для соединений настоящего изобретения описаны в Drugs of Today, vol. 19, Number 9, 1983, p. 499-538, в Topics in Chemistry, Chapter 31, p. 306-316 и в "Design of Prodrugs" by H. Bundgaard, Elsevier,1985, Chapter 1 (описания в этих документах включены в контекст в качестве ссылки). Далее специалистам в данной области должно быть понятно, что некоторые фрагменты, известные специалисту в данной области как "про-фрагменты", например, как описано Н. Bundgaard in "Design of Prodrugs" (описание,в котором документ включен в контекст в качестве ссылки), можно ввести в подходящие функциональные группы, когда такие функциональные группы присутствуют в соединении, описанном в первом аспекте. Соединения изобретения обычно находятся в твердой форме. В твердом состоянии соединения изобретения могут существовать в кристаллической или некристаллической форме или в виде их смеси. В случае соединения изобретения в кристаллической форме специалисту в данной области должно быть понятно, что могут образовываться фармацевтически приемлемые сольваты, в которые молекулы растворителя включаются в кристаллическую решетку в процессе кристаллизации. Сольваты могут включать неводные растворители, такие как этанол, изопропанол, ДМСО, уксусная кислота, этаноламин иEtOAc, или они могут включать воду в качестве растворителя, который включается в кристаллическую решетку. Сольваты, в которых вода является растворителем, который включается в кристаллическую решетку, обычно называют "гидратами". Гидраты включают стехиометрические гидраты, а также композиции, содержащие изменяемые количества воды. Изобретение включает все такие сольваты. Специалисту в данной области должно быть далее известно, что соединения изобретения в кристаллической форме, включая их различные сольваты, могут проявлять полиморфизм (т.е. способность существовать в различных кристаллических структурах). Эти различные кристаллические формы обычно известны как "полиморфы". Изобретение включает все такие полиморфы. Полиморфы имеют одинаковый химический состав, но различаются по упаковке, геометрическому расположению и другим описательным свойствам кристаллического твердого состояния. Полиморфы поэтому могут иметь разные физические свойства, такие как форма, плотность, твердость, деформируемость, стабильность и свойства растворения. Полиморфы обычно проявляют разные точки плавления, ИК-спектры и порошковые рентгенограммы, которые можно применять для идентификации. Специалисту в данной области должно быть понятно, что разные полиморфы можно получить, например, изменением или регулированием условий реакции или реагентов, применяемых при получении соединения. Например, изменения в температуре,давлении или растворителе могут приводить к получению полиморфов. Кроме того, один полиморф может приводить к получению полиморфов. Кроме того, один полиморф может самопроизвольно превращаться в другой полиморф при определенных условиях. В одном аспекте настоящее изобретение относится к N-[(2-трифторметил-1H-индол-5-ил)метил]-6(трифторметил)-3-пиридинкарбоксамиду в кристаллической форме. В другом аспекте настоящее изобретение относится к кристаллическому N-[(2-трифторметил-1Hиндол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамиду, отличающемуся тем, что он имеет XRPD(порошковую рентгенограмму), по существу, согласно фиг. 1. В следующем аспекте настоящее изобретение относится к кристаллическому N-[(2-трифторметил 1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамиду, отличающемуся тем, что он имеетXRPD (порошковую рентгенограмму), имеющую пики, по существу, представляемые в табл. 1. В другом варианте осуществления настоящее изобретение относится к кристаллическому N-[(2 трифторметил-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамиду, отличающемуся тем,что он имеет спектр комбинационного рассеяния согласно фиг. 2. Следовательно, согласно следующему аспекту изобретение относится к сольвату, гидрату, пролекарству или полиморфу соединений изобретения. Некоторые соединения изобретения существуют в одной или нескольких таутомерных формах. Все таутомеры и их смеси включены в объем настоящего изобретения. Некоторые соединения изобретения могут иметь один или несколько хиральных центров и поэтому существуют в виде ряда стереоизомерных форм. Соединения, имеющие один хиральный центр, могут существовать в виде энантиомеров или рацемической смеси, содержащей энантиомеры. Соединения,имеющие два или более хиральных центров, могут существовать в виде диастереомеров или энантиоме-3 018113 ров. Все стереоизомеры (например, энантиомеры и диастереомеры) и их смеси включены в объем настоящего изобретения. Рацемические смеси можно разделить для получения их индивидуальных энантиомеров с применением препаративной ВЭЖХ и разделить с получением индивидуальных энантиомеров с применением способов, известных специалисту в данной области. Кроме того, хиральные промежуточные соединения можно разделить и применять для получения индивидуальных энантиомеров. Изобретение включает также все подходящие изотопные варианты соединений изобретения. Изотопный вариант соединения изобретения определяется как вариант, у которого по меньшей мере один атом заменен атомом, имеющим такой же атомный номер, но имеющим атомную массу, отличную от атомной массы, обычно встречающуюся в природе. Примеры изотопов, которые можно включить в соединения изобретения, включают изотопы водорода, углерода, азота, кислорода, серы, фтора и хлора,такие как 2H, 3H, 13C, 14C, 15N, 17O, 1SO, 35S, 18F и 36Cl соответственно. Некоторые изотопные варианты изобретения, например варианты, в которые включен радиоактивный изотоп, такой как 3H или 14C, являются применимыми в исследованиях распределения лекарственного средства и/или субстрата в ткани. Изотопы тритий, т.е. 3H, и углерод-14, т.е. 14C, являются особенно предпочтительными вследствие легкости их получения и детектируемости. Кроме того, замещение изотопами, такими как дейтерий, т.е. 2H,может обеспечить некоторые терапевтические преимущества, являющиеся результатом более высокой метаболической стабильности, например увеличенный полупериод существования in vivo или требования уменьшенных доз, и поэтому в некоторых случаях такие изотопные варианты соединения могут быть предпочтительными. Изотопные варианты соединений изобретения обычно получают общепринятыми методиками, например иллюстративными способами или получениями, описанными далее в примерах и получениях с применением соответствующих изотопных вариантов подходящих реагентов. Соединения изобретения можно получать различными путями. В нижеследующих схемах реакций и далее в контексте, если не оговорено иначе, R1-R3 имеют значения, указанные в первом аспекте. Эти способы образуют следующие аспекты изобретения. На всем протяжении описания общие формулы обозначаются римскими числами (I), (II), (III), (IV) и т.д. Подгруппы этих общих формул указываются как (Ia), (Ib), (Ic) и т.д., (IVa), (IVb), (IVc) и т.д. Соединения формулы (I) можно получить согласно схеме 1 сочетанием соединений формулы (II) с соединениями формулы (III). Типичные условия содержат обработку подходящим агентом сочетания,таким как HATU, HOBt, DCC, в подходящем растворителе, таком как DCM или ДМФА. Альтернативные условия содержат превращение карбоновой кислоты (II) в соответствующий ацилхлорид с применением оксалилхлорида в подходящем растворителе (таком как ТГФ или DCM) с подходящим основанием (таким как триэтиламин). Схема 1 Или же соединения формулы (I) можно получить из других соединений формулы (I). Например, согласно схеме реакции 2 соединения формулы (Ia), где R2 представляет собой циано,можно получить из соединений формулы (Ib), где R2 представляет собой бром, реакцией с цианидом цинка и с применением подходящего катализатора в подходящем растворителе. Схема 2 Соединения формулы (IIIa), т.е. соединения формулы (III), где R1 представляет собой водород,можно получить согласно схеме 3. Обработка соединений формулы (IV) трифторуксусным ангидридом в присутствии основания (такого как триэтиламин) в подходящем растворителе (таком как DCM) дает соединения формулы (V). Галогенирование соединений формулы (V) подходящим источником радикала галогена, таким как сульфурилхлорид или N-бромсукцинимид, в подходящем растворителе (таком как тетрахлорид углерода) дает соединения формулы (VI). Обработка соединений формулы (VI) производным фосфина (таким как трифенилфосфин) дает соединения формулы (VII), которые можно циклизовать с получением соединений формулы (VIII). Типичные условия циклизации содержат нагревание в подходящем растворителе (таком как ДМФА) до температуры свыше 100C. Соединения формулы (III) получают восстановлением соединений формулы (VIII) бораном или борогидридом никеля. Соединения формулы (IIIb), т.е. соединения формулы (III), где R1 представляет собой C1-3 алкил,можно получить согласно схеме реакций 4 реакцией соединений формулы (VIII) с подходящим алкилгалогенидом (таким как метилиодид) в присутствии основания (такого как гидрид натрия) в подходящем растворителе (таком как ДМФА) с последующим восстановлением с применением борана или борогидрида никеля. Схема 4 Соли можно получить общепринятым образом реакцией с подходящей кислотой или производным кислоты. Соединения изобретения могут быть применимыми для лечения заболеваний и состояний, опосредуемых позитивной аллостерической модуляцией 7 nAChR, или заболеваний и состояний, которые связаны с модуляцией 7 nAChR. Заболевания или состояния, опосредуемые позитивной аллостерической модуляцией 7 nAChR, или заболевания и состояния, которые связаны с модуляцией 7 nAChR, включают (числа в скобках после перечисленных ниже заболеваний относятся к системе кодирования классификации в Diagnostic and Statistical Manual of Mental Disorders, 4th Edition, published by the American Psychiatric Association (DSM-IV), и/или International CIassification of Diseases, 10th Edition (ICD-10, следующие заболевания и состояния:(295.30), тип тяжелой формы шизофрении с преобладанием бессвязности, притупленными, парадоксальными эмоциями и отсутствием систематизированного бреда (295.10), кататонический тип (295.20), недифференцированный тип (295.90) и резидуальный тип (295.60; нарушение шизофренической формы(295.40); шизоаффективное расстройство (295.70) (включая подтипы биполярного типа и депрессивного типа); бредовое расстройство (297.1) (включающее подтипы эротоманического типа, типа мании величия, типа ревности, типа подозрительности, соматического типа, смешанного типа и неспецифического типа); кратковременное психотическое расстройство (298.8); разделяемое психотическое расстройство(297.3); психотическое расстройство вследствие общего медицинского состояния (включающее подтипы с бредом и галлюцинациями); индуцированное веществом психотическое расстройство (включающее подтипы с бредом (293.81) и с галлюцинациями (293.82; и другое, не указанное психотическое расстройство (298.9);ii) ослабление познавательной способности, включающее, например, ослабление познавательных функций, включающее расстройство внимания, ориентации, изучения, памяти (т.е. нарушения памяти,амнезию, относящиеся к амнезии нарушения, синдром транзиторной глобальной амнезии и связанное с возрастом ухудшение памяти) и функции языка (речи); а также ослабление познавательной способности в результате удара, болезни Альцгеймера, болезни Хантингтона, болезнь Пика, связанную со СПИДом деменцию или другие состояния деменции, такие как многоинфарктная деменция, алкогольная деменция, связанная с гипотироидизмом деменция, и деменция, связанная с другими дегенеративными нарушениями, такими как ослабление мозжечковой функции и боковой амиотрофический склероз; другие острые или субострые состояния, которые могут вызвать снижение познавательной способности, такие как делириозный синдром или депрессия (состояния псевдодеменции), травма, травма головы, связанное с возрастом снижение познавательной способности, удар, нейродегенерация, индуцированные лекарственным средством состояния, состояния, вызванные нейротоксичными агентами, легкое ослабление познавательной способности, связанное с возрастом ослабление познавательной способности, связанное с аутизмом ослабление познавательной способности, синдром Дауна, дефицит познавательной способно-5 018113 сти, связанный с другими заболеваниями, такими как шизофрения, биполярное нарушение, депрессия и другие психиатрические нарушения, и нарушения познавательной способности, связанные с послеэлектроконвульсивным лечением; и дискинетические нарушения, такие как болезнь Паркинсона, индуцированный нейролептическим средством паркинсонизм и поздняя дискинезия;iii) депрессия и расстройство настроения, например депрессивные эпизоды (включающие большой депрессивный эпизод, маниакальный эпизод, смешанный эпизод и гипоманиакальный эпизод); депрессивные состояния (включающие депрессивный эпизод тяжелой степени, дистимическое расстройство(300.4), другое, не указанное депрессивное состояние (311; биполярные расстройства (включая биполярное расстройство I, биполярное расстройство II (т.е. повторяющиеся депрессивные эпизоды тяжелой степени с гипоманиакальными эпизодами (296.89), циклотимическое нарушение (301.13) и другое, не указанное биполярное расстройство (296.80); другие расстройства настроения (включающие расстройство настроения вследствие общего медицинского состояния (293.83), которое включает подтипы с депрессивными признаками, с подобным депрессивному эпизоду тяжелой степени, с маниакальными признаками и со смешанными признаками); индуцированное веществом расстройство настроения (включая подтипы с депрессивными признаками, с маниакальными признаками и со смешанными признаками) и другое, не указанное расстройство настроения (296.90);iv) тревожные расстройства, например социальное тревожное расстройство; паническая атака; агорафобия, паническое расстройство; агорафобия без истории болезни панического расстройства (300.22); специфическая фобия (300.29) (включающая подтипы животного типа, типа природной окружающей среды, типа повреждения при инъекции в кровоток, типа ситуации и другого типа); социальная фобия(309.81); острое стрессовое расстройство (308.3); генерализованное тревожное расстройство (300.02); тревожное расстройство вследствие общего медицинского состояния (293.84); индуцированное веществом тревожное расстройство и другое, не указанное тревожное расстройство (300.00);v) связанные с веществом расстройства, например расстройства из-за применения вещества (включающие зависимость от вещества, пристрастие к веществу и злоупотребление веществом); индуцированные веществом расстройства (включающие интоксикацию веществом, синдром отмены приема вещества,индуцированный веществом делирий, индуцированная веществом персистентная деменция, индуцированное веществом персистентное, амнестическое нарушение, индуцированное веществом психотическое расстройство, индуцированное веществом расстройство настроения, индуцированное веществом тревожное расстройство, индуцированная веществом сексуальная дисфункция, индуцированное веществом расстройства сна и персистирующее галлюциногеном искажение восприятия ("стоп-кадр"); связанные с алкоголем расстройства (включающие алкогольную зависимость (303.90), злоупотребление алкоголем(305.00), алкогольную интоксикацию (303.00), синдром отмены приема алкоголя (291.81), делирий алкогольной интоксикации, делирий синдрома отмены приема алкоголя, индуцированная алкоголем персистирующая деменция, индуцированное алкоголем персистирующее, вызывающее потерю памяти расстройство, индуцированное алкоголем психотическое расстройство, индуцированное алкоголем расстройство настроения, индуцированное алкоголем тревожное расстройство, индуцированная алкоголем сексуальная дисфункция, индуцированное веществом расстройства сна и другое, не указанное, связанное с алкоголем расстройство (291.9; связанные с амфетамином (или подобным амфетамину веществом) нарушения (например, амфетаминовая зависимость (304.40), злоупотребление амфетамином (305.70),амфетаминовая интоксикация (292.89), синдром отмены приема амфетамина (292.0), делирий амфетаминовой интоксикации, индуцированное амфетамином психотическое расстройство, индуцированное амфетамином расстройство настроения, индуцированное амфетамином тревожное расстройство, индуцированная амфетамином сексуальная дисфункция, индуцированное амфетамином расстройства сна и другое,не указанное, связанное с амфетамином расстройство (292.9; связанные с кофеином расстройства(включающие интоксикацию кофеином (305.90), индуцированное кофеином тревожное расстройство,индуцированное кофеином расстройства сна и другое, не указанное, связанное с кофеином расстройство(292.9; связанные с каннабисом нарушения (включающие зависимость от каннабиса (304.30), синдром отмены каннабиса (305.20), интоксикация каннабисом (292.89), делирий интоксикации каннабиса, индуцированное каннабисом психотическое расстройство, индуцированное каннабисом расстройство настроения, и другое, не указанное, связанное каннабисом расстройство (292.9; связанные с кокаином нарушения (включающие кокаиновую зависимость (304.20), злоупотребление кокаином (305.60), кокаиновую интоксикацию (292.89), синдром отмены кокаина (292.0), делирий кокаиновой интоксикации, индуцированное кокаином психотическое расстройство, индуцированное кокаином расстройство настроения, индуцированное кокаином тревожное расстройство, индуцированная кокаином сексуальная дисфункция, индуцированное кокаином расстройства сна и другое, не указанное, связанное с кокаином расстройство (292.9; связанные с галлюциногеном расстройства (включающие зависимость от галлюциногена (304,50), злоупотребление галлюциногеном (305.30), интоксикация галлюциногеном (292.89), персистирующее галлюциногеном искажение восприятия ("стоп-кадр") (292.89), делирий галлюциногеновой интоксикации, индуцированное галлюциногеном психотическое расстройство, индуцированное галлюциногеном расстройство настроения, индуцированное галлюциногеном тревожное расстройство и дру-6 018113 гое, не указанное, связанное с галлюциногеном расстройство (292.9; связанные с ингаляционным средством расстройства (включающие зависимость от ингаляционного средства (304,60), злоупотребление ингаляционным средством (305.90), интоксикацию ингаляционным средством (292.89); делирий интоксикации ингаляционным средством, индуцированная ингаляционным средством персистирующая деменция, индуцированное ингаляционным средством психотическое расстройство, индуцированное ингаляционным средством расстройство настроения, индуцированное ингаляционным средством тревожное расстройство и другое, не указанное, связанное с ингаляционным средством расстройство (292.9; связанные с никотином расстройства (включая зависимость от никотина (305.1), синдром отмены никотина(292.0) и другое, не указанное, связанное с никотином расстройство (292.9; связанные с опиоидом нарушения (включая опиоидную зависимость (304.00), злоупотребление опиоидом (305.50), опиоидная интоксикация (292.89), синдром отмены опиоида (292.0), делирий опиоидной интоксикации, индуцированное опиоидом психотическое расстройство, индуцированное опиоидом расстройство настроения, индуцированная опиоидом сексуальная дисфункция, индуцированное опиоидом расстройство сна и не указанное другое, связанное с опиоидом расстройство (292.9; связанные с фенциклидином (или подобным фенциклидину веществом) нарушения (включающие фенциклидиновую зависимость (304.60), злоупотребление фенциклидином (305.90), фенциклидиновая интоксикация (292.89), делирий фенциклидиновой интоксикации, индуцированное фенциклидином психотическое расстройство, индуцированное фенциклидином расстройство настроения, индуцированное фенциклидином тревожное расстройство и не указанное другое, связанное с фенциклидином расстройство (292.9; нарушения, связанные с приемом седативных, снотворных или транквилизаторных средств (включающие зависимость от седативных, снотворных или транквилизаторных средств (304.10), злоупотребление седативными, снотворными или транквилизаторными средствами (305.40); интоксикацию, вызванную седативными, снотворными или транквилизаторными средствами (292.89); синдром отмены седативных, снотворных или транквилизаторных средств (292.0); делирий интоксикации, вызванной седативными, снотворными или транквилизаторными средствами (292.0), делирий отмены седативных, снотворных или транквилизаторных средств,персистирующая деменция, вызванная седативными, снотворными или транквилизаторными средствами,персистирующее нарушение памяти, вызванное седативными, снотворными или транквилизаторными средствами, психотическое расстройство, индуцированное седативными, снотворными или транквилизаторными средствами, расстройство настроения, индуцированное седативными, снотворными или транквилизаторными средствами, тревожное расстройство, индуцированное седативными, снотворными или транквилизаторными средствами, сексуальная дисфункция, индуцированная седативными, снотворными или транквилизаторными средствами, расстройство сна, индуцированное седативными, снотворными или транквилизаторными средствами, и не указанное другое, связанное с седативными, снотворными или транквилизаторными средствами расстройство (292.9; связанное с приемом нескольких веществ расстройство (включающее зависимость от нескольких веществ (304.80; и связанные с другими (или неизвестными) веществами расстройства (включающие прием анаболических стероидов, нитратных ингаляционных средств и оксида азота (III;vi) расстройства сна, например первичные расстройства сна, такие как диссомнии (включающие первичную инсомнию (307.42), первичную гиперсомнию (307.44), нарколепсию (347), связанные с дыханием расстройства сна (780.59), расстройства сна с циркадным ритмом (307.45) и другая, не указанная диссомния (307.47); первичные расстройства сна, такие как парасомнии (включающие расстройства сна с кошмарами (307.47), расстройства с ужасами во время сна (307.46), расстройство типа сомнамбулизма(307.46) и другая, не указанная парасомния (307.47); расстройства сна, связанные с другим психическим расстройством (включающие инсомнию, связанную с другим психическим расстройством (307.42), и гиперсомнию, связанную с другим психическим расстройством (307.44; расстройство сна, обусловленное общим медицинским состоянием, и индуцированное веществом расстройство сна (включающее подтипы типа инсомнии, типа гиперсомнии, типа парасомнии и смешанного типа);vii) расстройства пищевого поведения, такие как нервная анорексия (307.1) (включающая в себя подтипы ограничительного типа и типа приема пищи, связанного с пьянством/приема слабительного); нервная булимия (307.51) (включающая в себя подтипы слабительного типа и неслабительного типа); ожирение; компульсивное расстройство пищевого поведения; расстройство пищевого поведения, связанное с пьянством, и другое, не указанное расстройство пищевого поведения (307.50).viii) нарушения всего диапазона аутизма, включающие аутичное нарушение (299.00), нарушениеAsperger, нарушение Rett, дезинтегративное нарушение детского возраста и другое, не указанное первазивное нарушение развития;ix) синдром повышенной активности с дефицитом внимания (включающий в себя подтипы синдрома комбинированного типа повышенной активности с дефицитом внимания (314.01), синдром повышенной активности с дефицитом внимания, преимущественно невнимательного типа (314.00), синдром повышенной активности с дефицитом внимания типа импульсивной повышенной активности (314.01) и другой, не указанный синдром повышенной активности с дефицитом внимания (314.9; гиперкинетическое расстройство; разрушительные расстройства поведения, такие как детские и юношеские расстройства поведения (включающие подтипы типа начала детства (321.81), типа начала подросткового возраста(313.81), и другое, не указанное разрушительное расстройство поведения; и расстройства, характеризующиеся тиком, такие как расстройство Tourette (307.23); х) личностные расстройства, включающие подтипы параноидного расстройства личности (301.0),шизоидное расстройство личности (301.20), шизотипическое расстройство личности (301.22), антисоциальное расстройство личности (301.7), пограничное личностное расстройство (301.83), гистрионное личностное расстройство (301.50), нарциссическое расстройство личности (301.81), уклоняющееся расстройство личности (301.82), зависимое расстройство личности (301.6), обсессивно-компульсивное личностное расстройство (301.4) и другое, не указанное личностное расстройство (301.9);xi) сексуальные дисфункции, такие как расстройства полового влечения (включающие расстройство типа гипоактивного полового влечения (302.71) и расстройство типа сексуального отвращения (302.79; расстройства сексуального возбуждения (включающие расстройство женского сексуального возбуждения (302.72) и эректильная дисфункция у мужчин (302.72; оргазменное нарушение (включающее оргазменное нарушение женщин (302,73), оргазменное нарушение мужчин (302.74) и преждевременная эякуляция (302.75; половое болевое нарушение (включающее диспареунию (302.76) и вагинизм(306.51; другая, не указанная сексуальная дисфункция (302.70); половые извращения (включающие эксгибиционизм (302.4), фетишизм (302.81), поглаживание (302.89), педофилия (302.2), сексуальный мазохизм (302.83), сексуальный садизм (302.84), трансвестический фетишизм (302.3), вуайеризм (302.82) и другое, не указанное половое извращение (302.9; расстройства половой идентификации (включающие расстройство половой идентификации у детей (302.6) и расстройство половой идентификации у подростков или взрослых людей (302.85; и другое, не указанное сексуальное расстройство (302.9). Соединения изобретения могут быть также применимыми при лечении воспаления, воспалительной боли, ревматоидного артрита и сепсиса. В одном варианте осуществления пациентом является человек. Термин "лечение" включает профилактику, лечение симптомов и/или лечение лежащих в основе причин симптомов, когда такой термин является подходящим для уместного состояния(й). Таким образом, в одном аспекте настоящее изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения в качестве лекарственного средства. В одном аспекте настоящее изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении заболевания, которое связано со снижением функции никотинового рецептора 7 ацетилхолина. В одном аспекте настоящее изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении заболевания, которому приносит пользу позитивная аллостерическая модуляция никотинового рецептора 7 ацетилхолина. В одном аспекте настоящее изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения в качестве позитивного аллостерического модулятора никотинового рецептора 7 ацетилхолина. В другом аспекте изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении психотического расстройства. В одном варианте осуществления изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении шизофрении. В одном варианте осуществления изобретение относится к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении тревоги или депрессии. Изобретение относится также к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении когнитивного нарушения. Изобретение относится также к соединению формулы (I), описываемому в контексте ранее, или его соли для применения при лечении болезни Альцгеймера. В другом аспекте изобретение относится к применению соединения формулы (I), описываемого в контексте ранее, или его соли при изготовлении лекарственного средства для лечения заболевания, которое связано со снижением функции никотинового рецептора 7 ацетилхолина. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли для применения при лечении заболевания, которому приносит пользу позитивная аллостерическая модуляция никотинового рецептора 7 ацетилхолина. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для позитивной аллостерической модуляции никотинового рецептора 7 ацетилхолина. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для применения при лечении психотического расстройства. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для применения при лечении шизофрении. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для применения при лечении тревоги или депрессии. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для применения при лечении когнитивного нарушения. В другом аспекте настоящее изобретение относится к применению соединения формулы (I), описываемому в контексте ранее, или его соли при изготовлении лекарственного средства для применения при лечении болезни Альцгеймера. В другом аспекте изобретение относится к способу лечения заболевания, которое связано со снижением функции никотинового рецептора 7 ацетилхолина, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I), описываемому в контексте ранее,или его соли. В одном аспекте настоящее изобретение относится к способу лечения заболевания, которому приносит пользу позитивная аллостерическая модуляция никотинового рецептора 7 ацетилхолина, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы(I), описываемого в контексте ранее, или его соли. В одном аспекте настоящее изобретение относится к способу позитивной аллостерической модуляции никотинового рецептора 7 ацетилхолина, который содержит введение человеку эффективного количества соединения формулы (I), описываемому в контексте ранее, или его соли. В другом аспекте настоящее изобретение относится к способу применения при лечения психотического расстройства, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I), описываемому в контексте ранее, или его соли. В одном варианте осуществления изобретение относится к способу лечения шизофрении, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I),описываемому в контексте ранее, или его соли. В одном варианте осуществления изобретение относится к способу лечения страха или депрессии,который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I), описываемому в контексте ранее, или его соли. Изобретение относится также к способу лечения снижения познавательной способности, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I),описываемому в контексте ранее, или его соли. Изобретение относится также к способу лечения болезни Альцгеймера, который содержит введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I), описываемому в контексте ранее, или его соли. Обычно соединения формулы (I) или их соли можно вводить в дозах, которые составляют от приблизительно 0,1 до приблизительно 1000 мг в день и которые вводят в виде одной дозы или разделенных доз (т.е. от 1 до 4 доз в день), хотя неизбежно будут иметь место варианты, зависящие от вида, массы,возраста и состояния подвергаемого лечению субъекта, а также выбранного конкретного пути введения. В варианте изобретения дозу вводят один раз ежедневно. В варианте осуществления уровень дозы находится в диапазоне от приблизительно 0,1 до приблизительно 500 мг/кг массы тела в день. В следующем варианте осуществления уровень дозы находится в диапазоне от приблизительно 0,1 до приблизительно 100 мг/кг массы тела в день. Соединения формулы (I) и их соли могут быть также подходящими для применения в комбинации с другими активными средствами, такими как типичные и атипичные антипсихотические средства, стабилизаторы настроения, антидепрессанты, транквилизаторы, лекарственные средства от экстрапирамидальных побочных действий и средства для повышения познавательной способности, для обеспечения улучшенного лечения психотических нарушений. Комбинированными терапиями изобретения являются, например, введения вместе с вспомогательными средствами. Введение с вспомогательными средствами означает введение компонентов с одновременным окончанием действия или перекрывающееся введение каждого из компонентов в форме отдельных фармацевтических композиций или устройств. Эту схему терапевтического введения двух или более терапевтических агентов специалисты в данной области и в данном контексте обычно называют вспомогательным терапевтическим введением; она известна также как дополнительное терапевтическое введение. Любые и все лечебные схемы, в которых пациент получает раздельное введение компонентов, но с одновременным окончанием их действия, или перекрывающееся терапевтическое введение соединений формулы (I) или их солей и по меньшей мере одного антипсихотического агента, стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий или стимулятора познавания, находятся в объеме настоящего изобретения. В одном варианте осуществления дополнительного терапевтического введения, описываемого в контексте, пациента обыч-9 018113 но стабилизируют после терапевтического введения одного или нескольких компонентов в течение некоторого периода времени и затем ему вводят другой компонент. Соединения формулы (I) или их соли можно вводить в качестве дополнительного терапевтического лечения пациентам, которым вводят по меньшей мере один антипсихотический агент, стабилизатор настроения, антидепрессант, транквилизатор, лекарственное средство от экстрапирамидальных побочных действий или стимулятор познавания,но объем изобретения включает также дополнительное терапевтическое введение по меньшей мере одного антипсихотического агента, стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий или стимулятора познавания пациентам,которым вводят соединения формулы (I) или их соли. Комбинированные терапии изобретения можно также проводить одновременным введением. Одновременное введение означает схему лечения, при которой отдельные компоненты вводят вместе, либо в форме одной фармацевтической композиции или устройства, включающего в себя или содержащего оба компонента, либо в виде отдельных композиций или устройств, причем каждое содержит один из компонентов, вводимых одновременно. Такие комбинации отдельных индивидуальных компонентов для одновременного введения можно представить в форме набора отдельных частей. Поэтому в следующем аспекте изобретение относится к способу лечения психотического расстройства дополнительным терапевтическим введением соединения формулы (I) или его соли пациенту, получающему лечение введением по меньшей мере одного антипсихотического агента. В следующем аспекте изобретение относится к применению соединения формулы (I) или его соли при изготовлении лекарственного средства для дополнительного терапевтического введения с целью лечения психотического расстройства у пациента, получающего лечение введением по меньшей мере одного антипсихотического агента. Изобретение далее относится к соединению формулы (I) или его соли для применения при дополнительном терапевтическом введении для лечения психотического расстройства у пациента, получающего лечение введением по меньшей мере одного антипсихотического агента. В следующем аспекте изобретение относится к способу лечения психотического расстройства дополнительным терапевтическим введением по меньшей мере одного антипсихотического агента пациенту, получающему лечение введением соединения формулы (I) или его соли. В следующем аспекте изобретение относится к применению по меньшей мере одного антипсихотического агента при изготовлении лекарственного средства для дополнительного терапевтического введения при лечении психотического расстройства у пациента, получающего лечение введением соединения формулы (I) или его соли. Изобретение далее относится по меньшей мере к одному антипсихотическому агенту для дополнительного терапевтического введения при лечении психотического расстройства у пациента, получающего лечение введением соединения формулы (I) или его соли. В следующем аспекте изобретение относится к способу лечения психотического расстройства одновременным терапевтическим введением соединения формулы (I) или его соли в комбинации по меньшей мере с одним антипсихотическим агентом. Изобретение далее относится к применению комбинации соединения формулы (I) или его соли и по меньшей мере одного антипсихотического агента при изготовлении лекарственного средства для одновременного терапевтического введения при лечении психотического расстройства. Изобретение далее относится к применению соединения формулы (I) или его соли при изготовлении лекарственного средства для одновременного терапевтического введения по меньшей мере с одним антипсихотическим агентом при лечении психотического расстройства. Изобретение далее относится к соединению формулы (I) или его соли для применения при одновременном терапевтическом введении по меньшей мере с одним антипсихотическим агентом при лечении психотического расстройства. Изобретение далее относится к применению по меньшей мере одного антипсихотического агента при изготовлении лекарственного средства для одновременного терапевтического введения с соединением формулы (I) или его солью при лечении психотического расстройства. В следующем аспекте изобретение относится к набору частей для применения при лечении психотического расстройства, содержащему первую дозированную форму, содержащую соединение формулы(I) или его соль, и одну или несколько дополнительных дозированных форм, причем каждая содержит антипсихотический агент, для одновременного терапевтического введения. В другом аспекте изобретение относится к способу лечения психотического расстройства дополнительным терапевтическим введением соединения настоящего изобретения пациенту, получающему лечение введением активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения,антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий или стимулятора познавания. В следующем аспекте изобретение относится к применению соединения настоящего изобретения при изготовлении лекарственного средства для дополнительного терапевтического введения при лечении психотического расстройства у пациента, получающего лечение введением активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий или стимулятора познавания. Изобретение относится также к применению соединения настоящего изобретения при дополнительном терапевтическом введении для лечения психотического расстройства у пациента, получающего лечение введением активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий или стимулятора познавания. Изобретение далее относится к применению соединения настоящего изобретения для применения при дополнительном терапевтическом введении для лечения психотического расстройства у пациента,получающего лечение введением активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания. В следующем аспекте изобретение относится к способу лечения психотического расстройства дополнительным терапевтическим введением активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, пациенту, получающему лечение введением соединения настоящего изобретения. В следующем аспекте изобретение относится к применению активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при изготовлении лекарственного средства для дополнительного терапевтического введения при лечения психотического расстройства у пациента, получающего лечение введением соединения настоящего изобретения. Изобретение относится также к применению активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, для дополнительного терапевтического введения при лечении психотического расстройства у пациента, получающего лечение введением соединения настоящего изобретения. В следующем аспекте изобретение относится к способу лечения психотического расстройства одновременным терапевтическим введением соединения настоящего изобретения в комбинации с активным ингредиентом, выбранным из группы, состоящей из стабилизатора настроения, антидепрессанта,транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания. Изобретение далее относится к применению комбинации соединения настоящего изобретения и активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта,транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при изготовлении лекарственного средства для одновременного терапевтического введения при лечении психотического расстройства. Изобретение далее относится к применению комбинации соединения настоящего изобретения и активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта,транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, для одновременного терапевтического введения при лечении психотического расстройства. Изобретение далее относится к применению соединения настоящего изобретения при изготовлении лекарственного средства для одновременного терапевтического введения с активным ингредиентом, выбранным из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при лечении психотического расстройства. Изобретение далее относится к применению соединения настоящего изобретения для одновременного терапевтического введения с активным ингредиентом, выбранным из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при лечении психотического расстройства. Изобретение далее относится к соединению настоящего изобретения для применения для одновременного терапевтического введения с активным ингредиентом, выбранным из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при лечении психотического расстройства. Изобретение далее относится к применению активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, при изготовления лекарственного средства для одновременного терапевтического введения с соединением настоящего изобретения при лечении психотического расстройства. Изобретение далее относится к применению активного ингредиента, выбранного из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, для одновременного терапевтического введения с соединением настоящего изобретения при лечении психотического расстройства. В следующем аспекте изобретение относится к набору частей для применения при лечении психотического расстройства, содержащему первую дозированную форму, содержащую соединение настоящего изобретения, и одну или несколько дополнительных дозированных форм, причем каждая форма со- 11018113 держит активный ингредиент, выбранный из группы, состоящей из стабилизатора настроения, антидепрессанта, транквилизатора, лекарственного средства от экстрапирамидальных побочных действий и стимулятора познавания, для одновременного терапевтического введения. Примеры антипсихотических лекарственных средств, которые могут быть применимыми в настоящем изобретении, включают, но не ограничиваются перечисленным, блокаторы натриевых каналов; смешанные антагонисты 5HT/рецептора допамина; позитивные модуляторы mGluR5; антагонисты D3; антагонисты 5HT6; модуляторы никотинового альфа-7; ингибиторы глицинового транспортера GlyT1; частичный агонист D2/антагонист D3/антагонисты H3; модуляторы АМРА; антагонисты NK3, такие как озанетант и талнетант; атипичное антипсихотическое средство, например клозапин, оланзапин, рисперидон, кветиапин, арипиразол, зипразидон и амисульприд; бутирофеноны, такие как галоперидол, пимозид и дроперидол; фенотиазины, такие как хлорпромазин, тиоридазин, мезоридазин, трифлуоперазин, перфеназин, флуфеназин, тифлупромазин, прохлорперазин и ацетофеназин; тиоксантены, такие как тиотиксен и хлорпротиксен; тиенобензодиазепины; дибензодиазепины; бензизоксазолы; дибензотиазепины; имидазолидиноны; бензизотиазолилпиперазины; триазин, такой как ламотригин; дибензоксазепины, такие как локсапин; дигидроиндолоны, такие как молиндон; арипипразол; и их производные, которые обладают антипсихотической активностью. Примерами торговых наименований и поставщиков выбранных антипсихотических лекарственных средств, которые могут быть подходящими для применения в настоящем изобретении, являются следующие: клозапин (доступен под торговым названием CLOZARIL от MyIan, Zenith Goldline, UDL, Novartis); оланзапин (доступен под торговым названием ZYPREXA от Lilly); зипразидон (доступен под торговым названием GEODON от Pfizer); рисперидон (доступен под торговым названиемRISPERDAL, от Janssen); кветиапина фумарат (доступен под торговым названием SEROQUEL отAstraZeneca); сертиндол (доступен под торговым названием SERLECT); амисульприд (доступен под торговым названием SOLION от Sanofi-Synthelabo); галоперидол (доступен под торговым названиемHALDOL от Ortho-McNeil); галоперидола деканоат (доступен под торговым названием HALDOL decanoate; галоперидола лактат (доступен под торговым названием HALDOL и INTENSOL); хлорпромазин (доступен под торговым названием THORAZINE от SmithKline Beecham (GSK); флуфеназин(доступен под торговым названием PROLIXIN от Apothecon, Copley, Schering Teva and American Pharmaceutical Partners, Pasadena); флуфеназина деканоат (доступен под торговым названием PROLIXIN decanoate); флуфеназина энантат (доступен под торговым названием PROLIXIN); флуфеназина гидрохлорид (доступен под торговым названием PROLIXIN); тиотиксен (доступен под торговым названиемNAVANE от Pfizer); тиотиксена гидрохлорид (доступен под торговым названием NAVANE); трифлуоперазин (дигидрохлорид 10-[3-(4-метил-1-пиперазинил)пропил]-2-трифторметил)фенотиазина, доступен под торговым названием STELAZINE от SmithKline Beckman); перфеназин (доступен под торговым названием TRILAFON от Schering); перфеназин и амитриптилина гидрохлорид (доступен под торговым названием ETRAFON TRILAFON); тиоридазин (доступен под торговым названиемMELLARIL от Novartis, Roxane, HiTech, Teva and Alpharma); молиндон (доступен под торговым названием MOBAN от Endo); молиндона гидрохлорид (доступен под торговым названием MOBAN); локсапин (доступен под торговым названием LOXITANE от Watson); локсапина гидрохлорид (доступен под торговым названием LOXITANE) и локсапина сукцинат (доступен под торговым названием LOXITANE). Кроме того, можно применять бенперидол (Glianimon), перазин (Taxilan) или мелперон(Eunerpan). Другие подходящие антипсихотические лекарственные средства включают промазин (доступен под торговым названием SPARINE), трифлурпромазин (доступен под торговым названием VESPRIN),хлорпротиксен (доступен под торговым названием TARACTAN), дроперидол (доступен под торговым названием INAPSINE), ацетофеназин (доступен под торговым названием TINDAL), прохлорперазин(доступен под торговым названием COMPAZINE), метотримепразин (доступен под торговым названием NOZINAN), пипотиазин (доступен под торговым названием PIPOTRIL), илоперидон, пимозид и флупентиксол. Антипсихотические лекарственные средства, перечисленные выше под торговым названием, могут быть также доступными от других поставщиков под другим торговым названием. В одном следующем аспекте изобретения подходящие антипсихотические агенты включают оланзапин, рисперидон, кветиапин, арипипразол, галоперидол, клозапин, зипразидон, талнетант и озанетант. Стабилизаторы настроения, которые можно применять в терапии настоящего изобретения, включают вапроат лития, натрия/вапроевую кислоту/дивалпроэкс, карбамазепин, ламотригин, габапентин,топирамат, оксарбазепин и тиагабин. Антидепрессантные лекарственные средства, которые можно применять при терапии настоящего изобретения, включают антагонисты серотонина, антагонисты CRF-1, двойные антагонисты ингибитораCox-2/SSRI; тройные ингибиторы повторного поглощения допамина/норадреналина/серотонина; антагонисты NK1; двойные антагонисты NK1 и NK2; двойные антагонисты NK1/SSRI; антагонисты NK2; аго- 12018113 нисты серотонина (такие как рауволсцин, иохимбин и метоклопрамид); ингибиторы повторного поглощения серотонина (такие циталопрам, эсциталопрам, флуоксетин, флувоксамин, фемоксетин, индалпин,цимелдин, пароксетин и сертралин); двойные ингибиторы повторного поглощения серотонина/норадреналина (такие как венлафаксин, ребоксетин, дулоксетин и милнаципран); ингибиторы повторного поглощения норадреналина (такие как ребоксетин); трициклические антидепрессанты (такие как амитриптилин, кломипрамин, имипрамин, мапротилин, нортриптилин и тримипрамин); ингибиторы моноаминоксидазы (такие как изокарбоксазид, моклобемид, фенелзин и транилципромин); антагонисты 5HT3 (такие как, например, ондансетрон и гранисетрон) и другие (такие как бупропион, аминептин, радафаксин, миансерин, миртазапин, нефазодон и тразодон). Анксиолитики, которые можно применять в терапии настоящего изобретения, включают антагонисты V1b, антагонисты 5HT7 и бензодиазепины, такие как алпразолам и лоразепам. Лекарственные средства от экстрапирамидальных побочных действий, которые можно применять в терапии настоящего изобретения, включают антихолинергические средства (такие как бензтропин, бипериден, проциклидин и тригексифенидил), антигистамины (такие как дифенгидрамин) и допаминергические средства (такие как амантадин). Стимуляторы познавания, которые можно применять в терапии настоящего изобретения, включают, например, ингибиторы холинэстеразы (такие как такрин, донепезил, ривастигмин и галантамин), антагонисты H3 и агонисты мускаринового M1 (такие как цевимелин). В одном варианте осуществления активным ингредиентом для применения в комбинации с соединением настоящего изобретения является атипичное антипсихотическое средство, например клозапин,оланзапин, рисперидон, кветиапин, арипиразол, зипразидон или амисульприд. В одном варианте осуществления активным ингредиентом для применения в комбинации с соединением настоящего изобретения является обычное антипсихотическое средство, например хлорпромазин, тиоридазин, мезоридазин, флуфеназин, перфеназин, прохлорперазин, трифлуоперазин, тиотиксин,галоперидол, тифлурпромазин, пимозид, дроперидол, хлорпротиксен, молиндон или локсапин. В другом варианте осуществления активным ингредиентом для применения в комбинации с соединением настоящего изобретения является стабилизатор настроения, например валпроат лития, натрия/валпроевая кислота/дивалпроэкс, карбамазепин, ламотригин, габапентин, топирамат, оксарбазепин или тиагабин. В другом варианте осуществления активным ингредиентом для применения в комбинации с соединением настоящего изобретения является антидепрессант, например агонист серотонина (такой как рауволсцин, иохимбин или метоклопрамид); ингибитор повторного поглощения серотонина (такой как циталопрам, эсциталопрам, флуоксетин, флувоксамин, фемоксетин, индалпин, цимелдин, пароксетин или сертралин); двойной ингибитор повторного поглощения серотонина/норадреналина (такой как венлафаксин, ребоксетин, дулоксетин или милнаципран); ингибиторы повторного поглощения норадреналина(такие как ребоксетин); трициклические антидепрессанты (такие как амитриптилин, кломипрамин,имипрамин, мапротилин, нортриптилин или тримипрамин); ингибитор моноаминоксидазы (такой как изокарбоксазид, моклобемид, фенелзин или транилципромин) или другое соединение (такое как бупропион, аминептин, радафаксин, миансерин, миртазапин, нефазодон или тразодон). В другом варианте осуществления активным ингредиентом для применения в комбинации с соединением настоящего изобретения является анксиолитическое средство, например бензодиазепин, такой как алпразолам или лоразепам. Для применения в медицине соединения настоящего изобретения обычно вводят в виде стандартной фармацевтической композиции. Настоящее изобретение поэтому относится в следующем аспекте к фармацевтической композиции, содержащей соединение формулы (I), описываемое в контексте ранее,или его соль и фармацевтически приемлемый носитель или эксципиент. Фармацевтическую композицию можно применять при лечения любого из описанных в контексте состояний. Соединения изобретения можно вводить любым общепринятым способом, например пероральным,парентеральным (например, внутривенным), трансбуккальным, сублингвальным, назальным, ректальным или чрескожным введением, и фармацевтические композиции адаптированы соответственно этому способу. Соединения изобретения, которые являются активными при введении перорально, можно изготавливать в виде жидкостей или твердых композиций, например сиропов, суспензий или эмульсий, таблеток, капсул и лепешек. Жидкий препарат обычно состоит из суспензии или раствора соединения или его соли в подходящем жидком носителе(ях), например водном растворителе, таком как вода, этанол или глицерин, или неводном растворителе, таком как полиэтиленгликоль или масло. Препарат может содержать также суспендирующий агент, консервант, корригент или красящий агент. Композицию в форме таблетки можно получить с применением подходящего фармацевтического носителя(ей), обычно применяемого для получения твердых препаратов. Примеры таких носителей включают стеарат магния, крахмал, лактозу, сахарозу и целлюлозу. Композицию в форме капсулы можно получить с применением обычных методик капсулирования. Например, шарики, содержащие активный ингредиент, можно получить с применением стандартных носителей, и затем капсулу из твердого желатина можно заполнить этими шариками; или же, дисперсию или суспензию можно получить с применением любого подходящего фармацевтического носителя(ей),например водных камедей, целлюлоз, силикатов или масел, и затем капсулу из мягкого желатина можно заполнить дисперсией или суспензией. Обычные парентеральные композиции состоят из раствора или суспензии соединения либо соли в стерильном водном носителе или парентерально приемлемом масле, например полиэтиленгликоле, поливинилпирролидоне, лецитине, арахисовом масле или кунжутном масле. В альтернативном варианте раствор можно лиофилизовать и затем восстановить подходящим растворителем непосредственно перед введением. Композиции для назального введения можно изготовить общепринятым образом в виде аэрозолей,капель, гелей и порошков. Аэрозольные препараты обычно содержат раствор или тонкую суспензию активного вещества в фармацевтически приемлемом водном или неводном растворителе и обычно представлены в количествах одной или многих доз в стерильной форме в герметизированном контейнере,который может иметь форму картриджа или устройства для дополнения, для применения в устройстве для распыления. В альтернативном случае герметизированным контейнером может быть устройство для дозированного распределения, такое как назальный ингалятор для одной дозы или аэрозольный ингалятор, снабженный дозирующим клапаном, который предназначен для ликвидации после того, как содержимое контейнера истощится. Когда дозированная форма содержит аэрозольный ингалятор, она будет содержать пропеллент, которым может быть сжатый газ, такой как сжатый воздух, или органический пропеллент,такой как фторхлоруглеводород. Аэрозольными дозированными формами могут быть также аэрозольные ингаляторы, снабженные насосом. Композиции, подходящие для трансбуккального или сублингвального введения, включают таблетки, лепешки и пастилки, в которых активный ингредиент изготавливают в смеси с носителем, таким как сахар и аравийская камедь, трагакант или желатин, и глицерином. Композиции для ректального введения обычно имеют форму суппозиториев, содержащих общепринятую основу суппозитория, такую как какао-масло. Композиции, подходящие для чрескожного введения, включают мази, гели и пластыри. Композиция может быть в виде единичной дозированной формы, такой как таблетка, капсула или ампула. Каждая единичная доза для перорального введения может содержать, например, от 1 до 500 мг(и для парентерального введения содержит, например, от 0,1 до 50 мг) соединения формулы (I) или его соли, причем количество соединения вычислено в виде его свободного основания. В варианте осуществления единичная доза для перорального введения одержит от 50 до 450 мг. В следующем варианте осуществления единичная доза содержит от 100 до 400 мг. Для достижения согласованности с дополнительным введением, композиции каждого из компонентов или комбинация компонентов находится, например, в форме единичной дозы. Поддерживающие изобретение соединения Получение ряда соединений изобретения описано ниже. В методиках, которые приведены ниже, после каждого исходного вещества обычно указывается промежуточный продукт. Это делается только для оказания помощи квалифицированному химику. Исходное вещество не обязательно можно получать из указанного источника. Соединения изобретения и промежуточные продукты названы с применением программного обеспечения для химических названий ACD/Name PRO 6.02 (Advanced Chemistry Development Inc., Toronto,Ontario, M5H2L3, Canada). АббревиатурыDCC - дициклогексилкарбодиимид. Исходные вещества получали от коммерческих поставщиков и применяли без дополнительной очистки, если не указано иначе. Флэш-хроматографию проводили с применением предварительно заполненных колонок силикагеля Isolute FIash или Biotage в качестве неподвижной фазы и растворителей с аналитической чистотой в качестве элюентов, если не указано иначе. ЯМР-спектры получали при 298 K, 303,2 K или 300 K при указанной частоте с применением прибора либо Bruker DPX400, либо AV400, и спектры снимали в разбавленных растворах соединений вCDCl3, если не указано иначе. Все ЯМР-спектры были указаны относительно тетраметилсилана (ТМС, Н 0, С 0). Все константы взаимодействия указываются в Герцах (Гц) и мультиплетность обозначают как с(синглет), ушир. с (уширенный синглет), д (дублет), кв. (квартет), дд (дублет дублетов), дт (двойной триплет) и м (мультиплет). Записи общего ионного тока получали для положительной и отрицательной ионизации электрораспылением (ES+/ES-) и/или химической положительной и отрицательной ионизации при атмосферном давлении (АР+/АР-). При необходимости, указанные времена удерживания применяли в качестве показателя для очистки с применением масс-направленной автоматической очистки (MDAP). Очистка. Ряд соединений очищали с применением системы масс-направленной автоматической очистки В круглодонную колбу 4-амино-3-метилбензонитрил (Alfa Aesar, Avocado, Lancaster; 10,88 г, 82 ммоль) и Et3N (22,95 мл, 165 ммоль) перемешивали в DCM (200 мл) при 0C. Через капельную воронку медленно добавляли TFAA (13,95 мл, 99 ммоль) и смесь перемешивали при комнатной температуре в течение 30 мин. Реакционную смесь выливали в 2 М HCl (150 мл). Органический слой затем собирали и затем промывали насыщенным раствором бикарбоната натрия (150 мл), сушили (MgSO4), фильтровали и растворитель удаляли, получая при этом темно-желтое твердое вещество (19,37 г); m/z (ES-) 227 (M-1); 1 В круглодонной колбе N-(4-циано-2-метилфенил)-2,2,2-трифторацетамид (промежуточный продукт 1, 19,37 г, 85 ммоль), сульфурилдихлорид (27,6 мл, 340 ммоль) и дифенилпероксиангидрид (1,028 г, 4,24 ммоль) нагревали в тетрахлориде углерода (210 мл) при 100C в течение 3 ч. Смесь охлаждали до комнатной температуры и затем реакционную смесь выливали в 2 М HCl (350 мл). Органический слой затем собирали и растворитель удаляли, получая при этом N-[2-(хлорметил)-4-цианофенил]-2,2,2 трифторацетамид в виде оранжевого масла (25,54 г), который применяли на следующей стадии без дополнительной очистки. Это масло добавляли к трифенилфосфину (26,2 г, 100 ммоль) и смесь нагревали в толуоле (300 мл) при 110C в течение 3 ч. Смесь охлаждали до комнатной температуры на протяжении ночи, осадок отделяли фильтрованием и промывали небольшими количествами толуола и диэтилового простого эфира, получая при этом указанное в заголовке соединение в виде не совсем белого твердого вещества (29,91 г); m/z (ES+) 489; 1 Н ЯМР (400 МГц, CDCl3):12,32 (1H, с), 7,79-7,57 (16H, м), 7,50 (1H,д), 7,38 (1H, с), 6,18 (2H, д). Промежуточный продукт 3. 2-Трифторметил-1H-индол-5-карбонитрил Хлорид (5-циано-2-[(трифторацетил)амино]фенилметил)(трифенил)фосфония (промежуточный продукт 2, 50,41 г, 95 ммоль) нагревали в ДМФА (180 мл) при 140C в течение 7 ч. Смесь охлаждали до комнатной температуры и растворитель выпаривали. Этот остаток объединяли с соответствующим остатком из другого эксперимента (в котором промежуточный продукт 2, 7,9 г, 15,05 ммоль, нагревали в ДМФА (50 мл) при 155C в течение 2 ч). Объединенные остатки подвергали азеотропной перегонке с толуолом (100 мл 2). Образовавшийся остаток обрабатывали диэтиловым эфиром (500 мл), осадок отделяли фильтрованием и промывали диэтиловым эфиром (100 мл). Фильтрат выпаривали, образовавшееся оранжевое масло (60 г) растворяли в DCM (200 мл) и перемешивали при комнатной температуре. Добавляли изогексан до тех пор, пока раствор оставался мутным (400 мл), и смесь перемешивали в течение 3 дней. Присутствие осадка не наблюдали, поэтому смесь упаривали и хроматографировали (Biotage 75L, элюирование дихлорметаном), получая при этом указанное в заголовке соединение в виде бесцветного твердого вещества (21,7 г); m/z (ES-) 209 (M-1); 1 Н ЯМР (400 МГц, CDCl3):8,85 (1H, ушир.с), 8,08 5-Циано-2-(трифторметил)-1H-индол-3-карбоновую кислоту (промежуточный продукт 13, 2,09 г) растворяли в NMP (10 мл) и затем добавляли H2O (1 мл). Смесь нагревали до 130-140C на протяжении ночи в атмосфере азота. Раствор охлаждали до комнатной температуры и добавляли H2O (30 мл), раствор перемешивали в течение 40 мин и затем фильтровали. Осадок промывали H2O. Продукт затем сушили в вакууме при 40C, получая при этом указанное в заголовке соединение (1,42 г). 1 Н ЯМР (300 МГц,ДМСО-d6),8,26 (1H, с), 7,64 (2H, с), 7,18 (1H, с). Промежуточный продукт 4. [(2-Трифторметил-1H-индол-5-ил)метил]амин Раствор 2-трифторметил-1H-индол-5-карбонитрила (промежуточный продукт 3, 0,16 г, 0,761 ммоль) в тетрагидрофуране (5 мл), охлажденный на бане лед-вода, обрабатывали 1 М раствором комплекса боран-тетрагидрофуран (3,05 мл, 3,05 ммоль), добавляемым по каплям через шприц. Реакционную смесь затем оставляли для перемешивания в течение 18 ч, позволяя ей нагреться до комнатной температуры. Реакционную смесь затем гасили метанолом (10 мл) и перемешивали при комнатной температуре в течение 10 мин. Реакционную смесь затем выливали на картридж SCX (10 г) и хорошо промывали метанолом. Требуемый продукт затем элюировали с применением раствора 2 М аммиак/метанол. Упаривание досуха давало указанное в заголовке соединение, которое применяли на следующейстадии без дополнительной очистки. Промежуточный продукт 5. Гидрохлорид [(2-трифторметил-1H-индол-5-ил)метил]амина Раствор 2-(трифторметил)-1H-индол-5-карбонитрила (промежуточный продукт 3, 21,7 г, 103 ммоль) в ТГФ (300 мл), охлажденный на бане лед-вода, обрабатывали комплексом боран-тетрагидрофуран (250 мл, 250 ммоль), добавленным по каплям через капельную воронку. Смесь перемешивали в атмосфере аргона в течение 5 ч, позволяя ей нагреться до комнатной температуры. Смесь затем перемешивали в течение дополнительных 18 ч при комнатной температуре. По каплям добавляли метанол (100 мл) и смесь затем перемешивали в течение 20 мин при комнатной температуре. Растворители удаляли и остаток растворяли в метаноле (300 мл). Смесь затем нагревали при кипении с обратным холодильником в течение 1 ч. Смесь охлаждали до комнатной температуры, добавляли раствор HCl/простой эфир (1 М,200 мл) и растворители выпаривали. Остаток растирали с диэтиловым эфиром (2200 мл). Остаток перемешивали в DCM (50 мл) и до- 16018113 бавляли диэтиловый эфир (300 мл) и дополнительную порцию HCl в простом эфире (1 М, 100 мл). Смесь затем фильтровали в атмосфере Ar и твердое вещество сушили в вакуумном сушильном шкафу, получая при этом указанное в заголовке соединение в виде бесцветного твердого вещества (21,7 г); m/z (ES-) 213 2-(Трифторметил)-1H-индол-5-карбонитрил (промежуточный продукт 3A, 25 г), PtO2-H2O (3%, 750 мг) и MeOH (175 мл) добавляли в колбу для гидрирования. Добавляли 4 М раствор HCl в диоксане (89 мл) и реакционный сосуд продували N2 и затем Н 2. Смесь гидрировали при 60 фунт/кв.дюйм (413685,6 Па) Н 2 и 17-23C в течение 24 ч. Смесь фильтровали через целит и затем через фильтр PTFE 0,2 мкм. Затем добавляли смолу МР-ТМТ (15 мас.%) и суспензию перемешивали в течение 3 ч при 40C, охлаждали до 17-23C и затем фильтровали через подушку целита. Подушку целита и смолу промывали MeOH (100 мл). Раствор концентрировали до минимума вакуумной дистилляцией, добавляли н-пропанол (200 мл) и концентрировали до минимума. Добавляли толуол (200 мл), затем циклогексан (75 мл) и суспензию оставляли для перемешивания в течение 2 ч при 17-23C. Смесь затем охлаждали до 0-5C и оставляли для перемешивания в течение 2 ч. Твердое вещество отделяли фильтрованием и промывали толуолом, получая при этом указанное в заголовке соединение (25,3 г); 1 Н ЯМР (300 МГц, ДМСО-d6):8,55 (3H, с), 7,80 В 500 мл круглодонной колбе N-(4-циано-2-метилфенил)-2,2,2-трифторацетамид (промежуточный продукт 1; 7,3 г, 32,0 ммоль), NBS (5,98 г, 33,6 ммоль) и бензоилпероксид (70%) (1,162 г, 4,80 ммоль) добавляли к тетрахлориду углерода (150 мл). Реакционную смесь затем нагревали при кипении с обратным холодильником в атмосфере аргона в течение 4 дней. Реакционную смесь охлаждали до комнатной температуры, затем добавляли NBS (0,5 экв., 3 г) и бензоилпероксид (0,075 экв., 0,581 г). Реакционную смесь затем нагревали при кипении с обратным холодильником в течение дополнительных 18 ч. Реакционной смеси давали возможность охладиться до комнатной температуры, затем выливали в 2 М NaOH(100 мл). Органический слой собирали, затем промывали раствором метабисульфита натрия (10 г в 100 мл воды), сушили (MgSO4), фильтровали и растворитель удаляли. Образовавшееся оранжевое масло затем очищали пропусканием через слой силикагеля, элюируя 1-10% раствором EtOAc:изогексан. Требуемые фракции затем объединяли и упаривали досуха, получая при этом смесь 1:1 указанного в заголовке соединения и исходного вещества в виде оранжевого твердого вещества (9 г), которую затем применяли на следующей стадии без дополнительной очистки. Промежуточный продукт 7. Бромид (5-циано-2-[(трифторацетил)амино]фенилметил)(трифенил)фосфония В 250 мл круглодонной колбе N-[2-(бромметил)-4-цианофенил]-2,2,2-трифторацетамид (промежуточный продукт 6,6 г, 19,54 ммоль) растворяли в толуоле (100 мл). Добавляли трифенилфосфин (5,12 г,19,54 ммоль) и реакционную смесь нагревали до 85C в атмосфере аргона в течение 5 ч. Реакционной смеси давали возможность охладиться до комнатной температуры и образовавшееся желтое твердое вещество собирали, промывали толуолом, получая при этом указанное в заголовке соединение в виде желтого твердого вещества (6,5 г); m/z (ES+) 489; 1 Н ЯМР (400 МГц, ДМСО-d6):11,19 (1H, с), 7,79-7,57 Бромид (5-циано-2-[(трифторацетил)амино]фенилметил)(трифенил)фосфония (промежуточный продукт 7, 32 г) растворяли в ДМФА (150 мл) и добавляли обесцвечивающий уголь (32 г). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч. Реакционную смесь затем фильтровали,промывая ДМФА (100 мл). Затем к фильтрату добавляли N-бромсукцинимид (34,9 г) и реакционную смесь затем перемешивали при комнатной температуре на протяжении ночи. Реакционную смесь гасили насыщенным раствором метабисульфита натрия (500 мл) и перемешивали при комнатной температуре в течение 30 мин. Реакционную смесь затем экстрагировали этилацетатом (2400 мл) и органические экстракты объединяли, сушили (MgSO4), фильтровали и растворитель удаляли, получая при этом бромид(3-бром-5-циано-2-[(трифторацетил)амино]фенилметил)(трифенил)фосфония в виде неочищенного продукта, который затем применяли в следующей реакции без дополнительной очистки (37,2 г); m/z(ES+) 568 и 570 (M+1). Бромид (3-бром-5-циано-2-[(трифторацетил)амино]фенилметил)(трифенил)фосфония (37,2 г, неочищенный) растворяли в ДМФА (150 мл) и реакционную смесь нагревали до 130C при перемешивании в течение 3 ч. Реакционной смеси позволяли охладиться до комнатной температуры, затем гасили водой(400 мл). Реакционную смесь затем экстрагировали этилацетатом (3300 мл). Органический слой экстрагировали смесью 1:1 вода:насыщенный раствор соли (2600 мл), сушили (MgSO4), фильтровали и растворитель удаляли. Образовавшиеся остатки затем очищали фильтрованием через подушку силикагеля,элюируя 2-10% раствором EtOAc:изогексан, получая при этом указанное в заголовке соединение в виде не совсем белого твердого вещества (6 г); m/z (ES-) 287+289 (M-1); 1 Н ЯМР (400 МГц, ДМСО-d6):13,15 Раствор 2-(трифторметил)-5-циано-7-бром-1H-индола (промежуточный продукт 8; 200 мг, 0,692 ммоль) в ТГФ (10 мл), охлажденный на бане лед-вода, обрабатывали комплексом боран-тетрагидрофуран(1 М раствор в ТГФ, 1,522 мл, 1,522 ммоль), добавляемым по каплям через шприц, и перемешивали в атмосфере аргона в течение 18 ч при предоставлении возможности нагреться до комнатной температуры. Реакционную смесь затем гасили метанолом (5 мл) и перемешивали при комнатной температуре в течение 10 мин. Реакционную смесь затем упаривали досуха, получая при этом указанное в заголовке соединение в виде белой пены (230 мг), которое применяли на следующей стадии без дополнительной очистки; m/z 290/292 (M-H). Промежуточный продукт 10. 1-Метил-2-трифторметил-5-цианоиндол Гидрид натрия (60% в минеральном масле) (76 мг, 1,903 ммоль) добавляли к 2-трифторметил-1Hиндол-5-карбонитрилу (промежуточный продукт 3, 200 мг, 0,952 ммоль), перемешиваемому в ДМФА (5 мл) в атмосфере аргона при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и затем добавляли иодметан (0,119 мл, 1,903 ммоль). Реакционную смесь оставляли для перемешивания в течение дополнительного 1 ч. Реакционную смесь выливали в воду (50 мл) и экстрагировали этилацетатом (50 мл). Органический экстракт промывали смесью 1:1 вода:насыщенный раствор соли (50 мл 2), сушили (MgSO4), фильтровали и растворитель удаляли, получая при этом указанное в заголовке соединение (290 мг), которое затем применяли в следующей реакции без дополнительной очистки; 1H ЯМР (400 МГц, CDCl3):8,05 (1H, д), 7,59 (1H, дд), 7,46 (1H, д), 7,03 (1H,с), 3,90 (3H, с); m/z 225 (M+H). Промежуточный продукт 11. [1-Метил-2-(трифторметил)-1H-индол-5-ил]метиламин(2,36 мл, 2,36 ммоль), добавляемым по каплям через шприц, и перемешивали в атмосфере аргона в течение 24 ч. Реакционную смесь гасили метанолом (5 мл) и перемешивали при комнатной температуре в течение 10 мин. Реакционную смесь упаривали досуха, получая при этом неочищенное указанное в заголовке соединение в виде белой пены (300 мг), которое применяли на следующей стадии без дополнительной очистки. В круглодонную колбу, снабженную капельной воронкой, термометром, парциальным конденсатором горячего орошения и входным отверстием для азота, добавляли 4-циано-2-иоданилин (7,88 г), ацетонитрил (24 мл) и триэтиламин (4,5 мл). При поддержании температуры ниже 35-40C к суспензии добавляли трифторуксусный ангидрид (5,0 мл). Примечание: экзотермический эффект регулируют изменением скорости добавления. Реакционную смесь перемешивали в течение 30 мин, разбавляли водой (31,5 мл). Примечание: добавление начальной части является экзотермическим, и скорость добавления регулируют. Суспензию выдерживали при 15-20C в течение 60 мин. Продукт выделяли фильтрованием. Твердое вещество промывали 80% водным ацетонитрилом и сушили в вакууме, получая при этом указанное в заголовке соединение в виде бесцветного твердого вещества (9,9 г); 1 Н ЯМР (300 МГц, CDCl3)8,49 (1H, ушир.с), 8,45 (1H, д), 8,15 (1H, с), 7,75 (1H, д). Промежуточный продукт 13. 5-Циано-2-(трифторметил)-1H-индол-3-карбоновая кислотаCs2CO3 (95,82 г), CuI (3,36 г) и L-пролин (9,06 г) добавляли в реакционный сосуд на 1 л. Сосуд продували N2. Затем в реакционный сосуд добавляли ДМСО (80 мл) и содержимое перемешивали при 1823C в течение 10 мин. Затем N-(4-циано-2-иодфенил)-2,2,2-трифторацетамид (промежуточный продукт 12, 40 г) добавляли в разделительную воронку и растворяли в ДМСО (40 мл). Раствор промежуточного продукта 12 затем добавляли в реакционный сосуд на протяжении периода по меньшей мере 15 мин при регулировании выделения газа CO2. Реакционный раствор перемешивали в течение 10 мин. К реакционной смеси затем добавляли трет-бутилацетоацетат (19,5 мл). Реакционный раствор нагревали до 85-90C и перемешивали в течение 1 ч. К реакционному раствору затем добавляли дополнительные 0,5 экв. третбутилацетоацетата. Реакционную смесь затем перемешивали в течение дополнительного 1 ч. К реакционной смеси затем добавляли дополнительные 0,5 экв. трет-бутилацетоацетата и реакционную смесь перемешивали на протяжении ночи. После завершения реакции содержимое в сосуде охлаждали до 1823C. На протяжении периода 15 мин добавляли H2O (160 мл) при поддержании температуры реакции ниже 35C. Затем добавляли изопропилацетат (160 мл) и толуол (320 мл) с последующим добавлениемH2O (160 мл). Водный слой отделяли и органический слой промывали насыщенным раствором NH4Cl(200 мл). Из органического слоя затем удаляли растворитель вакуумной дистилляцией, уменьшая объем слоя до минимума. Добавляли DCM (160 мл) и температуру содержимого регулировали до 18-23C. На протяжении периода 15 мин добавляли трифторуксусную кислоту (34,95 мл). Раствор перемешивали на протяжении ночи. Твердое вещество отделяли фильтрованием и промывали DCM (280 мл). Твердое вещество сушили в вакуумном сушильном шкафу, получая при этом указанное в заголовке соединение(10 мл). Добавляли оксалилхлорид (0,131 мл, 1,494 ммоль), затем ДМФА (2,89 мкл, 0,037 ммоль) и реакционную смесь оставляли для перемешивания при комнатной температуре в течение 2 ч в атмосфере аргона. Реакционную смесь упаривали досуха и образовавшийся остаток растворяли в DCM (10 мл). Добавляли раствор [(2-трифторметил-1 Н-индол-5-ил)метил]амин (промежуточный продукт 4, 160 мг, 0,747 ммоль) в DCM (10 мл) с последующим добавлением триэтиламина (0,208 мл, 1,494 ммоль). Реакционную смесь оставляли для перемешивания при комнатной температуре в течение 1 ч. Реакционную смесь упаривали досуха и образовавшиеся остатки очищали MDAP, получая при этом указанное в заголовке соединение (176 мг); m/z (ES+) 388 (M+1); 1 Н ЯМР (400 МГц, d4 MeOD):9,35 (1H, д), 8,43 (1H, дд), 8,12(1500 мл) и тетрагидрофуран (5,1 л) помещали в колбу, снабженную капельной воронкой, термометром и отверстием для ввода азота. Смесь энергично перемешивали в течение 10-15 мин. Смесь охлаждали до 5C и медленно добавляли пропилфосфоновый ангидрид (3,2 л, 50 мас.% раствора). Смесь перемешивали при 15C в течение 2 ч. Смесь охлаждали до 5C и гасили медленным добавлением воды (505 мл). рН доводили до 5-6 добавлением 20 мас.% K3PO4 (2,9 л). Смесь разбавляли EtOAc (3,2 л) и температуру доводили до 15-20C. Фазы разделяли и органическую смесь промывали последовательно водой (1,5 л) и затем 5 мас.% раствором бикарбоната натрия (2,6 л). Смесь фильтровали и растворитель удаляли в вакууме до минимального объема. Добавляли изопропиловый спирт (2,0 л), смесь фильтровали и растворитель удаляли в вакууме два раза. Добавляли изопропиловый спирт (980 мл) и смесь нагревали до 7080C. Добавляли воду (1,5 л) при поддержании температуры выше 65C и проведении мониторинга мутности. Температуру регулировали до 65C, вносили затравку продукта (4,5 г) и смесь выдерживали при 65C в течение 30 мин. Смесь охлаждали до 5C на протяжении ночи и продукт выделяли фильтрованием, твердое вещество промывали холодным 10% раствором IPA в воде (1 л), затем сушили в вакуумном сушильном шкафу, получая при этом указанное в заголовке соединение (529 г); 1 Н ЯМР (300 МГц,ДМСО-d6)12,24 (1H, с), 9,48 (1H, с), 9,22 (1H, с), 8,52 (1H, с), 8,05 (1H, с), 7,66 (1H, с), 7,47 (1H, д), 7,32(1H, д), 7,00 (1H, с), 4,60 (2H, с). Соединение 1 А характеризовали следующим образом. Порошковая рентгенография (XRPD). Анализ порошковой рентгенографией проводили с применением излучения Cu K.alpha на порошковом дифрактометре Phillips X'pert Pro, Model PW3040 Pro, снабженном детектором Phillips X'CeleratorRTMS (Real Time Multi Strip). Данные собирали в режиме реального времени на протяжении непрерывного сканирования тета-два тета при 32 с/0,00167/стадию от 2 2 до 40 2. Напряжение и ток в трубке были 40 кВ и 40 мА. Рентгенограмма XRPD показана на фиг. 1. Углы характеристической XRPD указаны ниже в табл. 1. Предел ошибки составляет приблизительно 0,2 2 для каждого из установленных значений для пиков. Положения пиков измеряли с применением программного обеспечения PANalytical X'Pert Highscore Plus. Таблица 1 Спектр комбинационного рассеяния. Спектр комбинационного рассеяния соединения 1 А регистрировали с применением образца, помещенного на покрытое A1 предметное стекло, с применением спектрометра Nicolet 960 E.S.P. FT-Raman при разрешающей способности 4 см-1 с возбуждением от лазера Nd:VO4 (1064 нм) и выходом мощности 433 мВт. Спектр комбинационного рассеяния света показан на фиг. 2. Полосы наблюдали при 3270, 3205,3116, 3091, 3072, 3050, 3028, 2944, 2929, 2881, 1660, 1634, 1604, 1564, 1496, 1458, 1442, 1394, 1368, 1333,- 20018113 Указанное в заголовке соединение получали из 6-(2,2,2-трифторэтокси)пиридин-3-карбоновой кислоты (Apollo Scientific) и [(2-трифторметил-1H-индол-5-ил)метил]амина (промежуточный продукт 4) согласно способу, описываемому для соединения 1; m/z (ES+) 418 (M+1); 1 Н ЯМР (400 МГц, ДМСО-d6):12,21 (1H, с), 9,16 (1H, т), 8,74 (1H, с), 8,27 (1H, дд), 7,62 (1H, с), 7,44 (1H, д), 7,30 (1H, дд), 7,08 (1H, дд),7,00 (1H, с), 5,06 (2H, м), 4,57 (2H, д). Соединение 3. 6-Бром-N-[2-(трифторметил)-1H-индол-5-ил]метил-3-пиридинкарбоксамид(0,841 г, 4,39 ммоль), НОВТ (0,672 г, 4,39 ммоль) и DIPEA (2,8 мл, 16,03 ммоль) в DCM (50 мл) перемешивали при комнатной температуре в течение 18 ч. Смесь хорошо перемешивали с насыщенным водным раствором NaHCO3, органическую часть отделяли и водную часть дополнительно экстрагировали(EtOAc3). Объединенные органические слои сушили (картридж Phase-Sep) и упаривали при пониженном давлении, получая при этом белое твердое вещество. Растирание с диэтиловым эфиром на протяжении ночи и фильтрование давало неочищенное белое твердое вещество (1,16 г). Часть (88 мг) дополнительно очищали посредством MDAP, получая при этом указанное в заголовке соединение в виде белого твердого вещества (54 мг); m/z [M+H]+ 396/398 (M+1); 1 Н ЯМР (400 МГц, d4 MeOD):8,79 (1H, д), 8,10 Указанное в заголовке соединение получали методикой, аналогичной методике, описанной для соединения 3 с применением подходящей карбоновой кислоты и гидрохлорида [(2-трифторметил)-1 Ниндол-5-ил)метил]амина (промежуточный продукт 5); m/z [M+H]+ 345 (M+1); 1 Н ЯМР (400 МГц,d4MeOD):9,13 (1H, м), 8,39 (1H, дд), 7,99 (1H, дд), 7,68 (1H, с), 7,46 (1H, д), 7,34 (1H, д), 6,88 (1H, с),4,70 (2H, с). Соединение 5. N-[(2-Трифторметил-7-бром-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамид[(2-Трифторметил-7-бром-1H-индол-5-ил)метил]амин (промежуточный продукт 9, 230 мг, 0,785 ммоль) растворяли в DCM (10 мл) и добавляли 6-(трифторметил)никотиноилхлорид (ABCR; 181 мг,0,863 ммоль). Добавляли Et3N (0,219 мл, 1,570 ммоль) и реакционную смесь затем оставляли для перемешивания при комнатной температуре в течение 30 мин. Реакционную смесь гасили водой, затем органический слой собирали, сушили (MgSO4), фильтровали и упаривали досуха. Образовавшийся остаток очищали MDAP, получая при этом указанное в заголовке соединение (200 мг); m/z (ES+) 466468 (M+1); 1 Н ЯМР (400 МГц, CDCl3):9,08 (1H, д), 8,58 (1H, с), 8,33 (1H, дд), 7,82-7,76 (1H, м), 7,64 (1H, с), 7,52 В 5-мл пробирку микроволнового реактора N-[(2-трифторметил-7-бром-1H-индол-5-ил)метил]-6(трифторметил)-3-пиридинкарбоксамид (соединение 5, 50 мг, 0,107 ммоль), цианид цинка (37,8 мг, 0,322 ммоль) и Pd(Ph3P)4 (12,39 мг, 10,73 мкмоль) растворяли в ДМФА (2,5 мл) и дегазировали с применением аргона. Реакционную смесь затем нагревали в микроволновом реакторе при 150C в течение 30 мин. Реакционную смесь выливали в воду (20 мл) и экстрагировали этилацетатом (50 мл). Органический экстракт затем промывали смесью 1:1 воды и насыщенного раствора соли (20 мл 2), сушили (MgSO4),фильтровали и растворитель удаляли. Образовавшиеся остатки очищали MDAP и упаривали досуха, получая при этом указанное в заголовке соединение в виде белого твердого вещества (35 мг); m/z (ES+) 413[(1-Метил-2-трифторметилиндол-5-ил)метил]амин (промежуточный продукт 11, 150 мг, 0,657 ммоль) растворяли в DCM (10 мл) и добавляли 6-(трифторметил)никотиноилхлорид (ABCR; 165 мг,0,789 ммоль). Добавляли Et3N (0,183 мл, 1,315 ммоль) и реакционную смесь оставляли для перемешивания при комнатной температуре в течение 2 ч. Реакционную смесь гасили метанолом (10 мл) и упаривали досуха. Образовавшиеся остатки распределяли между этилацетатом и 1 М раствором лимонной кислоты. Органический слой собирали, сушили (MgSO4), фильтровали и растворитель удаляли. Образовавшиеся остатки затем очищали MDAP и упаривали досуха, получая при этом указанное в заголовке соединение (100 мг); m/z (ES+) 402 (M+1); 1H ЯМР (400 МГц, ДМСО-d6):9,50 (1H, т), 9,20 (1H, д), 8,51(1H, дд), 8,06 (1H, д), 7,67 (1H, с), 7,62 (1H, д), 7,39 (1H, дд), 7,10 (1H, с), 4,63 (2H, д), 3,85 (3H, с). Биологический анализ. РАМ-активность соединений изобретения в отношении 7 nAChR можно определять с применением следующего клеточного анализа потока ионов кальция, в котором применяют планшет-ридер для получения флуориметрического изображения (FLIPR) (см. Schroeder et al.; J. BiomolecuIar Screening, 1(2), p. 75-80, 1996). Клеточную линию GH4C1, стабильно трансфицированную 7 nAChR человека, суспендировали в 384-луночном планшете и инкубировали при 30C в течение 48 ч в атмосфере с 5% диоксида углерода. Среду для выращивания удаляли и клетки промывали три раза сбалансированным солевым раствором Хэнкса (HBSS), 20 мМ HEPES и 2,5 мМ пробенецидом, оставляя 20 мкл промывающего раствора в каждой лунке. Добавляли загрузочный раствор (20 мкл), содержащий HBSS, пробенецид, 1-4 мкМ Fluo4 AM(краситель-индикатор кальция) и плюроновую кислоту, и планшет инкубировали в течение 45 мин при 37C в атмосфере, не содержащей диоксид углерода. Клетки промывали три раза, оставляя 30 мкл в каждой лунке. Планшет, содержащий клетки, и краситель-индикатор кальция затем переносили в FLIPR. Анализ начинали сбором исходных данных с интервалами 10 с, с последующим добавлением испытуемого соединения в растворе буфера (0,33% ДМСО), и раствор разводили до конечной концентрации 10 мкМ, и серийное разведение содержимого лунок как 1:2 или 1:3 давало низкую концентрацию 1 нМ. Спустя дополнительно 5-10 мин добавляли 10 мкл 50 мкМ никотина и данные собирали в течение 2-3 мин. Никотин продуцировал образование быстрого, неустойчивого и репродуцируемого потока ионов кальция, который можно было потенцировать испытуемыми соединениями как позитивными аллостерическими модуляторами. Скрининг поддерживаемых изобретением соединений проводили с применением описанного выше анализа и получали величины pEC50, равные или больше чем 6,0, с максимальной потенциацией площади реакции приблизительно до 1200% относительно никотинового контроля. Скрининг поддерживаемого изобретением соединения 1 проводили с применением описанного выше анализа и получили величину pEC50 больше чем 6,0, с максимальной потенциацией площади реакции приблизительно до 1200% относительно никотинового контроля. Анализы in vivo, пригодные для оценки активности позитивных модуляторов никотинового рецептора 7, включают, но не ограничиваются перечисленным, анализы познавательной способности как на животных, не использовавшихся ранее в опытах по выработке навыка, так и фармакологически ослабленных животных, включая задержанную совместимость и несовместимость с положением, пассивное избегание, узнавание нового объекта, водный лабиринт Morris (или его варианты), лабиринт с радиальным рукавом, задачу выбора из пяти возможностей последовательных периодов времени реакции и выработку условно-рефлекторной контекстуальной реакции страха; анализы сенсорного гейтинга как у животных, не использовавшихся ранее в опытах по выработке навыка, так и фармакологически ослаблен- 22018113 ных животных, включая предварительное импульсное ингибирование рефлекса страха и звукового гейтинга, и анализы индуцированной лекарственным средством (например, амфетамином, морфином, фенциклидином) двигательной активности. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) или его соль где R1 представляет собой водород или C1-3 алкил;R2 представляет собой водород, галоген или циано и где Ra представляет собой галоген, C1-6 алкил, C1-6 алкокси, галогенС 1-6 алкил, галогенС 1-6 алкокси или циано. 2. Соединение по п.1 или его соль, где R1 представляет собой водород. 3. Соединение по любому предшествующему пункту или его соль, где R2 представляет собой водород. 4. Соединение, выбранное изN-[(1-метил-2-трифторметилиндол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамида или их солей. 5. Соединение по любому предшествующему пункту, где соль соединения является фармацевтически приемлемой солью. 6. N-[(2-Трифторметил-1H-индол-5-ил)метил]-6-(трифторметил)-3-пиридинкарбоксамид. 7. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли в качестве лекарственного средства. 8. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при лечении психотического расстройства. 9. Применение по п.8, где психотическим расстройством является шизофрения. 10. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при лечении когнитивного нарушения. 11. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения психотического расстройства. 12. Применение по п.11, где психотическим расстройством является шизофрения. 13. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения когнитивного нарушения. 14. Способ лечения психотического расстройства у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли. 15. Способ лечения шизофрении у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли. 16. Способ лечения когнитивного нарушения у человека, включающий введение эффективного количества соединения по любому из пп.1-6 или его фармацевтически приемлемой соли. 17. Фармацевтическая композиция, содержащая а) соединение по любому из пп.1-6 или его фармацевтически приемлемую соль и b) один или несколько фармацевтически приемлемых носителей или эксципиентов. Фиг. 1 Спектр комбинационного рассеяния соединения 1A
МПК / Метки
МПК: C07D 401/12, A61K 31/4439, A61P 25/18
Метки: модуляторов, рецептора, индолы, альфа-71, качестве, никотинового, подтипа, ацетилхолина
Код ссылки
<a href="https://eas.patents.su/25-18113-indoly-v-kachestve-modulyatorov-nikotinovogo-receptora-acetilholina-podtipa-alfa-71.html" rel="bookmark" title="База патентов Евразийского Союза">Индолы в качестве модуляторов никотинового рецептора ацетилхолина подтипа альфа-71</a>
Предыдущий патент: Вагинальная система доставки
Следующий патент: Устройство для генерации электроэнергии
Случайный патент: Набор элементов для сборки структур