Производные имидазола, как антагонисты глутаматного рецептора
Номер патента: 10577
Опубликовано: 30.10.2008
Авторы: Кольчевски Забине, Йэшке Георг, Фиайра Эрик, Чеккарелли Симона-Мария, Портер Ричард Хью Филлип, Бюттельманн Бернд
Формула / Реферат
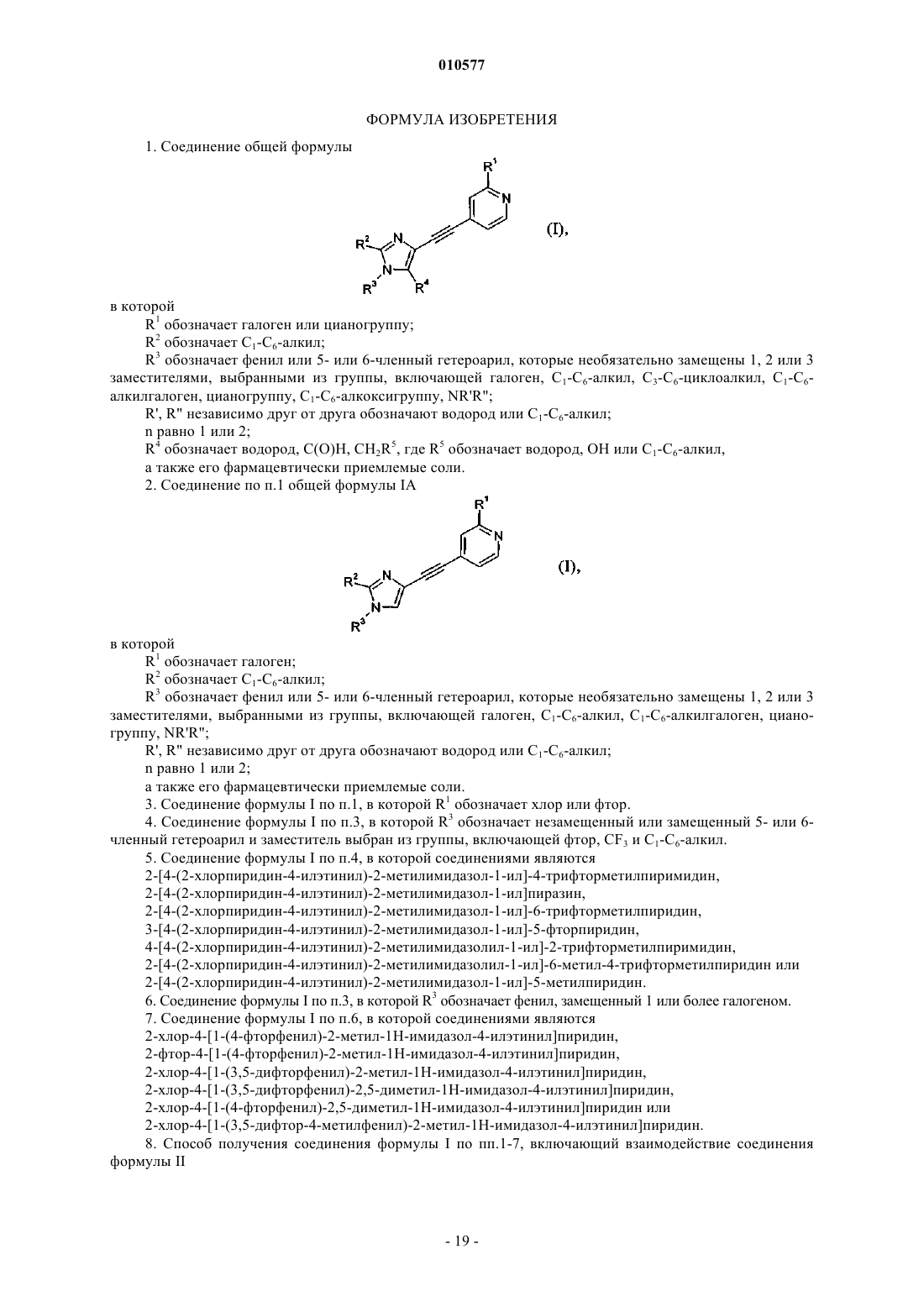
1. Соединение общей формулы
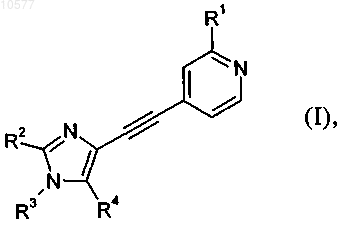
в которой
R1 обозначает галоген или цианогруппу;
R2 обозначает C1-C6-алкил;
R3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C3-C6-циклоалкил, C1-C6-алкилгалоген, цианогруппу, C1-C6-алкоксигруппу, NR'R";
R', R" независимо друг от друга обозначают водород или C1-C6-алкил;
n равно 1 или 2;
R4 обозначает водород, C(O)H, CH2R5, где R5 обозначает водород, ОН или С1-C6-алкил,
а также его фармацевтически приемлемые соли.
2. Соединение по п.1 общей формулы IA
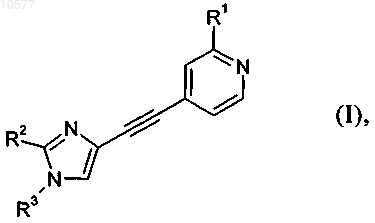
в которой
R1 обозначает галоген;
R2 обозначает C1-C6-алкил;
R3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C1-C6-алкилгалоген, цианогруппу, NR'R";
R', R" независимо друг от друга обозначают водород или C1-C6-алкил;
n равно 1 или 2;
а также его фармацевтически приемлемые соли.
3. Соединение формулы I по п.1, в которой R1 обозначает хлор или фтор.
4. Соединение формулы I по п.3, в которой R3 обозначает незамещенный или замещенный 5- или 6-членный гетероарил и заместитель выбран из группы, включающей фтор, CF3 и C1-C6-алкил.
5. Соединение формулы I по п.4, в которой соединениями являются
2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин,
2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиразин,
2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-трифторметилпиридин,
3-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиридин,
4-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-2-трифторметилпиримидин,
2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-6-метил-4-трифторметилпиридин или
2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-метилпиридин.
6. Соединение формулы I по п.3, в которой R3 обозначает фенил, замещенный 1 или более галогеном.
7. Соединение формулы I по п.6, в которой соединениями являются
2-хлор-4-[1-(4-фторфенил)-2-метил-1Н-имидазол-4-илэтинил]пиридин,
2-фтор-4-[1-(4-фторфенил)-2-метил-1Н-имидазол-4-илэтинил]пиридин,
2-хлор-4-[1-(3,5-дифторфенил)-2-метил-1Н-имидазол-4-илэтинил]пиридин,
2-хлор-4-[1-(3,5-дифторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]пиридин,
2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]пиридин или
2-хлор-4-[1-(3,5-дифтор-4-метилфенил)-2-метил-1Н-имидазол-4-илэтинил]пиридин.
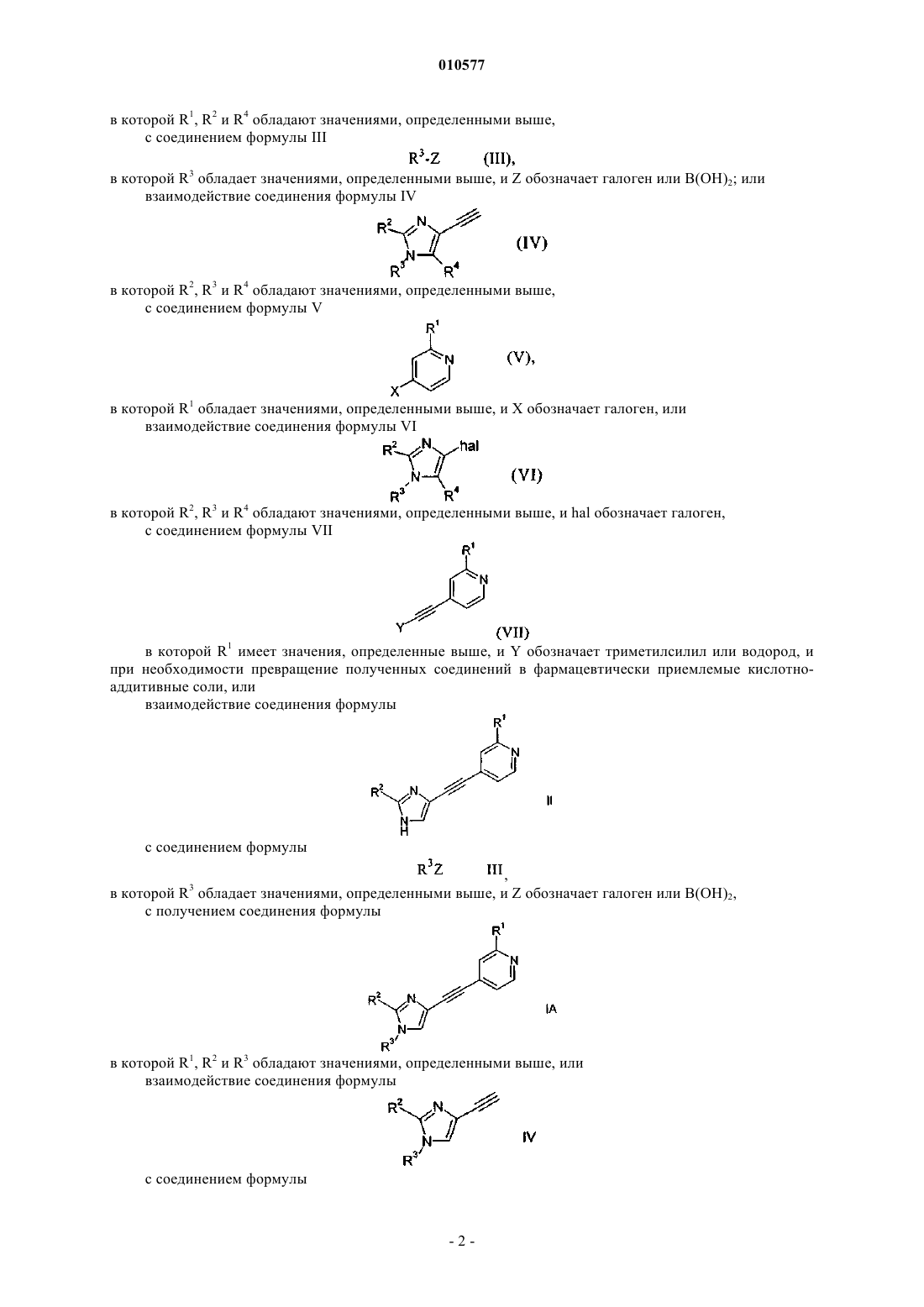
8. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы II
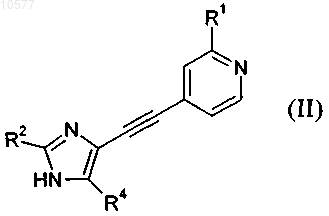
в которой R1, R2 и R4 обладают значениями, определенными в п.1,
с соединением формулы III
![]()
в которой R3 обладает значениями, определенными в п.1, и Z обозначает галоген или В(ОН)2.
9. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы IV
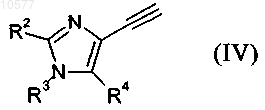
в которой R2, R3 и R4 обладают значениями, определенными в п.1,
с соединением формулы V
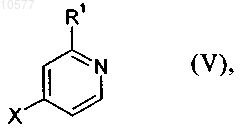
в которой R1 обладает значениями, определенными в п.1, и X обозначает галоген.
10. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы VI
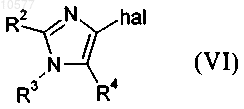
в которой R2, R3 и R4 обладают значениями, определенными в п.1, и hal обозначает галоген,
с соединением формулы VII
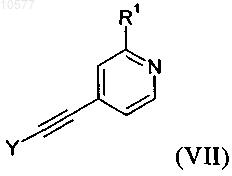
в которой R1 обладает значением, определенным в п.1, и Y обозначает триметилсилил или водород,
и, при необходимости, превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли.
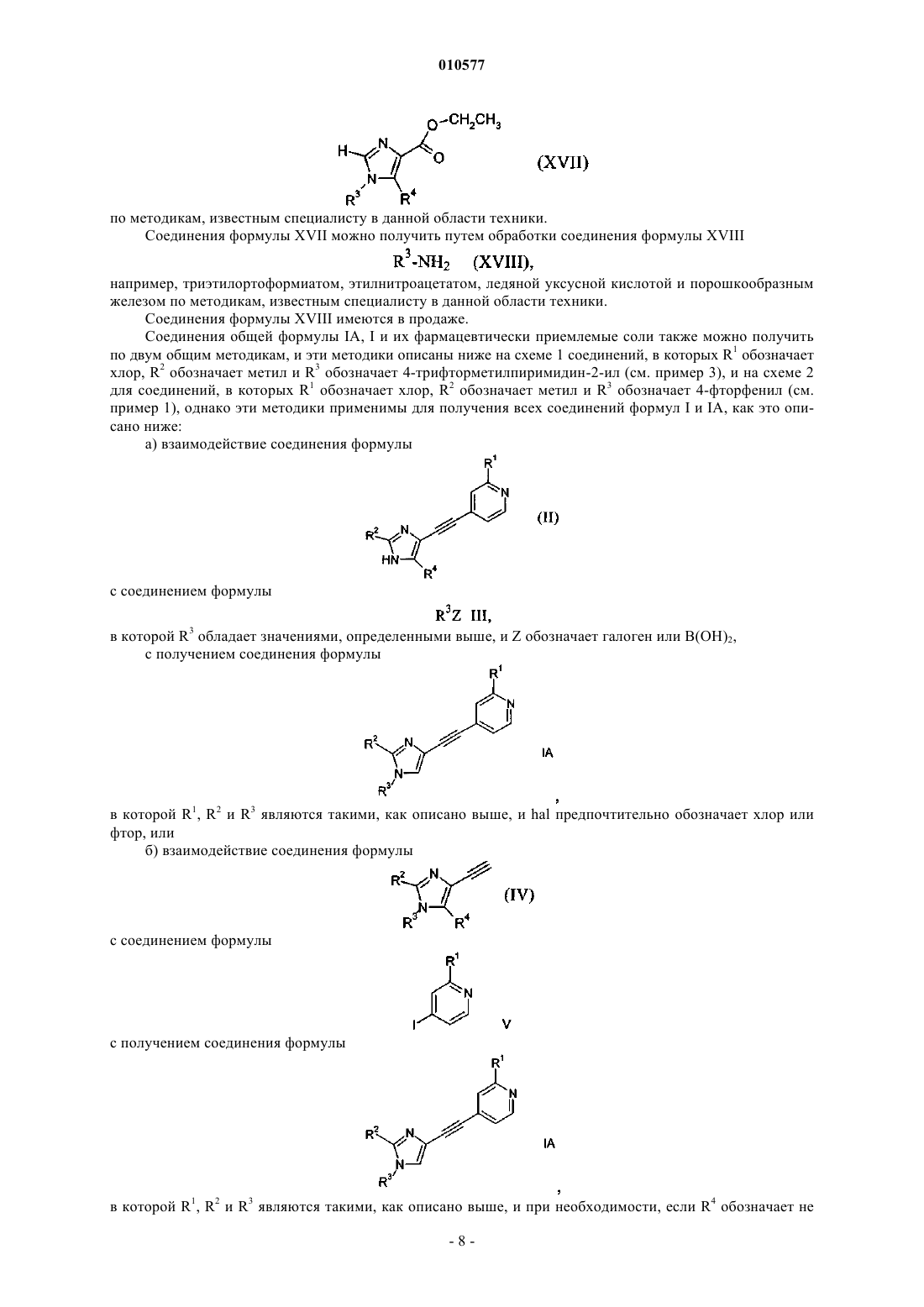
11. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы
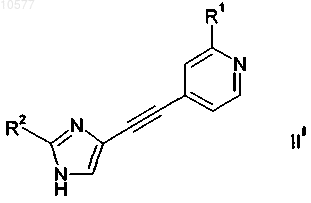
с соединением формулы
R3Z III
в которой R3 обладает значениями, определенными в п.1, и Z обозначает галоген или В(ОН)2,
с получением соединения формулы
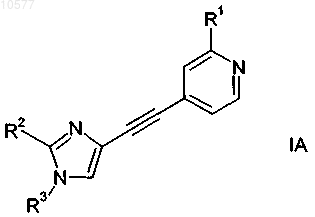
в которой R1, R2 и R3 обладают значениями, определенными в п.1.
12. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы
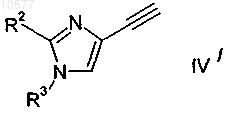
с соединением формулы
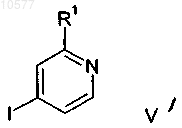
с получением соединения формулы
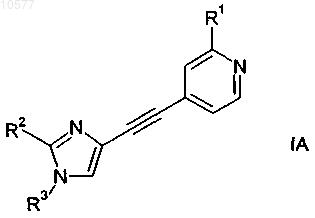
в которой R1, R2 и R3 обладают значениями, определенными в п.1,
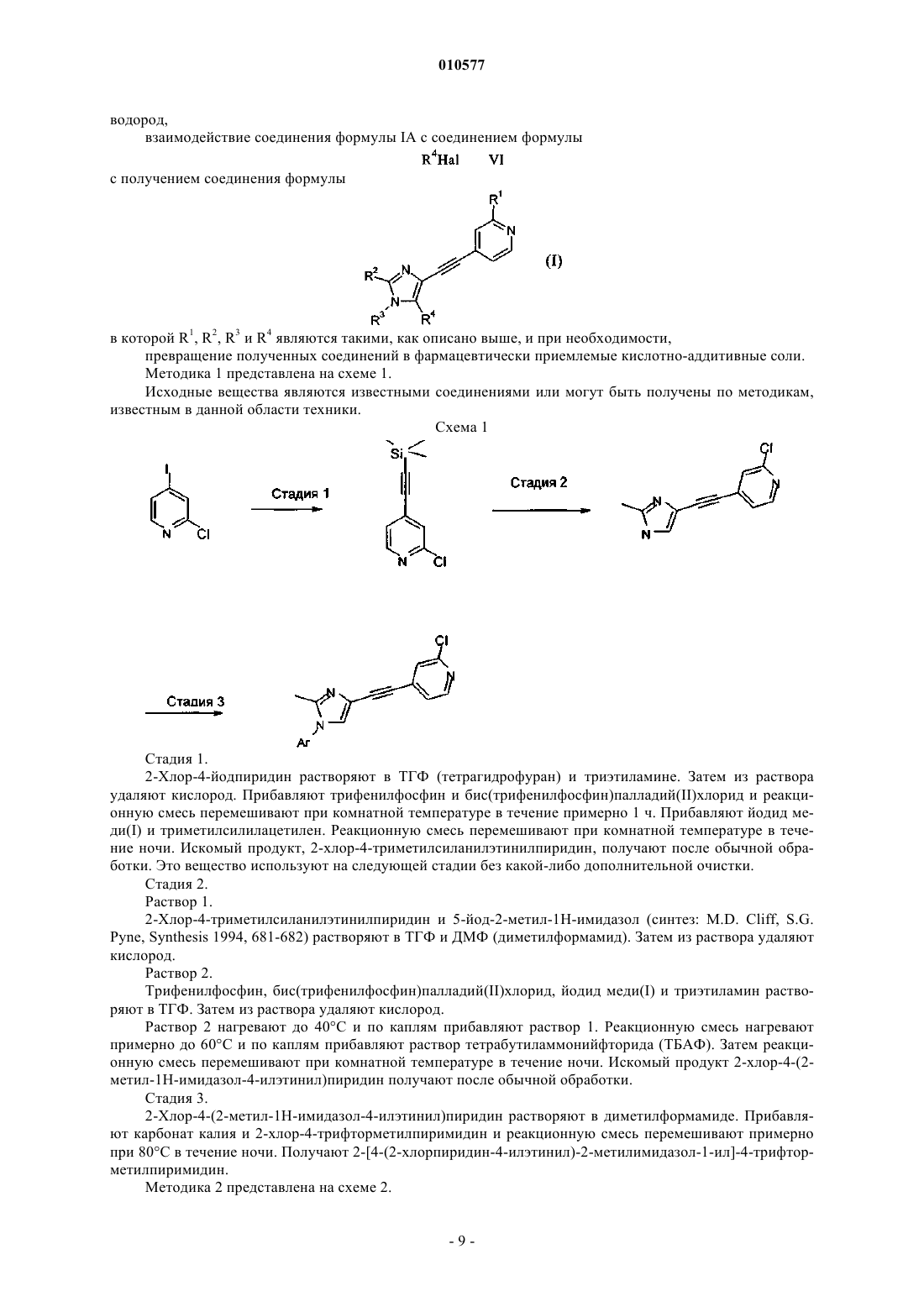
и при необходимости, если R4 обозначает не водород, взаимодействие соединения формулы IA с соединением формулы
R4Hal VI
с получением соединения формулы
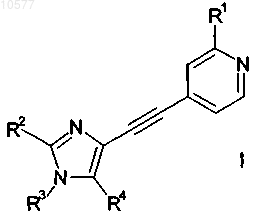
в которой R1, R2, R3 и R4 обладают значениями, определенными в п.1,
и при необходимости превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли.
13. Лекарственное средство, содержащее одно или большее количество соединений по любому из пп.1-7 и фармацевтически приемлемые инертные наполнители, предназначенное для лечения и предупреждения нарушений, опосредуемых рецептором mGluR5.
14. Лекарственное средство по п.13, предназначенное для лечения и предупреждения острых и/или хронических неврологических нарушений, в частности тревоги, или для лечения хронической и острой боли, или для лечения недержания мочи.
15. Применение соединения по любому из пп.1-7, а также его фармацевтически приемлемой соли для лечения или предупреждения заболеваний, опосредуемых рецептором mGluR5.
16. Применение соединения по любому из пп.1-7, а также его фармацевтически приемлемой соли для получения лекарственных средств, предназначенных для лечения или предупреждения нарушений, опосредуемых рецептором mGluR5.
17. Применение по п.16 для получения лекарственных средств, предназначенных для лечения и предупреждения острых и/или хронических неврологических нарушений, в частности тревоги, или для лечения хронической и острой боли, или для лечения недержания мочи.
Текст
010577 Сущность изобретения Настоящее изобретение относится к производным имидазола общей формулыR1 обозначает галоген или цианогруппу;R3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C3-C6-циклоалкил, C1-C6-алкилгалоген, цианогруппу, C1-C6-алкоксигруппу, NR'R";R', R" независимо друг от друга обозначают водород или C1-C6-алкил;R4 обозначает водород, C(O)H, CH2R5, где R5 обозначает водород, ОН или C1-C6-алкил,а также к их фармацевтически приемлемым солям. Предпочтительны соединения, которые имеют общую формулу IAR3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C1-C6-алкилгалоген, цианогруппу, NR'R";R', R" независимо друг от друга обозначают водород или C1-C6-алкил;n равно 1 или 2; и их фармацевтически приемлемые соли. Наиболее предпочтительными соединениями формулы I являются соединения, в которых R1 обозначает хлор или фтор, a R3 обозначает незамещенный или замещенный 5- или 6-членный гетероарил, в котором заместитель выбран из группы, включающей фтор, CF3 и C1-C6-алкил, особенно такие, как 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиразин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-трифторметилпиридин,3-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиридин,4-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-2-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-6-метил-4-трифторметилпиридин или 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-метилпиридин. Другими предпочтительными соединениями формулы I являются соединения, в которых R1 обозначает хлор или фтор, a R3 обозначает фенил, замещенный 1 или более галогеном, особенно такие, как 2-хлор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-фтор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин или 2-хлор-4-[1-(3,5-дифтор-4-метилфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Настоящее изобретение также относится к способам получения соединения формулы I, включающим взаимодействие соединения формулы II-1 010577 в которой R1, R2 и R4 обладают значениями, определенными выше,с соединением формулы III в которой R3 обладает значениями, определенными выше, и Z обозначает галоген или В(ОН)2; или взаимодействие соединения формулы IV в которой R1 обладает значениями, определенными выше, и X обозначает галоген, или взаимодействие соединения формулы VI в которой R1 имеет значения, определенные выше, и Y обозначает триметилсилил или водород, и при необходимости превращение полученных соединений в фармацевтически приемлемые кислотноаддитивные соли, или взаимодействие соединения формулы,в которой R3 обладает значениями, определенными выше, и Z обозначает галоген или В(ОН)2,с получением соединения формулы в которой R1, R2 и R3 обладают значениями, определенными выше, или взаимодействие соединения формулы в которой R1, R2, R3 и R4 обладают значениями, определенными выше, и, при необходимости, превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли. Настоящее изобретение относится к применению соединений формулы I или их фармацевтически приемлемых солей для лечения или предупреждения заболеваний, опосредуемых рецептором mGluR5,особенно для лечения и предупреждения острых и/или хронических неврологических нарушений, в частности тревоги, или для лечения хронической и острой боли, или для лечения недержания мочи, а также к лекарственным средствам, содержащим одно или большее количество соединений формулы I и фармацевтически приемлемые инертные наполнители, предназначенным для лечения и предупреждения нарушений, опосредуемых рецептором mGluR5. Раскрытие изобретения В перспективе соединения могут охватываться общей формулой IR1 обозначает галоген или цианогруппу;R3 обозначает арил или гетероарил, которые необязательно замещены с помощью 1, 2 или 3 заместителей, выбранных из группы, включающей галоген, низш. алкил, циклоалкил, низш. алкилгалоген,цианогруппу, низш. алкоксигруппу, NR'R", или с помощью 1-морфолинила, или с помощью 1-пирролидинила, необязательно замещенного с помощью (CH2)0,1OR, или с помощью пиперидинила, необязательно замещенного с помощью (CH2)0,1OR, или с помощью 1,1-диоксотиоморфолинила, или с помощью пиперазинила, необязательно замещенного с помощью низш. алкила или (СН 2)0,1-циклоалкила;R', R" независимо друг от друга обозначают водород, низш. алкил, (СН 2)0,1-циклоалкил илиR4 обозначает водород, C(O)H, CH2R5, где R5 обозначает водород, ОН, C1-C6-алкил, C3-С 12-циклоалкил,а также их фармацевтически приемлемые соли. В WO 02/46166, владельцем которой является заявитель, уже раскрыты замещенные производные имидазола как антагонисты mGluR5. Тем не менее, соединения, предлагаемые в настоящем изобретении,-3 010577 неожиданно обнаружили меньше побочных эффектов, чем соединения предшествующего уровня техники. Согласно изобретению неожиданно было установлено, что соединения общей формулы I являются антагонистами метаботропного глутаматного рецептора. Соединения формулы I отличаются тем, что они обладают ценными терапевтическими характеристиками. Их можно применять для лечения или предупреждения нарушений, опосредуемых рецептором mGluR5. В центральной нервной системе (ЦНС) передача стимула происходит путем взаимодействия нейротрансмиттера, который посылается нейроном, с нейрорецептором. Глутамат является главным возбуждающим нейротрансмиттером в головном мозге и играет особую роль в различных функциях центральной нервной системы (ЦНС). Глутаматзависимые рецепторы стимуляции подразделяются на две основные группы. Первая основная группа, а именно ионотропные рецепторы, образует контролируемые лигандом ионные каналы. Метаботропные глутаматные рецепторы(mGluR) относятся ко второй основной группе и, кроме того, относятся к семейству рецепторов, связывающих G-белок. В настоящее время известны 8 разных представителей этих mGluR, и некоторые из них даже обладают подтипами. В соответствии с их гомологией последовательностей, механизмами трансдукции сигналов и селективностью по отношению к агонистам эти 8 рецепторов можно подразделить на 3 подгруппы: mGluRl и mGluR5 относятся к группе I, mGluR2 и mGluR3 относятся к группе II и mGluR4, mGluR6,mGluR7 и mGluR8 относятся к группе III. Лиганды метаботропных глутаматных рецепторов, относящихся к первой группе, можно применять для лечения или предупреждения острых и/или хронических неврологических нарушений, таких как психоз, эпилепсия, шизофрения, болезнь Альцгеймера, расстройства познавательной способности и расстройства памяти, а также хроническая и острая боль. Другими патологическими состояниями, которые можно лечить, являются ограничение функции мозга, вызванное операциями шунтирования или трансплантатами, плохое кровоснабжение головного мозга, травмы спинного мозга, травмы головы, гипоксия, вызванная беременностью, остановка сердца и гипогликемия. Дополнительными патологическими состояниями, которые можно лечить, являются ишемия, хорея Гентингтона, боковой амиотрофический склероз (БАС), слабоумие, вызванное СПИД, поражения глаз, ретинопатия, идиопатический паркинсонизм или паркинсонизм, вызванный лекарственными средствами, а также патологические состояния, которые приводят к проявлениям дефицита глутамата,такие как, например, мышечные спазмы, судороги, мигрень, недержание мочи, злоупотребление никотином, злоупотребление опиатами, тревога, рвота, дискинезия и депрессии. Нарушениями, полностью или частично опосредуемыми посредством mGluR5, являются, например,острые, травматические и хронические дегенеративные процессы в нервной системе, такие как болезнь Альцгеймера, старческое слабоумие, болезнь Паркинсона, хорея Гентингтона, боковой амиотрофический склероз и рассеянный склероз, психические заболевания, такие как шизофрения и тревога, депрессия,боль и наркотическая зависимость (Expert Opin. Ther. Patents (2002), 12, (12. Селективные антагонисты mGluR5 особенно полезны для лечения тревоги и боли. Описаны соединения формулы I и их фармацевтически приемлемые соли, указанные выше соединения в качестве фармацевтически активных веществ и их получение. Описан способ получения соединений общей формулы I по общим методикам, указанным выше для соединений формулы I. Кроме того, описаны лекарственные средства, содержащие одно или большее количество соединений, предлагаемых здесь, и фармацевтически приемлемые инертные наполнители, предназначенные для лечения и предупреждения нарушений, опосредуемых рецептором mGluR5, таких как острые и/или хронические неврологические нарушения, в особенности тревога и хроническая или острая боль. Описано применение соединения, предлагаемого здесь, а также его фармацевтически приемлемой соли для изготовления лекарственного средства, предназначенного для лечения и предупреждения нарушений, опосредуемых рецептором mGluR5, указанных выше. Приведенные ниже определения общих терминов, использующихся в настоящем описании, применимы независимо от того, используются ли соответствующие термины поодиночке или в комбинации. Термин "низш. алкил", использующийся в настоящем описании, означает линейные или разветвленные насыщенные углеводородные остатки, содержащие от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода, такие как метил, этил, н-пропил, изопропил, н-бутил, трет-бутил и т.п. Термин "низш. алкоксил" означает низш. алкильный остаток, соответствующий приведенному выше определению, присоединенный через атом кислорода. Примеры "низш. алкоксильных" остатков включают метоксильный, этоксильный, изопропоксильный и т.п. Термин "галоген" означает фтор, хлор, бром и йод."Арил" означает ароматическую карбоциклическую группу, состоящую из 1 отдельного кольца или одного или большего количества конденсированных колец, в которой не менее чем 1 кольцо по своей природе является ароматическим. Предпочтительной арильной группой является фенил. Термин "гетероарил" означает ароматическое 5- или 6-членное кольцо, содержащее 1 или большее количество гетероатомов, выбранных из группы, включающей азот, кислород и фосфор. Предпочтитель-4 010577 ными являются гетероарильные группы, выбранные из числа азотсодержащих. Примерами таких гетероарильных групп являются пиридинил, пиразинил, пиримидинил и пиридазинил. Термин "циклоалкил" означает насыщенную карбоциклическую группу, содержащую 3-12 атомов углерода, предпочтительно 3-6 атомов углерода. Термин "фармацевтически приемлемая соль" относится к любой соли, полученной из неорганической или органической кислоты или основания. Формула I также включает соединения общей формулы IAR3 обозначает арил или гетероарил, которые необязательно замещены с помощью 1, 2 или 3 заместителей, выбранных из группы, включающей галоген, низш. алкил, низш. алкилгалоген, цианогруппу,NR'R", или с помощью 1-морфолинила, или с помощью 1-пирролидинила, необязательно замещенного с помощью (CH2)0,1OR, или с помощью пиперидинила, необязательно замещенного с помощью (CH2)0,1OR,или с помощью 1,1-диоксотиоморфолинила, или с помощью пиперазинила, необязательно замещенного с помощью низш. алкила или (СН 2)0,1-циклоалкила;R', R" независимо друг от друга обозначают водород, низш. алкил, (CH2)0,1-циклоалкил илиn равно 1 или 2; а также их фармацевтически приемлемые соли. Предпочтительными соединениями формул I и IA являются такие, в которых R1 обозначает хлор или фтор. Особенно предпочтительными являются такие соединения этой группы, в которых R3 обозначает незамещенный или замещенный гетероарил, в котором заместитель выбран из группы, включающей фтор, CF3 и низш. алкил, например следующие соединения: 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиразин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-трифторметилпиридин,3-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиридин,4-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-2-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-6-метил-4-трифторметилпиридин или 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-метилпиридин. Особенно предпочтительными также являются такие соединения этой группы, в которых R3 обозначает арил, замещенный 1 или большим количеством галогенов, например следующие соединения: 2-хлор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-фтор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин, или 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин. Соединения формулы I или IA можно получить способом, который включает взаимодействие:-5 010577 в которой R3 обладает значениями, определенными выше, и Z обозначает галоген или В(ОН)2; или в которой R1 обладает значениями, определенными выше, и Y обозначает триметилсилил или водород. Реакцию, описанную в разделе (а), можно проводить по стандартным методикам, например путем арилирования соединения формулы II с помощью ароматической бороновой кислоты и медного катализатора в растворителе, таком как дихлорметан или тетрагидрофуран (см., например, Colmann et al., Org.Lett. 2: 1233 (2000 или путем нагревания соединения формулы II и соединения формулы III, в которой Z обозначает галоген, с основанием, таким как карбонат калия или карбонат цезия, в растворителе, таком как диметилформамид, или при катализе с помощью Pd в условиях, описанных Бухвальдом (см., например,пример 8; Buchwald et al., Tetrahedron Lett. 40: 2657 (1999. Реакцию, описанную в разделе (б), можно проводить путем сочетания по Соногашира соединения формулы IV и соединения формулы V в присутствии, например, CuI, (Ph3P)2PdCl2, Et3N в растворителе, таком как тетрагидрофуран или диметилформамид(Sonogashira et al., Synthesis 777 (1977. В одном варианте выполнения X в соединении формулы V обозначает бром или йод. Реакцию, описанную выше в разделе (в), можно проводить, например, в присутствии CuI, (Ph3P)2PdCl2, Et3N, n-Bu4F в растворителе, таком как тетрагидрофуран или диметилформамид. Соли получают по стандартным методикам, известным специалисту в данной области техники. Соединения формул II, IV, VI и VII являются новыми и также являются вариантом выполнения настоящего изобретения. Соединения формул III и V имеются в продаже, или их получение известно специалисту в данной области техники. Соединения формулы II можно получить взаимодействием соединения формулы VIII(Synthesis 681-682 (1994. Соединения формулы IV можно получить взаимодействием соединения формулы IX в которой R2, R3 и R4 обладают значениями, определенными выше,-6 010577 с диметил(1-диазо-2-оксопропил)фосфонатом, как это описано в работе Ohira (Synth.Comm. 19: 561564 (1989. Соединения формулы VI можно получить взаимодействием соединения формулы VIII, приведенной выше, с соединением формулы X в которой R3 обладает значениями, определенными выше, и Z обозначает галоген или В(ОН)2. Реакцию можно проводить путем арилирования соединения формулы VIII с помощью ароматической бороновой кислоты (соединения формулы X) и медного катализатора в растворителе, таком как дихлорметан или тетрагидрофуран, в атмосфере кислорода (см., например, Colmann et al., Org. Lett. 2: 1233(2000 или путем нагревания с R3-Z, где Z обозначает галоген, с основанием, таким как карбонат калия или карбонат цезия, в растворителе, таком как диметилформамид, или при катализе с помощью Pd в условиях, описанных Бухвальдом (см., например, пример 8; Buchwald et al., Tetrahedron Lett. 40: 2657 (1999. Соединения формулы VII можно получить взаимодействием соединения формулы V, приведенной выше, с соединением формулы XI. Реакцию можно проводить путем сочетания по Соногашира в присутствии, например, CuI,(Ph3P)2PdCl2, Et3N в растворителе, таком как тетрагидрофуран или диметилформамид (Sonogashira et al.,Synthesis 777 (1977. Соединения формулы IX можно получить окислением соединения формулы XII по методикам, известным специалисту в данной области техники. Соединения формулы XII можно получить удалением защитной группы из соединения формулы XIII по методикам, известным специалисту в данной области техники. Соединения формулы XIII можно получить путем алкилирования соединения формулы XIV алкилирующим реагентом формулы XVa по методикам, известным специалисту в данной области техники. Исходные соединения формулы XVa имеются в продаже. Соединения формулы XIV можно получить путем обработки соединения формулы XV трет-бутилдиметилсилилхлоридом по методикам, известным специалисту в данной области техники. Соединения формулы XV можно получить путем обработки соединения формулы XVI восстановительным реагентом по методикам, известным специалисту в данной области техники. Соединения формулы XVI можно получить гидролизом соединения формулы XVII по методикам, известным специалисту в данной области техники. Соединения формулы XVII можно получить путем обработки соединения формулы XVIII например, триэтилортоформиатом, этилнитроацетатом, ледяной уксусной кислотой и порошкообразным железом по методикам, известным специалисту в данной области техники. Соединения формулы XVIII имеются в продаже. Соединения общей формулы IA, I и их фармацевтически приемлемые соли также можно получить по двум общим методикам, и эти методики описаны ниже на схеме 1 соединений, в которых R1 обозначает хлор, R2 обозначает метил и R3 обозначает 4-трифторметилпиримидин-2-ил (см. пример 3), и на схеме 2 для соединений, в которых R1 обозначает хлор, R2 обозначает метил и R3 обозначает 4-фторфенил (см. пример 1), однако эти методики применимы для получения всех соединений формул I и IA, как это описано ниже: а) взаимодействие соединения формулы с соединением формулы в которой R3 обладает значениями, определенными выше, и Z обозначает галоген или В(ОН)2,с получением соединения формулы в которой R1, R2 и R3 являются такими, как описано выше, и hal предпочтительно обозначает хлор или фтор, или б) взаимодействие соединения формулы в которой R1, R2, R3 и R4 являются такими, как описано выше, и при необходимости,превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли. Методика 1 представлена на схеме 1. Исходные вещества являются известными соединениями или могут быть получены по методикам,известным в данной области техники. Схема 1 Стадия 1. 2-Хлор-4-йодпиридин растворяют в ТГФ (тетрагидрофуран) и триэтиламине. Затем из раствора удаляют кислород. Прибавляют трифенилфосфин и бис(трифенилфосфин)палладий(II)хлорид и реакционную смесь перемешивают при комнатной температуре в течение примерно 1 ч. Прибавляют йодид меди(I) и триметилсилилацетилен. Реакционную смесь перемешивают при комнатной температуре в течение ночи. Искомый продукт, 2-хлор-4-триметилсиланилэтинилпиридин, получают после обычной обработки. Это вещество используют на следующей стадии без какой-либо дополнительной очистки. Стадия 2. Раствор 1. 2-Хлор-4-триметилсиланилэтинилпиридин и 5-йод-2-метил-1 Н-имидазол (синтез: M.D. Cliff, S.G.Pyne, Synthesis 1994, 681-682) растворяют в ТГФ и ДМФ (диметилформамид). Затем из раствора удаляют кислород. Раствор 2. Трифенилфосфин, бис(трифенилфосфин)палладий(II)хлорид, йодид меди(I) и триэтиламин растворяют в ТГФ. Затем из раствора удаляют кислород. Раствор 2 нагревают до 40 С и по каплям прибавляют раствор 1. Реакционную смесь нагревают примерно до 60 С и по каплям прибавляют раствор тетрабутиламмонийфторида (ТБАФ). Затем реакционную смесь перемешивают при комнатной температуре в течение ночи. Искомый продукт 2-хлор-4-(2 метил-1 Н-имидазол-4-илэтинил)пиридин получают после обычной обработки. Стадия 3. 2-Хлор-4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин растворяют в диметилформамиде. Прибавляют карбонат калия и 2-хлор-4-трифторметилпиримидин и реакционную смесь перемешивают примерно при 80 С в течение ночи. Получают 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин. Методика 2 представлена на схеме 2. Стадия 1. 4-Фторанилин при комнатной температуре перемешивают с триэтилортоформиатом, этилнитроацетатом и ледяной уксусной кислотой. Реакционную смесь кипятят с обратным холодильником в течение примерно 2 ч при механическом перемешивании. Прибавляют дополнительное количество этилнитроацетата и ледяной уксусной кислоты. Тремя порциями в течение 8 ч при кипячении реакционной смеси с обратным холодильником прибавляют порошкообразное железо. Прибавляют этилацетат и продолжают кипячение с обратным холодильником. Неочищенный продукт, этиловый эфир 1-(4-фторфенил)-1 Н-имидазол-4-карбоновой кислоты, используют на следующей стадии без какой-либо дополнительной очистки. Стадия 2. Неочищенный этиловый эфир 1-(4-фторфенил)-1 Н-имидазол-4-карбоновой кислоты растворяют в диоксане и растворе гидроксида натрия. Реакционную смесь кипятят с обратным холодильником в течение примерно 2 ч. Прибавляют древесный уголь и продолжают кипячение с обратным холодильником. Получают искомое соединение, 1-(4-фторфенил)-1 Н-имидазол-4-карбоновую кислоту. Стадия 3. 1-(4-Фторфенил)-1 Н-имидазол-4-карбоновую кислоту растворяют в ТГФ. По каплям прибавляют комплекс борана с тетрагидрофураном в ТГФ. Реакционную смесь кипятят с обратным холодильником в течение 2 ч и перемешивают при комнатной температуре в течение ночи. Затем реакционную смесь охлаждают до 0 С и по каплям прибавляют метанол. Растворители выпаривают и остаток растворяют в HCl и кипятят с обратным холодильником в течение 2 ч. Затем реакционную смесь охлаждают до 0 С и по каплям прибавляют раствор гидроксида натрия. Получают искомое соединение, [1-(4-фторфенил)-1 Нимидазол-4-ил]метанол. Стадия 4.[1-(4-Фторфенил)-1 Н-имидазол-4-ил]метанол растворяют в ДМФ. Прибавляют имидазол и трет-бутилдиметилхлорсилан (тБДМХС). Реакционную смесь перемешивают примерно при 45 С в течение ночи. Получают искомое соединение, 4-(трет-бутилдиметилсиланоксиметил)-1-(4-фторфенил)-1 Н-имидазол. Стадия 5. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-1 Н-имидазол растворяют в ТГФ и охлаждают до -78 С. По каплям прибавляют н-бутиллитий в гексане. Реакционную смесь нагревают до -25 С,выдерживают при -25 С в течение 10 мин и затем повторно охлаждают до -78 С. По каплям прибавляют йодметан. Реакционную смесь медленно нагревают до комнатной температуры и перемешивают при- 10010577 комнатной температуре в течение ночи. Получают искомое соединение, 4-(трет-бутилдиметилсиланоксиметил)-1-(4-фторфенил)-2-метил-1 Н-имидазол. Стадия 6. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-2-метил-1 Н-имидазол растворяют в ТГФ. Прибавляют тетрабутиламмонийфторид в ТГФ и реакционную смесь перемешивают при комнатной температуре в течение ночи. Получают искомое соединение, [1-(4-фторфенил)-2-метил-1 Н-имидазол-4-ил]метанол. Стадия 7.[1-(4-Фторфенил)-2-метил-1 Н-имидазол-4-ил]метанол растворяют в метиленхлориде. Прибавляют оксид марганца(IV) и реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Суспензию фильтруют через слой дикалита "speed plus" и получают искомое соединение, (4-фторфенил)2-метил-1 Н-имидазол-4-карбальдегид. Стадия 8. Диметиловый эфир (1-диазо-2-оксопропил)фосфоновой кислоты растворяют в метаноле. Прибавляют карбонат калия. При комнатной температуре по каплям прибавляют раствор 1-(4-фторфенил)-2-метил-1 Н-имидазол-4-карбальдегида в метаноле. Реакционную смесь перемешивают при комнатной температуре в течение ночи. Получают искомое соединение, 4-этинил-1-(4-фторфенил)-2-метил-1 Н-имидазол. Стадия 9. 2-Хлор-4-йодпиридин растворяют в ТГФ. Эту смесь откачивают и для удаления кислорода из раствора несколько раз повторно заполняют аргоном. Прибавляют трифенилфосфин и бис(трифенилфосфин)палладий(II)хлорид и реакционную смесь перемешивают при комнатной температуре в течение 1 ч. Прибавляют йодид меди(I) и 4-этинил-1-(4-фторфенил)-2-метил-1 Н-имидазол. Реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Получают искомый продукт, 2-хлор-4-[1-(4 фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Фармацевтически приемлемые соли соединений формулы I можно легко получить по методикам,которые сами по себе известны, и с учетом природы соединения, превращаемого в соль. Для образования фармацевтически приемлемых солей соединений формулы I, являющихся основаниями, пригодны неорганические или органические кислоты, такие как, например, хлористо-водородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота или лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винно-каменная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п. Для образования фармацевтически приемлемых солей соединений, являющихся кислотами, пригодны соединения, которые содержат щелочные металлы или щелочно-земельные металлы, например натрий, калий, кальций, магний и т.п., основные амины или основные аминокислоты. Соединения формулы I и их фармацевтически приемлемые соли, как уже отмечено выше, являются антагонистами метаботропного глутаматного рецептора и могут применяться для лечения или предупреждения нарушений, опосредуемых рецептором mGluR5, таких как острые и/или хронические неврологические нарушения, расстройства познавательной способности и расстройства памяти, а также острая и хроническая боль. Неврологическими нарушениями, которые можно лечить, являются, например, эпилепсия, шизофрения, тревога, острые, травматические и хронические дегенеративные процессы в нервной системе, такие как болезнь Альцгеймера, старческое слабоумие, хорея Гентингтона, БАС, рассеянный склероз, слабоумие, вызванное СПИД, поражения глаз, ретинопатия, идиопатический паркинсонизм или паркинсонизм, вызванный лекарственными средствами, а также патологические состояния, которые приводят к проявлениям дефицита глутамата, такие как, например, мышечные спазмы, судороги, мигрень, недержание мочи, злоупотребление этанолом, злоупотребление никотином, психозы, злоупотребление опиатами, тревога, рвота, дискинезия и депрессия. Другими патологическими состояниями, которые можно лечить, являются ограничение функции мозга, вызванное операциями шунтирования или трансплантатами, плохое кровоснабжение головного мозга, травмы спинного мозга, травмы головы, гипоксия, вызванная беременностью, остановка сердца и гипогликемия. Соединения формулы I и их фармацевтически приемлемые соли особенно полезны для применения в качестве анальгетиков. Типы боли, которые можно лечить, включают воспалительную боль, такую как артрит и ревматоидный артрит, васкулит, нейропатическую боль, такую как тригеминальная или герпетическая невралгия, диабетическая нейропатическая боль, каузалгия, гипералгезия, тяжелая хроническая боль, послеоперационная боль и боль, сопутствующая различными патологическими состояниями, таким как рак, стенокардия, почечная или желчная колика, менструация, мигрень и подагра. Фармакологическую активность соединений исследовали по следующей методике. Для проведения экспериментов по связыванию кДНК, кодирующую человеческий рецептор mGlu5a,временно трансфицировали в клетки EBNA по методике, которую описали Schlaeger and Christensen(Cytotechnology 15: 1-13 (1998. Гомогенаты клеточных мембран хранили при -80 С до дня проведения анализа, после чего их оттаивали и повторно суспендировали и политронизировали в связывающем буфере, содержащем 15 мМ Tris-HCl (Tris=трис(гидроксиметиламино)метан), 120 мМ NaCl, 100 мМ KCl,25 мМ CaCl2, 25 мМ MgCl2, при рН 7,4 до конечной концентрации, равной 20 мкг белка/лунка. Изотермы насыщения получали путем прибавления к этим мембранам [3 Н]МФЭП [2-метил-6- 11010577(фенилэтинил)пиридин] при 12 концентрациях (0,04-100 нМ) (при полном объеме, равном 200 мкл) в течение 1 ч при 4 С. Эксперименты по конкуренции проводили при постоянной концентрации[3 Н]МФЭП (2 нМ) и значения IC50 для исследуемых соединений определяли по 11 концентрациям (0,310000 нМ). Инкубацию проводили в течение 1 ч при 4 С. В конце инкубации мембраны фильтровали на "unifilter" (96-луночный белый микропланшет с фильтром, связанным с GF/C, предварительно инкубированный в течение 1 ч в содержащем 0,1% ПЭИ(полиэтиленимин) промывочном буфере, Packard BioScience, Meriden, CT) с использованием устройства для сбора клеток Filtermate 96 (Packard BioScience) и 3 раза промывали холодным буфером 50 мМ TrisHCl, рН 7,4. Неспецифическое связывание измеряли в присутствии 10 мкМ МФЭП. Радиоактивность фильтра определяли подсчетом (3 мин) с помощью сцинтилляционного счетчика для микропланшетовPackard Top-count с коррекцией на тушение после прибавления 45 мкл microscint 40 (Canberra PackardS.A., Zurich, Switzerland) и встряхивания в течение 20 мин. Для функциональных анализов измерения [Са 2+]i проводили в соответствии с описанием, которое ранее привели Porter et al. (Br. J. Pharmacol. 128: 13-20 (1999 на рекомбинантных человеческих рецепторах mGlu5a в клетках HEK-293. В эти клетки вводили краситель Fluo 4-AM (можно приобрести у фирмыFLUKA, конечная концентрация равна 0,2 мкМ). Измерения [Са 2+]i проводили с помощью флуориметрического визуализирующего считывателя планшетов (FLIPR, Molecular Devices Corporation, La Jolla, СА,USA). Оценку антагонистического воздействия проводили после предварительной 5-минутной инкубации с исследуемыми соединениями с последующим прибавлением субмаксимального количества агониста. Кривые ингибирования (антагонистического воздействия) аппроксимировали с помощью 4-параметрического логистического уравнения, что при использовании программного обеспечения (Xcel fit) для итеративной нелинейной аппроксимации кривой давало значения IC50 и коэффициента Хилла. Для экспериментов по связыванию приведены значения Ki для исследованных соединений. Значение Ki определяют по следующей формуле: в которой значения IC50 означают концентрации исследуемых соединений, которые приводят к 50% ингибированию конкурирующего радиолиганда ([3 Н]МФЭП). L означает концентрацию радиолиганда, использованную в эксперименте по связыванию, и значение Kd для радиолиганда определяется эмпирически для каждой партии приготовленных мембран. Соединения, предлагаемые в настоящем изобретении, являются антагонистами рецептора mGluR5a. Активности соединений формулы I, измеренные с помощью описанного выше анализа, находятся в диапазоне Ki70 нМ. Соединения формулы I и их фармацевтически приемлемые соли можно применять в качестве лекарственных средств, например в виде фармацевтических препаратов. Фармацевтические препараты можно вводить перорально, например в виде таблеток, таблеток с покрытием, драже, капсул из мягкого и твердого желатина, растворов, эмульсий или суспензий. Кроме того, введение также можно выполнить ректально, например в виде суппозиториев, или парентерально, например в виде растворов для инъекций. Для получения фармацевтических препаратов соединения формулы I и их фармацевтически приемлемые соли можно обработать с использованием фармацевтически инертных неорганических или органических носителей. В качестве таких носителей для таблеток, таблеток с покрытием, драже и капсул из твердого желатина можно использовать, например, лактозу, кукурузный крахмал и его производные,тальк, стеариновую кислоту и ее соли и т.п. Для капсул из мягкого желатина подходящими носителями являются, например, растительные масла, воска, жиры, полужидкие и жидкие полиолы; однако, в зависимости от природы активного вещества, в случае капсул из мягкого желатина носители обычно не требуются. Носителями, подходящими для приготовления растворов и сиропов, являются, например, вода,полиолы, сахароза, инвертный сахар, глюкоза и т.п. Для водных растворов растворимых в воде солей соединений формулы I, предназначенных для инъекций, можно использовать вспомогательные вещества,такие как спирты, полиолы, глицерин, растительные масла и т.п., но, как правило, они не требуются. Но- 12010577 сителями, подходящими для суппозиториев, являются, например, натуральные или отвержденные масла,воска, жиры, полужидкие или жидкие полиолы. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, вкусовые агенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать другие терапевтически полезные вещества. Как отмечено выше, объектом настоящего изобретения также являются лекарственные средства,содержащие соединение формулы I или их фармацевтически приемлемые соли и терапевтически инертный наполнитель, а также способ получения таких лекарственных средств, который состоит во включении одного или большего количества соединений формулы I или их фармацевтически приемлемых солей и,при необходимости, одного или большего количества других терапевтически полезных веществ в галенову дозировочную форму совместно с одним или большим количеством терапевтически инертных носителей. Дозировка может меняться в широких пределах и, разумеется, в каждом конкретном случае будет подбираться в соответствии с индивидуальными потребностями. Обычно в случае перорального или парентерального введения эффективная дозировка составляет 0,01-20 мг/кг/сутки, и для всех описанных показаний предпочтительной является дозировка, составляющая 0,1-10 мг/кг/сутки. Для взрослого человека, обладающего массой, равной 70 кг, соответствующая суточная доза составляет 0,7-1400 мг/сутки,предпочтительно от 7 до 700 мг/сутки. Представленные ниже примеры предназначены для дополнительного разъяснения настоящего изобретения. Пример 1. 2-Хлор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. 2-Хлор-4-йодпиридин (1,39 г, 5,8 ммоль) растворяли в 50 мл сухого ТГФ. Эту смесь откачивали и для удаления кислорода из раствора несколько раз повторно заполняли аргоном. Прибавляли трифенилфосфин (39 мг, 0,15 ммоль) и бис(трифенилфосфин)палладий(II)хлорид (170 мг, 0,24 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Прибавляли йодид меди(I) (28 мг,0,15 ммоль) и 4-этинил-1-(4-фторфенил)-2-метил-1 Н-имидазол (970 мг, 4,84 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 дней. Растворитель выпаривали. Остаток растворяли в 100 мл воды и трижды экстрагировали этилацетатом (порциями по 100 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат/триэтиламин, градиентный режим 1:0:010:10:1) и перекристаллизовывали из гептана и этилацетата. Искомый продукт получали в виде белого твердого вещества (545 мг, 36%), МС: m/е=312,1 (М+Н+). Пример 2. 2-Фтор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=296,1 (М+Н+), получали по общей методике примера 1 из 4-этинил 1-(4-фторфенил)-2-метил-1 Н-имидазола и 2-фтор-4-йодпиридина. Пример 3. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин. 2-Хлор-4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин (150 мг, 0,69 ммоль) растворяли в 5 мл диметилформамида. Прибавляли карбонат калия (190 мг, 1,37 ммоль) и 2-хлор-4-трифторметилпиримидин(189 мг, 0,66 ммоль) и реакционную смесь перемешивали при 80 С в течение ночи. Реакционную смесь выливали в 70 мл воды и трижды экстрагировали этилацетатом (порциями по 100 мл). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и выпаривали. Неочищенный продукт перекристаллизовывали из диэтилового эфира и искомое соединение получали в виде белого твердого вещества (190 мг, 76%), МС: m/е=364,1 (М+Н+). Пример 4. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиразин. Искомое соединение, МС: m/e=296,1 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-хлорпиразина. Пример 5. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-трифторметилпиридин. Искомое соединение, МС: m/e=363,11 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-фтор-6-(трифторметил)пиридина. Пример 6. 3-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиридин. Искомое соединение, МС: m/e=313,1 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3,5-дифторпиридина. Пример 7. 2-Хлор-4-[1-(4-хлорфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. 2-Хлор-4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин (150 мг, 0,69 ммоль) растворяли в 30 мл дихлорметана. Прибавляли порошкообразные молекулярные сита (3 , 200 мг), 4-хлорбензолбороновую кислоту (216 мг, 1,38 ммоль) и [Cu(OH)TMEDA]2Cl2 (113 мг, 0,24 ммоль). Через реакционную смесь в течение 5 мин пропускали кислород и перемешивание продолжали при комнатной температуре в течение ночи. Реакционную смесь фильтровали через слой дикалита "speed plus" и промывали с помощью 50 мл дихлорметана. Фильтрат промывали с помощью 50 мл воды, сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (гептан/ этилацетат, градиентный режим 100:03:2) и с помощью перекристаллизации из диизопропилового эфира. Искомое соединение получали в виде белого твердого вещества (42 мг, 19%), МС: m/e=329,2 (М+Н+).- 13010577 Пример 8. 2-Хлор-4-[1-(3,4-дихлорфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=363,7 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3,4-дихлорбензолбороновой кислоты. Пример 9. 2-Хлор-4-[1-(4-фторфенил)-2-изопропил-1 Н-имидазол-4-илэтинил]пиридинфумарат. Стадия 1. 1-(4-Фторфенил)-4-йод-2-изопропил-1 Н-имидазол. Искомое соединение, МС: m/e=331,1 (М+Н+), получали по общей методике примера 7 из 5-йод-2 изопропил-1 Н-имидазола и 4-фторбензолбороновой кислоты. Стадия 2. 2-Хлор-4-[1-(4-фторфенил)-2-изопропил-1 Н-имидазол-4-илэтинил]пиридинфумарат. Искомое соединение, МС: m/e=340,1 (М+Н+), получали по общей методике примера В, стадия 2, из 2-хлор-4-триметилсиланилэтинилпиридина и 1-(4-фторфенил)-4-йод-2-изопропил-1H-имидазола и кристаллизовали из метанола и 1,05 экв. фумаровой кислоты. Пример 10. 4-[1-(4-Фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин-2-карбонитрил. Искомое соединение, МС: m/e=303,1 (М+Н+), получали по общей методике примера 7 из 4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин-2-карбонитрила и 4-фторбензолбороновой кислоты. 4-(2-Метил-1 Н-имидазол-4-илэтинил)пиридин-2-карбонитрил. Трифенилфосфин (126 мг, 0,48 ммоль), бис(трифенилфосфин)палладий(II)хлорид (1,01 г, 1,44 ммоль) и триэтиламин (3,65 г, 101,2 ммоль) растворяли в 40 мл сухого ТГФ. Эту смесь откачивали и для удаления кислорода из раствора несколько раз повторно заполняли аргоном. Прибавляли 4-йод-2-метил-1 Нимидазол (Tetrahedron Letters 30 (11), 1409 (1989 (5,0 г, 20,8 ммоль), 4-триметилсиланилэтинилпиридин 2-карбонитрил (4,43 г, 22,1 ммоль) и йодид меди(I) (46 мг, 0,24 ммоль) и смесь нагревали до 60 С. По каплям в течение 30 мин прибавляли 1 М раствор тетрабутиламмонийфторида (24 мл, 24,0 ммоль). После завершения прибавления реакционную смесь перемешивали при 60 С в течение еще 1 ч. Растворитель выпаривали. Остаток растворяли в 200 мл воды и трижды экстрагировали с помощью 200 мл этилацетата. Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (метанол/метиленхлорид 5:95). Искомый продукт получали в виде светло-желтого твердого вещества (1,06 г, 21%), МС: m/e=208,9 (М+). 4-Триметилсиланилэтинилпиридин-2-карбонитрил. 4-Бром-2-пиридинкарбонитрил (Cesko-Slovenska Farmacie 25 (5), 181 (1976 (0,73 г, 4,0 ммоль) растворяли в 18 мл сухого ТГФ. Эту смесь откачивали и для удаления кислорода из раствора несколько раз повторно заполняли аргоном. Прибавляли трифенилфосфин (31 мг, 0,12 ммоль) и бис(трифенилфосфин)палладий(II)хлорид (141 мг, 0,20 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Прибавляли йодид меди(I) (23 мг, 0,12 ммоль) и триметилсилилацетилен (590 мг, 6,0 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 дней. Растворитель выпаривали. Остаток растворяли в 100 мл воды и трижды экстрагировали с помощью 100 мл этилацетата. Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (гептан/метиленхлорид 1:2). Искомый продукт получали в виде желтого масла (329 мг, 41%), МС: m/e=201,3 (М+Н+). Пример 11. 2-Хлор-4-[1-(2,4-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=330,4 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2,4-дифторбензолбороновой кислоты. Пример 12. 2-Хлор-4-[1-(3,4-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=330,4 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3,4-дифторбензолбороновой кислоты. Пример 13. 4-[1-(3,4-Дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин-2-карбонитрил. Искомое соединение, МС: m/e=321,5 (М+Н+), получали по общей методике примера 7 из 4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин-2-карбонитрила и 3,4-фторбензолбороновой кислоты. Пример 14. 2-Хлор-4-[1-(3-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=312,5 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3-фторбензолбороновой кислоты. Пример 15. 2-Хлор-4-[1-(3,5-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=330,3 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3,5-дифторбензолбороновой кислоты. Пример 16. 4-[1-(3,5-Дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин-2-карбонитрил. Искомое соединение, МС: m/e=321,4 (М+Н+), получали по общей методике примера 7 из 4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин-2-карбонитрила и 3,5-фторбензолбороновой кислоты. Пример 17. 2-Хлор-4-[1-(3-фтор-4-метилфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=326,4 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3-фтор-4-метилбензолбороновой кислоты. Пример 18. 2-Хлор-4-[1-(4-фтор-3-метилфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=326,4 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 4-фтор-3-метилбензолбороновой кислоты.- 14010577 Пример 19. 2-Хлор-4-[1-(3-хлор-4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=347,2 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3-хлор-4-фторбензолбороновой кислоты. Пример 20. 2-Хлор-4-[1-(4-метилфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=308,8 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 4-метилбензолбороновой кислоты. Пример 21. 2-Хлор-4-[1-(3-метоксифенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=324,8 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3-метоксибензолбороновой кислоты. Пример 22. 2-Хлор-4-[1-(4-метоксифенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=324,8 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 4-метоксибензолбороновой кислоты. Пример 23. 3-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]бензонитрил. Искомое соединение, МС: m/e=319,8 (М+Н+), получали по общей методике примера 7 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 3-цианбензолбороновой кислоты. Пример 24. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиримидин. Искомое соединение, МС: m/e=296,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-хлорпиримидина. Пример 25. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-метилпиримидин. Искомое соединение, МС: m/e=310,4 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-хлор-4-метилпиримидина. Пример 26. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-метоксипиримидин. Искомое соединение, МС: m/e=326,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-хлор-4-метоксипиримидина. Пример 27. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиримидин. Искомое соединение, МС: m/e=314,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-хлор-5-фторпиримидина. Пример 28. 4-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-2-трифторметилпиримидин. Искомое соединение, МС: m/e=364,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 4-хлор-2-трифторметилпиримидина. Пример 29. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-метилпиридин. Искомое соединение, МС: m/e=309,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-фтор-6-метилпиридина. Пример 30. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-метилпиридин. Искомое соединение, МС: m/e=309,5 (М+Н+), получали по общей методике примера 3 из 2-хлор-4(2-метил-1 Н-имидазол-4-илэтинил)пиридина и 2-фтор-5-метилпиридина. Пример 31. 4-[1-(6-Хлорпиридин-3-ил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин-2-карбонитрил. Искомое соединение, МС: m/e=320,0, 322,1 (М+Н+), получали по общей методике примера 7 из 4-(2 метил-1 Н-имидазол-4-илэтинил)пиридин-2-карбонитрила и 6-хлор-3-пиридинилбороновой кислоты. Пример 32. 2-Хлор-4-[1-(6-хлорпиридин-3-ил)-2-изопропил-1 Н-имидазол-4-илэтинил]пиридин. Стадия 1. 2-Хлор-5-(4-йод-2-изопропилимидазол-1-ил)пиридин. Искомое соединение, МС: m/e=348,4 (М+Н+), получали по общей методике примера 7 из 5-йод-2 изопропил-1 Н-имидазола и 4-хлорпиридин-5-бороновой кислоты. Стадия 2. 2-Хлор-4-[1-(6-хлорпиридин-3-ил)-2-изопропил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=358,1 (М+Н+), получали по общей методике примера В, стадия 2, из 2-хлор-4-триметилсиланилэтинилпиридина и 2-хлор-5-(4-йод-2-изопропилимидазол-1-ил)пиридина. Пример 33. 5-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-2-циклопропилпиридин. Стадия 1. 2-Хлор-5-(4-йод-2-метилимидазол-1-ил)пиридин. Искомое соединение, МС: m/e=320,2 (М+Н+), получали по общей методике примера 7 из 4-йод-2 метил-1 Н-имидазола и 4-хлорпиридин-5-бороновой кислоты. Стадия 2. 2-Хлор-5-(2-метил-4-триметилсиланилэтинилимидазол-1-ил)пиридин. Искомое соединение, МС: m/e=290,6 (М+Н+), получали по общей методике примера В, стадия 1, из 2-хлор-5-(4-йод-2-метилимидазол-1-ил)пиридина и триметилсилилацетилена. Стадия 3. 2-Циклопропил-5-(2-метил-4-триметилсиланилэтинилимидазол-1-ил)пиридин. 2-Хлор-5-(2-метил-4-триметилсиланилэтинилимидазол-1-ил)пиридин (425 мг, 1,47 ммоль) растворяли в 0,4 М циклопропилцинкхлориде в ТГФ (7,33 мл, 0,4 М в ТГФ) и прибавляли тетракис(трифенилфосфин)палладий (34 мг, 0,03 ммоль). Реакционную смесь кипятили с обратным холодильником в течение 16 ч и выливали в 50 мл насыщенного раствора бикарбоната натрия. Смесь трижды экстрагировали этилацетатом (порциями по 50 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (гептан/этилацетат, градиентный режим 100:01:1) и искомый продукт получали в виде светло-желтого твердого вещества (395 мг, 91%), МС: m/e=296,2 (М+Н+).- 15010577 Стадия 4. 2-Хлор-4-[1-(6-циклопропилпиридин-3-ил)-2-изопропил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=335,6 (М+Н+), получали по общей методике примера В, стадия 2, из 2-циклопропил-5-(2-метил-4-триметилсиланилэтинилимидазол-1-ил)пиридина и 2-хлор-4-йодпиридина. Пример 34. 2-Хлор-4-[1-(3,5-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. 2-Хлор-4-[1-(3,5-дифторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин (200 мг, 0,607 ммоль) растворяли в 10 мл ТГФ и охлаждали до -75 С. Прибавляли диизопропиламид лития (0,45 мл, 0,91 ммоль) и смесь перемешивали в течение 15 мин при -75 С. Прибавляли йодметан (0,05 мл, 0,85 ммоль) и перемешивание продолжали при -75 С в течение 2 ч. Реакцию останавливали насыщенным раствором NaHCO3 и экстрагировали водой и этилацетатом. Объединенные органические экстракты сушили над сульфатом натрия,фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (гептан/этилацетат, градиентный режим 90:1020:80) и с помощью перекристаллизации из этилацетата. Искомое соединение получали в виде белого твердого вещества (40 мг, 19%), МС: m/e=344,5 (М+Н+). Пример 35. 2-Хлор-4-[1-(4-фторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин. Искомое соединение, МС: m/e=326,5 (М+Н+), получали по общей методике примера 34 из 2-хлор-4[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридина. Пример 36. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-метил-4-трифторметилпиридин. Стадия 1. 2-(4-Йод-2-метилимидазол-1-ил)-6-метил-4-трифторметилпиридин. Искомое соединение, МС: m/e=368,0 (М+Н+), получали по общей методике примера 3 из 5-йод-2 метил-1 Н-имидазола и 2-хлор-6-метил-4-(трифторметил)пиридина. Стадия 2. 2-[4-(2-Хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-метил-4-трифторметилпиридин. Искомое соединение, МС: m/e=377,2 (М+Н+), получали по общей методике примера В, стадия 2, из 2-хлор-4-триметилсиланилэтинилпиридина и 2-(4-йод-2-метилимидазол-1-ил)-6-метил-4-трифторметилпиридина. Синтез промежуточных продуктов Пример А. 4-Этинил-1-(4-фторфенил)-2-метил-1 Н-имидазол. Стадия 1. Этиловый эфир 1-(4-фторфенил)-1 Н-имидазол-4-карбоновой кислоты. 4-Фторанилин (20,0 г, 175 ммоль) при комнатной температуре перемешивали с триэтилортоформиатом (35,4 г, 233 ммоль), этилнитроацетатом (28,5 г, 210 ммоль) и 4 мл ледяной уксусной кислоты. Реакционную смесь кипятили с обратным холодильником в течение 2 ч при механическом перемешивании. Прибавляли дополнительное количество триэтилортоформиата (200 мл) и ледяной уксусной кислоты (200 мл). Тремя порциями в течение 8 ч при кипячении реакционной смеси с обратным холодильником прибавляли порошкообразное железо (100 г, 1,79 моль). Прибавляли этилацетат (700 мл) и кипячение с обратным холодильником продолжали в течение еще 2 ч. Реакционную смесь фильтровали через слой дикалита "speed plus" и промывали с помощью 500 мл этилацетата. Растворители выпаривали и неочищенный продукт использовали на следующей стадии без какой-либо дополнительной очистки. Стадия 2. 1-(4-Фторфенил)-1 Н-имидазол-4-карбоновая кислота. Неочищенный этиловый эфир 1-(4-фторфенил)-1H-имидазол-4-карбоновой кислоты (175 ммоль) растворяли в 450 мл диоксана и 450 мл 2 н. раствора гидроксида натрия. Реакционную смесь кипятили с обратным холодильником в течение 2 ч. Прибавляли древесный уголь (1 г, Norit SA II) и кипячение с обратным холодильником продолжали в течение еще 20 мин. Смесь фильтровали горячей и промывали с помощью 50 мл 2 н. раствором гидроксида натрия. Фильтрат обрабатывали с помощью 550 мл 2 н. HCl и перемешивали при комнатной температуре в течение ночи. Твердое вещество отфильтровывали и сушили при 50 С и 15 мбар. Искомое соединение получали в виде почти белого твердого вещества (28 г,78%), МС: m/e=205,1 (М-Н). Стадия 3. [1-(4-Фторфенил)-1H-имидазол-4-ил]метанол. 1-(4-Фторфенил)-1 Н-имидазол-4-карбоновую кислоту (18 г, 87 ммоль) растворяли в 90 мл сухого ТГФ. По каплям прибавляли комплекс борана с тетрагидрофураном (174 мл, 1 М в ТГФ, 174 ммоль). Реакционную смесь кипятили с обратным холодильником в течение 2 ч и перемешивали при комнатной температуре в течение ночи. Реакционную смесь охлаждали до 0 С и по каплям прибавляли 100 мл метанола. Растворители выпаривали. Остаток растворяли в 100 мл 2 н. HCl и кипятили с обратным холодильником в течение 2 ч. Затем реакционную смесь охлаждали до 0 С и по каплям прибавляли 120 мл 2 н. раствора гидроксида натрия. Твердое вещество отфильтровывали и сушили при 50 С и 15 мбар. Искомое соединение получали в виде белого твердого вещества (13 г, 78%), МС: m/e=193,2 (М+Н)+. Стадия 4. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-1 Н-имидазол.- 16010577 перемешивали при 45 С в течение ночи и выливали в 500 мл воды. Водную фазу трижды экстрагировали этилацетатом (порциями по 200 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью хроматографии на колонке с силикагелем (метиленхлорид/метанол 98:2) и искомое соединение получали в виде светло-коричневого масла (20 г, 96%), МС: m/e=291,2 (М-СН 3), m/e=249,1 (М-трет-бутил). Стадия 5. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-2-метил-1 Н-имидазол. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-1 Н-имидазол (18,2 г, 59,2 ммоль) растворяли в 600 мл сухого ТГФ и охлаждали до -78 С. По каплям прибавляли н-бутиллитий (55,5 мл, 1,6 М в гексане, 88,8 ммоль). Реакционную смесь нагревали до -25 С, выдерживают при -25 С в течение 10 мин и затем повторно охлаждали до -78 С. По каплям прибавляли йодметан (7,4 мл, 11,8 ммоль). Реакционную смесь медленно нагревали до комнатной температуры и перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали. Остаток растворяли в 300 мл воды и трижды экстрагировали этилацетатом (порциями по 200 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью хроматографии на колонке с силикагелем (циклогексан/этилацетат, градиентный режим 50:5020:80) и искомое соединение получали в виде оранжевого масла (14,7 г, 77%), МС: m/e=321,1 (М+Н+). Стадия 6. [1-(4-Фторфенил)-2-метил-1 Н-имидазол-4-ил]метанол. 4-(трет-Бутилдиметилсиланоксиметил)-1-(4-фторфенил)-2-метил-1 Н-имидазол (14,7 г, 45,7 ммоль) растворяли в 200 мл ТГФ. Прибавляли тетрабутиламмонийфторид (91 мл, 1M в ТГФ, 91 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали. Остаток растворяли в 200 мл воды и трижды экстрагировали этилацетатом (порциями по 200 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт суспендировали в 150 мл этилацетата, отфильтровывали и сушили. Искомое соединение получали в виде белого твердого вещества (7,16 г, 76%), МС: m/e=207,1 (М+Н+). Стадия 7. 1-(4-Фторфенил)-2-метил-1 Н-имидазол-4-карбальдегид [1-(4-фторфенил)-2-метил-1 Н-имидазол-4-ил]метанол (7,16 г, 34,7 ммоль) растворяли в 2,3 л метиленхлорида. Прибавляли оксид марганца(IV) (26,8 г, 278 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 3 дней. Суспензию фильтровали через слой дикалита "speed plus" и промывали с помощью 1 л метиленхлорида. Растворители выпаривали и искомое соединение получали в виде белого твердого вещества(5,87 г, 83%), МС: m/e=205,1 (М+Н+). Стадия 8. 4-Этинил-1-(4-фторфенил)-2-метил-1 Н-имидазол. Диметиловый эфир (1-диазо-2-оксопропил)фосфоновой кислоты (6,51 г, 33,9 ммоль) растворяли в 100 мл метанола. Прибавляли карбонат калия (7,81 г, 56,5 ммоль). При комнатной температуре по каплям прибавляли раствор 1-(4-фторфенил)-2-метил-1 Н-имидазол-4-карбальдегида (5,77 г, 45 ммоль) в 100 ммоль метанола. Реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали. Остаток растворяли в 150 мл воды и трижды экстрагировали этилацетатом (порциями по 150 мл). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и выпаривали. Неочищенный продукт очищали с помощью флэш-хроматографии на силикагеле (гептан/этилацетат, градиентный режим 100:00:100) и искомое соединение получали в виде белого твердого вещества Стадия 1. 2-Хлор-4-триметилсиланилэтинилпиридин. 2-Хлор-4-йодпиридин (10,0 г, 41,8 ммоль) растворяли в 200 мл сухого ТГФ и 17,5 мл триэтиламина. Эту смесь откачивали и для удаления кислорода из раствора несколько раз повторно заполняли аргоном. Прибавляли трифенилфосфин (329 мг, 1,25 ммоль) и бис(трифенилфосфин)палладий(II)хлорид (1,47 г,2,09 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Прибавляли йодид меди(I) (239 мг, 1,25 ммоль) и триметилсилилацетилен (6,28 г, 6,39 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали. Остаток растворяли в 500 мл воды и трижды экстрагировали этилацетатом (порциями по 500 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью хроматографии на силикагеле (циклогексан/этилацетат 80:20). Искомый продукт получали в виде светло-коричневого полужидкого вещества (10 г, 100%). Это вещество использовали на следующей стадии без какой-либо дополнительной очистки. Стадия 2. 2-Хлор-4-(2-метил-1 Н-имидазол-4-илэтинил)пиридин. Раствор 1. 2-Хлор-4-триметилсиланилэтинилпиридин (8,9 г, чистота 100%, как это отмечено для стадии 1) и 5-йод-2-метил-1 Н-имидазол (13,24 г, 64 ммоль, синтез: M.D. Cliff, S.G. Pyne, Synthesis 1994, 681-682) растворяли в 75 мл сухого ТГФ и 20 мл сухого ДМФ. Эту смесь откачивали и для удаления кислорода из- 17010577 раствора несколько раз повторно заполняли аргоном. Раствор 2. Трифенилфосфин (223 мг, 0,85 ммоль), бис(трифенилфосфин)палладий(II)хлорид (1,79 г, 2,55 ммоль),йодид меди(I) (81 мг, 0,43 ммоль) и триэтиламин (8,87 мл, 64 ммоль) растворяли в 75 мл сухого ТГФ. Эту смесь также откачивали и для удаления кислорода из раствора несколько раз повторно заполняли аргоном. Раствор 2 нагревали до 40 С и по каплям прибавляли раствор 1. Реакционную смесь нагревали до 60 С и в течение 45 мин по каплям прибавляли раствор тетрабутиламмонийфторида (1M в ТГФ, 55 мл,55 ммоль). Затем реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали. Остаток растворяли в 200 мл воды и трижды экстрагировали этилацетатом (порциями по 200 мл). Объединенные органические экстракты сушили над сульфатом магния, фильтровали и выпаривали. Неочищенный продукт очищали с помощью хроматографии на силикагеле (метиленхлорид/метанол 95:5) и перекристаллизовывали из смеси метиленхлорида с этилацетатом. Искомый продукт получали в виде светло-коричневого твердого вещества (2,89 г, 31%). Пример С. 4-Хлор-2-трифторметилпиримидин. Это соединение получали по методике, описанной в работе S. Inoue, A.J. Saggiomo, E.A. Nodiff, J.Org. Chem. 1961, 26, 4504. Получение фармацевтических композиций Пример I. Таблетки указанного ниже состава получали обычным образом: Пример II. Таблетки указанного ниже состава получали обычным образом: Пример III. Получали капсулы следующего состава: Активный ингредиент, обладающий частицами подходящего размера, кристаллическую лактозу и микрокристаллическую целлюлозу равномерно смешивали друг с другом, просеивали и затем при перемешивании прибавляли стеарат магния и тальк. Готовую смесь помещали в капсулы соответствующего размера из твердого желатинаR1 обозначает галоген или цианогруппу;R3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C3-C6-циклоалкил, C1-C6 алкилгалоген, цианогруппу, C1-C6-алкоксигруппу, NR'R";R', R" независимо друг от друга обозначают водород или C1-C6-алкил;R4 обозначает водород, C(O)H, CH2R5, где R5 обозначает водород, ОН или С 1-C6-алкил,а также его фармацевтически приемлемые соли. 2. Соединение по п.1 общей формулы IAR3 обозначает фенил или 5- или 6-членный гетероарил, которые необязательно замещены 1, 2 или 3 заместителями, выбранными из группы, включающей галоген, C1-C6-алкил, C1-C6-алкилгалоген, цианогруппу, NR'R";R', R" независимо друг от друга обозначают водород или C1-C6-алкил;n равно 1 или 2; а также его фармацевтически приемлемые соли. 3. Соединение формулы I по п.1, в которой R1 обозначает хлор или фтор. 4. Соединение формулы I по п.3, в которой R3 обозначает незамещенный или замещенный 5- или 6 членный гетероарил и заместитель выбран из группы, включающей фтор, CF3 и C1-C6-алкил. 5. Соединение формулы I по п.4, в которой соединениями являются 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-4-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]пиразин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-6-трифторметилпиридин,3-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-фторпиридин,4-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-2-трифторметилпиримидин,2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазолил-1-ил]-6-метил-4-трифторметилпиридин или 2-[4-(2-хлорпиридин-4-илэтинил)-2-метилимидазол-1-ил]-5-метилпиридин. 6. Соединение формулы I по п.3, в которой R3 обозначает фенил, замещенный 1 или более галогеном. 7. Соединение формулы I по п.6, в которой соединениями являются 2-хлор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-фтор-4-[1-(4-фторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(3,5-дифторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин,2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1 Н-имидазол-4-илэтинил]пиридин или 2-хлор-4-[1-(3,5-дифтор-4-метилфенил)-2-метил-1 Н-имидазол-4-илэтинил]пиридин. 8. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы II в которой R1, R2 и R4 обладают значениями, определенными в п.1,с соединением формулы III в которой R3 обладает значениями, определенными в п.1, и Z обозначает галоген или В(ОН)2. 9. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы IV в которой R1 обладает значениями, определенными в п.1, и X обозначает галоген. 10. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы VI в которой R1 обладает значением, определенным в п.1, и Y обозначает триметилсилил или водород,и, при необходимости, превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли. 11. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулыR3Z в которой R обладает значениями, определенными в п.1, и Z обозначает галоген или В(ОН)2,с получением соединения формулы 3- 20010577 в которой R1, R2 и R3 обладают значениями, определенными в п.1. 12. Способ получения соединения формулы I по пп.1-7, включающий взаимодействие соединения формулы в которой R1, R2 и R3 обладают значениями, определенными в п.1,и при необходимости, если R4 обозначает не водород, взаимодействие соединения формулы IA с соединением формулы в которой R1, R2, R3 и R4 обладают значениями, определенными в п.1,и при необходимости превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли. 13. Лекарственное средство, содержащее одно или большее количество соединений по любому из пп.1-7 и фармацевтически приемлемые инертные наполнители, предназначенное для лечения и предупреждения нарушений, опосредуемых рецептором mGluR5. 14. Лекарственное средство по п.13, предназначенное для лечения и предупреждения острых и/или хронических неврологических нарушений, в частности тревоги, или для лечения хронической и острой боли, или для лечения недержания мочи. 15. Применение соединения по любому из пп.1-7, а также его фармацевтически приемлемой соли для лечения или предупреждения заболеваний, опосредуемых рецептором mGluR5. 16. Применение соединения по любому из пп.1-7, а также его фармацевтически приемлемой соли для получения лекарственных средств, предназначенных для лечения или предупреждения нарушений,опосредуемых рецептором mGluR5. 17. Применение по п.16 для получения лекарственных средств, предназначенных для лечения и предупреждения острых и/или хронических неврологических нарушений, в частности тревоги, или для лечения хронической и острой боли, или для лечения недержания мочи.
МПК / Метки
МПК: C07D 401/14, A61K 31/444, C07D 401/06, A61K 31/4439, A61P 25/28
Метки: глутаматного, имидазола, рецептора, производные, антагонисты
Код ссылки
<a href="https://eas.patents.su/22-10577-proizvodnye-imidazola-kak-antagonisty-glutamatnogo-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Производные имидазола, как антагонисты глутаматного рецептора</a>
Предыдущий патент: Способ очистки плазмидной днк
Следующий патент: Антивирусное средство на основе гемолимфы насекомых подкласса pterigota
Случайный патент: Способ изготовления электротехнической проволоки из алюминиевого сплава