Замещенные хиназолиновые соединения
Номер патента: 19110
Опубликовано: 30.01.2014
Авторы: Оклер Эрик, Лериш Каролине, Ле-Ру Жак, Миддлмисс Дейвид Н.
Формула / Реферат
1. Соединение, имеющее структуру (I), или его фармацевтически приемлемая соль
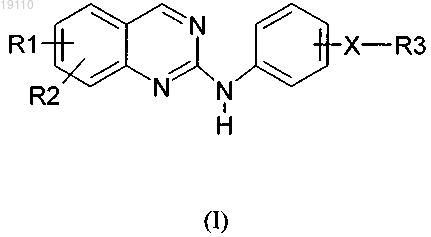
где R1 представляет собой фенил, необязательно замещенный фрагментами R9 и R10, и
R2 представляет собой водород или метил,
R3 представляет собой водород, С1-С4алкил, циклоалкил, гетероциклоалкил, арил, гетероарил,
-CN, -CF3, -OR4, -OCOR4, -COR4, -NR4R5, -NR4COR5, -NR4COOR5, -(С1-С4алкил)OR4, -(C1-C4алкил)COR4, -(С1-С4алкил)NR4R5, -(С1-C4алкил)NR4COR5, -(C1-C4алкил)NR4COOR5,
X представляет собой связь, или (CH2)aW(CH2)b, (CH2)aW(CH2)bY(CH2)c или -[(CH2)aW(CH2)b]m-(Z)e-[(CH2)cY(CH2)d]n,
где a, b, с и d представляют собой независимо 0, 1, 2 или 3,
е представляет собой 0, 1 или 2 и
n и m представляют собой независимо 0 или 1,
W представляет собой -СО-, -О-, -SO2-, -CH2-, -СНОН-, -NR6-, NR7CONR8 или NR7SO2NR8,
Y представляет собой -СО-, -О-, -SO2-, -СН2-, -СНОН- или -NR6-, NR7CONR8 или NR7SO2NR8 и
Z выбирают из группы, состоящей из циклоалкила, гетероциклоалкила, арила и гетероарила, и когда е представляет собой 2, тогда каждый фрагмент Z выбирают независимо друг от друга,
R4, R5 и R6 представляют собой независимо водород, С1-С4алкил, где R4 и R5 вместе могут образовывать 5-7-членное кольцо,
R7 и R8 представляют собой независимо водород, С1-С4алкил, где R7 и R8 вместе могут образовывать 5-7-членное кольцо,
где циклоалкил означает насыщенный моноциклический карбоцикл, содержащий от 3 до 7 атомов углерода,
гетероциклоалкил означает насыщенный моно- или бициклический гетероцикл, имеющий от 3 до 14 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы, и которые необязательно замещены R9 и/или R10,
арил означает моно- и бициклические ароматические карбоциклы, необязательно замещенные фрагментами R9 и/или R10,
гетероарил означает ароматический моно- или бициклический гетероцикл, имеющий от 5 до 10 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы, и которые необязательно замещены R9 и/или R10, и
R9 и R10 независимо выбирают из водорода, С1-С4алкила, циклоалкила, гетероциклоалкила, арила, гетероарила, -CN, -галогена, -CF3, =O, -OR4, -NR4R5, -NR4COR5, -NR4COOR5, -(С1-С4алкил)OR4,
-(C1-С4алкил)NR4R5, -(С1-С4алкил)NR4COR5, -(С1-С4алкил)NR4COOR5, -СООН, COOR4, где R4 и R5 определены выше,
за исключением 6-(2,6-диметилфенил)-N-(4-(4-метил-1-пиперазинил)фенил)-2-хиназолинамина и 6-(2,6-диметилфенил)-N-(4-((3-(1-пиперидинил)пропил)окси)фенил)-2-хиназолинамина.
2. Соединение по п.1, где циклоалкил выбран из циклопропила, циклобутила и циклопентила.
3. Соединение по п.1, где гетероциклоалкил имеет от 5 до 10 кольцевых членов.
4. Соединение по п.3, где гетероцикл имеет от 5 до 6 кольцевых членов.
5. Соединение по п.3, где гетероциклоалкил выбран из пирролидина, пиперидина, пиперазина и морфолина, каждый из которых необязательно замещен R9 и/или R10.
6. Соединение по п.1, где арил выбран из фенила, 1-нафтила и 2-нафтила.
7. Соединение по п.1, где гетероарил имеет от 5 до 6 кольцевых членов.
8. Соединение по п.1, где гетероарил выбран из пиридина, индола, бензофурана, оксазола, триазола и пиримидина, каждый из которых необязательно замещен R9 и/или R10.
9. Соединение по п.1, где R1 является замещенным R9 и R10, и где R9 и R10 представляет собой C1-С4алкил, галоген или -ОН.
10. Соединение по п.1, где R1 представляет собой фенил и является замещенным R9 и R10 в положениях 2, 5 или 6.
11. Соединение по п.1, где X представляет собой связь.
12. Соединение по п.1, где X представляет собой (CH2)aW(CH2)b, где а представляет собой 0, b представляет собой 2, W представляет собой -О-.
13. Соединение по п.1, где X представляет собой (CH2)aW(CH2)bY(CH2)c, где а представляет собой 0, b представляет собой 1 и с представляет собой 0, W представляет собой -О- и Y представляет собой
-СО-.
14. Соединение по п.1, где X представляет собой -[(CH2)aW(CH2)b]m-Z-[(CH2)cY(CH2)d]n, где m представляет собой 0, n представляет собой 1, с представляет собой 0, d представляет собой 0 или 2, Y представляет собой -СО- или отсутствует и Z представляет собой имидазолин-2-он или пиперазин.
15. Соединение по п.1, где R3 представляет собой С1-С4алкил.
16. Соединение по п.15, где R3 представляет собой СН3.
17. Соединение по п.1, где R9 представляет собой ОН.
18. Соединение по п.1, где R3 представляет собой гетероарильную группу.
19. Соединение по п.18, где R3 представляет собой пиридин.
20. Соединение по п.1, где R3 представляет собой гетероциклоалкил.
21. Соединение по п.20, где R3 представляет собой пирролидин, пиперидин, азепин, пиперазин или морфолин.
22. Соединение по п.1, где R3 представляет собой гетероциклоалкил, замещенный R9.
23. Соединение по п.22, где R9 представляет собой -СООН, COOR4, -N[CH3]2.
24. Соединение по п.1, выбранное из группы, состоящей из
[6-(2,6-диметилфенил)хиназолин-2-ил]-[4-(2-пирролидин-1-ил-этокси)фенил]амина;
4-хлор-3-{2-[4-(2-пирролидин-1-ил-этокси)фениламино]хиназолин-6-ил}фенола;
(R)-1-(2-{4-[6-(2,6-диметилфенил)хиназолин-2-иламино]фенокси}этил)пирролидин-2-карбоновой кислоты;
1-{4-[6-(2,6-диметилфенил)хиназолин-2-иламино]фенил}-3-(2-пирролидин-1-ил-этил)имидазолидин-2-она;
1-(4-{4-[6-(2,6-диметилфенил)хиназолин-2-иламино]фенил}пиперазин-1-ил)этанона;
(4-{4-[6-(2,6-диметилфенил)хиназолин-2-иламино]фенил}пиперазин-1-ил)пиридин-4-ил-метанона;
1-{4-[6-(2-хлор-5-гидроксифенил)хиназолин-2-иламино]фенил}-3-(2-пирролидин-1-ил-этил)имидазолидин-2-она;
2-{4-[6-(2-хлор-5-гидроксифенил)хиназолин-2-иламино]фенокси}-1-((R)-3-диметиламинопирролидин-1-ил)этанона;
1-((R)-3-диметиламинопирролидин-1-ил)-2-{4-[6-(2,6-диметилфенил)хиназолин-2-иламино]фенокси}этанона;
1-{4-[6-(2-хлор-5-гидроксифенил)хиназолин-2-иламино]фенил}-3-(2-метоксиэтил)имидазолидин-2-она;
3-{2-[4-(2-азепан-1-ил-этокси)фениламино]хиназолин-6-ил}-4-хлорфенола;
[6-(2,6-диметилфенил)хиназолин-2-ил]-(4-пиперазин-1-ил-фенил)амина;
4-хлор-3-{8-метил-2-[4-(2-пирролидин-1-ил-этокси)фениламино]хиназолин-6-ил}фенола;
[(R)-1-(2-{4-[6-(2-хлор-5-гидроксифенил)хиназолин-2-иламино]фенокси}ацетил)пирролидин-3-ил]диметиламмония;
[(R)-1-(2-{4-[6-(2-хлор-5-гидроксифенил)хиназолин-2-иламино]фенокси}ацетил)пирролидин-3-ил]диметиламмония;
4-хлор-3-[2-(3-гидроксиметилфениламино)-8-метилхиназолин-6-ил]фенола;
(R)-1-(2-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенокси}этил)пирролидин-2-карбоновой кислоты;
1-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}-3-(2-пирролидин-1-ил-этил)имидазолидин-2-она;
(R)-1-[2-(3-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}-2-оксоимидазолидин-1-ил)этил]пирролидин-2-карбоновой кислоты;
1-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}-3-[2-((R)-3-диметиламинопирролидин-1-ил)этил]имидазолидин-2-она;
1-(4-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}пиперазин-1-ил)этанона;
(4-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}пиперазин-1-ил)пиридин-4-ил-метанона;
(4-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}пиперазин-1-ил)пиридин-3-ил-метанона;
(4-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенил}пиперазин-1-ил)пиридин-2-ил-метанона;
2-{4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенокси}-1-((R)-3-диметиламинопирролидин-1-ил)этанона и их соли.
Текст
Изобретение относится к некоторым новым соединениям, к способам их получения и к способам лечения или улучшения состояния заболевания, обусловленного киназой. В частности, это изобретение относится к замещенным хиназолиновым соединениям, которые являются полезными в качестве селективных ингибиторов киназы, к способам получения таких соединений и к способам лечения или улучшения состояния заболевания, обусловленного киназой. В частности, способы относятся к лечению или улучшению состояния заболевания, обусловленного киназой, включая сердечно-сосудистые заболевания, диабет, нарушения, связанные с диабетом, воспалительные заболевания, иммунологические нарушения, злокачественные новообразования и заболевания глаз,такие как ретинопатии или дегенерация желтого пятна или другие витреоретинальные заболевания,и подобные. 019110 Изобретение относится к некоторым новым соединениям, к способам их получения и к способам лечения или улучшения состояния заболевания, относящегося к нарушению функции тирозинкиназы,такого как заболевание, связанное с повышенной проницаемостью сосудов или ангиогенезом. В частности, это изобретение относится к замещенным хиназолиновым соединениям, которые являются полезными в качестве селективных ингибиторов киназы, к способам получения таких соединений и к способам лечения или улучшения состояния, обусловленного киназой заболевания. В частности, способы относятся к лечению или улучшению состояния заболевания, относящегося к нарушению функции тирозинкиназы, включая сердечно-сосудистые заболевания, диабет, нарушения, связанные с диабетом, воспалительные заболевания, иммунологические нарушения, злокачественное новообразование и заболевания глаз, такие как ретинопатии или дегенерация желтого пятна или другие витреоретинальные заболевания и подобные. Пропускание жидкости и клеток из кровеносных сосудов является существенным фактором, содействующим воспалению, повреждению тканей, отеку и смерти во многих случаях. Указанное включает ишемизированное повреждение, токсический шок, ожоги, травму, аллергические и иммунные реакции. Проницаемость сосудов частично регулируется посредством межклеточной адгезии между эндотелиальными клетками. Монослой эндотелиальных клеток, выстилающий сосудистую систему, формирует барьер, который поддерживает целостность системы кровотока, но определенным образом обеспечивает пропускание растворимых факторов и лейкоцитов. Дисрегуляция этого процесса приводит к пропотеванию жидкости через сосуды в окружающие ткани, что сопровождается воспалением, связанным с патологическим состоянием отечности. Проницаемость сосудов является тонко отрегулированной функцией, которая может положительным образом влиять на защитные иммунные ответы и заживление ран; однако во многих патологических случаях, большое и/или хроническое пропотевание жидкости, так же как и перемещение иммуноцитов в ткани может иметь серьезные, а иногда опасные для жизни последствия. Патологическая проницаемость сосудов сетчатки глаза, которая приводит к отеку в области желтого пятна, является ведущей причиной потери зрения при таких болезнях, как диабетическая ретинопатия,экссудативная дегенерация желтого пятна, окклюзия сосудов сетчатки глаза, а также воспалительные состояния и состояния новообразований. Хотя многие болезненные процессы могут приводить к повышенной проницаемости сосудов посредством различных механизмов, известно, что цитокин ФРЭС (фактор роста эндотелия сосудов) играет основную роль в качестве индуктора пропотевания жидкости через сосуды. ФРЭС был сначала описан как сильный фактор сосудистой проницаемости (ФСП), выделяемый клетками опухоли, который стимулировал быстрое и обратимое увеличение капиллярной проницаемости(Senger и др., 1983, Science., 25, 219, 983-5). Повышенная проницаемость сосудов в случае ишемизированных ретинопатий и возможно также в случае экссудативной дегенерации желтого пятна и в случаях увеитов, например, коррелируют с уровнями ФРЭС (Fine и др, 2001, Am. J. Ophthalmol, 132, 794-796;Boyd и др., 2002, Arch Ophthalmol. 120, 1644-1650), и при этом антагонисты ФРЭС успешно использовались для уменьшения отека сетчатки глаза/отека желтого пятна в неовасулярных глазных болезнях, таких как возрастная дегенерация желтого пятна, что приводило к стабилизации или даже к улучшению остроты зрения в подгруппе задействованных пациентов. Путь, посредством которого ФРЭС вызывает сосудистую проницаемость, недавно был разгадан (Gavard and Gutkind, 2006, Nat Cell Biol., 8, 1223-1234) и было показано, что вызываемое посредством ФРЭС пропотевание жидкости через сосуды обусловлено членами цитоплазматических протеинкиназ протоонкогенов семейства Src. Протеинкиназы играют центральную роль в регулировании и обслуживании широкого разнообразия клеточных процессов и клеточных функций. Например, действие киназы действует как молекулярный переключатель, регулирующий клеточную пролиферацию, активацию и/или дифференциацию. В настоящее время получил широкое признание тот факт, что многие заболевания являются результатом аномальных клеточных ответов, вызванных сверхактивными проводящими путями, обусловленными протеинкиназой.Src-киназы формируют семейство мембранно-связанных, не-рецепторно зависимых тирозинкиназ, в которое у млекопитающих входят восемь членов: Src, Fyn, Yes, Fgr, Lyn, Hck, Lck и Blk (Bolen и др.,1997, Annu. Rev. Immunol 371), которые играют важную роль в передаче сигналов рецепторов и передаче информации в клетках (Thomas and Brugge, 1997, Annu Rev Cell Dev Biol., 13, 513-609). В то время как большинство Src-киназ широко экспрессируются (то есть, Src, Fyn, Yes), некоторые члены семейства,такие как Hck, Blk или Lck демонстрируют ограниченную экспрессию. Src-киназы играют ключевую роль в качестве мембранно-связанных молекулярных переключателей, которые связывают множество межклеточных сигналов с внутриклеточными сигнальными путями. Указанное является основанием для вовлечения Src-киназ в процессы клеточной пролиферации и дифференциации, так же как и в процессы неспецифической адгезии и миграции клеток (Thomas SM and JS Brugge, 1997, выше). Было подтверждено документально, что уровень Src-белка и активность Src-киназы являются значительно повышенными в злокачественных новообразованиях человека, включая злокачественные новообразования молочной железы, злокачественные новоообразования толстой кишки, злокачественные новообразования поджелудочной железы, некоторые В-клеточные лейкемии и лимфомы, злокачественные новообразования желудочно-кишечного тракта, мелкоклеточный рак легкого, злокачественные но-1 019110 вообразования мочевого пузыря, злокачественные новообразования простаты и яичников, меланому и саркому (Summy and Gallick, 2003, Cancer Metastasis Rev, 22, 337-58). Таким образом, ожидалось, что блокирование передачи сигналов при помощи ингибирования активности Src-киназы будет являться эффективным средством снижения интенсивности аберрантных проводящих путей, которые приводят к онкологическому перерождению клеток (Abram и др., 2000, Ехр. Cell Res., 254, 1; Russi и др., 2006, JPET,318, 161-172; Jallal и др., 2007, Cancer Research, 67, 1580-1588). Точно так же было подтверждено документально, что киназы семейства Src также являются важными для передачи сигналов в направлении рецепторов иммунных клеток. Fyn, подобно Lck, вовлечен в передачу сигналов ТкР (рецепторов Т-клеток) в Т-клетках (Appleby и др., 1992, Cell., 70, 751). Hck и Fgr вовлечены в передачу сигналов рецептора для Fc-фрагмента, приводящую к активации нейтрофила(Vicentini и др., 2002, J. Immunol., 168, 6446). Lyn и Src также участвуют в передаче сигналов рецептора для Fc-фрагмента, приводящую к высвобождению гистамина и других медиаторов аллергических реакций (Turner and Kinet, 1999, Nature, 402, B24). Указанные результаты предполагают, что ингибиторы киназ семейства Src могут быть полезными в лечении аллергических заболеваний и астмы. В соответствии с действием ФРЭС на проницаемость сосудов некоторые сообщения поддерживают роль Src-киназы в развитии отека. Например, дефицит Src, но не Fyn, или блокада Src уменьшали мозговой отек примерно до 55% после продолжительной мозговой ишемии у мышей (Paul и др., 2001, NatMed., 7 (2):222-7). Ранее было выявлено, что РР 1, ингибитор тирозинкиназы Src, уменьшает отек,уменьшает разрушение гемато-энцефалического барьера (ГЭБ), уменьшает экспрессию ФРЭС (Jadhav и др., 2007, J Neurosurg., 106, 680-686). Точно так же Scheppke и др. (2008, J Clin Invest., 118, 2337-2346) показали, что Src-киназы являются важными медиаторами пропотевания жидкости через сосуды, вызываемого ФРЭС и ишемией сетчатки глаз. Кроме того, от тирозинкиназ Src полностью зависит передача сигналов рецептора ФРЭС в клетках сосудистого эндотелия. Таким образом, активация Src-киназ, которая является результатом стимуляции рецепторов ФРЭС или других факторов роста, расположенных на эндотелиальных клетках или клеткахпредшественниках, вызывает ангиогенез, ответ, который может оказывать вредное воздействие на заболевания сетчатки глаз и роговицы, и который значительным образом способствует развитию опухоли и развитию метастаз. Было раскрыто несколько классов соединений, которые понижают интенсивность или, в частности,ингибируют активность киназ, в качестве возможного лечения вызываемых киназой заболеваний, в частности злокачественного новообразования. Например, WO 2001038315 описывает аминохиназолины в качестве ингибиторов циклинзависимых киназ.WO 2008068507 описывает пиридинилхиназолины в качестве ингибиторов Raf-серин/треонинкиназ для лечения злокачественного новообразования.WO 2008079988 описывает хиназолины в качестве ингибиторов PDK1-киназы для лечения пролиферативных заболеваний, таких как злокачественное новообразование.WO 2006118256 описывает производные хиназолина в качестве ингибиторов р 38 МАРК для ингаляции и для лечения различных воспалительных заболеваний и злокачественных новообразований.WO 2006039718 описывает арил и азотсодержащие бициклические соединения для применения в лечении вызываемых протеинкиназой болезней, включая воспаления, злокачественные новообразования и связанные с ними состояния.Raf-серин/треонинкиназ для лечения заболеваний, таких как злокачественное новообразование.WO 2004065378 описывает 2-аминопиридины в качестве ингибиторов cdk4 для лечения пролиферативных нарушений в клетках, таких как злокачественное новообразование, атеросклероз и рестеноз. Интересно, что WO 2006024034 описывает гетероциклические соединения, полученные из бензотриазина, триазинов, триазолов и оксадиазолов, такие как бензотриазиновые соединения (WO 2005096784) или соединения пиримидина (WO 2006101977), которые являются способными к ингибированию киназ, таких как члены семейства Src-киназ. Однако указанные лекарственные средства в то время, как они заявлены в качестве потенциально полезных в отношении лечения различных офтальмологических заболеваний (например, возрастной дегенерации желтого пятна, диабетической ретинопатии, диабетического отека желтого пятна, злокачественного новообразования и глаукомы), также являются липофильными и не растворимыми в воде (см. WO 2006133411). Как заявляют изобретатели в WO 2006133411, эти специфические свойства являются, в частности, полезными, в частности для применения для лечения глаз, так как указанные лекарственные средства, будучи не растворимыми в воде (растворимость в воде является меньше чем приблизительно 0,1 мг/мл при значении рН в диапазоне 4-8), обладают высокой эффективностью наполнения и незначительными потерями вследствие утечки по причине высокого распределения препарата в липосоме, которая применяется для его доставки к тканям, по сравнению с водой. Все патенты и публикации, упомянутые выше и далее, полностью включены здесь посредством ссылки.-2 019110 Глаз представляет собой сильно защищенный орган. В этом отношении лечение заболеваний глаз является, вероятно, наиболее сложной задачей, которая стимулирует разработку нового лекарственного средства, что подтверждает недостатки существующих методов лечения. Одной из самых удобных и самых безопасных форм доставки лекарственного средства в глаз являются глазные капли, поскольку они не являются инвазивными, не требуют медицинской помощи и потребуют небольших объемов для растворения лекарственного средства. Однако для того, чтобы быть подходящими для местной инстилляции, молекулы должны быть достаточно активными по отношению к их молекулярной цели, обладать физико-химическими свойствами, которые бы позволяли им пересекать мембраны клеток, и быть при этом достаточно растворимыми в водной среде, для того чтобы применять их для роговой оболочки глаз,в качестве раствора. Кроме того, крайне важно, чтобы указанные молекулы лекарственного средства были настолько бесцветными, насколько это является возможным, для того чтобы предотвратить окрашивание глазной ткани, что, в конечном счете, может повредить зрение. Кроме того, пациенты, участвующие в клинических испытаниях, не должны быть осведомленными о природе их лечения, что очевидным образом будет внушать предубеждение, когда действующий ингредиент является "интенсивно" окрашенным. Дополнительно по причине множественной перекрестной реактивности между киназами, является очень желательным, чтобы указанные молекулы лекарственного средства ингибировали целевые киназы с высокой степенью селективности. Отличительным признаком настоящего изобретения является обеспечение новых соединений, которые обладают повышенной растворимостью в воде по сравнению с конкурирующими соединениями. Другим отличительным признаком настоящего изобретения является обеспечение соединений, которые являются высокоактивными, в частности, в качестве ингибиторов киназ src и lyn. Другим отличительным признаком настоящего изобретения является обеспечение соединений, которые являются полезными для лечения заболевания, включая офтальмологическое заболевание, которое вовлекают в патологический процесс нарушения функции тирозинкиназы, такого как заболевание, связанное с повышенной проницаемостью сосудов или ангиогенезом. Другим отличительным признаком настоящего изобретения является обеспечение соединений, которые являются бесцветными или почти бесцветными, в частности, в растворе. Дополнительные отличительные признаки и преимущества настоящего изобретения будут изложены частично в описании, которое следует, и частично будут очевидными из описания, или с ними можно будет ознакомиться практически в соответствии с настоящим изобретением. Цели и другие преимущества настоящего изобретения будут реализованы и достигнуты посредством элементов и комбинаций, в частности, указанных в описании и в приложенной формуле изобретения. В соответствии с одним вариантом осуществления изобретения изобретение относится к соединениям, имеющим структуру (I), так же как к их фармацевтически приемлемой соли, гидрату или сольватуa, b, с и d представляют собой независимо 0, 1, 2 или 3,е представляет собой 0, 1 или 2 иn и m представляют собой независимо 0 или 1, иZ выбирают из группы, состоящей из циклоалкила, гетероциклоалкила, арила и гетероарила, и когда е представляет собой 2, тогда каждый фрагмент Z выбирают независимо друг от друга,R4, R5 и R6 представляют собой независимо водород, С 1-С 4 алкил, и где R4 и R5 вместе могут образовывать 5-7 членное кольцо,R7 и R8 представляют собой независимо водород, С 1-С 4 алкил, и где R7 и R8 вместе могут образовывать 5-7 членное кольцо. Как применяются здесь по всей заявке, любые термины используются в том смысле, что они подразумевают "по крайней мере одно", "по крайней мере, предпочтительно", "одно или более" или "ряд" со-3 019110 единений, на которые ссылаются, или этапов, если из контекста не следует иначе. В частности, "по крайней мере один" и "один или более" означает количество, которое представляет собой один или больше чем один, с особенным предпочтением один, два или три. Термин "и/или" везде, где применяется здесь, включает значение "и", "или" и "все или любая другая комбинация элементов, связанных с указанным термином". Термин "приблизительно", как применяется здесь, означает в пределах 20%, предпочтительно в пределах 10% и более предпочтительно в пределах 5% данного значения или диапазона. Как применяется здесь, термин "включающий", "содержащий" тогда, когда применяется для определения продуктов, композиций и способов, подразумевается означающим то, что продукты, композиции и способы включают соединения или этапы, на которые ссылаются, но исключают другие. Так как применяется здесь, термин "галоген" в качестве группы или части группы является родовым для фтора, хлора, брома или йода. Термин "циклоалкил" означает насыщенный моноциклический карбоцикл, содержащий от 3 до 7 атомов углерода, более предпочтительно до 5 атомов углерода. Примеры моноциклических циклоалкильных радикалов включают циклопропил, циклобутил, циклопентил и подобные. Термин "гетероциклоалкил" означает насыщенный моно- или бициклический гетероцикл, имеющий от 3 до 14 кольцевых членов, предпочтительно от 5 до 10 кольцевых членов и более предпочтительно от 5 до 6 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы, и которые необязательно замещены фрагментами R9 и/или R10. Примерами гетероциклоалкила являются пирролидин, пиперидин, пиперазин, морфолин и подобные. Термин "арил" включает моно- и бициклические ароматические карбоциклы, которые необязательно замещены фрагментами R9 и/или R10. Примеры арила включают фенил, 1-нафтил, 2-нафтил. Термин "гетероарил" означает ароматический моно- или бициклический гетероцикл, имеющий от 5 до 10 кольцевых членов, предпочтительно от 5 до 6 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы и которые необязательно замещены фрагментами R9 и/или R10. Примерами гетероарила являются пиридин, индол, бензофуран, оксазол,триазол, пиримидин и подобные.R9/R10 независимо выбирают из водорода, С 1-С 4 алкила, циклоалкила, гетероциклоалкила, арила,гетероарила, -CN, -галогена, -CF3, =О, -OR4, -NR4R5, -NR4COR5, -NR4COOR5, -(С 1-С 4 алкил)OR4, -(С 1 С 4 алкил)NR4R5, -(С 1-С 4 алкил)NR4COR5, -(С 1-С 4 алкил)NR4COOR5, -COOH, COOR4, с R4 и R5, как определено выше. Соединения изобретения могут содержать один или более хиральных центров по причине присутствия асимметричных атомов углерода, и по этой причине они могут существовать как ряд диастереоизомеров с R или S стереохимией в каждом хиральном центре. Изобретение включает все такие диастереоизомеры и их смеси. Формы пролекарств соединений формулы I также являются частью настоящего изобретения. Пролекарство может представлять собой производное биологически активного вещества ("исходное лекарственное вещество" или "исходная молекула"), которое потребует преобразования в организме, для того чтобы произошло высвобождение активного лекарства, и которое имеет улучшенные характеристики доставки, по сравнению с исходной молекулой лекарственного средства. Преобразование in vivo может быть, например, результатом процесса, такого как химический или ферментативный гидролиз сложного эфира карбоновой, фосфорной или серной кислоты, или восстановления, или окисления восприимчивой функциональной группы. Термин "соединение" здесь, как правило, относится к соединениям формулы I или к их фармацевтически приемлемой соли, гидрату, сольвату, кристаллической форме, отдельным диастереомерам или пролекарствам. Для применения в соответствии с изобретением в композициях формулы (I) в настоящее время предпочтительными являются следующие структурные особенности, в любой совместимой комбинации:R1 представляет собой предпочтительно арил, более предпочтительно фенил.R1 является предпочтительно замещенным с помощью R9 и R10, где R9/R10 представляет собой С 1-С 4 алкил (предпочтительно СН 3), галоген (предпочтительно -Cl), или -ОН.R1 представляет собой предпочтительно фенил и является замещенным с помощью R9 и R10 в положениях 2, 5 или 6.R2 представляет собой предпочтительно водород или метил.X представляет собой предпочтительно связь. В качестве альтернативы X представляет собой предпочтительно (CH2)aW(CH2)b, где а представляет собой 0, b представляет собой 2, W представляет собой -О-. В качестве альтернативы X представляет собой предпочтительно CH2)aW(CH2)bY(CH2)c, где а представляет собой 0, b представляет собой 1 и с представляет собой О, W представляет собой -О-, и Y представляет собой -СО-. В качестве альтернативы X представляет собой предпочтительно -[(CH2)aW(CH2)b]m-Z-4 019110[(CH2)cY(CH2)d]n, где m представляет собой 0, n представляет собой 1, с представляет собой 0, d представляет собой 0 или 2, Y представляет собой -СО- или отсутствует и Z представляет собой имидазолин 2-он или пиперазин. В соответствии с одним вариантом осуществления изобретения X является разветвленным в положении 3 или 4 фенильного фрагмента.R3 представляет собой предпочтительно C1-С 4 алкил, более предпочтительно СН 3. В качестве альтернативы R3 представляет собой С 1-С 4 алкильную группу, предпочтительно метильную группу, замещенную R9, где R9 представляет собой предпочтительно ОН. В качестве альтернативы R3 представляет собой предпочтительно гетероарильную группу, предпочтительно пиридин. В качестве альтернативы R3 представляет собой предпочтительно гетероциклоалкил, предпочтительно пирролидин, пиперидин, азепин, пиперазин или морфолин, более предпочтительно пирролидин. В качестве альтернативы R3 представляет собой предпочтительно гетероциклоалкил, замещенныйR9, где R9 представляет собой предпочтительно -СООН, COOR4, -N[CH3]2. Соединения изобретения включают соединения из примеров, приведенных здесь, в частности следующие, и их соль, гидрат, сольват:(4-4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенилпиперазин-1-ил)пиридин 2-ил-метанон; 2-4-[6-(2-хлор-5-гидроксифенил)-8-метилхиназолин-2-иламино]фенокси-1-R)-3-диметиламинопирролидин-1-ил)этанон. В соответствии с одним вариантом осуществления изобретения соединение изобретения представляет собой соль соединения формулы I. В отдельном варианте осуществления изобретения указанная соль представляет собой хлоргидрат. В соответствии с одним предпочтительным вариантом осуществления изобретения соединения изобретения имеют растворимость в воде более чем 0,1 мг/мл в диапазоне значений рН 4-8, предпочтитель-5 019110 но диапазон значений рН составляет 5-7, например растворимость в воде составляет приблизительно больше 0,5 мг/мл в диапазоне значений рН 5-7, например приблизительно больше 1 мг/мл в диапазоне значений рН 5-7. В соответствии с одним вариантом осуществления изобретения соединения изобретения имеют умеренный цвет, предпочтительно они являются бесцветными или имеют бледно-желтый цвет. Предпочтительные соединения настоящего изобретения действуют, прежде всего, на киназу lyn и/или src. В соответствии с одним вариантом осуществления изобретения соединения изобретения являются ингибиторами киназы lyn и/или src. В соответствии с одним вариантом осуществления изобретения соединения изобретения связываются с Src с ИК 50 (половина ингибирующей концентрации) меньше чем 1 мкМ, предпочтительно меньше чем 100 нМ, еще более предпочтительно меньше чем 10 нМ и предпочтительно меньше чем 1 нМ. В соответствии с одним вариантом осуществления изобретения соединения изобретения связываются с Lyn с ИК 50 меньше чем 1 мкМ, предпочтительно меньше чем 100 нМ, еще более предпочтительно меньше чем 10 нМ и предпочтительно меньше чем 1 нМ. В соответствии с одним вариантом осуществления изобретения обеспечиваются композиции, которые включают одно или более соединений изобретения и фармацевтически приемлемый носитель или водную среду. Как применяется здесь, термин "фармацевтически приемлемый" относится к носителям, которые не дают неблагоприятной, аллергической или другой нежелательной реакции, когда применяются к животному или человеку, соответствующим образом. Как применяется здесь, "фармацевтически приемлемый носитель" включает любые и все растворители, дисперсионные среды, оболочки, антибактериальные и противогрибковые вещества, изотонические и абсорбционные вещества, замедляющие вещества и подобные. Применение таких носителей для фармацевтических активных субстанций является известным в уровне техники. Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences", E. W. Martin. В предпочтительном варианте осуществления соединения изобретения составляют в соответствии с обычными процедурами в качестве фармацевтической композиции, адаптированной для введения в глаза. Дополнительные активные ингредиенты, такие как противовоспалительное вещество, химиотерапевтическое вещество, вещество против злокачественных новообразований, иммуномодулирующее вещество, терапевтическая вакцина на генной основе, продукт иммунотерапии, терапевтическое антитело и/или ингибиторы протеинкиназы также могут быть включены в композиции. В соответствии с одним вариантом осуществления изобретения соединения настоящего изобретения составляют для парентерального введения, например, их составляют для инъекций для внутривенного, внутримышечного, подкожного, или даже внутрибрюшинного способов введения. Приготовление водной композиции, которая содержит соединение или соединения изобретения, производится в пределах навыков уровня техники, в свете настоящего описания. Как правило, такие композиции могут быть подготовлены в качестве инъекционных лекарственных средств или в качестве жидких растворов, или в качестве суспензий; также могут быть приготовлены твердые формы, подходящие для того, чтобы использовать их для приготовления растворов или суспензий, которые получают в результате добавления жидкости перед инъекцией; и препаративные формы также могут быть превращены в эмульсию. В соответствии с другим вариантом осуществления изобретения соединения настоящего изобретения составляют для местного применения соединений изобретения, в частности для лечения офтальмологических заболеваний. Приготовление композиции, которая содержит соединение или соединения изобретения, производится в пределах навыков уровня техники, в свете настоящего описания. Как правило, такие композиции для местного применения могут быть приготовлены как мазь, гель или глазные капли. Офтальмологическая композиция для местного применения может дополнительно быть in situ гелеобразной водной препаративной формой. Такая препаративная форма включает гелеобразующее вещество в концентрации, которая является эффективной для того, чтобы способствовать образованию геля в результате контакта с глазом или со слезной жидкостью в наружной части глаза. Подходящие гелеобразующие вещества включают, но не ограничиваются ими, термоотверждающиеся полимеры, такие как тетра-замещенные этилендиаминовые блок-сополимеры этиленоксида и пропиленоксида (например,полоксамин); поликарбофил и полисахариды, такие как геллан, каррагинан (например, каппа-каррагинан и йота-каррагинан), хитозан и альгинатные смолы. Фраза "in situ гелеобразующий", как применяется здесь, охватывает не только жидкости с низкой вязкостью, которые образуют гели в результате контакта с глазом или со слезной жидкостью в наружной части глаза, но также и большое количество вязких жидкостей, таких как полужидкие и тиксотропные гели, которые демонстрируют значительно повышенную вязкость или плотность геля в результате введения в глаза. В соответствии с другим вариантом осуществления изобретения соединения настоящего изобретения составляют для перорального введения соединений изобретения. Приготовление композиции, которая содержит соединение или соединения изобретения, производится в пределах навыков уровня техники в свете настоящего описания. Как правило, такие композиции для перорального введения могут быть приготовлены как жидкие растворы или суспензии, таблетки, капсулы с замедленным высвобождением и-6 019110 другие твердые вещества для перорального введения. В соответствии с другим вариантом осуществления изобретения соединения настоящего изобретения составляют для внутриопухолевого введения соединений изобретения. Приготовление композиций,которые содержат соединение или соединения изобретения, производится в пределах навыков уровня техники, в свете настоящего описания. Как правило, такие композиции для внутриопухолевого введения могут быть приготовлены как раскрыто выше для других способов применения. В соответствии с другим вариантом осуществления изобретения соединения настоящего изобретения комбинируют с офтальмологически приемлемыми консервантами, веществами, усиливающими вязкость, веществами, усиливающими проникновение, буферными растворами, хлоридом натрия и водой,для того чтобы образовать водную, стерильную офтальмологическую суспензию или раствор. Препаративные формы офтальмологических растворов могут быть приготовлены при помощи растворения соединения в физиологически приемлемом изотоническом водном буферном растворе. Дополнительно офтальмологический раствор может включать офтальмологически приемлемое поверхностно-активное вещество, для того чтобы способствовать растворению соединения. Кроме того, офтальмологический раствор может содержать вещество, которое увеличивает вязкость, такое как гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или подобные, для того чтобы улучшить удерживание препарата в конъюнктивальном мешочке. Гелеобразующие вещества также могут применяться, включая, но не ограничиваясь ими, геллан и ксантановую камедь. Для того, чтобы приготовить стерильные офтальмологические препаративные формы в виде мази,активный ингредиент комбинируют с консервантом в соответствующем носителе, таком как минеральное масло, жидкий ланолин или медицинский вазелин. Соединения предпочтительно составляют как офтальмологические суспензии или растворы для местного применения со значением рН, которое составляет приблизительно 5-8 и более предпочтительно от приблизительно 6,5 до приблизительно 7,5. Обычно соединения в этих препаративных формах содержатся в количестве 0,001-5 вес.%, но предпочтительно в количестве 0,025-2 вес.%. Таким образом, в случае местного применения закапывают в глаза по 1-2 капли указанных препаративных форм 1-4 раза в день в соответствии с усмотрением квалифицированного практикующего врача. В другом варианте осуществления изобретения обеспечиваются способы лечения заболевания, связанного с нарушением функции тирозинкиназы, такие как заболевание, связанное с повышенной проницаемостью сосудов или ангиогенезом, которые включают введения терапевтически эффективного количества одного или более соединений изобретения пациенту, который нуждается в таком лечении. Как применяется здесь, термин "лечение" охватывает профилактику и/или терапию. Соответственно композиции и способы настоящего изобретения не ограничиваются терапевтическим применением и могут применяться для профилактики. По этой причине "лечение" состояния, заболевания или патологического состояния включает: (i) предотвращение или отсрочку появления клинических признаков состояния, заболевания или патологического состояния, которое развивается у пациента, который может страдать от него или который предрасположен к состоянию, заболеванию или патологическому состоянию, но еще не испытывает или не проявляет клинических или субклинических признаков состояния,заболевания или патологического состояния, (ii) подавление состояния, заболевания или патологического состояния, то есть угнетение или замедление развития заболевания или по крайней мере одного его клинического или субклинического признака, или (iii) ослабление заболевания, то есть вызывание регресса состояния, заболевания или патологического состояния или по крайней мере одного из его клинических или субклинических признаков. Как применяются здесь, термины "пациент" "субъект, который нуждается" означает любое животное; предпочтительно животное представляет собой позвоночное животное; в частности член вида млекопитающих, и включает, но не ограничивается ими, домашние животные (например, коровы, свиньи,овцы, лошади, собаки и кошки), приматы, включая людей. Термины "пациент", "субъект, который нуждается" никоим образом не ограничены статусом конкретного заболевания, они охватывают как пациентов, у которых указанная болезнь уже развилась, так и пациентов, которые не больны. Как применяются здесь, термины "терапевтически эффективное количество" означают любое количество соединения или композиции, которое вызывает биологический ответ ткани, животного или человека, клетки, органа. В соответствии с одним вариантом осуществления изобретения упомянутое заболевание, связанное с нарушением функции тирозинкиназы, является заболеванием, связанным с повышенной проницаемостью сосудов. В соответствии с другим вариантом осуществления изобретения упомянутое заболевание, связанное с нарушением функции тирозинкиназы, является заболеванием, связанным с ангиогенезом. В предпочтительном варианте осуществления заболевание, связанное с нарушением функции тирозинкиназы, является заболеванием, связанным с нарушением функции киназы src и/или lyn. В соответствии с одним вариантом осуществления изобретения упомянутое заболевание, связанное с нарушением функции тирозинкиназы, выбирают из группы, состоящей из инфаркта миокарда, инсульта, застойной сердечной недостаточности, ишемии или реперфузионного повреждения, травмы, злокаче-7 019110 ственного новообразования, отека, артрита или другого заболевания суставов, ретинопатии или витреоретинального заболевания, диабетической ретинопатии, отека желтого пятна, включая диабетический отек желтого пятна, дегенерацию желтого пятна, глаукому, аутоиммунное заболевание, синдром пропотевания жидкости через сосуды, воспалительное заболевание, отек, отторжение трансплантанта, ожог,или синдром острой дыхательной недостаточности, синдром расстройства дыхания у взрослых (СРДВ). В другом варианте осуществления изобретения обеспечиваются способы лечения офтальмологического заболевания, связанного с повышенной проницаемостью сосудов, которые включают введения терапевтически эффективного количества одного или более соединений изобретения пациенту, который нуждается в таком лечении. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску злокачественного новообразования, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску отека и/или ангиогенеза, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску дегенерации желтого пятна, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску диабетической ретинопатии, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску отека желтого пятна, включая диабетический отек желтого пятна, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску глаукомы, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску ретинопатии, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску витреоретинального заболевания, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В другом варианте осуществления изобретения обеспечиваются способы лечения пациента, имеющего или подвергающегося риску воспалительного заболевания, которые включают введение пациенту терапевтически эффективного количества одного или более соединений изобретения, посредством этого проводя лечение пациента. В еще одном варианте осуществления изобретения обеспечиваются способы лечения заболевания,включающего офтальмологическое заболевание и злокачественное новообразование, связанного с аномальной проницаемостью сосудов, которые включают введения терапевтически эффективного количества одного или более соединений изобретения в комбинации с противовоспалительным веществом, химиотерапевтическим веществом, противоопухолевым веществом, иммуномодулирующим веществом,терапевтической вакциной на генной основе, продуктом иммунотерапии, терапевтическим антителом и/или ингибитором киназы, пациенту, который нуждается в таком лечении. Введение соединений изобретения, в частности для офтальмологического применения, представляет собой предпочтительно местное применение. Однако изобретение не ограничивается местным применением, поэтому оно также включает, например, интраокулярную и периокулярную инъекцию, системное применение (например, пероральный или другой парентеральный способ применения, такие как, например, подкожные, внутримышечные, внутривенные способы введения) или внутриопухолевое введение. В еще одном варианте осуществления изобретения обеспечиваются способы доставки соединения изобретения к задней поверхности глаза, способ, включающий приготовление композиции, включающей фармацевтически эффективное количество по крайней мере одного соединения изобретения и доставку указанной композиции к глазу пациента, нуждающегося в такой доставке.-8 019110 В еще одном варианте осуществления изобретения обеспечиваются способы доставки соединения изобретения внутрь опухоли, способ, включающий приготовление композиции, включающей фармацевтически эффективное количество по крайней мере одного соединения изобретения и доставку указанной композиции в опухоль пациента, нуждающегося в такой доставке. Для того, чтобы приготовить композицию изобретения, и в частности офтальмологическую композицию или противоопухолевую композицию, терапевтически эффективное количество одного или более соединений изобретения помещают в носитель, как это известно в уровне техники. Например, офтальмологические препаративные формы для местного применения, содержащие стероиды, раскрыты в US 5041434, в то время как замедленное высвобождение офтальмологического лекарственного средства из офтальмологических препаративных форм и полимер с высокой молекулярной массой, который образует гель с высокой вязкостью, были описаны в US 4271143 и US 4407792. Кроме того, GB 2007091 описывает офтальмологическую композицию в форме геля, содержащего водный раствор карбоксивинилового полимера, растворимое в воде основное вещество и офтальмологическое лекарственное средство. В качестве альтернативы US 4615697 раскрывает композицию с контролированным высвобождением и способ применения, основанный на биоадгезии, и лекарственное вещество, такое как противовоспалительное вещество. Количество соединений изобретения, которые подлежат введению, и их концентрация в композициях, применяемых в способе изобретения, зависит от выбранного растворителя, системы доставки или средства доставки, клинического состояния пациента, побочных эффектов и устойчивости соединения в композиции. Таким образом, терапевт применяет соответствующий препарат, содержащий соответствующую концентрацию соединений изобретения, и выбирает количество вводимой препаративной формы в зависимости от клинического опыта по отношению к данному пациенту или в соответствии с подобными типами пациентов. В другом варианте осуществления изобретения обеспечиваются способы приготовления одного или более соединений изобретения или их фармацевтически приемлемой соли, гидрата, сольвата, соли кристаллической формы и их отдельных диастереомеров. Существует множество синтетических способов приготовления соединений изобретения, но все они основываются на знаниях в области химии, известных химику в сфере органического синтеза. Таким образом, соединения, представленные формулой I, могут быть синтезированы в соответствии с процедурами, описанными в литературе, и являются известными специалисту в данной области техники. Типичными литературными источниками являются "Advanced organic chemistry", 4-е издание (Wiley), J. March,"Comprehensive Organic Transformation", 2-е издание (Wiley), R. С. Larock, "Handbook of HeterocyclicChemistry", 2-е издание (Pergamon), A. R. Katritzky), обзорные статьи, такие, которые размещены в "Synthesis", "Acc. Chem. Res", "Chem. Rev", или первичные литературные источники, выявленные с помощью стандартного литературного поиска онлайн или из вторичных источников, таких как "Chemical Abstracts" или "Beilstein". Соединения изобретения могут быть синтезированы при помощи способов, аналогичных в приведенных здесь примерах, для получения конкретных представленных соединений. Используя процедуры, описанные в разделе примеров, и хорошо известные процедуры, специалист в данной области техники может приготовить раскрытые здесь соединения. В другом варианте осуществления изобретения обеспечивается набор, который включает упаковочный материал и композицию, содержащуюся в упаковочном материале, где упаковочный материал включает этикетку, на которой указано, что композиция может применяться для лечения заболеваний,связанных с аномальной проницаемостью сосудов, и где композиция включает один или более соединений изобретения. В другом варианте осуществления изобретения обеспечивается набор, который включает упаковочный материал и композицию, содержащуюся в упаковочном материале, где упаковочный материал включает этикетку, на которой указано, что композиция может применяться для лечения заболеваний,связанных с аномальной проницаемостью сосудов, которые выбраны из инфаркта миокарда, инсульта,застойной сердечной недостаточности, ишемии или реперфузионного повреждения, злокачественного новообразования, артрита или другого заболевания суставов, ретинопатии или витреоретинального заболевания, дегенерации желтого пятна, аутоиммунного заболевания, синдрома пропотевания жидкости через сосуды, воспалительного заболевания, отка, отторжения трансплантанта, ожога или синдрома острой дыхательной недостаточности или синдрома расстройства дыхания у взрослых (СРДВ), и где композиция включает один или более соединений изобретения. В одном предпочтительном варианте осуществления изобретения обеспечивается набор, который включает упаковочный материал и композицию, содержащуюся в упаковочном материале, где упаковочный материал включает этикетку, на которой указано, что композиция может применяться для лечения офтальмологических заболеваний, связанных с аномальной проницаемостью сосудов, и где композиция включает один или более соединений изобретения или их фармацевтически приемлемую соль, гидрат,сольват, кристаллическую форму соли и их отдельные диастереомеры. Специалисты в данной области техники способны оценить, что изобретение, описанное здесь, поддается вариациям и модификациям, кроме описанных специально.-9 019110 Изобретение включает все такие вариации и модификации. Изобретение также включает все этапы,признаки, препаративные формы и соединения, которые упомянуты, или которые указаны в описании,отдельно или совместно, и любые и все комбинации или любые два или более из этапов или признаков. Каждый документ, ссылка, патентная заявка или патент, процитированный в этом тексте, прямо включены здесь полностью посредством ссылки, что означает, что он должен читаться и рассматриваться читателем как часть этого текста. Такой документ, ссылка, патентная заявка или патент, процитированный в этом тексте, не повторяется в этом тексте, просто по причине краткости. Настоящее изобретение не должно быть ограничено в объеме отдельными вариантами осуществления, описанными здесь, которые предназначены только для целей иллюстрирования. Функционально эквивалентные продукты, препаративные формы и способы непосредственно находятся в пределах объема изобретения, как описано здесь. Изобретение, описанное здесь, может включать один или более диапазонов значений (например,величина, концентрация и т.д). Диапазон значений будет пониматься как такой, который включает все значения в пределах диапазона, включая значения, определяющие диапазон, и значения, граничащие с диапазоном, которые приводят к тому же или главным образом к тому же результату, как значения, непосредственно граничащие с тем значением, которое определяет границу диапазона. Следующие примеры приведены для того, чтобы проиллюстрировать приготовление соединений,которые являются объектом этого изобретения, но не должны рассматриваться как допускающие какиелибо ограничения формулы изобретения. Спектр протонного магнитного резонанса каждого соединения примеров соответствовал определенной структуре. Примеры 1 - Синтез соединений общей формулы (I) 1.1. Общий метод Этап А - Связывание 6-бромхиназолин-2-иламин с 1 экв. необязательно замещенной В 1,В 2 фенилбориновой кислоты в полярном растворителе при температуре -100-300 С, наиболее предпочтительно 50-150 С Этап В - Связывание 3- или 4-замещенного бромфенила с 1 экв. необязательно замещенного В 1,В 2 фенилхиназолин-2-иламина в полярном растворителе при температуре -100-300 С, наиболее предпочтительно 50-150 С Соединения формулы I и также исходные материалы для их приготовления приготавливают посредством способов, как описано в примерах, или посредством способов, известных per se, как описано в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der Organischen Chemie[Methods of Organic Chemistry], Georg Thieme Verlag, Штуттгарт; Organic Reactions, John WileySons,Inc., Нью-Йорк), соблюдая точность условий реакций, которые являются известными и подходящими для указанных реакций. Здесь также можно использовать варианты, которые являются известными per se, но не упомянуты здесь более детально. Исходные материалы для указанного процесса, если это является желательным, также могут быть образованы in situ, не выделяя их из реакционной смеси, а вместо этого незамедлительно превращая их далее в соединения формулы I. С другой стороны, является возможным провести реакцию поэтапно. Предпочтительно реакцию соединений проводят в присутствии подходящего растворителя, который предпочтительно является инертным, при соответствующих условиях реакции. Примерами подходящих растворителей являются углеводороды, такие как гексан, простой петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, такие как трихлорэтилен, 1,2-дихлорэтан, тетрахлорметан, хлороформ или дихлорметан; спирты, такие как метанол, этанол, изопропанол, н-пропанол, нбутанол или трет-бутанол; простые эфиры, такие как простой диэтиловый эфир, простой диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; простые гликолевые эфиры, такие как простой монометиловый эфир этиленгликоля или простой моноэтиловый эфир или простой диметиловый эфир этиленгликоля (диглим); кетоны, такие как ацетон или бутанон; амиды, такие как ацетамид, диметилацетамид,диметилформамид (ДМФ) или N-метилпирролидинон (НМП); нитрилы, такие как ацетонитрил; сульфоксиды, такие как диметилсульфоксид (ДМСО); нитросоединения, такие как нитрометан или нитробензол; сложные эфиры, такие как этилацетат, или смеси упомянутых растворителей или смеси с водой. Поляр- 10019110 ные растворители в основном являются предпочтительными. Примерами подходящих полярных растворителей являются хлорированные углеводороды, спирты, простые гликолевые эфиры, нитрилы, амиды и сульфоксиды или их смеси. Более предпочтительными являются амиды, в частности диметилформамид(ДМФ). Как указано выше, температура реакции находится в диапазоне между приблизительно -100 и 300 С, в зависимости от этапа реакции и применяемых условий. Время проведения реакции находится в основном в диапазоне между несколькими минутами и несколькими днями, в зависимости от реакционной способности соответствующих соединений и соответствующих условий реакции. Подходящее время проведения реакции легко может быть определено посредством способов, известных в уровне техники, например, при помощи наблюдения за ходом реакции. Основываясь на температурах реакции, приведенных выше, подходящее время проведения реакции в основном лежит в диапазоне между 10 мин и 48 ч. За каждым этапом реакции, описанным здесь, необязательно может следовать одна или более процедур обработки и/или процедур выделения. Подходящие указанные процедуры являются известными в уровне техники, например, из стандартных работ, таких как Houben-Weyl, Methoden der organischenChemie [Methods of Organic Chemistry], Georg-Thieme-Verlag, Штутгарт). Примеры таких процедур включают, но не ограничиваются ими, выпаривание растворителя, дистилляцию, кристаллизацию, фракционную кристаллизацию, процедуры экстрагирования, процедуры промывания, процедуры дигерирования,процедуры фильтрации, хроматографию, ВЭЖХ хроматографию и процедуры сушки, в частности процедуры сушки в вакууме и/или при повышенной температуре. Перечень сокращений и акронимов: АсОН - уксусная кислота, безв. - безводный, атм. - атмосфера(ы), БОК - трет-бутоксикарбонил,КДИ - 1,1'-карбонилдиимидазол, конц. - концентрированный, д. -день(и), расщ. - расщепление, ДМАЦ NN-диметилацетамид, ДМПУ - 1,3-диметил-3,4,5,6-тетрагидро-2(IH)-пиримидинон, ДМФ - NNдиметилформамид, ДМСО - диметилсульфоксид, ДФФА - дифенилфосфорилазид, ЭДКИ-1-(3 диметиламинопропил)-3-этилкарбодиимид, EtOAc - этилацетат, EtOH - этанол (100%), Et2O - диэтиловый эфир, Et3N - триэтиламин, ч - час(ы), МеОН - метанол, пет. эфир - петролейный эфир (интервал кипения 30-60 С), темп. - температура, ТГФ - тетрагидрофуран, ТФА - трифторАсОН, Тф трифторметансульфонил. Соединения общей формулы I настоящего изобретения могут быть приготовлены в соответствии с процедурами следующих этапов А и В, раскрытых выше, и в соответствии с примерами. Во всех препаративных методах весь исходный материал является известным или может быть легко приготовлен из известных исходных материалов. 1.2. Интермедиаты Во всех препаративных методах весь исходный материал является известным или может быть легко приготовлен из известных исходных материалов при помощи следующего общего метода: Соединения могут быть приготовлены в соответствии с общим методом, за которым следуют процедуры, изложенные в J. Heterocyclic Chem. 34, 385 (1997). Синтез интермедиата 2 6-(2-хлор-5-метоксифенил)хиназолин-2-иламина К раствору 2-хлор-5-метокси бориновой кислоты (14,42 г, 77,34 ммоль, 1,5 экв.), 6-бромхиназолин 2-иламин (11,55 г, 51,56 ммоль, 1 экв.) и Na2CO3 (21,86 г, 206,23 ммоль, 4 экв.) в смеси 120 мл ДМФ/30 мл EtOH/30 мл Н 2 О добавляли 2,311 г (5,16 ммоль, 0,1 экв.) тетракис(трифенилфосфин) палладий. Продукты реакции нагревали в сосуде с обратным холодильником (100 С) на протяжении 2 ч в атмосфере аргона. Затем их охлаждали до комнатной температуры, экстрагировали продукт при помощи ДХМ и рассола. Затем продукт промывали водой и простым эфиром, затем сушили, в результате чего получали 9,010 г (32 ммоль, 61%) бледно-желтого порошка. Интермедиат 1 (6-(2,6-диметилфенил)-иназолин-2-иламин) был синтезирован в соответствии с методом, раскрытым для интермедиата 2. Синтез интермедиата 3 3-(2-аминохиназолин-6-ил)-4-хлорфенола К суспензии 9,010 г (31,53 ммоль, 1 экв.) 6-(2-хлор-5-метоксифенил)хиназолин-2-иламина в 300 мл дихлорметана, охлажденного до температуры 0 С, осторожно добавляли 95 мл 1 М раствора 1M BBr3. Раствор размешивали на протяжении 16 ч. Затем значение рН было доведено до рН 8 при помощи добавления насыщенного раствора NaHCO3. Осажденный продукт фильтровали и промывали эфиром и суши- 11019110 ли, в результате чего получали 7,596 г (27,96 ммоль, 89%) бледно-желтого порошка. 1.3. Соединения изобретения Синтез соединения изобретения 6 К 52 мг (0,06 ммоль, 0,03 экв.) Pd2(dba) добавляли 3,17 мг (0,03 ммоль, 0,02 экв.) 5-(ди-трет-бутилфосфанил)-1',3',5'-трифенил-1'Н-[1,4']бипиразолила и 253 мг (4,52 ммоль, 2,15 экв.) КОН и 3 мл тетрамилового спирта и 400 мкл воды и суспензию размешивали на протяжении 10 мин. Затем добавляли 524 мг(2,10 ммоль, 1 экв.) 6-(2,6-диметилфенил)хиназолин-2-иламина и 681 мг (2,52 ммоль, 1,2 экв.) 1-[2-(4 бромфенокси)этил]пирролидина, за чем следовало добавление 3 мл тетрамилового спирта и 400 мкл воды, и смесь размешивали при температуре 80 С в атмосфере аргона на протяжении 5 ч. Раствор упаривали и продукт затем очищали при помощи флэш-хроматографии (градиент ДХМ/МеОН), в результате чего получали 110 мг (0,25 ммоль, 12%) желтого твердого вещества. Следующие соединения изобретения были приготовлены подобным способом, который описан выше: 2 - Анализ растворимости соединений изобретения Растворимость соединений определялась в водной среде, используя следующую процедуру. 2 мг соединения добавляли к 200 мкл буферного раствора (уксусная кислота/КОН) со значением рН 5. Раствор затем перемешивали на протяжении 24 ч при комнатной температуре и затем центрифугировали на протяжении 10 мин при скорости 16000 об./мин. Соответствующую надосадочную жидкость- 13019110 анализировали с помощью ВЭЖХ и УФ-детектирования. Вычисление концентрации соединения выполняли при помощи анализа площади под наклоном экспериментальной кривой по отношению к площади наклона градуировочного графика, полученного при отдельном использовании растворимого в ДМСО соединения при различных концентрациях. Протестированными соединениями являются: Эталонное соединение ниже является соединением, раскрытым в WO 2005096784 (соединение Cl) Таблица 1. 3 - Определение констант ингибирования соединений изобретения Скрининг и кинетические исследования, описанные здесь, были выполнены, используя запантетованную технологию Caliper Life Sciences' LabChip. Инструменты Caliper LC3000 и EZ Reader II широко применяются на протяжении процесса разработки лекарственного средства для подготовки анализа,предварительного скрининга, селективного скрининга, составления зависимости активности лекарственного вещества от структуры (SARs) и изучения механизма действия (МОА). Технология LabChip в частности хорошо подходит для ферментативных "объектов", таких как киназы, протеазы, фосфатазы, гистондеацетилазы (ГДАЦ), фосфодиэстеразы (ФДЭ) и ацилтрансферазы. Основное преимущество технологии состоит в разделении и непосредственном определении субстратов и продуктов, которое допускает более высокие соотношения "сигнал-шум" и меньше ошибочных положительных/отрицательных результатов. Указанное непосредственное определение также предусматривает идентификацию и исключение ферментативной активности, которая не связана с реакцией киназы, представляющей интерес. Общий анализ: В анализе изменения подвижности киназы при инкубации без субстрата применяют микрожидкостной чип, для того чтобы измерить превращение флуоресцентного пептидного субстрата в фосфорилированный продукт. Реакционную смесь из титрационного микропланшета с лунками подают через капиллярную трубочку на чип, где нефосфорилированный субстрат и фосфорилированный продукт разделены при помощи электрофореза и определены посредством лазерно-индуцированной флюоресценции. График сигнала флюоресценции в зависимости от времени показывает степень протекания реакции. Фосфорилированный продукт перемещается по чипу быстрее, чем нефосфорилированный субстрат, и сигналы- 14019110 от двух видов пептида проявляются как различные пики. Программное обеспечение анализа данных, полученных с помощью Caliper (HTSWA), определяет высоту пиков, с помощью которых вычисляют соотношение продукта к сумме пиков P/(P+S) и процент (%) превращения. Указанное значение применяют для того, чтобы сравнить лунки с соединением с контрольными лунками, которые представлены на планшете, и таким образом определяют % величины ингибирования для соединения. Формула, которую применяют для вычисления % ингибирования, является следующей, где C100% представляет собой средний % превращения лунок со 100% активностью, и С 0% представляет собой средний % превращения лунок с 0 % активностью: (1-(% превращения образца - C0%)/(C100%-C0%100 Специфический анализ: Анализ LC3000 Src и Lyn Соединения растворяли в 100%-м ДМСО и доводили до 25 Х конечной желательной концентрации,используемой в исследовании. Производили последовательное разведение до получения концентраций,предназначенных для отдельных исследований. 1 мкл каждой концентрации был перенесен, в двух повторностях в 384-луночный титрационный микропланшет от компании Greiner. Как правило, в каждую лунку добавляли 12 мкл буферного раствора фермента, содержащего очищенную киназу (различные поставщики), 100 мМ ГЭПЭС, значение рН 7.5, 1 мМ ДТТ (компания Calbiochem, 2333153), 10 мМ MgCl2(компания Sigma, M-1028) или 10 мМ MnCl2 (компания Sigma, М-1787) (специфический анализ) и 0,002% Brij-35 (компания Sigma, B4184). Соединение и фермент поддавали предварительной инкубации на протяжении 15 мин. Затем в каждую лунку добавляли 12 мкл пептида/буферного раствора АТФ, содержащего 100 мМ ГЭПЭС, значение рН 7.5, 1,5 мкМ флуоресцентно-меченного пептида (специфический для киназы, представляющей интерес), АТФ (с выраженным Км, компания Sigma, A9187) и 0,002%Brij-35, для того чтобы начать реакцию. Как правило, реакцию поддавали инкубации на протяжении 11,5 ч при комнатной температуре до получения достаточного (15-40%) превращения пептида в фосфорилированный продукт в линейном диапазоне реакции. Реакции прекращали при помощи добавления 45 мкл останавливающего буферного раствора (содержащего 20 мМ ЭДТК). Затем планшеты были прочитаны на LabChip 3000, с применением 12-трубочного LabChip. Значения % превращения и значения % ингибирования были получены, как описано, и кривые ИК 50 соединений были получены с помощью применения программы Graphpad Prism версии 4 или 5.01. Нелинейная кривая, построенная по точкам,где были использованы сигмоидальные кривые дозозависимых эффектов - величина соответствующего наклона была использована для построения кривой ИК 50 и определения значений ИК 50 и высоты наклонов. Было показано, что соединения изобретения имеют ИК 50, по отношению к киназам Src и Lyn10 нМ. 4 - Клеточный анализ соединений изобретения 4.1 - Анализ жизнеспособности с помощью CellTiter-Glo (АТФ)/анализ пролиферацииMDA-MB-231 является линией человеческих клеток злокачественного новообразования молочной железы, которые являются сильно зависимыми от проводящих путей Src-киназы, которые использовали для анализа жизнеспособности и пролиферации. Таким образом, соединения настоящего изобретения оценивались на предмет их способности к снижению жизнеспособности/пролиферации клеток MDAМВ-231, используя два различных метода, оба касающиеся метаболической активности клеток. Кроме того, некоторые соединения настоящего изобретения были протестированы на их ингибирующее действие против обусловленной ФРЭС пролиферации эндотелиальных клеток сосудов человека (человеческих эндотелиальных клеток пупочной вены). Особенности анализа: Клетки MDA-MB-231 сохраняли как адгезивные культуры не более чем 80% слившихся клеток, в 185 см 2 вентилируемой колбе для культур в среде, специфической для данной линии клеток, дополненной 10% фетальной бычьей сывороткой (ФБС) при температуре 37 С в 5% СО 2. Для анализа пролиферации адгезивные клетки собирали из колбы для культур с помощью трипсин-ЭДТК и ресуспендировали в соответствующей среде, содержащей 0,1-5% ФБС, для анализа. Клеточное содержимое АТФ (реактив CellTiter-Glo от компании Promega) устанавливали с помощью люминесцентной эмиссии, основанной на следующем принципе: В присутствии АТФ (вырабатываемого клеткой) люциферин превращается в оксилюциферин и излучает свет. Содержание АТФ внутри клетки является пропорциональным к количеству оксилюциферина и полученной люминесценции. Условия инкубации: 0,1 мл клеток в суспензии, составляющей 1000 клеток на 0,1 мл, высевают на белое плоское дно 96 луночного планшетов. Клеткам дают прикрепиться к планшетам на протяжении 2-4 ч перед тем, как добавить тестируемые соединения. 0,05 мл тестируемых соединений, суспендированных в соответствующей среде, добавляли в лунки,до получения конечного объема, составляющего 0,15 мл. Культуры инкубировали с помощью тестируемых соединений на протяжении 3-4 дней, перед тем как культуры анализировали на предмет жизнеспо- 15019110 собности клеток. Если инкубационные периоды являются более длительными чем 4 дня, то конечный объем культуры должен быть увеличен до 0,2 мл. В завершение обработки 0,05 мл культурной среды удаляют из каждой лунки с помощью многоканальной пипетки, пипетируя из поверхности лунки. При слабом излучении света в каждую лунку добавляли 0,1 мл реактива CellTiter-Glo и содержание каждой лунки осторожно перемешивали при помощи пипетирования вверх и вниз (Планшеты покрывали фольгой до того, как каждый планшет был прочитан на планшет-ридере Envision). Считывание: Люминесценцию анализируют на мультииндикаторном ридере Envision 2103 (компания PerkinElmer). Вычисление данных: Пролиферацию клеток выражают как процент контрольных лунок (необработанных). Было показано, что соединения изобретения ингибируют пролиферацию клеток с ИК 50 500 нМ. 4.2 - Анализ жизнеспособности с WST-1 (митохондриальный метаболизм)/анализ пролиферации Особенности анализа: Анализ показателей митохондриальной метаболической активности культивируемых клеток основан на скорости превращения субстрата WST-1 в продукт с оптической плотностью, установленной в 440 нм.MDA-MB-231 сохраняли как адгезивные культуры не более чем 80% слившихся клеток, в 185 см вентилируемой колбе для культур в среде, специфической для данной линии клеток, дополненной 10% фетальной бычьей сыворотки (ФБС) при температуре 37 С в 5% СО 2. Для анализа пролиферации адгезивные клетки собирали из колбы для культур с помощью трипсин-ЭДТК и ресуспендировали в соответствующей среде, содержащей 0,1-5% ФБС, для анализа. Анализ с WST-1 (реактив WST-1 от компании Roche) основан на митохондриальном метаболизме субстрата (4-[3-(4-йодфенил)-2-(4-нитрофенил)-2 Н-5-тетразолий]-1,3-бензолдисульфонат) в формазане и определении его абсорбционной способности при 440 нм. Условия инкубации: Кратное количество 0,1 мл клеток высевают на лунки. Клетки высевают при плотности 500-1000 клеток на 0,1 мл на чистое плоское дно 96-луночных планшетов. Клеткам дают прикрепиться к планшетам на протяжении 2-4 ч перед тем, как добавить тестируемые соединения. 0,05 мл тестируемых соединений, суспендированных в соответствующей среде, добавляли в лунки до получения конечного объема, составляющего 0,15 мл. Культуры инкубировали с помощью тестируемых соединений на протяжении 3-4 дней до того, как культуры анализировали на предмет жизнеспособности клеток. Если инкубационные периоды являются более длинными чем 4 дня, то конечный объем культуры повышали до 0,2 мл. В завершение обработки 0,015 мл раствора WST-1 добавляли в каждую лунку. Планшеты возвращали в инкубатор с СО 2 и инкубировали при температуре 37 С на протяжении 1-3 ч. После инкубации планшеты удаляли из инкубатора и помещали в шейкер для титрационных микропланшетов и осторожно встряхивали на протяжении 2 мин. Считывание: Оптическую плотность в 440 нм в каждой лунке определяли, используя планшет-ридер Spectra-maxplus 384. Вычисление данных: Пролиферацию клеток выражали как процент контрольных лунок (необработанных). Было показано, что соединения изобретения ингибируют пролиферацию с ИК 50500 нМ. 5. Данные in vivo Ингибирование пропотевания жидкости через сосуды на экспериментальной модели нарушения гемато-ретинального барьера у кролика Интравитреальная инъекция ФРЭС в глаз кролика приводит к обширному ретинальному пропотеванию жидкости через сосуды (Edelman and Lutz, 2003, Invest. Ophthalmol. Vis. Sci. 2003; 44: ARVO eabstract 328). На основании указанной животной экспериментальной модели мы исследовали эффективность местного применения соединения 7 изобретения на предмет уменьшения ретинального пропотевания жидкости в вызванном ФРЭС нарушении гемато-ретинального барьера у кролика. На протяжении четырех дней 3% тестируемого соединения 7 (30 мг/мл, 10% ПЭГ 400, 87% лабрафила), или контрольных продуктов без соединения изобретения вводили 4 раза в день в качестве местного применения (50 мкл) в правый глаз пяти кроликам. На второй день животные получали отдельную интравитреальную инъекцию 50 мкл (500 нг) рекомбинантного человеческого ФРЭС 165 (RD-системы) в правый глаз. Спустя 47 ч после введения ФРЭС(четвертый день исследования) через краевую ушную вену вводили флуоресцеин, который циркулировал на протяжении одного часа. Нарушение гемато-ретинального барьера анализировали через 48 ч после введения ФРЭС при по- 16019110 мощи измерения содержания флуоресцеина в витреоретинальной области, используя неинвазивную сканирующую визуальную флюорофотометрию. Результаты Мы выявили, что соединение изобретения уменьшает пропотевание жидкости через сосуды на 41%,по сравнению с контрольным соединением, обеспечивая доказательство того, что соединения в соответствии с изобретением являются полезными для уменьшения проницаемости сосудов, и в частности проницаемости сосудов, связанной с витреоретинальными заболеваниями/заболеваниями сетчатки глаз, такими как диабетическая ретинопатия, окклюзия вены сетчатки или возрастная дегенерация желтого пятна. Ингибирование пропотевания жидкости через сосуды на экспериментальной модели нарушения гематоретинального барьера у крысы Мы исследовали эффективность местного применения соединения 11 изобретения на предмет уменьшения ретинального пропотевания жидкости в вызванном ФРЭС нарушении гематоретинального барьера у крысы. Крыс обрабатывали отдельной интравитреальной инъекцией 5 мкл (100 нг) рекомбинантного человеческого ФРЭС 164 (RD-системы) в каждый глаз. На протяжении 27 ч после инъекции ФРЭС в глаза шестнадцати крыс шесть раз вводили в качестве местного применения (10 мкл) 0,51% тестируемого соединения 11 изобретения (5,1 мг/мл буферного раствора при значении рН 5 с 30% циклодекстрина) и контрольный продукт без соединения изобретения. 27 ч спустя после введения ФРЭС вводили внутривенно голубой Эванс (45 мг/кг) и краске давали циркулировать на протяжении 2 ч. Затем каждой крысе проводили инфузию 0,05 М цитратного буфера при значении рН 3.5 (температура 37 С) на протяжении 2 мин, чтобы вывести краску. Сразу же после указанной перфузии оба глаза энуклеировали,и голубой Эванс удаляли посредством выдерживания каждой сетчатой оболочки в формамиде (Qaum и др Invest. Ophthalmol. Vis. Sci.2001, т. 42,10). После этого измеряли абсорбционную способность при помощи спектрофотометра при 620 нм. Нарушение гематоретинального барьера было пропорционально концентрации голубого Эванс в сетчатой оболочке глаза, нормализованной концентрациями голубого Эванс в плазме. Результаты Мы выявили, что соединение изобретения уменьшает пропотевание жидкости через сосуды на 56%,по сравнению с контрольными соединениями, что является доказательством того, что соединения изобретения являются полезными для уменьшения проницаемости сосудов, и в частности проницаемости сосудов, связанной с витреоретинальными заболеваниями/заболеваниями сетчатки глаз, такими как диабетическая ретинопатия. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение, имеющее структуру (I), или его фармацевтически приемлемая сольR1 представляет собой фенил, необязательно замещенный фрагментами R9 и R10, иR2 представляет собой водород или метил,R3 представляет собой водород, С 1-С 4 алкил, циклоалкил, гетероциклоалкил, арил, гетероарил,-CN, -CF3, -OR4, -OCOR4, -COR4, -NR4R5, -NR4COR5, -NR4COOR5, -(С 1-С 4 алкил)OR4, -(C1C4 алкил)COR4, -(С 1-С 4 алкил)NR4R5, -(С 1-C4 алкил)NR4COR5, -(C1-C4 алкил)NR4COOR5,X представляет собой связь, или (CH2)aW(CH2)b, (CH2)aW(CH2)bY(CH2)c или -[(CH2)aW(CH2)b]m(Z)e-[(CH2)cY(CH2)d]n, гдеa, b, с и d представляют собой независимо 0, 1, 2 или 3,е представляет собой 0, 1 или 2 иn и m представляют собой независимо 0 или 1,W представляет собой -СО-, -О-, -SO2-, -CH2-, -СНОН-, -NR6-, NR7CONR8 или NR7SO2NR8,Y представляет собой -СО-, -О-, -SO2-, -СН 2-, -СНОН- или -NR6-, NR7CONR8 или NR7SO2NR8 иZ выбирают из группы, состоящей из циклоалкила, гетероциклоалкила, арила и гетероарила, и когда е представляет собой 2, тогда каждый фрагмент Z выбирают независимо друг от друга,R4, R5 и R6 представляют собой независимо водород, С 1-С 4 алкил, и где R4 и R5 вместе могут образовывать 5-7-членное кольцо,R7 и R8 представляют собой независимо водород, С 1-С 4 алкил, и где R7 и R8 вместе могут образовывать 5-7-членное кольцо,где циклоалкил означает насыщенный моноциклический карбоцикл, содержащий от 3 до 7 атомов углерода,- 17019110 гетероциклоалкил означает насыщенный моно- или бициклический гетероцикл, имеющий от 3 до 14 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы, и которые необязательно замещены R9 и/или R10,арил означает моно- и бициклические ароматические карбоциклы, необязательно замещенные фрагментами R9 и/или R10,гетероарил означает ароматический моно- или бициклический гетероцикл, имеющий от 5 до 10 кольцевых членов, который содержит один или более кольцевых членов гетероатома, выбранных из азота, кислорода и серы, и которые необязательно замещены R9 и/или R10, иR9 и R10 независимо выбирают из водорода, С 1-С 4 алкила, циклоалкила, гетероциклоалкила, арила,гетероарила, -CN, -галогена, -CF3, =O, -OR4, -NR4R5, -NR4COR5, -NR4COOR5, -(С 1-С 4 алкил)OR4, -(C1 С 4 алкил)NR4R5, -(С 1-С 4 алкил)NR4COR5, -(С 1-С 4 алкил)NR4COOR5, -СООН, COOR4, где R4 и R5 определены выше,за исключением 6-(2,6-диметилфенил)-N-(4-(4-метил-1-пиперазинил)фенил)-2-хиназолинамина и 6(2,6-диметилфенил)-N-(4-3-(1-пиперидинил)пропил)окси)фенил)-2-хиназолинамина. 2. Соединение по п.1, где циклоалкил выбран из циклопропила, циклобутила и циклопентила. 3. Соединение по п.1, где гетероциклоалкил имеет от 5 до 10 кольцевых членов. 4. Соединение по п.3, где гетероцикл имеет от 5 до 6 кольцевых членов. 5. Соединение по п.3, где гетероциклоалкил выбран из пирролидина, пиперидина, пиперазина и морфолина, каждый из которых необязательно замещен R9 и/или R10. 6. Соединение по п.1, где арил выбран из фенила, 1-нафтила и 2-нафтила. 7. Соединение по п.1, где гетероарил имеет от 5 до 6 кольцевых членов. 8. Соединение по п.1, где гетероарил выбран из пиридина, индола, бензофурана, оксазола, триазола и пиримидина, каждый из которых необязательно замещен R9 и/или R10. 9. Соединение по п.1, где R1 является замещенным R9 и R10, и где R9 и R10 представляет собой C1 С 4 алкил, галоген или -ОН. 10. Соединение по п.1, где R1 представляет собой фенил и является замещенным R9 и R10 в положениях 2, 5 или 6. 11. Соединение по п.1, где X представляет собой связь. 12. Соединение по п.1, где X представляет собой (CH2)aW(CH2)b, где а представляет собой 0, b представляет собой 2, W представляет собой -О-. 13. Соединение по п.1, где X представляет собой (CH2)aW(CH2)bY(CH2)c, где а представляет собой 0, b представляет собой 1 и с представляет собой 0, W представляет собой -О- и Y представляет собой-СО-. 14. Соединение по п.1, где X представляет собой -[(CH2)aW(CH2)b]m-Z-[(CH2)cY(CH2)d]n, где m представляет собой 0, n представляет собой 1, с представляет собой 0, d представляет собой 0 или 2, Y представляет собой -СО- или отсутствует и Z представляет собой имидазолин-2-он или пиперазин. 15. Соединение по п.1, где R3 представляет собой С 1-С 4 алкил. 16. Соединение по п.15, где R3 представляет собой СН 3. 17. Соединение по п.1, где R9 представляет собой ОН. 18. Соединение по п.1, где R3 представляет собой гетероарильную группу. 19. Соединение по п.18, где R3 представляет собой пиридин. 20. Соединение по п.1, где R3 представляет собой гетероциклоалкил. 21. Соединение по п.20, где R3 представляет собой пирролидин, пиперидин, азепин, пиперазин или морфолин. 22. Соединение по п.1, где R3 представляет собой гетероциклоалкил, замещенный R9. 23. Соединение по п.22, где R9 представляет собой -СООН, COOR4, -N[CH3]2. 24. Соединение по п.1, выбранное из группы, состоящей из
МПК / Метки
МПК: C07D 403/04, A61K 31/502, C07D 401/14, A61P 35/00
Метки: замещенные, хиназолиновые, соединения
Код ссылки
<a href="https://eas.patents.su/20-19110-zameshhennye-hinazolinovye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные хиназолиновые соединения</a>
Предыдущий патент: Хирургический материал для реконструкции дефектов костной ткани (варианты)
Следующий патент: Импульсный модулятор с формирователем ступенчатого напряжения
Случайный патент: Инсектицидные соединения, основанные на производных изоксазолина