Способ лечения злоупотребления алкоголем и аддикции
Формула / Реферат
1. Способ лечения злоупотребления алкоголем или аддикции, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I)
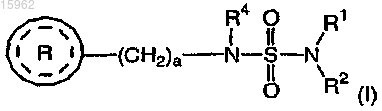
где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и C1-4алкила;
R4 выбран из группы, состоящей из водорода и C1-4алкила;
а равно 1 или 2;
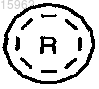 представляет собой
представляет собой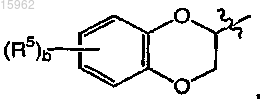
где b равно целому числу от 0 до 4;
каждый R5 независимо выбран из группы, состоящей из галогена и C1-4алкила;
или его фармацевтически приемлемой соли.
2. Способ по п.1, в котором вводят соединение формулы I,
где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и C1-4алкила;
R4 выбран из группы, состоящей из водорода и C1-4алкила;
а равно 1 или 2;
 представляет собой
представляет собой
,
где b равно целому числу от 0 до 2;
каждый R5 независимо выбран из группы, состоящей из галогена и С1-4алкила;
или его фармацевтически приемлемую соль.
3. Способ по п.2, в котором вводят соединение формулы I, где
R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и С1-4алкила;
R4 выбран из группы, состоящей из водорода и метила;
а равно 1 или 2;
выбран из группы, состоящей из
2-(2,3-дигидробензо[1,4]диоксинила),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинила),
2-(6-фтор-2,3-дигидробензо[1,4]диоксинила),
2-(5-фтор-2,3-дигидробензо[1,4]диоксинила),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинила),
2-(7-метил-2,3-дигидробензо[1,4]диоксинила),
2-(5-хлор-2,3-дигидробензо[1,4]диоксинила),
2-(6-бром-2,3-дигидробензо[1,4]диоксинила),
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинила) и
2-(8-хлор-2,3-дигидробензо[1,4]диоксинила);
или его фармацевтически приемлемую соль.
4. Способ по п.3, в котором вводят соединение формулы I,
где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и метила;
R4 выбран из группы, состоящей из водорода и метила;
а равно 1 или 2;

выбран из группы, состоящей из
2-(2,3-дигидробензо[1,4]диоксинила),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинила),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинила),
2-(7-метил-2,3-дигидробензо[1,4]диоксинила),
2-(6-бром-2,3-дигидробензо[1,4]диоксинила) и
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинила);
или его фармацевтически приемлемую соль.
5. Способ по п.1, где соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид или его фармацевтически приемлемую соль.
6. Способ лечения злоупотребления алкоголем или аддикции, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид или его фармацевтически приемлемую соль.
Текст
Дата публикации и выдачи патента Номер заявки СПОСОБ ЛЕЧЕНИЯ ЗЛОУПОТРЕБЛЕНИЯ АЛКОГОЛЕМ И АДДИКЦИИ Настоящее изобретение относится к способу лечения злоупотребления психоактивным веществом и/или аддикции, включающему введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества одного или нескольких производных бензоконденсированного гетероциклического сульфамида формулы (I), где значения радикалов в соединении формулы (I) приведены в описании. Кроме того, настоящее изобретение относится к способу лечения злоупотребления алкоголем и/или аддикции, включающему введение субъекту,нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы 015962 Область техники, к которой относится изобретение Настоящее изобретение относится к применению производных бензоконденсированного гетероциклического сульфамида для лечения злоупотребления психоактивным веществом и аддикции. Уровень техники изобретения Злоупотребление алкоголем, обычно характеризующееся дезадаптированной картиной применения алкоголя, приводящее к клинически значительному ухудшению здоровья или дистрессу, является серьезной медицинской и социальной проблемой. Предполагалось, что средства, вызывающие селективное снижение потребления алкоголя животными без вызывания параллельного уменьшения приема воды или пищи, вероятно, являются клинически эффективными при лечении алкоголизма у людей (Myers, 1994). Дайдзин, активный ингредиент китайского растения Radix pureariea (RP), применяемый в качестве традиционного средства для лечения хронического алкоголизма в Китае, имеет следующий профиль: он уменьшает потребление алкоголя у золотистого хомячка без уменьшения приема воды или пищи (Keungand Vallee, 3, 1993). В противоположность этому было показано, что многие лекарственные средства, в том числе специфические серотонергические агонисты (например, сертралин) и антагонисты опиатов(например, налоксон и налтрексон), подавляют потребление алкоголя у животных и в то же время также снижают потребление воды или пищи (Myers, 1994). Однако хотя атипичные антипсихотические средства предлагались в качестве возможных средств для лечений злоупотребления различными психоактивными веществами, такая лекарственная терапия может вызывать значительный метаболизм в печени пациентов, злоупотребляющих различными психоактивными веществами. Популяция пациентов с печеночной недостаточностью очень велика. Следовательно, может быть подходящим лечение пациентов,злоупотребляющих различными психоактивными веществами, атипичными антипсихотическими средствами, которые значительно не метаболизируются в печени. Поэтому сохраняется необходимость в эффективном лечении злоупотребления психоактивным веществом и/или аддикции к нему, в большей степени при злоупотреблении, в частности, алкоголем, кокаином, героином, метамфетамином, кетамином, Экстази, никотином, оксиконтином/оксикодоном, кодеином, морфином и т.п. и/или аддикции к ним. Сущность изобретения Настоящее изобретение относится к способу лечения злоупотребления психоактивным веществом и/или аддикции к нему, включающему введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и низшего алкила;R4 выбран из группы, состоящей из водорода и низшего алкила; а равно целому числу от 1 до 2; выбран из группы, состоящей из где b равно целому числу от 0 до 4 и с равно целому числу от 0 до 2; каждый R5 независимо выбран из группы, состоящей из галогена, низшего алкила и нитро; при условии, что когда то а равно 1; или его фармацевтически приемлемой соли. Настоящее изобретение далее относится к способу лечения злоупотребления психоактивным веществом и/или аддикции к нему, включающему введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (II) или его фармацевтически приемлемой соли. Примером изобретения служит способ лечения злоупотребления алкоголем и/или аддикции, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества любого из описанных здесь соединений или фармацевтических композиций. Следующим примером изобретения служит способ лечения злоупотребления и/или аддикции к веществу, выбранному из группы, состоящей из алкоголя, кокаина, героина, метамфетамина, кетамина,Экстази, никотина, оксиконтина/оксикодона, кодеина, морфина, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества любого из описанных здесь соединений. Подробное описание изобретения Настоящее изобретение относится к способу лечения злоупотребления психоактивным веществом и/или аддикции к нему, включающему введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где, а, R1, R2 и R4 имеют значения, указанные в данном описании. Настоящее изобретение далее относится к способам лечения злоупотребления психоактивным веществом и/или аддикции к нему совместной терапией, включающим введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества по меньшей мере одного средства против аддикции и охарактеризованного здесь соединения формулы (I) или формулы (II). Применяемый здесь термин вещество, когда оно относится к психоактивным веществам злоупотребления и/или аддикции, будет включать, если не оговорено особо, любое легальное или нелегальное вещество, к которому у субъекта или пациента может развиться аддикция. Классы лекарственных средств, которые могут вызвать злоупотребление, включают, но не ограничиваются перечисленным,стимуляторы, галлюциногены, барбитураты, природные и синтетические опиоиды и бензодиазепины. Подходящие примеры этих соединений включают, но не ограничиваются перечисленным, алкоголь, кокаин, героин, метамфетамин, кетамин, Экстази, никотин, оксиконтин/оксикодон, кодеин, морфин и т.п. Применяемый здесь термин средство против аддикции будет означать, если не оговорено особо,любое фармацевтическое средство, которое применимо для лечения злоупотребления психоактивным веществом и/или аддикции к нему. Более конкретно, средства против аддикции включают лекарственные средства для замещения, лекарственные средства для замены (например, героин на метадон), лекарственные средства, которые блокируют страстное желание, лекарственные средства, которые блокируют или ослабляют симптомы отмены, лекарственные средства, которые блокируют приятные ощущения и вознаграждения при злоупотреблении психоактивным веществом и т.п. Подходящие примеры включают, но не ограничиваются перечисленным, налтрексон (в том числе вивтрекс), налмефен, антабус,акампросат, палиперидон и т.п. Когда веществом аддикции является алкоголь, средством против аддикции, применяемым в способах совместной терапии настоящего изобретения, предпочтительно является налтрексон. Термин субъект, применяемый здесь, относится к животному, предпочтительно млекопитающе-2 015962 му, наиболее предпочтительно человеку, который был объектом лечения, наблюдения или эксперимента. Термин терапевтически эффективное количество, применяемый здесь, означает, что количество активного соединения или фармацевтического средства вызывает биологическую или медицинскую реакцию в тканевой системе, организме животного или человека, который обследуется исследователем,ветеринаром, врачом или другим клиницистом, которая включает ослабление симптомов подвергаемого лечению заболевания или нарушения. В одном из вариантов осуществления настоящего изобретения R1 выбран из группы, состоящей из водорода и метила. В другом варианте осуществления настоящего изобретения R2 выбран из группы,состоящей из водорода и метила. В еще одном варианте осуществления настоящего изобретения R1 и R2,каждый, представляют собой водород или R1 и R2, каждый, представляют собой метил. В одном из вариантов осуществления настоящего изобретения -(CH2)а- выбран из группы, состоящей из -CH2- и -CH2-CH2-. В другом варианте осуществления настоящего изобретения -(СН 2)апредставляет собой -CH2-. В одном из вариантов осуществления настоящего изобретения R4 выбран из группы, состоящей из водорода и метила, предпочтительно R4 представляет собой водород. В одном из вариантов осуществления настоящего изобретения а равно 1. В одном из вариантов осуществления настоящего изобретения b равно целому числу от 0 до 2. В другом варианте осуществления настоящего изобретения с равно целому числу от 0 до 2. В другом варианте осуществления настоящего изобретения b равно целому число от 0 до 1. Еще в одном варианте осуществления настоящего изобретения с равно целому числу от 0 до 1. Еще в одном варианте осуществления настоящего изобретения сумма b и с равна целому числу от 0 до 2, предпочтительно целому числу от 0 до 1. Еще в одном варианте осуществления настоящего изобретения b равно целому числу от 0 до 2 и с равно 0. В одном из вариантов осуществления настоящего изобретения В другом варианте осуществления настоящего изобретения В одном из вариантов осуществления настоящего изобретения выбран из группы, состоящей из 2-(2,3-дигидробензо[1,4]диоксинила), 2-(бензо[1,3]диоксолила), 3-(3,4-дигидробензо[1,4]диоксепинила),2-(6-хлор-2,3-дигидробензо[1,4]диоксинила), 2-(6-фтор-2,3-дигидробензо[1,4]диоксинила), 2-(хроманила), 2-(5-фтор-2,3-дигидробензо[1,4]диоксинила), 2-(7-хлор-2,3-дигидробензо[1,4]диоксинила), 2-(6 хлорбензо[1,3]диоксолила), 2-(7-нитро-2,3-дигидробензо[1,4]диоксинила), 2-(7-метил-2,3-дигидробензо[1,4]диоксинила), 2-(5-хлор-2,3-дигидробензо[1,4]диоксинила), 2-(6-бром-2,3-дигидробензо[1,4]диоксинила), 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинила), 2-(8-хлор-2,3-дигидробензо[1,4]диоксинила), 2(2,3-дигидронафто[2,3-b][1,4]диоксинила) и 2-(4-метилбензо[1,3]диоксолила). выбран из группы, состоящей из 2 В другом варианте осуществления настоящего изобретения варианте осуществления настоящего изобретения выбран из группы, состоящей из 2-(2,3 дигидробензо[1,4]диоксинила), 2-(7-метил-2,3-дигидробензо[1,4]диоксинила) и 2-(6-бром-2,3-дигидробензо[1,4]диоксинила). В одном из вариантов осуществления настоящего изобретения R5 выбран из группы, состоящей из водорода и низшего алкила. В другом варианте осуществления настоящего изобретения R5 выбран из хлора, фтора, брома и метила. В одном варианте осуществления настоящего изобретения стереоцентр у соединения формулы (I) имеет S-конфигурацию. В другом варианте осуществления настоящего изобретения стереоцентр у соединения формулы (I) имеет R-конфигурацию. В одном из вариантов осуществления настоящего изобретения соединение формулы (I) присутствует в виде энантиомерно обогащенной смеси, где % энантиомерного обогащения (% ее) больше чем приблизительно 75%, предпочтительно больше чем приблизительно 90%, более предпочтительно больше чем приблизительно 95%, наиболее предпочтительно больше чем приблизительно 98%. Дополнительные варианты осуществления настоящего изобретения включают соединения, у которых заместители, выбранные для одного или нескольких символов, указанных здесь (т.е. R1, R2, R3, R4,X-Y и А), независимо выбраны так, чтобы быть любым индивидуальным заместителем или любой подгруппой заместителей, выбранных из полного списка, указываемого здесь. Репрезентативные соединения настоящего изобретения, применимые для лечения злоупотребления алкоголем и аддикции, перечислены в приведенной ниже табл. 1. Дополнительные соединения настоящего изобретения, применимые для лечения злоупотребления алкоголем и аддикции, перечислены в табл. 3. В приведенных ниже табл. 1 и 2 столбец, озаглавленный стерео, указывает стереоконфигурацию у атома углерода гетероцикла, присоединенного у связи, обозначенной звездочкой. Когда не имеется никакого обозначения, соединение было получено в виде смеси соединений с разными стереоконфигурациями. Когда дано обозначение "R" или "S", стереоконфигурация основана на энантиомерно обогащенном исходном веществе. Таблица 1 Репрезентативные соединения формулы (I) Применяемый здесь термин галоген, если не оговорено особо, будет означать хлор, бром, фтор и иод. Применяемый здесь термин алкил, если не оговорено особо, независимо от того, применяют ли его отдельно или как часть группы-заместителя, включает неразветвленные и разветвленные цепи. Например, алкильные радикалы включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил,трет-бутил, пентил и т.п. Если не оговорено особо, термин низший применительно к алкилу означает углеродную цепь из 1-4 атомов углерода. Применяемый здесь термин алкокси, если не оговорено особо, будет означать кислородсодержащий простой эфирный радикал описанных выше алкильных групп с неразветвленной или разветвленной цепью. Например, метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и т.п. Применяемое здесь обозначениебудет означать присутствие стереогенного центра. Когда конкретная группа является замещенной (например, алкил, арил и т.д.), такая группа может иметь один или несколько заместителей, предпочтительно от одного до пяти заместителей, более пред-5 015962 почтительно от одного до трех заместителей, наиболее предпочтительно от одного до двух заместителей,независимо выбранных из списка заместителей. Со ссылкой на заместители термин независимо означает, что когда возможным является присутствие более чем одного такого заместителя, такие заместители могут быть одинаковыми или отличными друг от друга. При применении стандартной номенклатуры на всем протяжении данного описания концевая часть указанной боковой цепи описывается первой с последующим описанием соседней функциональной группы по направлению к месту присоединения. Так, например, заместитель фенил-алкил-аминокарбонил-алкил относится к группе формулыDCC = дициклогексилкарбодиимид,DCE = дихлорэтан,DCM = дихлорметан,DIPEA или DIEA = диизопропилэтиламин,ДМФА = N,N-диметилформамид,ДМСО = диметилсульфоксид,EDC = этилкарбодиимид,Et3N или TEA = триэтиламин,Et2O = диэтиловый простой эфир,ЕА или EtOAc = этилацетат,EtOH = этанол,IPA = 2-пропанол,Hept = гептан,НОВТ = 1-гидроксибензотриазол,ВЭЖХ = высокоэффективная жидкостная хроматография,LAH = литийалюминийгидрид,М или МеОН = метанол,ЯМР = ядерный магнитный резонанс,Pd-C = катализатор палладий-на-угле,ВЭЖХ ОФ = высокоэффективная жидкостная хроматография с обращенной фазой,RT или rt = комнатная температура,TEA = триэтиламин,TFA = трифторуксусная кислота,ТГФ = тетрагидрофуран,ТСХ = тонкослойная хроматография. Когда соединения согласно данному изобретению имеют по меньшей мере один хиральный центр,они могут соответственно существовать в виде энантиомеров. Когда соединения обладают двумя или более хиральными центрами, они могут дополнительно существовать в виде диастереомеров. Должно быть понятно, что такие изомеры и их смеси включены в объем настоящего изобретения. Кроме того,некоторые из кристаллических форм соединений могут существовать в виде полиморфов, и предполагается, что как таковые они включены в настоящее изобретение. Кроме того, некоторые соединения могут образовывать сольваты с водой (т.е. гидраты) или обычными органическими растворителями, и также предполагается, что такие сольваты включены в объем настоящего изобретения. Для применения в медицине соли соединений данного изобретения относятся к нетоксичным фармацевтически приемлемым солям. Однако другие соли могут быть применимыми при получении соединений согласно изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений включают кислотно-аддитивные соли, которые можно, например, получить смешиванием раствора соединения с раствором фармацевтически приемлемой кислоты, такой как хлористо-водородная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, когда соединения изобретения имеют кислотную часть, их подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов, например соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли, образованные с подходящими органическими лигандами, например соли четвертичного аммония. Таким образом, репрезентативные фармацевтически приемлемые соли включают следующие соли: ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, кальций эдетат, камсилат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эзилат,фумарат, глюцептат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробро-6 015962 мид, гидрохлорид, гидроксинафтоат, иодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, аммониевую соль Nметилглюкамина, олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат,салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат. Репрезентативные кислоты и основания, которые можно применять при получении фармацевтически приемлемых солей, включают следующие: кислоты, включающие уксусную кислоту, 2,2-дихлоруксусную кислоту, ацилированные аминокислоты, адипиновую кислоту, альгиновую кислоту, аскорбиновую кислоту, L-аспарагиновую кислоту, бензолсульфоновую кислоту, бензойную кислоту, 4-ацетамидобензойную кислоту, (+)-камфорную кислоту,камфорсульфоновую кислоту, (+)-(1S)-камфор-10-сульфоновую кислоту, каприновую кислоту, капроновую кислоту, каприловую кислоту, янтарную кислоту, лимонную кислоту, цикламовую кислоту, додецилсерную кислоту,этан-1,2-дисульфоновую кислоту,этансульфоновую кислоту,2 гидроксиэтансульфоновую кислоту, муравьиную кислоту, фумаровую кислоту, галактаровую кислоту,гентизовую кислоту, глюкогептоновую кислоту, D-глюконовую кислоту, D-глюкуроновую кислоту, Lглутаминовую кислоту, -оксоглутаровую кислоту, гликолевую кислоту, гиппуровую кислоту, бромисто-водородную кислоту, хлористо-водородную кислоту, (+)-L-молочную кислоту, -DL-молочную кислоту, лактобионовую кислоту, малеиновую кислоту, (-)-L-яблочную кислоту, малоновую кислоту,(+)-DL-миндальную кислоту, метансульфоновую кислоту, нафталин-2-сульфоновую кислоту, нафталин 1,5-дисульфоновую кислоту, 1-гидрокси-2-нафтойную кислоту, никотиновую кислоту, азотную кислоту,олеиновую кислоту, оротовую кислоту, щавелевую кислоту, пальмитиновую кислоту, памоевую кислоту,фосфорную кислоту, L-пироглутаминовую кислоту, салициловую кислоту, 4-аминосалициловую кислоту, себациновую кислоту, стеариновую кислоту, янтарную кислоту, серную кислоту, дубильную кислоту,(+)-L-винную кислоту, тиоциановую кислоту, п-толуолсульфоновую кислоту и ундециленовую кислоту,и основания, включающие аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, деанол, диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин,гидрабамин, 1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин, пиперазин, гидроксид калия, 1-(2-гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Соединения формулы (I) можно получить согласно способу, указанному на схеме 1. Схема 1 Соответственно этому подходящим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с сульфамидом, известным соединением, предпочтительно, когда сульфамид присутствует в количестве в диапазоне от приблизительно 2 до приблизительно 5 экв., в органическом растворителе, таком как ТГФ, диоксан и т.п., предпочтительно при повышенной температуре в диапазоне от приблизительно 50 до приблизительно 100 С, более предпочтительно приблизительно при температуре флегмы, получая при этом соответствующее соединение формулы (Ia). В альтернативном случае подходящим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с подходящим образом замещенным соединением формулы (XI), известным соединением или соединением, полученным известными методами, в присутствии основания, такого как TEA, DIPEA, пиридин и т.п., в органическом растворителе, таком как ДМФА, ДМСО и т.п., получая при этом соответствующее соединение формулы (I). Соединения формулы (X), где способу, указанному на схеме 2. Соответственно этому подходящим образом замещенное соединение формулы (XII), известное соединение или соединение, полученное известным методом (например, как описано на приведенной выше схеме 2), подвергают взаимодействию с NH4OH, известным соединением необязательно в органическом растворителе, таком как ацетонитрил и т.п., получая при этом соответствующее соединение формулы(XIII). Соединение формулы (XIII) подвергают взаимодействию с подходящим образом выбранным восстанавливающим агентом, таким как LAH и т.п., в органическом растворителе, таком как ТГФ, диэтиловый простой эфир и т.п., получая при этом соответствующее соединение формулы (Ха). Соединения формулы (X), где бу, указанному на схеме 3., можно получить согласно спосо Схема 3 Согласно этому подходящим образом замещенное соединение формулы (XIV), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с NH4OH в присутствии средства сочетания, такого как DCC и т.п., необязательно в органическом растворителе, таком как ацетонитрил и т.п., получая при этом соответствующее соединение формулы (XV). Соединение формулы (XV) подвергают взаимодействию с подходящим образом выбранным восстанавливающим агентом, таким как LAH и т.п., в органическом растворителе, таком как ТГФ, диэтиловый простой эфир и т.п., получая при этом соответствующее соединение формулы (Xb). выбран из Соединения формулы (X), где гласно способу, указанному на схеме 4. Схема 4 и где а равно 2, можно получить со Соответственно этому подходящим образом замещенное соединение формулы (XVI), где J1 представляет собой подходящую уходящую группу, такую как Br, Cl, I, тозил, мезил, трифлил (трифторметилсульфонил) и т.п., известное соединение или соединение, полученное известными методами (например, активацией соответствующего соединения, у которого J1 представляет собой ОН), подвергают взаимодействию с цианидом, таким как цианид калия, цианид натрия и т.п., в органическом растворителе,таком как ДМСО, ДМФА, ТГФ и т.п., получая при этом соответствующее соединение формулы (XVII). Соединение формулы (XVII) восстанавливают согласно известным методам, например взаимодействием с подходящим восстанавливающим агентом, таким как LAH, боран и т.п., получая при этом соответствующее соединение формулы (Хс). Соединения формулы (X), где выбран из согласно способу, указанному на схеме 5. Схема 5 Соответственно этому подходящим образом замещенное соединение формулы (XVIII), известное соединение или соединение, полученное известными методами, активируют согласно известному методу, получая при этом соответствующее соединение формулы (XIX), где J2 представляет собой подходящую уходящую группу, такую как тозилат, Cl, Br, J, мезилат, трифлат и т.п. Соединение формулы (XIX) подвергают взаимодействию с фталимидной солью, такой как фталимид калия, фталимид натрия и т.п., в органическом растворителе, таком как ДМФА, ДМСО, ацетонитрил и т.п., предпочтительно при повышенной температуре в диапазоне от 50 до приблизительно 200 С, более предпочтительно приблизительно при температуре флегмы, получая при этом соответствующее соединение формулы (XX). Соединение формулы (XX) подвергают взаимодействию с N2H4, известным соединением, в органическом растворителе, таком как этанол, метанол и тому подобное, предпочтительно, при повышенной температуре в диапазоне от приблизительно 50 С до приблизительно 100 С, более предпочтительно,приблизительно при температуре флегмы и тому подобное, получая при этом соответствующее соединение формулы (Xd). выбран Специалисту в данной области должно быть очевидно, что соединения формулы (X), где можно подобным образом получить согласно известным методам или, например, согласно способам,указанным в приведенных выше схемах 2-5, выбором и заменой соответствующих бензоконденсированных соединений нафтилконденсированными соединениями. Специалисту в данной области далее будет очевидно, что когда требуется индивидуальный энантиомер (или смесь энантиомеров, которая обогащена одним энантиомером) соединения формулы (X),можно применять указанные выше способы, описываемые в схемах 1-5, заменой подходящего исходного соединения соответствующим индивидуальным энантиомером (или смесью энантиомеров, которая обогащена одним энантиомером). Специалисту в данной области будет очевидно, что когда стадию реакции настоящего изобретения можно проводить в различных растворителях или системах растворителей, указанную стадию реакции можно также проводить в смеси подходящих растворителей или систем растворителей. Когда способы получения соединений согласно изобретению дают смесь стереоизомеров, эти изомеры можно разделить общепринятыми методиками, такими как препаративная хроматография. Соеди-9 015962 нения можно получить в рацемической форме, или индивидуальные энантиомеры можно получить либо энантиоспецифическим синтезом, либо разделением. Соединения можно, например, разделить на их энантиомерные компоненты стандартными методиками, такими как образование диастереомерных пар образованием соли с оптически активной кислотой, такой как (-)-ди-п-толуоил-D-винная кислота и/или(+)-ди-п-толуоил-L-винная кислота, с последующей фракционной кристаллизацией и регенерацией свободного основания. Соединения можно также разделить образованием диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного вещества. В альтернативном случае соединения можно разделить с применением хиральной колонки ВЭЖХ. В процессе получения соединений настоящего изобретения любым из способов может быть необходимо и/или желательно защитить чувствительные или реакционноспособные группы у любой из рассматриваемых молекул. Этого можно достичь при помощи общепринятых защитных групп, таких как защитные группы, описанные в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press,1973 и T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons, 1991. Защитные группы можно удалить на пригодной последующей стадии с применением методов, известных в данной области. Способ лечения злоупотребления алкоголем и/или аддикции, описанный в настоящем изобретении,можно также проводить с применением фармацевтической композиции, включающей любое из описываемых здесь соединений и фармацевтически приемлемый носитель. Фармацевтическая композиция может содержать между приблизительно 0,1 и 1000 мг, предпочтительно приблизительно 50-500 мг соединения и может быть преобразована в любую форму, подходящую для выбранного метода введения. Носители включают необходимые и инертные фармацевтические эксципиенты, включающие, но не ограничивающиеся перечисленным, связывающие вещества, суспендирующие агенты, смазывающие вещества,корригенты, подслащивающие вещества, консерванты, красители и покрытия. Композиции, подходящие для перорального введения, включают твердые формы, такие как пилюли, таблетки, мелкие капсулы,капсулы (причем каждая такая форма включает препараты с немедленным высвобождением, регулируемым во времени высвобождением и стойко поддерживаемым высвобождением), гранулы и порошки, и жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, применимые для парентерального введения, включают стерильные растворы, эмульсии и суспензии. Соединения настоящего изобретения можно вводить преимущественно в виде разовой суточной дозы или общую суточную дозу можно вводить в виде разделенных доз два, три или четыре раза в день. Кроме того, соединения настоящего изобретения можно вводить в интраназальной форме посредством местного применения подходящих интраназальных устройств или посредством трансдермальных кожных пластырей, хорошо известных среднему специалисту в данной области. При введении в форме системы для трансдермальной доставки введение дозы будет, конечно, непрерывным, а не прерывистым на всем протяжении схемы приема лекарственного средства. Например, для орального введения в форме таблетки или капсулы активный лекарственный компонент можно комбинировать с оральным, нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и т.п. Кроме того, когда желательно или необходимо, в смесь можно также включить подходящие связывающие вещества; смазывающие вещества, дезинтегрирующие агенты и окрашивающие агенты. Подходящие связывающие вещества включают, без ограничения, крахмал, желатин, природные сахара, такие как глюкоза или -лактоза, кукурузные подслащивающие вещества, природные и синтетические камеди, такие как аравийская камедь, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтеграторы включают, без ограничения, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п. Жидкие формы содержат включающие подходящие корригенты ароматизирующие суспендирующие или диспергирующие агенты, такие как синтетические и природные камеди, например трагакант,аравийская камедь, метилцеллюлоза и т.п. Для парентерального введения желательными являются стерильные суспензии и растворы. Изотонические препараты, которые обычно содержат подходящие консерванты, применяют, когда желательным является внутривенное введение. Соединения данного изобретения можно вводить в любой из вышеуказанных композиций и согласно схемам приема лекарственного средства, установленным в данной области, всегда, когда требуется лечение злоупотребления алкоголем и/или аддикции. Суточная доза продуктов может варьировать на протяжении широкого диапазона от 0,01 до 150 мг/кг для взрослого человека в день. Для орального введения композиции предпочтительно предоставляют в форме таблеток, содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200,250, 500 и 1000 мг активного ингредиента для симптоматической регулировки дозы для подвергаемого лечению пациента. Эффективное количество лекарственного средства обычно доставляют в организм при уровне дозы от приблизительно 0,1 до приблизительно 1500 мг/кг массы тела в день. Предпочтительно диапазон составляет от приблизительно 0,1 до приблизительно 100,0 мг/кг массы тела в день, более предпочтительно от приблизительно 0,5 до приблизительно 50 мг/кг массы тела в день, наиболее предпочтительно от приблизительно 1,0 до приблизительно 25,0 мг/кг массы тела в день. Соединения- 10015962 можно вводить по схеме введения 1-4 раза в день. Оптимальные дозы, которые нужно ввести, может легко определить специалист в данной области,они будут варьировать в зависимости от конкретного применяемого соединения, способа введения; активности препарата и успеха в улучшении патологического состояния. Кроме того, факторы, связанные с конкретным, подвергаемым лечению пациентом и включающие возраст, массу, диету пациента и время введения, могут привести к необходимости регулировки доз. Специалист в данной области должен знать, что испытания in vivo и in vitro с применением подходящих, известных и обычно приемлемых клеточных и/или животных моделей предсказывают способность испытуемого соединения лечить или предотвращать данное нарушение. Специалист в данной области далее должен понимать, что клинические испытания с участием человека, включающие сначала испытания на диапазон и эффективность доз для здоровых пациентов и/или пациентов, страдающих данным нарушением, можно выполнять согласно методам, хорошо известным в клинических и медицинских областях. Нижеследующие примеры предложены для облегчения понимания изобретения и не предназначены и не должны истолковываться как ограничение любым путем изобретения, изложенного в формуле изобретения, которая приведена ниже. Пример 1. 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил]метил)сульфамид (соединение 3). Катехин (5,09 г, 46,2 ммоль) и карбонат калия смешивают в ацетонитриле и нагревают при температуре рефлюкса в течение 1 ч. Добавляют 2-хлорметил-3-хлор-1-пропен (5,78 г, 46,2 ммоль) и проведение реакции продолжают при температуре рефлюкса в течение 24 ч. Раствор охлаждают до комнатной температуры и фильтруют. Фильтрат упаривают и остаток разбавляют водой и экстрагируют диэтиловым эфиром (3). Объединенный органический раствор сушат над MgSO4 и концентрируют. Хроматография(2% этиловый простой эфир в гексане) дает 3-метилен-3,4-дигидро-2 Н-бензо[b][1,4]диоксепин в виде бесцветного масла. МС (ESI): 163,2 (М+Н+). 1(100 мл). При 0 С добавляют комплекс боран-ТГФ (1,0 М в ТГФ, 10,3 мл). Реакционную смесь перемешивают при RT в течение 5 ч. Добавляют аминосульфоновую кислоту (6,97 г, 61,6 ммоль). Реакционную смесь нагревают при температуре рефлюкса на протяжении ночи. Реакционную смесь охлаждают до комнатной температуры и добавляют водный гидроксид натрия (3,0 М, 100 мл). Раствор экстрагируют этилацетатом (3100 мл). Объединенный органический раствор сушат над MgSO4. Раствор концентрируют в вакууме и очищают хроматографией (2-8% метанол в дихлорметане), получая при этом 3,4 дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)амин в виде бесцветного масла. МС (ESI): 180,1 (М+Н+). 1H ЯМР (300 МГц, ДМСО), : 6,92 (м, 4 Н), 4,21 (м, 2 Н), 4,07 (м, 2 Н), 3,33 (ушир., 2 Н), 3,16 (д, J=4 Гц, 1 Н), 2,72 (д, J=4 Гц, 1 Н), 2,30 (м, 1 Н). 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил]метил)амин (2,90 г, 16,2 ммоль) и сульфамид (3,11 г,32,4 ммоль) смешивают в сухом диоксане (60 мл) и нагревают при температуре рефлюкса на протяжении ночи. Добавляют хлороформ и осадок удаляют фильтрованием. Фильтрат концентрируют в вакууме и очищают хроматографией (2-8% ацетон в дихлорметане), получая при этом указанное в заголовке соединение в виде беловатого твердого вещества. МС 258,8 (М+Н+). 1 Рацемический 2,3-дигидро-1,4-бензодиоксин-2-илметиламин (4,4 г, 26 ммоль) и сульфамид (5,1 г,53 ммоль) смешивают в 1,4-диоксане (100 мл) и нагревают при температуре рефлюкса в течение 2 ч. Реакционную смесь охлаждают до комнатной температуры и небольшое количество твердого вещества отделяют фильтрованием и удаляют. Фильтрат упаривают в вакууме и остаток очищают с применением колоночной флэш-хроматографии (DCM:метанол - 10:1), получая при этом белое твердое вещество. Твердое вещество перекристаллизовывают из DCM, получая при этом указанное в заголовке соединение- 11015962 в виде белого твердого вещества. Т. пл.: 97,5-98,5 С. Элементный анализ: Вычисл.: С, 44,25; Н, 4,95; N, 11,47; S, 13,13. Найдено: С, 44,28; Н, 4,66; N, 11,21; S, 13,15. 1 Катехин (10,26 г, 93,2 ммоль), метоксид натрия (25 мас.% в метаноле, 40,3 г, 186 ммоль) и метилдихлорацетат (13,3 г, 93,2 ммоль) смешивают в сухом метаноле (100 мл). Раствор нагревают при температуре рефлюкса на протяжении ночи. Реакционную смесь охлаждают до комнатной температуры, подкисляют добавлением концентрированной хлористо-водородной кислоты и затем объем ее уменьшают в вакууме приблизительно до 50 мл. Добавляют воду и смесь экстрагируют диэтиловым простым эфиром(3100 мл). Объединенный органический раствор сушат MgSO4, концентрируют до получения коричневого твердого вещества и хроматографируют (2% этилацетат в гексане), получая при этом метиловый эфир бензо[1,3]диоксол-2-карбоновой кислоты в виде бесцветного масла. МС (ESI): 195,10 (М+Н+). 1H ЯМР (300 МГц, CDCl3) : 6,89 (ушир., 4 Н), 6,29 (с, 1 Н), 4,34 (кв, J=7 Гц, 2 Н), 1,33 (т, J=7 Гц, 3 Н). К метиловому эфиру бензо[1,3]диоксол-2-карбоновой кислоты (7,21 г, 40,0 ммоль) добавляют гидроксид аммония (29% в воде, 10 мл) и достаточное количество ацетонитрила для получения гомогенной смеси (5 мл). Раствор перемешивают в течение 2 ч при комнатной температуре и затем добавляют дистиллированную воду. Амид бензо[1,3]диоксол-2-карбоновой кислоты, осажденный в виде белого твердого вещества, собирают фильтрованием и применяют без дополнительной очистки. МС (ESI): 160,00 (М+Н+). 1(ТГФ, 100 мл). К раствору при комнатной температуре медленно добавляют литийалюминийгидрид(LAH, 1M в ТГФ, 39,5 мл, 39,5 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 24 ч. Для разрушения избыточного LAH добавляют дистиллированную воду. Добавляют водный гидроксид натрия (3,0 М, 100 мл) и раствор экстрагируют этилацетатом (3100 мл). Объединенный органический раствор промывают водой и сушат над MgSO4. Растворитель выпаривают, получая при этом Сбензо[1,3]диоксол-2-илметиламин в виде бесцветного масла. МС (ESI): 152,1 (М+Н+). 1H ЯМР (300 МГц, CDCl3) : 6,87 (м, 4 Н), 6,09 (т, J=4 Гц, 1 Н), 3,13 (д, J=4 Гц, 2 Н). С-Бензо[1,3]диоксол-2-илметиламин (2,94 г, 19,4 ммоль) и сульфамид (3,74 г, 38,9 ммоль) смешивают в сухом диоксане (50 мл) и раствор нагревают при температуре рефлюкса на протяжении ночи. Реакционную смесь концентрируют и остаток хроматографируют (2-10% ацетон в дихлорметане), получая при этом указанное в заголовке соединение в виде белого твердого вещества. МС (ESI): 230,0 (М+Н+). 1 Катехин (13,2 г, 0,12 ммоль) и карбонат калия (16,6 г, 0,12 моль) перемешивают в ДМФА (250 мл) и добавляют (2R)-глицидилтозилат (22,8 г, 0,10 моль) и реакционную смесь перемешивают при 60 С в течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и разбавляют ледяной водой (1 л) и экстрагируют диэтиловым эфиром (4 раза). Объединенный органический раствор промывают 3 раза 10% карбонатом калия, один раз водой, один раз насыщенным раствором соли и упаривают в вакууме,получая при этом белое твердое вещество, которое очищают колоночной флэш-хроматографией(DCM:метанол - 50:1), получая при этом 2S)-2,3-дигидробензо[1,4]диоксин-2-ил)метанол в виде твердого вещества. Твердое вещество (13,3 г, 68 ммоль) растворяют в пиридине (85 мл), охлажденном до 0 С, добав- 12015962 ляют п-толуолсульфонилхлорид (13,0 г, 68 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь разбавляют диэтиловым эфиром (1 л) и 1 н. HCl (1,2 л). Органический слой отделяют и промывают 2 раза 1 н. HCl (500 мл), 4 раза водой (150 мл), один раз насыщенным раствором соли, сушат (MgSO4) и упаривают в вакууме, получая при этом белое твердое вещество, которое очищают колоночной флэш-хроматографией (гептан:ЕА - 2:1), получая при этом (2S)2,3-дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты в виде белого твердого вещества. Белое твердое вещество смешивают с фталимидом калия (14,4 г; 7 8 ммоль) в ДМФ (250 мл) и нагревают при температуре рефлюкса в течение 1 ч, охлаждают до комнатной температуры и выливают в энергично перемешиваемую воду (1,5 л) и перемешивают 30 мин. Белое твердое вещество отделяют фильтрованием и твердое вещество промывают несколько раз водой, 2% NaOH и снова водой и оставляют для сушки на воздухе, получая при этом (2S)-2-(2,3-дигидробензо[1,4]диоксин-2-илметил)изоиндол 1,3-дион в виде белого порошкообразного твердого вещества. Порошкообразное белое твердое вещество смешивают с гидразином (2,75 г, 86 ммоль) в EtOH (225 мл) и нагревают при температуре рефлюкса в течение 2 ч, охлаждают до комнатной температуры и добавляют 1 н. HCl до рН 1,0 и перемешивают в течение 15 мин. Белое твердое вещество отделяют фильтрованием и промывают свежим EtOH (твердое вещество удаляют) и фильтрат упаривают в вакууме до получения твердого вещества, которое распределяют между диэтиловым простым эфиром и разбавленным водным NaOH. Раствор в диэтиловом эфире сушат (Na2SO4) и упаривают в вакууме, получая при этом светло-желтое масло. Масло очищают колоночной флэш-хроматографией (DCM:MeOH - 10:1), получая при этом масло. Часть масла (4,82 г, 29 ммоль) в 2-пропаноле (250 мл) обрабатывают 1 н. HCl (30 мл) и нагревают на паровой бане до достижения гомогенности и затем дают ему возможность охладиться до комнатной температуры. Спустя 3 ч смесь охлаждают льдом в течение 2 ч. Белое хлопьевидное твердое вещество (соответствующая соль HCl (2S)-C-(2,3-дигидробензо[1,4]диоксин-2-ил)метиламина) отделяют фильтрованием и затем снова перекристаллизовывают из 2-пропанола, получая при этом белое твердое вещество.[]D = -69,6 (с=1,06, EtOH). Белое твердое вещество распределяют между DCM и разбавленным NaOH и слой DCM сушат(Na2SO4) и упаривают в вакууме, получая при этом (2S)-С-(2,3-дигидробензо[1,4]диоксин-2-ил) метиламин в виде масла.[]D=-57,8 (с=1,40, CHCl3). Масло (2,1 г, 12,7 ммоль) и сульфамид (2,44 г, 25,4 ммоль) нагревают при температуре рефлюкса в диоксане (75 мл) в течение 2 ч и сырой продукт очищают колоночной флэш-хроматографией(DCM:MeOH, 10:1), получая при этом белое твердое вещество, которое перекристаллизовывают из DCM,получая при этом указанное в заголовке соединение в виде белого кристаллического твердого вещества. Т. пл. 102-103 С. Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (8,25 г, 5,0 ммоль) и триэтиламин (1,52 г, 15 ммоль) смешивают в ДМФ (10 мл) охлаждают на ледяной бане, когда добавляли диметилсульфамоилхлорид (1,44 г, 10 ммоль). Реакционную смесь затем перемешивают в течение 3 ч с продолжением охлаждения. Реакционную смесь распределяют между этилацетатом и водой и раствор в этилацетате промывают насыщенным раствором соли, сушат (MgSO4) и упаривают в вакууме, получая при этом масло. Масло очищают с применением колоночной флэш-хроматографии (этилацетат:гептан - 1:1), получая при этом белое твердое вещество, которое перекристаллизовывают (этилацетат/гексан), получая при этом указанное в заголовке соединение в виде белого хлопьевидного твердого вещества. Т. пл. 76-78 С. МС 273 (МН+). Элементный анализ: Вычисл.: С, 48,52; Н, 5,92; N, 10,29; S, 11,78. Найдено: С, 48,63; Н, 5,62; N, 10,20; S, 11,90. Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (825 мг, 5 ммоль) растворяют в этилформиате (15 мл), раствор нагревают при температуре рефлюкса в течение 30 мин и упаривают в вакууме, получая при этом N-(2,3-дигидробензо[1,4]диоксин-2-илметил)формамид в виде масла. Масло в диэтиловом эфире (25 мл) обрабатывают 1 М LAH в ТГФ (9,0 мл, 9,0 ммоль) при 0 С и перемешивают в течение 5 ч при комнатной температуре. Реакционную смесь охлаждают на ледяной бане и гасят водой (0,50 мл) с последующим гашением 3 н. NaOH (0,50 мл) и водой (0,50 мл). Смесь затем перемешивают при комнатной температуре в течение 1 ч. Твердое вещество отделяют фильтрованием и фильтрат упаривают в вакууме, получая при этом остаток, который распределяют между 1 н. HCl и диэтиловым эфиром. Водную фазу делают основной 1 н. NaOH и экстрагируют диэтиловым эфиром. Органическую фазу сушат (MgSO4) и упаривают в вакууме, получая при этом (2,3-дигидробензо[1,4]диоксин 2-илметил)метиламин в виде масла. МС 180 (МН+). 1H ЯМР (CDCl3) : 6,85 (м, 4 Н), 4,30 (м, 2 Н), 4,02 (дд, J=7,9, 11,6 Гц, 1 Н), 2,85 (м, 2 Н), 2,50 (с, 3 Н). Масло (380 мг, 2,1 ммоль) и сульфамид (820 мг, 8,5 ммоль) смешивают в диоксане (15 мл), смесь нагревают при температуре рефлюкса в течение 1,5 ч и упаривают в вакууме, получая при этом неочищенный остаток. Остаток очищают колоночной хроматографией (зтилацетат/гептан, 1:1) и образовавшееся твердое вещество перекристаллизовывают из смеси этилацетат/гексан, получая при этом указанное в заголовке соединение в виде белого твердого вещества. Т. пл. 97-98 С. МС 257 (М-1). Элементный анализ: Вычисл.: С, 46,50; Н, 5,46; N, 10,85; S, 12,41. Найдено: С, 46,48; Н, 5,65; N, 10,90; S, 12,07. 1 По методике, описанной в приведенном выше примере 4, 4-хлоркатехин подвергают реакции, получая при этом смесь (2S)-C-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламина и (2S)-C-(6-хлор-2,3 дигидробензо[1,4]диоксин-2-ил)метиламин (отношение изомеров 6-хлор:7-хлор по данным ОФ ВЭЖХ приблизительно 3:1). Смесь растворяют в 2-пропаноле (100 мл) и добавляют 1 н. HCl в диэтиловом эфире до достижения рН 1,0. Гидрохлоридную соль, которая осаждается, отделяют фильтрованием (2,65 г) и перекристаллизовывают из смеси метанол/IPA, получая при этом белые кристаллы. Белые кристаллы распределяют между DCM и разбавленным NaOH. Слой DCM сушат и упаривают в вакууме, получая при этом очищенный[]D=-67,8 (с=1,51, CHCl3). Масло (7,75 ммоль) и сульфамид (1,50 г, 15,5 ммоль) смешивают в диоксане (50 мл) и нагревают при температуре рефлюкса в течение 2,0 ч, охлаждают до комнатной температуры и упаривают в вакууме, получая при этом твердое вещество. Продукт очищают при помощи колоночной флэшхроматографии с применением смеси DCM/метанол, 20:1, получая при этом указанное в заголовке соединение в виде белого твердого вещества. МС 277 (М-1).(дд, J=2,4, 11,5 Гц, 1 Н), 4,05 (дд, J=7,l, 11,5 Гц, 1 Н), 3,45 (м, 2 Н). Элементный анализ: Вычисл.: С, 38,78; Н, 3,98; N, 10,05. Найдено: С, 38,80; Н, 3,67; N, 9,99. Фильтраты кристаллизованной гидрохлоридной соли (2S)-C-(6-хлор-2,3-дигидробензо[1,4]диоксин- 14015962 2-ил)метиламина, полученные, как указано выше, отделяют (отношение изомеров 6-хлор:7-хлор приблизительно 1:1) и упаривают в вакууме, получая при этом твердое вещество, которое распределяют междуDCM (200 мл) и разбавленным NaOH (0,5 М, 50 мл). Раствор в DCM промывают один раз насыщенным раствором соли, сушат (Na2SO4) и упаривают в вакууме, получая при этом масло, которое очищают при помощи ВЭЖХ с обращенной фазой (10-50% ACN с 0,16% TFA в воде с 0,20% TFA), получая при этом(2S)-С-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламин в виде остатка. Остаток смешивают с сульфамидом (0,90 г, 9,4 ммоль) в диоксане (25 мл) и нагревают при температуре рефлюкса в течение 2,5 ч, охлаждают до комнатной температуры и упаривают в вакууме, получая при этом масло. Масло очищают колоночной флэш-хроматографией с применением смеси DCM/метанол 10:1, получая при этом (2S)-(-)-N-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид в виде белого твердого вещества. МС 277 (М-1). 1 Хроман-2-карбоновую кислоту (4,5 г, 25 ммоль) и НОВТ (3,86 г, 25 ммоль) смешивают в DCM (40 мл) и ДМФА (10 мл). При комнатной температуре добавляют диметиламинопропилэтилкарбодиимид(EDC, 4,84 г, 25 ммоль) и реакционную смесь перемешивают в течение 30 мин. Добавляют гидроксид аммония (2,26 мл, 33,4 ммоль) и реакционную смесь перемешивают в течение 16 ч. Реакционную смесь разбавляют DCM (50 мл) и водой (50 мл) и рН смеси регулируют до приблизительно рН 3,0 1 н. HCl. Фазу DCM отделяют и водную фазу экстрагируют DCM. Объединенные фазы DCM сушат (Na2SO4) и упаривают в вакууме, получая при этом масло, которое очищают колоночной флэш-хроматографией (этилацетат), получая при этом масло. Масло (5,35 г, 30 ммоль) в ТГФ (90 мл) перемешивают, когда добавляют 1 М LAH в ТГФ (36 мл, 36 ммоль), и реакционную смесь затем перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь гасят водой, перемешивают в течение 2 ч, раствор декантируют, сушат (Na2SO4) и упаривают в вакууме, получая при этом С-хроман-2-илметиламин в виде масла. Полученный в виде масла амин (1,63 г, 10 ммоль) и сульфамид (1,92 г, 20 ммоль) смешивают в диоксане (50 мл) и доводят до температуры рефлюкса в течение 2 ч. Раствор охлаждают и упаривают в вакууме, получая при этом масло, которое очищают посредством колоночной хроматографии(DCM:метанол, 10:1), получая при этом белое твердое вещество. Твердое вещество перекристаллизовывают из смеси этилацетат/гексан, получая при этом хроман-2-илметилсульфамид в виде белого твердого вещества. Т. пл. 100-101 С. МС 241 (M-1). Элементный анализ: Вычисл.: С, 49,57; Н, 5,82; N, 11,56; S, 13,23. Найдено: С, 49,57; Н, 5,80; N, 11,75; S, 13,33. Пример 9. 2-(2,3-Дигидробензо[1,4]диоксин-2-ил)этилсульфамид (соединение 16). Цианид калия (2,05 г, 31,5 ммоль) добавляют к 2-бромметил-(2,3-дигидробензо[1,4]диоксину) (6,87 г, 30 ммоль) в ДМСО (90 мл) и перемешивают при температуре окружающей среды в течение 20 ч. Реакционную смесь затем разбавляют водой (250 мл) и дважды экстрагируют диэтиловым эфиром. Экстракт в диэтиловом эфире промывают водой, затем дважды промывают насыщенным раствором соли, сушат(Na2SO4) и упаривают в вакууме, получая при этом 2-цианометил-(2,3-дигидробензо[1,4]диоксин) в виде белого твердого вещества. 1H ЯМР (CDCl3)6,89 (м, 4 Н), 4,50 (м, 1 Н), 4,31 (дд, J=2,3, 11,5 Гц, 1 Н), 4,08 (дд, J=6,2, 11,6 Гц,1 Н), 2,78 (д, J=6,1, Гц, 2 Н). 2-Цианометил-(2,3-дигидробензо[1,4]диоксин) растворяют в ТГФ (50 мл) и добавляют 1 М ВН 3 в ТГФ (80 мл, 80 ммоль) и реакционную смесь нагревают при температуре рефлюкса в течение 5 ч, затем перемешивают при температуре окружающей среды в течение 16 ч. При охлаждении на ледяной бане добавляют 2 н. HCl до достижения рН 1,0. Реакционную смесь затем перемешивают в течение 1 ч при комнатной температуре и упаривают в вакууме, получая при этом масло. Масло распределяют между 3 н.NaOH и диэтиловым эфиром и раствор в диэтиловом эфире промывают насыщенным раствором соли,- 15015962 сушат (Na2SO4) и упаривают в вакууме, получая при этом неочищенный 2-(2,3-дигидробензо[1,4]диоксин-2-ил)этиламин. МС (М+Н)+ 180. Неочищенный 2-(2,3-дигидробензо[1,4]диоксин-2-ил)этиламин в диоксане (100 мл) смешивают с сульфамидом (3,0 г, 31 ммоль) и нагревают при температуре рефлюкса в течение 2 ч. Раствор охлаждают и упаривают в вакууме с получением оранжевого твердого вещества, которое очищают колоночной хроматографией (DCM:MeOH - 10:1), получая при этом белое твердое вещество. Твердое вещество перекристаллизовывают из DCM, получая при этом указанное в заголовке соединение в виде твердого вещества. МС (М-1) 257. Т. пл. 101-103 С (с поправкой). 1(200 мл). Добавляют (2R)-глицидилтозилат (9,12 г, 40 ммоль) и реакционную смесь перемешивают при 60 С в течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и затем разбавляют ледяной водой (600 мл) и экстрагируют диэтиловым эфиром (4 раза). Объединенный органический раствор промывают 3 раза 10% карбонатом калия, два раза насыщенным раствором соли, сушат (MgSO4) и упаривают в вакууме, получая при этом вязкое масло (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин)метанола.(2S)-2-(6,7-Дихлор-2,3-дигидробензо[1,4]диоксин)метанол в виде масла (6,4 г, 27 ммоль) растворяют в пиридине (50 мл), охлажденном до 0 С. Затем добавляют п-толуолсульфонилхлорид (5,2 г, 27 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь разбавляют диэтиловым эфиром и 1 н. HCl (750 мл) и органический слой отделяют и промывают 2 раза 1 н. HCl (250 мл), один раз водой (150 мл), два раза насыщенным раствором соли, сушат (MgSO4) и упаривают в вакууме, получая при этом (2S)-6,7-дихлор-2,3-дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты в виде светло-желтого твердого вещества. 1(2S)-6,7-Дихлор-2,3-дигидробензо[1,4]диоксин)-2-илметиловый эфир толуол-4-сульфоновой кислоты (8,0 г, 20,5 ммоль) смешивают с фталимидом калия (6,1 г, 33 ммоль) в ДМФА (75 мл) и нагревают при температуре рефлюкса в течение 1 ч, охлаждают до комнатной температуры и выливают в энергично перемешиваемую воду (0,5 л) и затем перемешивают 30 мин. Белое твердое вещество отделяют фильтрованием и твердое вещество промывают несколько раз водой, 2% NaOH и снова водой и затем оставляют для сушки на воздухе, получая при этом (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин)-2 илметил)изоиндол-1,3-дион (6,0 г, 80%) в виде белого порошковидного твердого вещества. Белое порошковидное твердое вещество смешивают с гидразином (1,06 г, 33 ммоль) в EtOH (80 мл) и нагревают при температуре рефлюкса в течение 2 ч, затем охлаждают до комнатной температуры. Добавляют 1 н. HCl для регулирования рН реакционной смеси до рН 1,0 и реакционную смесь затем перемешивают в течение 15 мин. Белое твердое вещество отделяют фильтрованием и промывают свежимEtOH (твердое вещество удаляют) и фильтрат упаривают в вакууме до получения твердого вещества,которое распределяют между диэтиловым эфиром и разбавленным водным NaOH. Раствор в диэтиловом эфире сушат (Na2SO4) и упаривают в вакууме, получая при этом (2S)-2-аминометил-(6,7-дихлор-2,3 дигидробензо[1,4]диоксин) в виде вязкого масла. 1H ЯМР (CDCl3):6,98 (с, 1 Н), 6,96 (с, 1 Н), 4,25 (дд, J=2,0, 11,2 Гц, 1 Н), 4,15 (м, 1 Н), 4,0 (м, 1 Н),2,97 (д, J=5,5 Гц, 2 Н). Часть масла (3,8 г, 16 ммоль) и сульфамид (3,1 г, 32,4 ммоль) в диоксане (100 мл) нагревают при температуре рефлюкса в течение 2 ч и сырой продукт очищают колоночной флэш-хроматографией(DCM:MeOH, 20:1), получая при этом указанное в заголовке соединение в виде белого твердого вещества, которое перекристаллизовывают из смеси этилацетат/гексан, получая при этом указанное в заголовке соединение в виде белого кристаллического твердого вещества. МС [М-H]- 311,0. Т. пл. 119-121 С. Указанное в заголовке соединение получают согласно методике, описанной выше в примере 4, исходя из 4-метилкатехина, в виде белого твердого вещества, которое перекристаллизовывают из смеси этилацетат/гексан, получая при этом указанное в заголовке соединение в виде белого твердого вещества. МС [М-Н]- 257. 1H ЯМР (CDCl3):6,76 (м, 1 Н), 6,66 (м, 2 Н), 4,80 (м, 1 Н), 4,57 (ушир. с, 1 Н), 4,40 (м, 1 Н), 4,28 (м,1 Н), 4,03 (дд, J=6,9, 11,4 Гц, 1 Н), 3,45 (м, 2 Н), 2,25 (с, 3 Н). Элементный анализ: Вычисл.: С, 46,50; Н, 5,46; N, 10,85; S, 12,41. Найдено: С, 46,65; Н, 5,60; N, 10,84; S, 12,61. Пример 13. Предпочитающие алкоголь крысы в модели in vivo. Взрослые самцы селективно выведенных предпочитающих алкоголь крыс (которые, как известно в данной области, являются пригодными для изучения действия испытуемых соединений на потребление алкоголя) делили на три группы для введения наполнителя и соединения 8 (50 и 100 мг/кг, перорально). Крыс помещали по отдельности в проволочные клетки с ячейками при постоянной комнатной температуре 221 С и цикле свет-темнота 12:12 (8:00-20:00, темнота). Животным давали корм Agway ProlabRat/Mouse/Hamster 3000 formula и воду ad libitum. Потребление алкоголя определяли с применением стандартного метода выбора из двух бутылок. Животным сначала предоставляли свободный доступ к воде в градуированной трубке Рихтера в течение 2 дней. Затем у них был доступ только к раствору 10% (об./об.) этанола в течение 3 последовательных дней. В течение этого периода животные приучались к питью из трубок Рихтера и вкусу и фармакологическим действиям алкоголя. После этого им предоставляли свободный доступ как к воде, так и раствору 10% алкоголя в течение по меньшей мере 4 последовательных недель и на всем протяжении периода изучения. Крысы имели свободный доступ к пище. Потребление воды и алкоголя регистрировали через 4, 6 и 24 ч после обработки, тогда как потребление корма измеряли через 24 ч. Массу тела животных измеряли каждый день. После установления стабильной базовой линии для потребления алкоголя, пищи и воды крысам вводили либо наполнитель, либо соединение 8 посредством желудочного зонда для кормления с применением программы рандомизированного испытания с перекрестным распределением. Чтобы была возможность сравнения эффективности действия этих соединений на потребление алкоголя с разработанным, FDA-одобренным лекарственным средством, в позитивный контроль включали налтрексон. Некоторым крысам давали оральную дозу налтрексона (20 мг/кг). Интервал между обработками был по меньшей мере 3 дня. Потребление алкоголя и воды регистрировали через 4, 6 и 24 ч после введения лекарственного средства и потребление пищи регистрировали через 24 ч. Всего использовали 8-10 животных на группу. Указанные ниже результаты представлены как среднее значениеSEM (средне-квадратичное отклонение). Потребление алкоголя (г/кг) вычисляли умножением объема потребленного алкоголя в мл на 10% и 0,7893 (плотность этанола)/масса тела в кг. Предпочтение потребления алкоголя, выраженное в процентах, вычисляли следующим образом: (объем потребленного алкоголя в мл/общее потребление жидкости в мл)100 (Rezvani and Grady, 1994; Rezvani et al., 1997). Статистические различия между группами, обработанными лекарственным средством, и контрольными группами определяли с применением критерия ANOVA и Тэкки-Стьюдента для множественных сравнений. Как показано ниже в табл. 4, соединение 8 уменьшало потребление этанола предпочитающими алкоголь крысами через 6 ч (доза 50 и 100 мг/кг) после дозирования. Пример 14. В качестве конкретного варианта осуществления получения оральной композиции 100 мг соединения 8, полученного, как в примере 7, смешивают с достаточно тонко измельченной лактозой для получения общего количества смеси 580-590 мг для заполнения твердой желатиновой капсулы размера О. Хотя в приведенном выше описании указываются принципы настоящего изобретения вместе с примерами, представленными для цели иллюстрации, должно быть понятно, что практика изобретения включает все из обычных вариантов, адаптации и/или модификаций, как входящих в объем нижеследующей формулы изобретения и ее эквивалентов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения злоупотребления алкоголем или аддикции, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и C1-4 алкила;R4 выбран из группы, состоящей из водорода и C1-4 алкила; а равно 1 или 2; представляет собой где b равно целому числу от 0 до 4; каждый R5 независимо выбран из группы, состоящей из галогена и C1-4 алкила; или его фармацевтически приемлемой соли. 2. Способ по п.1, в котором вводят соединение формулы I,где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и C1-4 алкила;R4 выбран из группы, состоящей из водорода и C1-4 алкила; а равно 1 или 2; представляет собой,где b равно целому числу от 0 до 2; каждый R5 независимо выбран из группы, состоящей из галогена и С 1-4 алкила; или его фармацевтически приемлемую соль. 3. Способ по п.2, в котором вводят соединение формулы I, гдеR1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и С 1-4 алкила;R4 выбран из группы, состоящей из водорода и метила; а равно 1 или 2; выбран из группы, состоящей из 2-(2,3-дигидробензо[1,4]диоксинила),2-(6-хлор-2,3-дигидробензо[1,4]диоксинила),2-(6-фтор-2,3-дигидробензо[1,4]диоксинила),2-(5-фтор-2,3-дигидробензо[1,4]диоксинила),2-(7-хлор-2,3-дигидробензо[1,4]диоксинила),- 18015962 2-(7-метил-2,3-дигидробензо[1,4]диоксинила),2-(5-хлор-2,3-дигидробензо[1,4]диоксинила),2-(6-бром-2,3-дигидробензо[1,4]диоксинила),2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинила) и 2-(8-хлор-2,3-дигидробензо[1,4]диоксинила); или его фармацевтически приемлемую соль. 4. Способ по п.3, в котором вводят соединение формулы I,где R1 и R2 выбраны, каждый независимо, из группы, состоящей из водорода и метила;R4 выбран из группы, состоящей из водорода и метила; а равно 1 или 2; выбран из группы, состоящей из 2-(2,3-дигидробензо[1,4]диоксинила),2-(6-хлор-2,3-дигидробензо[1,4]диоксинила),2-(7-хлор-2,3-дигидробензо[1,4]диоксинила),2-(7-метил-2,3-дигидробензо[1,4]диоксинила),2-(6-бром-2,3-дигидробензо[1,4]диоксинила) и 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинила); или его фармацевтически приемлемую соль. 5. Способ по п.1, где соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор-2,3 дигидробензо[1,4]диоксин-2-илметил)сульфамид или его фармацевтически приемлемую соль. 6. Способ лечения злоупотребления алкоголем или аддикции, включающий введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид или его фармацевтически приемлемую соль.
МПК / Метки
МПК: A61K 31/353, A61P 25/30, A61P 25/36, A61P 25/34, A61K 31/357, A61P 25/32
Метки: алкоголем, лечения, способ, аддикции, злоупотребления
Код ссылки
<a href="https://eas.patents.su/20-15962-sposob-lecheniya-zloupotrebleniya-alkogolem-i-addikcii.html" rel="bookmark" title="База патентов Евразийского Союза">Способ лечения злоупотребления алкоголем и аддикции</a>
Предыдущий патент: Снижение электростатического заряда в способе полимеризации
Следующий патент: Способ непрерывного получения крупнокристаллических продуктов
Случайный патент: Способ изготовления термоэлектрических модулей и припой для его осуществления