Акрилоилзамещенные производные дистамицина, способы их получения, применение в качестве противоопухолевых средств и фармкомпозиции
Номер патента: 1863
Опубликовано: 22.10.2001
Авторы: Бериа Итало, Кальдарелли Марина, Францетти Кристина, Бьясоли Джованни, Коцци Паоло, Каполонго Лаура
Формула / Реферат
1. Акрилоилзамещенные производные дистамицина формулы
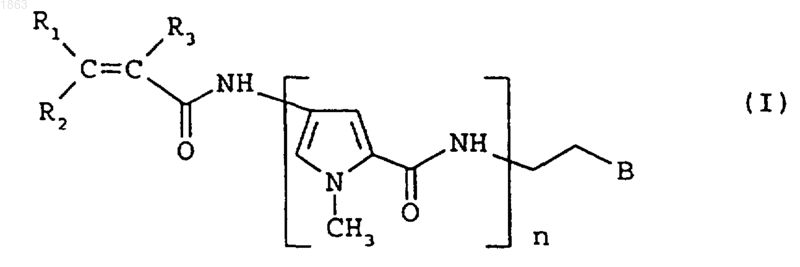
где n обозначает 2, 3 или 4;
R1 или R2 выбирают, каждый независимо, из водорода, галогена и C1-C4 алкила;
R3 обозначает водород или галоген;
В выбирают из
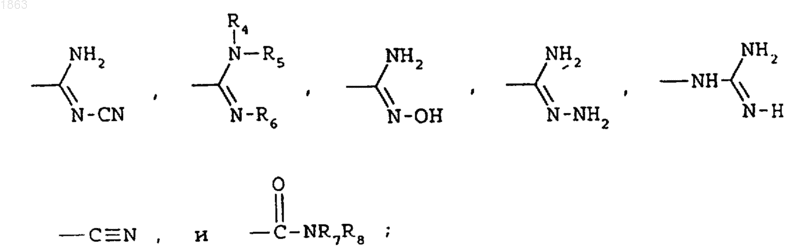
где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или C1-C4 алкил, при условии, что, по меньшей мере, один из R4, R5 и R6 обозначает C1-C4 алкил;
или их фармацевтически приемлемые соли.
2. Соединение по п.1, отличающееся тем, что n обозначает 3 или 4;
R1 и R2 oбозначают водород;
R3 обозначает хлор или бром;
В выбирают из
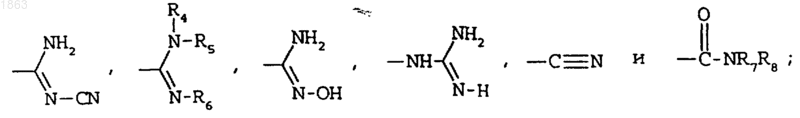
где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или метил, при условии, что, по крайней мере, один из R4, R5 и R6 обозначает метил;
или их фармацевтически приемлемые соли.
3. Соединение по п.1, отличающееся тем, что его выбирают из группы, включающей
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N-метиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N-метиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N-метиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N'-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N'-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N'-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бpoмакриламидо)пиррол-2-карбоксамидо)пиррол-2-каpбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим;
2-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)этилгуанидин;
2-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)этилгуанидин;
2-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)этилгуанидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионитрил;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионитрил;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионитрил;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-(4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N-метиламид;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a -бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N-метиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-N,N'-диметиламидин;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим;
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин и
3-(1-метил-4-(1-метил-4-(1-метил-4-(a -хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид и их фармацевтически приемлемые соли.
4. Способ получения соединения формулы (I) по п.1, который включает взаимодействие соединения формулы
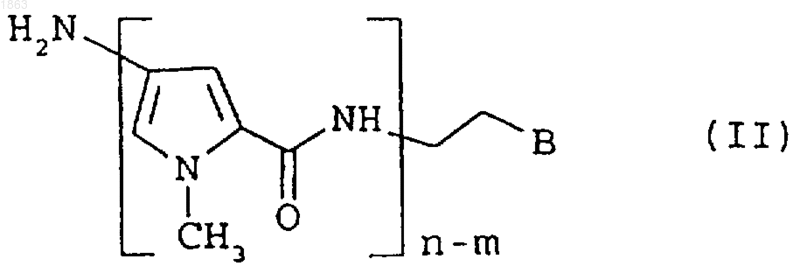
где n обозначает 2, 3 или 4;
m обозначает 0 или 1;
В выбирают из
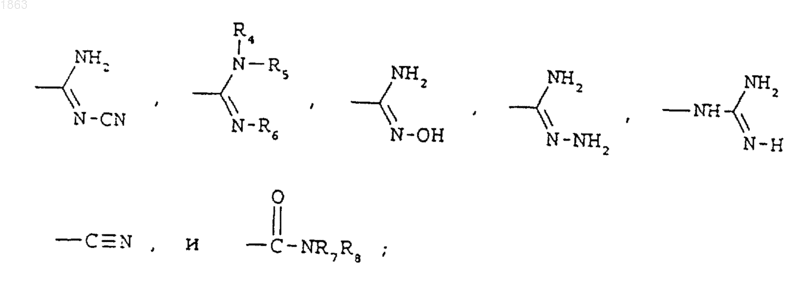
где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или C1-C4 алкил, при условии, что, по крайней мере, один из R4, R5 и R6 обозначает C1-C4 алкил;
с соединением формулы
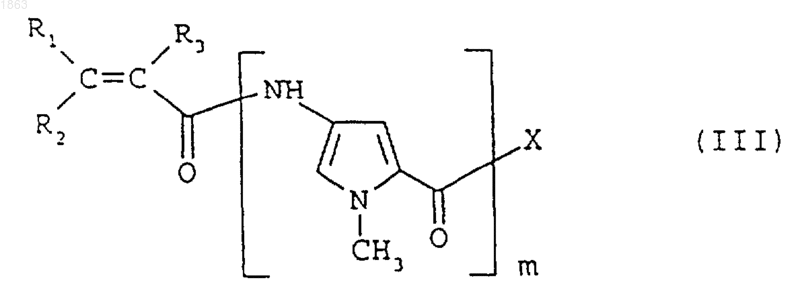
где R1 и R2 выбирают, каждый независимо, из водорода, галогена и C1-C4 алкила; R3 обозначает водород или галоген; Х обозначает гидрокси или удаляемую группу; а m имеет вышеуказанные значения; в присутствии основания и, если необходимо, превращение соединения формулы I в его фармацевтически приемлемую соль.
5. Способ получения соединения формулы (I) по п.1, где В обозначает -Cº N, который включает взаимодействие соединения формулы
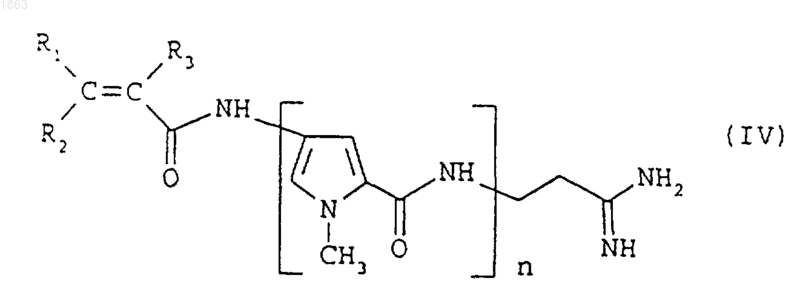
где n, R1, R2 и R3 такие, как определено выше;
с янтарным ангидридом в присутствии основания и, если необходимо, превращение соединения формулы (I) в его фармацевтически приемлемую соль.
6. Применение соединения по одному из пп.1-3 для получения лекарственного средства для лечения рака.
7. Фармацевтическая композиция, содержащая активно действующее вещество и фармацевтически приемлемые носители и/или разбавители, отличающаяся тем, что в качестве активно действующего вещества содержит эффективное количество соединения по пп.1-3.
Текст
Настоящее изобретение касается новых алкилированных противоопухолевых и противовирусных средств, относящихся к известному антибиотику дистамицину А который принадлежит к классу пирроламидиновых антибиотиков и о котором известно, что он взаимодействует обратимо и селективно с DNAAT-последовательностями, препятствуя как репликации, так и транскрипции [Nature, 203, 1064DE-А-1795539 описывает получение производных дистамицина, в которых формилгруппа дистамицина замещена водородом или кислотным остатком органической С 1-С 4 алифатической кислоты или циклопентилпропионовой кислоты. ЕР-В-246.868 описывает аналоги дистамицина, в которых формилгруппа дистамицина замещена ароматическим, алициклическим или гетероциклическим заместителями, несущими алкилированные группы. В международной патентной заявке WO 90/11277 описан широкий класс акрилоилзамещенных производных дистамицина, в которых акрилоил-радикал связан с кольцом пиррола посредством простой связи или через ароматическую или гетероциклическую группу дикарбоксамида. В настоящее время обнаружено, что новый класс производных дистамицина, определенных ниже, в которых формилгруппа дистамицина замещена акрилоил-радикалом, в то время как амидингруппа замещена различными азотсодержащими концевыми группами, обладает ценными биологическими свойствами. Таким образом, данное изобретение относится к новым производным дистамицина формулы (I), определенной ниже, к способу их получения, к содержащим их фармацевтическим композициям и к их применению в терапии,особенно в качестве противоопухолевых и противовирусных средств. Поэтому цель данного изобретения составляют акрилоилзамещенные производные дистамицина формулыR3 обозначает водород или галоген; В выбирают из где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или C1-C4 алкил, при условии,что, по меньшей мере, один из R4, R5 и R6 обозначает C1-C4 алкил; или их фармацевтически приемлемые соли. Объем изобретения включает также все возможные изомеры, охватываемые формулой(I), как раздельно, так и в форме их смеси, равно как мeтаболиты и фармацевтически приемлемые биопредшественники (иначе называемые пролекарствами) соединений формулы (I). Алкильные группы могут быть разветвленными или линейными. C1-C4 алкильная группа предпочтительно обозначает метил или этил. Атом галогена предпочтительно обозначает хлор, бром или фтор. Предпочтительно R4,R5, R6, R7 и R8 обозначают, каждый независимо,водород, метил или этил, при условии, что, по меньшей мере, один из R4, R5 и R6 обозначает метил или этил. Фармацевтически приемлемыми солями соединений формулы (I) являются их соли с фармацевтически приемлемыми, либо неорганическими, либо органическими кислотами. Примерами неорганических кислот служат хлористо-водородная, бромисто-водородная, серная и азотная кислоты, примерами органических кислот являются уксусная, пропионовая, янтарная, малоновая, лимонная, винная, метансульфоновая и п-толуолсульфоновая кислоты. Предпочтительным классом соединений согласно изобретению является тот класс формулы (I),где n обозначает 3 или 4;R3 обозначает хлор или бром; В выбирают из где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или метил, при условии, что,по меньшей мере, один из R4, R5 и R6 обозначает метил; или их фармацевтически приемлемые соли. Примерами конкретных соединений согласно изобретению, особенно в форме солей,предпочтительно с хлористо-водородной (соляной) кислотой, являются следующие:(30) 3-(1-метил-4-(1-метил-4-(1-метил-4(-хлоракриламидо)пиррол-2-карбоксамидо) пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид. Соединения формулы (I) и их соли согласно изобретению могут быть получены одним из следующих способов, которые включают где R1 и R2 выбирают, каждый независимо, из водорода, галогена и C1-C4 алкила; R3 обозначает водород или галоген; Х обозначает гидрокси или удаляемую группу; a m имеет вышеуказанные значения; или где n, R1, R2 и R3 - такие, как определено выше; с янтарным ангидридом, и, если необходимо, превращение соединения формулы (I) в его фармацевтически приемлемую соль. В соединениях формулы (III), X обозначает гидрокси или удаляемую группу, которую выбирают, к примеру, из хлор, 2,4,5-трихлорфенокси, 2,4-динитрофенокси, сукцинимидо-Nокси, имидазолилгруппы и тому подобных. Взаимодействие по способу (а) между соединением формулы (II) и соединением форму 001863 6 лы (III) может быть проведено согласно известным способам, к примеру, тем, что описаны в ЕР-В-246.868. Взаимодействие между соединением формулы (II) и соединением формулы (III), где Х обозначает гидрокси, предпочтительно проводят при молярном соотношении (II):(III) от 1:1 до 1:2, в органическом растворителе, таком как,к примеру, диметилсульфоксид, гексаметилфосфотриамид, диметилацетамид, диметилформамид, этанол, бензол или пиридин, в присутствии органического или неорганического основания, такого как, к примеру, триэтиламин, диизопропилэтиламин или карбонат или бикарбонат натрия или калия, и конденсирующего агента, такого как, к примеру, N-этил-N'-(3 диметиламинопропил)карбодиимид,N,N'-дициклогексилкарбодиимид и/или гидрат 1 гидроксибензотриазола. Реакционную температуру можно варьировать приблизительно от-10 до 100 С, а реакционное время приблизительно от 1 до 24 ч. Взаимодействие между соединением формулы (II) и соединением формулы (III), где Х обозначает удаляемую группу, определенную выше, может быть проведено при молярном соотношении (II):(III) от 1:1 до 1:2 в органическом растворителе, таком как, к примеру, диметилсульфоксид, диоксан, пиридин, бензол, тетрагидрофуран или их смеси с водой, необязательно в присутствии органического основания,к примеру, N,N'-диизопропилэтиламина, триэтиламина, или неорганического основания, к примеру, бикарбоната натрия или калия, при температуре приблизительно от 0 до 100 С, и варьировании реакционного времени приблизительно от 2 до 48 ч. Возможное превращение соединения формулы (I) в его фармацевтически приемлемую соль может быть выполнено известным общепринятым способом. Соединения формулы (II) являются известными соединениями или могут быть получены известными способами (см., например,Tetrahedron Letters 31, 1299 (1990), Anticancer(I) гидролитическим деформилированием в основной или кислотной среде соединений формулы(II) восстановлением нитрогруппы по известным методикам соединений формулы в свою очередь могут быть получены, исходя из аналогов дистамицина формулы(I) NH2-CN, при этом получают соединение формулы (I), в котором В обозначает(II) NH2-OH, при этом получают соединение формулы (I), в котором В обозначает(III) NH2-NH2, при этом получают соединение формулы (I), в котором В обозначает(IV) NHR4R5, при этом получают соединение формулы (I), в котором В обозначает и затем, возможно, с использованием H2NR6,при этом получают соединение формулы (I), в котором В обозначает(V) янтарного ангидрида, при этом получают соединение формулы (I), в котором В обозначает -CN;(VI) воды в щелочной среде, при этом получают соединение формулы (I), в котором В обозначает -CO-NR7R8, где R7 и R8 оба обозначают водород;(VII) HNR7R8, при этом получают соединение формулы (I), в котором В обозначает и затем с использованием воды в щелочной среде, при этом получают соединение формулы (I),в котором В обозначает -CO-NR7R8, где R7 и R8 оба обозначают, каждый независимо, водород или C1-C4 алкил, при условии, что, по меньшей мере, один из R7 и R8 обозначает C1-C4 алкил. Взаимодействие между соединением формулы (VII) и одним из реагентов, перечисленных в пунктах (I), (II), (III), (IV) или (VII), может быть проведено известными способами, к примеру, способом, приведенным в US4.766.142, Chem. Revs. 1961, 155; J.Med.Chem. 1984, 27, 849-857; Chem. Revs. 1970, 151 и "The(VII) с янтарным ангидридом (см. пункт (V) выше) предпочтительно проводят при молярном соотношении (VII):янтарный ангидрид от 1:1 до 1:3 в органическом растворителе, таком как, к примеру, диметилсульфоксид, диметилформамид, в присутствии органического или неорганического основания, такого как, к примеру,триэтиламин, диизопропилэтиламин, карбонат натрия или калия и тому подобного. Реакционную температуру можно варьировать приблизительно от 25 до 100 С, а реакционное время приблизительно от 1 до 12 ч. Взаимодействие с водой в щелочной среде(см. пункты (VI) и (VII) выше) может быть проведенo согласно общепринятым способам,обычно применяемым для щелочного гидролиза, к примеру, обработкой субстрата избытком гидроокиси натрия или калия, растворенной в воде или в смеси воды с органическим растворителем, к примеру, диоксаном, тетрагидрофураном или ацетонитрилом, при температуре 9 приблизительно от 50 до 100 С, за время, варьируемое приблизительно от 2 до 48 ч. Соединения формулы (III) являются известными соединениями или могут быть получены, исходя из известных соединений по хорошо известным в органической химии реакциям: см., к примеру, J.C.S. 1947-1032 и JACT 62,3495 (1940). Соединения формулы (VI) могут быть получены где n, m и Х имеют вышеуказанные значения,взаимодействием с соединением формулы где В' выбирают из с подходящим соединением амина, как определено по пунктам (I), (II) или (IV) выше. Соединения формул (VII), (VIII), (IX) и (X) являются известными соединениями или могут быть получены известными способами (см., например, Tetrahedron 34, 2389-2391, 1978; J.Org.Chem., 46, 3492-3497, 1981). Реакцию по способу (b) предпочтительно проводят при молярном соотношении (IV): янтарный ангидрид от 1:1 до 1:3 в органическом растворителе, таком как, к примеру, диметилсульфоксид или диметилформамид, в присутствии органического или неорганического основания, такого как, к примеру, триэтиламин, диизопропилэтиламин, карбонат натрия или калия и тому подобного. Реакционную температуру можно варьировать приблизительно от 25 до 100 С, а реакционное время приблизительно от 1 до 12 ч. Соединения (IV) могут быть получены известными способами, к примеру, способами,описанными в WO 90/11277. 10 Получение солей соединения формулы (I),равно как получение свободного соединения из соли, может быть выполнено известными стандартными способами. Для разделения смеси изомеров формулы(I) на отдельные изомеры можно также следовать хорошо известным способам, таким как, к примеру, фракционированная кристаллизация или хроматография. Соединения формулы (I) могут быть очищены общепринятыми способами, такими как, к примеру, хроматография на колонке с силикагелем или окисью алюминия и/или перекристаллизация из органического растворителя,такого как, к примеру, низший алифатический спирт, к примеру, метиловый, этиловый или изопропиловый спирт, или диметилформамид. Фармакология Соединения формулы (I) согласно изобретению полезны в качестве противоопухолевых и противовирусных средств. В частности, они проявляют цитостатические свойства в отношении опухолевых клеток, так что они могут быть полезны для ингибирования роста различных опухолей у млекопитающих, включая человека,таких как, к примеру, карциномы (рак), например рак молочной железы, рак лгкого, рак мочевого пузыря, рак толстой кишки, опухоли яичника и внутриматочные опухоли. Другими неоплазиями, при которых соединения согласно изобретению могут находить применение, являются, к примеру, саркомы, например саркомы мягких тканей и костей, и гематологические злокачественные опухоли, такие как, к примеру,лейкозы. Противоопухолевую активность in vitro (в лабораторном сосуде) оценивают путем изучений цитотоксичности, выполняемых на крысиных L1210 лейкозных клетках. Клетки извлекают из опухолей in vivo (в живом организме) и адаптируют в культуре клеток. Используют клетки до десятого пассажа. Цитотоксичность определяют, подсчитывая выжившие клетки после 48 часовой обработки. Процент роста клеток в обработанных культурах сравнивают с процентом роста клеток в контрольных образцах. Значения IC50 (концентрации, ингибирующей 50% клеточного роста относительно контролей) рассчитывают по зависимости доза-ответная реакция. Соединения согласно изобретению испытывались также in vivo на L1210 крысиный лейкоз и на М 5076 крысиную ретикулосаркому с применением нижеследующей методики, показывая очень хорошую противоопухолевую активность.L1210 крысиный лейкоз поддерживают invivo путем i.v. (внутривенной) серийной трансплантации. Для экспериментов 105 клеток впрыскивают i.p. (внутрибрюшинно) CD2F1 самкам мышей, поставляемым Charles River Italy. На начало эксперимента возраст животных состав 11 ляет 8-10 недель. Соединения вводят i.v. на день+1 после инъекций опухолевых клеток. М 5076 ретикулосаркому поддерживают invivo путем i.m. (внутримышечной) серийной трансплантации. Для экспериментов 5105 клетки впрыскивают i.m. C57B16 самкам мышей, поставляемым Charles River Italy. На начало экспериментов возраст животных составляет 8-10 недель. Соединения вводят i.v. на день 3, 7 и 11 после инъекций опухолевых клеток. Оценивают продолжительность выживания мыши и рост опухоли и выражают активность в терминах Т/С% и Т.I.%. средняя продолжительность выживания обработанной группы Т/С =100 средняя продолжительность выживания необработанной группы Т.I. = % ингибирования роста опухоли относительно контроля Тох: число мышей, умерших от токсичности. Определение Тох производят, когда мышь умирает до контроля и/или когда обнаруживается значительная потеря веса тела и/или наблюдается уменьшение размера селезнки и/или печени. Соединения согласно изобретению проявляют также значительную эффективность в подавлении репродуктивной активности патогенных вирусов и защите клеток ткани от вирусных инфекций. К примеру, они демонстрируют активность против DNA вирусов, таких как, к примеру, герпес, например вирусы простого герпеса и опоясывающего герпеса, против вируса коровьей оспы, РНК-вирусов, таких как, к примеру, риновирус и аденовирус, и против ретровирусов, таких как, к примеру, вирусы саркомы, например вирус саркомы молочной железы, и вирусов лейкоза, к примеру, вирус лейкоза Friend'a. К примеру, эффективность против вирусов герпеса, Коксаки и респираторно-синцитиального вирусов исследовалась в жидкой среде следующим образом. Образцы последовательного двукратного разбавления соединений от 200 до 1,5 мкг/мл распределяли, дублируя, по 0,1 мл/ячейка в 96-ячеечные микропластины для культуры ткани. Сразу же добавляли по 0,1 мл/ячейка суспензий клеток (2105 клеток/мл),зараженных приблизительно 510-3 TC1D50 вирус/клетка. После 3-5-дневной инкубации при 37 С в СO2 5% культуры клеток оценивали с помощью исследования под микроскопом и определяли минимальную ингибирующую концентрацию(MIC), MIC является минимальной концентрацией, которая определяет снижение цитопатического эффекта по сравнению с зараженными контролями. Соединения согласно изобретению могут быть введены млекопитающим, включая людей, 001863 12 обычными способами, например, парентерально, в частности, путем внутривенной инъекции или внутривенного вливания, внутримышечно,подкожно, местно или перорально. Доза зависит от возраста, веса и состояния пациента и от способа введения. К примеру, подходящая дозировка для введения взрослым людям может варьироваться в пределах приблизительно от 0,1 до 150-200 мг на дозу 1-4 раза в день. Объектом изобретения являются также фармацевтические композиции, которые включают соединение формулы (I) в качестве активной основы в совокупности с одним или более фармацевтически приемлемым носителем и/или разбавителем. Фармацевтические композиции согласно изобретению обычно получают, следуя общепринятым способам, и вводят в фармацевтически приемлемой форме. К примеру, растворы для внутривенной инъекции или вливания могут содержать в качестве носителя, например, стерильную воду или предпочтительно они могут быть в форме стерильных водных изотонических растворов соли. Суспензии или растворы для внутримышечных инъекций могут содержать вместе с активным соединением фармацевтически приемлемый носитель, к примеру, стерильную воду, оливковое масло, этилолеат, гликоли, например, пропиленгликоль, и, если необходимо,подходящее количество лидокаингидрохлорида. В формах для местного применения, например, кремах, примочках или пастах, при дерматологическом лечении активный ингредиент может быть смешан с обычными маслянистыми или эмульгирующими эксципиентами. Твердые пероральные формы, к примеру,таблетки и капсулы, могут содержать вместе с активным соединением разбавители, например лактозу, декстрозу, сахарозу, кукурузный крахмал и картофельный крахмал; смазывающие вещества, к примеру, двуокись кремния, тальк,стеариновую кислоту, стеарат магния или кальция и/или полиэтиленгликоли; связывающие средства, например, крахмалы, гуммиарабик,желатин, метилцеллюлозу, карбоксиметилцеллюлозу, поливинилпирролидон; разъединяющие средства, например крахмал, альгиновую кислоту, альгинаты, натрийкрахмалгликолят; пенящиеся смеси; красители, подсластители; смачивающие средства, например лецитин, полисорбаты, лаурилсульфаты; и вообще, не токсичные и фармакологически не активные вещества,применяемые по технологии приготовления лекарственного средства. Такой фармацевтический препарат может быть получен известными способами, например путем смешивания, гранулирования, таблетирования, покрытия сахарной оболочкой или покрытия пленкой. Целью изобретения являются и соединения формулы (I) для применения при терапевтическом лечении людей или животных. 13 Кроме того, изобретение представляет способ лечения опухолей и вирусных инфекций у нуждающихся в этом пациентов, который включает введение указанному пациенту композиции согласно изобретению. Далее, объектом изобретения является комбинированный способ лечения рака или улучшения состояния страдающих раком млекопитающих, включая людей, указанный способ включает введение соединения формулы (I) или его фармацевтически приемлемой соли и дополнительного противоопухолевого средства,достаточно точно по времени и в количествах,достаточных для получения терапевтически полезного действия. Данное изобретение обеспечивает также комбинированные препараты для одновременного, раздельного или последовательного применения в противораковой терапии, включающие соединение формулы (I), или его фармацевтически приемлемую соль, и дополнительное противоопухолевое средство. Подразумевается, что термин "противоопухолевое средство" включает как отдельное противоопухолевое лекарство, так и "коктейли",т.е. смеси таких лекарственных средств согласно клинической практике. Примеры противоопухолевых средств, которые могут быть составлены с соединением формулы (I) или напротив, могут быть введены при комбинированном способе лечения, включают доксорубицин,дауномицин, эпирубицин, идарубицин, этопозид, фторурацил, мелфалан, циклофосфамид, 4 деметоксидауномицин, блеомицин, винбластин и митомицин или их смеси. Последующие примеры приведены для иллюстрации изобретения, но не ограничивают объем заявленного изобретения. Пример 1. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионцианамидин. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионцианамидингидрохлорид. К раствору 324 мг цианамида в 20 мл ДМФ добавляют 186 мг гидрида натрия. Смесь перемешивают при комнатной температуре в течение 30 мин и затем добавляют к раствору одного грамма (1 г) дистамицина А в 10 мл ДМФ. Раствор перемешивают при комнатной температуре 2 ч, затем добавляют уксусную кислоту до рН=7. Растворитель удаляют при пониженном давлении и сырой остаток чистят флэшхроматографией (метиленхлорид/метанол : 9/1),получая 900 мг 3-[1-метил-4-[1-метил-4-[1 метил-4-формамидопиррол-2-карбоксамидо] пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионцианамидина, который растворяют в 50 мл метанола и добавляют 5 мл 2 н. соляной 14 кислоты. Реакционную смесь перемешивают при комнатной температуре два дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 200 мл этилацетата, получая после фильтрования 600 мг промежуточного продукта.(d, J=1.7 Hz, 1H), 7.06 (d, J=1.7 Hz, 1H), 6.94 (d,J=1.7 Hz, 1H), 6.88 (d, J=1.7 Hz, 1H), 3.81 (s, 3 Н),3.79 (s, 3 Н), 3.75 (s, 3 Н), 3.41 (m, 2H), 2.70 (m,2H). Стадия II. Промежуточный 1-метил-4-(бромакриламидо)пиррол-2-карбоксилхлорид. К раствору -бромакриловой кислоты (1,7 г) в сухом СН 3 СN (5 мл) добавляют за 1 ч раствор N,N'-дициклогексилкарбодиимида (1,2 г) в 20 мл СН 3 СN и образовавшуюся суспензию перемешивают при 25 С в течение 20'. Белый осадок отфильтровывают и полученный раствор добавляют к раствору гидрохлорида 1-метил-4 амино-пиррол-2-карбоновой кислоты (1 г) в 20 мл Н 2 О и 1,4 г NаНСО 3. Раствор перемешивают 1 ч при 25 С, затем добавляют 2 н. НСl до рН=3. Растворитель удаляют при пониженном давлении и сырой остаток чистят флэш-хроматографией (метиленхлорид/метанол : 95/5), получая 1,2 г 1-метил-4 -(-бромакриламидо)пиррол 2-карбоновой кислоты, которую растворяют в бензоле (40 мл) и добавляют 10 мл SOCl2. Раствор нагревают до температуры кипения с обратным холодильником в течение 1 ч и затем упаривают досуха в вакууме, получая 1,4 г промежуточного продукта. Аналогичным способом и при использовании подходящих исходных материалов может быть получен следующий продукт: 1-метил-4-(-хлоракриламидо)пиррол-2 карбоксилхлорид. Стадия III. Указанное в заглавии соединение. К раствору 206 мг промежуточного продукта, полученного на стадии I, 100 мг NаНСО 3 в 40 мл воды и 20 мл диоксана, добавляют раствор 175 мг промежуточного продукта, полученного на стадии II, в 40 мл диоксана. Раствор перемешивают 2 ч при 25 С, затем растворитель упаривают в вакууме и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 10/1), получая 150 мг указанного в заглавии соединения в виде желтого твердого вещества. 3.85 (s, 6H), 3.84 (s, 3H), 3.79 (s, 3H), 3.45 (b.s.,2H), 2.6 (b.s., 2H). Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионцианамидин и 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионцианамидин. Пример 2. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропион-N-метиламидингидрохлорид. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидиндигидрохлорид. Раствор 2 г дистамицина А в 50 мл ДМФ обрабатывают 0,38 мл метиламингидрохлорида 80%. Через 8 ч добавляют дополнительно 0,25 эквивалент метиламингидрохлорида 80%. Раствор упаривают досуха и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 8/2), получая 1,5 г 3-[1-метил-4-[1-метил-4[1-метил-4-формамидопиррол-2-карбоксамидо] пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидингидрохлорида, который растворяют в 40 мл метанола и добавляют 5 мл 2 н. соляной кислоты. Реакционную смесь перемешивают при комнатной температуре два дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 200 мл этилацетата, получая после фильтрования 1,4 г промежуточного продукта.(d, J=6 Hz, 3H), 2.61 (m, 2H). Аналогичным способом и при использовании подходящего исходного материала может быть получен следующий продукт: 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N,N-диметиламидиндигидрохлорид. Стадия II. Указанное в заглавии соединение. Раствор 170 мг 1-метил-4-(-бромакриламидо)пиррол-2-карбоксилхлорида (полу 001863 16 ченного, как указано в примере 1, стадии II) в 30 мл диоксана добавляют к раствору промежуточного продукта, полученного на стадии I (162 мг), и 75 мг NаНСО 3 в 25 мл Н 2 О. Раствор перемешивают в течение 2 ч при комнатной температуре, подкисливают 2 н. НСl до рH=5 и затем упаривают в вакууме. Сырой продукт чистят флэш-хроматографией(метиленхлорид/метанол : 8/2), получая 120 мг указанного в заглавии соединения в виде желтого твердого вещества.(s, 1H), 9.5 (b.s., 1H), 9.1 (b.s., 1H), 8.5 (b.s., 1H),8.22 (t, J=5.9 Hz, 1H), 6.9-7.3 (m, 8H), 6.68 (d,J=2.8 Hz, 1H), 6.22 (d, J=2.8 Hz, 1H), 3.85 (s, 6H),3.84 (s, 3H), 3.80 (s, 3H), 3.48 (b.s., 2H), 2.79 (s,3H), 2.62 (b.s., 2H). Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-(1-метил-4-(1-метил-4-(1-метил-4-(1-метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN,N-диметиламидингидрохлорид;(b.s., 3H), 2.77 (t, J=6.5 Hz, 2H); 3-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропион-N-метиламидингидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-Nметиламидингидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропион-N,N-диметиламидингидрохлорид и 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN,N-диметиламидингидрохлорид. Пример 3. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропион-N,N'-диметиламидингидрохлорид. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбокс 17 амидо]пропион-N,N'-диметиламидиндигидрохлорид. Раствор 1,5 г дистамицина А в 40 мл ДМФ нагревают до 80 С и обрабатывают 4 мл метиламингидрохлорида 80%. Через 4 ч добавляют дополнительно 5-эквивалент (4 мл) метиламингидрохлорида 80%. Раствор упаривают досуха и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 8/2), получая 1,2 г 3[1-метил-4-[1-метил-4-[1-метил-4-формамидопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N,N'-диметиламидингидрохлорида, который растворяют в 40 мл метанола и добавляют 5 мл 2 н. раствор соляной кислоты. Реакционную смесь перемешивают при комнатной температуре два дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 200 мл этилацетата, получая после фильтрования 1,4 г промежуточного продукта.(d, J=1.7 Hz, 1H), 6.92 (d, J=1.7 Hz, 1H), 3.92 (s,3H), 3.89 (s, 3H), 3.86 (s, 3H), 3.60-3.40 (m, 2H),3.02 (d, J=6 Hz, 3H), 2.80 (d, J=6 Hz, 3H), 2.72 (m,2H). Стадия II. Указанное в заглавии соединение. Раствор 200 мг 1-метил-4-(-бромакриламидо)пиррол-2-карбоксилхлорида (полученного, как указано в примере 1, стадии II) в 10 мл бензола добавляют к раствору промежуточного продукта, полученного на стадии I (250 мг), и 76 мг NаНСО 3 в 5 мл H2O. Раствор перемешивают в течение 1 ч при комнатной температуре, затем упаривают при пониженном давлении и сырой продукт чистят флэш-хроматографией (метиленхлорид/метанол : 85/15), получая 185 мг указанного в заглавии соединения в виде желтого твердого вещества.=44375 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-кар 001863 18 боксамидо]пиррол-2-карбоксамидо]пропионN,N'-диметиламидингидрохлорид и 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2 карбоксамидо]пиррол-2-карбоксамидо]пропионN,N'-диметиламидингидрохлорид; Пример 4. 3-[1-метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамидоксим. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамидоксим-гидрохлорид. Раствор 2 г дистамицина А в 35 мл ДМФ нагревают до 80 С и обрабатывают 0,46 мл 1 М гидроксиламина в ДМФ. Через 30' добавляют дополнительно 1 эквивалент 1 М гидроксиламина в ДМФ. Раствор упаривают досуха и сырой остаток чистят флэш-хроматографией (метиленхлорид/метанол : 9/1), получая 1,50 г 3-[1 метил-4-[1-метил-4-[1-метил-4-формамидопиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пиррол-2-карбоксамидо]пропионамидоксима,который растворяют в 50 мл метанола и добавляют 10 мл 2 н. НСl. Раствор перемешивают при комнатной температуре 2 дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 200 мл этилацетата, получая после фильтрования 1,4 г промежуточного продукта.(m, 2H); 2.22 (m, 2H). Стадия II. Указанное в заглавии соединение. К раствору 277 мг промежуточного продукта, полученного на стадии I, и 137 мгNаНСО 3 в 55 мл Н 2 О в добавляют раствор 203 мг 1-метил-4-(-бромакриламидо)пиррол-2-карбоксилхлорида (полученного как указано в примере 1, стадии II) в 55 мл диоксана. Раствор перемешивают 5 ч при комнатной температуре,затем упаривают в вакууме и сырой остаток чистят флэш-хроматографией (метиленхлорид/метанол : 85/15), получая 90 мг указанного в заглавии соединения в виде красноватокоричневого твердого вещества.=51155 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамидоксим и 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим. Пример 5. 2-[1-Мeтил-4-[1-мeтил-4-[1 мeтил-4-[1-мeтил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] этилгуанидин-гидрохлорид. Стадия I. Промежуточный 2-аминоэтилгуанидин-дигидрохлорид. Раствор промышленногоN-BOCэтилендиамина (1 г) в сухом этаноле (100 мл) и 2-метил-2-тиопсевдокарбамид-гидроиодида (1,5 г) нагревают до температуры кипения с обратным холодильником в течение 8 ч. Растворитель удаляют при пониженном давлении и сырой остаток чистят флэш-хроматографией (метиленхлорид/метанол : 9/1), получая 1,5 г N-BOC-2 аминоэтилгуанидин-гидроиодида в виде желтого масла, которое растворяют в 5 н. метанольном растворе соляной кислоты (20 мл) и перемешивают при комнатной температуре 3 ч. Белый осадок собирают, промывают сухим этанолом,получая 700 мг промежуточного продукта.(метиленхлорид/метанол : 8/2), получая 800 мг 2-[1-метил-4-[1 метил-4-[1-метил-4-нитропиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]этилгуанидин-гидрохлорида,который растворяют в метаноле (100 мл) с добавленным 1 н. раствором соляной кислоты (2 мл) и восста 001863psi=50 фунт/кв. дюйм=345 кПа) в аппарате Парра. Раствор, полученный после отфильтровывания катализатора, упаривают в вакууме и твердый остаток промывают сухим этанолом, получая 750 мг промежуточного продукта в виде коричневого порошка.(s, 3 Н), 3.82 (s, 3 Н), 3.28 (m, 4H). Аналогичным способом и с применением подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионцианамидингидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамидоксимгидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидиндигидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N,N'-диметиламидиндигидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамидгидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидгидрохлорид и 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрилгидрохлорид. Стадия III. Указанное в заглавии соединение. Раствор 250 мг 1-метил-4-(-бромакриламидо)пиррол-2-карбоксилхлорида (полученного, как указано в примере 1, стадии II) в 15 мл бензола добавляют к раствору промежуточного продукта, полученного на стадии II (250 мг), и 82 мг NаНСО 3 в 5 мл H2O. Раствор энергично перемешивают в течение 8 ч при комнатной температуре, затем упаривают в вакууме и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 8/2), получая 220 мг указанного в заглавии соединения в виде желтого твердого вещества.=48792 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 2-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] этилгуанидингидрохлорид; 2-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]этилгуанидингидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-брoмакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропион-N-метиламидингидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN-метиламидингидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-Nметиламидингидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропион-N,N'-диметиламидин-гидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN,N'-диметиламидин-гидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-кар 001863 22 боксамидо)пиррол-2-карбоксамидо)пропионN,N'-диметиламидин-гидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионамидоксим; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионамид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамид и 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-Nметиламид. Пример 6. 3-[1-Метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил-гидрохлорид. К раствору 1 г дистамицина А в 20 мл ДМФ добавляют 550 мг янтарного ангидрида и 950 мг К 2 СО 3. Раствор нагревают при 60 С 3 ч,затем упаривают досуха и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 9/1), получая 750 мг 3-[1-метил-4-[1 метил-4-[1-метил-4-формамидопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2 карбоксамидо]пропионитрила, который растворяют в 20 мл метанола и добавляют 5 мл 2 н. НСl. Раствор перемешивают при комнатной температуре 2 дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 20 мл этилацетата, получая после фильтрования 560 мг промежуточного продукта. Стадия II. Указанное в заглавии соединение. 23 К раствору 80 мг -бромакриловой кислоты в 10 мл ДМФ добавляют 57 мг дициклогексилкарбодиимида. Раствор перемешивают при комнатной температуре 20', затем добавляют 110 мг промежуточного продукта, полученного на стадии 1 и 20 мг бикарбоната натрия. Смесь перемешивают при комнатной температуре 8 ч, растворитель упаривают в вакууме и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 9/1), получая 100 мг указанного в заглавии соединения в виде желтого твердого вещества.=37068 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил; 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил; 3-[1-метил-4-[1-метил-4-[1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропион-N-метиламидин-гидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропиoн-N,N'-димeтилaмидин-гидpoxлopид; 3-[1-метил-4-[1-метил-4-[1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидo]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамидоксим; 3-[1-метил-4-[1-метил-4-[1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионцианамидин; 3-[1-метил-4-[1-метил-4-[1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамид. Пример 7. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамид. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксами 001863 24 до]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамид-гидрохлорид. К раствору 1 г дистамицина А в 50 мл ацетонитрила и 50 мл воды добавляют 10 мл 1 н.NaON и раствор нагревают при 60 С 4 ч. Растворитель упаривают досуха и сырой остаток чистят флэш-хроматографией (метиленхлорид/ метанол : 9/1), получая 800 мг 3-[1-метил-4-[1 метил-4-[1-метил-4-формамидопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2 карбоксамидо]пропионамида, который растворяют в 20 мл метанола и добавляют 5 мл 2 н. НСl. Раствор перемешивают при комнатной температуре 2 дня, растворитель упаривают в вакууме и твердый остаток суспендируют в 50 мл этилацетата, получая после фильтрования 600 мг промежуточного продукта в виде светлокоричневого твердого вещества. Аналогичным способом и с применением подходящего исходного материала может быть получен следующий продукт: 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламид-гидрохлорид. Стадия II. Указанное в заглавии соединение. Раствор 260 мг 1-метил-4-(-бромакриламидо)пиррол-2-карбоксилхлорида (полученного, как указано в примере 1, стадии II) в 25 мл диоксана добавляют к раствору промежуточного продукта, полученного на стадии II (420 мг) в 25 мл ацетонитрила и 25 мл диоксана и 0,27 мл триэтиламина. Раствор перемешивают в течение 1 ч при комнатной температуре, затем упаривают в вакууме и сырой остаток чистят флэш-хроматографией(метиленхлорид/метанол : 8/2), получая 220 мг указанного в заглавии соединения в виде желтого твердого вещества.=53146 Аналогичным способом и с применением подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионамид; 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамид и 25 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбокcaмидo]пиppoл-2-кapбoкcaмидo]пpoпиoн-Nмeтилaмид. Пример 8. 3-[1-метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидин-гидрохлорид. Стадия I. Промежуточный 3-[1-метил-4-[1 метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N-метиламидин-дигидрохлорид. 1,2 г 3-[1-метил-4-[1-метил-4-[1-метил-4 нитропиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрила (получен как указано в J.Med.Chem. 22,1296-1301, 1979) суспендируют в сухом этаноле и раствор насыщают сухим хлористым водородом. Через 24 ч при комнатной температуре растворитель упаривают и остаток обрабатывают двумя эквивалентами раствора метиламина в сухом этаноле. После 24 ч при комнатной температуре растворитель упаривают в вакууме и остаток чистят флэш-хроматографией, получая 500 мг 3-[1-метил-4-[1-метил-4-[1-метил-4 нитропиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-Nметиламидин-гидрохлорида, который растворяют в смеси метанол-диоксан-10% соляная кислота (4:1:1) и восстанавливают над Рd-диоксан 10% соляная кислота (4:1:1) и восстанавливают над Pd-катализатором (10% на активированном угле) в атмосфере водорода (50 psi) в аппарате Парра. Раствор, полученный после отфильтровывания катализатора, упаривают в вакууме и твердый остаток суспендируют в сухом этаноле и фильтруют, получая 500 мг промежуточного продукта.(s, 3H), 3.85 (s, 3H), 3.79 (s, 3H), 3.60-3.40 (m,2H), 2.80 (d, J=6 Hz, 3H), 2.61 (m, 2H). Аналогичным способом и при использовании подходящих исходных материалов может быть получен следующий продукт: 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионцианамидин-гидрохлорид; 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионамидоксимгидрохлорид и 26 3-[1-метил-4-[1-метил-4-[1-метил-4-аминопиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропион-N,N'-диметиламидин-дигидрохлорид. Стадия II. Указанное в заглавии соединение. К раствору 70 мг -бромакриловой кислоты в 8 мл ДМФ добавляют 51 мг дициклогексилкарбодиимида. Раствор перемешивают при комнатной температуре 20', затем добавляют 108 мг промежуточного продукта, полученного на стадии I и 17 мг бикарбоната натрия. Смесь перемешивают при комнатной температуре 10 ч, растворитель упаривают в вакууме и сырой остаток чистят флэшхроматографией (метиленхлорид/метанол : 8/2),получая 50 мг указанного в заглавии соединения в виде желтого твердого вещества.(m, 2H). Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN-метиламидин-гидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-Nметиламидин-гидрохлорид; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионN,N'-диметиламидин-гидрохлорид и 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионамидоксим. Пример 9. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-(-бромакриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил. К раствору 350 мг 3-[1-метил-4-[1-метил-4[1-метил-4-[1-метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пиррол-2-карбоксамидо]пропионамидингидро 27 хлорида (получен как указано в WO 90/11277) в 20 мл ДМФ добавляют 120 мг янтарного ангидрида и 165 мг К 2 СО 3. Раствор нагревают при 60 С 3 ч, затем растворитель упаривают при пониженном давлении и сырой остаток чистят флэш-хроматографией=45606 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-[бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропионитрил и 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-хлоракриламидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пропионитрил. Пример 10. 3-[1-Метил-4-[1-метил-4-[1 метил-4-[1-метил-4-[-хлоракриламидо)пиррол 2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пропион-N-метиламидингидрохлорид. К раствору промежуточного продукта, полученного как указано в примере 2, стадии I, и 100 мг NаНСО 3 в 15 мл воды добавляют 395 мг 1-метил-4-(-хлоракриламидо)пиррол-2-карбоксилхлорида в 15 мл бензола. Реакционную смесь энергично перемешивают в течение 4 ч, затем растворитель упаривают в вакууме и сырой остаток чистят флэш-хроматографией (метиленхлорид/метанол : 8/2), получая 135 мг указанного в заглавии соединения в виде желтого порошка.=44232 Аналогичным способом и при использовании подходящих исходных материалов могут быть получены следующие продукты: 3-[1-метил-4-[1-метил-4-[1-метил-4-[1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-кар 001863 28 боксамидо]пиррол-2-карбоксамидо]пиррол-2 карбоксамидо]пропион-N-метиламидингидрохлорид и 3-[1-метил-4-[1-метил-4-[1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо]пиррол-2-карбоксамидо]пиррол-2-карбоксамидо] пиррол-2-карбоксамидо]пропион-N-метиламидингидрохлорид. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Акрилоилзамещенные производные дистамицина формулыR3 обозначает водород или галоген; В выбирают из где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или C1-C4 алкил, при условии,что, по меньшей мере, один из R4, R5 и R6 обозначает C1-C4 алкил; или их фармацевтически приемлемые соли. 2. Соединение по п.1, отличающееся тем,что n обозначает 3 или 4;R3 обозначает хлор или бром; В выбирают из где R4, R5, R6, R7 и R8 обозначают, каждый независимо, водород или метил, при условии, что,по крайней мере, один из R4, R5 и R6 обозначает метил; или их фармацевтически приемлемые соли. 3. Соединение по п.1, отличающееся тем,что его выбирают из группы, включающей 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбокс 29 амидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионцианамидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропион-N-метиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2 карбоксамидо)пиррол-2-карбоксамидо)пропионN-метиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропион-Nметиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропион-N,N'-диметиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионN,N'-диметиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионN,N'-диметиламидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионамидоксим; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бpoмакриламидо)пиррол-2-карбоксамидо)пиррол-2-каpбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим; 3-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пропионамидоксим; 2-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) этилгуанидин; 2-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-бромакриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)этилгуанидин; 2-(1-метил-4-(1-метил-4-(1-метил-4-(1 метил-4-(-хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)этилгуанидин; 3-(1-метил-4-(1-метил-4-(1-метил-4-(бромакриламидо)пиррол-2-карбоксамидо)пир 001863 3-(1-метил-4-(1-метил-4-(1-метил-4-(хлоракриламидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо)пиррол-2-карбоксамидо) пропионамид и их фармацевтически приемлемые соли. 4. Способ получения соединения формулы(I) по п.1, который включает взаимодействие соединения формулы 32 где R1 и R2 выбирают, каждый независимо, из водорода, галогена и C1-C4 алкила; R3 обозначает водород или галоген; Х обозначает гидрокси или удаляемую группу; а m имеет вышеуказанные значения; в присутствии основания и, если необходимо, превращение соединения формулыI в его фармацевтически приемлемую соль. 5. Способ получения соединения формулы(I) по п.1, где В обозначает -CN, который включает взаимодействие соединения формулы где n, R1, R2 и R3 такие, как определено выше; с янтарным ангидридом в присутствии основания и, если необходимо, превращение соединения формулы (I) в его фармацевтически приемлемую соль. 6. Применение соединения по одному из пп.1-3 для получения лекарственного средства для лечения рака. 7. Фармацевтическая композиция, содержащая активно действующее вещество и фармацевтически приемлемые носители и/или разбавители, отличающаяся тем, что в качестве активно действующего вещества содержит эффективное количество соединения по пп.1-3.
МПК / Метки
МПК: C07D 207/34, A61P 35/00, A61K 31/40
Метки: акрилоилзамещенные, применение, способы, фармкомпозиции, получения, дистамицина, производные, качестве, противоопухолевых, средств
Код ссылки
<a href="https://eas.patents.su/17-1863-akriloilzameshhennye-proizvodnye-distamicina-sposoby-ih-polucheniya-primenenie-v-kachestve-protivoopuholevyh-sredstv-i-farmkompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Акрилоилзамещенные производные дистамицина, способы их получения, применение в качестве противоопухолевых средств и фармкомпозиции</a>
Предыдущий патент: Электрокаротаж слоистого грунтового образования
Следующий патент: Магнитоэлектрическая машина с постоянными магнитами (её варианты), способ и пресс-форма для её изготовления
Случайный патент: Кабина лифта для шахт лифтов с укороченным оголовком





















