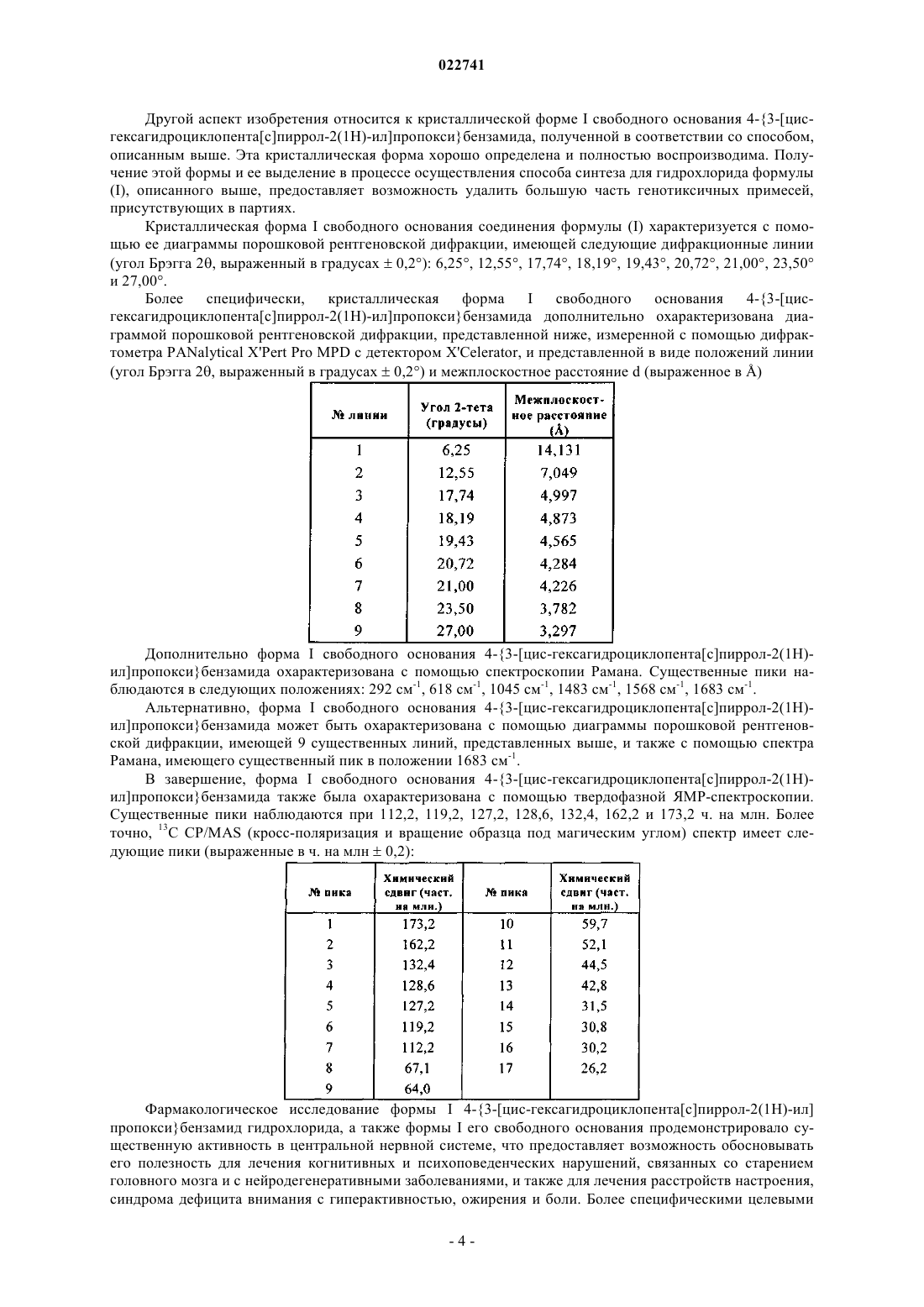
Способ синтеза и кристаллическая форма 4-{3-[цис-гексагидроциклопента[c]пиррол-2(1н)-ил]пропокси}бензамид гидрохлорида и фармацевтические композиции, которые ее содержат
Номер патента: 22741
Опубликовано: 29.02.2016
Авторы: Лерестиф Жан-Мишель, Гейяр Марина, Буаре Матьё, Робер Никола, Летелльер Филипп, Лекув Жан-Пьер, Мёнье Луак
Формула / Реферат
1. Способ промышленного синтеза соединения формулы (I)
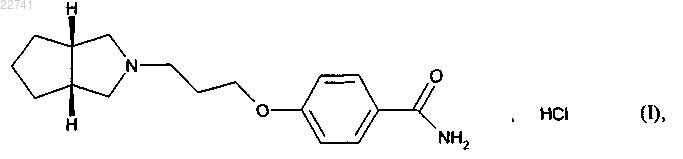
который отличается тем, что соединение формулы (II)
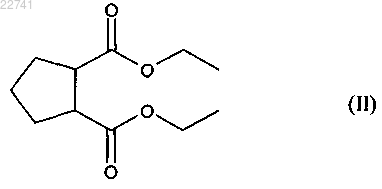
подвергают реакции с аммиаком при температуре больше чем 100°С с образованием соединения формулы (III)
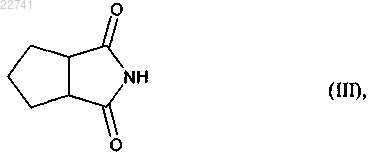
которое восстанавливают, получая бициклический амин формулы (IV)
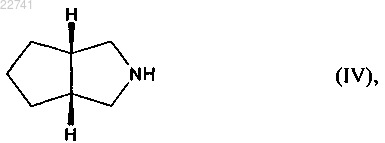
где это соединение впоследствии подвергают
либо реакции сочетания в щелочных условиях в полярной среде с соединением формулы (V)
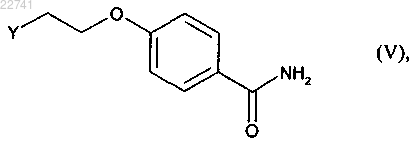
где Y представляет собой -СН2-Hal, где Hal представляет собой галоген, или группу -CH2-OSO2-R, где R представляет собой (С1-С6)алкильную группу или -С6Н4-СН3 группу,
или восстановительному аминированию в кислой среде с соединением формулы (V¢)
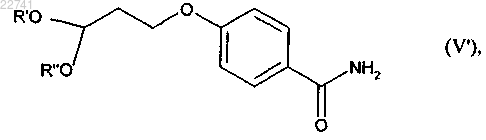
где R' и R" представляют собой, каждый независимо друг от друга, (C1-С6)алкильную группу, или R' и R" вместе образуют группу -(СН2)n-, где n = 2-3, или одна из групп R' и R" представляет собой атом водорода, а другая представляет собой (C1-С6)алкильную группу,
или восстановительному аминированию с соединением формулы (V'')
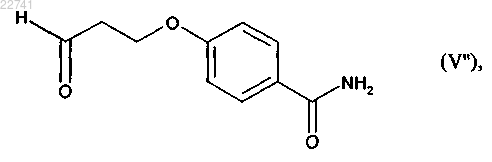
получая свободное основание соединения формулы (I), которое помещают в HCl с образованием соединения формулы (I), которое выделяют в виде твердого вещества.
2. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакционную смесь, полученную после осуществления реакции соединения формулы (II) с аммиаком, подвергают пиролизу.
3. Способ синтеза соединения формулы (I) в соответствии с п.2, где пиролиз осуществляют при температуре больше или равной 200°С.
4. Способ синтеза соединения формулы (I) в соответствии с п.2, где пиролиз осуществляют при температуре больше или равной 280°С.
5. Способ синтеза соединения формулы (I) в соответствии с п.1, где превращение соединения формулы (III) в соединение формулы (IV) осуществляют в присутствии водорода и металла или металлосодержащего катализатора.
6. Способ синтеза соединения формулы (I) в соответствии с п.1, где соединение формулы (V) представляет собой 4-(3-хлорпропокси)бензамид.
7. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в присутствии карбоната, амина или гидроксида.
8. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в присутствии карбоната калия или триэтиламина.
9. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в полярной среде, состоящей из одного или нескольких полярных растворителей, выбранных из воды, спиртов, кетонов, простых эфиров, амидов, ДМСО и ацетонитрила.
10. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в смеси вода/ацетонитрил или смеси вода/изопропанол.
11. Способ синтеза соединения формулы (I) в соответствии с п.1, где стадию образования соли в присутствии HCl осуществляют в растворителе, выбранном из воды, ацетона и спирта.
12. Способ синтеза соединения формулы (I) в соответствии с п.1, где стадию образования соли в присутствии HCl осуществляют в ацетоне или изопропаноле.
13. Способ синтеза соединения формулы (I) в соответствии с одним из пп.1-6, где соединение формулы (I) подвергают перекристаллизации.
14. Соединение формулы (V)
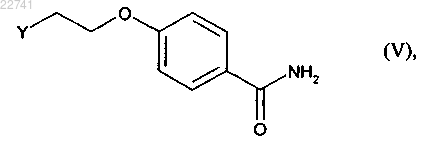
в которой Y представляет собой группу -CH2-OSO2-R, где R представляет собой (C1-С6)алкильную группу или -C6H4-СН3 группу.
15. Применение соединения формулы (V) в соответствии с п.14 для синтеза соединения формулы (I).
16. Соединение формулы (V¢)
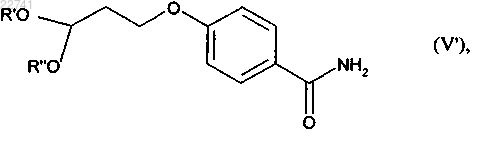
в которой R' и R" представляют собой, каждый независимо друг от друга, (С1-С6)алкильную группу, или R' и R" вместе образуют группу -(СН2)n-, где n = 2-3, или одна из групп R' и R" представляет собой атом водорода, а другая представляет собой (C1-С6)алкильную группу.
17. Соединение формулы (V¢) в соответствии с п.16, которое представляет собой 4-(3,3-диэтоксипропокси)бензамид.
18. Применение соединения формулы (V¢) в соответствии с п.16 или 17 для синтеза соединения формулы (I).
19. Применение соединения формулы (V"), раскрытого в п.1, для синтеза соединения формулы (I).
20. Кристаллическая форма I соединения формулы (I), раскрытого в п.1
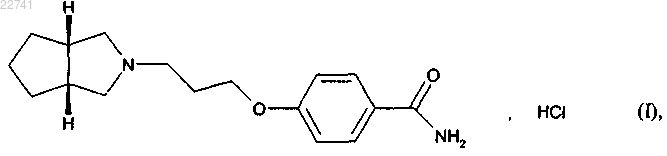
которая характеризуется диаграммой порошковой рентгеновской дифракции, имеющей следующие дифракционные линии (угол Брэгга 2θ, выраженный в градусах ±0,2°): 16,97°, 17,84°, 18,90°, 20,32°, 23,87°, 27,10°, 27,86° и 30,34°.
21. Кристаллическая форма I соединения формулы (I) в соответствии с п.20, которая характеризуется следующей диаграммой порошковой рентгеновской дифракции, измеренной с помощью дифрактометра PANalytical X'Pert Pro MPD с детектором X'Celerator и представленной в виде положений линии (угол Брэгга 2θ, выраженный в градусах ±0,2°) и межплоскостного расстояния d (выраженного в Å):
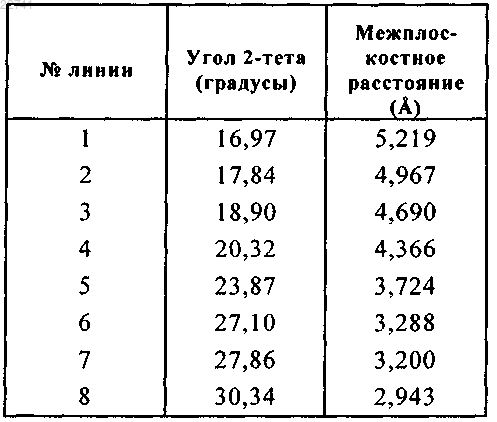
22. Кристаллическая форма I соединения формулы (I) в соответствии с п.20 или 21, которая характеризуется спектром Рамана, имеющим существенный пик в положении 1606 см-1 или 1676 см-1.
23. Кристаллическая форма I соединения формулы (I) в соответствии с одним из пп.20-22, которая характеризуется спектром Рамана, имеющим существенные пики в положениях 1676 см-1, 1606 см-1, 1564 см-1, 1152 см-1, 830 см-1 и 296 см-1.
24. Фармацевтическая композиция, которая содержит в качестве активного компонента кристаллическую форму I 4-{3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси}бензамид гидрохлорида в соответствии с одним из пп.20-23, в комбинации с одним или несколькими фармацевтически приемлемыми, нетоксичными, инертными носителями.
25. Фармацевтическая композиция в соответствии с п.24, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли.
26. Фармацевтическая композиция в соответствии с п.24, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменции с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией.
27. Применение кристаллической формы I 4-{3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси}бензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства для лечения нарушений гистаминергической системы.
28. Применение кристаллической формы I 4-{3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси}бензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли.
29. Применение кристаллической формы I 4-{3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси}бензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменции с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией.
30. Кристаллическая форма I свободного основания соединения формулы (I), раскрытого в п.1
которая характеризуется диаграммой порошковой рентгеновской дифракции, имеющей следующие дифракционные линии (угол Брэгга 2θ, выраженный в градусах ±0,2°): 6,25°, 12,55°, 17,74°, 18,19°, 19,43°, 20,72°, 21,00°, 23,50° и 27,00°.
31. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.30, которая характеризуется следующей диаграммой порошковой рентгеновской дифракции, измеренной с помощью дифрактометра PANalytical X'Pert Pro MPD с детектором X'Celerator и представленной в виде положений линии (угол Брэгга 2θ, выраженный в градусах ±0,2°) и межплоскостного расстояния d (выраженного в Å):
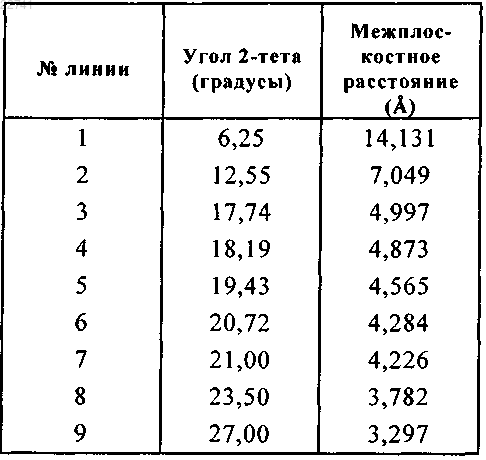
32. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.30 или 31, которая характеризуется спектром Рамана, имеющим существенный пик в положении 1683 см-1.
33. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с одним из пп.30-32, которая характеризуется спектром Рамана, имеющим существенные пики в положениях 292 см-1, 618 см-1, 1045 см-1, 1483 см-1, 1568 см-1, 1683 см-1.
34. Кристаллическая форма I свободного основания соединения формулы (I), раскрытого в п.1
которая характеризуется твердофазным 13С CP/MAS ЯМР спектром, имеющим следующие пики (выраженные в ч. на млн ±0,2): 112,2, 119,2, 127,2, 128,6, 132,4, 162,2 и 173,2 ч. на млн.
35. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.34, которая характеризуется твердофазным 13С CP/MAS ЯМР спектром, имеющим следующие пики (выраженные в ч. на млн ±0,2):
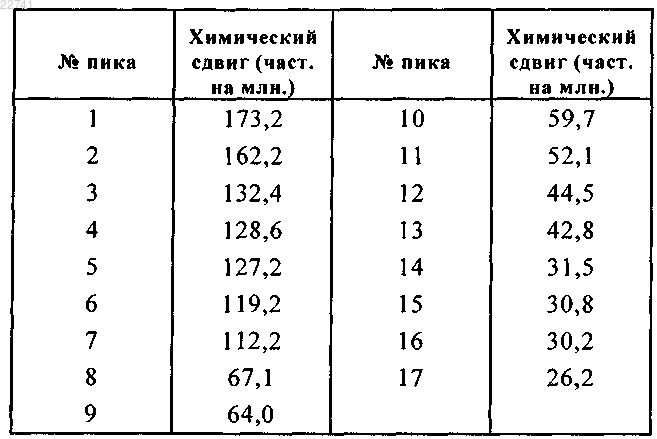
36. Фармацевтическая композиция, которая содержит в качестве активного компонента кристаллическую форму I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 в комбинации с одним или несколькими фармацевтически приемлемыми, нетоксичными, инертными носителями.
37. Фармацевтическая композиция в соответствии с п.36, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли.
38. Фармацевтическая композиция в соответствии с п.36, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменцией с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией.
39. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства для лечения нарушений гистаминергической системы.
40. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли.
41. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменцией с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией.
Текст
В изобретении описан промышленный способ синтеза соединения формулы (I), стадии получения которого приведены в формуле изобретения, кристаллическая форма указанного выше соединения и кристаллические формы свободного основания этого соединения. Также в изобретении описана фармацевтическая композиция, содержащая эти формы, и применение их для лечения различных заболеваний и приготовления лекарственных форм. Соединение формулы (I)(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) Настоящее изобретение относится к способу промышленного синтеза 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида формулы (I) Настоящее изобретение также относится к кристаллической форме I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида, к способу ее приготовления, а также к фармацевтическим композициям, которые ее содержат. Кристаллическую форму I свободного основания соединения формулы (I), кроме того, также получают с помощью способа согласно изобретению, и она составляет неотъемлемую часть изобретения, так же как и фармацевтические композиции, которые ее содержат. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид обладает свойствами взаимодействия с центральными гистаминергическими системами in vivo. Эти свойства обеспечивают его активность в центральной нервной системе и, более специфически, для лечения нарушений познавательных способностей, связанных со старением головного мозга и с нейродегенеративными заболеваниями. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид, его приготовление в форме оксалата и его терапевтическое применение было описано в патентной заявке WO 2005/089747. Учитывая фармацевтическую ценность этого соединения, важной является возможность его получения с помощью эффективного способ синтеза, который легко переместить в промышленный масштаб,получая 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорид с хорошим выходом и отличной чистотой. Также является важной возможность получения 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамид гидрохлорида в точно определенной, полностью воспроизводимой кристаллической форме, которая имеет ценные фильтрационные характеристики и легко может быть превращена в лекарственное средство. В патентной заявке WO 2005/089747 описано получение 4-3-[цис-гексагидроциклопента[с]пиррол 2(1H)-ил]пропоксибензамид оксалата за три стадии, используя в качестве исходного вещества 4 гидроксибензонитрил, который подвергается реакции О-алкилирования перед сочетанием с кольцевой системой октагидроциклопента[с]пиррольного типа с образованием 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензонитрила. Последнее соединение в завершение подвергается щелочному гидролизу для получения 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси бензамида, который кристаллизируется в форме оксалата. Выход для этих трех стадий составляет 46,6%. Настоящее изобретение относится к новому промышленному способу синтеза, который обеспечивает получение 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида с удовлетворительной чистотой с фармацевтической точки зрения и с эффективным выходом с промышленной точки зрения. В соответствии с этим способом представляется возможным обеспечивать чрезвычайно низкий уровень генотоксичных примесей, который соответствует нормативным требованиям. Настоящее изобретение относится более специфически к способу промышленного синтеза соединения формулы (I) где способ характеризуется тем, что соединение формулы (II) подвергают реакции с аммиаком при температуре больше чем 100 С с образованием соединения формулы (III) которое восстанавливают, получая бициклический амин формулы (IV) где это соединение впоследствии подвергают либо реакции сочетания в щелочных условиях в полярной среде с соединением формулы (V) где R' и R" представляют собой, каждый независимо друг от друга, (C1-С 6)алкильную группу, или R' и R" вместе образуют группу -(СН 2)n-, где n = 2-3, или одна из групп R' и R" представляет собой атом водорода, а другая представляет собой (C1-С 6)алкильную группу,или восстановительному аминированию с соединением формулы (V) получая свободное основание соединения формулы (I), которое помещают в присутствии HCl с образованием соединения формулы (I), которое выделяют в виде твердого вещества. В предпочтительном варианте осуществления изобретения реакционную смесь, полученную после осуществления реакции соединения формулы (II) с аммиаком, подвергают пиролизу. Указанный пиролиз осуществляют предпочтительно при температуре больше или равной 200 С и еще более предпочтительно при температуре больше или равной 280 С. Превращение соединения формулы (III) в соединение формулы (IV) благоприятно осуществляют в присутствии водорода и металла или металлосодержащего катализатора. Предпочтительным является соединение формулы (V), которое представляет собой 4-(3 хлорпропокси)бензамид. Реакцию сочетания соединения формулы (IV) с соединением формулы (V) предпочтительно осуществляют в присутствии карбоната, амина или гидроксида. Из предпочтительных карбонатов, аминов и гидроксидов могут быть указаны карбонат калия, карбонат цезия, триэтиламин, пиридин, гидроксид калия, гидроксид натрия и гидроксид лития. Еще более предпочтительно реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в присутствии карбоната калия или триэтиламина. Эту реакцию также предпочтительно осуществлять в полярной среде, состоящей из одного или нескольких полярных растворителей, выбранных из воды, спиртов, кетонов, простых эфиров, амидов,ДМСО и ацетонитрила. Предпочтительными спиртами являются метанол, этанол, изопропанол и бутанол. Предпочтительные растворители также включают ацетон и метилэтилкетон из кетонов, тетрагидрофуран, метилтетрагидрофуран и циклопентилметиловый эфир из простых эфиров и также N-метил-2 пирролидон из амидов. Еще более предпочтительно реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в смеси вода/ацетонитрил или смеси вода/изопропанол. В случае восстановительного аминирования в кислой среде соединения формулы (IV) с соединением формулы (V') последнее соединение предпочтительно представляет собой 4-(3,3 диэтоксипропокси)бензамид. Кроме того, стадию образования соли из свободного основания соединения формулы (I) в присутствии HCl предпочтительно осуществляют в растворителе, выбранном из воды, ацетона и спирта. Предпочтительные спирты представляют собой метанол, этанол и изопропанол. Ацетон и изопропанол являются особенно предпочтительными для этой стадии образования соли. Необязательно, соединение формулы (I), выделенное после окончания стадии образования соли,подвергают перекристаллизации. Важно отметить, что этот способ синтеза предоставляет возможность получения соединения 4-3[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид исключительно с удовлетворительным выходом в промышленном масштабе, а не его транс-гомолога. Кроме этого преимущества он предоставляет возможность поддерживать уровень генотоксичных примесей (в особенности 4-(3 хлорпропокси)бензамида), присутствующих в партиях, значительно ниже нормативных параметров. Соединения формулы (V), где Y представляет собой группу -CH2-OSO2-R, где R представляет собой(C1-С 6)алкильную группу или -C6H4-CH3 группу, и соединения формулы (V') являются новыми и пригодны в качестве промежуточных соединений для синтеза соединения формулы (I). Соединение формулы(V") также пригодно в качестве промежуточного соединения для синтеза соединения формулы (I). Изобретение также относится к кристаллической форме I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида, полученной в соответствии со способом,описанным выше. Эта кристаллическая форма точно определена, полностью воспроизводима и, следовательно, имеет ценные характеристики фильтрации, высушивания, стабильности и легко может быть превращена в лекарственное средство. Кристаллическая форма I соединения формулы (I) характеризуется диаграммой порошковой рентгеновской дифракции, имеющей следующие дифракционные линии (угол Брэгга 2, выраженный в градусах 0,2): 16,97, 17,84, 18,90, 20,32, 23,87, 27,10, 27,86 и 30,34. Более специфически, кристаллическая форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамид гидрохлорида дополнительно охарактеризована диаграммой порошковой рентгеновской дифракции, представленной ниже, измеренной с помощью дифрактометра PANalytical X'Pert ProMPD с детектором X'Celerator, и представленной в виде положений линии (угол Брэгга 2, выраженный в градусах 0,2) и межплоскостное расстояние d (выраженное в ) Более того, форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида охарактеризована с помощью спектроскопии Рамана. Существенные пики наблюдаются в следующих положениях: 1676 см-1, 1606 см-1, 1564 см-1, 1152 см-1, 830 см-1 и 296 см-1. Альтернативно, форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида может быть охарактеризована с помощью диаграммы порошковой рентгеновской дифракции, имеющей 8 существенных линий, представленной выше, и также с помощью спектра Рамана, имеющего существенный пик в положении 1606 см-1 или 1676 см-1. Такая полученная кристаллическая форма имеет преимущество, предоставляющее возможность особенно быстрой и эффективной фильтрации и также приготовления фармацевтических препаратов,имеющих стабильный и воспроизводимый состав, что является особенно благоприятным, если эти препараты предназначены для перорального введения. Кроме того, форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорида имеет заслуживающие внимания свойства быстрого растворения. Форма, полученная таким образом, является достаточно стабильной, что предоставляет возможность ее хранения в течение продолжительного периода без определенных условий относительно температуры, освещенности, влажности или уровней кислорода. Более специфически, было обнаружено, что форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорида является очень стабильной в течение периодов вплоть до 18 месяцев при следующих условиях: при 25 С при уровне влажности 60% в двойном пакете полиэтилена,при 30 С при уровне влажности 65% в двойном пакете полиэтилена,при 30 С при уровне влажности 85% в двойном пакете полиэтилена. Другой аспект изобретения относится к кристаллической форме I свободного основания 4-3-[цисгексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида, полученной в соответствии со способом,описанным выше. Эта кристаллическая форма хорошо определена и полностью воспроизводима. Получение этой формы и ее выделение в процессе осуществления способа синтеза для гидрохлорида формулы(I), описанного выше, предоставляет возможность удалить большую часть генотиксичных примесей,присутствующих в партиях. Кристаллическая форма I свободного основания соединения формулы (I) характеризуется с помощью ее диаграммы порошковой рентгеновской дифракции, имеющей следующие дифракционные линии(угол Брэгга 2, выраженный в градусах 0,2): 6,25, 12,55, 17,74, 18,19, 19,43, 20,72, 21,00, 23,50 и 27,00. Более специфически, кристаллическая форма I свободного основания 4-3-[цисгексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида дополнительно охарактеризована диаграммой порошковой рентгеновской дифракции, представленной ниже, измеренной с помощью дифрактометра PANalytical X'Pert Pro MPD с детектором X'Celerator, и представленной в виде положений линии Дополнительно форма I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамида охарактеризована с помощью спектроскопии Рамана. Существенные пики наблюдаются в следующих положениях: 292 см-1, 618 см-1, 1045 см-1, 1483 см-1, 1568 см-1, 1683 см-1. Альтернативно, форма I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамида может быть охарактеризована с помощью диаграммы порошковой рентгеновской дифракции, имеющей 9 существенных линий, представленных выше, и также с помощью спектра Рамана, имеющего существенный пик в положении 1683 см-1. В завершение, форма I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамида также была охарактеризована с помощью твердофазной ЯМР-спектроскопии. Существенные пики наблюдаются при 112,2, 119,2, 127,2, 128,6, 132,4, 162,2 и 173,2 ч. на млн. Более точно, 13 С CP/MAS (кросс-поляризация и вращение образца под магическим углом) спектр имеет следующие пики (выраженные в ч. на млн 0,2): Фармакологическое исследование формы I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил] пропоксибензамид гидрохлорида, а также формы I его свободного основания продемонстрировало существенную активность в центральной нервной системе, что предоставляет возможность обосновывать его полезность для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения,синдрома дефицита внимания с гиперактивностью, ожирения и боли. Более специфическими целевыми нейродегенеративными заболеваниями являются болезнь Альцгеймера, болезнь Паркинсона, болезнь Пика, корсаковский психоз, деменция с тельцами Леви, фронтальная и субкортикальная деменция, лобно-височная деменция и сосудистая деменция. Изобретение также относится к фармацевтическим композициям, которые содержат в качестве активного компонента кристаллическую форму I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1 Н)ил]пропоксибензамид гидрохлорида, или кристаллическую форму I его свободного основания, совместно с одним или несколькими подходящими нетоксичными, инертными наполнителями. Из фармацевтических композиций в соответствии с изобретением более специфически можно упомянуть те композиции, которые пригодны для перорального, парентерального (внутривенного или подкожного) или назального введения, таблетки или драже, гранулы, подъязычные таблетки, капсулы, лепешки, суппозитории, кремы, мази, кожные гели, препараты для инъекций, суспензии для питья и жевательные резинки. Пригодная дозировка может изменяться в соответствии с природой и тяжестью нарушения, путем введения и также возрастом и весом пациента. Пригодная дозировка изменяется от 1-100 мг в сутки на одно или несколько введений. Предпочтительно кристаллическая форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорида вводится в суточных дозах (выраженных в виде эквивалента свободного основания) 2, 5 и 20 мг (или, другими словами, 2,25, 5,63 и 22,52 мг гидрохлорида). Примеры, представленные ниже, иллюстрируют изобретение. Приготовление 1. 4-(3-Хлорпропокси)бензамид. 10,5 кг 4-гидроксибензамида, 10,58 кг карбоната калия и 83 кг ацетонитрила вносили в реактор. Смесь перемешивали и затем добавляли 24,14 кг раствора 1-бром-3-хлорпропана. Реакционную смесь нагревали в колбе с обратным холодильником в течение 4 ч. Добавляли воду (105 л) в горячем состоянии, после этого смесь охлаждали до 5 С и фильтровали. Фильтровальный осадок промывали водой и затем ацетонитрилом. Указанный в заглавии продукт получали в форме порошка с выходом 82%. Точка плавления: 144 С. Приготовление 2. 4-(3-Оксопропокси)бензамид. Стадия А. 4-(3,3-Диэтоксипропокси)бензамид. 500 мг 4-гидроксибензамида, 1,51 г карбоната калия, 10 мл ДМФА и 730 мг 3-хлор-1,1 диэтоксипропана добавляли в колбу. Реакционную смесь перемешивали при 100 С в течение 18 ч. и затем добавляли 5 мл воды. Водную фазу экстрагировали этилацетатом и затем органические фазы собирали, промывали водой и концентрировали при пониженном давлении. Продукт получали в форме порошка с выходом 89% и с химической чистотой 95%. Точка плавления: 108 С. Стадия В. 4-(3-Оксопропокси)бензамид. 5 г продукта, полученного на стадии А, 100 мл ТГФ и 94 мл 1 н. раствора соляной кислоты добавляли в колбу. Смесь перемешивали при температуре окружающей среды в течение 1 ч. Водную фазу экстрагировали дихлорметаном и затем органические фазы концентрировали при пониженном давлении. Продукт получали в форме твердого вещества с выходом 96% и с химической чистотой 93%. Пример 1. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорид. Стадия А. Тетрагидроциклопента[с]пиррол-1,3(2 Н,3 аН)-дион. Загружали 1 кг диэтил 1,2-циклопентандикарбоксилата и 1,02 кг 27% аммиака в автоклав. Реакционную смесь нагревали в автоклаве при температуре 130 С минимум в течение 4 ч. После охлаждения до 60 С и дегерметизации осуществляли упаривание растворителя. После этого остаток подвергали пиролизу 280 С в течение 1 ч. Имид очищали путем перегонки в вакууме (4-12 мбар) при температуре 200 С. После выделения указанный в заглавии продукт получали с выходом 96%. Точка плавления: 89 С. Стадия В. цис-Октагидроциклопента[с]пиррол. 1 кг имида со стадии А, 250 г хромита меди и 2 л диоксана загружали в реактор. Реакционную смесь перемешивали при температуре 265 С и под давлением водорода 205 бар до завершения абсорбции водорода. После охлаждения реактора катализатор отфильтровали. Гидрирующие жидкости загружали в сепаратор и затем добавляли 0,37 л воды. Значение рН доводили до рН меньше 3 путем добавления серной кислоты 96%. Нижнюю, водную фазу сливали. После добавления 2,5 л воды оставшийся диоксан удаляли путем азеотропной перегонки с мониторингом рефракционного индекса. Затем рН доводили до 13 путем добавления 30% раствора гидроксида натрия. Указанный в заглавии продукт очищали путем азеотропной перегонки с водой, получая 30% раствор по весу с выходом 83%. Стадия С. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид. 13,35 кг 4-(3-хлорпропокси)бензамида, полученного в соответствии с приготовлением 1, 10,33 кг карбоната калия и 168 кг ацетонитрила вносили в реактор. Смесь перемешивали. После этого загружали 34,74 кг цис-октагидроциклопента[с]пиррола в 30% водном растворе, 26,7 л воды. Реакционную смесь нагревали с обратным холодильником до израсходования всего исходного вещества. Затем добавляли воду (13,3 л). Смесь охлаждали до 5 С, после этого фильтровали и промывали водой. Указанный в загла-5 022741 вии продукт получали в форме твердого вещества с выходом 81% и с химической чистотой 96%. 1H ЯМР:(600,13 МГц; ДМСО-d6; 300 K): 7,82 (d, 2H, J=9,0 Гц); 7,79 (bs, 1H); 7,14 (bs, 1H); 6,95 (d,2H, J=9,0 Гц); 4,06 (t, 2H, J=6,5 Гц); 2,57 (m, 2H); 2,48 (m, 2 Н); 2,44 (bt, 2H, J=6,5 Гц); 2,14 (bd, 2H, J=7,5 Гц); 1,86 (qt, 2H, J=6,5 Гц); 1,65-1,55 (m, 3 Н); 1,45-1,38 (m, 1H); 1,37-1,30 (m, 2H),где bs: широкий синглет; bd: широкий дублет; bt: широкий триплет. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 6-8, свидетельствовала о том, что получена кристаллическая форма I свободного основания. Стадия D. 4-3-[цис-Гексагидроииклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорид. 14,69 кг 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида и 122 л воды вносили в реактор. Также приготавливали раствор 6,81 кг 37% соляной кислоты в 11,54 л воды. 13,75 кг раствора этой кислоты добавляли в реактор. Смесь перемешивали в течение 1 ч при температуре окружающей среды и затем в течение 1 ч 30 мин при 60 С. Суспензию фильтровали в горячем состоянии и фильтр затем промывали водой. После этого осуществляли замену растворителя на фильтрате, поддерживая объем постоянным, и получали соотношение изопропанол:вода 9:1. Продукт выделяли при 0 С и полученный осадок промывали изопропанолом. В конечном итоге получали указанный в заглавии продукт с выходом 89% и с химической чистотой больше 99%. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 4-5, свидетельствовала о том, что получали кристаллическую форму I гидрохлорида. Стадия Е. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорид. Гидрохлоридную соль, полученную на стадии D, перекристаллизовывали из смеси изопропанола(264 кг) и воды (37,4 л). Смесь нагревали в колбе с обратным холодильником в течение 45 мин. Раствор фильтровали в горячем состоянии и затем промывали изопропанолом. После этого инициировали кристаллизацию при 55 С. Смесь поддерживали при этой температуре в течение 40 мин, после этого охлаждали до 0 С. Через несколько часов, продукт выделяли путем фильтрации. После промывания изопропанолом указанный в заглавии продукт получали в форме порошка с выходом 93% и с химической чистотой больше 99%. Точка плавления: 213-215 С. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 4-5, свидетельствовала о том, что получали кристаллическую форму I гидрохлорида. Пример 2. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорид. Стадия А. Тетрагидроциклопента[с]пиррол-1,3(2 Н,3aH)-дион. Процедура была аналогичной описанной на стадии А примера 1. Стадия В. иис-Октагидроциклопента[с]пиррол. Процедура была аналогичной описанной на стадии В примера 1. Стадия С. 4-3-[иис-Гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид. 15,2 кг 4-(3-хлорпропокси)бензамида, 40,28 кг цис-октагидроциклопента[с]пиррола в 30% водном растворе, 63,84 кг воды, 21,48 кг изопропанола и 14,39 кг триэтиламина вносили в реактор. Реакционную смесь перемешивали и нагревали с обратным холодильником до израсходования всего исходного вещества. Реакционную после этого смесь охлаждали до 20 С, после этого фильтровали и промывали смесью изопропанола и воды. Продукт получали в форме порошка с выходом 83% и с химической чистотой 97%. 1H ЯМР:(600,13 МГц; ДМСО-d6; 300 K): 7,82 (d, 2H, J=9,0 Гц); 7,79 (bs, 1H); 7,14 (bs, 1H); 6,95 (d,2H, J=9,0 Гц); 4,06 (t, 2H, J=6,5 Гц); 2,57 (m, 2H); 2,48 (m, 2 Н); 2,44 (bt, 2 Н, J=6,5 Гц); 2,14 (bd, 2H, J=7,5 Гц); 1,86 (qt, 2H, J=6,5 Гц); 1,65-1,55 (m, 3 Н); 1,45-1,38 (m, 1 Н); 1,37-1,30 (m, 2 Н),где bs: широкий синглет; bd: широкий дублет; bt: широкий триплет. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 6-8, свидетельствовала о том, что получена кристаллическая форма I свободного основания. Стадия D. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорид. 16,49 кг 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида, 16,36 кг ацетона,6,76 кг концентрированной водной соляной кислоты и 18,96 кг воды вносили в реактор. Смесь перемешивали и нагревали при 50 С в течение 1 ч. После этого смесь фильтровали в горячем состоянии во втором реакторе, содержащем 57,67 кг ацетона и 1,65 кг воды. После этого смесь доводили до флегмы и 73,32 кг ацетона добавляли. Флегму поддерживали в течение 10 мин и затем охлаждали до 0 С. Продукт отфильтровали и полученное твердое вещество промывали ацетоном. Продукт получали в форме порошка с выходом 85% и с химической чистотой больше 99%. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 4-5, свидетельствовала о том, что получали кристаллическую форму I гидрохлорида. Пример 3. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорид. Стадия А. Тетрагидроциклопента[с]пиррол-1,3(2 Н,3 аН)-дион. Процедура была аналогичной описанной на стадии А примера 1. Стадия В. цис-Октагидроциклопента[с]пиррол. Процедура была аналогичной описанной на стадии В примера 1. Стадия С. цис-Октагидроциклопента[с]пиррол гидрохлорид. 2 г цис-октагидроциклопента[с]пиррола растворяли в 10 мл этанола в колбе. Раствор охлаждали до 0 С и после этого добавляли 1,64 мл концентрированной соляной кислоты раствор (11 М). Реакционную смесь перемешивали при 20 С в течение 30 мин, после этого концентрировали при пониженном давлении. Реакционную смесь перемешивали в метил-трет-бутиловом простом эфире при 0 С. Продукт выделяли путем фильтрации в форме твердого вещества с выходом 83% и с химической чистотой 99%. Тонка плавления: 126 С. Стадия D. 4-3-[цис-Гексагидроциклопента[с]пиррол-2(1 Н)-ил]пропоксибензамид гидрохлорид. 915 мг продукта, полученного на стадии С, 1,65 г триацетоксиборогидрида натрия, 45 мл ТГФ и 7,5 мл триметил ортоформиата добавляли в реактор. После этого добавляли 1 г соединения, полученного в приготовлении 2. Реакционную смесь нагревали при 40 С в течение 50 мин и затем охлаждали до температуры окружающей среды. После этого добавляли насыщенный NaHCO3 раствор. Водную фазу экстрагировали этилацетатом и затем органические фазы объединяли и промывали водой. Органическую фазу высушивали над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток суспендировали в смеси изопропанол/вода в присутствии соляной кислоты. Реакционную смесь нагревали при 40 С, затем охлаждали до 5 С. Продукт выделяли путем фильтрации в форме твердого вещества с выходом 33% и с химической чистотой 98%. Характеристика продукта, образованного таким образом, используя техники, представленные в примерах 4-5, свидетельствовала о том, что получали кристаллическую форму I гидрохлорида. Пример 4. Кристаллическая форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси бензамид гидрохлорида. Перед записью диаграммы дифракции рентгеновских лучей образцы, полученные в соответствии с процедурой, описанной в одном из примеров 1-3, измельчали в течение 30 с при 30 Гц в присутствии 100 мкл безводного этанола на 200 мг активного компонента в контейнере из нержавеющей стали объемом 25 мл, содержащем 2 шарика из нержавеющей стади. Запись данных осуществляли с помощью дифрактометра PANalytical X'Pert Pro MPD с детекторомX'Celerator в следующих условиях: напряжение 45 кВ, сила тока 40 мА,установка: тета/тета,анод: медь,K -1 длина волны: 1,54060 , K -2 длина волны: 1,54443 ,соотношение K -2/K -1: 0,5,режим измерения: непрерывно от 3 до 55 (угол Брэгга 2) с дискретностью 0,017,время измерения на стадию: 35,53 с. Таким образом полученная диаграмма порошковой рентгеновской дифракции формы I 4-3-[цисгексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида представлена в виде положений линии (угол Брэгга 2, выраженный в градусах 0,2), межплоскостное расстояние (выраженное в) и относительная интенсивность (выраженная в процентах относительно наиболее интенсивной линии). Существенные линии собраны в следующей таблице: Таким образом определяли следующие параметры: моноклинная кристаллическая элементарная ячейка,параметры элементарной ячейки: а = 10,6621 , b = 10,4945 , с = 15,6542 ,= 101,949,спейсерная группа: Р 1 21/с 1 (14),число молекул в элементарной ячейке: 4,объем элементарной ячейки: Vэлементарной ячейки = 1713,637 3,плотность: d = 1,2590 г/см 3. Пример 5. Кристаллическая форма I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропокси бензамид гидрохлорида. Форму I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида характеризовали с помощью спектроскопии Рамана. Спектры записывали в режиме на отражение (PerkinElmer) и трансмиссионном режиме (Cobalt) с лазерной фокусировкой 785 и 830 нм соответственно, используя CCD. Сдвиг длины волны зависит от материала и является характеристикой этого материала,который предоставляет возможность анализа химического состава и молекулярной расстановки исследуемого образца. Получали спектры в режиме на отражение с мощностью лазерного излучения 400 мВт, размер пятна 100 мкм, пять экспозиций по 5 с и спектральное разрешение 2 см-1,в трансмиссионном режиме с мощностью лазерного излучения 650 мВт, размер пятна 4 мм, двадцать экспозиций по 3 с и спектральное разрешение 2 см-1. Исследуемая спектральная область находилась в интервале от 0 до 3278 см-1 в режиме на отражение и от 37 до 2400 см-1 в трансмиссионном режиме. Существенные пики наблюдаются в следующих положениях: 1676 см-1, 1606 см-1, 1564 см-1, 1152[с]пиррол-2(1H)-ил]пропоксибензамида. Запись данных осуществляли с помощью дифрактометра PANalytical X'Pert Pro MPD с детекторомX'Celerator в следующих условиях: напряжение 45 кВ, сила тока 40 мА,установка: тета/тета,анод: медь,K -1 длина волны: 1,54060 ,K -2 длина волны: 1,54443 , соотношение K -2/K -1: 0,5,режим измерения: непрерывно от 3 до 55 (угол Брэгга 2) с дискретностью 0,017,время измерения на стадию: 35,53 с. Диаграмма порошковой рентгеновской дифракции формы I свободного основания 4-3-[цисгексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида, полученной в соответствии со способом одного из примеров 1-3, представлена в виде положений линии (угол Брэгга 2, выраженный в градусах 0,2), межплоскостное расстояние (выраженное в ) и относительная интенсивность (выраженная в процентах относительно наиболее интенсивной линии). Существенные линии собраны в следующей таблице:[с]пиррол-2(1H)-ил]пропоксибензамида. Форму I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида характеризовали с помощью спектроскопии Рамана. Спектры записывали в трансмиссионном режиме (Cobalt) с лазерной фокусировкой 830 нм, используя CCD. Сдвиг длины волны зависит от материала и является характеристикой этого материала, который предоставляет возможность анализа химического состава и молекулярной расстановки исследуемого образца. Получали спектры с мощностью лазерного излучения 650 мВт, размер пятна 4 мм, двадцать экспозиций по 0,9 с и спектральное разрешение 2 см-1. Исследуемая спектральная область находилась в интервале от 37 до 2400 см-1. Существенные пики наблюдаются в следующих положениях: 292 см-1, 618 см-1, 1045 см-1, 1483 см-1,1568 см-1, 1683 см-1. Пример 8. Кристаллическая форма I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида. Форму I свободного основания 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамида также характеризовали с помощью твердофазной ЯМР-спектроскопии. Твердофазные 13 С ЯМР спектры записывали при температуре окружающей среды, используя спектрометр Bruker SB Avance с типом зонда 4-мм CP/MAS SB VTN в следующих условиях: частота: 125,76 МГц,ширина спектра: 40 кГц,скорость вращения под магическим углом: 13 кГц,импульсная программа: Cross Polarization с декомпозицией SPINAL64 (мощность декомпозиции 80 кГц),задержка рецикла: 10 с,время исследования: 47 мс,время контакта: 4 мс,число сканирований: 4096. Таким образом, полученные спектры представляли относительно образца адамантана. Наблюдаемые пики представлены в следующей таблице (выраженные в ч. на млн 0,2): Пример 9: Фармацевтическая композиция. Состав для приготовления 1000 таблеток, каждая содержит 5 мг активного компонента (в пересчете на эквивалент основания) ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ промышленного синтеза соединения формулы (I) который отличается тем, что соединение формулы (II) подвергают реакции с аммиаком при температуре больше чем 100 С с образованием соединения формулы (III) которое восстанавливают, получая бициклический амин формулы (IV) где это соединение впоследствии подвергают либо реакции сочетания в щелочных условиях в полярной среде с соединением формулы (V) где R' и R" представляют собой, каждый независимо друг от друга, (C1-С 6)алкильную группу, или R' и R" вместе образуют группу -(СН 2)n-, где n = 2-3, или одна из групп R' и R" представляет собой атом водорода, а другая представляет собой (C1-С 6)алкильную группу,или восстановительному аминированию с соединением формулы (V) получая свободное основание соединения формулы (I), которое помещают в HCl с образованием соединения формулы (I), которое выделяют в виде твердого вещества. 2. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакционную смесь, полученную после осуществления реакции соединения формулы (II) с аммиаком, подвергают пиролизу. 3. Способ синтеза соединения формулы (I) в соответствии с п.2, где пиролиз осуществляют при температуре больше или равной 200 С. 4. Способ синтеза соединения формулы (I) в соответствии с п.2, где пиролиз осуществляют при температуре больше или равной 280 С. 5. Способ синтеза соединения формулы (I) в соответствии с п.1, где превращение соединения формулы (III) в соединение формулы (IV) осуществляют в присутствии водорода и металла или металлосодержащего катализатора. 6. Способ синтеза соединения формулы (I) в соответствии с п.1, где соединение формулы (V) представляет собой 4-(3-хлорпропокси)бензамид. 7. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в присутствии карбоната, амина или гидроксида. 8. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в присутствии карбоната калия или триэтиламина. 9. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в полярной среде, состоящей из одного или нескольких полярных растворителей, выбранных из воды, спиртов, кетонов, простых эфиров, амидов,ДМСО и ацетонитрила. 10. Способ синтеза соединения формулы (I) в соответствии с п.1, где реакцию сочетания соединения формулы (IV) с соединением формулы (V) осуществляют в смеси вода/ацетонитрил или смеси во- 10022741 да/изопропанол. 11. Способ синтеза соединения формулы (I) в соответствии с п.1, где стадию образования соли в присутствии HCl осуществляют в растворителе, выбранном из воды, ацетона и спирта. 12. Способ синтеза соединения формулы (I) в соответствии с п.1, где стадию образования соли в присутствии HCl осуществляют в ацетоне или изопропаноле. 13. Способ синтеза соединения формулы (I) в соответствии с одним из пп.1-6, где соединение формулы (I) подвергают перекристаллизации. 14. Соединение формулы (V) в которой Y представляет собой группу -CH2-OSO2-R, где R представляет собой (C1-С 6)алкильную группу или -C6H4-СН 3 группу. 15. Применение соединения формулы (V) в соответствии с п.14 для синтеза соединения формулы (I). 16. Соединение формулы (V) в которой R' и R" представляют собой, каждый независимо друг от друга, (С 1-С 6)алкильную группу, илиR' и R" вместе образуют группу -(СН 2)n-, где n = 2-3, или одна из групп R' и R" представляет собой атом водорода, а другая представляет собой (C1-С 6)алкильную группу. 17. Соединение формулы (V) в соответствии с п.16, которое представляет собой 4-(3,3-диэтоксипропокси)бензамид. 18. Применение соединения формулы (V) в соответствии с п.16 или 17 для синтеза соединения формулы (I). 19. Применение соединения формулы (V"), раскрытого в п.1, для синтеза соединения формулы (I). 20. Кристаллическая форма I соединения формулы (I), раскрытого в п.1 которая характеризуется диаграммой порошковой рентгеновской дифракции, имеющей следующие дифракционные линии (угол Брэгга 2, выраженный в градусах 0,2): 16,97, 17,84, 18,90, 20,32, 23,87,27,10, 27,86 и 30,34. 21. Кристаллическая форма I соединения формулы (I) в соответствии с п.20, которая характеризуется следующей диаграммой порошковой рентгеновской дифракции, измеренной с помощью дифрактометра PANalytical X'Pert Pro MPD с детектором X'Celerator и представленной в виде положений линии 22. Кристаллическая форма I соединения формулы (I) в соответствии с п.20 или 21, которая характеризуется спектром Рамана, имеющим существенный пик в положении 1606 см-1 или 1676 см-1. 23. Кристаллическая форма I соединения формулы (I) в соответствии с одним из пп.20-22, которая характеризуется спектром Рамана, имеющим существенные пики в положениях 1676 см-1, 1606 см-1, 1564 см-1, 1152 см-1, 830 см-1 и 296 см-1. 24. Фармацевтическая композиция, которая содержит в качестве активного компонента кристаллическую форму I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)-ил]пропоксибензамид гидрохлорида в соответствии с одним из пп.20-23, в комбинации с одним или несколькими фармацевтически приемлемыми, нетоксичными, инертными носителями. 25. Фармацевтическая композиция в соответствии с п.24, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли. 26. Фармацевтическая композиция в соответствии с п.24, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменции с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией. 27. Применение кристаллической формы I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства для лечения нарушений гистаминергической системы. 28. Применение кристаллической формы I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли. 29. Применение кристаллической формы I 4-3-[цис-гексагидроциклопента[с]пиррол-2(1H)ил]пропоксибензамид гидрохлорида в соответствии с одним из пп.20-23 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменции с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией. 30. Кристаллическая форма I свободного основания соединения формулы (I), раскрытого в п.1 которая характеризуется диаграммой порошковой рентгеновской дифракции, имеющей следующие дифракционные линии (угол Брэгга 2, выраженный в градусах 0,2): 6,25, 12,55, 17,74, 18,19, 19,43,20,72, 21,00, 23,50 и 27,00. 31. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.30,которая характеризуется следующей диаграммой порошковой рентгеновской дифракции, измеренной с помощью дифрактометра PANalytical X'Pert Pro MPD с детектором X'Celerator и представленной в виде положений линии (угол Брэгга 2, выраженный в градусах 0,2) и межплоскостного расстояния d (выраженного в ): 32. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.30 или 31, которая характеризуется спектром Рамана, имеющим существенный пик в положении 1683 см-1. 33. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с одним из пп.30-32, которая характеризуется спектром Рамана, имеющим существенные пики в положениях 292 см-1, 618 см-1, 1045 см-1, 1483 см-1, 1568 см-1, 1683 см-1. 34. Кристаллическая форма I свободного основания соединения формулы (I), раскрытого в п.1 которая характеризуется твердофазным 13 С CP/MAS ЯМР спектром, имеющим следующие пики (выраженные в ч. на млн 0,2): 112,2, 119,2, 127,2, 128,6, 132,4, 162,2 и 173,2 ч. на млн. 35. Кристаллическая форма I свободного основания соединения формулы (I) в соответствии с п.34,которая характеризуется твердофазным 13 С CP/MAS ЯМР спектром, имеющим следующие пики (выраженные в ч. на млн 0,2): 36. Фармацевтическая композиция, которая содержит в качестве активного компонента кристаллическую форму I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 в комбинации с одним или несколькими фармацевтически приемлемыми, нетоксичными, инертными носителями. 37. Фармацевтическая композиция в соответствии с п.36, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли. 38. Фармацевтическая композиция в соответствии с п.36, предназначенная для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменцией с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией. 39. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства для лечения нарушений гистаминергической системы. 40. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных со старением головного мозга и с нейродегенеративными заболеваниями, и также для лечения расстройств настроения, синдрома дефицита внимания с гиперактивностью, ожирения и боли. 41. Применение кристаллической формы I свободного основания соединения формулы (I) в соответствии с одним из пп.30-35 для приготовления лекарственного средства, предназначенного для лечения когнитивных и психоповеденческих нарушений, связанных с болезнью Альцгеймера, болезнью Паркинсона, болезнью Пика, корсаковским психозом, деменцией с тельцами Леви, фронтальной и субкортикальной деменцией, лобно-височной деменцией и сосудистой деменцией.
МПК / Метки
МПК: C07C 235/42, A61P 25/00, A61K 31/403, C07D 209/52
Метки: форма, синтеза, которые, кристаллическая, способ, фармацевтические, композиции, содержат, гидрохлорида, 4-{3-[цис-гексагидроциклопента[c]пиррол-2(1н)-ил]пропокси}бензамид
Код ссылки
<a href="https://eas.patents.su/14-22741-sposob-sinteza-i-kristallicheskaya-forma-4-3-cis-geksagidrociklopentacpirrol-21n-ilpropoksibenzamid-gidrohlorida-i-farmacevticheskie-kompozicii-kotorye-ee-soderzhat.html" rel="bookmark" title="База патентов Евразийского Союза">Способ синтеза и кристаллическая форма 4-{3-[цис-гексагидроциклопента[c]пиррол-2(1н)-ил]пропокси}бензамид гидрохлорида и фармацевтические композиции, которые ее содержат</a>
Предыдущий патент: Устройство для очистки короткого волокна от костры и неволокнистых примесей
Следующий патент: Система и способ безопасных операций управления скважиной
Случайный патент: Питающий бункер для поршневых насосов