Лечение вич
Формула / Реферат
1. Способ лечения ВИЧ, включающий введение пациенту пептида кортикотропинвысвобождающего фактора (CRF) и пептида проопиомеланокортина или продукта, содержащего проопиомеланокортин.
2. Способ по п.1, где достигаются один или несколько следующих эффектов: сокращение вирусной нагрузки; увеличение количества CD4 клеток или увеличение количества CD8 клеток.
3. Способ по п.1, где CRF является нечеловеческим CRF.
4. Способ по п.3, где CRF является CRF козы.
5. Способ по любому из пп.1-4, дополнительно включающий введение одного или нескольких регуляторных пептидов или рилизинг-факторов.
6. Способ по п.5, где факторы выбраны из группы, включающей a-HLA, TGF-b и IL-10.
7. Способ по любому из предыдущих пунктов, дополнительно включающий введение одного или нескольких соединений, выбранных из вазопрессина, бета-эндорфина и энкефалина.
8. Способ по любому из предыдущих пунктов, дополнительно включающий введение связывающего белка CRF, CRF-BP.
9. Способ по любому из предыдущих пунктов, дополнительно включающий введение двух или нескольких соединений, выбранных из альфа-, бета- и гамма-меланоцитстимулирующего гормона (MSH); адренокортикотропина (АСТН); бета- и гамма-липотропина (LPH).
Текст
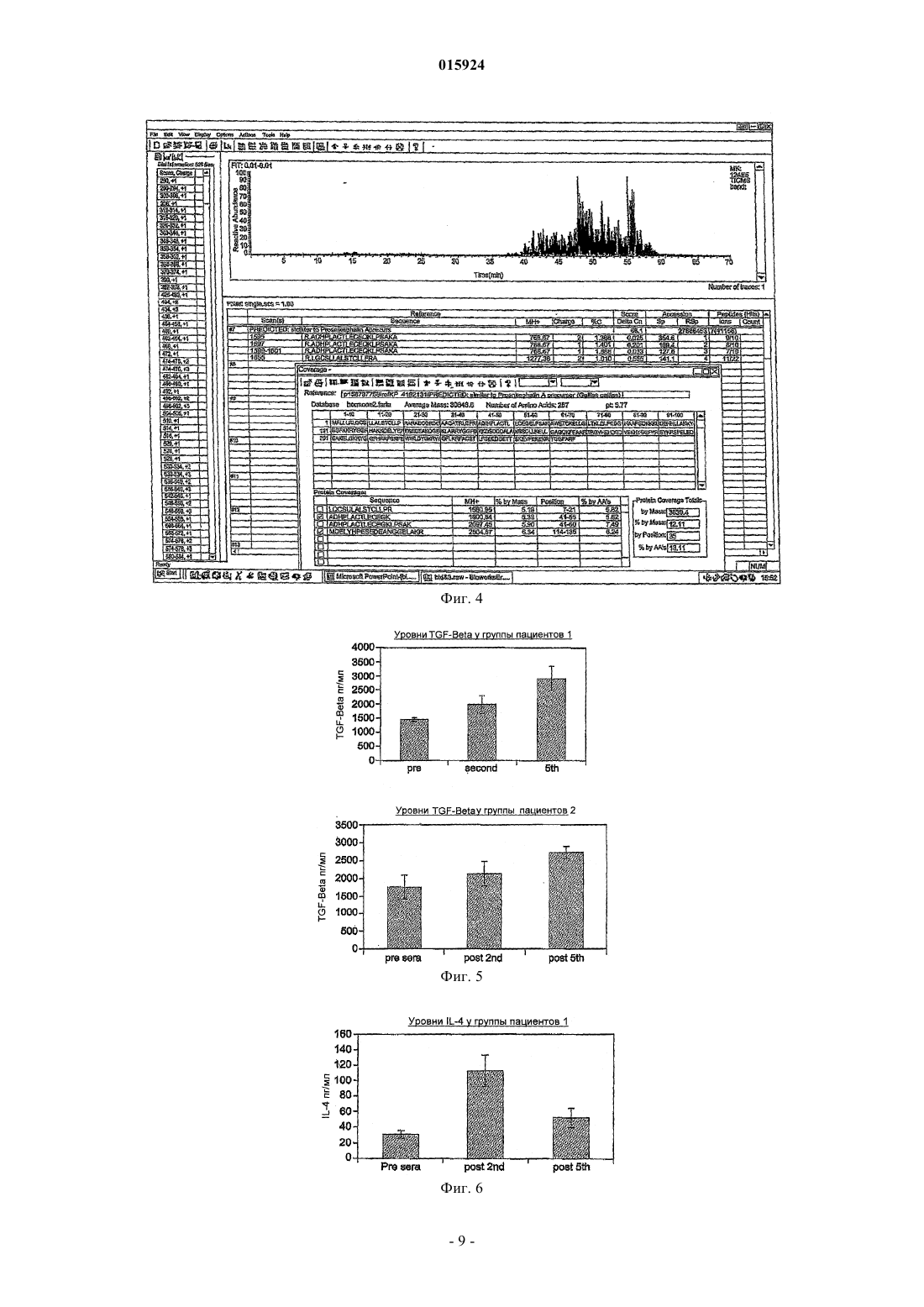
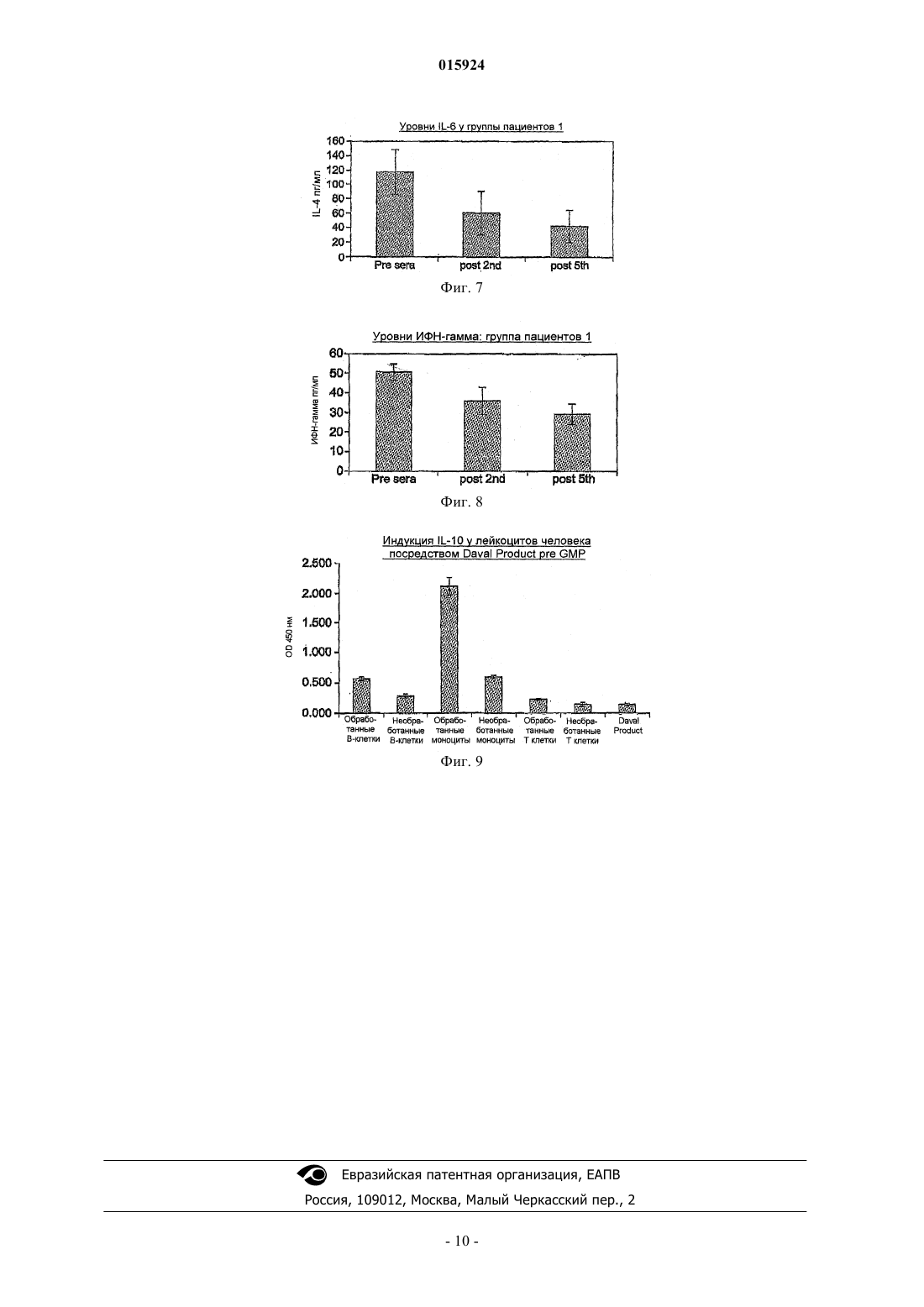
Дата публикации и выдачи патента Номер заявки Предлагаются способы лечения ВИЧ с помощью пептидов проопиомеланокортина (РОМС) и кортикотропинвысвобождающего фактора (CRF) и их продуктов, а также применение таких пептидов для получения лекарственных средств. 015924 Область техники Настоящее изобретение относится к способам лечения ВИЧ и к применению РОМС и/или CRF пептидов для получения лекарственного средства для лечения ВИЧ. Уровень техники Эпидемия вируса/синдрома приобретенного иммунодефицита человека (ВИЧ/СПИД) является причиной более чем 20 млн смертельных случаев во всем мире и в настоящее время поразила приблизительно 40 млн человек. Это оказывает серьезное социально-экономическое влияние особенно на развивающиеся страны. До настоящего времени единственным эффективным оружием против ВИЧ и СПИДа является терапия, в частности высокоактивная антиретровирусная терапия (HAART). Однако она не является доступной по всему миру, может иметь токсичные побочные эффекты, и часто те, кто больше всего нуждается, лишены такого лечения. Поэтому необходимость в эффективной терапевтической вакцине против ВИЧ или профилактическом лечении стали все более и более чрезвычайно необходимыми. Заявка на международный патент PCT/GB2005/050108 описывает применение кортикотропинвысвобождающего фактора (CRF) и/или пептидов проопиомеланокортина (РОМС) в лечении спектра заболеваний у больных. Читателя отсылают к PCT/GB2005/050108 для списка заболеваний, которые можно лечить. Подготовка продукта сыворотки козы описана в заявках на международные патентыWO 03/004049 и WO 03/064472; теперь мы полагаем, что этот серологический продукт может быть пригодным источником CRF и РОМС пептидов, которые могут быть применены в настоящем изобретении. Мы установили, что CRF и/или РОМС пептиды пригодны для лечения ВИЧ и, в частности, для снижения вирусной нагрузки и/или повышения количества CD4+ и CD8 клеток у больных.CRF является пептидом, который образуется в гипоталамусе, и считается, что он вовлечен в ответ на стресс. Человеческий CRF подробно описан в ссылке 122560 OMIM (online mendelian inheritance inman, доступном через http://www.ncbi.nlm.nih.gov/). Нуклеотидная и аминокислотная последовательности человеческого CRF также известны и имеют номер доступа ВС 011031 в GENBANK. Знание данных последовательности и размера для человеческого CRF позволит квалифицированному специалисту определить эквивалентную информацию для нечеловеческого CRF, включая CRF козы. CRF также известен как кортикотропинвысвобождающий гормон (CRH). Под "CRF пептидом" понимают любой пептид, имеющий соответствующую последовательность,структуру или функцию. Для квалифицированного специалиста будет очевидно, что каноническая нуклеотидная и/или аминокислотная последовательности, данные для человеческого CRF в статье GENBANK, на которую ссылаются выше, могут быть различны до известной степени, не повреждая структуру или функцию пептида. В частности, аллельные варианты и функциональные мутанты включены в объем настоящего определения. Мутанты могут включать консервативные аминокислотные замены и фрагменты и производные CRF. Введение CRF пациенту, как полагают, стимулирует продукцию эндогенного CRF, который, в свою очередь, стимулирует продукцию проопиомеланокортина (РОМС) и соответствующих составляющих его пептидов. РОМС является пептидом (прогормоном), продуцируемым гипофизом (так же как и многими другими органами, определенными опухолями, такими как меланомой, и нормальными клетками кожи), который является предшественником ряда кортикотропных гормонов, которые проявляют ряд эффектов на организм. РОМС является предшественником альфа-, бета- и гамма-меланоцитстимулирующего гормона(MSH); адренокортикотропного гормона (АСТН); бета- и гамма-липоторопина (LPH) и бета-эндорфина. Все эти гормоны получаются расщеплением единственного большого предшественника, РОМС, и названы здесь "продуктами РОМС". Человеческий РОМС подробно описан в статье 176830 OMIM (online mendelian inheritance in man,доступном через http://www.ncbi.nlm.nih.gov/). Нуклеотидная и аминокислотная последовательности человеческого РОМС также известны и имеют номер доступа ВС 065832 в GENBANK. Человеческий РОМС дает начало гликозилированному белковому предшественнику, имеющему молекулярную массу 31 кДа. Под "РОМС пептидом" подразумевают любой пептид, имеющий соответствующую последовательность, структуру или функцию. Для квалифицированного специалиста будет очевидно, что каноническая нуклеотидная и/или аминокислотная последовательности, приведенные для человеческого РОМС в статье GENBANK, на которую ссылаются выше, могут быть различны до известной степени, не повреждая структуру или функцию пептида. В частности, аллельные варианты и функциональные мутанты включены в объем настоящего определения. Мутанты могут включать консервативные аминокислотные замены."РОМС пептид", как применено в настоящем описании, относится к любому пептиду, действующему как предшественник по меньшей мере одной формы MSH, АСТН, по меньшей мере одной формы LPH, эндорфина, метэнкефалина и лейэнкефалина; и предпочтительно всех -, - и -MSH; ACTH; - и -LPH; и -эндорфина, метэнкефалина и лейэнкефалина.-1 015924 Сущность изобретения Согласно первому аспекту настоящего изобретения представлен способ лечения ВИЧ, содержащий введение пациенту пептида кортикотропин рилизинг-гормона (CRF). Лечение может быть применено для достижения одного или более следующих далее эффектов: снижение вирусной нагрузки, увеличение CD4 клеток или увеличение CD8 клеток. Мы полагаем, что лечение может быть успешно применено против ВИЧ и СПИДа у пациентовлюдей. Не желая быть связанными теориями, мы полагаем, что лечение ограничивает и контролирует распространение вируса по организму посредством снижения уровней чрезмерного иммунного ответа,необходимого для репликации и распространения вируса. Кроме того, оно может управлять воспалением, вызванным условно-патогенными инфекциями и последующей продукцией провоспалительных цитокинов, которые поддерживают и стимулируют репликацию и распространение вируса. Само по себе оно снижает вирусную нагрузку у ВИЧ пациентов, увеличивает количества CD4 и CD8 в крови, улучшает либидо, стимулирует аппетит и значительно улучшает качество жизни ВИЧ/СПИД пациентов.CRF может быть нечеловеческим CRF; предпочтительно CRF копытного и наиболее предпочтительно CRF козы. Неожиданно было установлено, что сыворотка козы содержит CRF, в особенности,если коза была подвергнута физиологическому стрессу, такому как кровотечение или иммунизация. Это предоставляет удобный источник CRF для фармацевтических композиций настоящего изобретения. Также полагают, что CRF может иметь самоподдерживающийся эффект у пациента, у которого введение исходного количества CRF приводит к продукции эндогенного CRF пациентом; таким образом, начальное введение низкого уровня CRF может иметь значительный эффект у пациента, включая увеличение уровней РОМС пептидов. Конечно, пептиды, полученные от животных помимо коз, могут быть применены, также как и рекомбинантные или другие источники пептида. Введение пептидов, как применено в настоящем изобретении, может быть достигнуто перорально или парентерально. Способы парентеральной доставки включают местное, внутриартериальное, внутримышечное, подкожное, костно-мозговое, внутриоболочковое, внутрижелудочковое, внутривенное, интраперитонеальное или внутриносовое введение. В дополнение к действующим веществам применяемые композиции могут включать подходящие фармацевтически приемлемые носители, включая наполнители и другие компоненты, которые облегчают обработку действующих соединений в лекарственные средства, подходящие для фармацевтического введения. Фармацевтические композиции для перорального приема могут быть составлены, применяя фармацевтически приемлемые носители, известные в области техники в дозировках, подходящих для перорального приема. Такие носители позволяют составить также композиции, такие как таблетки, пилюли,драже, капсулы, жидкости, гели, сиропы, кашица, суспензии и т.п., подходящие для глотания субъектом. Фармацевтические препараты для перорального приема могут быть получены путем комбинирования действующих соединений с твердым наполнителем, необязательно размалывая получаемую смесь и обрабатывая смесь гранул, после добавления подходящих добавочных соединений, если желательно получить таблетки или драже. Подходящие наполнители включают углеводные или белковые наполнители,такие как сахар, включая лактозу, сахарозу, маннитол, сорбитол; крахмал из кукурузы, пшеницы, риса,картофеля или других растений; целлюлозу, такую как метилцеллюлозу, гидроксипропилметилцеллюлозу или натрия карбоксиметилцеллюлозу; и камеди, включая арабскую и трагакант; так же как и белки,такие как желатин и коллаген. При желании, можно добавить солюбилизирующие вещества, такие как поперечно сшитый поливинилпирролидон, агар, альгиновую кислоту или соль таковой. Драже могут быть представлены с подходящими покрытиями, такими как концентрированные растворы сахара, которые могут также содержать арабскую камедь, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль, диоксид титана, растворы лака и подходящие органические растворители или смеси растворителей. Красители или пигменты можно добавлять к таблеткам или покрытиям драже для идентификации продукта или различения количеств действующего соединения. Фармацевтические композиции, которые могут быть применены перорально, включают плотно заполненные капсулы, сделанные из желатина, так же как и мягкие, герметичные капсулы, сделанные из желатина и покрытия, такого как глицерин или сорбит. Плотно заполненные капсулы могут содержать действующие вещества, смешанные с наполнителем или связывающими веществами, такими как лактоза или крахмалы, смазывающими веществами, такими как тальк или стеарат магния, и, необязательно, стабилизаторами. В мягких капсулах действующие соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидком парафине или жидком полиэтиленгликоле с или без стабилизаторов. Фармацевтические композиции для парентерального введения включают водные растворы действующих соединений. Для инъекций фармацевтические композиции изобретения могут быть составлены в водных растворах, предпочтительно в физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или физиологический солевой буфер. Инъекции водных суспензий могут содержать вещества, которые повышают вязкость суспензии, такие как натрий карбоксиметилцеллюлоза, сорбитол или декстран. Дополнительно, суспензии действующих соединений могут быть приготовлены как соответствующие масляные суспензии для инъекций. Подходящие липофильные растворители или транс-2 015924 портные средства включают жирные масла, такие как масло сезама, или синтетические эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Необязательно, суспензия может также содержать подходящие стабилизаторы или средства, которые увеличивают растворимость соединений для возможности получения высококонцентрированных растворов. Для местного или носового введения в композиции можно применять смачивающие вещества, подходящие для специфического барьера, который требуется преодолеть. Фармацевтические композиции для применения в настоящем изобретении могут быть получены преимущественно в соответствии со стандартными способами получения, известными в области техники. Пептиды или композиции для применения в настоящем изобретении могут быть лиофилизированы. Это улучшает срок хранения и устойчивость продукта и улучшает транспортабельность. Это особенно полезно для применения в теплых климатах и где услуги охлаждения могут быть свободно не доступны. Лиофилизированный продукт может быть ресуспендирован перед введением. Способ может далее включать введение одного или более пептидрегулирующего или рилизингфактора, которые могут вызвать каскад высвобождения дополнительных пептидов множеством клеток пациента. Такие дополнительные факторы предпочтительно получают из того же самого источника, как и CRF, в частности из сыворотки козы. Подходящие факторы, среди других, включают -HLA, TGF- иIL-10. В предпочтительных вариантах осуществления способ может включать введение одного или нескольких из вазопрессина, бета-эндорфина и энкефалина. В определенных вариантах осуществления способ может включать введение CRF связывающего белка, CRF-BP. Он связывает CRF и может действовать как резервуар для последующего высвобождения CRF у пациента. Способ может дополнительно включать введение РОМС пептида или РОМС продукта; определенные РОМС продукты могут быть пригодны для введения пациенту для стимуляции дополнительной продукции или получения желательной реакции прежде, чем эндогенный РОМС сможет быть получен. Дополнительный аспект настоящего изобретения предоставляет способ лечения ВИЧ, содержащий введение РОМС пептида и/или РОМС продукта пациенту. Предпочтительно РОМС является нечеловеческим РОМС; обычно РОМС копытного; и наиболее предпочтительно РОМС козы. Хотя РОМС производится в гипофизе и, как ожидается, не будет присутствовать в сыворотке, по меньшей мере, в значительной степени, было неожиданно установлено, что сыворотка козы содержит РОМС, РОМС-связанные пептиды и молекулы, связанные с каскадом РОМС,особенно когда коза подвергается физиологическому стрессу, такому как кровотечение или иммунизация. Это представляет удобный источник для РОМС для фармацевтических композиций настоящего изобретения. Также полагают, что РОМС может иметь самоподдерживающийся эффект у пациента, так что введение начального количества РОМС приводит к эндогенной продукции РОМС у пациента; таким образом, начальное введение низкого уровня РОМС может иметь значительное влияние на пациента. Как сCRF пептидами, можно применять источники пептидов РОМС помимо козы, включая рекомбинантный РОМС. Считается, что при введении РОМС и связанных с ним молекул субъекту пептид расщепляется для предоставления одного или более продуктов РОМС в свободно доступной форме субъекту; также происходит индукция молекулярного каскада, который стимулирует гипоталамо-гипофизарнонадпочечниковую ось (НРА). Согласно дополнительному аспекту изобретения представлен способ лечения ВИЧ, включающий введение двух или нескольких из альфа-, бета- и гамма-меланоцитстимулирующих гормонов (MSH); адренокортикотропного гормона (АСТН); бета- и гамма-липотропина (LPH) и бета-эндорфина. Учитывая вероятный протеолиз РОМС при введении, может быть возможным достигнуть подобных эффектов посредством введения двух или более из индивидуальных гормонов, полученных из РОМС. Перечисленные гормоны могут быть предоставлены как индивидуальные пептиды или как одна или более молекул предшественника (например, частичные продукты расщепления РОМС). Предпочтительно три, четыре,пять, шесть или семь из гормонов включены в фармацевтическую композицию, которая (необязательно вместе с CRF) запускает каскад для длительной продукции таких молекул. Различные компоненты могут быть представлены в комбинации с одной или более молекулами носителя, которые связывают один или несколько компонентов и, таким образом, служат депо или резервом для высвобождения компонента. Молекула носителя может также быть применена в комбинации с РОМС и связанными с ним пептидами. Оптимальная дозировка РОМС или CRF пептидов еще не была определена, однако может подойти назначение пептидов в дозировке от 0,01 до 10 мг/кг субъекту, более предпочтительно от 0,01 до 5 мг/кг,от 0,025 до 2 мг/кг и наиболее предпочтительно от 0,05 до 1 мг/кг. Точная дозировка, которая будет применяться, может быть различна в зависимости от таких факторов, как возраст, пол и вес пациента, способа введения и композиции, так же как природы и тяжести расстройства, которое будут лечить. Могут быть приняты во внимание другие факторы, такие как диета,время введения, состояние пациента, комбинирование лекарственных средств и реакции чувствительности. Эффективный режим лечения может определить клинический врач, ответственный за лечение. Мо-3 015924 гут быть назначены одно или несколько введений, и обычно благоприятные эффекты наблюдаются после серии по меньшей мере трех, пяти или более введений. Повторное введение может быть желательным для поддержания благоприятных эффектов композиции. Лечение можно применять посредством любого эффективного пути, предпочтительно посредством подкожной инъекции, хотя альтернативные пути, которые можно применять, включают внутримышечную или внутрираневую инъекцию, пероральный, аэрозольный, парентеральный или местный. При лечении предпочтительно используется жидкая композиция, хотя можно применять и другие композиции. Жидкая композиция может быть восстановлена из лиофилизированной композиции. Например, композицию можно смешивать с подходящими фармацевтически приемлемыми носителями и можно получать в виде твердой пищи (таблетки, пилюли, капсулы, гранулы и т.д.) в подходящей композиции для перорального, местного или парентерального введения. Изобретение также представляет применение CRF для получения лекарственного средства для лечения ВИЧ. Также представлено применение РОМС для получения лекарственного средства для лечения ВИЧ. CRF или РОМС можно выделять, очищенные CRF или РОМС, при этом предпочтительно их применять в комбинации с различными другими компонентами, как обсуждено выше. В частности, можно применять биоактивные белки носители и вазопрессин. Краткое описание чертежей Эти и другие аспекты настоящего изобретения будут теперь описаны посредством примера только в отношении приведенных чертежей, на которых: на фиг. 1-4 представлены результаты масс-спектрометрии продуктов ферментативного расщепления компонентов сыворотки; на фиг. 5-9 приведено подтверждение переключения в воспалительном профиле пациентов после лечения композицией. Подробное описание изобретения Публикации международных патентов WO 03/004049 и WO 03/064472 описывают получение композиции сыворотки козы. Краткое описание способа получения приведено ниже. Подготовка серологической композиции. Козе делают прививку посредством внутримышечной инъекции лизированным вирусом ВИЧ-3b,суспендированным в нормальном коммерческом супернатанте, применяя внутримышечную инъекцию ВИЧ-3b в концентрации 109 вирусных частиц в мл. Вирус предварительно убит высокой температурой при 60 С в течение 30 мин. В оптимизированной процедуре козе каждую неделю в течение четырех недель делают инъекцию, затем на шестой неделе животному делают кровоизвлечение для получения реагента. Приблизительно 400 см 3 крови забирают у козы в стерильных условиях. Животному можно провести повторное кровоизвлечение через 10-14 дней, когда объем крови восполнен. Для стимулирования продукции действующих компонентов в сыворотке может быть полезно применять режим перед кровоизвлечением. Все последующие шаги подготовки предпочтительно выполнять при 4 С, если не указано иначе. Далее для отделения сыворотки кровь центрифугируют и для удаления больших сгустков и частиц сыворотку фильтруют. Далее сыворотку обрабатывают пересыщенным сульфатом аммония(47%-ный раствор при 4 С) преципитации антител и другого материала. Полученный раствор центрифугирую в Beckman J6M/E центрифуге при 3500 об/мин в течение 45 мин, после чего надосадочную жидкость удаляют. Преципитированные иммуноглобулины и другой твердый материал ресуспендируют в буфере PBS (фосфатный солевой буфер), достаточном для повторного растворения преципитата. Далее раствор подвергают диафильтрации в буфере PBS с границей пропускания молекулярной массы 10000 дальтон (Да) при 4 С. После диафильтрации продукт фильтруют через 0,2-микронный фильтр в стерильный контейнер и доводят концентрацию белка до от 4 до 5 мг/мл. Раствор помещают в пузырьки для создания единичных лекарственных форм по 1 мл и оставляют на хранение при -22 С до применения. Анализ серологической композиции. В PCT/GB2005/050108 сообщается, что серологическая композиция, подготовленная таким образом, содержит РОМС и CRF пептиды и указывает на активную роль этих пептидов в эффектах сыворотки. Краткое изложение анализа сыворотки представлено ниже. Образец композиции фракционировали на геле и выполняли Вестерн-блоттинг, используя при этом антитела кэндорфину. Определяли сильный сигнал, обозначая присутствиеэндорфина, хотя видимая молекулярная масса составила приблизительно 31 кДа, намного больше, чем ожидаемый размерэндорфина. Это заставило предположить, чтоэндорфин присутствовал в образце как часть большего пептида; размера, соответствующего такому для РОМС. Выполняют масс-спектрометрию композиции и обнаруживают по меньшей мере два РОМСпроизводных пептида,эндорфин и кортикотропинсвязанные молекулы. CRH-BP был также идентифицирован.-4 015924 Фиг. 1-4. Пептиды РОМС и CRF-BP были идентифицированы в продукте посредством Thermofinnegan LCQ масс-спектрометрии. CRF главным образом регулирует синтез и секрецию АСТН в передней доле гипофиза. Введение РОМС и/или составляющих его пептидов в дополнение к CRF и CRF-BP, как думают,инициирует каскадный эффект, таким образом усиливая продукцию системной и поддерживающей увеличенных концентраций пептидов РОМС. CRF-BP способен действовать в качестве источника CRF. На фиг. 1-4 представлены пики, полученные при масс-спектрометрическом анализе триптических гидролизатов материала, очищенного от примесных белков посредством SDS-PAGE. Как указано выше,некоторые из этих молекул являются индукторами и регуляторами каскада РОМС. Дополнительное исследование, применяя более прицельный анализ (например, фракционирование пептидов, иммунопреципитацию и концентрирование), покажет большее количество присутствующих пептидов. На фиг. 1 указано присутствие производного РОМС-кортикотропина, на фиг. 2 - то же для CRF-BP, на фиг. 3 - то же для проэнкефалина А и на фиг. 4 - то же для проэнкефалина В. Присутствие CRF-BP предполагает, что материал содержит некоторое количество CRF, в то время как РОМС и связанные пептиды также очевидно присутствуют. Мы также изучили эффекты лечения серологической композицией из собственных сывороток пациентов. Эти эффекты описаны ниже. Доказательство переключения с провоспалительного ТН-1 профиля на противовоспалительный цитокиновый профиль ТН-2 у получавших лечение пациентов. На фиг. 5 представлены уровни TGF- в сыворотке двух групп пациентов (здоровые добровольцы) до и после лечения продуктами козьей сыворотки, приготовленными как описано. Две группы пациентов(n=3 для каждой группы) продемонстрировали отличающиеся реакции по полученным концентрациямTGF-, но все пациенты продемонстрировали увеличение серологических уровней в ответ на лечение(pre sera=серологические уровни пациентов перед лечением; post 2nd и post 5th=после 2-го и 5-го введения). Данные показывают, что лечение вызывает повышение концентрации противовоспалительного цитокина TGF-. На фиг. 6 представлены уровни IL-4 в сыворотке одной группы пациентов до (pre-sera) и после лечения. Можно заметить, что после лечения (post 2nd) уровни IL-4 значительно возросли в сыворотках пациентов (n=5). Однако после 5-го введения уровни IL-4 у всех пациентов снизились, но остались выше,чем были перед лечением. IL-4, как известно, снижает продукцию провоспалительных цитокинов клетками ТН-1. Может быть, что закономерные изменения в концентрации, наблюдаемые у всех пациентов,согласуются с ролью IL-4 в переключении с ТН-1 на ТН-2. На фиг. 7 представлены уровни IL-6 в сыворотках одной группы пациентов до и после лечения. Можно заметить, что после лечения (post 2nd и post 5th) уровни IL-6 в сыворотках пациентов (n=4) снижаются. На фиг. 8 представлены уровни IFN- в сыворотках одной группы пациентов до и после лечения. Можно заметить, что после лечения (post 2nd и post 5th) уровни IFN- в сыворотках пациентов снижаются. На фиг. 9 представлено, что обработка человеческих клеток периферической крови (РВМС) вызывает продукцию противовоспалительного цитокина IL-10 субполуляцией моноцитов. Т- и В-лимфоциты и моноциты были отделены от РВМС, полученных от добровольцев. Все типы клетки обработали эквивалентными лозами продукта в течение 16 ч и их супернатанты анализировали на содержание IL-10,применяя ELISA. Можно заметить, что уровни IL-10, продуцируемого популяцией Т-лимфоцитов, не изменялся в ответ на обработку, и что только небольшое увеличение IL-10 было индуцировано у Влимфоцитов. Однако значительное увеличение концентрации IL-10 в ответ на обработку было вызвано в популяции моноцитов. Все измерения были сделаны в трех повторенияхстандартные отклонения. Эти данные являются репрезентативными по меньшей мере для трех отдельных экспериментов. Вывод и заключения. Выше и в PCT/GB2005/050108 мы показали, что продукт сыворотки козы, как описано, содержит пептиды и продукты РОМС и пептиды CRF. Мы также показали, что введение продукта сыворотки вызывает переключение в воспалительном профиле пациентов. В WO 03/004049 описано применение продукта сыворотки козы, полученного как описано, для лечения пациентов с ВИЧ. В этой публикации высказано предположение, что благоприятные эффекты сыворотки на ВИЧ являются результатом присутствия anti-Fas и anti-HLA молекул, но нет никакого предположения, что могли присутствовать РОМС или CRF пептиды. В публикации представлены наблюдения, что у пациентов, получивших сыворотку, происходит увеличение числа CD4 и CD8 клеток, снижение вирусной нагрузки и снижение значений Р 24. В WO 02/07760 также описывается получение и применение того же самого продукта сыворотки козы для лечения пациентов с ВИЧ. В публикации представлены экспериментальные данные, показывающие нейтрализацию SIV in vitro. В примере 3 публикации описано получение продукта сыворотки козы таким же способом, как и в настоящем описании. Введение сыворотки приводит к уменьшению ВИЧ вирусной нагрузки (определяемой как количество копий РНК ВИЧ-1 в мл плазмы) и увеличению-5 015924 числа CD4 и CD8 клеток. Опять же, никакого предположения о том, что это может быть результатом присутствия РОМС или CRF пептидов, не сделано. Ввиду результатов PCT/GB2005/050108 и данных, представленных в настоящем описании, что продукт сыворотки козы содержит пептиды и продукты РОМС и пептиды CRF и что эти пептиды и продукты являются активными биологическими веществами, мы полагаем, что эти пептиды и продукты могут быть пригодны в лечении ВИЧ и/или СПИДа у людей для получения среди других эффектов одного или нескольких из снижения вирусной нагрузки, увеличения количества CD4 клеток и увеличения количества CD8 клеток. Также известно, что ВИЧ вызывает разнообразные поражения центральной нервной системы(ЦНС), которые приводят к нейродегенерации и ряду нервных болезней. Они включают ВИЧ-энцефалит,ВИЧ-лейкоэнцефалопатию, аксональное повреждение и диффузную полиодистрофию, которая связана с гибелью нейронов различной степени тяжести. Последнее, как полагают, является результатом процесса апоптоза. Эти состояния приводят к потере когнитивной функции и деменции. Ввиду описанных эффектов POMC/CRF пептидов при нейродегенеративных нарушениях (см. PCT/GB2005/050108), вероятно,что такие пептиды могут быть применены для облегчения этих симптомов ВИЧ/СПИДа, так же как и непосредственно ВИЧ/СПИДа. Было также сообщено, что гипоталамо-гипофизарно-надпочечниковая ось (НРА) у людей, зараженных вирусом ВИЧ, нефункциональна. Воздействие на сеть цитокинов может иметь благоприятные эффекты в контроле ВИЧ-инфекции. Стимуляция рецепторов меланокортина на воспалительных клетках могла бы быть эффективным терапевтическим подходом для изменения течения ВИЧ-инфекции. Пептиды, производные проопиомеланокортина, присутствующие в продукте сыворотки, описанном в настоящем описании, включают адренокортикотропный гормон [АСТН(1-39)], -меланоцит стимулирующий гормон [-MSH(1-13)] и родственные аминокислотные последовательности. Пептиды меланокортина обладают мощной противовоспалительной/антицитокиновой активностью. Цитокины, такие как интерлейкин-1 (IL-1) и фактор некроза опухолей (TNF), могут быть вредными для ВИЧ зараженных пациентов. Были исследованы эффекты меланокортинов на продукцию IL-1 и TNF в крови ВИЧ-пациентов. Когда продукцию цитокинов измеряли в образцах цельной крови, стимулируемых LPS в присутствии или отсутствии -MSH(1-13), -MSH(11-13), АСТН(1-24) или АСТН(1-39),было установлено, что меланокортины снижали продукцию обоих цитокинов зависимым от концентрации образом. В отдельных экспериментах на мононуклеарных клетках нормальной периферической крови (РВМС) было установлено, что -MSH(1-13) подавляет продукцию IL-10 и TNF-, индуцированных посредством гликопротеида gp 120 капсида ВИЧ. Эти результаты предполагают, что стимуляция рецепторов меланокортина на воспалительных клетках могла бы стать новым способом снижения продукции цитокинов, которые поддерживают репликацию ВИЧ. РОМС и CRF пептиды и продукты, или индивидуально или в комбинации, представляют новый фармацевтический продукт, который обладает способностью регулировать НРА ось и служить источником меланокортинов и регулятором продукции меланокортинов. В частности, как представляют, он преобразовывает чрезмерный провоспалительный ТН 1 в противовоспалительный ТН 2 цитокиновый профиль. Таким образом, продукция и высвобождение воспалительных цитокинов подвергается регуляции. Существует доказательство, которое подтверждает заявление, что ВИЧ-инфекция облегчается посредством инфицирования моноцитов-макрофагов посредством множественных механизмов. АктивацияNF-kB условно-патогенными инфекциями при СПИДе увеличивает экспрессию рецепторов CCR5 и экспрессию TNF-, оба из которых являются разрешающими для поддерживания ВИЧ инфицирования. В дополнение, было установлено, что сокращение вирусной нагрузки связано с лечением зараженной и/или воспаленной ткани; это дополнительно поддерживает связь между активацией иммунитета и репликацией вируса. Таким образом, лечение пациентов POMC/CRF пептидами и/или продуктами, которые снижают воспаление ткани и уровни провоспалительных цитокинов и активации макрофагов, будут снижать инфективность клеток у пациентов и, возможно, распространение инфекции на органы тела, такие как мозг. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения ВИЧ, включающий введение пациенту пептида кортикотропинвысвобождающего фактора (CRF) и пептида проопиомеланокортина или продукта, содержащего проопиомеланокортин. 2. Способ по п.1, где достигаются один или несколько следующих эффектов: сокращение вирусной нагрузки; увеличение количества CD4 клеток или увеличение количества CD8 клеток. 3. Способ по п.1, где CRF является нечеловеческим CRF. 4. Способ по п.3, где CRF является CRF козы. 5. Способ по любому из пп.1-4, дополнительно включающий введение одного или нескольких регуляторных пептидов или рилизинг-факторов. 6. Способ по п.5, где факторы выбраны из группы, включающей -HLA, TGF- и IL-10. 7. Способ по любому из предыдущих пунктов, дополнительно включающий введение одного или нескольких соединений, выбранных из вазопрессина, бета-эндорфина и энкефалина. 8. Способ по любому из предыдущих пунктов, дополнительно включающий введение связывающего белка CRF, CRF-BP. 9. Способ по любому из предыдущих пунктов, дополнительно включающий введение двух или нескольких соединений, выбранных из альфа-, бета- и гамма-меланоцитстимулирующего гормона (MSH); адренокортикотропина (АСТН); бета- и гамма-липотропина (LPH).
МПК / Метки
МПК: A61K 38/35, A61K 38/22, A61K 38/34, A61K 38/17, A61K 38/33, A61P 37/02
Код ссылки
<a href="https://eas.patents.su/11-15924-lechenie-vich.html" rel="bookmark" title="База патентов Евразийского Союза">Лечение вич</a>
Предыдущий патент: Гуманизированное антитело к c-kit и его применение
Следующий патент: Способ получения полипептидов
Случайный патент: Производные гетероарилпиперидинов и -пиперазинов в качестве фунгицидов