Серотонинергические средства
Номер патента: 5925
Опубликовано: 25.08.2005
Авторы: Келли Майкл Джерард, Чилдерс Уэйн Эверетт, Розенцвейг-Липсон Шэрон Джой
Формула / Реферат
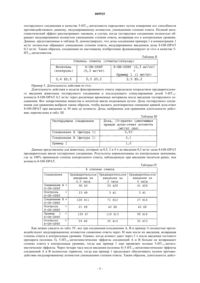
1. Соединение формулы (III)
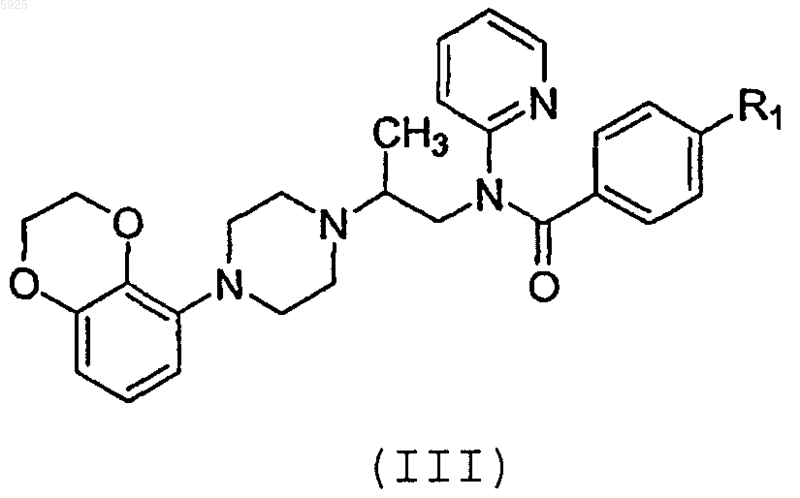
где R1 представляет собой циано, нитро, трифторметил или галоген или его фармацевтически приемлемые кислотно-аддитивные соли.
2. Соединение по п.1, где R1 представляет собой циано.
3. Соединение, представляющее собой (R)-4-циано-N-{2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил}-N-пиридин-2-илбензамид или его фармацевтически приемлемые кислотно-аддитивные соли.
4. Соединение, представляющее собой гидрохлорид (R)-4-циано-N-{2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил}-N-пиридин-2-илбензамида.
5. Соединение по любому из пп.1-4, где R-изомер находится в энантиомерном избытке по отношению к S-изомеру.
6. Соединение по любому из пп.1-5, где содержание R-стереоизомера составляет около 90 мас.% или более и S-стереоизомера около 10 мас.% или менее.
7. Соединение по любому из пп.1-5, где содержание R-стереоизомера составляет около 99 мас.% и S-стереоизомера около 1 мас.%.
8. Соединение, представляющее собой (R)-4-циано-N-{2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил}-N-пиридин-2-илбензамид или его фармацевтически приемлемую кислотно-аддитивную соль, в значительной степени свободную от его S-стереоизомера.
9. Соединение по любому из пп.1-8, в виде соли хлористо-водородной кислоты.
10. Фармацевтическая композиция, содержащая соединение или его фармацевтически приемлемую соль по любому из пп.1-9 и фармацевтически приемлемый носитель или наполнитель.
11. Фармацевтическая композиция, содержащая (R)-4-циано-N-{2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил}-N-пиридин-2-илбензамид или его фармацевтически приемлемую кислотно-аддитивную соль, в значительной степени свободную от его S-стереоизомера, и фармацевтически приемлемый носитель или наполнитель.
12. Способ лечения страдающего нарушением ЦНС пациента, заключающийся во введении указанному пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
13. Способ лечения тревожного состояния или депрессии у нуждающегося в этом пациента, заключающийся во введении нуждающемуся в этом пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
14. Способ лечения шизофрении у нуждающегося в этом пациента, заключающийся во введении пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
15. Способ лечения дефицита памяти или когнитивной дисфункции у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
16. Способ лечения алкогольной, никотиновой и лекарственной абстиненций у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
17. Способ лечения болезни Паркинсона и моторных нарушений у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
18. Способ лечения мигрени у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
19. Способ лечения нарушений питания у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
20. Способ лечения сексуальной дисфункции у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
21. Способ лечения недержания мочи у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
22. Способ лечения инсульта у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
23. Способ лечения эндокринных нарушений у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
24. Способ лечения нарушений сна у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
25. Способ лечения нарушений, связанных с дефицитом внимания, у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
26. Способ лечения синдрома Туретта, аутизма, социальных фобий, нарушений, связанных с гиперактивностью или терморегуляторных нарушений у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.
27. Способ получения соединения по п.1, заключающийся в ацилировании соединения формулы (IV)
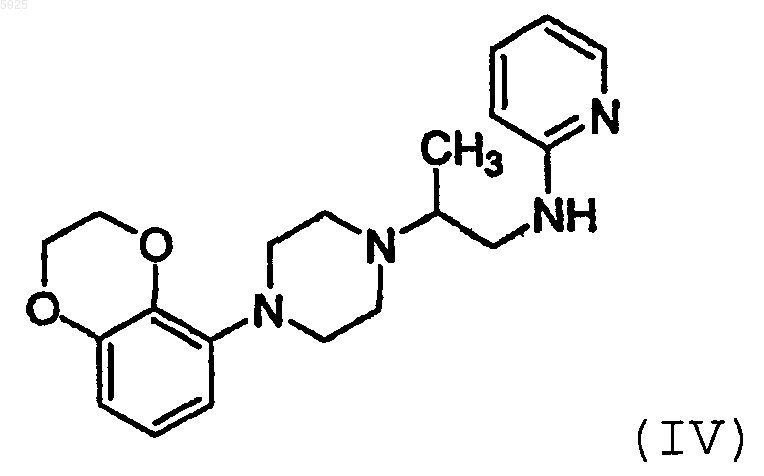
с применением ацилирующего средства, содержащего группу

где значение R1 определено в п.1;
с последующим преобразованием полученного основного соединения указанной здесь формулы (III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот.
28. Способ получения соединения по п.1, заключающийся в алкилировании амида или тиоамида формулы (VI)
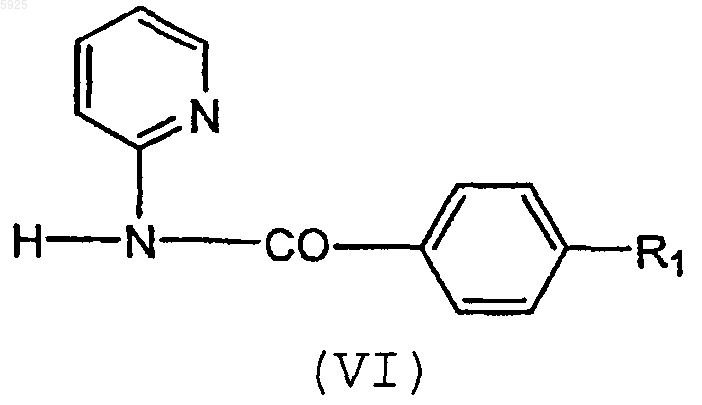
(где значение R1 определено выше) алкилирующим средством (например, галогенид или тозилат), предоставляющим группу формулы (VII)
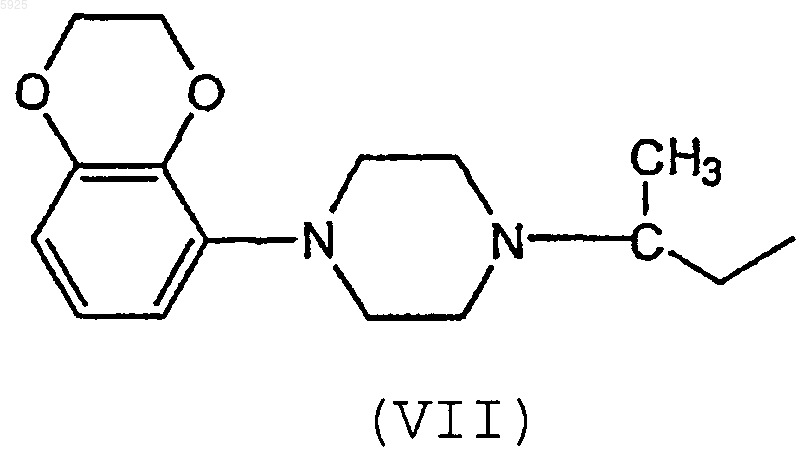
с последующим преобразованием полученного основного соединения указанной здесь формулы (III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот.
29. Способ получения соединения по п.1, заключающийся в алкилировании соединения формулы (VIII)
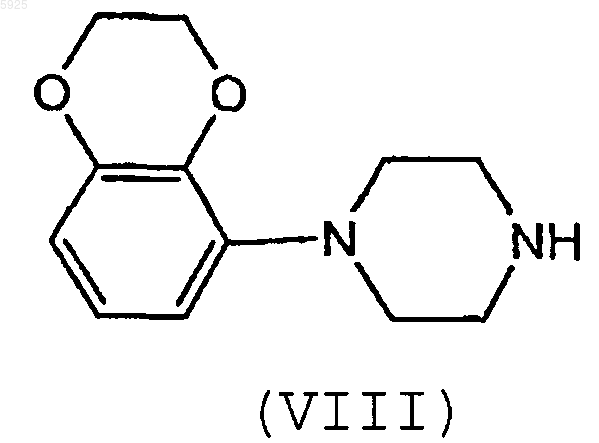
соединением формулы (IX)
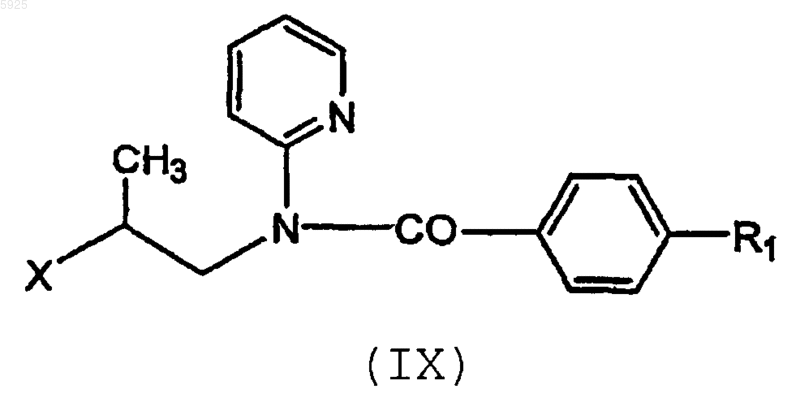
(где значение R1 определено выше и X представляет собой удаляемую группу),
с последующим преобразованием полученного основного соединения указанной здесь формулы (III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот.
30. Способ получения соединения по п.1, заключающийся в гетероарилировании соединения формулы (X)
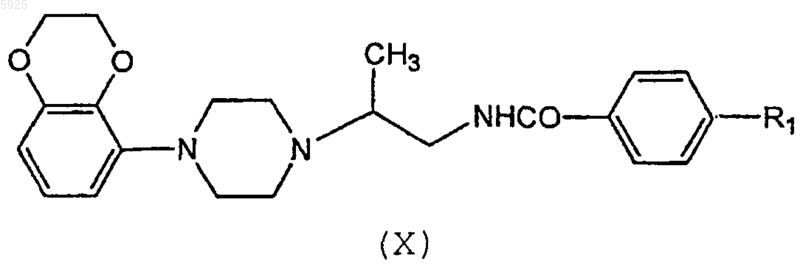
(где значение R1 определено выше) соединением, предоставляющим 2-пиридильную группу;
с последующим преобразованием полученного основного соединения указанной здесь формулы (III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы эрф S-формой, или наоборот.
31. Способ получения соединения по п.1, заключающийся во взаимодействии пиперазинового производного формулы
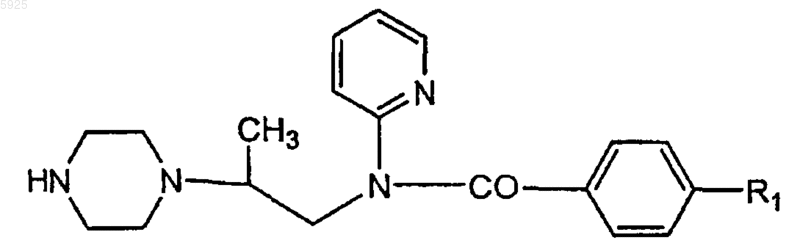
(где значение R1 определено выше) с фторзамещенным соединением формулы

с последующим преобразованием полученного основного соединения указанной здесь формулы (III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот.
Текст
005925 Область изобретения Настоящее изобретение относится к новым производным пиперазина, их применению и содержащим их фармацевтическим композициям. Новые соединения могут использоваться в качестве 5-НТ 1Aсвязывающих агентов, в частности в качестве антагонистов 5-НТ 1 А-рецепторов. Предпосылки изобретения В патенте США 6127357 описаны соединения общей формулы (I) и их фармацевтически приемлемые кислотно-аддитивные соли, где А представляет собой алкиленовую цепь из 2-4 атомов углерода, необязательно замещенную одним или несколькими низшими алкильными группами,Z представляет собой кислород или серу,R представляет собой Н или низший алкил,R1 представляет собой моно- или бициклический арильный или гетероарильный радикал,R2 представляет собой моно- или бициклический гетероарильный радикал, иR3 представляет собой водород, низший алкил, циклоалкил, циклоалкенил, циклоалкил(низший)алкил, арил, арил(низший)алкил, гетероарил, гетероарил(низший)алкил, группу формулы -NR4R5 [где R4 представляет собой водород, низший алкил, арил или арил(низший)алкил и R5 представляет собой водород, низший алкил, -СО(низший)алкил, арил, -СОарил, арил(низший)алкил, циклоалкил или циклоалкил(низший)алкил, или R4 и R5 вместе с атомом азота, к которому они оба присоединены, представляют собой насыщенное гетероциклическое кольцо, которое может содержать дополнительный гетероатом],или группу формулы OR6 [где R6 представляет собой низший алкил, циклоалкил, циклоалкил(низший)алкил, арил, арил(низший)алкил, гетероарил или гетероарил(низший)алкил]. В WO 97/03982 описаны соединения общей формулы (II) включая энантиомеры и их фармацевтически приемлемые кислотно-аддитивные соли. Соединения формулы (II) подпадают под объем патента США 6127357, но конкретно в нем не раскрыты. Отмечено, что соединения формулы II обладают in vivo сильной антагонистической активностью в отношении 5-HT1A при введении пероральным путем. Подробное описание изобретения Новые соединения по изобретению характеризуются структурной формулой (III) где R1 представляет собой циано, нитро, трифторметил или галоген, или их фармацевтически приемлемые кислотно-аддитивные соли. Как используется здесь, галоген относится к хлору, фтору, брому и йоду. Соединения формулы III содержат асимметричный атом углерода. Таким образом, они могут существовать в различных стереоизомерных формах или их смесях, включая рацематы. В некоторых предпочтительных осуществлениях стереоизомер R (формула IIIa) является предпочтительным.-1 005925 В соответствии с некоторыми осуществлениями изобретения, R-стереоизомер находится в энантиомерном избытке по отношению к S-стереоизомеру. Предпочтительно, соединение содержит значительно большую долю R-стереоизомера, чем S-стереоизомера. В предпочтительных осуществлениях соединение состоит, как минимум, примерно из 90 мас.% его R-стереоизомера и примерно 10 мас.% или менее его S-стереоизомера. В других осуществлениях изобретения, соединение состоит, по крайней мере, примерно из 99 мас.% его R-стереоизомера и примерно 1 или менее мас.% его S-стереоизомера, например, в основном свободный от S-стереоизомера, наиболее предпочтительно в основном чистого или чистого R-стереоизомера. Предпочтительные стереоизомеры можно выделить из рацемических смесей любым способом, известным специалистам в данной области, включая высокоэффективную жидкостную хроматографию (HPLC) и получение и кристаллизацию хиральных солей. См., например, Jacques, et al.,Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen, S. H., et al., Tetrahedron 33:2725 (1977); Eliel, E. L. Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); Wilen, S.H. Tables of Resolving Agents and Optical Resolutions p. 268 (E. L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972). Наиболее предпочтительными соединениями по изобретению являются (R)-4-циано-N-2-[4-(2,3 дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил-N-пиридин-2-илбензамид и его фармацевтически приемлемые кислотно-аддитивные соли. Фармацевтически приемлемые соли представляют собой кислотно-аддитивные соли, которые можно получить из соединения вышеуказанной общей формулы и фармацевтически приемлемой кислоты,такой как, например, бензойная, фосфорная, серная, соляная, бромистоводородная, лимонная, малеиновая, яблочная, миндальная, слизевая, азотная, фумаровая, янтарная, виннокаменная, уксусная, молочная,памовая, пантотеновая, бензолсульфоновая или метансульфокислота. Соединения по настоящему изобретению можно получить известными способами из известных исходных веществ, доступных посредством стандартных способов. Например, соединения можно получить посредством общих способов, описанных в ЕР-А 0512755 и WO 97/03982. Таким образом, данное изобретение относится к способу получения соединения формулы (III), который включает одно из следующих: а) ацилирование соединения формулы (IV) где значения R1 определены здесь; или b) алкилирование амида или тиоамида формулы (VI) или с) алкилирование соединения формулы (VIII)(где значения R1 определены выше и Х представляет собой удаляемую группу)d) гетероарилирование соединения формулы (X)(где значения R1 определены выше) соединением, вводящим 2-пиридильную группу; е) взаимодействие пиперазинового производного формулыf) преобразования основного соединения указанной здесь формулы (III) в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот; илиg) разделение рацемической смеси формулы (III) с получением энантиомерного избытка R-формы относительно S-формы, или наоборот. Данные описанные способы включают ацилирование амина формулы (IV) известным хлоридом бензола (V) или альтернативными ацилирующими производными. Примеры ацилирующих производных включают ангидрид кислоты, имидазолиды (например, полученные из карбонилдиимидазола) или активированные сложные эфиры. где R1 представляет собой циано, галоген, трифторметил или нитро. Новые соединения по настоящему изобретению представляют собой сильнодействующие агенты,связывающие 5-HT1A, селективно связывающиеся с 5-НТ 1A-рецептором. Более того при тестировании с помощью стандартных фармацевтических способов, новые соединения по изобретению проявляют себя как антагонисты 5-HT1A-рецептора. Кроме того, новые соединения формулы (III) являются уникальными по сравнению с ранее описанными антагонистами 5-HT1A-рецепторов, так как, при введении in vivo, они обладают наибольшей длительностью действия в качестве антагонистов 5-HT1A-рецептора. Примеры Настоящее изобретение проиллюстрировано нижеследующим примером. Специалистам в области органического синтеза могут быть известны другие пути синтеза соединения по изобретению. Реагенты и промежуточные соединения, применяющиеся здесь, или являются коммерчески доступными, или получаются согласно стандартным, описанным в литературе, процедурам. Пример 1. (R)-4-Циано-N-2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил-Nпиридин-2-илбензамид.(0,846 г, 2,38 ммоль) в дихлорметане (20 мл) обрабатывали добавлением по каплям раствора хлорида 4 цианобензоила в дихлорметане (1,1 эквивалента, 2,63 ммоль в 5 мл) при 0 С. После перемешивания в течение 16 ч смесь выливали в гексан (100 мл) для осаждения указанного в заголовке соединения в виде его моногидрохлоридной соли (белое твердое вещество, 1,2 г, 97% выход), которую перекристаллизовали из дихлорметана/гексана.[] 25/D = + 56 (с = 0,6, МеОН) Элементный анализ для С 28 Н 29N5O31,0 НСl Вычислено: С 64,67; Н 5,81; N 13,47. Найдено: С 64,69; Н 5,93; N 13,52. Для демонстрации наибольшей длительности действия соединения формулы (III), пример 1 сравнили с представительными соединениями патента США 6127357 и WO 97/03892. Представительные соединения патента США 6127357 имеют циклогексамидную группу и 2 метоксифенилпиперазиновую группу. Примером наиболее сильнодействующего соединения данной общей структуры (и наиболее эффективным соединением, описанным в патенте США 6127357) является соединение А, описанное в "примере 3" в патенте США 6127357. Единственным другим классом соединений в патенте США 6127357, для которого представлены данные, являются соединения, обладающие циклогексамидной группой и бензодиоксинилпиперазиновой группой ("пример 17" в патенте США 6127357). Небольшое подмножество данного класса соединений конкретно заявлено в WO 97/03892, с предпочтительным соединением, являющимся соединением В ("пример А 1" в WO 97/03892). Поэтому данные два предпочтительных примера из ЕР-А-0512755 и WO 97/03892 выбрали как типичные для сравнения с соединениями формулы (III). Пример 2. Профиль связывания. Соединения тестировали на предмет связывания с клонированными человеческими 5-НТ 1Aрецепторами, стабильно трансфецированными в клетки СНО с применением [3H]8-OH-DPAT в качестве радиолиганда 5-HT1A (соответственно общему способу, описанному в J. Dunlop et al., J. Pharmacol. Tox.Methods, 40, 47-55(1998. Как показано в табл. 1, соединения по настоящему изобретению показывают высокую аффинность в отношении 5-НТ 1A-рецептора. Пример 3. Функциональная активность in vitro. Для определения активности, присущей соединениям, использовали клональную клеточную линию,стабильно трансфецированную человеческим 5-НТ 1A-рецептором (соответственно общему способу, описанному в J. Dunlop et al., J. Pharmacol. Tox. Methods, 40, 47-55(1998. Данные представлены в табл. I. Как показано в табл. I, соединения по настоящему изобретению препятствуют способности 10 нМ 8-OHDPAT ингибировать форсколин-стимулированную продукцию цАМФ зависимым от концентрации образом. Таблица I Пример 4. Функциональная активность in vivo. Способность соединений к функционированию in vivo в качестве 5-НТ 1 А-антагонистов оценили у крыс с применением модели фиксированного ответа (D. Blackman, in "Operant Conditioning: An Experimental Analysis of Behavior", J. Butcher, ed., Methuen and Co., Ltd., London). По данной модели, крысы обучены отвечать (нажимом рычага) в фиксированном отношении 30 согласно графику представления пищи для того, чтобы получать активную добавку к пище. Введение 5-НТ 1A-агониста 8-OH-DPAT уменьшает степень контрольного ответа (оцениваемого путем введения носителя плацебо). Активность-4 005925 тестируемого соединения в качестве 5-НТ 1A-антагониста определяют путем измерения его способности противодействовать данному, индуцированному агонистом, уменьшению степени ответа. Полный антагонистический эффект рассматривают таковым, в случае, когда тестируемое соединение полностью обращает индуцированное агонистом уменьшение степени ответа, возвращая его к контрольным уровням. Данные, представленные в таблице II, демонстрируют, что дозы соединения примера 1 в концентрации 1 мг/кг полностью обращают уменьшение степени ответа, индуцированное введением дозы 8-OH-DPAT 0,3 мг/кг. Таким образом, соединения по настоящему изобретению функционируют in vivo в качестве 5HT1A-антагонистов. Таблица II Пример 5. Длительность действия in vivo. Длительность действия в модели фиксированного ответа определили посредством предварительного введения животным тестируемого соединения и последующего стимулирования дозой 5-НТ 1Aагониста 8-OH-DPAT 0,3 мг/кг через различные временные интервалы после введения тестируемого соединения. Все лекарственные вещества и носители ввели подкожным путем. Дозы тестируемого соединения для сравнения выбрали таким образом, чтобы вызвать десятикратное смещение кривой доза-ответ 8-OH-DPAT при введении за 30 мин до агониста. Дозы, выбранные для сравнения длительности действия, перечислены в табл. III. Таблица III Данные представлены для животных, которым за 0,5, 2 и 4 ч до введения 0,3 мг/кг дозы 8-OH-DPAT предварительно ввели тестируемое соединение. Результаты нормализованы по контрольным значениям,где за 100% принимали степень контрольного ответа, наблюдаемую при введении носителя ранее, чем агониста 8-OH-DPAT. Таблица IV Как можно увидеть из табл. IV, все три соединения (cоединение А, В и пример 1) полностью противодействуют индуцированному агонистом снижению ответа через 30 мин после их введения, возвращая степень ответа к контрольным уровням. Однако, когда агонист дают через 2 ч после введения тестового препарата (колонка 3), 5-НТ 1A-антагонистические эффекты соединений А и В больше не возвращают степень ответа к контрольным уровням, тогда как пример 1 еще проявляет полные 5-HT1A-антагонистические эффекты. Через четыре часа после введения (колонка 4) 5-НТ 1A-антагонистические эффекты соединений А и В полностью теряются, тогда как пример 1 продолжает обеспечивать полное противодействие индуцированному агонистом уменьшению степени ответа. Таким образом, длительность дейст-5 005925 вия примера 1 проявляется дольше чем 4 ч, тогда как длительность действия соединений А и В находится где-то между 30 мин и 2 ч. Увеличенная длительность действия новых соединений по настоящему изобретению, по сравнению с классами соединений, описанных в патентах США 6127357 и WO 97/03892, особенно полезна ввиду того, что можно вводить меньшее число доз соединения для создания подобного терапевтического эффекта. Соединения по настоящему изобретению можно применять для лечения людей, страдающих от нарушений ЦНС, таких как шизофрения (и другие психотические нарушения, такие как паранойя и маниакально-депрессивный психоз), болезнь Паркинсона и другие моторные нарушения, тревожные состояния(например, нарушения, связанные с генерализованными тревожными состояниями, острое тревожное состояние с реакцией паники и навязчивые маниакальные нарушения), депрессия (такая как при потенциировании ингибиторов обратного захвата серотонина и ингибиторы обратного захвата серотонина и норадреналина), синдром Туретта, мигрень, аутизм, нарушения с дефицитом внимания, гиперреактивные нарушения. Соединения по настоящему изобретению также можно использовать для лечения нарушений сна, социальных фобий, боли, нарушений терморегуляции, эндокринных нарушений, недержания мочи,сосудоспазма, инсульта, пищевых нарушений, таких как, например, тучность, анорексия и булемия, сексуальной дисфункции и лечения алкогольной, лекарственной и никотиновой абстиненций. Соединения по настоящему изобретению также можно использовать для лечения когнитивной дисфункции. Таким образом, соединения по настоящему изобретению можно использовать для лечения когнитивной дисфункции, ассоциированной с ослаблением умственной возможности мозга при болезни Альцгеймера и других деменций, включая болезнь Леви, васкулярную и постинсультную деменции. В соответствии с настоящим изобретением, также можно лечить когнитивную дисфункцию, связанную с хирургическими процедурами, травмами головного мозга или инсультом. Кроме того, соединения по настоящему изобретению можно использовать для лечения заболеваний, в которых когнитивная дисфункция является сопутствующей, таких как, например, болезнь Паркинсона, аутизм и нарушения с дефицитом внимания. Как используется здесь в смысле предоставления соединения или вещества, относящихся к данному изобретению, "предоставленный" означает или непосредственное применение такого соединения или вещества, или применение пролекарственного средства, производного, или аналога, формирующего эффективное количество соединения или вещества в организме. Пролекарственные средства можно получить так, как описано в Design of Prodrugs, Bundgaard, H.WileySons, Inc. 1995). Соединения по настоящему изобретению можно вводить перорально или парентерально, чистыми или в комбинации с традиционными фармацевтическими носителями. Подходящие твердые носители могут включать одно или несколько веществ, которые могут также действовать в качестве вкусовых агентов, смазочных материалов, растворителей, суспендирующих агентов, наполнителей, скользящих веществ, компрессионных добавок, связующих веществ, средств дезинтеграции таблетки или инкапсулирующих материалов. В порошках носитель представляет собой тонко диспергированное твердое вещество, смешанное с тонко диспергированным активным ингредиентом. В таблетках, активный ингредиент и носитель, обладающий необходимыми компрессионными свойствами, смешаны в подходящих пропорциях и спрессованы в желательную форму и размер. Порошки и таблетки могут содержать до 99% активного ингредиента. Подходящие твердые носители включают, например, фосфат кальция, стеарат магния, тальк, сахара, лактозу, декстрин, крахмал, желатин, целлюлозу, метилцеллюлозу, натрия карбоксиметилцеллюлозу, поливинилпирролидин, низкоплавкие воска и ионобменные смолы. Жидкие носители можно использовать в приготовлении растворов, суспензий, эмульсий, сиропов и эликсиров. Активный ингредиент по изобретению может быть растворен или суспендирован в фармацевтически допустимом жидком носителе, таком как вода, органический растворитель, смеси обоих или фармацевтически допустимых маслах и жиру. Жидкий носитель может содержать другие подходящие фармацевтические добавки, такие как солюбилизаторы, эмульгаторы, буферы, консерванты, подсластители, вкусовые агенты,суспендирующие агенты, сгущающие агенты, цвета, регуляторы вязкости, стабилизаторы или осморегуляторы. Подходящие примеры жидких носителей для орального или парентерального введения включают воду (особенно содержащую указанные выше добавки, например, производные целлюлозы, предпочтительно, раствор натрия карбоксиметилцеллюлозы), спирты (включая одноатомные спирты и многоатомные спирты, например, гликоли) и их производные и масла (например, фракционированные кокосовое и арахисовое масла). Для парентерального введения носители могут представлять собой масляные эфиры, такие как этилолеат и изопропилмиристат. Стерильные жидкие носители применяют в стерильных композициях жидких форм для парентерального введения. Жидкие фармацевтические композиции,-6 005925 представляющие собой стерильные растворы или суспензии, можно использовать, например, путем внутримышечной, внутрибрюшинной или подкожной инъекции. Стерильные растворы также можно вводить внутривенно. Форма для перорального введения может представлять собой жидкую или твердую композицию. Предпочтительно, фармацевтические композиции, содержащие настоящие соединения, находятся в разделенной на единицы дозированной форме, например, таблетках или капсулах. В такой форме композицию подразделяют на дозированные единицы, содержащие подходящие количества активных ингредиентов. Разделенные на единицы дозированные формы могут представлять собой расфасованные композиции, например, расфасованные порошки, флаконы, ампулы, наполненные шприцы или саше, содержащие жидкости. Альтернативно, разделенная на единицы дозированная форма может представлять собой, например, капсулу или таблетку саму по себе, или она может представлять собой подходящее число любых таких композиций в упакованной форме. Терапевтически эффективные дозы для применения могут варьироваться или регулироваться врачом и обычно находятся в диапазоне от 0,5 мг до 750 мг, соответственно конкретному состоянию(ям) подлежащего лечению и размера, возраста и картины ответа пациента. Настоящее изобретение может быть осуществлено в других конкретных формах без отклонения от его сути и существенных свойств, и, таким образом, для указания сферы применения изобретения следует ссылаться на прилагаемую формулу изобретения, а не на предшествующее описание. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (III) где R1 представляет собой циано, нитро, трифторметил или галоген или его фармацевтически приемлемые кислотно-аддитивные соли. 2. Соединение по п.1, где R1 представляет собой циано. 3. Соединение, представляющее собой (R)-4-циано-N-2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил-N-пиридин-2-илбензамид или его фармацевтически приемлемые кислотноаддитивные соли. 4. Соединение, представляющее собой гидрохлорид (R)-4-циано-N-2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил-N-пиридин-2-илбензамида. 5. Соединение по любому из пп.1-4, где R-изомер находится в энантиомерном избытке по отношению к S-изомеру. 6. Соединение по любому из пп.1-5, где содержание R-стереоизомера составляет около 90 мас.% или более и S-стереоизомера около 10 мас.% или менее. 7. Соединение по любому из пп.1-5, где содержание R-стереоизомера составляет около 99 мас.% иS-стереоизомера около 1 мас.%. 8. Соединение, представляющее собой (R)-4-циано-N-2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил) пиперазин-1-ил]пропил-N-пиридин-2-илбензамид или его фармацевтически приемлемую кислотноаддитивную соль, в значительной степени свободную от его S-стереоизомера. 9. Соединение по любому из пп.1-8, в виде соли хлористо-водородной кислоты. 10. Фармацевтическая композиция, содержащая соединение или его фармацевтически приемлемую соль по любому из пп.1-9 и фармацевтически приемлемый носитель или наполнитель. 11. Фармацевтическая композиция, содержащая (R)-4-циано-N-2-[4-(2,3-дигидробензо[1,4]диоксин-5-ил)пиперазин-1-ил]пропил-N-пиридин-2-илбензамид или его фармацевтически приемлемую кислотно-аддитивную соль, в значительной степени свободную от его S-стереоизомера, и фармацевтически приемлемый носитель или наполнитель. 12. Способ лечения страдающего нарушением ЦНС пациента, заключающийся во введении указанному пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 13. Способ лечения тревожного состояния или депрессии у нуждающегося в этом пациента, заключающийся во введении нуждающемуся в этом пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 14. Способ лечения шизофрении у нуждающегося в этом пациента, заключающийся во введении пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9.-7 005925 15. Способ лечения дефицита памяти или когнитивной дисфункции у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 16. Способ лечения алкогольной, никотиновой и лекарственной абстиненций у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 17. Способ лечения болезни Паркинсона и моторных нарушений у нуждающегося в этом пациента,заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 18. Способ лечения мигрени у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 19. Способ лечения нарушений питания у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 20. Способ лечения сексуальной дисфункции у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 21. Способ лечения недержания мочи у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 22. Способ лечения инсульта у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 23. Способ лечения эндокринных нарушений у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 24. Способ лечения нарушений сна у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 25. Способ лечения нарушений, связанных с дефицитом внимания, у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 26. Способ лечения синдрома Туретта, аутизма, социальных фобий, нарушений, связанных с гиперактивностью или терморегуляторных нарушений у нуждающегося в этом пациента, заключающийся во введении пациенту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-9. 27. Способ получения соединения по п.1, заключающийся в ацилировании соединения формулы где значение R1 определено в п.1; с последующим преобразованием полученного основного соединения указанной здесь формулы(III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот,или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот. 28. Способ получения соединения по п.1, заключающийся в алкилировании амида или тиоамида формулы (VI)(где значение R1 определено выше) алкилирующим средством (например, галогенид или тозилат), предоставляющим группу формулы (VII) с последующим преобразованием полученного основного соединения указанной здесь формулы (III),определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над Sформой, или наоборот. 29. Способ получения соединения по п.1, заключающийся в алкилировании соединения формулы(где значение R1 определено выше и Х представляет собой удаляемую группу),с последующим преобразованием полученного основного соединения указанной здесь формулы(III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот,или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот. 30. Способ получения соединения по п.1, заключающийся в гетероарилировании соединения формулы (X)(где значение R1 определено выше) соединением, предоставляющим 2-пиридильную группу; с последующим преобразованием полученного основного соединения указанной здесь формулы(III), определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот,или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над S-формой, или наоборот. 31. Способ получения соединения по п.1, заключающийся во взаимодействии пиперазинового производного формулы с последующим преобразованием полученного основного соединения указанной здесь формулы (III),определенного в п.1, в его фармацевтически приемлемую кислотно-аддитивную соль, или наоборот, или разделением рацемической смеси формулы (III) для получения энантиомерного избытка R-формы над Sформой, или наоборот. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6
МПК / Метки
МПК: A61P 25/28, C07D 405/12, A61K 31/44
Метки: средства, серотонинергические
Код ссылки
<a href="https://eas.patents.su/10-5925-serotoninergicheskie-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Серотонинергические средства</a>
Предыдущий патент: Ассоциация или комбинация антагониста рецептора св1 и сибутрамина, содержащие их фармацевтические композиции и их применение для лечения ожирения
Следующий патент: Нестероидные ингибиторы воспалений
Случайный патент: Способ получения водорода