4-[5-метил-3-фенилизоксазол-4-ил] бензолсульфонамид
Номер патента: 3754
Опубликовано: 28.08.2003
Авторы: Год Генри Т., Медич Джон Р., Маклофлин Кэтлин Т., Йонан Эдвард Э., Тэлли Джон Дж.
Формула / Реферат
1. Соединение 4-[5-метил-3-фенилизоксазол-4-ил]бензосульфонамид или его фармацевтически приемлемые соли.
2. Применение соединения по п.1 для получения кристаллической формы B 4-[5-метил-3-фенилизоксазол-4-ил]бензосульфонамида.
Текст
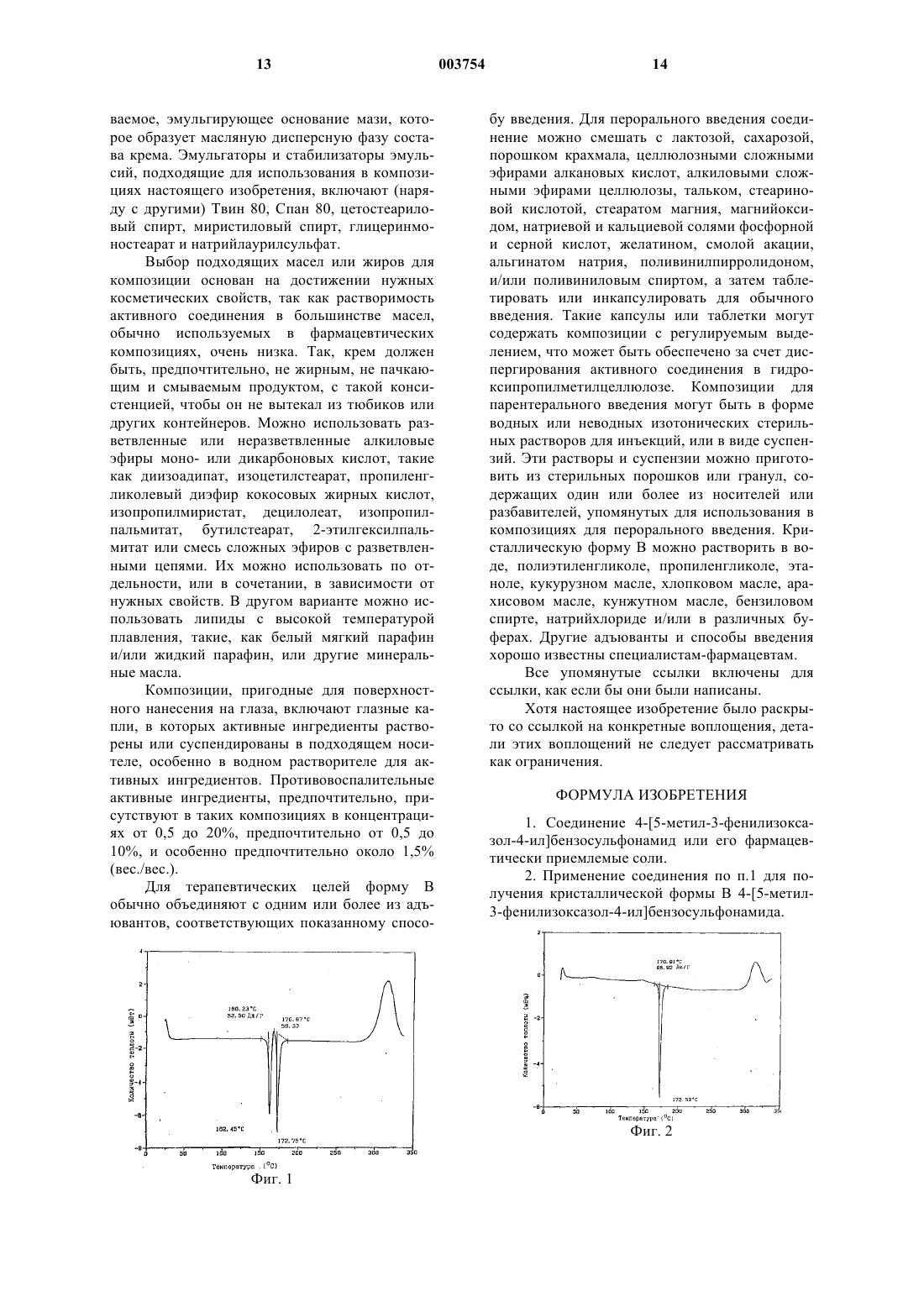
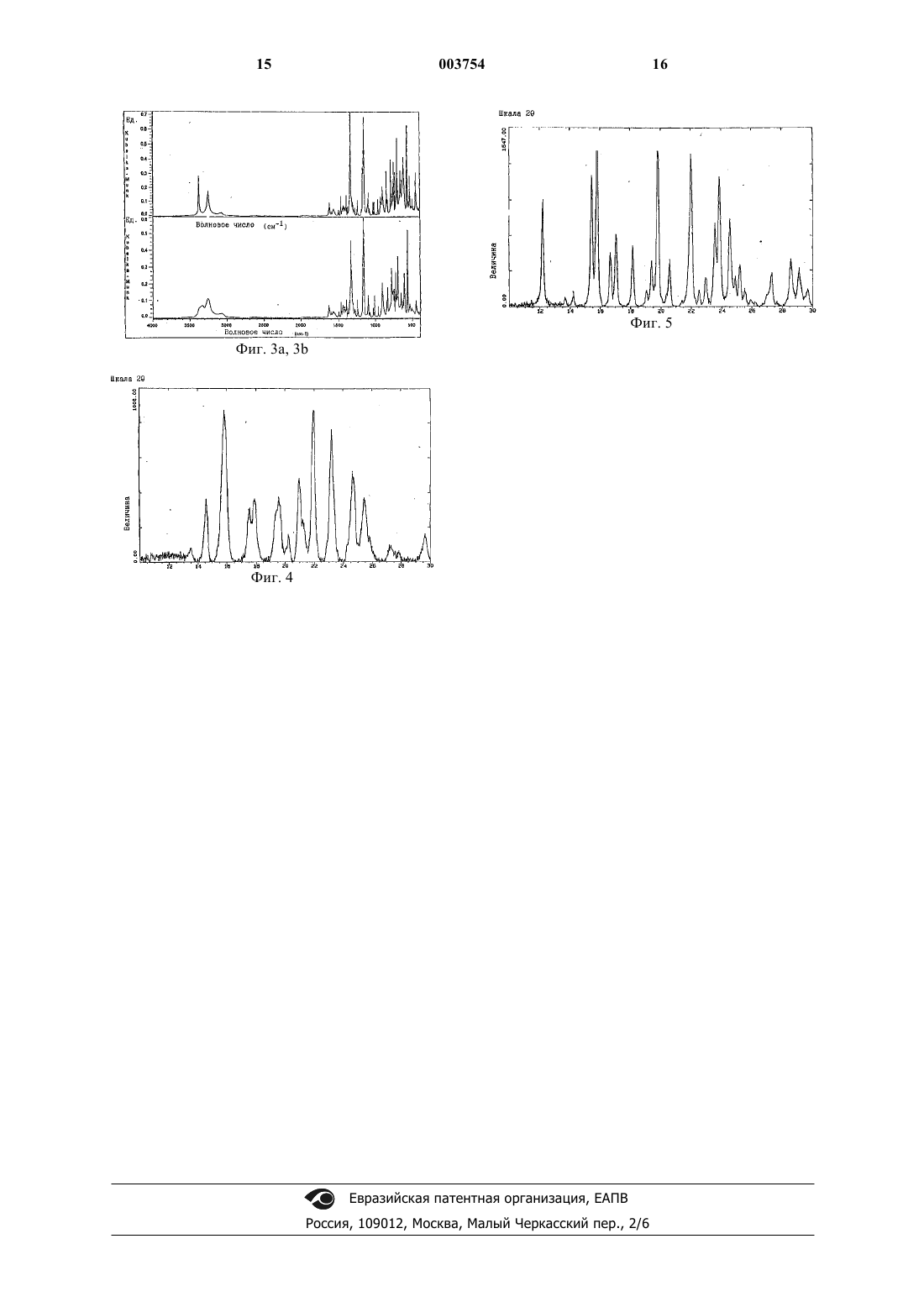
1 Область изобретения Настоящее изобретение относится к области противовоспалительных фармацевтических средств, и более конкретно относится к 4-[5 метил-3-фенилизоксазол-4-ил]бензолсульфонамиду и к его применению для получения его определенной кристаллической формы. Предпосылки изобретения Простагландины играют основную роль в воспалительных процессах, и ингибирование продуцирования простагландинов, особенноPGG2, PGN2 и PGE2, давно стало общей целью в разработке противовоспалительных лекарств. Однак, обычные нестероидные противовоспалительные лекарства (НСПЛ), которые проявляют активность в отношении уменьшения боли, вызываемой простагландинами, и опухания, связанного с воспалительным процессом, также оказываются активными, воздействуя на другие процессы, регулируемые простагландинами и не связанные с воспалительным процессом. Поэтому использование высоких доз большинства общепринятых НСПЛ может привести к серьезным побочным эффектам, включая опасные для жизни язвы, что ограничивает их терапевтический потенциал. Альтернативу НСПЛ составляет использование кортикостероидов, которые отличаются еще более серьезными побочными эффектами, особенно в случае длительного лечения. Ранее было обнаружено, что НСПЛ предотвращают продуцирование простагландинов за счет ингибирования ферментов в схеме арахидоновая кислота/простагландин в организме человека, включающей фермент циклооксигеназу (ЦОГ). Недавнее обнаружение индуцируемого фермента, связанного с воспалительным процессом (названного "циклооксигеназа-2 (ЦОГ 2)" или "простагландин G/H синтаза II"), предоставляет ценную мишень для ингибирования,что более эффективно снижает воспаления и вызывает меньшее количество и более слабые побочные эффекты, связанные с ингибированием циклооксигеназы-1 (ЦОГ-1). Для всех фармацевтических соединений и композиций химическая и физическая стабильность лекарственного соединения очень важна для промышленной разработки такого лекарственного вещества. Такая стабильность включает стабильность в условиях окружающей среды,особенно устойчивость к влаге и стабильность в условиях хранения. Повышенная стабильность в различных условиях хранения необходима для того, чтобы противостоять различным возможным условиям хранения на протяжении срока годности промышленного продукта. Стабильные лекарства позволяют избежать необходимости в специальных условиях хранения, а также частой замены имеющихся запасов. Лекарственное соединение должно быть также стабильным в процессе изготовления, который часто требует измельчения лекарства для того, чтобы 2 обеспечить одинаковый размер частиц и площадь поверхности лекарственного препарата. Нестабильные материалы часто претерпевают полиморфные изменения. Поэтому любые модификации лекарственного вещества, которые улучшают его свойства стабильности, обеспечивают значительные преимущества по сравнению с менее стабильными веществами. Было обнаружено, что 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид можно получить в различных кристаллических формах. Ранее полученный материал (форма "А") нестабилен после механического измельчения (помола), и также термически нестабилен. Полученная недавно кристаллическая форма (форма "В") описывается как более стабильная и обладающая улучшенными физическими свойствами. Краткое описание рисунков Фиг. 1 представляет картину 4-[5-метил-3 фенилизоксазол-4-ил]бензолсульфонамида формы А, полученную на дифференциальном сканирующем калориметре. (ДСК). Фиг. 2 представляет картину 4-[5-метил-3 фенилизоксазол-4-ил]бензолсульфонамида формы В, полученную на дифференциальном сканирующем калориметре. Фиг. 3 представляет инфракрасный спектр 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамида формы В. Фиг. 3b представляет инфракрасный спектр 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамида формы А. Фиг. 4 представляет образец дифракции рентгеновских лучей 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамида формы А. Фиг. 5 представляет образец дифракции рентгеновских лучей 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамида формы В. Подробное описание изобретения Было обнаружено, что 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид можно получить в кристаллической форме, обозначенной"Форма В". Форму В можно охарактеризовать следующими методами. Плавление Точки плавления определяют либо на приборе для определения точки плавления Томаса Гувера [Thomas Hoover], либо на приборе для определения точки плавления Mettler FP900Thermosystem. Интервалы плавления определяют с помощью дифференциальной сканирующей калориметрии на ТА Instruments DifferentialScanning Calorimeter (Model 2100 controller,Model 912 dualcalorimeter). Образец (1-2 мг) помещают в негерметичную алюминиевую кювету и нагревают со скоростью 10 С/мин. Для формы А плавление начинается при 160,2 С с экзотермой при 170,9 С, соответствующей перестройке кристаллов (см. фиг. 1). Для формы В плавление происходит при 170,9 С (пик 172,5 С). Пример ДСК для формы В представлен на фиг. 2. 3 Инфракрасная спектроскопия Инфракрасные спектры получают на спектрометре Nicolet DRIFT (инфракрасный спектр диффузного отражения с Фурье преобразованием) Magna System 550. При этом используют систему Spectra-Tech Collector и 3 мм держатель для образцов. Образцы (2%) анализируют в КВr и сканируют от 400 до 4000 см-1. Пример инфракрасного спектра поглощения формы В представлен на фиг. 3 а, а формы А - на фиг. 3b. По оси Y отложено отражение в единицах Кубелла-Мунка (Kubella-Munk) с поправкой. Инфракрасный спектр формы В характеризуется поглощением при примерно 3377, 1170,1151, 925, 844, 745, 729 и 534 см-1, что отличается от полос поглощения, наблюдаемых в спектре формы А. Инфракрасный спектр формы А характеризуется частично поглощением около 723 см-1, что отличается от наблюдаемого в спектре формы В. Кристаллы формы В настоящего изобретения, предпочтительно, демонстрируют инфракрасный спектр, практически соответствующий представленному на фиг. 3 а. Дифракция рентгеновских лучей в порошках Анализ осуществляют с помощью дифрактометра для порошкообразных образцовSiemens d5000. Экспериментальные результаты получают для значений 20 в интервале от 2 до 50 с шагом 2 с. В таблице представлены значения параметров основных пиков в значениях 2 величин, и интенсивности для формы В. Пример дифракционной картины рентгеновских лучей для формы А представлен на рис.5. Значительные различия между формой А и формой В очевидны для пиков 12,221, 15,447, 17,081, 19,798 и 23,861. ПикУгол-2, град. Paccт. D Пик И/Имакс, % Сps 1 12,221 7,2361 502,38 63,29 2 13,693 6,4617 38,03 4,79 3 14,227 6,2203 51,46 6,48 4 15,447 5,7314 599,94 75,58 5 15,801 5,6039 793,79 100,00 6 16,678 5,3110 239,95 30,23 7 17,081 5,1868 331,31 41,74 8 18,165 4,8796 270,21 34,04 9 19,066 4,6510 73,16 9,22 10 19,400 4,5717 200,13 25,21 11 19,798 4,4807 789,23 99,43 12 20,578 4,3126 209,43 26,38 13 22,008 4,0354 691,33 87,09 14 22,540 3,9414 71,87 9,05 15 22,975 3,8678 137,23 17,29 16 23,580 3,7699 394,27 49,67 17 23,861 3,7261 602,27 75,87 18 24,553 3,6226 397,23 50,04 19 25,206 3,5302 192,44 24,24 20 25,560 3,4822 77,74 9,79 21 25,940 3,4320 31,47 3,96 22 26,200 3,3985 20,87 2,63 Форму В можно получить в результате рекристаллизации 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамида из подходящего растворителя. Для получения формы В 4-[5 метил-3-фенилизоксазол-4-ил]бензолсульфонамид растворяют в некотором объеме растворителя и охлаждают до образования кристаллов. Предпочтительно, добавлять соединение к растворителю при температуре, по крайней мере,около 25 С. Более предпочтительно, чтобы температура растворителя была между 30 С и температурой кипения растворителя. Еще более предпочтительна температура в интервале от около 65 до 75 С. Альтернативно горячий растворитель можно добавлять к соединению, и эту смесь можно охлаждать до образования кристаллов. Предпочтительно, чтобы температура растворителя составляла, по крайней мере, 25 С. Более предпочтительно, чтобы температура растворителя была в интервале около 50-80 С. Еще более предпочтительна температура в интервале около 65-75 С. Предпочтительно, чтобы количество растворителя в смеси было примерно в 3 раза больше количества соединения. Более предпочтительно, чтобы количество растворителя превышало количество соединения примерно в 7-10 раз. Предпочтительно медленно охлаждать раствор для осаждения формы В. Более предпочтительно охлаждать раствор со скоростью менее чем около 0,5 С/мин. Еще более предпочтительно охлаждать раствор со скоростью около 0,3 С/мин, или меньше. Подходящим растворителем является растворитель или смесь растворителей, которая растворяет соединение и все примеси при повышенной температуре, но после охлаждения,преимущественно осаждается форма В. Подходящий растворитель выбирают из спирта, метил-трет-бутилового эфира, метилэтилкетона и комбинации растворителей, выбранных из спирта, метил-трет-бутилового эфира, ацетонитрила, воды, ацетона, тетрагидрофурана и метилэтилкетона. Предпочтительны спирт или водный спирт. Более предпочтительный растворитель выбирают из метанола, водного метанола, этанола, водного этанола, изопропилового спирта и водного изопропилового спирта. Еще более предпочтительны водный метанол, метанол, этанол 3 А, водный этанол и смесь изопропанол/метанол; Альтернативно соединение растворяют в одном растворителе, и добавляют сорастворитель для кристаллизации целевой формы. 5 Полученные таким образом кристаллы формы В выделяют из растворителя, например,фильтрованием или центрифугированием. Предпочтительно, кристаллы высушивают, и более предпочтительно при температуре в интервале от около 30 до около 100 С. Еще более предпочтительно высушить кристаллы в вакууме. Альтернативно форму В можно получить,нагревая форму А при температуре, достаточной для превращения в форму В. Предпочтительно, форму А подогревают при температуре в интервале от 50 до около 140 С. Получение Нижеследующие примеры содержат подробные описания способов получения формы В. Эти подробные описания соответствуют объему изобретения, предназначены для его иллюстрации. Эти подробные описания представлены только для иллюстративных целей, и никоим образом не ограничивают объем изобретения. Все части даны по весу, а температуры указаны в С, если нет других указаний. 4-[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид получают следующим способом,причем этанол 3 А является водным этанолом(5% воды) денатурированным метанолом. Пример 1. Стадия 1. Получение деоксибензоиноксима. Тригидрат ацетата натрия (152,5 г, 1,12 моля, 1,1 экв) добавляют к деоксибензоину (200 г, 1,02 моля), и растворяют в этаноле (3 А, 0,8 л) и воде (0,24 л) в 5 л колбе с механической мешалкой, обратным холодильником и термометром. Раствор перемешивают и нагревают до 701 С. К гидроксиламингидрохлориду (78,0 г,1,12 моля, 1,1 экв.) добавляют воду (0,1 л) в отдельной 500 мл колбе при перемешивании. Раствор гидроксиламингидрохлорида переносят в раствор деоксибензоина, поддерживая при этом температуру реакционной смеси примерно при 70 С. Эту смесь нагревают до кипения (около 84 С), и выдерживают при этой температуре в течение 40 мин. Смесь охлаждают до 40 С в течение 2 ч, и выливают в реакционную смесь воду (10,5 л). Реакционную смесь охлаждают до 20 С в течение еще 1 ч при перемешивании. Образуются кристаллы чистого оксима, которые выделяют фильтрованием (воронка Бюхнера,фильтровальная бумага Ватман 1), используя вакуум, промывают смесью 50 мл 3 А этанола и 100 мл воды, и водой (1 л). Твердую часть сушат в вакууме в течение 2 ч, и при 55 С в вакууме в течение 12 ч, получая чистый деоксибензоиноксим (213,2 г, 99%). Стадия 2. Получение 5-гидрокси-5-метил 3,4-дифенилизоксазолина. Деоксибензоиноксим (стадия 1) растворяют в безводном ТГФ (565 мл) в атмосфере азота. Раствор охлаждают до -20 С. Раствор обрабатывают литийдиизопропиламидом (2 М, 800 мл,1,60 моля), давая температуре реакционной смеси повыситься до 10-15 С. Реакционную смесь 6 охлаждают до температуры в интервале от -10 до -20 С, и к раствору добавляют безводный этилацетат (218 мл), давая возможность температуре повыситься до максимум 25 С и выдерживают в течение 30 мин при 25 С. Реакционную смесь охлаждают до около 0 С. Добавляют воду в колбу для охлаждения и охлаждают до 05 С. Предварительно охлажденную реакционную смесь переносят из реактора в колбу для охлаждения, поддерживая температуру охлаждаемой смеси ниже 25 С. Охлажденную смесь охлаждают до 0-5 С. К смеси добавляют хлористо-водородную кислоту (12 М), поддерживая температуру ниже 25 С во время добавления за счет регулирования скорости добавления, и перемешивают до тех пор, пока не растворится вся твердая часть (5 мин). рН перемешиваемой смеси оказывается в интервале значений рН 3-4. Слои разделяют и органический слой удаляют. К органическому слою добавляют гептан при перемешивании. Органический слой перегоняют до тех пор, пока температура в колбе не достигает 90-91 С. Раствор охлаждают до 5 С и фильтруют. Твердую часть промывают двумя порциями по 300 мл смеси этилацетатгептан(20/80), охлажденной до 5 С. Твердый продукт сушат на воронке несколько часов, а затем сушат при комнатной температуре в вакууме, продувая азотом в течение уикэнда, получая изоксазолин (108, 75 г, 57,7%). Стадия 3. Получение 4-[(5-метил-3-фенил)-4-изоксазолил]бензолсульфонамида. 5-гидрокси-5-метил-3,4-дифенилизоксазолин (стадия 2) (142 г, 0,56 моля) растворяют в дихлорметане (568 мл) в 3-х литровой круглодонной колбе, снабженной рубашкой для обогрева, механической мешалкой, холодильником,регулятором температуры J-KEM и термопарой,получая суспензию. Эту суспензию перемешивают и охлаждают до 10 С. К суспензии добавляют хлорсульфоновую кислоту (335 мл,586,3 г, 5,04 моля), поддерживая температуру в колбе ниже 20 С за счет регулирования скорости добавления. Смесь нагревают до температуры кипения с обратным холодильником (около 40 С), выдерживают при этой температуре в течение 5 ч, затем охлаждают до 0-5 С. Охлажденный реакционный раствор медленно переносят в трехгорлую трехлитровую круглодонную колбу (с механической мешалкой и термопарой), содержащую воду (1000 мл), предварительно охлажденную до 0-5 С, при интенсивном перемешивании, и поддерживая температуру реактора ниже 10 С. Смесь перемешивают еще 5 мин. Слои разделяют. В отдельной 3-х литровой колбе (с механической мешалкой, внешней баней со смесью льда и соли, с термопарой) 28% гидроксид аммония (700 мл) охлаждают до 05 С. Метиленхлоридный раствор переносят в перемешиваемый раствор гидроксида аммония,поддерживая температуру ниже 10 С. Эту смесь перемешивают при комнатной температуре в 7 течение 60 мин. Полученную суспензию фильтруют, и твердую часть промывают водой (200 мл) и сушат, получая 4-[(5-метил-3-фенил)-4 изоксазолил]бензолсульфонамид в виде твердого вещества белого цвета (94,3 г, 53,5%). Стадия 4. Перекристаллизация 4-[(5-метил 3-фенил)-4-изоксазолил]бензолсульфонамида. 4-[(5-метил-3-фенил)-4-изоксазолил]бензолсульфонамид со стадии 3 растворяют в 300 мл кипящего метилэтилкетона (2-бутанон), и разбавляют 10% водным изопропиловым спиртом (300 мл (270 мл безводного изопропилового спирта и 30 мл воды. Этот материал охлаждают до комнатной температуры, после чего образуются кристаллы. Кристаллы выделяют фильтрованием и сушат в вакуумном шкафу (10 мм рт.ст., 100 С), получая чистую форму В (112,95 г, 65%); т.пл. 172-173 С. Пример 2.[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид (пример 1, стадия 3) (3 г) объединяют со смесью 80% этанол 3 А/20% вода (9 мл),и нагревают до тех пор, пока не растворится твердая часть. Колбу охлаждают на бане с водопроводной водой, и выдерживают в течение 1 ч для образования осадка. Твердую часть отфильтровывают и промывают этанолом 3 А. Полученный материал нагревают досуха в вакууме(50-60 С, 508 мм рт.ст.). Этот материал идентифицируют как форму В. Пример 3.[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид (пример 1, стадия 3) объединяют с этанолом (100 мл), и нагревают до тех пор, пока не растворится твердая часть (около 70 С). Колбу охлаждают до 20-25 С в течение более 1,5 ч и выдерживают в течение 30 мин для образования осадка. Твердую часть отфильтровывают(фильтровальная бумага Ватман 1), и промывают водой. Полученный материал нагревают досуха в вакууме (90 С, 50-100 мм рт.ст.). Образующийся материал идентифицируют как форму В. Пример 4.[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид (пример 1, стадия 3) (9,8 г), метанол (73,5 мл) и воду (24,5 мл) объединяют и нагревают до 65-70 С. Раствор выдерживают около 10 мин и фильтруют пока он горячий для удаления всех частиц. Раствор медленно охлаждают до 50 С (около 0,3 С/мин), и выдерживают при 50 С в течение 1 ч (кристаллизация начинается во время процесса выдерживания). Далее раствор охлаждают до 5 С (около 0,3 С/мин) и выдерживают при 5 С в течение 1 ч. Продукт выделяют фильтрованием и промывают 10 мл холодной смеси метанол/вода (75/25). Продукт сушат при 95-100 С в течение 4 ч, получая 8,55 г формы В. Пример 5. Смесь метанол/изопропанол (80/20, 120 мл) добавляют к [5-метил-3-фенилизоксазол-4 003754(25 г), и нагревают до около 68 С. Этот раствор выдерживают примерно 15 мин и фильтруют через стеклянную фильтровальную воронку пока он горячий для удаления любых частиц. Раствор медленно охлаждают до 5 С в течение 3,3 ч (около 0,3 С/мин) и выдерживают при 5 С в течение 2 ч. Продукт выделяют фильтрованием и промывают 10 мл холодной смеси метанол/изопропанол (80/20). Продукт сушат при 95100 С в течение 3 ч, получая 11 г формы В. Сравнительный пример 6.[5-метил-3-фенилизоксазол-4-ил]бензолсульфонамид (пример 1, стадия 3) (10 г) объединяют с 20 мл смеси вода: метанол (25:75), и нагревают до растворения твердой части. Колбу с раствором помещают в лед, и смесь быстро охлаждают до 10 С, причем при охлаждении не наблюдается кристаллизации. Затем на дне колбы образуется несколько кристаллов, и вскоре происходит быстрая кристаллизация. Оставляют на 10 мин. Твердую часть отфильтровывают и промывают 75% водным метанолом. Материал нагревают досуха в вакууме, продувая азотом (50-60 С,504 мм рт.ст.). Полученный материал идентифицируют как форму А. Настоящее изобретение включает также способ лечения или предупреждение нарушений, связанных с циклооксигеназой-2, таких как воспаления у пациента, причем способ включает введение пациенту с таким воспалением или нарушением, или восприимчивому к такому воспалению или нарушению, терапевтически эффективного количества кристаллической формы В 4-[5-метил-3-фенилизоксазол-4-ил] бензолсульфонамида. Форма В 4-[5-метил-3-фенилизоксазол-4 ил]бензолсульфонамида может быть полезна для (но не ограничивается этим) лечения воспалений у пациента, и для лечения других связанных с циклооксигеназой-2 нарушений, например, в качестве анальгетика для лечения боли или головной боли, или в качестве антипиретика для лечения лихорадки. Так например, форму В можно использовать для лечения артритов,включая (но не ограничиваясь ими) ревматоидный артрит, спондилоартриты, подагрический артрит, остеоартрит, системную красную волчанку и ювенильный артрит. Форму В можно использовать для лечения астмы, бронхита,менструальных болей, при преждевременных родах, для лечения тенденитов, бурситов, болезней печени, включая гепатит, связанные с кожей состояния, такие, как псориаз, экзема,ожоги и дерматиты, и при лечении послеоперационных воспалений, включая офтальмические операции, такие как операции катаракты и рефрактивную хирургию. Форму В можно также использовать для лечения желудочно-кишечных состояний, таких как воспалительные кишечные заболевания, болезнь Крона, гастриты, синдром раздраженного кишечника и язвенные колиты. 9 Форму В можно также использовать для профилактики или лечения раковых заболеваний, таких как рак прямой кишки, рак груди, легких,простаты, мочевого пузыря, матки и кожи. Форму В можно использовать для лечения глаукомы, ангиогенеза и ретинопатии. Форму В можно использовать для лечения воспалений при таких заболеваниях, как сосудистые заболевания, включая атеросклероз, мигрени, нодозный периартериит, тироидит, апластическая анемия, болезнь Ходкинса, склередема, ревматическая лихорадка, диабет типа I. Заболевания нервно-мышечных связей, включая псевдопаралитическую астению, заболевания белого вещества, включая рассеянный склероз, саркоидоз,нефротический синдром, синдром Бекета, полимиозит, гингивит, нефрит, гиперчувствительность, отеки после хирургии, ишемию миокарда и т.п. Форму В можно также использовать для лечения таких офтальмических заболеваний, как ретинит, конъюктивит, ретинопатия, увеит,глазная фотофобия и острые поражения ткани глаза. Форму В можно также использовать для лечения воспаления легких, такого как связанное с вирусной инфекцией, и кистозного фиброза. Форму В можно также использовать для лечения некоторых поражений центральной нервной системы, таких как деменция, связанная с поражениями коры головного мозга, включая болезнь Альцгеймера, и поражений центральной нервной системы в результате удара, ишемии,припадка и травмы. Форму В можно использовать в качестве противовоспалительных агентов,таких как те, которые используют для лечения артритов, причем она обладает тем дополнительным преимуществом, что связанные с ней побочные эффекты оказываются менее серьезными. Форма В может быть также полезна при лечении аллергических ринитов, синдрома затрудненного дыхания, синдрома эндотоксинного шока, остеопороза и для ингибирования костной резорбции. Форма В может также оказаться полезной для снятия боли, и не только послеоперационной, но и для снятия зубной,мышечной боли и боли, связанной с раком. Форма В может быть полезной для профилактики сердечно-сосудистых заболеваний, таких как атеросклероз, заболеваний печени и деменций,таких как болезнь Альцгеймера. Помимо того, что эта форма пригодна для лечения людей, ее можно также использовать в ветеринарии для лечения домашних животных,экзотических животных и животных на фермах,включая таких как млекопитающие, грызуны и т.п. Более предпочтительные животные включают лошадей, собак и кошек. Предлагаемую форму В можно также использовать в совместной терапии, частично или полностью вместо других обычных противовоспалительных агентов, например, вместе со стероидами, нестероидными противовоспалительными препаратами, ингибиторами 5-липо 003754BPC 15, соединение SmithKline Beecham SB209247, и SKF соединение SKF-104493. Предпочтительно антагонисты рецептора LTB4 выбирать из кальцитрола, эбселена, Вауеr Вау-х 1005, Ciba Geigy соединения CGS-25019C, LeoFrederick PF-5901, 3M Pharmaceuticals R-840,рилопирокс, флобуфен, линазоласт, лонаполен,мазопрокол, оназоласт, тенидап, зилеутон,пранлукаст, тепоксалин, рилопирокс, флезеластингидрохлорид, эназадремфосфат и бунопроласт. Рассматриваемую форму В можно также использовать в комбинированной терапии с опоидами и другими анальгетиками, включая наркотические анальгетики, антагонисты рецептора Мu, антагонисты рецептора Карра, ненаркотические (т.е. неаддиктивные) анальгетики,ингибиторы захвата моноамина, агенты, регулирующие аденозин, производные каннабиноида,антагонисты вещества Р, антагонисты рецепторов нейрокинина-1 и блокаторы канальцев натрия (наряду с другими). Более предпочтительными были бы комбинации с соединениями,выбранными из морфина, мепередина, кодеина,пентазоцина, бупренорфина, буторфанола, дезоцина, мептазинола, гидрокодона, оксикодона,метадона, трамадола (Tramadol (+) энантиомер),DuP 747, Динофрина А, Энадолина, RP-60180,HN-11608, Е-2078, ICI-204448, ацетаминофена(парацетамола), пропоксифена, налбуфина, Е 4018, филенадола, мирфентанила, амитриптилина, DuP631, трамадола -)энантиомер), GP531, акадезина, АКI-1, AKI-2, GP-1683, GP-3269,4030W92,рацемата трамадола,Е-2078,АХС 3742, SNX-111, ADL2-1294, ICI-204448,СТ-3, СР-99994 и СР-99994. Настоящее изобретение включает фармацевтическую композицию, включающую терапевтически эффективное количество кристаллической формы В 4-[5-метил-3-фенилизоксазол 4-ил]бензолсульфонамида вместе с, по крайней мере, одним фармацевтически приемлемым носителем, адьювантом или разбавителем. В объем настоящего изобретения также включен класс фармацевтических композиций,включающих кристаллическую форму В вместе с одним или более из нетоксичных фармацевтически приемлемых носителей и/или разбавителей и/или адъювантов (все вместе именуемые здесь материалами "носителя"), и, при желании,других активных ингредиентов. Форму В настоящего изобретения можно вводить любым подходящим способом, предпочтительно в форме фармацевтической композиции, адаптированной к такому способу, и в дозе, эффективной для предназначенного лечения. Активную форму В и композиции можно, например, вводить перорально, внутривенно, внутрибрюшинно,подкожно, внутримышечно или поверхностно. Для перорального способа введения фармацевтическая композиция может быть в форме,например, таблеток, капсул, суспензий или жидкостей. Фармацевтическую композицию,предпочтительно, приготавливают в форме единичной дозы, содержащей определенное количество активного ингредиента. Примеры таких единичных доз включают таблетки или капсулы. Активный ингредиент можно также вводить в виде инъекций композиций, в которых в качестве подходящего носителя можно использовать солевой раствор, декстрозу или воду. Количество терапевтически активного соединения, которое вводят, и дозовый режим для лечения болезненного состояния соединением и/или композицией настоящего изобретения зависят от различных факторов, включая возраст, вес, пол и состояние здоровья пациента,тяжесть заболевания и конкретно используемое соединение, и поэтому могут меняться в широких пределах. Фармацевтическая композиция может содержать активные ингредиенты в интервале от около 0,1 до 2000 мг, предпочтительно в интервале от около 0,5 до 500 мг, и еще более предпочтительно от около 1 до 100 мг. Подходящей может быть дневная доза от около 0,01 до 100 мг/кг веса тела, предпочтительно от около 0,5 до около 20 мг/кг веса тела, и наиболее предпочтительно от около 0,1 до 10 мг/кг веса тела. Дневную дозу можно вводить в виде одной или четырех доз в день. 12 В случае псориаза и других кожных заболеваний может оказаться предпочтительным наносить препараты формы В для поверхностного нанесения на пораженные участки 2 или 4 раза в день. При воспалениях глаз или других внешних тканей, например, рта и кожи, композиции предпочтительно наносить в виде мазей или кремов для поверхностного нанесения, или в виде суппозиториев, содержащих активные ингредиенты в полном количестве, например,0,075-30% (вес./вес.), предпочтительно 0,2-20%(вес./вес.). При изготовлении композиции в виде мази активные ингредиенты можно использовать либо с парафиновым, либо со смешивающимся с водой основанием мази. В другом варианте активные ингредиенты можно приготовить в виде крема в основании крема типа масло-в-воде. При желании водная фаза основания крема может включать, например, по крайней мере, 30% (вес./вес.) полиатомного спирта, такого как пропиленгликоль, бутан-1,3-диол, маннит, сорбит, глицерин, полиэтиленгликоль и их смеси. Желательно, чтобы композиции для поверхностного нанесения включали соединение,которое повышает абсорбцию или проникновение активного ингредиента через кожу или другие пораженные участки. Примеры таких улучшающих проникновение через кожу агентов включают диметилсульфоксид и родственные аналоги. Форму В можно также вводить с помощью трансдермального приспособления. Предпочтительно поверхностное введение осуществлять,используя пластырь типа резервуар с пористой мембраной, или твердую матрицу. В любом случае активный ингредиент непрерывно поступает из резервуара или микрокапсул через мембрану в проницаемый для активного агента слой адгезива, который находится в контакте с кожей или слизистой реципиента. Если активный агент абсорбируется через кожу, реципиенту вводят регулируемый, заранее определенный поток активного агента. В случае микрокапсул этот инкапсулированный агент может также функционировать как мембрана. Масляная фаза эмульсий настоящего изобретения может состоять из известных ингредиентов, объединенных известным способом. Хотя такая фаза может включать только эмульгатор,она может включать смесь, по крайней мере,одного эмульгатора с жиром или маслом, или как с жиром, так и с маслом. Предпочтительно,чтобы гидрофильный эмульгатор был включен наряду с липофильным эмульгатором, который играет роль стабилизатора. Предпочтительно также включить и масло и жир. Вместе, эмульгатор (эмульгаторы) со стабилизатором (стабилизаторами) или без него представляет так называемый эмульгирующий воск, и этот воск,вместе с маслом и жиром образует, так назы 13 ваемое, эмульгирующее основание мази, которое образует масляную дисперсную фазу состава крема. Эмульгаторы и стабилизаторы эмульсий, подходящие для использования в композициях настоящего изобретения, включают (наряду с другими) Твин 80, Спан 80, цетостеариловый спирт, миристиловый спирт, глицеринмоностеарат и натрийлаурилсульфат. Выбор подходящих масел или жиров для композиции основан на достижении нужных косметических свойств, так как растворимость активного соединения в большинстве масел,обычно используемых в фармацевтических композициях, очень низка. Так, крем должен быть, предпочтительно, не жирным, не пачкающим и смываемым продуктом, с такой консистенцией, чтобы он не вытекал из тюбиков или других контейнеров. Можно использовать разветвленные или неразветвленные алкиловые эфиры моно- или дикарбоновых кислот, такие как диизоадипат, изоцетилстеарат, пропиленгликолевый диэфир кокосовых жирных кислот,изопропилмиристат, децилолеат, изопропилпальмитат, бутилстеарат, 2-этилгексилпальмитат или смесь сложных эфиров с разветвленными цепями. Их можно использовать по отдельности, или в сочетании, в зависимости от нужных свойств. В другом варианте можно использовать липиды с высокой температурой плавления, такие, как белый мягкий парафин и/или жидкий парафин, или другие минеральные масла. Композиции, пригодные для поверхностного нанесения на глаза, включают глазные капли, в которых активные ингредиенты растворены или суспендированы в подходящем носителе, особенно в водном растворителе для активных ингредиентов. Противовоспалительные активные ингредиенты, предпочтительно, присутствуют в таких композициях в концентрациях от 0,5 до 20%, предпочтительно от 0,5 до 10%, и особенно предпочтительно около 1,5%(вес./вес.). Для терапевтических целей форму В обычно объединяют с одним или более из адъювантов, соответствующих показанному спосо 003754 14 бу введения. Для перорального введения соединение можно смешать с лактозой, сахарозой,порошком крахмала, целлюлозными сложными эфирами алкановых кислот, алкиловыми сложными эфирами целлюлозы, тальком, стеариновой кислотой, стеаратом магния, магнийоксидом, натриевой и кальциевой солями фосфорной и серной кислот, желатином, смолой акации,альгинатом натрия, поливинилпирролидоном,и/или поливиниловым спиртом, а затем таблетировать или инкапсулировать для обычного введения. Такие капсулы или таблетки могут содержать композиции с регулируемым выделением, что может быть обеспечено за счет диспергирования активного соединения в гидроксипропилметилцеллюлозе. Композиции для парентерального введения могут быть в форме водных или неводных изотонических стерильных растворов для инъекций, или в виде суспензий. Эти растворы и суспензии можно приготовить из стерильных порошков или гранул, содержащих один или более из носителей или разбавителей, упомянутых для использования в композициях для перорального введения. Кристаллическую форму В можно растворить в воде, полиэтиленгликоле, пропиленгликоле, этаноле, кукурузном масле, хлопковом масле, арахисовом масле, кунжутном масле, бензиловом спирте, натрийхлориде и/или в различных буферах. Другие адъюванты и способы введения хорошо известны специалистам-фармацевтам. Все упомянутые ссылки включены для ссылки, как если бы они были написаны. Хотя настоящее изобретение было раскрыто со ссылкой на конкретные воплощения, детали этих воплощений не следует рассматривать как ограничения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение 4-[5-метил-3-фенилизоксазол-4-ил]бензосульфонамид или его фармацевтически приемлемые соли. 2. Применение соединения по п.1 для получения кристаллической формы В 4-[5-метил 3-фенилизоксазол-4-ил]бензосульфонамида.
МПК / Метки
МПК: A61K 31/42, C07D 261/08, A61P 29/00
Метки: бензолсульфонамид, 4-[5-метил-3-фенилизоксазол-4-ил
Код ссылки
<a href="https://eas.patents.su/9-3754-4-5-metil-3-fenilizoksazol-4-il-benzolsulfonamid.html" rel="bookmark" title="База патентов Евразийского Союза">4-[5-метил-3-фенилизоксазол-4-ил] бензолсульфонамид</a>
Предыдущий патент: Способ получения 1-замещенных 5- или 3-гидроксипиразолов
Следующий патент: Способ и устройство для соединения труб на нефтяных месторождениях
Случайный патент: Способ и устройство для разжижения при сдвиге материала, содержащего твердое вещество