Способ получения замещённых бензимидазола
Номер патента: 5773
Опубликовано: 30.06.2005
Авторы: Брукс Руди Лоран Мария, Де Смале Дирк, Леэр Стефан Марсель Херман
Формула / Реферат
1. Способ получения замещенных бензимидазолов общей формулы (I)
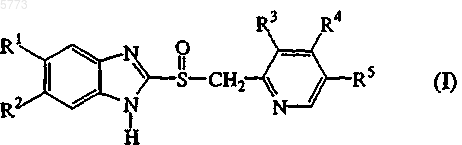
где R1 и R2 одинаковые или отличаются друг от друга и выбраны из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые или отличаются друг от друга, и выбраны из водорода, метила, метокси, метоксипропокси или трифторэтокси,
включающий стадии
a) взаимодействия соединения общей формулы (II)
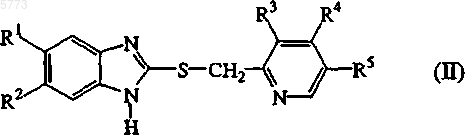
с окислителем в подходящем растворителе,
b) экстракции реакционной смеси водным раствором щелочи, имеющим pH в интервале от 9,50 до 12,00, и удаления водного слоя,
c) экстракции органического слоя, полученного на предыдущей стадии, водным раствором щелочи, имеющим pH 13,00 или выше, и удаления органического слоя,
d) выделения соединения формулы (I) из водного слоя, полученного на предыдущей стадии.
2. Способ по п.1, где на стадии b) первой экстракции pH составляет от 10,50 до 11,50.
3. Способ по п.1 или 2, где окислитель выбран из м-хлорпероксибензойной кислоты, монопероксифталата, пероксида водорода (в присутствии или в отсутствие катализаторов), перманганатов, N-хлор- или N-бромсукцинимида, 1,3-дибром-5,5-диметилгидантоина, 2-гидропероксигексафтор-2-пропанола, йодосилбензола, ацетилацетоната марганца (III), кислорода (в присутствии или в отсутствие катализаторов), озона, пероксимоносульфата, тетраоксида рутения, пербората, перйодата, ацилнитратов, трет-бутилгидропероксида, диметилдиоксиранов, гипохлорита, нитрата церия-аммония, 2-нитробензолсульфинилхлорид/супероксида калия, N-сульфонилоксазиридинов, бромита натрия или бензоилпероксида.
4. Способ по п.3, где окислителем является м-хлорпероксибензойная кислота.
5. Способ по любому из пп.1-4, где соединения формулы (I) бензимидазольного типа выбирают из рабепразола, омепразола, пантопразола, лансопразола и эсомепразола.
6. Способ по п.5, где соединением формулы (I) бензимидазольного типа является рабепразол.
7. Способ по п.6, где на стадии b) первой экстракции pH составляет от 10,70 до 11,20, предпочтительно pH варьирует от 10,85 до 10,95.
8. Способ удаления сульфонов формулы (III)
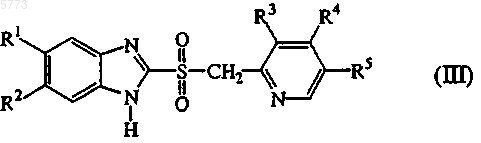
где R1 и R2 одинаковые или отличаются друг от друга, которые выбирают из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые или отличаются друг от друга, выбранные из водорода, метила, метокси, метоксипропокси или трифторэтокси,
из реакционной смеси, включающей сульфоксиды формулы (I)
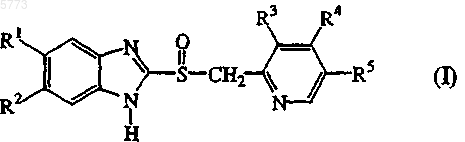
путем экстракции реакционной смеси водным раствором щелочи, pH которого варьирует от 9,50 до 12,00, удаления водного слоя и выделения сульфоксидов формулы (I) из органического слоя.
9. Способ по п.8, где на стадии экстракции pH составляет от 10,50 до 11,50.
10. Способ по любому из пп.8 или 9, где сульфоксидом формулы (I) является рабепразол.
Текст
005773 Настоящее изобретение относится к усовершенствованному способу получения ингибиторов протонного насоса бензимидазольного типа, таких как рабепразол, омепразол, пантопразол, лансопразол и эсомепразол. Соединение бензимидазольного типа, или его соль со щелочным металлом, обладает сильным ингибиторным действием на так называемый протонный насос. В общем смысле, они могут использоваться для профилактики и лечения заболеваний млекопитающих, особенно человека, связанных с секрецией желудочной кислоты, включая, например, желудочно-глоточный рефлюкс, гастрит, дуоденит, язву желудка и язву двенадцатиперстной кишки. Ингибиторы протонного насоса бензимидазольного типа легко разрушаются в кислых или нейтральных условиях, и для их получения требуются особые условия реакции. Способы получения указанных соединений бензимидазольного типа были раскрыты, например, в ЕР-0005129, ЕР-0066287, ЕР 0174726 и ЕР-0268956. Настоящее изобретение предоставляет усовершенствованный способ получения соединений бензимидазольного типа общей формулы (I) где R1 и R2 одинаковые, или отличаются друг от друга, и выбраны из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые, или отличаются друг от друга, и выбраны из водорода, метила, метокси,метоксипропокси или трифторэтокси,включающий стадии а) взаимодействия соединения общей формулы (II) с окислителем в подходящем растворителе,b) экстракции реакционной смеси водным раствором щелочи, имеющим рН в интервале от 9,50 до 12,00, и удаления водного слоя,c) экстракции органического слоя, полученного на предыдущей стадии, водным раствором щелочи,имеющим рН 13,00 или выше, и удаления органического слоя,d) выделения соединения формулы (I) из водного слоя, полученного на предыдущей стадии. Подразумевается, что термин "ингибиторы протонного насоса бензимидазольного типа", "соединения бензимидазольного типа" или "соединения формулы (I)", включает как нейтральную форму указанных соединений, так и соли указанных соединений со щелочными металлами. Соли щелочных металлов,например, представляют собой соли Mg2+, Ca2+, Na+, K+ или Li+, предпочтительно соли Мg2+ или Na+. Применяющиеся соединения бензимидазольного типа формулы (I) включают рацемическую форму, или по существу чистый энантиомер, или соли отдельных энантиомеров со щелочными металлами. Ниже приведены структурные формулы некоторых из указанных ингибиторов протонного насоса бензимидазольного типа лансопразол Подходящие ингибиторы протонного насоса бензимидазольного типа, раскрыты, например, в ЕР-0268956,ЕР-0005129 и ЕР-0174726. ЕР-0652872 раскрывает эзомепразол, т.е., магниевую соль (-)-энантиомера омепразола. Обычно соединения формулы (I) бензимидазольного типа получают путем окисления промежуточных сульфидных соединений формулы (II) в подходящем растворителе. На стадии окисления используют такой окислитель, как м-хлорпероксибензойная кислота, монопероксифталат, пероксид водорода (в присутствии или в отсутствие катализаторов), перманганаты, N-хлорили N-бромсукцинимид, 1,3-дибром-5,5-диметилгидантоин, 2-гидропероксигексафтор-2-пропанол, йодосилбензол, ацетилацетонат марганца (III), кислород (в присутствии или в отсутствие катализаторов),озон, пероксимоносульфат, тетраоксид рутения, перборат, перйодат, ацилнитраты, трет-бутилгидропероксид, диметилдиоксираны, гипохлорит, нитрат церия/аммония, 2-нитробензолсульфинилхлорид/надперекись калия, N-сульфонилоксазиридины, бромит натрия, бензоилпероксид и т. п., в системе растворителей, включающей органический растворитель, такой как, например, дихлорметан. Так как ингибиторы протонного насоса бензимидазольного типа легко разрушаются в кислых или нейтральных условиях, реакционную смесь обычно обрабатывают в основных условиях. Основные условия способствуют разложению любого нежелательного окислителя, все еще присутствующего в реакционной смеси, а также нейтрализации любой кислоты, образующейся в процессе реакции окисления с участием окислителя. Основной проблемой, связанной с окислительной реакцией превращения сульфидных промежуточных соединений формулы (II) в сульфоксидные соединения формулы (I), является переокисление, т.е.,окисление сульфоксидов формулы (I) до сульфонов формулы (III) Избежать образования сульфонов формулы (III) в результате переокисления практически невозможно, а свести его к минимуму можно путем проведения реакции окисления при низкой температуре и ограничения количества окислителя. Обычно количество окислителя составляет менее 1 молярного эквивалента по отношению к исходному веществу, т.е., к сульфидным промежуточным соединениям формулы (II), в результате превращению неизбежно подвергается менее 100% исходного вещества. Как пра-2 005773 вило, количество окислителя выбирают так, чтобы достичь компромисса между максимальным превращением исходного вещества, максимальным образованием сульфоксидов формулы (I) и минимальным образованием нежелательных сульфонов формулы (III). Кроме того, часто подтверждается, что удаление сульфонов формулы (III) является сложным, длительным и дорогим процессом, особенно, если требуется применение хроматографии высокого разрешения в промышленном масштабе. Целью настоящего изобретения является предоставление улучшенного способа синтеза соединений формулы (I) бензимидазольного типа, который является более удобным и более эффективным, чем ранее известные способы. В настоящем изобретении данная цель достигается путем предоставления усовершенствованного способа получения соединений общей формулы (I) бензимидазольного типа, включающего стадии а) взаимодействия соединения общей формулы (II) с окислителем в подходящем растворителе,b) экстракции реакционной смеси водным раствором щелочи, имеющим рН в интервале от 9,50 до 12,00, и удаления водного слоя,c) экстракции органического слоя, полученного на предыдущей стадии, водным раствором щелочи,имеющим рН 13,00 или выше, и удаления органического слоя,d) выделения соединения формулы (I) из водного слоя, полученного на предыдущей стадии. Усовершенствованный способ имеет преимущество, состоящее в том, что на первой стадии экстракции b) удаляются все образующиеся сульфоны формулы (III), а на второй стадии экстракции с) удаляются все непрореагировавшие сульфиды формулы (II), и в результате водный слой на стадии d) содержит только целевые соединения формулы (I) бензимидазольного типа, которые можно легко очистить до степени, необходимой для фармацевтических препаратов. Другое преимущество усовершенствованного способа состоит в том, что можно использовать больше окислителя, что позволяет получать более высокий выход соединений формулы (I) и более низкие уровни непрореагировавших сульфидов формулы (II), так как любые образующиеся нежелательные сульфоны формулы (III) легко удаляются на первой стадии экстракции, дальнейшая очистка выделенных сульфоксидов формулы (I) становится гораздо более легкой. Окислителем, используемым в вышеописанном усовершенствованном способе, может служить мхлорпероксибензойная кислота, монопероксифталат, пероксид водорода (в присутствии или в отсутствие катализаторов), перманганаты, N-хлор- или N-бромсукцинимид, 1,3-дибром-5,5-диметилгидантоин, 2 гидропероксигексафтор-2-пропанол, йодосилбензол, ацетилацетонат марганца (III), кислород (в присутствии или в отсутствие катализаторов), озон, пероксимоносульфат, тетраоксид рутения, перборат, перйодат, ацилнитраты, трет-бутилгидропероксид, диметилдиоксираны, гипохлорит, нитрат церия/аммония, 2 нитробензолсульфинилхлорид/надперекись калия, N-сульфонилоксазиридины, бромит натрия, бензоилпероксид, или любой другой окислитель, подходящий для окисления сульфидов формулы (II). Предпочтительно используют м-хлорпероксибензойную кислоту. Упомянутый окислитель соответственно используют в количестве, составляющем от 0,5 до 2,0 молярных эквивалентов по отношению к исходному веществу, т.е., к сульфидам формулы (II). Оптимальное количество окислителя зависит от типа используемого окислителя, конкретного сульфида формулы (II), а также от других условий реакции, таких, как растворитель и температура, и может быть легко определено опытным специалистом. Водным щелочным раствором на первой и второй стадиях экстракции может служить водный раствор любого неорганического основания, такого, как гидроксид натрия, гидроксид калия, карбонат натрия и т.п.; или водный раствор любого органического основания, такой как водный раствор аммиака и т.п. рН на первой стадии экстракции варьирует в основном от 9,50 до 12,00 и, предпочтительно, от 10,50 до 11,50. Если соединением формулы (I) бензимидазольного типа является рабепразол, рН предпочтительно варьирует от 10,70 до 11,20, более предпочтительно, рН варьирует от 10,85 до 10,95. Соединения формулы (I) могут быть выделены из водного слоя на стадии d) , например, путем добавления к указанному водному слою органического растворителя, такого, как, например, дихлорметан,и снижения рН, в результате чего соединения формулы (I) переходят в органический слой. Снизить рН можно, например, добавив водный раствор ацетата аммония. Затем указанный органический слой концентрируют под вакуумом,получая целевые соединения формулы (I). Конкретными соединениями формулы (I) бензимидазольного типа, которые можно получить по усовершенствованному способу настоящего изобретения, являются рабепразол, омепразол, пантопразол,лансопразол и эсомепразол, в особенности, рабепразол.-3 005773 В другом аспекте настоящее изобретение также предоставляет способ удаления сульфонов формулы (III), где R1 и R2 одинаковые, или отличаются друг от друга, и выбраны из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые, или отличаются друг от друга, и выбраны из водорода, метила,метокси, метоксипропокси или трифторэтокси из реакционной смеси, включающей сульфоксиды формулы (I), где R1 и R2 одинаковые, или отличаются друг от друга, и выбраны из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые, или отличаются друг от друга, и выбраны из водорода, метила, метокси, метоксипропокси или трифторэтокси путем экстракции реакционной смеси водным раствором щелочи, рН которого варьирует от 9,50 до 12,00, предпочтительно от 10,50 до 11,50, удаления водного слоя и выделения сульфоксидов формулы (I) из органического слоя. Если сульфоксидом формулы (I) является рабепразол, рН предпочтительно варьирует от 10,70 до 11,20, более предпочтительно рН варьирует от 10,85 до 10,95. В предпочтительном воплощении упомянутого способа удаления сульфонов формулы (III) сульфоксид формулы (I) представляет собой рабепразол. Далее настоящее изобретение иллюстрируется с помощью примеров, не ограничивающих данное изобретение. Экспериментальная часть В описанных ниже процедурах используются следующие аббревиатуры: "m-СРВА" обозначает мета-хлорпероксибензойную кислоту, "PTBI" обозначает 2-4-(3-метоксипропокси)-3-метил-2-пиридинил]метил]тио]-1 Н-бензимидазол, "PPSI" обозначает 2-4-(3-метоксипропокси)-3-метил-2-пиридинил]метил]сульфинил]-1 Н-бензимидазол (также известный как рабепразол), и SUBI обозначает 24-(3-метоксипропокси)-3-метил-2-пиридинил]метил]сульфонил]-1 Н-бензимидазол. Пример 1. К раствору PTBI (0,25 моль) в дихлорметане (688 мл), перемешиваемому при температуре -20 С, в течение 1 ч добавляют раствор m-СРВА (0,22 моль) в дихлорметане (330 мл), поддерживая при этом температуру реакционной смеси -20 С. Реакционную смесь перемешивают 30 мин при -20 С. Стадия первой экстракции К органическому слою добавляют воду (368 мл) и рН повышают до 10,40 с помощью раствораNaOH (10%). рН реакционной смеси доводят до рН=10,85 водным раствором NH3 и водный слой отделяют от органического слоя. Стадия второй экстракции К органическому слою добавляют воду (368 мл) и рН повышают до 13,0 с помощью раствора NaOH(10%). Органический слой удаляют и к водному слою добавляют дихлорметан (168 мл). При перемешивании добавляют водный раствор ацетата аммония до получения рН 10,50. Водный слой отделяют от органического слоя и органический слой концентрируют при пониженном давлении, получая остаток. Данный остаток кристаллизуют из ацетона, получая PPSI (0,143 моль, 57%). Пример 2. К раствору PTBI (0,25 моль) в дихлорметане (688 мл), перемешиваемому при температуре -20 С, в течение 1 ч добавляют раствор m-СРВА (0,15 моль) в дихлорметане (360 мл), поддерживая при этом температуру реакционной смеси -20 С. Реакционную смесь перемешивают 30 мин при -20 С. Стадия экстракции К органическому слою добавляют воду (368 мл) и рН повышают до 13,0 с помощью раствора NaOH(10%). Органический слой удаляют и к водному слою добавляют дихлорметан (168 мл). При перемешивании добавляют водный раствор ацетата аммония до получения рН 10,50. Водный слой отделяют от органического слоя и органический слой концентрируют при пониженном давлении, получая остаток. Данный остаток кристаллизуют из ацетона, получая PPSI (0,11 моль, 44%). Чистоту полученного PPSI измеряют с помощью ВЭЖХ на колонке Nucleosil 100 С 18 (5 мкм, 150 мм х 4,6 мм внутр.диам.), используя изократическое элюирование со скоростью потока 1 мл/мин, подвижную фазу, включающую 40% элюента А и 60% элюента В (элюент А представляет собой смесь 0,05 М KН 2 РО 4 и 0,05 М Na2HPO4, pH 7, в соотношении 2:1 (об./об.); элюент В представляет собой метанол) и УФ-детекцию при 290 нм.-4 005773 Таблица 1. Сравнение параметров реакции (выход PPSI определяют после кристаллизации по отношению к исходному веществу PTBI) Предназначенный для применения в фармацевтических препаратах PPSI, широко известный как рабепразол, не должен содержать более 0,8% сульфона SUBI. Следовательно, стадия первой экстракции, в процессе которой происходит удаление из реакционной смеси всех образовавшихся сульфонов, позволяет использовать более высокое количество окислителя, обеспечивая таким образом значительно более высокий выход PPSI без необходимости изменять процедуру обработки, т.е. кристаллизацию, для получения сульфоксида PPSI, содержащего 0,8% или менее сульфона SUBI. Пример 3. Методика общего окисления и экстракции. А. Способ А (включающий дополнительную стадию экстракции для удаления сульфонов формулы (III К раствору сульфидного промежуточного соединения формулы (II) (0,05 моль) в дихлорметане(137,5 мл), перемешиваемому при температуре -40 С, в течение 1 ч добавляют раствор m-СРВА (0,92 эквивалента или 0,046 моль) в дихлорметане (82,5 мл), поддерживая температуру реакционной смеси при-40 С. Реакционную смесь перемешивают 30 мин при -40 С. Стадия первой экстракции Охлаждение реакционной смеси останавливают, затем рН повышают до 10,40 с помощью раствораNaOH (10%) и к органическому слою добавляют воду (75 мл). рН реакционной смеси доводят до рН=11,10 водным раствором NH3 и водный слой отделяют от органического слоя. Стадия второй экстракции К органическому слою, полученному на предыдущей стадии, добавляют воду (75 мл) и рН повышают до 13,0 с помощью раствора NaOH (10%). Органический слой удаляют и к водному слою добавляют дихлорметан (75 мл). При перемешивании добавляют водный раствор ацетата аммония до получения рН 10,44. Водный слой отделяют от органического слоя и органический слой концентрируют при пониженном давлении, получая твердый остаток.B. Способ В (без дополнительной стадии экстракции для удаления сульфонов формулы (III К раствору сульфидного промежуточного соединения формулы (II) (0,05 моль) в дихлорметане (137,5 мл), перемешиваемому при температуре -40 С, в течение 1 ч добавляют раствор m-СРВА (0,92 эквивалента или 0,046 моль) в дихлорметане (82,5 мл), поддерживая температуру реакционной смеси при -40 С. Реакционную смесь перемешивают 30 мин при -40 С. Стадия экстракции Охлаждение реакционной смеси останавливают, затем рН повышают до 13,0 с помощью раствораNaOH (10%) и к органическому слою добавляют воду (75 мл). Органический слой удаляют и к водному слою добавляют дихлорметан (75 мл). При перемешивании добавляют водный раствор ацетата аммония до получения рН 10,50. Водный слой отделяют от органического слоя и органический слой концентрируют при пониженном давлении, получая твердый остаток.C. Результаты В нижеследующей табл. 2 приведены результаты для ингибиторов протонного насоса рабепразола,омепразола и лансопразола, которые были получены при использовании способа А (включающего дополнительную стадию экстракции для удаления сульфонов формулы (III и способа В (без дополнительной стадии экстракции для удаления сульфонов формулы (III. Исходным сульфидом формулы (II) для получения рабепразола является 2-4-(3 метоксипропокси)-3-метил-2-пиридинил]метил]тио]-1 Н-бензимидазол. Исходным сульфидом формулы(II) для получения омепразола является 5-метокси-2-(4-метокси-3,5-диметил-2-пиридинил)метил]тио]1 Н-бензимидазол. Исходным сульфидом формулы (II) для получения лансопразола является 2-3 метил-4-(2,2,2-трифторэтокси)-2-пиридинил]метил]тио]-1 Н-бензимидазол. Количество сульфонов формулы (III) и соединений формулы (I), присутствующих в твердых остатках, полученных по способу А или по способу В, измеряют с помощью ВЭЖХ на колонке Nucleosil 100 С 18 (5 мкм, 150 мм х 4,6 мм внутр.диам.), используя изократическое элюирование со скоростью потока 1 мл/мин, подвижную фазу, включающую 40% элюента А и 60% элюента В (элюент А представляет собой смесь 0,05 М KН 2 РО 4 и 0,05 М Na2HPO4, рН 7, в соотношении 2:1 (об./об.); элюент В представляет собой метанол), и УФ-детекцию при 290 нм. Стандартное отклонение составляет менее 5%.-5 005773 Таблица 2. Количество сульфонов формулы (III) и соединений формулы (I), присутствующих в полученных твердых остатках ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения замещенных бензимидазолов общей формулы (I) где R1 и R2 одинаковые или отличаются друг от друга и выбраны из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые или отличаются друг от друга и выбраны из водорода, метила, метокси, метоксипропокси или трифторэтокси,включающий стадии а) взаимодействия соединения общей формулы (II)b) экстракции реакционной смеси водным раствором щелочи, имеющим рН в интервале от 9,50 до 12,00, и удаления водного слоя,c) экстракции органического слоя, полученного на предыдущей стадии, водным раствором щелочи,имеющим рН 13,00 или выше, и удаления органического слоя,d) выделения соединения формулы (I) из водного слоя, полученного на предыдущей стадии. 2. Способ по п.1, где на стадии b) первой экстракции рН составляет от 10,50 до 11,50. 3. Способ по п.1 или 2, где окислитель выбран из м-хлорпероксибензойной кислоты, монопероксифталата, пероксида водорода (в присутствии или в отсутствие катализаторов), перманганатов, N-хлорили N-бромсукцинимида, 1,3-дибром-5,5-диметилгидантоина, 2-гидропероксигексафтор-2-пропанола,йодосилбензола, ацетилацетоната марганца (III), кислорода (в присутствии или в отсутствие катализаторов), озона, пероксимоносульфата, тетраоксида рутения, пербората, перйодата, ацилнитратов, третбутилгидропероксида, диметилдиоксиранов, гипохлорита, нитрата церия-аммония, 2-нитробензолсульфинилхлорид/супероксида калия, N-сульфонилоксазиридинов, бромита натрия или бензоилпероксида. 4. Способ по п.3, где окислителем является м-хлорпероксибензойная кислота. 5. Способ по любому из пп.1-4, где соединения формулы (I) бензимидазольного типа выбирают из рабепразола, омепразола, пантопразола, лансопразола и эсомепразола. 6. Способ по п.5, где соединением формулы (I) бензимидазольного типа является рабепразол. 7. Способ по п.6, где на стадии b) первой экстракции рН составляет от 10,70 до 11,20, предпочтительно рН варьирует от 10,85 до 10,95. 8. Способ удаления сульфонов формулы (III) где R1 и R2 одинаковые или отличаются друг от друга, которые выбирают из водорода, метокси или дифторметокси, R3, R4 и R5 одинаковые или отличаются друг от друга, выбранные из водорода, метила, метокси, метоксипропокси или трифторэтокси,из реакционной смеси, включающей сульфоксиды формулы (I) путем экстракции реакционной смеси водным раствором щелочи, рН которого варьирует от 9,50 до 12,00, удаления водного слоя и выделения сульфоксидов формулы (I) из органического слоя. 9. Способ по п.8, где на стадии экстракции рН составляет от 10,50 до 11,50. 10. Способ по любому из пп.8 или 9, где сульфоксидом формулы (I) является рабепразол.
МПК / Метки
МПК: C07D 401/12
Метки: бензимидазола, способ, получения, замещённых
Код ссылки
<a href="https://eas.patents.su/8-5773-sposob-polucheniya-zameshhyonnyh-benzimidazola.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения замещённых бензимидазола</a>
Предыдущий патент: 17α-фторалкилстероиды, способ их получения и содержащие эти соединения фармацевтические композиции
Следующий патент: 3′-пролекарства 2′-дезокси-β-l-нуклеозидов
Случайный патент: Способ утилизации металлов












