Псевдополиморф (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4r-(3s-гидрокси-1-метил)пиперидинил]-4h-1-бензопиран-4-она
Номер патента: 5247
Опубликовано: 30.12.2004
Авторы: Силви Гари Л., Бафус Гари Л., Харрисон-Боумэн Кристин М.
Формула / Реферат
1. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]-4H-1-бензопиран-4-она, имеющий порошковую рентгенограмму, характеризующуюся расстояниями D
| Расстояние D-Е |
| 12.708 |
| 4.323 |
| 5.594 |
| 5.349 |
| 3.590 |
2. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]-4H-1-бензопиран-4-она, имеющий порошковую рентгенограмму, характеризующуюся расстояниями D и относительными интенсивностями
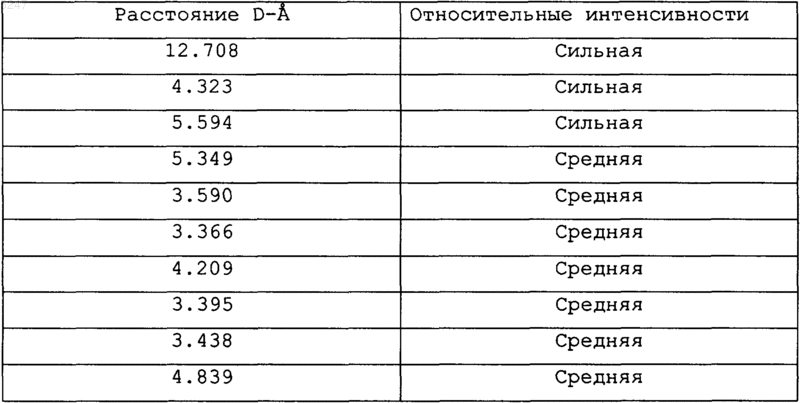
3. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]-4H-1-бензопиран-4-она, имеющий порошковую рентгенограмму, характеризующуюся расстояниями D и относительными интенсивностями в процентах
![]()
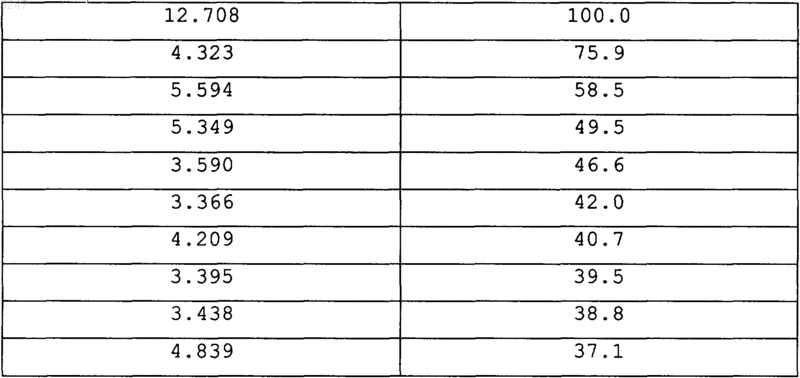
4. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]-4H-1-бензопиран-4-она, имеющий порошковую рентгенограмму, показанную в таблице.

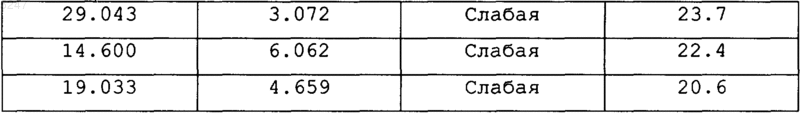
5. Способ получения формы I по пп.1, 2, 3 или 4, включающий
(a) объединение достаточного количества формы II с достаточным количеством соответствующего азеотропного растворителя с образованием азеотропной смеси;
(b) азеотропную отгонку азеотропной смеси, достаточную для образования формы I; и
(c) необязательное извлечение формы I из продукта дистилляции.
6. Способ по п.5, где растворитель является кетонным растворителем.
7. Способ по п.6, где растворитель является метилэтилкетоном.
8. Способ по п.5, где кристаллическую форму I извлекают фильтрацией формы I.
9. Способ по п.5, где температура азеотропной отгонки составляет от около 73 до около 80шC.
Текст
1 Предшествующий уровень Соединение (-)-цис-2-(2-хлорфенил)-5,7 дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1-бензопиран-4-он или одна из его фармацевтически приемлемых солевых форм(известная как Флавопиридол) является иммуномодулятором и противовоспалительным средством (патент США 4900727) и ингибитором кодируемых онкогеном киназ или тирозинкиназ рецептора фактора роста (патент США 5284856). Флавопиридол является сильным ингибитором циклинзависимых киназ (CDKs),включающих CDK1, CDK2, CDK4, CDK6 иcdk7/циклин H), при этом он обладает возможностью вызывать ингибирование продвижения клеточного цикла в G1 и G2 посредством множественных механизмов, связанных с ингибированием cdk. Смотри: International Journal of Oncology 9: 1143-1168 (1996). Было показано, что флавопиридол ингибирует также семейство EGF рецепторов, рецептор, связанный с семействомSRC киназ, и преобразующие сигнал киназы. Эксперименты in vitro и in vivo показали, что флавопиридол способен ингибировать широкий диапазон типов опухолей человека, лейкозов и лимфом.(-)-цис-2-(2-хлорфенил)-5,7-дигидрокси 8[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1 бензопиран-4-он или его фармацевтически приемлемая соль кристаллизируется в виде множества сольватов при использовании растворителей, таких как этанол, ДМСО, метанол, ацетонитрил/изопропанол, этанол/изопропанол и изопропанол и в виде сольватных гидратов при использовании комбинаций растворителей, таких как этанол/ и изопропанол/вода. Самой подходящей сольватной формой является этанольный сольват гидрохлорида флавопиридола (далее в описании форма II). Хотя форма II удовлетворяет фармацевтическим стандартам, она имеет склонность абсорбировать воду в том случае, когда не упакована в водонепроницаемую упаковку, вследствие чего увеличиваются производственные затраты. Для удобного манипулирования и получения разрешений от фармакомитетов по всему миру желательно иметь максимально возможную устойчивость кристаллической структуры. Цель настоящего изобретения предусматривает форму флавопиридола в виде формы,обладающей превосходными физическими свойствами, подходящей для использования в фармацевтической композиции. Сущность изобретения Настоящее изобретение включает псевдополиморф формы I, который определен порошковой рентгенограммой. Форма I предпочтительно не содержит форму II и/или другие формы флавопиридола. Она является пригодной в фармацевтической композиции, содержащей 2 эффективное количество формы I и фармацевтически приемлемый носитель. Форма I является полезной в качестве ингибитора протеинкиназы, ингибитора циклинзависимой киназы и при терапии различных форм рака. Форма I дополнительно характеризуется способностью быть менее гигроскопичной, чем форма II, и имеет меньший ожидаемого прирост веса при сравнительных относительных влажностях. Форму I получают объединением достаточного количества формы II с достаточным количеством соответствующего азеотропного растворителя, вследствие чего образуется азеотропная смесь; азеотропной перегонки полученной азеотропной смеси, достаточной для образования формы I; и необязательным выделением формы I из полученного продукта. Описание чертежей Фиг. 1: Установленный порошковой рентгенограммой (XRPD) предел обнаружения формы II в форме I. Для оценки предела обнаружения формы II в форме I аккуратно взвешивали различные количества формы II и тщательно перемешивали(в неизмельченном виде) с формой I. Всю смесь переносили в платиновый держатель образца и выравнивали с использованием предметного стекла. Все образцы сканировали со скоростью 0,2/мин. в диапазоне 2 12-16. Проводили, по меньшей мере, повторные определения для каждого уровня пика, XRPD усредняли и измеряли высоту пика при 213,8. Установленный предел обнаружения формы II в форме I составляет 3%. Подробное описание изобретения Форма I представляет собой гидрохлорид(-)-цис-2-(2-хлорфенил)-5,7-дигидрокси 8[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1 бензопиран-4-она. Она является таким же активным ингредиентом, как и флавопиридол, но отличается от известных кристаллов флавопиридола тем, что является безводной и/или не содержит сольват, т.е. представляет собой псевдополиморф известных форм флавопиридола. Форма I идентифицирована дифракцией рентгеновских лучей на образце порошка (порошковыми рентгенограммами), полученной с использованием СuK-альфа-излучения, характеризующейся расстояниями D следующим образом: Форму I идентифицируют также порошковыми рентгенограммами, полученными с использованием СuK-альфа-излучения, характеризующимися расстояниями D и относительными интенсивностями. 4 Форма I предпочтительно по существу не содержит форму II и/или другие формы флавопиридола. Выражение по существу не содержит форму II и/или другие формы флавопиридола означает, что форма II и/или другие формы флавопиридола присутствуют, как показано порошковой дифракцией рентгеновских лучей или ядерным магнитным резонансом (ЯМР), в количестве менее 10, 9, 8, 7, 6, 5, 4 и 3%. Выражение другие формы флавопиридола включает основные и солевые формы, которые являются подходящими и включают гидраты, сольваты или сольватные гидраты, но не включают форму I или форму II. Форма II означает сольват/гидрат гидрохлорида (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси-1-метил)пиперидинил]4 Н-1-бензопиран-4-она в этаноле/воде, описанный порошковой дифракцией рентгеновских лучей, полученной с использованием СuKальфа-излучения, в табл. 2. Таблица 2 Порошковая дифракция рентгеновских лучей более полно описана в табл. 1. Таблица 1 Форму I предпочтительно получают объединением достаточного количества формы II с достаточным количеством соответствующего азеотропного растворителя, вследствие чего образуется азеотропная смесь; азеотропной перегонкой азеотропной смеси, достаточной для образования формы I; и необязательным выделением формы I из продукта дистилляции. Выражение достаточное количество формы II означает количество, необходимое для образования такого количества кристаллов формы I, которое может быть извлечено. Специалисты в данной области могут определить указанное количество экспериментально. Выражение достаточное количество подходящего растворителя означает подходящий растворитель в количестве, достаточном, по меньшей мере, для частичного растворения формы II, вследствие которого образуется реакционная смесь, указанное количество может быть определено специалистом в данной области экспериментально. В описанных далее экспериментах даны примеры количеств, которые могут быть использованы. Выражение соответствующие условия большей частью зависит от выбранного подходящего растворителя. Так, например, если соответствующие условия включают азеотропную 5 перегонку (дистилляцию), выбирают соответствующий азеотропный растворитель. Выражение подходящий растворитель означает растворитель, который, по меньшей мере, частично растворяет форму II и дает возможность образованию кристаллов формы I. Подходящий растворитель может быть соответствующим азеотропным растворителем или же иным, указанным в данном описании. Выражение азеотропная смесь относится к жидкой смеси двух или более веществ, которые ведут себя как одно вещество, при этом пар,полученный частичным выпариванием жидкости, имеет тот же состав, что и жидкость. Постоянно кипящая смесь показывает по сравнению с другими смесями такого же вещества или максимальную, или минимальную точку кипения. Выражение азеотропная дистилляция относится к типу перегонки, в которой к подлежащей отделению смеси добавляют вещество для образования азеотропной смеси с одним или несколькими компонентами первоначальной смеси. Обычно азеотропную смесь нагревают до температуры, при которой из формы II отделяется сольват/вода. Образованные таким образом азеотропы будут иметь точки кипения, отличающиеся от точек кипения первоначальной смеси. Выражение соответствующий(ие) азеотропный(ые) растворитель(и) включает кетонные растворители, такие как ацетон, метилэтилкетон и подобные растворители; алифатические сложноэфирные растворители, такие как этилацетат, метилацетат, метилформиат, этилформиат, изопропилацетат и подобные; смеси кетонных растворителей и алифатических сложноэфирных растворителей; С 5-С 8-алифатические растворители, такие как пентан, гексан и подобные; алифатические нитрилы, такие как ацетонитрил; бензол, толуол, пиридин и т.д. Смотри,например, Practical Organic Chemistry, 3 rd ed.,John Wiley and Sons, 1956, например, стр.10-11,данный источник информации включен в описание в качестве ссылки. Используемое в данном описании выражение подходящая температура относится к такой температуре, которая обеспечивает возможность кристаллизации формы I без существенного повреждения образующейся таким образом формы I. При азеотропной дистилляции будет иметься точка кипения, при которой отделяется сольват и/или вода. В указанной точке форма I находится в форме кристалла, который осаждается и который можно извлечь отделением. Обычно это можно осуществить фильтрацией кристалла или выпариванием растворителя или иным способом отделения растворителя от кристалла или кристалла от растворителя. Может быть также подходящей сушка растворителя, например вы 005247 6 паривание при комнатной температуре или при нагреве. Важной отличительной особенностью формы I по сравнению с формой II является способность формы II не абсорбировать легко воду из атмосферы. Настоящее изобретение предусматривает форму флавопиридола, которая имеет во фракциях прирост веса, вследствие абсорбции воды, менее 5%, включая 4, 3, 2, 1 и менее 1% (обычно около 1-2%) при относительной влажности около 75% и даже при относительной влажности около 90% (прирост веса в данном случае составляет около 3,5%). Форма II в виде сольвата/гидрата показывала медленный,но постоянный прирост веса около 4% при относительной влажности до около 60%. При относительной влажности более 60% форма II показывала прирост веса около 15-20%. Пример 1. Получение флавопиридола формы I. В 600 мл химический стакан помещают примерно 6 г флавопиридола формы II. При перемешивании медленно добавляют 300 мл метилэтилкетона (МЕК), при этом получают суспензию. Раствор медленно нагревают до 50 С до появления мутности. Температуру увеличивают до около 73 С при перемешивании и добавляют 100 мл растворителя. Когда раствор был доведен до сильного кипения, из него начинает выпадать осадок и оседать на дно. Температуру увеличивают и устанавливают равной 80 С (точка кипения МЕК) в течение нескольких минут, при этом получают дополнительный осадок, который удаляют и дают возможность охладиться до около 55 С. Конечный объем раствора 325 мл фильтруют в вакууме через воронку Бюхнера с использованием фильтровальной бумаги 1 Ватман; в результате получали плотный желтый хлопьевидный порошок в виде толстого ломтя. Структуру подтверждают масс-спектрометрией, ядерным магнитным резонансом и Фурье ИК спектроскопией и дифракцией рентгеновских лучей на образце порошка. Пример 2. Методика дифракции рентгеновских лучей на порошке. Порошковые рентгенограммы (XRPD) получали на дифрактометре Scintag XDS 2000 /,работающем с излучением меди при 45 кВ и 40 мA, с использованием охлажденного кремниевого детектора Kevex Psi Peltier. Для сбора данных использовали щели источника излучения 2 и 4 мм и щели детектора излучения 0,5 и 0,3 мм. Полученный образец осторожно измельчали с использованием агатовой ступки и пестика в течение примерно одной минуты, помещали в платиновый держатель образца и выравнивали с использованием предметного стекла. Порошковые рентгенограммы образцов получали при сканировании в диапазоне 2 от 2 до 42 со скоростью 1/мин. Калибрование XDS 2000 вери 7 фицировали ежегодно с использованием в качестве стандартного образца кремниевого порошка. Пример 3. Защита от гигроскопичности сравнение формы I и формы II Проводили сравнительный анализ динамической сорбции пара (DVS) формы II и формы I. Анализ динамической сорбции водяного пара (DVS). Форму II исследовали при 25 С с использованием анализатора динамической сорбции пара DVS-1 в системах измерения на поверхности. Образец весом примерно 14,8 мг помещали в тарированный кварцевый держатель образца при начальной влажности помещения, установленной примерно на относительную влажность(RH) 48%. Во время исследований использовали скорость потока влажного/сухого азота 200 см 3/мин. Устанавливали следующий полный программный цикл: 30 мин. при начальной RH,затем при RH 0, 20, 40, 60, 80, 90, 95 и 98%,причем длительность экспозиции в каждой выбранной точке влажности, зависящая от dm/dt,равного менее 0,001%, составляла 60 мин. Максимальное время, допускаемое в одной любой выбранной точке влажности, было равно 24 ч. Сбор данных осуществляли в течение полного цикла около 4 дней. После завершения полного цикла образец выдерживали при значении RH,равном значению начальной влажности. Форму I исследовали при 25 и 40 С с использованием анализатора DVS-1. Данные собирали в течение двух полных циклов. Образцы весом 10,4 и 16,7 мг помещали в соответствующие тарированные кварцевые держатели образца при начальной влажности помещения, установленной примерно на RH 46% и RH 33% соответственно. В данном исследовании использовали дополнительную выбранную точку RH 75%. Сбор данных в течение 2 полных циклов осуществляли при 25 С около 7 дней и при 40 С в течение около 17 дней. После завершения исследования каждого 2-го цикла образцы выдерживали при значении RH, равном значению начальной влажности. Порошковые рентгенограммы (XRPD) получали на дифрактометре Scintag XDS 2000 /,работающем с излучением меди при 45 кВ и 40 мА, с использованием кремниевого детектора,охлажденного Kevex Psi Peltier. Для сбора данных использовали щели источника излучения 2 и 4 мм и щели детектора излучения 0,5 и 0,3 мм. Образцы формы II осторожно измельчали с использованием агатовой ступки и пестика в течение примерно одной минуты, помещали в платиновый держатель образца и выравнивали с использованием предметного стекла. Образцы,взятые во время или после испытания на гигроскопичность, вследствие ограниченного количества доступного образца, не измельчали. В каждом случае порошковые рентгенограммы скани 005247 ровали в диапазоне 2 от 2 до 42 со скоростью 1/мин. Калибрование XDS 2000 верифицировали с использованием кремниевого порошка. Для экспериментов, осуществляемых при различных относительных влажностях, использовали DVS-2, анализатор динамической сорбции пара в системах измерения на поверхности большей емкости. С использованием скорости потока 500 см 3/мин форму II выдерживали при выбранных значениях RH и периодически осуществляли отбор проб образца для анализаXRPD. Неизмельченный материал помещали в платиновую чашку и перед анализом при вышеуказанных условиях выравнивали с использованием предметного стекла. Форма II показывала медленный, но непрерывный прирост веса до RH примерно 60%,равный примерно 4%, при этом при относительной влажности более 60% наблюдали дополнительный прирост веса, равный 15-20%. По сравнению с формой II форма I показывала прирост веса при RH около 75%, равный примерно 1-2%,плюс дополнительный прирост веса при RH около 90%, равный 3,5%. При RH выше около 90% наблюдался прирост веса около 30%. Таким образом, форму II следует считать гигроскопичной, тогда как форму I следует считать гигроскопичной при RH выше около 75%. Порошковая дифракция рентгеновских лучей при переменной влажности показала, что когда влажность увеличивается, имеется явное уменьшение кристалличности в форме II и значительное изменение порошковой рентгенограммы, которое предположительно обусловлено потерей этанола. Очевидно, что до достижения чрезвычайно высокой относительной влажности (т.е.98%) форма I удерживает свою кристалличность, тогда как в указанной точке она утрачивает кристалличность и становится аморфной. Как следует из полученных результатов,форма I по сравнению с формой II имеет превосходные физические свойства и является подходящей для использования в фармацевтической композиции. Пример 4. Форма II Реактор загружают в атмосфере азота (-)цис-1-метил-4R-(2,4,6-триметоксифенил)-3S-пиперидинолом и уксусным ангидридом. Во время перемешивания с постоянной скоростью добавляют этерат трифторида бора и полученный раствор охлаждают до температуры 8-20 С. После завершения добавления образованную смесь перемешивают при 20-30 С в течение 3-5 ч. Реакционную смесь охлаждают до 8-12 С и при перемешивании добавляют смесь воды со льдом и затем водный раствор гидроксида натрия до достижения рН 10-11. Смесь экстрагируют этилацетатом. Этилацетатные экстракты объединяют и концентрируют в вакууме. Остаток переносят в метанол и воду. Затем добавляют гидроксид натрия(примерно 50% водный раствор). Реакционную смесь перемешивают при 20-30 С в течение 2-3 ч. Смесь выпаривают при пониженном давлении и температуре 80 С. Остаток охлаждают до температуры 15-20 С и с использованием концентрированной соляной кислоты рН доводят до значения 8,5-9,5. Твердые осадки, собранные фильтрацией, промывают деминерализованной водой и сушат при пониженном давлении, при этом получают -)-цис-1-метил-4-(3-ацетил-4,6 диметокси-2-гидрокси)фенил-3-пиперидинол). Затем -)-цис-1-метил-4-(3-ацетил-4,6-диметокси-2-гидрокси)фенил-3-пиперидинол) порциями добавляют к перемешиваемой суспензии трет-бутоксида калия в сухом N,Nдиметилформамиде при такой скорости, чтобы температура не превышала 20 С. После завершения добавления образованную смесь перемешивают в течение одного часа при температуре 30 С. Метил 2-хлорбензоат добавляют с такой скоростью, чтобы температура не превышала 30 С. Образованную смесь перемешивают при 20-30 С в течение 4-6 ч. Добавляют деминерализованную воду, затем концентрированную соляную кислоту до достижения рН смеси 6-8. Смесь два раза экстрагируют с использованием хлороформа. Хлороформные экстракты объединяют вместе и концентрируют при пониженном давлении. После охлаждения оставшегося масла до температуры 40 С добавляют концентрированную соляную кислоту. Затем смесь перемешивают при 40 С в течение 2 ч или, когда необходимо, в течение ночи. После охлаждения реакционной смеси до 15-30 С добавляют воду и хлороформ. Полученную смесь подщелачивают с использованием раствора гидроксида натрия (50%) до рН 8,5-10,5. Фазы разделяют. Затем водный слой экстрагируют хлороформом. Объединенные органические экстракты выпаривают при пониженном давлении с получением -цис-2-(2-хлорфенил)-5,7-диметокси-8[4R-(3Sгидрокси-1-метил)пиперидинил]-4 Н-1-бензопиран-4-она в виде масла, которое непосредственно используют на следующей стадии без очистки. К (-)-цис-2-(2-хлорфенил)-5,7-диметокси 8[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1 бензопиран-4-ону добавляют хинолин и пиридин. Образованную смесь нагревают при перемешивании до 160-190 С. Перемешивание продолжают при поддержании температуры 160190 С в течение 2 ч. После охлаждения реакционной смеси до 90-110 С добавляют воду. Полученную смесь подщелачивают с использованием насыщенного раствора карбоната натрия до рН 7,5-8,5. Смесь этанола дважды экстрагируют смесью этанола и хлороформа. Объединенные экстракты выпаривают досуха с получением сырого 10 перидинил]-4 Н-1-бензопиран-4-она в виде коричневой смолы, которую очищают следующим образом. К сырому(+)-цис-2-(2-хлорфенил)-5,7 дигидрокси-8-[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1-бензопиран-4-ону добавляют ацетон. Полученную смесь перемешивают при 55-60 С в течение 30-60 мин, затем охлаждают до 15-20 С и перемешивают в течение еще 1-2 ч. Осажденное твердое вещество выделяют фильтрацией, дважды промывают ацетоном и сушат при пониженном давлении с получением (+)-цис-2-(2-хлорфенил)5,7-дигидрокси-8-[4R-(3S-гидрокси-1-метил)пиперидинил]-4 Н-1-бензопиран-4-она в очищенной форме. Свободное основание с предыдущей стадии суспендируют в этаноле и подкисляют концентрированной соляной кислотой с такой скоростью, чтобы температура не превышала 30 С. Во время процесса все твердое вещество сначала растворяется и затем осаждается гидрохлорид. Суспензию охлаждают до 0-10 С и перемешивают в течение 1 ч при поддержании температуры. Кристаллы выделяют фильтрацией и промывают холодным этанолом с получением сырого гидрохлорида (-)-цис-2-(2-хлорфенил)5,7-дигидрокси-8[4R-(3S-гицрокси-1-метил)пиперидинил]-4 Н-1-бензопиран-4-она. К сырому гидрохлориду (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она добавляют этанол. Полученную смесь нагревают до 70-79 С, перемешивают в течение 1 ч при поддержании температуры и затем фильтруют,пока она еще горячая. Фильтр промывают горячим этанолом. Фильтрат концентрируют атмосферной перегонкой до удаления от около 60 до около 80% летучих компонентов. Затем оставшуюся суспензию охлаждают до 0-10 С, выделяют фильтрацией осадок и сушат при пониженном давлении с получением очищенного этанольного сольвата гидрохлорида (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она в виде желтого твердого вещества. После извлечения формы I можно получить фармацевтическую композицию. Используемое в данном описании выражение фармацевтическая композиция означает терапевтически эффективное количество формы I с фармацевтически приемлемым носителем. Выражение фармацевтически приемлемый носитель означает вещество, которое является нетоксичным, не оказывает влияние на терапевтический профиль формы I и является подходящим для способа введения. Форму I предпочтительно вводят внутривенно в течение периода времени, подходящего для химиотерапии рака. Форму I предпочтительно смешивают с одним или несколькими фармацевтически приемлемыми носителями. Так, например, форма I может быть смешана для внутривенного 11 введения больному с изоосмотическими жидкостями и жидкостями с регулируемыми значениями рН, такими как вода, смесь декстроза/вода или смесь солевой раствор/вода. Выражение эффективное количество включает терапевтически эффективное количество, количество, эффективное для ингибирования протеинкиназ, количество, эффективное для ингибирования циклинзависимой киназы, и количество формы I, эффективное для ингибирования опухоли, которое будет изменяться в зависимости от индивидуума, сопутствующей терапии, вида заболевания и других переменных факторов. Эффективное количество формы I будет примерно таким же, как количество формы II. Обычно доза формы I будет составлять от 0,001 мг/кг массы тела до 100 мг/кг массы тела в день. Флавопиридол является пригодным для лечения ряда болезненных состояний или заболеваний вследствие ингибирования протеинкиназ и в особенности, как указывалось выше,циклинзависимых киназ. Предполагается, что флавопиридол будет пригодным для лечения широкого диапазона раковых заболеваний,включающих, например, лейкоз, мезотелиому и раки легкого (крупноклеточный, мелкоклеточный и немелкоклеточный), прямой кишки, молочной железы, яичников, меланомы простаты,почек, тела матки и центральной нервной системы. Все цитированные в данном описании статьи и патенты включены в него в качестве ссылок. 3. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она,имеющий порошковую рентгенограмму, характеризующуюся расстояниями D и относительными интенсивностями в процентах. 4. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она,имеющий порошковую рентгенограмму, показанную в таблице. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она,имеющий порошковую рентгенограмму, характеризующуюся расстояниями D Расстояние D12.708 4.323 5.594 5.349 3.590 2. Псевдополиморф формы I, представляющий собой гидрохлорид (-)-цис-2-(2 хлорфенил)-5,7-дигидрокси-8[4R-(3S-гидрокси 1-метил)пиперидинил]-4 Н-1-бензопиран-4-она,имеющий порошковую рентгенограмму, характеризующуюся расстояниями D и относительными интенсивностями. 5. Способ получения формы I по пп.1, 2, 3 или 4, включающий(а) объединение достаточного количества формы II с достаточным количеством соответствующего азеотропного растворителя с образованием азеотропной смеси;(b) азеотропную отгонку азеотропной смеси, достаточную для образования формы I; и(с) необязательное извлечение формы I из продукта дистилляции. 6. Способ по п.5, где растворитель является кетонным растворителем. 7. Способ по п.6, где растворитель является метилэтилкетоном. 8. Способ по п.5, где кристаллическую форму I извлекают фильтрацией формы I. 14 9. Способ по п.5, где температура азеотропной отгонки составляет от около 73 до около 80 С.
МПК / Метки
МПК: A61K 31/435, A61P 35/00, C07D 405/04
Метки: псевдополиморф, цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4r-(3s-гидрокси-1-метил)пиперидинил]-4h-1-бензопиран-4-она
Код ссылки
<a href="https://eas.patents.su/8-5247-psevdopolimorf-cis-2-2-hlorfenil-57-digidroksi-84r-3s-gidroksi-1-metilpiperidinil-4h-1-benzopiran-4-ona.html" rel="bookmark" title="База патентов Евразийского Союза">Псевдополиморф (-)-цис-2-(2-хлорфенил)-5,7-дигидрокси-8[4r-(3s-гидрокси-1-метил)пиперидинил]-4h-1-бензопиран-4-она</a>
Предыдущий патент: Стекло для стеклотары
Следующий патент: Способ отрицательной регуляции активности gdf-8
Случайный патент: Способ получения высокоинфекционного вируса гриппа, стабильного при низких ph












