Способ лечения застойной сердечной недостаточности
Номер патента: 5035
Опубликовано: 28.10.2004
Авторы: Вэйс Дуглас Кирк, Страмм Лоренс Е., Хит Вилльям Фрэнсиз, Джиросек Майкл Р.
Формула / Реферат
1. Способ лечения застойной сердечной недостаточности у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества ингибитора протеинкиназы C формулы Ia или Ib, где в формуле Ia
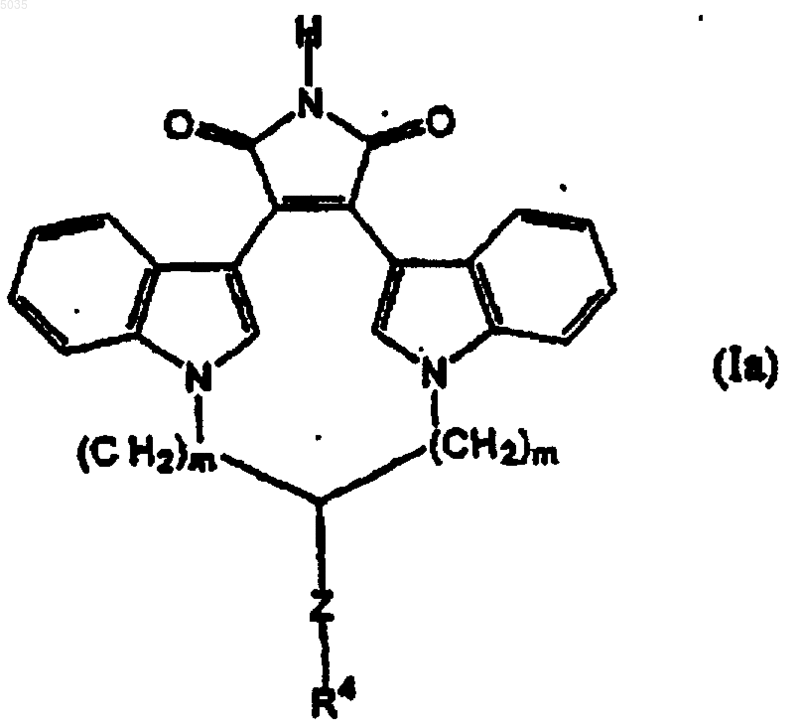
Z представляет -(CH2)p- или -(CH2)p-O-(CH2)p-; R4 представляет гидрокси, -SH, C1-C4алкил, (CH2)mарил, -NH(арил), -N(CH3)(CF3), -NH(CF3) или -NR5R6; R5 представляет водород или C1-C4алкил; R6 представляет водород, C1-C4алкил или бензил; p представляет 0, 1 или 2; и m независимо представляет 2 или 3;
и в формуле Ib
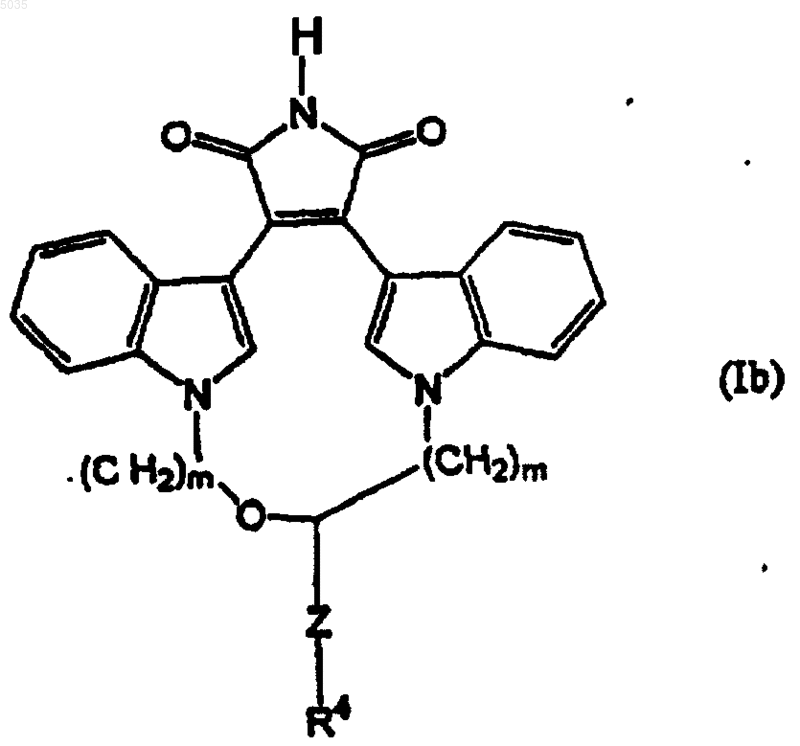
Z представляет -(CH2)p-; R4 представляет -NR5R6, -NH(CF3) или -N(CH3)(CF3); R5 и R6 независимо представляют H или C1-C4алкил; p представляет 0, 1 или 2; и m независимо представляет 2 или 3, или их фармацевтически приемлемой соли, пролекарства или сложного эфира.
2. Способ лечения застойной сердечной недостаточности у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества ингибитора протеинкиназы C (S)-3,4-[N,N'-1,1'-((2''-этокси)-3'''(O)-4'''(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(H)-пиррол-2,5-диона или его кислой соли.
Текст
1 Эта заявка является заявкой в частичное продолжение заявки США 08/643 706, Heathet al., поданной 6 мая 1996 г., которая является выделенной из заявки США 08/413 735, Heathet al., поданной 30 марта 1995 г., которая является заявкой в частичное продолжение заявки США 08/316 973, Heath et al., поданной 3 октября 1994 г., которая является заявкой в частичное продолжение заявки США 08/163 060,Heath et al., поданной 7 декабря 1993 г. Предпосылки к созданию изобретения 1. Область изобретения. Настоящее изобретение в широком смысле относится к способу лечения дисфункции эндотелиальных клеток сосудов, особенно, дисфункции, индуцированной гипергликемией. Настоящее изобретение, в частности, относится к применению конкретного класса селективных ингибиторов изофермента протеинкиназы С (ПКС) для лечения состояний, связанных с атеросклерозом, особенно сердечно-сосудистых заболеваний, связанных с дисфункцией эндотелиальных клеток сосудов. 2. Описание предшествующего уровня. Повреждение или дисфункция эндотелия сосудов является распространенной чертой,присущей многим состояниям, которое предрасполагает организм к ускоренному развитию атеросклеротического сердечно-сосудистого заболевания. Одним из наиболее распространенных факторов, которые вызывают дисфункцию эндотелиальных клеток, является гипергликемия. Наблюдения наводят на мысль о том,что гипергликемия является непосредственно токсичной по отношению к эндотелиальным клеткам. С помощью экспериментальных методик, таких как индуцированная ацетилхолином вазодилатация, множество исследований показало, что дисфункция эндотелиальных клеток является очевидной на модели диабета у экспериментальных животных. Несколько исследований на человеке показали, что сходная дисфункция эндотелия существует и у людей, страдающих диабетом. Несмотря на то, что некоторые типы диабета сопровождаются другими факторами риска сердечно-сосудистых заболеваний, такими как ожирение, гипертензия и дислипидемии, эти сопутствующие факторы риска не являются ответственными за повышенный риск развития клинических проявлений атеросклероза, наблюдаемых у пациентов, страдающих диабетом. Несколько исследовательских групп высказали предположение о том, что наличие микроальбуминурии у пациентов, как страдающих,так и не страдающих диабетом, отражает общее ухудшение функции их эндотелиальных клеток. У пациентов, страдающих диабетом, начало микроальбуминурии связано со значительным повышением риска появления клинических проявлений атеросклеротического макроваскулярного заболевания, который не зависит от других 2 общепринятых сердечно-сосудистых факторов риска. В популяциях людей, не страдающих диабетом, начало микроальбуминурии связано с повышением риска развития макроваскулярного атеросклероза и сердечно-сосудистого заболевания. Так, распространенная дисфункция эндотелиальных клеток, связанная с началом микроальбуминурии, сильно коррелирует с резким возрастанием сердечно-сосудистых заболеваний. Эти открытия предполагают, что нарушение функций эндотелиальных клеток кровеносных сосудов могут представлять из себя этиологический фактор, объясняющий возрастание частоты сердечно-сосудистых заболеваний, наблюдающееся у пациентов как страдающих, так и не страдающих диабетом, если у них имеется микроальбуминурия. Более того, лечение микроальбуминурии было связано со снижением уровня липидов крови и кровяного давления. Дисфункция эндотелиальных клеток кровеносных сосудов, помимо того, что она предрасполагает пациента к хроническим осложнениям, связана также с острым осложнением атеросклероза,таким как ишемическореперфузионное повреждение. Пациенты как страдающие, так и не страдающие диабетом,относятся к группе повышенного риска внезапной смерти вследствие, главным образом, сердечно-сосудистых причин. Пациенты, страдающие диабетом, также имеют повышенный коэффициент смертности после инфаркта миокарда. Повышенный коэффициент смертности после инфаркта миокарда и повышенная частота внезапной смерти у пациентов, страдающих диабетом, может быть связана с более высокой степенью дисфункции эндотелия кровеносных сосудов, вызванного гипергликемией, помимо присущей инфаркту дисфункции эндотелиальных клеток, связанной с ишемическореперфузионным повреждением. Популяции, не имеющие явного диабета,но демонстрирующие более легкие повышения уровней глюкозы, также находятся в группе повышенного риска развития клинических проявлений атеросклероза, например, цереброваскулярных заболеваний, заболеваний периферических сосудов, ишемических состояний миокарда и внезапной смерти. В популяциях с нарушенной толерантностью к глюкозе атеросклеротические заболевания распространены шире. Данные, полученные для нескольких заболеваний, показывают, что предрасположенность к развитию атеросклероза, такая как гипертензия и гиперхолестеринемия, связана с дисфункцией эндотелия, а устранение этих факторов,предрасполагающих к развитию атеросклероза у пациента, улучшает дисфункцию эндотелия. С улучшением функции эндотелиальных клеток,которое наблюдается со снижением гиперхолестеринемии, коррелирует снижение частоты сердечно-сосудистых эпизодов. Так, лечение,улучшающее функцию эндотелиальных клеток 3 кровеносных сосудов, должно снижать риск развития клинических проявлений сердечнососудистых заболеваний. При моделировании ишемии-реперфузии на экспериментальных животных, не страдающих диабетом, наблюдается активация протеинкиназы С, которая участвует в патогенезе повреждения миокарда на модели ишемииреперфузии. На моделях ишемии-реперфузии при отсутствии диабета это повреждение, которое стимулирует патологические процессы, наблюдающиеся при острой ишемии миокарда,наблюдается дисфункция эндотелиальных клеток, которая усугубляет разрушение сердечной мышцы после этого повреждения. Защита от повреждения эндотелиальных клеток на этой модели уменьшает поражение миокарда после повреждения,вызванного ишемиейреперфузией. Допуская, что модель повреждения миокарда при ишемии-реперфузии отражает процессы, наблюдающиеся при острых ишемических состояниях миокарда, таких как инфаркт миокарда, лечение пациентов, не имеющих диабета и страдающих острой ишемией миокарда, с помощью ингибитора ПКС, как ожидается, будет демонстрировать уменьшение повреждения миокарда и осложнений, связанных с этим повреждением (например, аритмий, внезапной смерти, увеличения размеров инфаркта, застойной сердечной недостаточности, повторной ишемии и т.п.). Убиквитарная природа изоферментов протеинкиназы С и их важная роль в физиологии дают толчок к поиску высокоселективных ингибиторов ПКС. Принимая во внимание данные,свидетельствующие о связи определенных изоферментов с болезненными состояниями, можно сделать вывод о том, что ингибирующие соединения, селективные по отношению к одному или двум изоферментам протеинкиназы С по сравнению с другими изоферментами ПКС и другими протеинкиназами, являются превосходными терапевтическими агентами. Такие соединения должны демонстрировать более высокую эффективность и более низкую токсичность благодаря своей специфичности. В настоящее время существуют ограниченные средства лечения дисфункции эндотелиальных клеток и болезненных состояний, связанных с атеросклерозом, особенно связанных с ними сердечно-сосудистых заболеваний. Таким образом, существует потребность внедрения новых терапевтических агентов для лечения болезненных состояний, связанных с атеросклерозом, особенно сердечно-сосудистых заболеваний. Краткое описание существа изобретения 4 Целью настоящего изобретения является создание способа лечения застойной сердечной недостаточности. Цель настоящего изобретения проиллюстрирована одним или более вариантами осуществления, описанными ниже. В варианте осуществления настоящего изобретения обеспечивается способ лечения застойной сердечной недостаточности, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества ингибитора конкретной протеинкиназы С. Настоящее изобретение обеспечивает данную область медицины соединениями, которые являются профилактическими и эффективными при лечении дисфункции эндотелиальных клеток кровеносных сосудов. Следовательно, эти соединения могут применяться для лечения или ингибирования начала болезненных состояний,связанных с атеросклерозом, особенно, сердечно-сосудистых заболеваний, связанных с дисфункцией эндотелиальных клеток кровеносных сосудов. Подробное описание изобретения Открытием настоящего изобретения является тот факт, что применение определенного класса ингибиторов протеинкиназы С уменьшает дисфункцию эндотелиальных клеток сосудов,связанную с атеросклеротическими болезненными состояниями, и, в частности, с дисфункцией эндотелиальных клеток, индуцированной гипергликемией. Следовательно, такие соединения могут применяться в терапевтических целях, для лечения множества атеросклеротических болезненных состояний, особенно сердечно-сосудистых заболеваний, а также профилактически, для ингибирования развития таких заболеваний. Способ настоящего изобретения использует селективные ингибирующие протеинкиназу С соединения формулы Iа: где Z представляет -(СН 2)р- или -(СН 2)р-O(СН 2)р-; R4 представляет гидрокси, -SH, C1-C4 алкил, (СН 2)mарил, -NH(арил), -N(CH3)(CF3),-NH(CF3) или -NR5R6; R5 представляет водород или С 1-С 4 алкил; R5 представляет водород, C1-C4 алкил или бензил; р представляет 0, 1 или 2; и m независимо представляет 2 или 3,или их фармацевтически приемлемые соли, пролекарства или сложные эфиры. Наиболее предпочтительными соединениями являются соединения формулы Iа, в которых Z представ 5 ляет -СН 2; a R4 представляет -NH2, -NH(CF3) или-NR5R6; -NH(CF3) или -N(СН 3)(CF3), R5 и R6 независимо представляют Н или C1-C4 алкил; и р представляет 0, 1 или 2; и m независимо представляет 2 или 3,или их фармацевтически приемлемые соли, пролекарства или сложные эфиры. Наиболее предпочтительными соединениями являются соединения формулы (Ib), в которых р равно 1, aR5 и R6 представляют метил. Эти соединения и способы их получения известны и описаны Heath et al., ЕР публикация 0657458 А 1, которая включена в настоящий документ в качестве ссылки. Поскольку соединения формулы Iа и Ib содержат основную часть, они могут существовать также в форме фармацевтически приемлемых солей присоединения кислот. Кислоты,которые широко применяются для получения таких солей, включают неорганические кислоты, такие как хлористо-водородная, бромистоводородная, иодисто-водородная, серная и фосфорная кислота, а также органические соли,такие как паратолуолсульфоновая, метансульфоновая, щавелевая, парабромфенилсульфоновая, угольная, янтарная, лимонная, бензойная,уксусная кислота и родственные им неорганические и органические кислоты. Такие фармацевтически приемлемые соли включают, следовательно, сульфат, пиросульфат, бисульфат, сульфит, бисульфит, фосфат, однозамещенный фосфат, двузамещенный фосфат, метафосфат, пирофосфат, хлорид, бромид, иодид, ацетат, пропионат, деканоат, каприлат, акрилат, формиат,изобутират, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберат, себакат, фумарат, малеат, 2-бутин-1,4-диоат, 3-гексин-2,5-диоат,бензоат, хлорбензоат, гидроксибензоат, метоксибензоат, фталат, ксилолсульфонат, фенилацетат, фенилпропионат, фенилбутират, цитрат,лактат, гиппурат, -гидроксибутират, гликолят,малеат, тартрат, метансульфонат, пропансульфонат, нафталин-1-сульфонат, нафталин-2 сульфонат, манделат и т.п. Помимо фармацевтически приемлемых солей могут существовать также и другие соли. Они могут служить промежуточными соединениями при очистке этих соединений, при получении других солей или при идентификации и изучении свойств этих соединений или промежуточных соединений. 6 Фармацевтически приемлемые соли соединений формулы Iа и Ib могут существовать также в форме различных сольватов, таких как сольваты с водой, метанолом, этанолом, диметилформамидом, этилацетатом и т.п. Могут изготавливаться также смеси таких сольватов. Источник такого сольвата может быть из растворителя кристаллизации, свойственный растворителю получения или кристаллизации, или побочный по отношению к такому растворителю. Установлено, что могут существовать различные стереоизомерные формы соединений формул Iа и Ib. Эти соединения обычно получают в виде рацематов и могут использоваться в качестве таковых. При необходимости, можно выделять или синтезировать оба отдельных энантиомера с помощью обычных методик. Такие рацематы и отдельные энантиомеры, а также их смеси образуют части соединений, используемых в способах настоящего изобретения. Соединения, используемые в настоящем изобретении, включают также фармацевтически приемлемые пролекарства соединений формулIа и Ib. Пролекарство представляет собой лекарство, которое было химически модифицировано и может быть биологически неактивным по отношению к месту своего действия, но которое может распадаться или модифицироваться посредством одного или более ферментативных процессов или других in vivo процессов до родительской биологически активной формы. Это пролекарство, вполне вероятно, может иметь отличный от родительской формы фармакокинетический профиль, который обеспечивает более легкое всасывание через эпителий слизистых оболочек, более хорошее образование соли или лучшую растворимость и/или более высокую системную стабильность (например, увеличение биологического полупериода существования в плазме). В типичном случае такие химические модификации включают следующее: 1) сложноэфирные или амидные производные, которые могут расщепляться эстеразами или липазами; 2) пептиды, которые могут распознаваться специфичными или неспецифичными протеазами; или 3) производные, которые накапливаются в месте действия посредством мембранной селекции пролекарственной формы или модифицированной пролекарственной формы; или любая комбинация от 1 до 3, см. выше. Стандартные методики отбора и изготовления подходящих пролекарственных производных описаны, например, Н. Bundgaard, Design of Prodrugs,(1985). Синтез различных бис-индол-Н-малеимидных производных описан Davis et al. в патенте США 5 057 614, а синтез предпочтительных для применения по настоящему изобретениюAl, включенных в настоящий документ в качестве ссылок. Один особенно предпочтительный для применения по настоящему изобретению ингибитор протеинкиназы С является соединением,описанным в примере 5s, S)-3,4-[N,N'-l,l'-2 этокси)-3(О)-4(N,N-диметиламино)бутан)бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-дионгидрохлорид), вышеупомянутой публикации ЕР 0 657 458 А 1. Это соединение является эффективным ингибитором протеинкиназы С. Оно является селективным в отношении протеинкиназы С по сравнению с другими киназами, также высокоселективным в отношении изофермента,т.е. оно селективно в отношении изоферментов бета-1 и бета-2. Было показано, что это соединение нормализует дисфункцию эндотелиальных клеток на модели диабета у экспериментальных животных в дозах, прогнозировавшихся в отношении ингибирования ПКС-. Эти данные представлены в публикации Hidehiro etal., Science, том 272, стр. 728-731, 1996, и включены в настоящее описание в качестве ссылки. У грызунов с диабетом, получавших стрептозотоцин и аллоксан, это соединение нормализовало изменения кровотока в сетчатке и активности сосудистой Na/K-АТФазы, вызванные диабетом. Изменения сетчаточного кровотока отражают патологию регуляции кровотока эндотелиальными клетками, вызванную гипергликемией. Снижение активностиNa/K-АТФазы является показателем дисфункции эндотелиальных клеток (Gupta, et al., J. Clin.Invest., 90:727-732 (1991. Способность этого соединения нормализовать эти отклонения, вызванные диабетом, демонстрирует его защитный эффект в отношении эндотелия при гипергликемических состояниях. Помимо этого, это соединение блокировало микроальбуминурию,маркер широко распространившейся дисфункции эндотелиальных клеток. Так, у грызунов с диабетом это соединение снижало опосредованную глюкозой токсичность в отношении эндотелиальных клеток и ингибировало дисфункцию эндотелиальных клеток, связанную с развитием атеросклеротической макроваскулярной болезни. Дисфункция эндотелиальных клеток кровеносных сосудов в большой степени связана с атеросклеротическим сердечно-сосудистым заболеванием у пациентов с диабетом и без диабета. Соединения настоящего изобретения, будучи активными в отношении нормализации нарушений функций эндотелиальных клеток кровеносных сосудов, являются особенно полезными для лечения сердечно-сосудистых заболеваний, например, стабильной стенокардии,нестабильной стенокардии, вариантной стенокардии, сердечно-сосудистой ишемии, внезапной смерти и инфаркта миокарда, особенно сер 005035 8 дечно-сосудистых заболеваний, связанных с гипергликемией. Нарушение функций эндотелиальных клеток кровеносных сосудов, помимо того, что оно предрасполагает пациента к хроническим осложнениям атеросклероза, связано также с острым осложнением атеросклероза,таким как ишемическо-реперфузионное повреждение (Ku, Science, 218:576-578 (1982); Van(1987); Mehta, et al., Cir. Res., 64:43-54 (1989. Эти соединения, полезные для способа настоящего изобретения, являются терапевтически эффективными в отношении снижения дисфункции эндотелиальных клеток, которая наблюдается после ишемического эпизода, и в отношении уменьшения клинических последствий, связанных с этой патологией, например,внезапной смерти и более высокого коэффициента смертности после инфаркта миокарда. Соединения настоящего изобретения могут применяться также для снижения риска сердечно-сосудистых заболеваний у пациентов с гипергликемией. Нормальный диапазон уровней глюкозы натощак составляет от 75 до 105 мг/дл(4,2 - 5,8 ммоль/л) и до 140 мг/дл (до 7,8 ммоль/л) через два часа после приема пищи. Таким образом, эти соединения могут применяться профилактически для лечения пациентов,у которых уровни глюкозы находятся около верхней границы нормы, а также пациентов с нарушенной толерантностью к глюкозе, гипертензией, гиперхолестеринемией и диабетом. Термин "лечение", используемый в настоящем документе, описывает уход и лечение пациента с целью борьбы с заболеванием, состоянием или нарушением и включает введение соединения настоящего изобретения для предупреждения появления симптомов или осложнений (профилактическое использование), облегчения этих симптомов или осложнений или устранения заболевания, состояния или нарушения. Термин "селективный в отношении изофермента" означает ингибирование изофермента протеинкиназы С бета-1 или бета-2, предпочтительное по сравнению с другими изоферментами протеинкиназы С, альфа, гамма, дельта,эпсилон, зета и эта. В общем, соединения, пригодные для настоящего изобретения, демонстрируют минимум восьмикратную разницу(предпочтительно, десятикратную) между дозировками, требующимися для ингибирования изофермента ПКС бета-1 или бета-2, и дозировками, требующимися для такого же ингибирования изофермента протеинкиназы С альфа, по измерениям анализов ПКС. Эти соединения демонстрируют эту разницу на протяжении целого диапазона ингибирования, а в качестве примеров приводятся величины IС 50, т.е. 50% ингибирование. Таким образом, селективные в отношении изофермента соединения ингибируют изоферменты протеинкиназы С бета-1 и бета-2 при значительно более низких концентрациях и 9 более низкой токсичности, благодаря минимальному ингибированию других изоферментов ПКС. Для опытного специалиста будет очевидно, что терапевтически эффективное количество, например, количество, ингибирующее дисфункцию эндотелиальных клеток, ингибитора протеинкиназы С по настоящему изобретению представляет собой количество, достаточное для ингибирования дисфункции эндотелиальных клеток или для ингибирования развития сердечно-сосудистого заболевания, и что это количество может варьировать, inter alia, в зависимости от размеров участка поврежденной ткани, концентрации соединения в фармацевтической композиции и веса тела пациента. В целом, количество ингибитора протеинкиназы С,которое необходимо ввести в качестве терапевтического агента для лечения сердечнососудистого заболевания и для ингибирования начала сосудистого заболевания, как обсуждалось выше, будет определяться лечащим врачом конкретно для каждого случая. В качестве руководства при определении соответствующей дозы следует принимать во внимание распространенность дисфункции эндотелиальных клеток,вес тела и возраст пациента. В целом, подходящей дозой является такая доза, которая обеспечивает концентрацию ингибитора протеинкиназы С в участке, подвергаемом лечению, в пределах от 0,5 нМ до 200 мкМ,чаще от 0,5 нМ до 200 нМ. Ожидается, что концентрации в сыворотке в пределах от 0,5 нМ до 10 нМ будут достаточны для большинства случаев. Чтобы получить эти терапевтические концентрации, пациенту, нуждающемуся в таком лечении, по всей видимости, надо будет вводить дозы приблизительно от 0,001 мг/кг веса тела в день до 50,0 мг/кг веса тела в день. Обычно требуется не более чем около 10,0 мг/кг веса тела в день ингибитора протеинкиназы С. Как отмечалось выше, вышеупомянутые количества могут изменяться в зависимости от конкретного случая. Для опытного специалиста будет также очевидно, что профилактически эффективное количество ингибитора протеинкиназы С по настоящему изобретению представляет собой количество, достаточное для ингибирования или снижения риска появления сердечно-сосудистого заболевания. Это количество варьирует в зависимости от степени воздействия факторов риска. В целом, количество ингибитора протеинкиназы С, которое необходимо ввести в качестве профилактического агента для предупреждения сердечно-сосудистого заболевания, будет определяться лечащим врачом конкретно для каждого случая. В качестве руководства при определении соответствующей дозы следует брать за основу дозу ингибиторов ПКС при их использовании в качестве терапевтических 10 агентов. Обычно она будет находиться в пределах от 50 до 150% от обсуждавшейся выше терапевтической дозировки. Из соединений формул Iа и Ib, перед введением изготавливаются готовые лекарственные формы. Подходящие фармацевтические готовые формы изготавливаются известными способами с использованием хорошо известных и доступных ингредиентов. При изготовлении композиций, подходящих для применения в способе наcтоящегo изобретения, активный ингредиент обычно будет смешиваться с носителем или разбавляться носителем, или помещаться внутрь носителя, который может быть в форме капсулы, саше, бумажного пакетика или другого контейнера. Когда носитель служит разбавителем,он может быть твердым, полутвердым и жидким материалом, который действует как носитель,наполнитель или среда для активного ингредиента. Так, композиции могут быть в форме таблеток, пилюль, порошков, пастилок, саше, облаток. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения застойной сердечной недостаточности у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества ингибитора протеинкиназы С формулы Iа или Ib, где в формуле IаR4 представляет гидрокси, -SH, C1-C4 алкил,(СН 2)mарил, -NН(арил), -N(СН 3)(CF3), -NH(CF3) или -NR5R6; R5 представляет водород или С 1-С 4 алкил; R6 представляет водород, С 1-С 4 алкил или бензил; р представляет 0, 1 или 2; и m независимо представляет 2 или 3; и в формуле Ib-NR R6, -NH(CF3) или -N(СН 3)(CF3); R5 и R6 независимо представляют Н или C1-C4 алкил; р представляет 0, 1 или 2; и m независимо представляет 2 или 3, или их фармацевтически приемлемой соли, пролекарства или сложного эфира. 5 2. Способ лечения застойной сердечной недостаточности у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффектив 12 ного количества ингибитора протеинкиназы С(S)-3,4-[N,N'-1,1'-2-этокси)-3(О)-4(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)пиррол-2,5-диона или его кислой соли.
МПК / Метки
МПК: A61K 31/404, C07D 487/22, A61P 9/04
Метки: лечения, сердечной, застойной, недостаточности, способ
Код ссылки
<a href="https://eas.patents.su/7-5035-sposob-lecheniya-zastojjnojj-serdechnojj-nedostatochnosti.html" rel="bookmark" title="База патентов Евразийского Союза">Способ лечения застойной сердечной недостаточности</a>
Предыдущий патент: Производные тиооксиндола
Следующий патент: Способ количественного анализа пробы минерала, устройство и флюс для осуществления такого способа
Случайный патент: Способы быстрого доступа к сети интернет посредством "установления соединения по требованию" с помощью аналоговых модемов, игнорируя долгие модемные согласования











