Новый фармацевтический препарат
Номер патента: 3031
Опубликовано: 26.12.2002
Авторы: Сасс Майкл Джон, Блэклер Пол Дэвид Джеймс, Мур Стефен, Жиль Робер Гордон
Формула / Реферат
1. Полиморфная форма соли 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона и малеиновой кислоты (соединение 1), отличающаяся тем, что она имеет:
(i) инфракрасный спектр, содержащий пики при 1752, 1546, 1154, 621 и 602 см-1; и/или
(ii) спектр комбинационного рассеяния, содержащий пики при 1751, 1243, и 602 см-1; и/или
(iii) спектр ядерного магнитного резонанса твердого тела, содержащий пики при 111,9; 114,8; 119,6; 129,2; 134,0; 138,0; 144,7; 153,2; 157,1; 170,7; 172,0 и 175,0 м.д.; и/или
(iv) порошковую рентгенограмму (ПР), которая показывает вычисленные параметры кристаллической решетки 6,46; 5,39; 4,83; 4,68; 3,71; 3,63; 3,58 и 3,48 ангстрем.
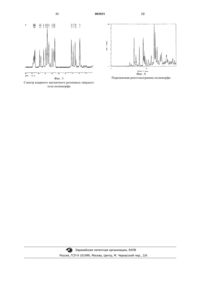
2. Полиморф по п.1, который имеет инфракрасный спектр, по существу, в соответствии с фиг. 1.
3. Полиморф по п.1 или 2, который имеет спектр комбинационного рассеяния, по существу, в соответствии с фиг. 2.
4. Полиморф по любому из пп.1-3, который имеет спектр ядерного магнитного резонанса твердого тела, по существу, в соответствии с фиг. 3 и/или табл. 1.
5. Полиморф по любому из пп.1-4, который имеет порошковую рентгенограмму (ПР), по существу, в соответствии с фиг. 4 и/или табл. 2.
6. Полиморф по любому из пп.1-5 в выделенной форме.
7. Полиморф по любому из пп.1-6 в чистой форме.
8. Полиморф по любому из пп.1-7 в кристаллической форме.
9. Способ получения полиморфа по п.1, отличающийся тем, что раствор соединения (I) в денатурированном этаноле при повышенной температуре охлаждают так, чтобы обеспечить кристаллизацию полиморфа, после которой полиморф выделяют из денатурированного этанола.
10. Фармацевтическая композиция, содержащая эффективное, нетоксичное количество полиморфа по п.1 и его фармацевтически приемлемый носитель.
11. Полиморф по п.1 для использования в качестве активного терапевтического вещества.
12. Полиморф по п.1 для использования при лечении и/или профилактике сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений.
13. Применение полиморфа для изготовления лекарственного препарата для лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений.
14. Способ лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений у человека или других млекопитающих, который включает введение эффективного, нетоксичного количества полиморфа человеку или другому млекопитающему при необходимости.
Текст
1 Настоящее изобретение относится к новому фармацевтическому препарату, способу получения фармацевтического препарата и применению фармацевтического препарата в медицине. Международная заявка на патент, номер публикации WO 94/05659 описывает некоторые производные тиазолидиндиона, имеющие гипогликемическую и гиполипидемическую активность, включая соль 5-[4-[2-(N-метил-N-(2 пиридил)амино)этокси]бензил]тиазолидин-2,4 диона и малеиновой кислоты (в дальнейшем также называемую как соединение (I. Международные заявки на патент, номера публикаций WO 99/31093, WO 99/31094 и WO 99/31095, каждая, описывают различные гидраты соединения (I). Было обнаружено, что соединение (I) существует в новой полиморфной форме, которая является особенно подходящей для масштабного производства и манипуляций с ним. Новую форму можно получить эффективным, экономичным и воспроизводимым способом, особенно удобным для крупномасштабного производства. Новая полиморфная форма (полиморф) также имеет полезные фармацевтические свойства и, в частности, показано, что она полезна для лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и некоторых его осложнений. Соответственно настоящее изобретение предлагает полиморфную форму соли 5-[4-[2(N-метил-N-(2-пиридил)амино)этокси]бензил] тиазолидин-2,4-диона и малеиновой кислоты,отличающуюся тем, что она:(i) имеет инфракрасный спектр, содержащий пики при 1752, 1546, 1154, 621 и 602 см-1; и/или(ii) имеет спектр комбинационного рассеяния, содержащий пики при 1751, 1243 и 602 см-1; и/или(iii) имеет спектр ядерного магнитного резонанса твердого тела, содержащий пики при 111,9; 114,8; 119,6; 129,2; 134,0; 138,0; 144,7; 153,2; 157,1; 170,7; 172,0 и 175,0 м.д. (ррт); и/или(ПР), которая показывает вычисленные параметры кристаллической решетки 6,46; 5,39; 4,83; 4,68; 3,71; 3,63; 3,58 и 3,48 . В одном предпочтительном аспекте, полиморф имеет инфракрасный спектр, по существу,в соответствии с фиг. 1. В одном предпочтительном аспекте полиморф имеет спектр комбинационного рассеяния,по существу, в соответствии с фиг. 2. В одном предпочтительном аспекте полиморф имеет спектр ядерного магнитного резонанса твердого тела, по существу, в соответствии с фиг. 3 и/или табл. 1. 2 В одном предпочтительном аспекте полиморф имеет порошковую рентгенограмму (ПР),по существу, в соответствии с фиг. 4 и/или табл. 2. Настоящее изобретение охватывает полиморф, выделенный в чистой форме или смешанный с другими веществами, например, с известными формами соединения (I) или любым другим веществом. Таким образом, в одном аспекте предлагается полиморф в выделенной форме. В дальнейшем аспекте предлагается полиморф в чистой форме. В еще одном дальнейшем аспекте предлагается полиморф в кристаллической форме. Настоящее изобретение также предлагает способ получения полиморфа, отличающийся тем, что раствор соединения (I) в денатурированном этаноле при повышенной температуре предпочтительно в диапазоне от 65 до 70 С,например 67,5 С, охлаждают предпочтительно до температуры в диапазоне от 20 до 25 С так,чтобы обеспечить кристаллизацию полиморфа. Предпочтительно раствор фильтруют перед охлаждением. В вышеописанном способе в раствор можно ввести затравку полиморфа, чтобы вызвать кристаллизацию, но это не является существенным. Затем полиморф выделяют из денатурированного этанола. Раствор соединения (I) в денатурированном этаноле удобно получают, растворяя соединение (I) в требуемом количестве денатурированного этанола при повышенной температуре, например при 60 или 70 С. Удобно, когда полиморф выделяют из денатурированного этанола фильтрованием и последующей сушкой. В дальнейшем аспекте изобретение предлагает способ превращения полиморфа в соединение (I), где в раствор полиморфа в подходящем растворителе, таком как ацетон или этанол,вносят затравку соединения (I); предпочтительно реакцию проводят в инертной атмосфере,например в азоте. Как правило, раствор полиморфа получают, растворяя полиморф при повышенной температуре в растворителе, таком как ацетон или этанол. Соединение (I) получают по известным процедурам, таким как процедуры, описанные вWO 94/05659. Описание WO 94/05659 включается здесь ссылкой. Чтобы избежать неясности, используемый здесь термин соединение (I) относится к форме 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона, соли малеиновой кислоты, как описывается и характеризуется в международной заявке на патент, номер публикации WO 94/05659. Используемый здесь термин денатурированный этанол означает этанол, содержащий небольшие количества метанола, обычно вплоть до 5% об./об. метанола, такие как от 0,9 до 5% 3 об./об. метанола, например этанол, содержащий 4% об./об. метанола. Используемый здесь термин профилактика состояний, связанных с сахарным диабетом,включает лечение состояний, таких как резистентность к инсулину, пониженная толерантность к глюкозе, гиперинсулинемия и обусловленный беременностью диабет. Сахарный диабет предпочтительно означает тип II сахарного диабета. Связанные с диабетом состояния включают гипергликемию, резистентность к инсулину и ожирение. Далее связанные с диабетом состояния включают гипертензию, сердечнососудистые заболевания, особенно атеросклероз, некоторые расстройства питания, в частности регуляцию аппетита и приема пищи у пациентов, страдающих от расстройств, связанных с недоеданием, таких как анорексия нервоза, и расстройств, связанных с перееданием, таких как ожирение и анорексия булимия. Дополнительные состояния, связанные с диабетом,включают синдром поликистоза яичников и индуцированную стероидами резистентность к инсулину. Рассматриваемые здесь осложнения, связанные с сахарным диабетом, включают почечные заболевания, особенно почечные заболевания, связанные с развитием типа II диабета,включающие диабетическую нефропатию, гломерулонефрит, гломерулярный склероз, почечный синдром, гипертензивный нефросклероз и последнюю стадию почечной болезни. Как указывалось выше, соединение по изобретению имеет полезные терапевтические свойства. Настоящее изобретение соответственно предлагает полиморф для применения в качестве активного терапевтического вещества. Более конкретно, настоящее изобретение предлагает полиморф для применения при лечении и/или профилактике сахарного диабета,состояний, связанных с сахарным диабетом, и его некоторых осложнений. Полиморф можно вводить как таковой или предпочтительно в виде фармацевтической композиции, также содержащей фармацевтически приемлемый носитель. Рецептура полиморфа и его дозировки обычно являются такими,как описывается для соединения (I) в международной заявке на патент, номер публикации WO 94/05659 или WO 98/55122. Соответственно настоящее изобретение также предлагает фармацевтическую композицию, содержащую полиморф и его фармацевтически приемлемый носитель. Полиморф обычно вводят в виде единичной дозированной формы. Активное соединение можно вводить любым подходящим способом, но обычно пероральным или парентеральным способом. Для такого использования соединение обычно будет применяться в форме фармацевтической компо 003031 4 зиции вместе с фармацевтическим носителем,разбавителем и/или эксципиентом, хотя точная форма композиции естественно будет зависеть от способа введения. Композиции получают смешиванием и соответственно приспосабливают для перорального, парентерального или местного введения, и как таковые они могут быть в форме таблеток,капсул, пероральных жидких препаратов, порошков, гранул, лепешек, пастилок, восстанавливаемых порошков, растворов или суспензий для инъекций и вливаний, суппозиториев и приспособлений для чрезкожного введения. Композиции, вводимые перорально, являются предпочтительными, в частности пероральные композиции с приданной формой, поскольку они более удобны для общего использования. Таблетки и капсулы для перорального введения обычно представлены в унифицированной дозе и содержат традиционные эксципиенты, такие как связующие вещества, наполнители, разбавители, вещества, способствующие изготовлению таблетки, смазывающие вещества, дезинтегранты, красители, корригенты и смачивающие средства. Таблетки могут быть покрыты в соответствии с хорошо известными в данной области методами. Подходящие для использования наполнители включают целлюлозу, маннит, лактозу и другие сходные средства. Подходящие дезинтегранты, включают крахмал, поливинилпирролидон и производные крахмала, такие как натрийгликолят крахмала. Подходящие смазывающие вещества включают, например, стеарат магния. Подходящие фармацевтически приемлемые смачивающие средства включают лаурилсульфат натрия. Твердые пероральные композиции можно приготовить традиционными методами смешивания, наполнения, таблетирования или аналогичными. Повторяющиеся операции смешивания можно использовать, чтобы распределить активное вещество по всему объему таких композиций, применяющих большие количества наполнителей. Такие операции, конечно, являются традиционными в данной области. Пероральные жидкие препараты могут быть в форме, например, водных или масляных суспензий, растворов, эмульсий, сиропов или эликсиров, или могут быть представлены в виде сухих продуктов для восстановления водой или другим подходящим растворителем перед использованием. Такие жидкие препараты могут содержать обычные добавки, такие как суспендирующие средства, например, сорбит, сироп,метилцеллюлозу, желатин, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гель стеарата алюминия или гидрогенизированные пищевые жиры, эмульгирующие средства, например, лецитин, моноолеат сорбита или аравийскую камедь; неводные растворители (которые могут включать пищевые масла), например миндаль 5 ное масло, фракционированное кокосовое масло, маслянистые сложные эфиры, такие как сложные эфиры глицерина, пропиленгликоля или этилового спирта; консерванты, например метил- или пропил-п-гидроксибензоат или сорбиновую кислоту, и если желательно традиционные корригенты или красители. Для парентерального введения готовят жидкие единичные дозированные формы, содержащие соединение по настоящему изобретению и стерильный растворитель. Соединение в зависимости от растворителя и концентрации может быть либо суспендированным, либо растворенным. Парентеральные растворы обычно готовят, растворяя активное соединение в растворителе и стерилизуя фильтрованием, перед заполнением в подходящий сосуд или ампулу и запаиванием. Благоприятным является, когда в растворителе также растворяют адъюванты,такие как местные обезболивающие средства,консерванты и буферные вещества. Для увеличения стабильности, композицию можно заморозить после заполнения в сосуд и воду удалить под вакуумом. Парентеральные суспензии готовят, по существу, таким же образом за исключением того, что активное соединение суспендируют в растворителе вместо растворения и стерилизуют обработкой этиленоксидом перед суспендированием в стерильном растворителе. Полезно,когда в композицию включают поверхностноактивное вещество или смачивающий реагент,чтобы содействовать однородному распределению активного соединения. Кроме того, такие композиции могут содержать дополнительные активные агенты, такие как антигипертензивные средства и мочегонные средства. Кроме того, полиморф можно использовать в комбинации с другими антидиабетическими веществами, как например со средствами,усиливающими секрецию инсулина, например,сульфонилмочевиной, бигаунидами, такими как метформин, ингибиторами альфа-глюкозидазы,такими как акарбоза, бэта-агонистами, и инсулином, такими как описанные в WO 98/57649,WO 98/57634, WO 98/57635 или WO 98/57636. Другие антидиабетические вещества, их количества и способы введения являются такими,как описывается в вышеуказанных публикациях. Рецептура полиморфа и его дозировки в указанных комбинациях обычно являются такими,как описывается для соединения (I) в вышеуказанных публикациях. Как является обычной практикой, композиции будут как правило сопровождаться письменными или напечатанными указаниями по использованию при проводимом медицинском лечении. Использованный здесь термин фармацевтически приемлемый охватывает соединения,композиции и ингредиенты для использования как при лечении людей, так и в ветеринарии: 6 например, термин фармацевтически приемлемая соль охватывает ветеринарно-приемлемую соль. Настоящее изобретение далее предлагает способ лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений у человека или других млекопитающих, который включает введение эффективного, нетоксичного количества полиморфа человеку или другому млекопитающему при необходимости этого. Удобно, что активный ингредиент можно вводить в виде фармацевтической композиции,определенной выше, и это представляет особый аспект настоящего изобретения. При лечении и/или профилактике сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений полиморф можно принимать в дозах, таких как вышеописанные дозы. Аналогичные режимы дозировок подходят для лечения и/или профилактики других млекопитающих, отличных от человека. В дальнейшем аспекте настоящее изобретение предлагает применение полиморфа для изготовления медицинского препарата для лечения и/или профилактики сахарного диабета,состояний, связанных с сахарным диабетом, и его некоторых осложнений. Никакие вредные токсикологические эффекты при вышеуказанном лечении для соединений по изобретению не обнаружены. Следующие примеры иллюстрируют изобретение, но они никоим образом не ограничивают его. Пример 1. Получение полиморфа. Смесь малеиновой кислоты (2,10 г) и 5-[4[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона (6,0 г) нагревают до 70 С в денатурированном этаноле (60 мл, 5% об./об. метанола) пока не будет получено полное растворение. Полученный в результате раствор фильтруют, вновь нагревают до 67,5 С и затем охлаждают до 20-25 С. Полученный в результате кристаллический продукт отфильтровывают, промывают денатурированным этанолом (10 мл) и сушат при 50 С в вакууме, получая полиморф (6,61 г, 83%). Пример 2. Превращение полиморфа в соединение (I). Полиморф (10,0 г) добавляют к денатурированному этанолу (90 мл) в атмосфере азота. Полученную в результате смесь перемешивают,нагревают до 68 С и выдерживают при этой температуре в течение 30 мин. Проводят горячее фильтрование раствора в предварительно нагретый сосуд (56 С) и фильтр промывают горячим денатурированным этанолом (10 мл). Температуру фильтрата доводят до 60 С и затем охлаждают при перемешивании. При 55 С в раствор вводят затравку соединения (I) (0,4 г) и при перемешивании продолжают охлаждение. 7 Полученную в результате суспензию перемешивают при температуре окружающей среды в течение 1 ч и твердое вещество отделяют фильтрованием, промывают денатурированным этанолом и сушат при 50 С в вакууме, получая 8,4 г (84%) соединения (I). Пример 3. Превращение полиморфа в соединение (I). Полиморф (5,0 г) добавляют к ацетону(170 мл) и смесь перемешивают и нагревают до температуры образования флегмы. После полного растворения раствор нагревают при температуре образования флегмы в течение 30 мин,затем фильтруют. Отфильтрованный раствор концентрируют дистилляцией при атмосферном давлении (собирают 120 мл дистиллята). Оставшийся раствор перемешивают и охлаждают со скоростью примерно 1 С/мин и при 50 С вводят затравку соединения (I) (0,2 г). Продолжают охлаждение со скоростью 1 С/мин, и когда температура суспензии достигнет 20 С, перемешивание продолжают в течение 1 ч. Твердое вещество отделяют фильтрованием, промывают ацетоном и сушат при 50 С в вакууме, получая 4,2 г (84%) соединения (I). Характеризующие данные Для полиморфа были получены следующие характеризующие данные. А. Инфракрасный спектр. Спектр инфракрасного поглощения дисперсии полиморфа в минеральном масле получают, используя Nicolet 710 FT-IR спектрометр при разрешении 2 см-1. Данные преобразуют в цифровую форму с интервалами 1 см-1. Полученный спектр показан на фиг. 1. Положения пиков следующие: 1752, 1709, 1642, 1613, 1576,1546, 1514, 1412, 1359, 1329, 1317, 1291, 1261,1242, 1220, 1212, 1204, 1182, 1171, 1154, 1126,1112, 1097, 1075, 1056, 1032, 1016, 966, 937, 918,906, 861, 842, 821, 809, 792, 762, 743, 715, 665,656, 650, 621, 602, 560, 541, 524 и 507 см-1. В. Комбинационное рассеивание. Спектр комбинационного рассеивания записывают в стеклянном сосуде, используя спектрометр Perkin Elmer 2000R с разрешением 4 см-1 и он показан на фиг. 2 (ось Х показывает интенсивность, ось Y показывает смещение частоты при комбинационном рассеянии света см-1,1800-200 см-1). Возбуждение получают, используя лазер Nd:YAG (1064 нм) с выходной мощностью 400 мВт. Положения пиков следующие: 1751, 1683, 1614, 1586, 1547, 1468, 1449, 1382,1344, 1317, 1243, 1211, 1181, 1150, 1076, 1016,991, 918, 841, 825, 773, 742, 652, 637, 619, 602,512, 470, 428, 406, 350 и 325 см-1. С. ЯМР. Спектр 13 С ЯМР CP-MAS 90,56 МГц полиморфа показан на фиг. 3. Химические сдвиги сведены в табл. 1. Данные записывают при температуре окружающей среды и частоте вращения 10 кГц на спектрометре Bruker AMX360 с поперечной поляризацией 1,6 мс и временем 8 повторения 15 с. Химические сдвиги определяют по сигналу карбоксила тестового образца глицина при 176,4 м.д. (ррт) в качестве внешнего стандарта относительно тетраметилсилана, и считается, что их точность находится в пределах 0,5 м.д. Таблица 1 Химические сдвиги 13 С полиморфа Химический сдвиг (м.д.) 38,0 49,4 51,9 57,6D. Порошковая рентгенограмма (ПР). Порошковая рентгенограмма (ПР) полиморфа показана ниже на фиг. 4, и краткое описание углов ПР и характеристики вычисленных параметров кристаллической решетки полиморфа даются в табл. 2. Данные получают на диффрактометре Bruker D8 Advance с тэта/тэта геометрией, сконфигурированным с Сu анодом, первичной и вторичной щелями Соллера, вторичным монохроматором и сцинцилляционным детектором. Используют следующие условия получения данных: Трубчатый анод Сu Напряжение генератора 40 кВ Ток генератора 40 мА Начальный угол 2,02 Конечный угол 35,02 Размер шага 0,022 Время на шаг 2,5 с Таблица 2 Углы порошковой рентгенограммы и характеристика вычисленных параметров кристаллической решетки полиморфа Угол дифракции (2) 9,2 11,6 12,3 13,7 14,0 14,7 14,9 15,3 16,4 18,4 18,7 19,0 19,3 20,0 21,0 21,9 22,5 23,3 24,0 24,5 24,9 25,6 Параметр кристаллической решетки (Ангстрем) 9,63 7,65 7,17 6,46 6,32 6,03 5,95 5,77 5,39 4,83 4,74 4,68 4,59 4,44 4,22 4,07 3,94 3,81 3,71 3,63 3,58 3,48 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Полиморфная форма соли 5-[4-[2-(Nметил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона и малеиновой кислоты (соединение I), отличающаяся тем, что она имеет:(i) инфракрасный спектр, содержащий пики при 1752, 1546, 1154, 621 и 602 см-1; и/или(iii) спектр ядерного магнитного резонанса твердого тела, содержащий пики при 111,9; 114,8; 119,6; 129,2; 134,0; 138,0; 144,7; 153,2; 157,1; 170,7; 172,0 и 175,0 м.д.; и/или(iv) порошковую рентгенограмму (ПР), которая показывает вычисленные параметры кристаллической решетки 6,46; 5,39; 4,83; 4,68; 3,71; 3,63; 3,58 и 3,48 ангстрем. 2. Полиморф по п.1, который имеет инфракрасный спектр, по существу, в соответствии с фиг. 1. 3. Полиморф по п.1 или 2, который имеет спектр комбинационного рассеяния, по существу, в соответствии с фиг. 2. 4. Полиморф по любому из пп.1-3, который имеет спектр ядерного магнитного резонан Фиг. 1 Инфракрасный спектр полиморфа 10 са твердого тела, по существу, в соответствии с фиг. 3 и/или табл. 1. 5. Полиморф по любому из пп.1-4, который имеет порошковую рентгенограмму (ПР),по существу, в соответствии с фиг. 4 и/или табл. 2. 6. Полиморф по любому из пп.1-5 в выделенной форме. 7. Полиморф по любому из пп.1-6 в чистой форме. 8. Полиморф по любому из пп.1-7 в кристаллической форме. 9. Способ получения полиморфа по п.1,отличающийся тем, что раствор соединения (I) в денатурированном этаноле при повышенной температуре охлаждают так, чтобы обеспечить кристаллизацию полиморфа, после которой полиморф выделяют из денатурированного этанола. 10. Фармацевтическая композиция, содержащая эффективное, нетоксичное количество полиморфа по п.1 и его фармацевтически приемлемый носитель. 11. Полиморф по п.1 для использования в качестве активного терапевтического вещества. 12. Полиморф по п.1 для использования при лечении и/или профилактике сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений. 13. Применение полиморфа для изготовления лекарственного препарата для лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений. 14. Способ лечения и/или профилактики сахарного диабета, состояний, связанных с сахарным диабетом, и его некоторых осложнений у человека или других млекопитающих, который включает введение эффективного, нетоксичного количества полиморфа человеку или другому млекопитающему при необходимости. Фиг. 2 Спектр комбинационного рассеяния полиморфа Фиг. 3 Спектр ядерного магнитного резонанса твердого тела полиморфа
МПК / Метки
МПК: C07D 417/12, A61K 31/427, A61P 3/10
Метки: фармацевтический, препарат, новый
Код ссылки
<a href="https://eas.patents.su/7-3031-novyjj-farmacevticheskijj-preparat.html" rel="bookmark" title="База патентов Евразийского Союза">Новый фармацевтический препарат</a>