Промежуточное соединение для использования в синтезе доцетаксела и способ его получения
Формула / Реферат
1. Химическое соединение, имеющее формулу
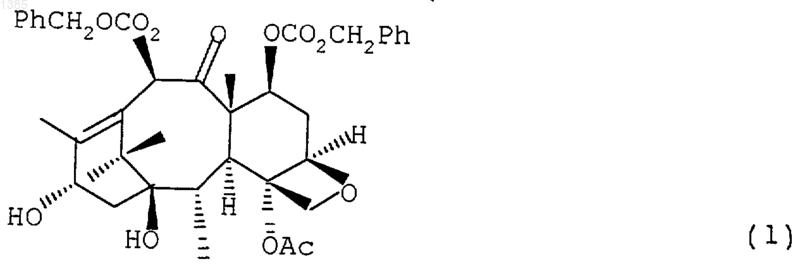
2. Способ получения соединения, имеющего формулу
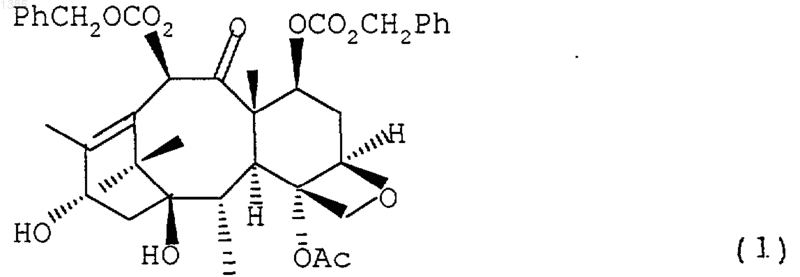
включающий стадию ацилирования 10-деацетилбаккатина III, по крайней мере, 1,5 эквивалентами н-бутиллития и, по крайней мере, 1,5 эквивалентами бензилхлорформиата в тетрагидрофуране.
3. Способ по п.2, по которому 10-деацетилбаккатин III сначала растворяют в вышеуказанном тетрагидрофуране с образованием раствора, затем добавляют н-бутиллитий с образованием первой смеси, и после этого к вышеуказанной первой смеси добавляют указанный бензилхлорформиат с образованием второй смеси.
4. Способ по п.3, по которому указанный н-бутиллитий находится в гексановом растворе, причем н-бутиллитий в гексане по каплям добавляют к указанному раствору.
5. Способ по п.3, по которому перед добавлением н-бутиллития указанный раствор охлаждают до температуры -20шС или ниже.
6. Способ по п.5, по которому указанный раствор охлаждают до температуры около -78шС.
7. Способ по п.5, по которому указанную первую смесь перемешивают при пониженной температуре в течение около пяти минут и указанную вторую смесь перемешивают при пониженной температуре в течение около одного часа.
8. Способ по п.7, по которому указанную вторую смесь гасят хлоридом аммония и после этого концентрируют до остатка.
9. Способ по п.8, включающий стадию растворения указанного остатка в органическом растворителе, не смешиваемом с водой, после чего полученный раствор промывают сначала водой, а затем рассолом с получением органического слоя.
10. Способ по п.9, включающий стадии удаления, сушки и перекристаллизации указанного органического слоя.
11. Способ по п.10, по которому перекристаллизацию проводят с использованием смеси этилацетат/гексан.
12. Способ по п.2, по которому стадию ацилирования указанного 10-деацетилбаккатина III проводят с использованием, по крайней мере, двух эквивалентов н-бутиллития и, по крайней мере, двух эквивалентов бензилхлорформиата.
Текст
1 Данная заявка является частичным продолжением нашей более ранней заявки S. N. 08/609083, поданной 29 февраля 1996 г. и озаглавленной "Промежуточное соединение для синтеза доцетаксела и способ его получения". Область изобретения Данное изобретение относится к синтезу доцетаксела из предшествующих соединений. Более конкретно, данное изобретение касается синтеза доцетаксела с использованием защищенного подходящим образом 10-деацетилбаккатина III, который этерифицируют кислотой с подходящим образом защищенной боковой цепью с получением промежуточного соединения, которое затем может подвергаться снятию защиты, ацилироваться и дополнительно подвергаться снятию защиты для получения доцетаксела. Предпосылки изобретения Известно, что различные производные таксана проявляют противоопухолевую активность. Благодаря этой активности таксаны привлекли повышенное внимание научной и медицинской общественности. Первичным среди них является соединение, называемое "паклитаксел", на которое в литературе также ссылаются как на "таксол". Паклитаксел был одобрен для химиотерапии некоторых различных видов опухолей, и клинические испытания указывают на то, что паклитаксел предлагает широкую область потенциальной антилейкемической и опухолетормозящей активности. Паклитаксел является природным таксановым дитерпеноидом, который найден в некоторых видах тисса (род Тахасеае). К сожалению,концентрация этого соединения является очень низкой. Этот вид вечнозеленого растения также является медленно растущим. Для получения одного килограмма паклитаксела (кора тиссовых деревьев обычно обнаруживает наибольшую концентрацию паклитаксела) требуется приблизительно 16000 фунтов (7248 кг) коры. Таким образом, длительность получения паклитаксела путем выделения делает этот метод получения непривлекательным. В то время как в тиссовых деревьях паклитаксел содержится в крайне низких концентрациях, существуют различные другие таксановые соединения, такие как Баккатин III, цефаломанин, 10-деацетилбаккатин III и другие, которые также могут быть экстрагированы из коры тисса. Некоторые из этих таксановых соединений экстрагируются более легко и с более высоким выходом. Действительно, 10-деацетилбаккатинIII в относительно высокой концентрации может экстрагироваться из листьев тисса как возобновляемого источника. Среди различных таксановых соединений,которые, как было найдено, проявляют противоопухолевую активность, есть соединение известное как "доцетаксел". Это соединение также продается фирмой Rhone-Poulenc Sante под тор 001385 2 говой маркой Taxotere . Доцетаксел имеет следующую формулу Как видно из этой формулы, доцетаксел подобен паклитакселу, за исключением включения трет-бутоксикарбонильной (трет-ВОС) группы у азота в С 3'. Цель настоящего изобретения - предоставить новый, полезный и эффективный способ присоединения защищенной боковой цепи Акольца к скелету защищенного Баккатина III,который затем может превращаться в доцетаксел. Еще одной целью настоящего изобретения является предоставление нового соединения в форме подходящим образом защищенного Баккатина III, которое может использоваться в полусинтезе доцетаксела, а также способа получения такого соединения. Согласно настоящему изобретению далее описывается новое и полезное химическое соединение, имеющее формулу Формула 1 Настоящее изобретение направлено также на способ получения этого соединения ацилированием 10-деацетилбаккатина III, по меньшей мере, 1,5 эквивалентами н-бутиллития и, по меньшей мере, 1,5 эквивалентами бензилхлорформиата и тетрагидрофурана. Предпочтительно, способ получения С 7,С 10 дикарбобензилоксибаккатина III достигается растворением 10-деацетилбаккатина III в тетрагидрофуране с образованием раствора, после чего добавляют, по меньшей мере, 1,5 эквивалента, и предпочтительно, 2 эквивалента нбутиллития с образованием первой смеси, и после этого к первой смеси добавляют, по меньшей мере, 1,5 эквивалента, предпочтительно 2 эквивалента, бензилхлорформиата с образованием второй смеси. Вторая смесь может гаситься раствором хлорида аммония и затем концентрироваться до остатка. Данный остаток может затем растворяться в органическом растворителе, не смешиваемом с водой, с образованием раствора остатка, после чего раствор остатка промывается водой и затем рассолом с образованием органического слоя. Органический слой 3 может затем удаляться, сушиться и перекристаллизовываться или хроматографироваться предпочтительно смесью этилацетат/гексан. По предпочтительной методике реакции осуществляют при пониженной температуре-20 С или ниже. Температура раствора 10 деацетилбаккатина III понижается до температуры предпочтительно около -78 С. Затем по каплям к этому раствору добавляют нбутиллитий в гексане с образованием первой смеси. Первую смесь перемешивают при пониженной температуре в течение приблизительно 5 мин. Затем к первой смеси при пониженной температуре добавляют бензилхлорформиат с образованием второй смеси, и вторую смесь перемешивают в течение приблизительно 1 ч при температуре не более 0 С. Эти и другие цели настоящего изобретения станут более понятными после рассмотрения последующего подробного описания примеров воплощения изобретения. Подробное описание примеров воплощения изобретения В широком смысле настоящее открытие относится к химическому процессу эффективного получения доцетаксела, а также к промежуточному соединению и их предшественникам. Более конкретно, настоящее изобретение раскрывает новое химическое соединение в виде С 7, С 10-ди-CBZ 10-деацетилбаккатина III в качестве полезного промежуточного продукта в получении доцетаксела. С 7, С 10-ди-CBZ 10 деацетилбаккатин III этерифицируют 3-фенилизосериновой кислотой, в имеющей гидрируемую бензильную защитную группу при С 2' С 13 гидроксиле Баккатина III. Общий процесс,описанный здесь, включает получение С 7, С 10 ди-CBZ 10-деацетилбаккатина III, получение подходящим образом защищенной 3-фенилизосериновой кислоты, имеющей гидрируемую защитную группу бензильного типа при С 2',конденсацию этих двух соединений, и последующее снятие защиты, ацилирование при С 3' азоте для присоединения трет-бутоксикарбонильной группы, с последующим дополнительным снятием защиты с получением доцетаксела. А. Получение С 7, С 10 дикарбобензокси 10-деацетилбаккатина III. С 7, С 10-ди-CBZ 10-деацетилбаккатин III Реакция I Согласно способу 10-деацетилбаккатин III растворяют в безводном ТНF (ТГФ, т.е. тетрагидрофуране) и охлаждают в атмосфере азота до температуры менее -20 С, но предпочтительно до -78 С. По каплям добавляют н-бутиллитий(1,6 М в гексане), и раствор перемешивают при пониженной температуре в течение приблизительно 5 мин. Необходимо добавить, по меньшей мере, 1,5 эквивалента н-бутиллития, чтобы получить значительный выход продукта, однако, предпочитается 2 эквивалента. Затем по каплям добавляют бензилхлорформиат (снова для получения значительного выхода необходимо,по меньшей мере, 1,5 эквивалента бензилхлорформиата, предпочтительно 2 эквивалента), и смесь перемешивают на протяжении периода в 1 ч, в течение которого смеси дают возможность подогреться до температуры не более чем на 0 С. Затем смесь гасят холодным насыщенным хлоридом аммония, для устранения избытка нбутиллития и ацетилхлорида, и смесь концентрируют в вакууме. Остаток помещают в этилацетат, один раз промывают водой, затем рассолом, чтобы удалить ненужные соли. Затем органический слой может подвергаться сушке и концентрироваться в вакууме, а остаток перекристаллизовывают или хроматографируют на колонке со смесью этилацетат/гексан, с получением С 7, С 10-ди-CBZ 10-деацетилбаккатина III в виде белого твердого вещества с общим выходом более 80%. В. Получение боковой цепи 3-фенилизосерина. Получение боковой цепи (2R, 3S) этилового эфира N-CBZ O-защищенного 3-фенилизосерина, где С 2' гидроксигруппа защищена гидрируемой защитной группой бензильного типа(формула 2), может быть достигнуто из исходного соединения этилового эфира (2R, 3S) 3 фенилизосерина с помощью следующих двух реакций. Первой реакцией является Реакция II В данном случае этиловый эфир (2R, 3S) 3 фенилизосерина альтернативно растворяют либо в равных частях смеси диэтиловый эфир:вода, либо в равных частях смеси метилтрет-бутиловый эфир:вода, и раствор охлаждают до 0 С. Затем к раствору добавляют карбонат натрия и по каплям в течение приблизительно 5 мин добавляют бензилхлорформиат. Полученную смесь перемешивают при 0 С около 1 ч. После 1 ч перемешивания раствор выливают в воду и экстрагируют метиленхлоридом или этилацетатом, по желанию. Органический слой отделяют, сушат и концентрируют в вакууме до остатка. Затем остаток перекристаллизовывают из смеси этилацетат/гексан с получением этилового эфира N-CBZ 3-фенилизосерина. Данное промежуточное соединение затем защищают гидрируемой защитной группой бензильного типа несколькими путями. Например, 5 один из путей получения защищенной боковой цепи заключается в следующем Реакция III В данном случае гидрируемой защитной группой бензильного типа является бензилолксиметил (ВОМ). Для получения данного соединения этиловый эфир N-CBZ 3-фенилизосерина растворяют в безводном ТГФ в атмосфере азота и охлаждают до пониженной температуры, такой как -40 С или -78 С, например, в ванне сухой лед/ацетон. Затем по каплям добавляют агент алкиллитий, такой как н-бутиллитий,хотя желательно, чтобы алкиллитиевый агент был с алкилом с прямой цепью. В любом случае, реакция наилучшим образом проводится при температуре не более 0 С. Получаемую смесь перемешивают около 10 мин. Затем по каплям в течение около 5 мин добавляют бензилоксиметилхлорид (ВОМ-Сl) и смесь перемешивают приблизительно от 2 до 5 ч при пониженной температуре. После этого раствор подогревают до 0 С и гасят водой, чтобы удалить избыток н-бутиллития. Полученную смесь концентрируют в вакууме до остатка, и данный остаток помещают в этилацетат, промывают водой и рассолом, чтобы удалить ненужные соли. Затем органический слой может сушиться и перегоняться в вакууме, а остаток перекристаллизовывают из смеси этилацетат/гексан или хроматографируют с использованием смеси этилацетат/гексан, получая этиловый эфир NCBZ С 2'-ВОМ 3-фенилизосерина. Еще один путь получения этилового эфираN-CBZ C2'-OBOM 3-фенилоксиизосерина достигается растворением этилового эфира N-CBZ(2R, 3S)-3-фенилизосерина в безводном метиленхлориде. После этого добавляют третичное аминовое основание, такое как диизопропилэтиламин наряду с ВОМ-Сl, и смесь нагревают с обратным холодильником в течение 24 ч. Хотя этот способ дает этиловый эфир N-CBZ C2'ВОМ-3-фенилизосерина реакция протекает более медленно, чем по способу, описанному выше, однако, он может быть более предпочтительным из-за более высокого выхода. В этом случае соединение не очищают, а осуществляют последующие стадии процесса с сырой формой. В каждом случае полученный этиловый эфир N-CBZ C2'-ОВОМ-(2R, 3S)-3-фенилизосерина, либо в очищенном виде по первому пути,либо в сырой форме по второму пути, может просто превращаться в соответствующую кислоту по реакции Реакция IV Защищенный этиловый эфир растворяют в смеси этанол/вода (соотношение 8:1). К раствору добавляют гидроокись лития (или другой подходящий щелочной гидроксид), и полученную смесь перемешивают приблизительно 3 ч для омыления соединения. Затем смесь подкисляют (1 н. соляной кислотой) и экстрагируют этилацетатом. Полученный органический слой отделяют, сушат и концентрируют под вакуумом. Остаточную кислоту затем отделяют для использования без дальнейшей очистки. Это дает желаемый N-CBZ C2'-ОВОМ-(2R,3S)-3 фенилизосерин. Когда этиловый эфир N-CBZ C2'-ОВОМ-3 фенилизосерина используют в сыром виде и превращают в N-CBZ С 2'-ОВОМ-(2R,3S)-3 фенилизосерин, необходимо в дальнейшем очистить конечный продукт. Эту очистку осуществляют путем растворения продукта в толуоле,затем по каплям добавляют один эквивалент дициклогексиламина, и получаемый раствор перемешивают в течение 30 мин. Затем эту смесь концентрируют в вакууме, и полученный остаток перекристаллизовывают из смеси этилацетат/гексан с получением дициклогексиламиновой соли N-CBZ C2'-OBOM-(2R,3S)-3-фенилизосерина. Затем очищенный N-CBZ С 2'ОВОМ-(2R,3S)-3-фенилизосерин выделяют путем растворения данной дициклогексиламиновой соли в метиленхлориде или другом галогенированном растворителе с последующей промывкой метиленхлоридом с несколькими порциями 1 н. НСl. Органический слой затем промывают несколькими порциями воды для удаления гидрохлорида дициклогексиламина. Далее его промывают одной порцией насыщенного солевого раствора и перегоняют в вакууме,получая желаемую кислоту. Сам бензил является еще одним примером гидрируемой защитной группы бензильного типа, который может использоваться вместо ВОМ. Этиловый эфир N-CBZ 2'-бензил-3 фенилизосерина получают, как описано выше,(но заменяют ВОМ-Сl бензилбромидом), в соответствии с реакцией Реакция V Этиловый эфир CBZ защищенного (2R,3S)-3-фенилизосерина растворяют в безводном ТГФ в атмосфере азота и охлаждают до пониженной температуры, такой как -40 С или-78 С, например в ванне из смеси сухой лед/ацетон, затем по каплям добавляют алкил 7 литиевый реагент такой как н-бутиллитий, хотя желательно, чтобы алкиллитиевый реагент был с алкилом с прямой цепью. Получаемую смесь перемешивают около 10 мин. Затем по каплям в течение приблизительно 5 мин добавляют бензилбромид (ВnВr), и смесь перемешивают приблизительно в течение 25 ч при пониженной температуре. После этого раствор подогревают до 0 С и гасят водой для разрушения избытка нбутиллития. Полученную смесь концентрируют под вакуумом до остатка, и данный остаток помещают в этилацетат и промывают водой, для удаления литийбромидной соли, затем следует промывка рассолом. Органический слой сушат и концентрируют под вакуумом, а остаток перекристаллизовывают из смеси этилацетат/гексан или хроматографируют с использованием смеси этилацетат/гексан с получением этилового эфира N-CBZ 2'-бензил 3-фенилизосерина. Этиловый эфир N-CBZ 2'-бензил 3-фенилизосерина альтернативно может быть получен по реакции Реакция VI К перемешиваемому раствору NaH в безводном ТГФ в атмосфере азота в течение 5 мин добавляют этиловый эфир N-CBZ-3-фенилизосерина, растворенный в ДМФ. Затем смесь перемешивают при 0 С в течение 30 мин. Затем по каплям на протяжении 5 мин добавляют бензилбромид (1,1 эквивалента) и перемешивают еще 2 ч. Затем смесь гасят водoй для разложения избытка гидрида натрия. После этого добавляют либо диэтиловый эфир, либо метилтрет-бутиловый эфир. Затем органический слой промывают четырьмя порциями воды для удаления ДМФ и бромида натрия. Далее смесь промывают рассолом, сушат и концентрируют под вакуумом с получением этилового эфира NCBZ С 2'-бензил 3-фенилизосерина, который потом легко можно превратить в N-CBZ С 2'бензил 3-фенилизосерин с помощью процесса,описанного выше (реакция IV). В этом случае вместо бензилоксиметила (ВОМ) С 2' защитной группой является бензил. С. Этерификация защищенного Баккатина III с боковой цепью. Этерификация С 7, С 10 ди-CBZ 10-диацетилбаккатина III с боковой цепью N-CBZ С 2'защищенного 3-фенилизосерина (где С 2' гидроксил защищен любой гидрируемой группой бензильного типа) достигается, как показано ниже. Предпочтительной гидрируемой бензильной группой является ВОМ (бензилоксиметил).(1 эквивалент) формулы 1 и кислотную боковую цепь (6 эквивалентов) формулы 2 растворяют в толуоле. К этой смеси добавляют 4-диметиламинопиридин (ДМАП) и диизопропилкарбодиимид (6 эквивалентов), и получаемую смесь нагревают примерно при 60 - 80 С в течение 1 5 ч. Следует отметить, что другие диалкилкарбодиимиды могут заменять диизопропилкарбодиимид, причем одним из примеров является дициклогексилкарбодиимид. Затем раствору дают охлаждаться до комнатной температуры, и затем добавляют равный объем диэтилового эфира. Получающийся раствор охлаждают до 0 С и выдерживают при этой температуре в течение 24 ч. На этой стадии кристаллизуется, главным образом, примесь мочевины. По истечении 24 ч раствор фильтруют, и остаток прополаскивают либо этиловым эфиром, либо метил-трет-бутиловым эфиром. Объединенные органические фазы промываютсоляной кислотой (5%), водой и рассолом. Органическую фазу отделяют, сушат и концентрируют под вакуумом. Затем получаемый остаток растворяют в смеси этилацетат/гексан и элюируют на силикагеле. Элюент затем концентрируют под вакуумом с получением желаемого C3'NCBZ С 2'-ОВОМ-С 7, С 10 ди-CBZ 10-диацетилбаккатина III формулыD. Снятие защиты и обработка ди-третбутил дикарбонатом и снятие защиты с образованием доцeтаксела. Следующая реакция удаляет CBZ защитные группы в С 7, С 10 и С 3' азоте боковой цепи.(ВОМ используется здесь в качестве примера С 2' гидрируемой защитной группы бензильного типа) Реакция VIII Продукт формулы 3 растворяют в смеси изопропанол/этилацетат, к которой добавляют катализатор Pearlman'а. Полученную смесь гидрируют при 1 атм водорода в течение, по мень 9 шей мере, 24 ч. После этого смесь фильтруют через диатомовую землю и концентрируют под вакуумом до остатка, получая в результате амин, который используют без дальнейшей очистки. На следующей стадии, трет-ВОС группа может присоединяться к N-C3' боковой цепи в соответствии со следующей реакцией Реакция IX. Амин помещают в безводный ТГФ, а для ускорения реакции может добавляться третичное аминовое основание с последующим добавлением ди-трет-бутилдикарбоната. Смесь перемешивают в течение 24 ч, а затем концентрируют под вакуумом и повторно растворяют в этилацетате. Органическую фазу затем промывают водой и рассолом. Затем полученную органическую фазу отделяют, сушат и концентрируют под вакуумом с получением сырого С 2'ОВОМ доцетаксела. На этой стадии необходимо очищать сырой С 2'-ОВОМ доцетаксел. Это можно осуществить с помощью хроматографии на колонке и/или перекристаллизации из смеси этилацетат/гексан. Предпочтительным является проведение хроматографии на колонке со смесью этилацетат/гексан с получением элюента,который концентрируют в вакууме с образованием остатка, с последующей перекристаллизацией остатка из смеси этилацетат/гексан с получением С 2'-ОВОМ доцетаксела по существу в чистом виде. Бензилоксиметильную защитную группу удаляют следующим образом Реакция X. Очищенный C2'-OBOM доцетаксел растворяют в изопропаноле и добавляют катализатор Pearlman'a. Затем смесь гидрируют либо при 1 атм водорода, либо при 40 фунт/дюйм 2 водорода в течение, по меньшей мере, 24 ч. Затем смесь фильтруют через диатомовую землю и концентрируют под вакуумом с получением сырого доцетаксела. В тех случаях, когда С 2' положение в боковой цепи защищено группойO-Вn, сырой доцетаксел можно получить по методу, описанному в литературе (Kanazawa A.,Denis J. N. and Green A. E., J. Org. Chem., 59(1994), 1238). Таким образом, настоящее изобретение было описано с определенной степенью подробности, направленной на иллюстрацию данного изобретения. Следует понимать, что, хотя настоящее изобретение определяется последующей формулой изобретения, в приведенных примерах воплощения настоящего изобретения 10 могут производиться модификации или изменения без отступления от описанных концепций изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Химическое соединение, имеющее формулу включающий стадию ацилирования 10 деацетилбаккатина III, по крайней мере, 1,5 эквивалентами н-бутиллития и, по крайней мере,1,5 эквивалентами бензилхлорформиата в тетрагидрофуране. 3. Способ по п.2, по которому 10 деацетилбаккатин III сначала растворяют в вышеуказанном тетрагидрофуране с образованием раствора, затем добавляют н-бутиллитий с образованием первой смеси, и после этого к вышеуказанной первой смеси добавляют указанный бензилхлорформиат с образованием второй смеси. 4. Способ по п.3, по которому указанный н-бутиллитий находится в гексановом растворе,причем н-бутиллитий в гексане по каплям добавляют к указанному раствору. 5. Способ по п.3, по которому перед добавлением н-бутиллития указанный раствор охлаждают до температуры -20 С или ниже. 6. Способ по п.5, по которому указанный раствор охлаждают до температуры около-78 С. 7. Способ по п.5, по которому указанную первую смесь перемешивают при пониженной температуре в течение около 5 мин и указанную вторую смесь перемешивают при пониженной температуре в течение около 1 ч. 8. Способ по п.7, по которому указанную вторую смесь гасят хлоридом аммония и после этого концентрируют до остатка. 9. Способ по п.8, включающий стадию растворения указанного остатка в органическом растворителе, не смешиваемом с водой, после чего полученный раствор промывают сначала водой, а затем рассолом с получением органического слоя. 10. Способ по п.9, включающий стадии удаления, сушки и перекристаллизации указанного органического слоя. 11. Способ по п.10, по которому перекристаллизацию проводят с использованием смеси этилацетат/гексан. 12. Способ по п.2, по которому стадию ацилирования указанного 10-деацетилбаккатина
МПК / Метки
МПК: C07D 305/14
Метки: соединение, доцетаксела, получения, использования, промежуточное, способ, синтезе
Код ссылки
<a href="https://eas.patents.su/7-1385-promezhutochnoe-soedinenie-dlya-ispolzovaniya-v-sinteze-docetaksela-i-sposob-ego-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Промежуточное соединение для использования в синтезе доцетаксела и способ его получения</a>
Предыдущий патент: Контактный/бесконтактный двухрежимный портативный объект.
Следующий патент: Композиции, содержащие антигрибковый агент и ацетатный буфер.
Случайный патент: Способ ломки материалов на заготовки и устройство для его осуществления.











