Соединение для офтальмологической хирургии и способ ее осуществления
Номер патента: 790
Опубликовано: 24.04.2000
Авторы: Сэламон Джозеф К., Израэл Стэнли К., Гэлин Мэйлс А.
Формула / Реферат
1. Соединение для офтальмологической хирургии, отличающееся тем, что оно содержит вязкоупругий полимер и агент, выбираемый из группы, состоящей из миотических агентов и мидриатических агентов.
2. Соединение по п.1, отличающееся тем, что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - атропин.
3. Соединение по п.1, отличающееся тем, что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - гилокарпин.
4. Соединение по п.1, отличающееся тем, что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - фенилэфрин.
5. Соединение по п.1, отличающееся тем, что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - изопилокарпин.
6. Соединение по п.1, отличающееся тем, что вязкоупругий полимер и агент образуют комплекс, являющийся ацетилхолин гиалуронатом.
7. Соединение по п.1, отличающееся тем, что оно включает в себя анионный вязкоупругий полимер и катионный агент, выбираемый из группы, состоящей из миотических агентов и мидриатических агентов.
8. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - сульфат атропина.
9. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет собой сульфат хондроитина, а агент - гидрохлорид пилокарпина.
10. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид фенилэфрина.
11. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет гиалуронат натрия, а агент - ацетилхолин хлорид.
12. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид пилокарпина.
13. Соединение по п.7, отличающееся тем, что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид изопилокарпина.
14. Лекарственное средство, отличающееся тем, что оно включает в себя биодеградирующие микрокапсулы, которые содержат агент, выбираемый из группы, состоящей из миотических агентов и мидриатических агентов.
15. Лекарственное средство по п.14, отличающееся тем, что микрокапсулы выполнены из полилактида.
16. Лекарственное средство по п.14, отличающееся тем, что микрокапсулы выполнены из сополи (лактидгликолида).
17. Лекарственное средство по п.14, отличающееся тем, что оно дополнительно содержит вязкоупругий полимер.
18. Лекарственное средство, отличающееся тем, что оно включает в себя растворимые мицеллы сополимера, содержащие агент, выбираемый из группы, состоящей из миотических агентов и мидриатичных агентов, при этом мицеллы включают в себя гидрофильную и гидрофобную часть, а агент абсорбируется в гидрофобную часть мицеллы сополимера.
19. Лекарственное средство по п.18, отличающееся тем, что мицелла содержит блоксополимер окись этилена-окись пропилена окись этилена.
20. Лекарственное средство по п.19, отличающееся тем, что мицелла дополнительно содержит фенилэфрин.
21. Лекарственное средство по п.18, отличающееся тем, что дополнительно содержит вязкоупругий полимер.
22. Способ поддержания структурной целостности передней камеры глаза во время хирургии с одновременным поддержанием требуемого размера зрачка, включающий в себя использование лекарственных соединений, отличающийся тем, что лекарственные соединения выбирают согласно п.1 или 21.
Текст
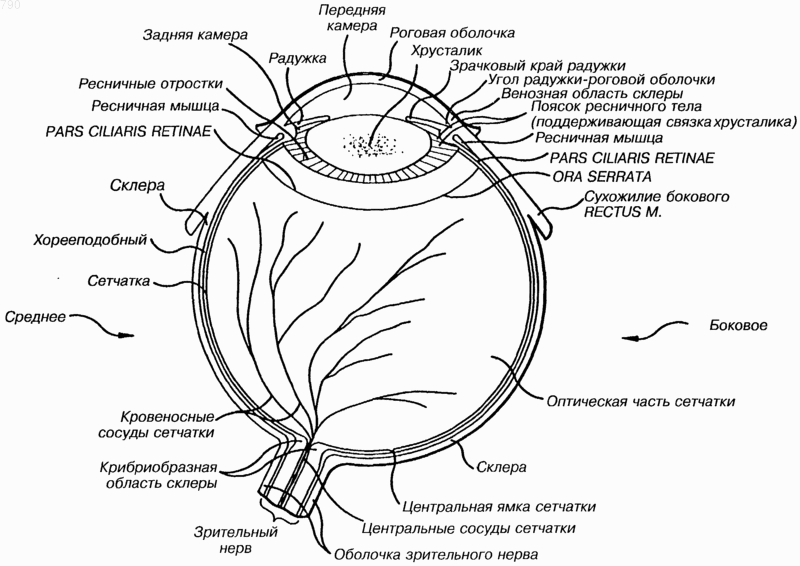
1 Настоящее изобретение относится к соединениям, содержащим вязкоупругий полимер и миотический или мидриатический агент, которые поддерживают структурную целостность передней камеры глаза в течение офтальмологической хирургии, тем самым защищая ткани,образующие и облицовывающие передний сегмент, от потенциальной опасности и, в принципе, обеспечивая постоянную подачу миотического или мидриатического агента. Настоящее изобретение также предлагает соединения, в которых постоянное выделение миотического или мидриатического агента опосредовано микрокапсулами или мицеллами сополимера. Предыстория изобретения Поддержка целостности анатомических компонентов глаза облегчает тонкие манипуляции, производимые внутри малых областей в офтальмологической хирургии,Один из компонентов, который можно контролировать, это передняя камера глаза. Как показано на фиг.1, передняя камера расположена между роговицей и радужной оболочкой глаза. Сразу же за радужной оболочкой следует хрусталик глаза, который размещается между передней камерой и более обширной стекловидной камерой, заполненной стекловидным телом. Поддержание структурной целостности передней камеры минимизирует риск того, что эндотелий или/и радужная оболочка будут повреждены во время проведения операции. Введение вязкоупругих материалов, таких как гиалуронат натрия, сульфат хондроитина, гидроксилпропил-метилцеллюлоза и метилцеллюлоза, в переднюю камеру не позволяет камере сплющиваться (коллапс) при хирургии. Другой компонент, который можно контролировать, это размер зрачка. В ходе хирургии по снятию катаракты желательно, чтобы зрачок был расширен с тем, чтобы доступ к хрусталику был упрощен и было облегчено введение имплантата задней камеры. В этом отношении использовались самые разные мидриатические лекарства, такие, как атропин (холинергический блокатор), фенилэфрин (адренергический стимулятор) и ингибиторы простагландина, и до сих пор преимущественно вводятся наружным наложением. Наоборот, в рефракционных имплантатах и вторичных имплантатах афакия желателен меньший ("миотический") зрачок, чтобы уменьшить травму радужной оболочки, избежать переднего синехиаза, предотвратить образование складок в радужной оболочке и облегчить соответствующее позиционирование имплантата. Применяемые наружно пилокарпин и карбахол (холинергические стимуляторы) и физостигмин, бромид демекария, иодид эхотиофата и изофлюрофат (ингибиторы холинестеразы) использовались для этой цели. Однако во время проведения хирургии и в открытом глазе эффективность локальной ле 000790 2 карственной терапии снижается. Разбавление и отцеживание мешают применению постоянной лекарственной терапии в высоких дозах. Даже непосредственное введение миотических агентов, таких как ацетилхолин-хлорид или карбахол не обеспечивает долгосрочного эффекта и нередко требует частых повторных введений в глаз. Предыдущие попытки достигнуть долгосрочного поддержания эффективных уровней лекарств предполагали технологию непрерывного отпуска лекарств с использованием систематического или трансдермального приема или с размещением биоэрозионного устройства подачи лекарств вне глаза. Такие способы использовались прежде всего для контроля внутриглазного давления у пациентов с глаукомой. Однако до этого изобретения не было изобретено способа, который сочетал бы постоянную подачу мидриатических или миотических лекарств с поддержанием структурной целостности передней камеры. Краткое изложение изобретения Настоящее изобретение относится к соединениям, которые можно использовать для поддержания структурной целостности передней камеры глаза и для обеспечения длительного выделения миотического или мидриатического агента. В разных примерах выполнения этого изобретения соединения включают в себя вязкоупругий полимер, где длительное выделение миотического или мидриатического агента опосредовано ионными взаимодействиями. В других примерах выполнения изобретения длительное выделение миотического или мидриатического агента опосредовано микрокапсулами или мицеллами сополимера. В конкретных примерах выполнения соединения можно применять для обеспечения и быстрого выделения миотического или мидриатического агента и более медленного длительного выделения. Описание чертежей На фиг.1 - представлена иллюстрация Клементе, 1978 г., в "Anatomy", Lea and Fibiger,Филадельфия, фиг.501; на фиг. 2. - проиллюстрирован эффект разбавления миотического или мидриатического агента в передней камере глаза, вызываемый обычной скоростью текучести (оборота) внутриглазной жидкости в присутствии или в отсутствии вязкоупругого комплекса полимерлекарство. Кривая А представляет несвязанное лекарство = 0,0500 моль/л в физиологическом(солевом) растворе; кривая В представляет несвязанное лекарство = 0,025 моль/л плюс вязкоупругий комплекс полимер-лекарство = 0,0500 эквивалент/л в физиологическом растворе; и кривая С представляет вязкоупругий комплекс полимер-лекарство =0,100 эквивалент/л в физиологическом растворе. 3 Подробное описание изобретения Для ясности представления, но не посредством ограничения, подробное описание изобретения подразделяется на следующие разделы:(4) соединения согласно изобретению и(5) способы использования соединений согласно изобретению. Вязкоупругие полимеры Настоящее изобретение предусматривает соединения, содержащие вязкоупругие полимеры, включая, не ограничиваясь этим, анионные вязкоупругие полимеры - гиалуроновую кислоту (гиалуронат), сульфат хондроитина, сульфат дерматана, карбоксиметилцеллюлозу, сульфат гепарина, сульфат кератана, карбоксиметилгидроксипропил-целлюлозу, карбоксиметилгидроксиэтил-целлюлозу, сульфат целлюлозы, фосфат целлюлозы, карбоксиметилгуар, карбоксиметилгидроксипропилгуар, карбоксиметилгидроксиэтилгуар, смолу ксантана, каррагеенан, анионные полисахариды, анионные белки и полипептиды, анионный полиакриламид, анионный поли-N-винилпирроллидон, анионный полидиметил акриламида, полимеры и сополимеры 2 акриламидо-2-метил-пропансульфоновой кислоты, акриловую кислоту и метакриловую кислоту. Вышеуказанные соединения в своих неионизированных формах могут функционировать как кислотные полимеры; в своих ионизированных формах эти соединения могут функционировать как полимерные анионы. Молекулярный вес вязкоупругих полимеров этого изобретения колеблется от 50.000 до 8.000.000 дальтонов в зависимости от выбранного полимера. Например, средний молекулярный вес от 1.000.000 до 5.000.000 дальтонов обычно используется для гиалуроната натрия,тогда как средний молекулярный вес более 80.000 дальтонов обычно используется для гидроксипропилметил-целлюлозы. Концентрация вязкоупругого полимера может меняться от 1 мг/мл до 60 мг/мл и предпочтительно от 5 мг/мл до 30 мг/мл. Вязкость вязкоупругого полимера может меняться от 1000 сантистоксов до 60.000 сантистоксов и предпочтительно от 2,500 до 5,500 сантистоксов для гидроксипропилметилцеллюлозы и от 20,000 до 40,000 сантистоксов для гиалуроната натрия. Такие значения вязкости не только позволяют вводить полимер в глаз путем инъекции или выдавливания, но они также достаточны, чтобы оставаться внутри передней камеры (т.е. они легко не сойдут), поддерживать ее структурную целостность и позволять легкое удаление. Кроме того, вязкоупругие полимеры этого изобретения растворимы в воде и могут со временем элюироваться. 4 Миотические агенты Настоящее изобретение предусматривает соединения, содержащие миотические агенты,включая, но не ограничиваясь этим, пилокарпин, изопилокарпин, гидрохлорид пилокарпина,нитрат пилокарпина, гидрохлорид изопилокарпина, нитрат изопилокарпина, карбахол, физостигмин, сульфат физостигмина, сульфит физостигмина, бромид демекария, иодид экотиофата и хлорид ацетилхолина. Предпочтительные агенты - это члены семейства соединений пилокарпина и изопилокарпина. Миотические агенты этого изобретения могут применяться в нейтральном или в заряженном, катионном виде в зависимости от характера длительной подачи лекарств, которую должно обеспечивать соединение. Из вышеизложенного перечня к числу агентов, которые считаются основными, относятся: пилокарпин,изопилокарпин и физостигмин; к числу агентов,считающихся гидрофобными, относятся: пилокарпин, изопилокарпин и физостигмин; а агенты, считающиеся катионными - это бромид демекария, иодид экотиопата, гидрохлорид пилокарпина, нитрат пилокарпина, гидрохлорид изопилокарпина, нитрат изопилокарпина, карбахол,сульфат физостигмина, хлорид ацетилхолина и сульфит физостигмина. Мидриатические агенты Настоящее изобретение предусматривает наличие соединений, содержащих мидриатические агенты, включая, но не ограничиваясь этим, атропин, сульфат атропина, гидрохлорид атропина, метилбромид атропина, метилнитрат атропина, атропин гипердюрик, атропин Nоксид, фенилэприн, гидрохлорид фенилэфрина,гидроксиамфетамин, гидробромид гидроксиамфетамина, иодид гидроксиамфетамина, циклопентолат, гидрохлорид циклопентолата, гоматропин, гидробромид гоматропина, гидрохлорид гоматропина, метилбромид гоматропина, скополамин, гидробромид скополамина, гидрохлорид скополамина, метилбромид скополамина, метилнитрат скополамина, скополамин N-оксид,тропикамид, гидробромид тропикамида и гидрохлорид тропикамида. Предпочтительные агенты - члены семейства соединений атропина и семейства соединений фенилэфрина. Мидриатические агенты изобретения могут применяться в нейтральном или в заряженном, катионном, виде в зависимости от характера длительной подачи лекарств, которую должно обеспечивать соединение. Из вышеизложенного перечня к числу агентов, которые считаются основными, относятся: атропин, фенилэфрин,гидроксиамфетамин, циклопентолат, гоматропин, скополамин и тропикамид; к числу гидрофобных агентов относятся атропин, фенилэфрин, гидроксиамфетамин, циклопентолат, гоматропин, скополамин и тропикамид; а агенты,считающиеся катионными - это сульфат атропина, гидрохлорид атропина, метилбромид 5 атропина, метилнитрат атропина, атропин гипердюрик, атропин N-оксид, гидрохлорид фенилэфрина, иодид гидроксиамфетамина, гидробромид гидроксиамфетамина, гидрохлорид циклопентолата, гидробромид гоматропина, гидрохлорид гоматропина, метилбромид гоматропина, гидробромид скополамина, гидрохлорид скополамина, метилбромид скополамина, метилнитрат скополамина, скополамин N-оксид,тропикамид и гидробромид тропикамида. Соединения согласно изобретению Это изобретение предусматривает соединения, которые обеспечивают длительное выделение миотических или мидриатических агентов, как описано выше, в котором выделение агента опосредовано (1) ионными (включая кислотно-щелочные) взаимодействиями; (2) микрокапсулами; или (3) мицеллами сополимеров. Соединения также являются средством для поддержания структурной целостности передней камеры глаза. В первом наборе неограничивающих примеров выполнения изобретения предусматривается наличие соединений, в которых длительное выделение миотического или мидриатического агента достигается посредством ионных взаимодействий между агентом и вязкоупругим полимером. В конкретных примерах выполнения соединение может содержать анионный вязкоупругий полимер и катионный миотический или мидриатический агент, и в этом случае катионный агент соединения, будучи помещен в глаз,может выделяться путем замещения эндогенными ионами натрия или калия или другими естественно встречаемыми катионами. В одном конкретном неограничительном примере анионная вязкоупругая полимерная кислота может являться гиалуронатом натрия, а катионный агент может быть мидриатическим агентом сульфатом атропина, где при подготовке соединения сульфат (или бисульфат) натрия удаляется с использованием избытка сульфата атропина в присутствии меньшего количества гиалуроната натрия после чего следует диализ. Этот процесс можно повторять несколько раз, чтобы приготовить гиалуронат атропина высокой чистоты. В другом конкретном неограничительном примере анионный вязкоупругий полимер может являться сульфатом хондроитина, а катионный агент может быть миотическим агентом пилокарпином, который можно комбинировать путем взаимодействия сульфата натрия хондроитина с гидрохлоридом пилокарпина. В еще одном конкретном неограничительном примере выполнения можно осуществить ионообменное взаимодействие между гиалуронатом натрия и гидрохлоридом фенилэфрина, что дает гиалуронат фенилэфрина. Во втором родственном наборе неограничительных примеров выполнения изобретения предусматривается наличие соединений, в которых длительное выделение миотического или 6 мидриатического агента достигается посредством ионных кислотно-щелочных взаимодействий между агентом и вязкоупругим полимером. В конкретных примерах выполнения соединение может содержать кислотный вязкоупругий полимер и щелочной миотический или мидриатический агент, и в этом случае соединение,будучи помещенным в глаза с приблизительно нейтральным рН, обеспечит относительно медленное выделение миотического или мидриатического агента путем ионного замещения лекарства из существующих катионов. В одном конкретном неограничительном примере кислотная вязкоупругая полимерная кислота может являться гиалуроновой кислотой, а щелочной агент может быть мидриатическим агентом атропином. Когда эти два соединения комбинируются в соединении, можно образовать полимерную соль гиалуронат атропина. В другом конкретном неограничительном примере выполнения изобретения гиалуроновая кислота может реагировать с щелочным миотическим лекарством пилокарпином в воде в температурном диапазоне от 5 до 50 С (где пилокарпин становится протонированным поликислотой и становится солью вязкоупругого полимера), за чем следует диализ или сверхтонкая фильтрация для удаления непрореагировавшего пилокарпина. Затем получившееся соединение гиалуронат пилокарпина можно, как альтернатива, либо стерилизовать и установить на соответствующее значение рН и осмолальности для использования (например, и не как ограничение, где диапазон рН составляет примерно 6,8-7,8 и предпочтительно 7,2-7,4 и осмолальность составляет 285+/-55 мОсм/кг и предпочтительно 290-320 мОсм/кг), либо его можно извлечь путем высушивания in vacuo или лиофилизацией. Еще в другом конкретном неограничительном примере выполнения изобретения гиалуроновая кислота может взаимодействовать с мидриатическим агентом фенилэфрином в водном растворе с использованием избытка фенилэфрина, после чего следует диализ, что дает в результате гиалуронат фенилэфрина. В неограничительном примере, относящемся к длительному выделению миотического или мидриатического агента из передней камеры глаза, на фиг. 2 описаны три характерных условия с использованием объема внутриглазной жидкости 310 микролитров и скорости текучести (оборота) внутриглазной жидкости 1,5 микролитра в минуту (Шенвальд, 1993, "Фармакокинетика в отпуске глазных лекарств" (глава 10) в "Biopharmaceuticals of Ocular Drug Delivery", CRC Press, Inc., Бока Рейтон, Флорида). Единицы для несвязанного лекарства даны в молях на литр, а единицы для вязкоупругих полимеров даны в единицах эквивалентов на литр,что описывало бы любой вязкоупругий полимер с любым миотическим или мидриатическим лекарством. 7 На фиг. 2 кривая А представляет несвязанное лекарство, для которого начальная концентрация в 0,0500 моль/л снижается до 0,0084 моль/л после 6 ч разбавления в глазе, вызванного скоростью текучести внутриглазной жидкости. Кривая В на фиг. 2 представляет комбинацию несвязанного лекарства (отсутствует вязкоупругий полимер) и образовавшего ионный комплекс (связанного) лекарства- вязкоупругого полимера. На этой кривой комплекс вязкоупругого полимера - лекарства имеет предсказанную кооперативную постоянную связи 5 х 10-2 (Хаякава и др., 1983, "Macromolecules", 16: 1642). Это значение было определено для карбоксиметилцеллюлозы (как образцового анионного вязкоупругого полимера) с гидрофильным катионом иона додецилтриметиламмония. Из кривой В можно видеть, что при начальной концентрации несвязанного лекарства в 0,0500 молей на литр, при 6 ч текучести внутриглазной жидкости 0,0340 молей на литр медикамента остается в передней камере. Эта конечная концентрация более чем в 4 раза больше, чем конечная концентрация несвязанного лекарства, наблюдаемая спустя 6 ч. Кривая С на фиг. 2 представляет образовавшие комплекс с ионом (связанные) лекарство-вязкоупругий полимер, где начальная концентрация в 0,100 эквивалентов на литр (дающая равновесную начальную концентрацию 0,500 молей на литр несвязанного лекарства) снижается до 0,0354 молей на литр после 6 часов пребывания в глазе, что вызывается текучестью внутриглазной жидкости. Эта конечная концентрация более чем в 4 раза больше конечной концентрации несвязанного лекарства и немного больше, чем концентрация на кривой В. На этой кривой комплекс вязкоупругого полимера-лекарства имеет предсказанную кооперативную постоянную связи 5 х 10-2 (Хаякава и др., 1983, "Macromolecules", 16: 1642). Таким образом, из фиг. 2 можно видеть,что два условия образовавшего ионный комплекс миотического или мидриатического комплекса лекарство-полимер ясно показывают эффект длительного выделения лекарства во времени по сравнению с несвязанным лекарством в передней камере глаза. В третьем наборе неограничительных примеров выполнения этого изобретения предусматривается наличие соединений, содержащих микрокапсулы, которые растворимы или могут увеличиваться (распухать) в водной среде и предпочтительно биодеградируют, которые сами по себе содержат миотический или мидриатический агент, где агент может элюироваться со временем, когда микрокапсула медленно растворяется, распадается или распухает. Обычно такие микрокапсулы могут при желании быть меньше, чем длина волны света, чтобы предотвратить рассеивание света и ухудшение зрение. 8 В этой процедуре выбранный агент вводится в микрокапсулу во время образования микрокапсулы. Поскольку вязкость микрокапсул обычно низкая, можно добавить вязкоупругий полимер для поддержки внешней камеры. Растворимые микрокапсулы можно получать из самих по себе биодеградирующих полимеров, таких, как поли-DL-лактид или поли-DLлактид-согликолид, которые в сухом виде можно превратить в микрокапсулы, содержащие соответствующий агент (Кларк и др., 1994,"Polymer Preprints", 35(2): 73). В качестве альтернативы растворимые микрокапсулы можно получать из чувствительных к рН полимеров,где изменение рН может вызывать расширение микрокапсулы, что приводит к системе длительного отпуска лекарства. Пример такого чувствительного к рН полимера - это поли(1-)лизин-альт-терефталевая кислота, которая расширяется при значениях рН более 6 (Макино и др., 1994, "Polymer Preprints", 35: 54). Биодеградирующие микрокапсулы, содержащие миотический или мидриатический агент, могут готовиться с использованием полимеров, таких,как полилактид или полилактид-согликолид,которые разлагаются спустя некоторое время. В четвертом наборе неограничительных примеров выполнения изобретения предусматривается наличие соединений, содержащих растворимые мицеллы сополимера, которые содержат миотический или мидриатический агент,где мицеллы содержат гидрофильную и гидрофобную части, и агент (в его незаряженном виде) абсорбируется в гидрофобную часть мицеллы сополимера (Арка и др., 1994, "Polymer Preprints", 35: 71). При равновесии можно ожидать,что гидрофобное лекарство, такое, как фенилэфрин, будет находиться как внутри, так и снаружи мицеллы сополимера. Когда препарат помещается в переднюю камеру глаза, по мере того как внешний агент удаляется, внутренний агент может медленно выделяться. По своей природе такие мицеллы сополимера могут предпочтительно быть гидрофильными-гидрофобными или гидрофильными-гидрофобнымигидрофильными. Предпочтительно гидрофильные блоки получаются из окиси этилена, а гидрофобные блоки из окиси пропилена (блоксополимеры окиси этилена-окиси пропилена-окиси этилена продаются под товарными наименованиями Pluronic или Ploxamer). Соединения, содержащие мицеллы сополимера, можно перемешивать с вязкоупругим полимером, таким,как гидроксипропилметилцеллюлоза, чтобы поддерживать структурную целостность передней камеры. Далее настоящее изобретение предусматривает наличие соединений, содержащих ряд миотических агентов или ряд мидриатических агентов. Количество миотического или мидриатического агента, присутствующего в соединении, 9 может быть таким, которое дает желаемый терапевтический эффект; иначе говоря, желаемый размер зрачка в течение требуемого периода времени. Такие количества будут меняться для разных агентов, но их легко определить с использованием зависимостей доза-реакция на дозу, известных специалистам. Концентрация миотического или мидриатического агента может колебаться от 0,001 мг/мл до 20 мг/мл и предпочтительно от 0,025 мг/мл до 10 мг/мл. В качестве одного конкретного неограничительного примера, если миотическое лекарство - это ацетилхолин хлорид, состав комплекса полимер-лекарство можно приготовить с использованием раствора ацетилхолин хлорида с ацетилхолин гиалуронатом, где концентрация ацетилхолина может быть 10 мг/мл и осмолальность может устанавливаться на 305 мОсм/кг маннитом. В качестве другого конкретного неограничительного примера, если миотический агент это гидрохлорид пилокарпина, состав комплекса полимер-лекарство можно готовить, используя раствор гидрохлорида пилокарпина с гиалуронатом пилокарпина, где концентрация пилокарпина может составлять 1 мг/мл и осмолальность устанавливаться на 305 мОсм/кг маннитом. В качестве еще другого конкретного неограничительного примера при использовании мидриатического лекарства сульфата атропина можно приготовить раствор гиалуроната атропина, содержащего сульфат атропина, где концентрация атропина может быть 0,3 мг/мл и осмолальность можно установить на 305 мОсм/кг маннитом. В каждом из вышеизложенных примеров в этом абзаце катионное лекарство можно перемешать с комплексом полимер-лекарство в стерильной воде и затем можно установить осмолальность,используя нейтральный агент маннит. Ввиду того, что во время офтальмологической хирургии важно поддерживать осмолальность передней камеры глаза, соединения этого изобретения предпочтительно проявляют такую осмолальность, что их введение в глаз не может пагубно изменить осмолальность передней камеры. Сообщалось, что осмолальность естественного содержимого передней камеры составляет 301-305 мОсм/кг ("Geigy Scientific Tables",том 1, под ред. К.Лентнера, восьмое издание,1981, Базель, Швейцария). Осмолальность ионного комплекса вязкоупругого полимера и лекарства можно поддерживать избытком лекарства в виде его соли (например, раствор 3,0% фенилэфрин хлорида является изотоничным по сравнению с раствором NaCl с 0,9 весовыми процентами), или раствором нейтрального агента или в комбинации с ним, например, с глицерином (где раствор с 2,6 вес.% является изотоничным относительно раствора NaCl с 0,9 вес.%, или маннитом (где раствор с 5,07% является изотоничным относительно раствора NaCl с 0,9 вес.%). Если используются традиционные изотоничные растворы, которые могут содер 000790 10 жать ионы натрия, ионы калия, ионы кальция и т.д., такие ионы могут преждевременно заместить образовавшее комплекс с ионом лекарство,выделяя его в раствор, и может потребоваться добавить избыток катионного лекарства, чтобы снова установить равновесие полимерлекарство. В предпочтительных примерах выполнения изобретения осмолальность соединений может составлять примерно от 280 до 340 мОсм/кг и предпочтительно примерно от 280 до 340 мОсм/кг. Чтобы поддержать структурную целостность передней камеры глаза, соединения должны быть достаточно вязкими, чтобы предотвратить камеру от сжатия (коллапса) во время хирургических манипуляций. Однако соединения должны быть также достаточно текучими, чтобы их можно было ввести в переднюю камеру посредством инъекции или выдавливания, а также чтобы их можно было удалить (например,промыванием) в заключении хирургической процедуры. Соответственно, вязкость соединения согласно изобретению составляет от 1000 до 60000 сантистоксов и предпочтительно от 2500 до 40000 сантистоксов. Если применяются вязкоупругие полимеры, концентрации вязкоупругого полимера предпочтительно примерно 10-30 мг/мл в водном (предпочтительно изотоническом) растворе. Способы использования соединений согласно изобретению Соединения этого изобретения особенно полезны, когда их используют в разных офтальмологических хирургических процедурах, таких как желательно проводимые, когда зрачок расширен, включая внутрикапсульную и внекапсульную хирургию и процедуры вскрытия полого органа, и процедуры, желательно проводимые, когда зрачок сужен, включая хирургию передних сегментов, такую как хирургическое отделение спаек стекловидного тела/роговицы,отделение спаек радужной оболочки/роговицы и помещение факических рефракционных имплантатов и вторичных афакических имплантатов. Например, и не в виде ограничения, соединения, содержащие мидриатический агент, согласно изобретению, можно использовать в стандартной внекапсульной хирургии катаракты, выполняемой под местной или расположенной позади глазного яблока анастезией. Следует отметить, что анестезия позади глазного яблока обычно делает радужную оболочку немного более чувствительной к расширяющим или сужающим зрачок каплям (закон Старлинга). Затем мидриатическое соединение этого изобретения можно инъецировать в переднюю камеру до или/и после соответствующей капсулотомии(вскрытия влагалища глазного яблока). Затем можно проводить промывание, аспирацию, отжимание или факоэмульгирование катаракты. Затем можно вставить имплантат, и остаточный 11 мидриатический вязкий материал можно промыть из глаза. При таких процедурах соединение этого изобретение может помочь извлечению хрусталика и помещению имплантата. В другом неограничительном примере миотические соединения согласно этому изобретению можно использовать в стандартных процедурах помещения миопического рефракционного имплантата. После проведения парацентеза миотическое соединение можно инъецировать в переднюю камеру. Затем можно сделать входной надрез, можно позиционировать имплантат, на рану можно наложить шов, и вязкое миотическое соединение можно промыть из глаза. Применение соединений этого изобретения дает ряд преимуществ. Во-первых, настоящее изобретение предусматривает наличие соединения, которое одновременно обеспечивает и механическую, и фармацевтическую активность, полезную в офтальмологической хирургии. Во-вторых, соединения этого изобретения можно использовать для удовлетворения давно ощущаемой потребности в средствах получения длительного выделения миотических или мидриатических агентов в течение хирургии. Втретьих, соединения этого изобретения могут предотвратить или уменьшить подъем внутриглазного давления, который может быть связан с использованием вязкоупругого раствора, не содержащего миотического агента. В-четвертых, применять соединения изобретения можно для предотвращения заднего (последующего) или переднего синехиаса путем поддержания зрачка расширенным непосредственно после операции. Более того, во время обычной хирургии с потерей камеры и гипотонией имеется потеря тонуса и функции радужной оболочки. Поскольку вязкие соединения этого изобретения поддерживают камеру и некоторую степень внутриглазного давления и находятся в контакте с радужной оболочкой в течение длительного времени, устанавливается эффект резервуара,так что одновременно достигаются поддержание камеры, улучшенный тонус и реакция радужной оболочки и отпуск лекарства. Кроме того, особенно если желателен миоз (сужение зрачка), долгосрочное воздействие миотиков может притупить потенциал подъема давления вязкоупругого материала. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение для офтальмологической хирургии, отличающееся тем, что оно содержит вязкоупругий полимер и агент, выбираемый из группы, состоящей из миотических агентов и мидриатических агентов. 2. Соединение по п.1, отличающееся тем,что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - атропин. 12 3. Соединение по п.1, отличающееся тем,что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - гилокарпин. 4. Соединение по п.1, отличающееся тем,что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - фенилэфрин. 5. Соединение по п.1, отличающееся тем,что вязкоупругий полимер представляет собой гиалуроновую кислоту, а агент - изопилокарпин. 6. Соединение по п.1, отличающееся тем,что вязкоупругий полимер и агент образуют комплекс, являющийся ацетилхолин гиалуронатом. 7. Соединение по п.1, отличающееся тем,что оно включает в себя анионный вязкоупругий полимер и катионный агент, выбираемый из группы, состоящей из миотических агентов и мидриатических агентов. 8. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - сульфат атропина. 9. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет собой сульфат хондроитина, а агент - гидрохлорид пилокарпина. 10. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид фенилэфрина. 11. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет гиалуронат натрия, а агент - ацетилхолин хлорид. 12. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид пилокарпина. 13. Соединение по п.7, отличающееся тем,что вязкоупругий полимер представляет собой гиалуронат натрия, а агент - гидрохлорид изопилокарпина. 14. Лекарственное средство, отличающееся тем, что оно включает в себя биодеградирующие микрокапсулы, которые содержат агент,выбираемый из группы, состоящей из миотических агентов и мидриатических агентов. 15. Лекарственное средство по п.14, отличающееся тем, что микрокапсулы выполнены из полилактида. 16. Лекарственное средство по п.14, отличающееся тем, что микрокапсулы выполнены из сополи (лактидгликолида). 17. Лекарственное средство по п.14, отличающееся тем, что оно дополнительно содержит вязкоупругий полимер. 18. Лекарственное средство, отличающееся тем, что оно включает в себя растворимые мицеллы сополимера, содержащие агент, выбираемый из группы, состоящей из миотических агентов и мидриатичных агентов, при этом мицеллы включают в себя гидрофильную и гидрофобную часть, а агент абсорбируется в гидрофобную часть мицеллы сополимера. 19. Лекарственное средство по п.18, отличающееся тем, что мицелла содержит блоксополимер окись этилена-окись пропилена окись этилена. 20. Лекарственное средство по п.19, отличающееся тем, что мицелла дополнительно содержит фенилэфрин. 21. Лекарственное средство по п.18, отличающееся тем, что дополнительно содержит вязкоупругий полимер. 22. Способ поддержания структурной целостности передней камеры глаза во время хирургии с одновременным поддержанием требуемого размера зрачка, включающий в себя использование лекарственных соединений, отличающийся тем, что лекарственные соединения выбирают согласно п.1 или 21.
МПК / Метки
МПК: A61K 31/74, A61F 2/14
Метки: способ, осуществления, хирургии, офтальмологической, соединение
Код ссылки
<a href="https://eas.patents.su/8-790-soedinenie-dlya-oftalmologicheskojj-hirurgii-i-sposob-ee-osushhestvleniya.html" rel="bookmark" title="База патентов Евразийского Союза">Соединение для офтальмологической хирургии и способ ее осуществления</a>












