Новый способ получения дронедарона
Формула / Реферат
1. Способ получения дронедарона формулы (I) или его соли, который включает стадии, на которых:
(а) восстанавливают нитрогруппу соединения формулы (II)
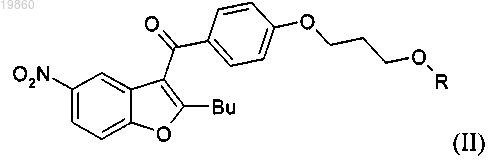
в которой "Bu" означает н-бутил;
R означает водород или защитную группу, которая может быть удалена гидрированием,
с получением соединения формулы (III)
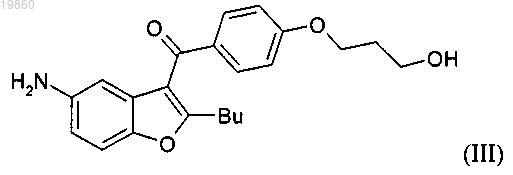
(b) бис-мезилируют полученное таким образом соединение (III) с получением соединения формулы (IV)
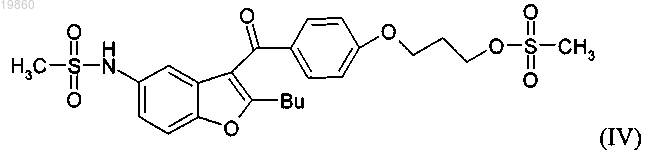
(с) замещают мезилоксигруппу соединения формулы (IV) дибутиламиногруппой с получением дронедарона формулы (I)
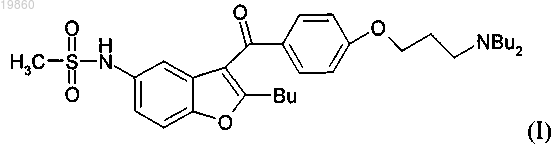
(d) необязательно превращают дронедарон в его соль.
2. Способ по п.1, в котором на стадии (d) дронедарон превращают в его гидрохлоридную соль.
3. Способ по п.1 или 2, в котором стадия восстановления (а) представляет собой каталитическое восстановление.
4. Способ по любому из пп.1-3, в котором стадию мезилирования (b) осуществляют с мезилгалогенидом.
5. Способ по п.4, в котором указанный мезилгалогенид представляет собой мезилхлорид.
6. Способ по любому одному из пп.1-5, в котором на стадии мезилирования (b) мезилгалогенид добавляют при температуре 0-5°С.
7. Способ по п.6, в котором стадию мезилирования (b) затем продолжают при комнатной температуре.
8. Способ по пп.4-7, в котором указанный мезилгалогенид используют, по меньшей мере, в удвоенном количестве по отношению к соединению формулы (III) в молярном выражении.
9. Соединение формулы (IV)
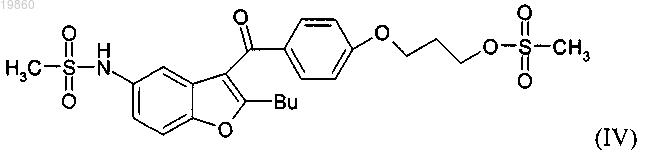
в которой "Bu" означает н-бутил,
и его соли и сольваты.
10. Способ по любому одному из пп.1-8, в котором соединение формулы (II) получают из соединения формулы (V)
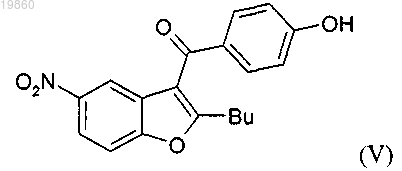
в которой "Bu" означает н-бутил,
взаимодействием с 3-галоген-1-пропанолом или защищенным 3-галоген-1-пропанолом.
Текст
НОВЫЙ СПОСОБ ПОЛУЧЕНИЯ ДРОНЕДАРОНА Изобретение относится к новому способу получения дронедарона и его солей, в частности к способу синтеза, который позволяет получить указанное соединение и его соли с хорошими выходами, высокой частотой и промышленно выгодным путем; изобретение также касается нового синтеза промежуточных соединений.(71)(73) Заявитель и патентовладелец: ЛАБОРАТОРИО КИМИКО ИНТЕРНАЦИОНАЛЕ С.П.А. (IT) Область техники, к которой относится изобретение Настоящее изобретение относится к новому способу получения дронедарона и его солей, в частности к способу синтеза, который позволяет получить указанные соединения с хорошими выходами, высокой чистотой и промышленно выгодным способом. Изобретение также касается нового синтеза промежуточных соединений. Уровень техники Соединение с химическим названием N-[2-бутил-3-(4-(3-(дибутиламино)пропокси)бензоил)-5 бензофуранил]метансульфонамид, международным непатентованным названием которого является"дронедарон", имеет следующую формулу (I): в которой "Bu" означает н-бутил. Дронедарон представляет собой лекарственный препарат, который уже в течение некоторого времени продается как средство для лечения аритмии сердца. Известные способы синтеза дронедарона очень сложны и связаны с введением различных функциональных групп в бензофурановое кольцо посредством нескольких стадий и очисток, что негативно сказывается на выходе и промышленной применимости указанных способов. Документ WO 2009/044143 раскрывает способ получения дронедарона, который включает взаимодействие 2-бутил-3-(4-гидроксибензоил)-5-нитробензофурана с производным защищенного дибутиламина, восстановление нитрогруппы, мезилирование и, наконец, превращение полученного производного в его соль. Сущность изобретения Цель настоящего изобретения заключается в разработке способа получения дронедарона, который является простым для осуществления в промышленности, который обеспечивает хорошие выходы и в котором используются легко очищаемые промежуточные соединения. Таким образом, в соответствии с одним из аспектов настоящее изобретение касается способа получения дронедарона формулы (I), приведенной выше, или его соли, который содержит следующие стадии:(а) восстановление нитрогруппы соединения формулы (II)R означает водород или защитную группу, которая может быть удалена гидрированием,с получением соединения формулы (III)(b) бис-мезилирование полученного таким образом соединения (III) с получением соединения формулы (IV)(с) замещение мезилоксигруппы соединения (IV) дибутиламиногруппой с получением дронедарона формулы (I)(d) необязательное превращение дронедарона в его соль. В соответствии с преимущественными вариантами осуществления изобретения соли дронедарона являются фармацевтически приемлемыми солями. Наиболее предпочтительная соль представляет собой гидрохлорид. Под "защитной группой, которая может быть удалена гидрированием" авторы в настоящем изобретении подразумевают защитную группу гидроксила, которую можно удалить каталитическим гидриро-1 019860 ванием; указанные группы хорошо известны квалифицированному в данной области специалисту и включают, например, бензильную группу или аллильную группу. Стадия (а). Стадия восстановления (а) нитрогруппы может быть выполнена с использованием любого восстанавливающего агента, подходящего для превращения нитрогруппы в аминогруппу. Согласно предпочтительному варианту осуществления изобретения восстановление (а) выполняют каталитически с использованием водорода, например, в присутствии катализатора Pd/C или PtO2 в подходящем растворителе,например низшем спирте, таком как метанол, этанол, 1-пропанол, 2-пропанол, бутанол или их смеси. Реакция восстановления может быть проведена при температуре между комнатной температурой и приблизительно 50C, например около 25-45C, преимущественно около 30C. Водород может быть подан в реакцию под давлением, например при давлении приблизительно 4 бар в подходящем автоклаве. Протекание реакции может отслеживаться согласно методикам, известным квалифицированному в данной области специалисту, в конце восстановления катализатор может быть удален фильтрованием и желаемое соединение может быть выделено концентрированием растворителя и, при необходимости,очищено, например, кристаллизацией. Стадия (b). Стадия бис-мезилирования (b) позволяет одновременно мезилировать аминогруппу, образованную на стадии (а), и гидроксильную группе, присутствующую в боковой цепи. Данная стадия является особенно важной, поскольку она позволяет посредством одной простой реакции и ввести функциональную сульфонамидную группу (присутствующую в конечном соединении), и заместить гидроксигруппу мезилоксигруппой, т.е. оптимальной уходящей группой, подходящей для последующего замещения дибутиламиногруппой. Реакция может быть выполнена с мезилирующим агентом, например галогенидом метилсульфонила (мезилгалогенидом), предпочтительно мезилхлоридом, в подходящем растворителе, например хлорированном растворителе, таком как дихлорметан, или ацетонитриле, преимущественно при температурах ниже или равных комнатной температуре. В частности, первую часть реакции, относящуюся к добавлению мезилирующего агента, осуществляют при температурах около 0C, например около 0-5C или даже ниже, в то время как продолжение реакции преимущественно происходит при комнатной температуре. Мезилирующий агент, разумеется, должен использоваться в достаточных количествах, чтобы мезилировать две функциональные группы (амино и гидрокси), т.е. в молярном выражении по крайней мере в удвоенном количестве относительно соединения формулы (III), предпочтительно более чем в удвоенном молярном количестве относительно соединения формулы (III). В конце реакции мезилирования желаемое соединение выделяют в соответствии с приемами, хорошо известными квалифицированному в данной области специалисту, и, при необходимости или при желании, очищают. Стадия (с). Стадия (с) получения дронедарона включает замещение мезилоксигруппы дибутиламиногруппой и предпочтительно выполняется в подходящем полярном апротонном растворителе, таком как диметилформамид, ацетонитрил, предпочтительно ацетонитрил, в присутствии дибутиламина. Реакция может быть выполнена при температурах чуть выше комнатной и конечное соединение формулы (I), при желании или необходимости, может быть выделено согласно приемам, известным специалисту, квалифицированному в данной области техники. Альтернативно, дронедарон не выделяют и не очищают, а используют в сыром виде на стадии образования соли (d). Стадия (d). Стадия образования соли (d) является необязательной, и, при желании, данную стадию выполняют в соответствии с любым способом, известным квалифицированному в данной области специалисту, который позволяет приготовить желаемую соль дронедарона без изменения функциональных групп, присутствующих в молекуле. Так, дронедарон, например, может быть превращен в гидрохлоридную соль в ходе реакции с хлористо-водородной кислотой в соответствующем растворителе, как хорошо известно специалисту в данной области техники. Технические подробности относительно способа по настоящему изобретению будут представлены в следующей экспериментальной части описания. Соединение формулы (IV) представляет собой новое соединение (молекулу) и является дополнительным объектом настоящего изобретения, вместе с его солями и/или сольватами. Исходное соединение формулы (II) может быть получено согласно любому возможному методу синтеза. Согласно предпочтительному варианту осуществления изобретения соединение формулы (II) получают исходя из соединения формулы (V) взаимодействием с 3-галоген-1-пропанолом, например 3-хлор-1-пропанолом, или защищенным 3-галоген-1-пропанолом, в подходящих реакционных условиях. Пример данного получения представлен в экспериментальной части настоящего описания. Под "защищенным 3-галоген-1-пропанолом" авторы изобретения подразумевают 3-галоген-1 пропанол, в котором гидроксильная группа защищена группой R, как определено выше. В соответствии с другими аспектами изобретение также касается получения дронедарона согласно описанным выше стадиям (a)-(d), в которых исходное соединение формулы (II) синтезируют, исходя из указанного выше соединения формулы (V), преимущественно согласно раскрытому выше способу получения. Все промежуточные продукты обсуждаемых выше реакций могут быть легко выделены и, при желании или необходимости, очищены кристаллизацией. Как известно, кристаллизация представляет собой простой способ, который легко осуществить в промышленном масштабе (по сравнению, например, с очисткой хроматографическими методами). В частности, реакция мезилирования обычно представляет собой критическую реакцию для получения дронедарона, и полученный продукт обычно требует тщательной очистки, почти всегда хроматографической. Было обнаружено, однако, что, когда реакцию мезилирования выполняют не последней(т.е. именно так, как предложено в настоящем изобретению), можно избежать очистки мезилированного промежуточного продукта хроматографией и, тем не менее, получить конечный продукт с высоким выходом и хорошей чистотой. Как указано, простота способов очистки очень важна для удобства промышленного получения. Таким образом, действуя в соответствии с настоящим изобретением, дронедарон можно преобразовать в соль напрямую, так как нет необходимости выделять и очищать его в конце стадии (с). Что касается способов предшествующего уровня техники, то способ по настоящему изобретению позволяет получить дронедарон и его соли чистыми и с хорошими выходами, без необходимости направлять промежуточные реакционные продукты на дополнительные трудоемкие стадии очистки, в том числе когда способ выполняют в промышленном масштабе. Осуществляя способы из предшествующего уровня техники, заявитель установил, что указанные стадии очистки были необходимы для того, чтобы получить дронедарон с необходимой фармацевтической степенью чистоты, что, как следствие, негативно сказывалось на выходах способа в целом и на стоимости при промышленном производстве. Экспериментальная часть Пример 1 (стадия а). Получение 3-4-[(5-амино-2-бутил-1-бензофуран-3-ил)карбонил]феноксипропан-1-ола (формула(формула (II, растворенного в 1800 мл метанола, загружают в стеклянный автоклав Бюхи (Buchi). Затем добавляют 9 г Pd/C 10% (50% Н 2 О) и загружают Н 2 при давлении 4 бар. Смесь оставляют при перемешивании, поддерживая температуру ниже 40C. Как только поглощение водорода завершается, реакцию оставляют при перемешивании в течение приблизительно дополнительного 1 ч, до тех пор пока не установится температура 25 С. Катализатор отфильтровывают на панели Celite и содержащий продукт спиртовой раствор концентрируют для получения осадка. Сырой продукт кристаллизуют, извлекая из него 400 мл толуола, и продукт сушат под вакуумом при 40C в течение 6-7 ч. Получают 151 г продукта, указанного в заголовке. Выход: 91%. 1(2 Н, t); 4,20 (2 Н, t); 6,63 (2 Н, m); 6,94 (2 Н, d, J=8,7 Гц); 7,25 (1H, m); 7,82 (2H, d; J=8,7 Гц). Температура плавления = 86-90 С. Пример 2 (стадия b). Получение 3-4-[2-бутил-5-метансульфонамид-1-бензофуран-3-ил)карбонил]феноксипропилметансульфоната (формула (IV. 124,3 г (1,09 моль) мезилхлорида в 250 мл дихлорметана добавляют по каплям в раствор 150 г соединения со стадии (а) (0,408 моль) и 86,2 г пиридина (1,09 моль) в 1200 мл дихлорметана, проверяя,чтобы температура не превысила 10C. Как только добавление по каплям завершают, реакционную смесь оставляют при комнатной температуре приблизительно на 24 ч. 1000 мл деионизированной воды, предварительно охлажденной до 0-5C, добавляют к органической фазе и две фазы перемешивают в течение приблизительно 10 мин. Затем водную фазу удаляют и дихлорметан последовательно промывают: 1000 мл водного раствора 0,1 н. HCl, 1000 мл водного раствора 2% NaHCO3 и 1000 мл деионизированной воды. Органическую фазу сушат над Na2SO4, соль отфильтровывают и растворитель выпаривают при пониженном давлении. К полученному таким образом осадку добавляют 1500 мл толуола, смесь кипятят с обратным холодильником до полного растворения твердой фазы и оставляют остывать. Затем смесь охлаждают в течение 3-4 ч при 0-4C и твердую фазу отфильтровывают. Влажный продукт промывают на фильтре примерно 150 мл толуола, предварительно охлажденного до 0-5C, выгружают и сушат при 40 С в течение 6-7 ч. Получили 197 г продукта, указанного в заголовке. Выход 92%. 1(1H, dd, J=8,7 Гц, J=2,2 Гц); 7,45 (1H, d, J=8,7 Гц); 7,79 (2H, d, J=8,7 Гц). Температура плавления = 132-136C. Пример 3 (стадии c и d). Получение дронедарона HCl) (формула (I)HCl). К суспензии 195 г (0,372 моль) димезила в 1560 мл ацетонитрила добавляют 207 г (1,60 моль) дибутиламина. Раствор кипятят с обратным холодильником в течение 4-5 ч. Как только реакцию завершают,смесь доводят до 40-45 С и растворитель перегоняют при пониженном давлении. К осадку добавляют 957 мл толуола и 750 мл деионизированной воды. Как только водную фазу отделяют, загружают 750 мл деионизированной воды и рН раствора доводят до 4,6-4,8 80% раствором уксусной кислоты. Смесь оставляют при перемешивании в течение приблизительно 5-10 мин, затем водную фазу отделяют и поддерживают любую интерфазу (межфазу), образованную с органической фазой. Толуол дважды промывают с 750 мл 1% раствора NaCl и с 750 мл 2% водного раствора бикарбоната. Проверяют рН водной фазы: если он равен около 6,5-7, то воду отделяют; если ниже, то добавляют твердый бикарбонат натрия до тех пор, пока не будет достигнута величина, указанная выше. Дополнительно выполняют две операции промывания органической фазы с 750 мл деионизированной воды. Добавляют 7 г углерода и фазу толуола оставляют при перемешивании при 40-50C в течение приблизительно 1 ч. Раствор фильтруют горячим на панели Celite и органическую фазу без углерода концентрируют при пониженном давлении. Полученный таким образом осадок растворяют в 585 мл ацетона при 30-35C. 36,4 г 37% HCl добавляют по каплям при указанной температуре, поддерживая смесь ниже 40C. Реакцию оставляют медленно остывать и после приблизительно 2 ч охлаждают до 0-5 С. Через 1 ч твердую фазу отфильтровывали и влажный продукт промывали примерно 150 мл ацетона. Сырой гидрохлорид дронедарона перекристаллизовывают из ацетона и сушат под вакуумом при 40C в течение 6-7 ч. Получают 156 г гидрохлорида дронедарона. Выход: 71%. Чистота ВЭЖХ 99%. 1(2H, m); 2,90 (3 Н, s); 2,95 (2H, t); 3,06 (4H, m); 3,24 (2H, m); 4,23 (2H, t); 6,92 (2H, d, J=8,7 Гц,); 7,19 (1H, d,J=2,1 Гц); 7,31 (1H, dd, J=8,7 Гц, J=2,1 Гц); 7,40 (1H, d, J=8,7 Гц); 7,76 (2H, d, J=8,7 Гц); 11,90 (1H, s). Температура плавления = 141-145C. Пример 4. Получение 3-4-[(2-бутил-5-нитро-1-бензофуран-3-ил)карбонил]феноксипропан-1-ола (формула (II. К раствору 222 г (0,655 моль) 2-бутил-3-(4-гидроксибензоил)-5-нитробензофурана (формулы (V в 1780 мл ДМФ добавляют 312 г (2,26 моль) карбоната калия, 11 г (0,066 моль) йодида калия и 11 г (0,034 моль) тетрабутиламмонийбромида. Реакционную смесь нагревают до 50C и приблизительно через 30 мин добавляют по каплям 100 г 3-хлор-1-пропанола. В конце добавления по каплям реакционную смесь доводят до 80-85C и оставляют при перемешивании в течение 4-5 ч. Как только реакция завершается, смесь охлаждают до 40-50C и неорганические соли удаляют фильтрованием. Органический растворитель отгоняют при пониженном давлении, поддерживая температуру около 60-70C, и осадок растворяют в 2220 мл толуола. После выполнения трех операций промывания органической фазы, каждого с 1130 мл деионизированной воды, толуол концентрируют до получения осадка. Сырой продукт растворяют примерно в 100 мл этилацетата и смесь оставляют охлаждаться при 0-4C в течение приблизительно 12 ч. Твердый осадок отфильтровывают, влажный продукт промывают небольшим количеством этилацетата, предварительно охлажденного до 0-5C, и сушат под вакуумом при 40C в течение 6-7 ч. Получили 181 г 3-4-[(2-бутил-5-нитро-1-бензофуран-3-ил)карбонил]феноксипропан-1-ола (формула (II. Выход: 69%. 1 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения дронедарона формулы (I) или его соли, который включает стадии, на которых:(а) восстанавливают нитрогруппу соединения формулы (II)R означает водород или защитную группу, которая может быть удалена гидрированием,с получением соединения формулы (III)(b) бис-мезилируют полученное таким образом соединение (III) с получением соединения формулы(с) замещают мезилоксигруппу соединения формулы (IV) дибутиламиногруппой с получением дронедарона формулы (I)(d) необязательно превращают дронедарон в его соль. 2. Способ по п.1, в котором на стадии (d) дронедарон превращают в его гидрохлоридную соль. 3. Способ по п.1 или 2, в котором стадия восстановления (а) представляет собой каталитическое восстановление. 4. Способ по любому из пп.1-3, в котором стадию мезилирования (b) осуществляют с мезилгалогенидом. 5. Способ по п.4, в котором указанный мезилгалогенид представляет собой мезилхлорид. 6. Способ по любому одному из пп.1-5, в котором на стадии мезилирования (b) мезилгалогенид добавляют при температуре 0-5 С. 7. Способ по п.6, в котором стадию мезилирования (b) затем продолжают при комнатной температуре. 8. Способ по пп.4-7, в котором указанный мезилгалогенид используют, по меньшей мере, в удвоенном количестве по отношению к соединению формулы (III) в молярном выражении. 9. Соединение формулы (IV) в которой "Bu" означает н-бутил,и его соли и сольваты. 10. Способ по любому одному из пп.1-8, в котором соединение формулы (II) получают из соединения формулы (V)
МПК / Метки
МПК: C07D 307/82
Метки: способ, новый, получения, дронедарона
Код ссылки
<a href="https://eas.patents.su/6-19860-novyjj-sposob-polucheniya-dronedarona.html" rel="bookmark" title="База патентов Евразийского Союза">Новый способ получения дронедарона</a>










