Способ ингибирования ингибитора 1 активатора плазминогена.
Номер патента: 1003
Опубликовано: 28.08.2000
Авторы: Берг Дэвид Т., Гриннелл Брайан В., Ричардсон Марк А.
Формула / Реферат
1. Способ ингибирования ингибитора 1 активатора плазминогена, включающий назначение нуждающемуся в этом человеку эффективного количества соединения
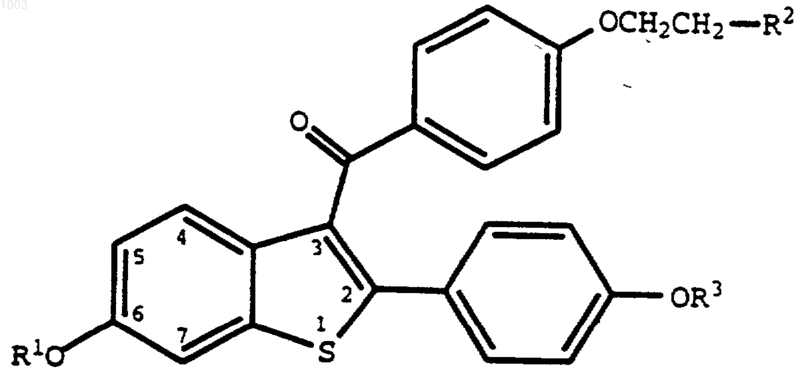
где R1 и R3 представляют независимо друг от друга водород, -СН3, 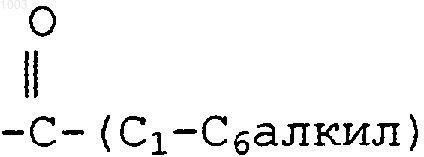 , или
, или 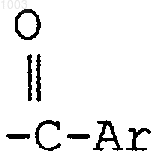
где Аr - необязательно замещенный фенил;
R2 выбирают из группы, состоящей из пирролидино, гексаметиленимино и пиперидино;
и его фармацевтически приемлемой соли и сольвата.
2. Способ по п.1, отличающийся тем, что указанное соединение является его хлористо-водородной солью.
3. Способ по п.1, отличающийся тем, что указанное соединение является

или его хлористо-водородной солью.
Текст
1 Фибринолитическая система играет ключевую роль в поддержании нормального гемостатического баланса. Критическим фактором этой системы является ингибитор плазминогенного активатора 1 (PAI-1), который снижает эндогенную способность к удалению фибрина путем ингибирования активатора плазминогена,такого как тканевый активатор плазминогена типа (tPA). Исследования документально подтверждают, что повышение PAI-1 связано с повышением риска глубокого венозного тромбоза. Повышение PAI-1 также обнаружено у пациентов, страдающих инфарктом миокарда и сепсисом. В связи с тем, что ослабление фибринолитической способности связано с повышением риска заболеваний сердечно-сосудистой системы, снижение PAI-1 должно приводить к кардиопротекции. Действительно, последние исследования по анализу уровня PAI-1 у женщин до и после наступления менопаузы в FraminghamOffspring Study продемонстрировали, что у женщин в постклемактерическом периоде заметно более высокий уровень PAI-1, который может быть снижен до доклемактерического уровня с помощью эстрогенной терапии. Полагают, что общему воздействию эстрогенной заместительной терапии на снижение риска заболеваний сердца способствует это снижение активности PAI-1. Хотя PAI-1 может вырабатываться в различных тканях, его существенное количество секретируется клетками сосудистого эндотелия. Сосудистый эндотелий составляет главный орган, который действует в процессах регулирования свертывания крови, воспаления и обмена жидкостей и медиаторов между внутрисосудистыми полостями и тканями паренхимы. Вследствие этого, правильное функционирование эндотелия имеет решающее значение во всей системе гомеостаза. Так как количество PAI-1 в клетках эндотелия может повышаться в ответ на некоторые стимулы, в число которых входят цитокины, он приводит к состоянию дисфункции, в результате которой могут развиться нарушения свертывания, местные и системные сосудистые воспаления и усиление развития и разрыв атеросклеротической бляшки. Эти эффекты могут в дальнейшем привести к различным состояниям, включая инфаркт миокарда,глубокий венозный тромбоз и диссеминированный интраваскулярный тромбоз. Так как PAI-1, осуществляя местный контроль за обменом между эндотелиальными клетками и плазмой, может играть главную роль во многих патологических процессах, агенты,которые ингибируют экспрессию PAI-1 в эндотелии, могут быть пригодны в лечении таких состояний, как сепсис, раны, включая основные тканевые повреждения и травмы, синдром общего воспалительного ответа, септический синдром, септический шок и синдром множественной дисфункции органов (включая DIC коагу 001003 2 лопатия потребления), а также в лечении инфаркта миокарда, глубокого венозного тромбоза, диссеминированного внутрисосудистого тромбоза, разрыва атеросклеротической бляшки и связанных с ними осложнений. Кроме того,из-за решающей роли фибрина в биологии клеток опухоли, агенты, которые модулируют PAI1, могут найти применение в качестве антиметастатических агентов. Данное изобретение предлагает способы ингибирования ингибитора 1 активатора плазминогена, состоящие в назначении нуждающемуся в этом человеку эффективного количества соединения формулы I где R1 и R3 представляет независимо друг от друга водород, -СН 3, илиR2 выбирают из группы, состоящей из пирролидино, гексаметиленимино и пиперидино; и их фармацевтически приемлемые соли и сольваты. Настоящее изобретение касается открытия того, что группа 2-фенил-3-ароилбензотиофенов(бензотиофенов) формулы I пригодна для ингибирования PAI-1. Способы применения, предложенные данным изобретением, состоят в назначении человеку, нуждающемуся в этом, дозы соединения формулы I или его фармацевтически приемлемой соли или сольвата, которые эффективны для ингибирования PAI-1 или тех физиологических условий, которые связаны с его избыточным количеством. Термин ингибировать включает его общепринятые значения, которые включают препятствование, предупреждение,сдерживание и замедление, остановку, реверсирование прогрессирования, тяжести или результирующего симптома или эффекта. Ралоксифен, соединение данного изобретения, являющийся хлористо-водородной солью соединения формулы I, в которой R1 и R3 - это водород и R2 - это 1-пиперидинил, является молекулой - регулятором ядра. Показано, что ралоксифен связывается с рецептором эстрогена, и считается, что он является молекулой, чья функция и фармакология являются антиэстрогенными, и что он блокирует способность эстрогена активировать маточные ткани и эстро 3 гензависимые формы рака грудной железы. Действительно, ралоксифен блокирует действие эстрогена в некоторых клетках; однако в других видах клеток ралоксифен активирует те же гены и демонстрирует такое же фармакологическое действие, что и эстроген, например, в развитии остеопороза и гиперлипидемии. Таким образом,ралоксифен относится к антиэстрогенам со смешанными свойствами агонист-антагонист. В настоящее время полагают, что уникальный профиль действия ралоксифена и его отличия от действия эстрогена существуют благодаря уникальной активации и/или супрессии действия различных генов рецепторным комплексом ралоксифен-эстроген, что препятствует активации и/или супрессии генов эстроген-эстроген рецепторного комплекса. Следовательно, хотя ралоксифен и эстроген пригодны и конкурируют по отношению к одним и тем же рецепторам, фармакологический результат их генного регулирования трудно предсказать, и он уникален для каждого. В основном, соединение составляется в лекарственную форму с обычными эксципиентами, разбавителями или носителями и спрессовывается в таблетки или составляется в виде эликсиров или растворов, удобных для орального применения или для внутримышечного или внутривенного введения. Соединения могут быть введены чреcкожно и могут быть составлены в виде дозированных форм с замедленным высвобождением и т.п. Соединения, используемые в способах настоящего изобретения, можно получить в соответствии с известными методиками, описанными в патентах США 4,133,814; 4,418,068 и 4,380,635. В основном, процесс начинается с бензо[b]тиофена, имеющего 6-гидроксильную группу и 2-(4-гидроксифенильную) группу. Исходное соединение защищено, ацилировано и лишено защиты для образования соединений формулы I. Примеры получения подобных соединений описаны в вышеуказанных патентах США. Необязательно замещенный фенил включает фенил и фенил, замещенный одним или двумя C1-С 6 алкилом, С 1-С 4 алкокси, гидрокси,нитро, хлором, фтором, или три(хлор или фтор)метилом. Соединения, используемые в способах данного изобретения, образуют фармацевтически приемлемые соли присоединения кислоты или основания с большим количеством органических и неорганических кислот и оснований и включают физиологически приемлемые соли,которые часто используются в фармацевтической химии. Такие соли также являются частью настоящего изобретения. Неорганические кислоты, использующиеся для образования подобных солей, включают хлористо-водородную кислоту,бромисто-водородную,иодистоводородную, азотную, серную, фосфорную, гипофосфорную и т.п. Также могут быть исполь 001003 4 зованы соли - производные органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые и гидроксиалкандионовые кислоты, ароматические кислоты,алифатические и ароматические сульфоновые кислоты. Такие фармацевтически приемлемые соли включают ацетат, фенилацетат трифторацетат, акрилат, аскорбат, бензоат, хлорбензоат,динитробензоат, гидроксибензоат, метоксибензоат, метилбензоат, о-ацетоксибензоат, нафтален-2-бензоат, бромид, изобутират, фенилбутират, -гидроксибутират, бутин-1,4-диоат, гексин-1,4-диоат, капрат, каприлат, хлорид, цинамат, цитрат, формат, фумарат, гликолят, гептаноат, гиппурат, лактат, малат, малеат, гидроксималеат, малонат, манделат, мезилат, никотинат, изоникотинат, нитрат, оксалат, фталат, терафталат, фосфат, кислый ортофосфат, вторичный ортофосфат, метафосфат, пирофосфат, пропиолат, пропионат, фенилпропионат, салицилат,себакат, сукцинат, суберат, сульфат, бисульфат,пиросульфат, сульфит, бисульфит, сульфонат,бензолсульфонат, р-бромфенилсульфонат, хлорбензолсульфонат, этансульфонат, 2-гидроксиэтансульфонат, метансульфонат, нафтален-1 сульфонат, нафтален-2-сульфонат, р-толуолсульфонат, ксилолсульфонат, тартрат и т.п. Предпочтительной солью является хлористоводородная соль. Фармакологически приемлемые соли присоединения кислот обычно получают взаимодействием соединения формулы I с эквимолярным или избыточным количеством кислоты. Реагенты обычно соединяют в общем растворителе, таком как диэтиловый эфир или бензол. Соль обычно выпадает в осадок в течение от 1 часа до 10 дней и может быть выделена фильтрацией, или растворитель может быть выпарен общеизвестными способами. Основания, используемые для получения солей, включают гидроксид аммония и гидроксиды щелочных и щелочно-земельных металлов, карбонаты, а также алифатические и первичные, вторичные и третичные амины, алифатические диамины. Основания, особенно пригодные для получения солей присоединения,включают гидроксид аммония, карбонат калия,метиламин, диэтиламин, этилендиамин и циклогексиламин. Фармацевтически приемлемые соли обычно характеризуются лучшей растворимостью по сравнению с соединениями, производными которых они являются, поэтому они более удобны для получения лекарственной формы в виде жидкости или эмульсии. Фармацевтические готовые лекарственные формы можно получить с помощью известных из предшествующего уровня методик. Например, соединения могут образовывать лекарственную форму с обычными эксципиентами, разбавителями или носителями, и могут быть со 5 ставлены в форме таблетки, капсул, суспензий,порошков и т.п. Эксципиентами, разбавителями и носителями, пригодными для подобных лекарственныых форм, являются следующие: наполнители и заменители, такие как крахмал,сахара, маннит и кремнийсодержащие производные; связывающие агенты, такие как карбоксиметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин и поливинилпирролидон; увлажняющие агенты, такие как глицерин; дезинтегрирующие агенты, такие как карбонат кальция и бикарбонат натрия; агенты для замедления растворения, такие как парафин; ускорители резорбции, такие как четвертичные аммониевые соединения; поверхностноактивные агенты, такие как цетиловый спирт,моностеарат глицерина, адсорбционные носители, такие как каолин и бентонит; и смазывающие материалы, такие как тальк, кальций, стеарат магния и твердые полиэтиленгликоли. Соединения также могут быть составлены в форме эликсиров или растворов, удобных для орального применения, или в виде растворов для парентерального применения, например для внутримышечного, подкожного или внутривенного введения. Кроме того, соединения хорошо пригодны для получения таких лекарственных форм, как дозированные формы с длительным высвобождением и т.п. Лекарственные формы могут быть составлены таким образом, чтобы высвобождался только или преимущественно активный ингредиент в определенных участках пищеварительного тракта, возможно через определенный период времени. Покрытия оболочки защитные матрицы могут быть получены,например, из полимерных веществ или восков. Для ингибирования PAI-1 или любого другого описанного в заявке применения требуется определенная дозировка соединения формулы I,и она зависит от тяжести заболевания, пути введения и других факторов, и обычно подбирается лечащим врачом. В общем случае приемлемая и эффективная дневная доза составляет от 0,1 до около 1000 мг/день, и более точно от 50 до 200 мг/день. Такие дозы назначаются нуждающемуся в них человеку для приема от 1 до около 3 раз в день, или более часто, если это необходимо,для эффективного ингибирования PAI-1 или для любого другого описанного применения. Обычно более предпочтительным является введение соединения формулы I в виде соли присоединения кислоты, как при применении фармацевтических средств, имеющих основную группу, такую как пиперидиновое кольцо. Также удобно вводить подобное соединение оральным путем. Для этого предлагаются следующие оральные дозированные формы. ГОТОВЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ В последующих препаративных формах Активный ингредиент означает соединение формулы I. 6 Лекарственная форма 1: Желатиновые капсулы. Твердые желатиновые капсулы получают,используя следующее: Ингредиент Активный ингредиент Крахмал, NF Крахмал в виде текучего порошка Силиконовая жидкость 350 сантистокс (сСт) Ингредиенты смешивают, пропускают через сито с ячейками 45 по стандарту США и помещают в твердые желатиновые капсулы. Примеры лекарственных форм ралоксифена в виде капсул показаны ниже: Лекарственная форма 2: Капсула, содержащая ралоксифен Ингредиент Ралоксифен Крахмал/NF Крахмал в виде текучего порошка Силиконовая жидкость 350 сСт Лекарственная форма 3: Капсула, содержащая ралоксифен Ингредиент Ралоксифен Крахмал, NF Крахмал в виде текучего порошка Силиконовая жидкость 350 сСт Лекарственная форма 4: Капсула, содержащая ралоксифен Ингредиент Ралоксифен Крахмал, NF Крахмал в виде текучего порошка Силиконовая жидкость 350 сСт Лекарственная форма 5: Капсула, содержащая ралоксифен Ингредиент Ралоксифен Крахмал, NF 7 Крахмал в виде текучего порошка Силиконовая жидкость 350 сСт Показанные выше лекарственные формы могут быть изменены в соответствии с разумными вариантами. Таблетированные лекарственные формы готовят используя приведенные ниже ингредиенты: Лекарственная форма 6: Таблетки Ингредиент Активный ингредиент Целлюлоза микрокристаллическая Диоксид кремния, мелкодисперсный Стеариновая кислота Компоненты смешивают и спрессовывают для образования таблетки. В другом случае, таблетки, каждая из которых содержит 0,1-1000 мг активного ингредиента, получают следующим образом: Лекарственная форма 7: Таблетки Ингредиент Активный ингредиент Крахмал Целлюлоза микрокристаллическая Поливинилпирролидон (в виде 10% раствора в воде) Натрий карбоксиметилцеллюлоза Стеарат магния Тальк Активный ингредиент, крахмал и целлюлозу пропускают через сито с ячейками 45 стандарта США и тщательно перемешивают. Раствор поливинилпирролидона смешивают с полученными порошками, которые затем пропускают через сито с ячейками 14 стандарта США. Полученные таким образом гранулы высушивают при 50-60 С и пропускают через сито с ячейками 18 стандарта США. Натрий карбоксиметилцеллюлозу, стеарат магния и тальк,предварительно пропущенные через сито 60 стандарта США, затем добавляют к гранулам и после смешивания спрессовывают на таблетирующей машине с получением таблеток. Суспензии, содержащие 0,1-1000 мг медикамента на 5 мл дозу, получают следующим образом: 8 Лекарственная форма 8: Суспензии Ингредиент Активный ингредиент Натрий карбоксиметилцеллюлоза Сироп Раствор бензойной кислоты Корригент Краситель Очищенная вода до Медикамент пропускают через сито с ячейками 45 стандарта США и смешивают с карбоксиметилцеллюлозой и сиропом с образованием однородной пасты. Раствор бензойной кислоты, ароматизатор и краситель разбавляют некоторым количеством воды и добавляют при перемешивании. Дополнительное количество воды затем добавляют до получения требующегося объема. Анализ эндотелиальных клеток PAI-1 96-луночную планшету для культуры тканей готовят с 5 х 104 человеческих эндотелиальных клеток (HUVEC) на лунку в среде Clonetics для роста эндотелиальных клеток (EGM), дополненных 2% FBS. После инкубирования в течение ночи при 37 С среду замещают средой,не содержащей сыворотку (DMEM/F-12 среда,20mM-HEPES, рН 7,5, 50 мкг/мл гентамицина,1 мкг/мл человеческого трансферрина и 1 мкг/мл бычьего инсулина) с соединением 1 или без него (где R1 и R3 - это водород и R2 - это пирролидино), и с 1 нм IL-1-бeta или без него. После инкубирования в течение ночи при 37 С образцы культуральной среды исследуются на секрецию PAI-1, используя Imubind,plasma PAI-1 твердофазный иммуносорбентный метод (ELISA) (American Diagnostic Inc. 822/1S). РЕЗУЛЬТАТЫ Эндотелиальные клетки пупочной вены человека (HUVEC) были обработаны соединением 1, конкурентным к введению PAI-1 с IL-1. В начальном эксперименте с несколькими клонами клеток, полученными от коммерческого поставщика (Clonetics), мы обнаружили, что некоторые клоны не способны к ответу на 17 бета эстрадиол, и таким образом непригодны для экспериментов по определению воздействия соединения 1 на секрецию PAI-1. Как показано в табл.1, используя линию клеток, способную к ответу на эстроген, мы наблюдали, что соединение 1 значительно понижает индукцию PAI-1,вызванную IL-1 при ее концентрации в 0,5 нм. Как показано в табл.2, при использовании различных клонов эстрогенчувствительных клеток,соединение 1 ингибировало индуцированнуюIL-1 секрецию зависимым от концентрации образом. Эти данные показывают, что соединение 1 является очень сильным ингибитором выделения PAI-1 активированными эндотелиальными клетками, и должно приводить к кардиопротекторному действию при кардиоваскулярных нарушениях, благодаря повышению фибринолитической способности. Кроме того, положительное воздействие соединения 1 на уменьшение PAI-1 может быть использовано в тех случаях, при которых повышение его уровня связано с патологией. Таблица 1. Воздействие соединения 1 на секрецию PAI-1 эндотелиальными клетками человека Обработка Таблица 2. Концентрация при ответе на действие соединения 1 на секрецию PAI-1 эндотелиальными клетками человека Обработка 5 х 10-9 М соединения 1 5 х 10-10 М соединения 1 5 х 10-11 М соединения 1 5 х 10-12 M соединения 1 5 х 10-13 М соединения 1 5 х 10-14 М соединения 1 10 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ ингибирования ингибитора 1 активатора плазминогена, включающий назначение нуждающемуся в этом человеку эффективного количества соединения где R1 и R3 представляют независимо друг от друга водород, -СН 3,R2 выбирают из группы, состоящей из пирролидино, гексаметиленимино и пиперидино; и его фармацевтически приемлемой соли и сольвата. 2. Способ по п.1, отличающийся тем, что указанное соединение является его хлористоводородной солью. 3. Способ по п.1, отличающийся тем, что указанное соединение является
МПК / Метки
МПК: A61K 31/4025
Метки: ингибирования, способ, активатора, ингибитора, плазминогена
Код ссылки
<a href="https://eas.patents.su/6-1003-sposob-ingibirovaniya-ingibitora-1-aktivatora-plazminogena.html" rel="bookmark" title="База патентов Евразийского Союза">Способ ингибирования ингибитора 1 активатора плазминогена.</a>
Предыдущий патент: Замещенные тетрациклические производные тетрагидрофурана
Следующий патент: Конденсированные производные имидазола в качестве модуляторов множественной лекарственной устойчивости
Случайный патент: Производные бензазола и их применение в качестве модуляторов jnk










