Способ превращения пептидов класса эхинокандина в их с4-гомотирозиновые монодезокси-аналоги
Номер патента: 2909
Опубликовано: 31.10.2002
Авторы: Мукхопадхиаи Триптикумар, Кумар Ерра Котесвара Сатия Вийая, Яиванти Кения
Формула / Реферат
1. Способ превращения пептидов класса эхинокандина формулы
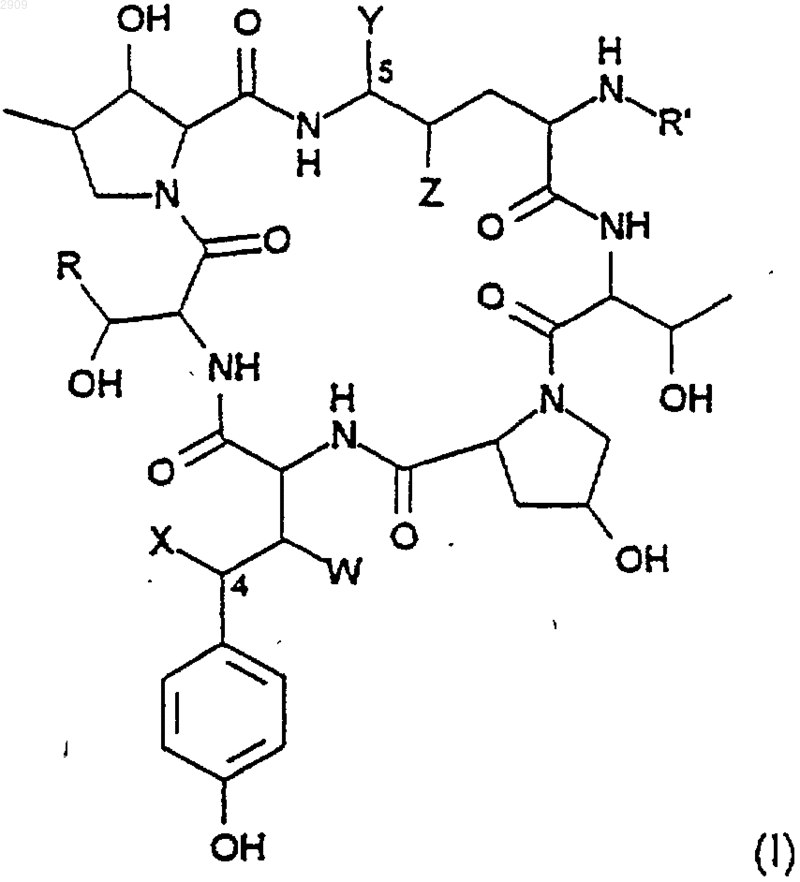
в которой W, X, Y, Z, R и R' имеют значения, определенные ниже
| W | Х | Y | ||
| 1. | Эхинокандин В | ОН | ОН | OH |
| 2. | Пневмокандин А0 | ОН | ОН | OH |
| 3. | Пневмокандин A1 | Н | ОН | OH |
| 4. | Пневмокандин А2 | ОН | OH | Н |
| 5. | Пневмокандин В0 | ОН | OH | OH |
| 6. | Пневмокандин B2 | ОН | OH | Н |
| 7. | Пневмокандин С0 | ОН | OH | OH |
| 8. | Мулундокандин | ОН | OH | OH |
| Z | R | R' | |
| 1. | OH | СН3 | Линолеоил |
| 2. | OH | CH2-CONH2 | 10,12-Диметил-миристоил |
| 3. | OH | CH2-CONH2 | " |
| 4. | Н | CH2-CONH2 | " |
| 5. | OH | CH2-CONH2 | " |
| 6. | Н | CH2-CONH2 | " |
| 7. | OH | CH2-CONH2 | " |
| 8. | OH | Н | 12-Метил-тетрадеканоил |
в их С4-гомотирозиновые монодезокси-аналоги формулы I, в которой W, X, Y, Z, R и R' имеют следующие ниже значения
| W | X | Y | ||
| 1. | Дезоксиэхинокандин В. (Эхинокандин С) | ОН | Н | ОН |
| 2. | Дезоксипневмокандин Ао | ОН | Н | OH |
| 3. | Дезоксипневмокандин A1 | Н | Н | OH |
| 4. | Дезоксипневмокандин A2 | ОН | Н | Н |
| 5. | Дезоксипневмокандин Во | ОН | Н | OH |
| 6. | Дезоксипневмокандин В2 | ОН | Н | Н |
| 7. | Дезоксипневмокандин Со | ОН | Н | OH |
| 8. | Дезоксимулундокандин | ОН | Н | OH |
| Z | R | R' | |
| 1. | OH | СН3 | Линолеоил |
| 2. | OH | СН2-СОNН2 | 10,12-Диметилмиристоил |
| 3. | OH | CH2-CONH2 | " |
| 4. | Н | CH2-CONH2 | " |
| 5. | OH | CH2-CONH2 | " |
| 6. | Н | CH2-CONH2 | " |
| 7. | OH | CH2-CONH2 | " |
| 8. | OH | Н | 12-Метилтетрадеканоил |
который включает одностадийное селективное восстановление гидроксильной группы C4-hTyr (гомотирозина) эхинокандинов в их монодезокси-аналоги в нейтральных условиях без предварительной защиты/удаления защиты в равной степени доступной гидроксильной группы С5-Orn (орнитина) и выделение очищенного монодезокси-соединения из сырой реакционной смеси.
2. Способ по п.1, в котором мулундокандин превращают в дезоксимулундокандин.
3. Способ по п.1 или 2, в котором реакцию восстановления осуществляют с помощью гидрогенолиза с никелем Ренея в этаноле при рН 7 и комнатной температуре.
4. Способ по пп.1-3, в котором гидрогенолиз осуществляют при соотношении 6,8 мл никеля Ренея на миллимоль мулундокандина.
Текст
Данное изобретение относится к способу превращения пептидов класса эхинокандина формулы I особенно к способу превращения мулундокандина (соединения формулы II) Ингибиторы синтеза 1,3 глюкана являются эффективными противогрибковыми агентами против Candida albicans, а также Pneumocystis carini, условно-патогенного организма,ответственного за часто фатальный пневмонит(пульмонит) у ВИЧ-инфицированных пациентов и других иммунологически "скомпрометированных" (т.е. обладающих недостаточным иммунитетом вследствие иммунодефицитного заболевания или действия иммуносупрессоров) носителей. Из всех структурных классов ингибиторов синтеза 1,3 глюкана только эхинокандины привлекли значительное внимание[см.: J. Med. Chem. 35, 198-200 (1992)]. Пептиды класса эхинокандина являются циклическими гексапептидами, имеющими липофильную боковую цепь. Опубликовано несколько способов превращения эхинокандинов в соответствующие дезокси-аналоги в кислотных условиях [см.:Tetrahedron Letts., 33, 4529-4532 (1992); патентная заявка США 222157, датированная 4 апреля 1994]. Указанные способы предусматривают селективное восстановление гидроксильной группы C4-hTyr (гомотирозина) эхинокандинов в их монодезокси-аналоги с предварительной защитой/удалением в равной степени доступной гидроксильной группы С 5-Orn (орнитина). Мулундокандин [J. Antibiotics, 40, 275-280 и 281-289 (1987)] и дезоксимулундокандин [патент ИндииIN 169830; J. Antibiotics, 45, 618623 (1992)], имеющие противогрибковые свойства, были выделены из Aspergillus sydowiiMulundensis Roy (культура no. HIL Y-30462). Обнаружено, что дезоксимулундокандин обладает лучшей противогрибковой активностью,чем мулундокандин. Однако продуцирование дезоксимулундокандина во время ферментации является в 200 раз меньшим, чем мулундокандина. Путем обширного исследования и экспериментирования обнаружено, что пептиды класса эхинокандина формулы I могут превращаться в соответствующие C4-hTyr монодезоксианалоги, в частности мулундокандин в дезоксимулундокандин, в нейтральных условиях. Соответственно целью данного изобретения является предоставление способа превращения пептидов класса эхинокандина формулы I в соответствующие С 4-гомотирозиновые монодезоксианалоги, особенно мулундокандина (соединения формулы II) в дезоксимулундокандин (соединение формулы III). Согласно изобретению, предоставляется способ превращения пептидов класса эхинокандина формулы IW Х Y Z 1. Эхинокандин В ОН ОН ОН ОН 2. Пневмокандин А 0 ОН ОН ОН OH 5. Пневмокандин В 0 ОН ОН ОН OH 6. Пневмокандин В 2 ОН ОН Н 7. Пневмокандин С 0 ОН ОН OH OH 8. Мулундокандин ОН ОН OH OH в их С 4-гомотирозиновые монодезоксианалоги формулы I, в которой W, X, Y, Z, R и R' имеют следующие ниже значения: особенно, способ превращения мулундокандина (соединения формулы II) который предусматривает одностадийное селективное восстановление гидроксильной группыC4-hTyr (гомотирозина) эхинокандинов в их монодезокси-аналоги, в особенности в нейтральных условиях, без предварительной защиты/удаления защиты в равной степени доступной гидроксильной группы С 5-Orn (орнитина) и выделение очищенного монодезоксисоединения из сырой реакционной смеси. Превращение эхинокандинов в их монодезокси-аналоги с помощью селективного восстановления C4-hTyr может проводиться с помощью гидрогенолиза с никелем Ренея в растворителях, таких как метанол, этанол или диоксан,при рН 3-9. Предпочтительно, селективное восстановление осуществляют путем гидрогенолиза с никелем Ренея в этаноле при рН 7 и комнатной температуре при соотношении 6,8 мл никеля Ренея на миллимоль мулундокандина. Очищенные монодезокси-соединения изобретения могут, например, быть выделены из сырой реакционной смеси следующим образом: С помощью фракционирования с использованием хроматографии с нормальной фазой (с использованием глинозема (оксида алюминия) или силикагеля в качестве стационарной фазы и таких элюентов, как петролейный эфир, этилацетат, дихлорметан, хлороформ, метанол или их сочетания), хроматографии с обращенной фазой (с использованием силикагеля обращенной фазы, подобного диметилоктадецилсилилсиликагелю, также называемому RP-18, или диметилоктилсилилсиликагелю, также называемому RP-8, в качестве стационарной фазы и элюентов, таких как вода, буферы, такие как фосфатный, ацетатный, нитратный (рН 2-8) и органические растворители, такие как метанол,ацетонитрил, ацетон, тетрагидрофуран или сочетания растворителей), гель-проникающей хроматографии - с использованием смол, таких как "Sephadex LH-20" (Pharmacia Chemical Industries, Швеция), TSKgel Toyopearl HW (TosoHaas, Tosoh Corporation, Япония), в растворителях, таких как метанол, хлороформ или этилацетат или их сочетания, или Sephadex G-10 иSephadex G-25 в воде; или с помощью противоточной хроматографии с использованием двухфазной элюирующей системы из вплоть до двух или более растворителей, таких как вода, метанол, этанол, изопропанол, н-пропанол, тетрагидрофуран, ацетон, ацетонитрил, метиленхлорид, хлороформ, этилацетат, петролейный эфир,бензол и толуол. Эти приемы могут использоваться повторно или могут использоваться сочетания различных приемов. Противоточная хро 5 матография (жидкость-жидкостная хроматография) с использованием двухфазной элюирующей системы на змеевике ITO предпочтительна для очистки соединений изобретения. Следующий экспериментальный пример является иллюстрацией данного изобретения и не ограничивает его объем. Пример 1. Мулундокандин (220 мг, 2,2 мМ) в этаноле(8 мл) перемешивают с 15 мл никеля Ренея W-2(рН 7) в этаноле (30 мл) в течение 3 ч при комнатной температуре. После отстаивания в течение 15 мин раствор супернатанта декантируют и никель Ренея промывают этанолом 3 х 30 мл при перемешивании и фильтруют. Объединенные этанольные растворы концентрируют перегонкой при пониженном давлении 60-70 мм/Hg при 35 С, получая 160 мг (75%) сырого дезоксимулундокандина в виде слегка зеленого твердого вещества. Сырой продукт очищают с помощью жидкость-жидкостной хроматографии на змеевикеITO с использованием верхнего слоя СН 2 Сl2:МеОН:n-РrОН:Н 2 О в качестве стационарной фазы и нижнего слоя в качестве подвижной фазы восходящим образом. Змеевики(15 + 25 + 215 мл) соединяют последовательно и поддерживают скорость потока 0,6 мл/мин при величине хода поршня 60 и давлении 0,5 бар. За очисткой дезоксимулундокандина следят по биоактивности против Candida albicans и Aspergillus niqer и с помощью аналитической жидкостной хроматографии высокого давленияCH3CN:H2O; скорость потока: 1 мл/мин; длина волны: 220 нм]. Фракции (4,5 мл каждая), содержащие дезоксимулундокандин, объединяют,концентрируют с помощью перегонки при пониженном давлении 60-70 мм/Нg при 35 С и лиофилизуют, получая чистый дезоксимулундокандин [65 мг (выход 30%)]. Во время указанной очистки дезоксимулундокандина выделяют также непрореагировавший мулундокандин с выходом 10%. Полусинтетический дезоксимулундокандин идентичен во всех отношениях природно выделенному соединению, и физикохимические данные приведены в табл. 1. Внешний вид Температура плавления 6 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ превращения пептидов класса эхинокандина формулыW Х Y Z 1. Эхинокандин В ОН ОН ОН ОН 2. Пневмокандин А 0 ОН ОН ОН OH 3. Пневмокандин A1 Н ОН ОН OH 4. Пневмокандин А 2 ОН ОН Н 5. Пневмокандин В 0 ОН ОН ОН OH 6. Пневмокандин В 2 ОН ОН Н 7. Пневмокандин С 0 ОН ОН OH OH 8. Мулундокандин ОН ОН OH OH в их С 4-гомотирозиновые монодезокси-аналоги формулы I, в которой W, X, Y, Z, R и R' имеют следующие ниже значения который включает одностадийное селективное восстановление гидроксильной группы C4-hTyr(гомотирозина) эхинокандинов в их монодезокси-аналоги в нейтральных условиях без предварительной защиты/удаления защиты в равной степени доступной гидроксильной группы С 5Orn (орнитина) и выделение очищенного монодезокси-соединения из сырой реакционной смеси. 2. Способ по п.1, в котором мулундокандин превращают в дезоксимулундокандин. 3. Способ по п.1 или 2, в котором реакцию восстановления осуществляют с помощью гидрогенолиза с никелем Ренея в этаноле при рН 7 и комнатной температуре. 8 4. Способ по пп.1-3, в котором гидрогенолиз осуществляют при соотношении 6,8 мл никеля Ренея на миллимоль мулундокандина.
МПК / Метки
МПК: C07K 7/56, A61K 38/12, A61P 31/00
Метки: с4-гомотирозиновые, способ, монодезокси-аналоги, превращения, класса, пептидов, эхинокандина
Код ссылки
<a href="https://eas.patents.su/5-2909-sposob-prevrashheniya-peptidov-klassa-ehinokandina-v-ih-s4-gomotirozinovye-monodezoksi-analogi.html" rel="bookmark" title="База патентов Евразийского Союза">Способ превращения пептидов класса эхинокандина в их с4-гомотирозиновые монодезокси-аналоги</a>
Предыдущий патент: Фармацевтические композиции на основе тизоксанида и нитазоксанида
Следующий патент: Новые порфирины и их применение
Случайный патент: Усовершенствованное интермодальное рельсовое транспортное средство для образования состава









