Способ получения нитробифенилов
Номер патента: 1071
Опубликовано: 30.10.2000
Авторы: Рак Михаель, Айкен Карл, Шэфер Петер, Ранг Харальд, Гебхардт Иоахим
Формула / Реферат
1. Способ получения нитробифенилов формулы I
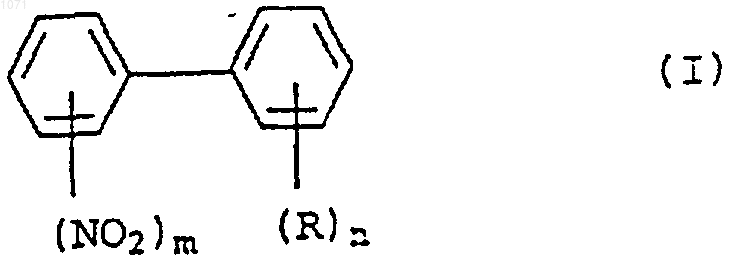
в которой m обозначает 1 или 2, R обозначает галоген, R' или OR', где R' представляет собой С-органический радикал, который в условиях реакции может нести инертные группы, причем n обозначает 0, 1, 2 или 3, а при значении n, равном 2 или 3, радикалы R могут быть также разными, отличающийся тем, что хлорнитробензол формулы II

в присутствии основания и палладиевого катализатора, выбранного из группы, включающей: а) комплекс палладий-триарилфосфан с палладием, степень окисления которого равна 0, б) соль палладия в присутствии триарилфосфана в качестве комплексного лиганда или в) при необходимости нанесенный на носитель металлический палладий, в присутствии триарилфосфана подвергают в растворителе взаимодействию с фенилборной кислотой формулы IIIa

одним из ее алкиловых эфиров формулы IIIb, где R1 обозначает С1-С6алкил, или одним из ее ангидридов.
2. Способ по п.1, отличающийся тем, что в качестве соединения формулы II применяют 2-нитрохлорбензол.
3. Способ по п.1, отличающийся тем, что исходят из фенилборной кислоты, замещенной только в положении 4, в качестве соединения формулы IIIa и 2-хлорнитробензола в качестве соединения формулы II.
4. Способ по пп.1-3, отличающийся тем, что применяют фенилборную кислоту формулы IIIa, несущую в качестве единственного заместителя в положении 4 фтор, хлор или метильную группу.
5. Способ по пп.1-4, отличающийся тем, что исходят из 4-хлорфенилборной кислоты в качестве соединения формулы IIIa.
6. Способ по пп.1-5, отличающийся тем, что в качестве палладиевого катализатора а) по п.1 применяют тетракис(трифенилфосфан) палладий.
7. Способ по пп.1-5, отличающийся тем, что применяют палладиевый катализатор б) по п.1.
8. Способ по пп.1-5, отличающийся тем, что в качестве палладиевого катализатора в) по п.1 применяют металлический палладий на активированном угле в присутствии трифенилфосфана, фенильные группы которого замещены в общей сложности 1-3 сульфонатными группами.
Текст
1 Настоящее изобретение относится к способу получения нитробифенилов формулы I в которой m обозначает 1 или 2, R обозначает галоген, R' или OR', где R' представляет собой С-органический радикал, который в условиях реакции может нести инертные группы, где n обозначает 0,1, 2 или 3, а при значении n, равном 2 или 3, радикалы R могут быть также разными. Способ отличается тем, что хлорнитробензол формулы II 2 циклогексил и 1-метилциклогексил; а также фенильные и феноксигруппы. К инертным в условиях реакции заместителям С-органических радикалов R' относятся предпочтительно галоген, равно как и алкильные и алкоксильные группы. Среди других С-органических радикалов(-СНО). В составе ангидридов представлены обычно продукты соединения двух или нескольких эквивалентов фенилборной кислоты IIIa при выделении воды, содержащих межмолекулярные В-O-В-мостики. Предпочтительными являются ангидриды формулы IIIc. в присутствии палладиевого катализатора и основания подвергают в растворителе взаимодействию с фенилборной кислотой (IIIa) одним из ее алкиловых эфиров формулы IIIb,где R1 обозначает С 1-С 6 алкил, или одним из ее ангидридов. Из Synth. Commun. 11, с. 513 (1981) известно, что реакцией сочетания фенилборной кислоты с хлорбензолом в присутствии тетракис(трифенилфосфан)палладия и метанолята натрия невозможно получить бифенил. В Tetrahedron Lett. 32, с. 2277 (1991) указывается, что реакция сочетания между фенилборной кислотой и хлорбензолом при использовании катализатора дихлорида [1,4-бис(дифенилфосфан)бутан]палладия(II) дает выход лишь 28%. Исходя из вышеизложенного, в основу изобретения была положена задача разработать экономичный способ получения нитробифенилов, который можно осуществлять с помощью широко доступных палладиевых катализаторов. В соответствии с этой задачей был создан представленный выше способ. Фенилборные кислоты IIIa, их эфиры IIIb и ангидриды, как, например, формулы IIIc, обозначаемые в последующем общим понятием"соединения бора формулы III", общеизвестны либо могут быть получены по известной методике (ср., например, Org. Synth. Coll. том IV,стр. 68). Предпочтительными С-органическими радикалами R' являются следующие:- циклоалкильные группы, прежде всего с 3-10 атомами углерода, такие как циклопентил, В последующем следует учитывать, что указанные количества касательно соединений бора формулы III всегда относятся к эквивалентам фенилборной кислоты. В принципе возможно применение алкиловых эфиров формулы IIIb, в которой R1 обозначает С 1-С 6 алкил. Предпочтительными алкиловыми эфирами IIIb являются диметиловые и диэтиловые эфиры. При осуществлении способа по изобретению предпочтительно исходить из фенилборных кислот IIIa. Другая предпочтительная возможность состоит в том, что исходят из соединений бора формулы III, в которых R представляет собой С 1-С 4 алкильную группу или галоген и прежде всего метил, фтор или хлор. Кроме вышеназванных, в качестве исходного материала предпочтительны соединения бора формулы III, в которых n имеет значение,равное 1, и прежде всего равное 0. К наиболее предпочтительным в качестве исходного соединения IIIa относятся 4 метилфенилборная кислота, 4-фторфенилборная кислота и прежде всего 4-хлорфенилборная кислота. Предпочтительно исходить из нитрохлорбензолов формулы II, которые несут одну единственную нитрогруппу (m=1), в частности 4 нитрохлорбензол и прежде всего 2 нитрохлорбензол. Соединения бора формулы III (эквиваленты фенилборной кислоты) применяют по отношению к соединениям II обычно с избытком до 50%-ного, предпочтительно до 20%-ного и особенно предпочтительно в эквимолярных количествах. В качестве основания могут применяться органические основания, как, например, третич 3 ные амины. Предпочтительное применение находит, например, триэтиламин или диметилциклогексиламин. В качестве основания применяют предпочтительно гидроксиды щелочных металлов, гидроксиды щелочно-земельных металлов, карбонаты щелочных металлов, карбонаты щелочноземельных металлов, гидрокарбонаты щелочных металлов, ацетаты щелочных металлов,ацетаты щелочно-земельных металлов, алкоголяты щелочных металлов и алкоголяты щелочно-земельных металлов, используют их смеси и прежде всего индивидуальные основания. Особенно предпочтительны в качестве основания из числа вышеназванных гидроксиды щелочных металлов, гидроксиды щелочноземельных металлов, карбонаты щелочных металлов, карбонаты щелочно-земельных металлов и гидрокарбонаты щелочных металлов. К наиболее предпочтительным в качестве основания относятся гидроксиды щелочных металлов,например, гидроксид натрия и гидроксид калия,а также карбонаты щелочных металлов и гидрокарбонаты щелочных металлов, как, например,карбонат лития, карбонат натрия и карбонат калия. В способе по изобретению основание применяют предпочтительно в количестве от 100 до 500, особенно предпочтительно от 150 до 400 мол.% в пересчете на соединение бора формулыIII. Пригодными для использования палладиевыми катализаторами являются палладиевые лигандные комплексы с палладием, степень окисления которого равна 0, соли палладия в присутствии комплексных лигандов или при необходимости нанесенный на носитель металлический палладий, предпочтительно в присутствии комплексных лигандов. Приемлемые комплексные лиганды представляют собой нейтральные лиганды, такие как триарилфосфаны, которые в арильных кольцах необязательно могут быть замещены. Водорастворимость палладиевых комплексов можно улучшить за счет заместителей из числа следующих: солевые группы сульфокислот, группы сульфокислот, солевые группы карбоновых кислот, группы карбоновых кислот, солевые группы фосфоновых кислот, группы фосфоновых кислот, фосфониевые группы, пералкиламмониевые группы, гидроксильные группы и полиэфирные группы. Из числа палладиевых лигандных комплексов с палладием, степень окисления которого равна 0, используют предпочтительно тетракис(трифенилфосфан) палладий, а также тетракис [три (о-толил)фосфан] палладий. В солях палладия, используемых в присутствии комплексных лигандов, палладий представлен обычно со степенью окисления, равной двум положительным зарядам. Предпочтитель 001071 4 но использование ацетата палладия или хлорида палладия. Как правило, применяют сочетание 2-6 эквивалентов вышеназванных комплексных лигандов, прежде всего трифенилфосфана, в сочетании с одним эквивалентом палладиевой соли(1984. В остальном растворимые палладиевые комплексы такого типа общеизвестны (ср., например, Angew. Chem. 105, с. 1589 (1993 и поэтому не требуют каких-либо дальнейших пояснений. Металлический палладий применяют предпочтительно в порошкообразной форме либо нанесенным на соответствующий носитель, как, например, палладий на активированном угле, палладий на оксиде алюминия, палладий на карбонате бария, палладий на сульфате бария, палладий на карбонате кальция, палладий на силикатах алюминия, такой как монтморрилонит, палладий на SiO2 и палладий на карбонате кальция, соответственно с содержанием палладия в каждом случае от 0,5 до 12 мас.%. Все эти катализаторы наряду с палладием и носителем могут содержать также другие добавки, например свинец. При применении нанесенного при необходимости на носитель металлического палладия особенно предпочтительно использовать его совместно с вышеназванными комплексными лигандами, в частности, в случае палладия на активированном угле - в присутствии трифенилфосфана в качестве такого комплексного лиганда, причем фенильные группы в составе трифенилфосфана предпочтительно замещены в общей сложности одной-тремя сульфонатными группами. Как правило, применяют 2-3 эквивалента вышеназванных комплексных лигандов на эквивалент металлического палладия. Палладиевый катализатор в способе по изобретению применяют в количестве от 0,01 до 10, предпочтительно от 0,05 до 5 и прежде всего от 0,1 до 3 мол.% в пересчете на соединение II. Предлагаемый согласно изобретению способ можно осуществлять по двухфазному механизму, включающему водную фазу и твердую фазу, т.е. катализатор. Водная фаза при этом может содержать помимо воды также водорастворимый органический растворитель. Пригодными для использования в способе по изобретению органическими растворителями являются среди прочих простые эфиры, например, диметоксиэтан, диметиловый эфир диэтиленгликоля,тетрагидрофуран, диоксан и трет-бутилметиловый эфир, углеводороды, например гексан,гептан, циклогексан, бензол, толуол и ксилол,спирты, например, метанол, этанол, 1-пропанол,2-пропанол, этиленгликоль, 1-бутанол, 2 бутанол и трет-бутанол, кетоны, например, ацетон, этилметилкетон и изобутилметилкетон,амиды, например, диметилформамид, диметилацетамид и N-метилпирролидон, применяемые 5 соответственно индивидуально либо в смесях друг с другом. Предпочтительны из названных растворителей простые эфиры, например диметоксиэтан и тетрагидрофуран, углеводороды,например, циклогексан, толуол и ксилол, спирты, например, этанол, 1-пропанол, 2-пропанол,1-бутанол и трет-бутанол, применяемые соответственно индивидуально либо в смесях друг с другом. Согласно одному из особенно предпочтительных вариантов в способе по изобретению применяют воду, один или несколько нерастворимых в воде и один или несколько водорастворимых растворителя, например, смеси из воды,толуола и этанола или из воды, толуола и тетрагидрофурана, предпочтительно в каждом случае в объемном соотношении 1:2:1. Общее количество растворителя составляет обычно от 3000 до 500 и прежде всего от 2000 до 700 г на моль соединения II. Для осуществления способа по изобретению соединение формулы II, соединение бора формулы III, основание, а также каталитическое количество палладиевого катализатора целесообразно вводить в смесь из воды и одного или нескольких инертных органических растворителей и перемешивать при температуре в интервале от 0 до 150C, предпочтительно от 30 до 120 С в течение 1-50 ч, предпочтительно 2-24 ч. Способ может проводиться в обычных для таких способов аппаратах и поэтому нет необходимости в дальнейших пояснениях. По завершении реакции образующийся в виде твердого вещества палладиевый катализатор отделяют, например, путем фильтрации, и из сырого продукта удаляют растворитель, соответственно растворители. В случае неполностью водорастворимых продуктов водорастворимые палладиевые катализаторы или комплексные лиганды при отделении водной фазы следует полностью удалять из сырого продукта. Затем по известным специалисту и в соответствии с особенностями получаемого продукта методам, таким, например, как перекристаллизация, дистилляция, сублимация, зонный расплав,кристаллизация из расплава или хроматография,может проводиться последующая очистка. Образовавшийся по завершении реакции в виде твердого вещества катализатор можно, как правило, простым путем выделять, регенерировать и возвращать в процесс, благодаря чему снижаются расходы на технологические операции и количество содержащих палладий отходов. С помощью способа по изобретению могут быть получены, например, следующие соединения: 4'-фтор-2-нитробифенил, 4'-метил-2-нитробифенил, 4'-метокси-2-нитробифенил, 4'-бром-2 нитробифенил, 3'-фтор-2-нитробифенил, 3'хлор-2-нитробифенил, 3'-бром-2-нитробифенил,3'-метил-2-нитробифенил, 3'-метокси-2-нитробифенил, 4'-фенил-2-нитробифенил, 4'-трифтор 001071 6 метил-2-нитробифенил,4'-фтор-4-нитробифенил, 4'-хлор-4-нитробифенил, 4'-бром-4-нитробифенил, 4'-метил-4-нитробифенил, 4'-циано-4 нитробифенил, 2-нитробифенил, 4-нитробифенил. Предлагаемый согласно изобретению способ обеспечивает получение соединений формулы I с высоким выходом и высокой степенью чистоты. Получаемые по способу согласно изобретению нитробифенилы пригодны в качестве форпродуктов для бифениламинов, представляющих собой, в свою очередь, промежуточные продукты для получения фунгицидных действующих веществ, предназначенных для защиты растений (см. европейскую заявку ЕР 545099). Синтез 4'-xлop-2-нитpoбифeнилa. Пример 1. К раствору из 9,45 г 2-нитрохлорбензола и 10,3 г 4-хлорфенилборной кислоты в 60 мл тетрагидрофурана добавляли при перемешивании и в атмосфере азота раствор из 9,6 г гидроксида натрия в 60 мл воды. Затем смесь смешивали с 70 мг ацетата палладия (II) и 370 мг трифенилфосфана. Смесь при перемешивании кипятили с обратным холодильником (70 С) до тех пор,пока весь 2-нитрохлорбензол не прореагировал(приблизительно 8 ч). После охлаждения реакционную смесь смешивали с 80 мл воды и 80 мл трет-бутилметилового эфира и органическую фазу отделяли. После фильтрации через 10 г силикагеля и выпаривания растворителя получили 13,95 г указанного в заголовке соединения чистотой 95% (ГХ). Пример 2. К раствору из 4,7 г 2-нитрохлорбензола и 5,6 г 4-хлорфенилборной кислоты в 30 мл 1,2 диметоксиэтана при перемешивании и в атмосфере азота добавляли раствор из 8 г карбоната натрия в 30 мл воды. Затем смесь смешивали с 320 мг палладия на активированном угле (10 мас.%) и 320 мг трифенилфосфана. Далее смесь при перемешивании кипятили с обратным холодильником до тех пор, пока весь 2 нитрохлорбензол не прореагировал (приблизительно 22 ч). После охлаждения реакционную смесь смешивали с 50 мл воды и 50 мл третбутилметилового эфира и органическую фазу отделяли. После фильтрации и выпаривания растворителя получили 6,7 г указанного в заголовке соединения чистотой 92,7% (ГХ). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ формулы I реакции может нести инертные группы, причемn обозначает 0, 1, 2 или 3, а при значении n,равном 2 или 3, радикалы R могут быть также разными, отличающийся тем, что хлорнитробензол формулы II в присутствии основания и палладиевого катализатора, выбранного из группы, включающей: а) комплекс палладий-триарилфосфан с палладием, степень окисления которого равна 0, б) соль палладия в присутствии триарилфосфана в качестве комплексного лиганда или в) при необходимости нанесенный на носитель металлический палладий, в присутствии триарилфосфана подвергают в растворителе взаимодействию с фенилборной кислотой формулы IIIa одним из ее алкиловых эфиров формулы IIIb,где R1 обозначает С 1-С 6 алкил, или одним из ее ангидридов. 2. Способ по п.1, отличающийся тем, что в качестве соединения формулы II применяют 2 нитрохлорбензол. 8 3. Способ по п.1, отличающийся тем, что исходят из фенилборной кислоты, замещенной только в положении 4, в качестве соединения формулы IIIa и 2-хлорнитробензола в качестве соединения формулы II. 4. Способ по пп.1-3, отличающийся тем,что применяют фенилборную кислоту формулыIIIa, несущую в качестве единственного заместителя в положении 4 фтор, хлор или метильную группу. 5. Способ по пп.1-4, отличающийся тем,что исходят из 4-хлорфенилборной кислоты в качестве соединения формулы IIIa. 6. Способ по пп.1-5, отличающийся тем,что в качестве палладиевого катализатора а) по п.1 применяют тетракис(трифенилфосфан) палладий. 7. Способ по пп.1-5, отличающийся тем,что применяют палладиевый катализатор б) по п.1. 8. Способ по пп.1-5, отличающийся тем,что в качестве палладиевого катализатора в) по п.1 применяют металлический палладий на активированном угле в присутствии трифенилфосфана, фенильные группы которого замещены в общей сложности 1-3 сульфонатными группами.
МПК / Метки
МПК: C07C 205/12, C07B 37/04
Метки: получения, способ, нитробифенилов
Код ссылки
<a href="https://eas.patents.su/5-1071-sposob-polucheniya-nitrobifenilov.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения нитробифенилов</a>
Предыдущий патент: Электростимулятор желудочно-кишечного тракта.
Следующий патент: Распределительный шкаф с системой тушения пожара
Случайный патент: Одоризатор газа









