Нафталинмочевины как усилители поглощения глюкозы
Номер патента: 6763
Опубликовано: 28.04.2006
Авторы: Скоу Стивен Р., Манчем Прасад, Спивак Уэйн, Ши Сонюйянь, Козловски Майкл Р., Лум Роберт Т.
Формула / Реферат
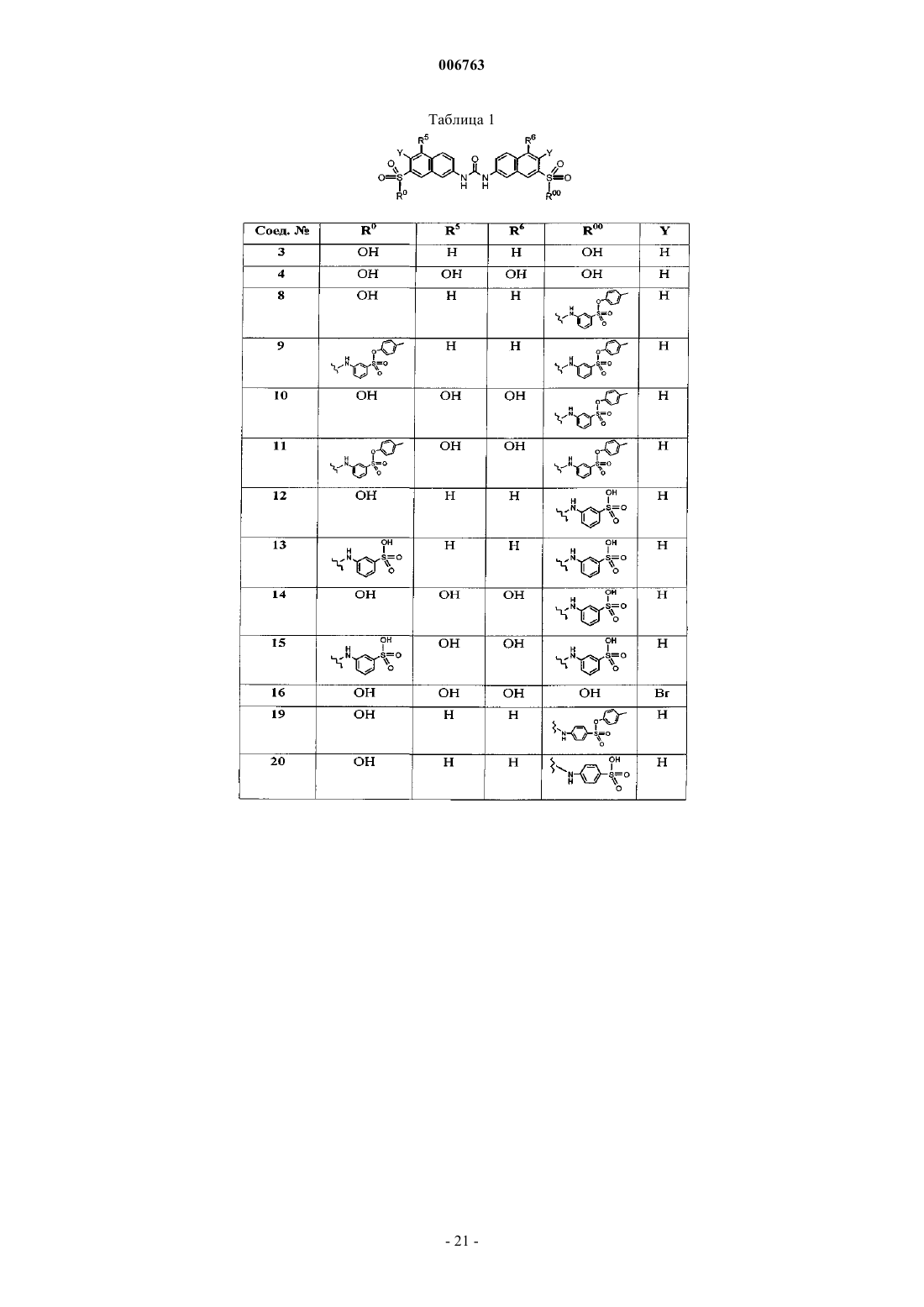
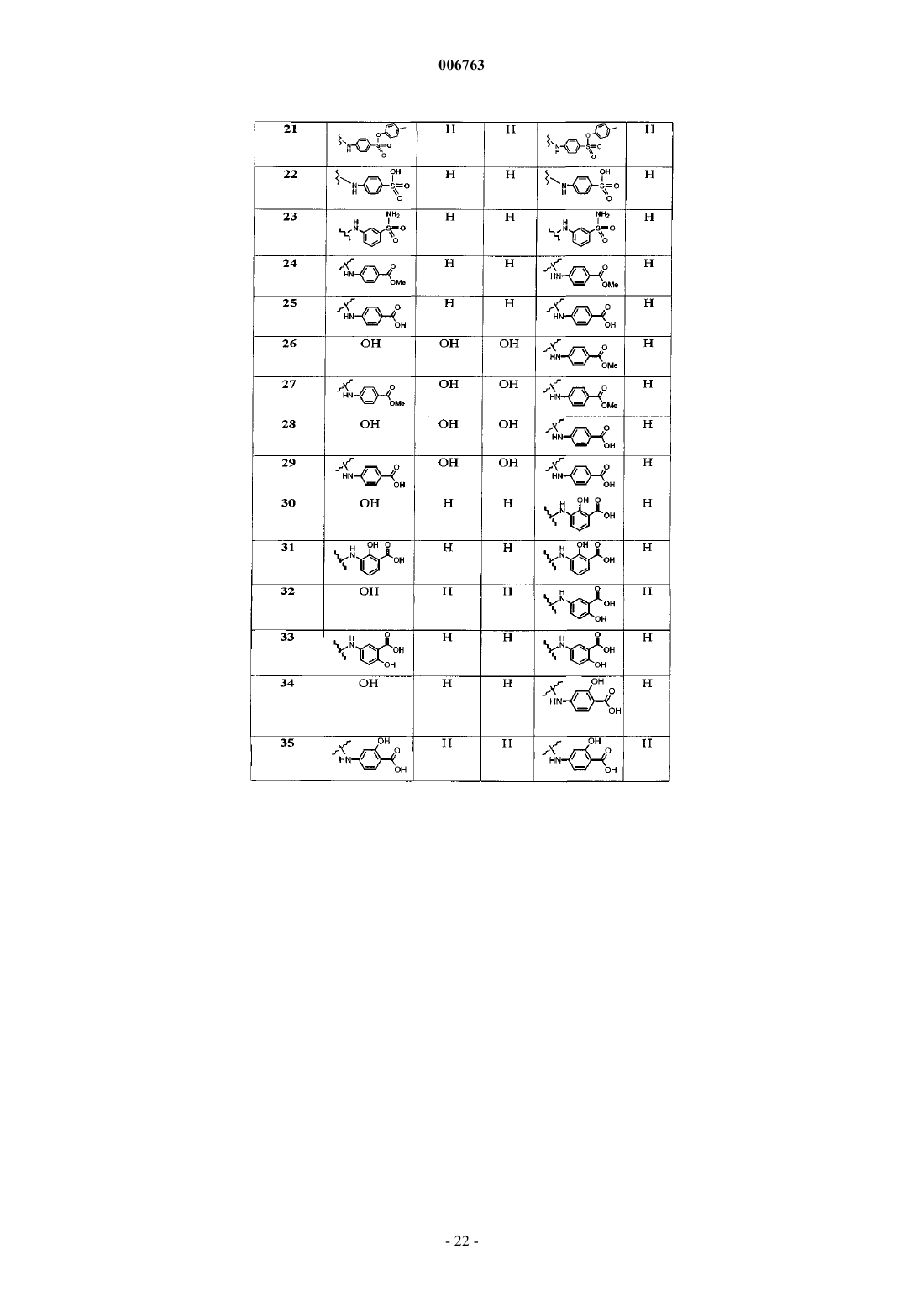
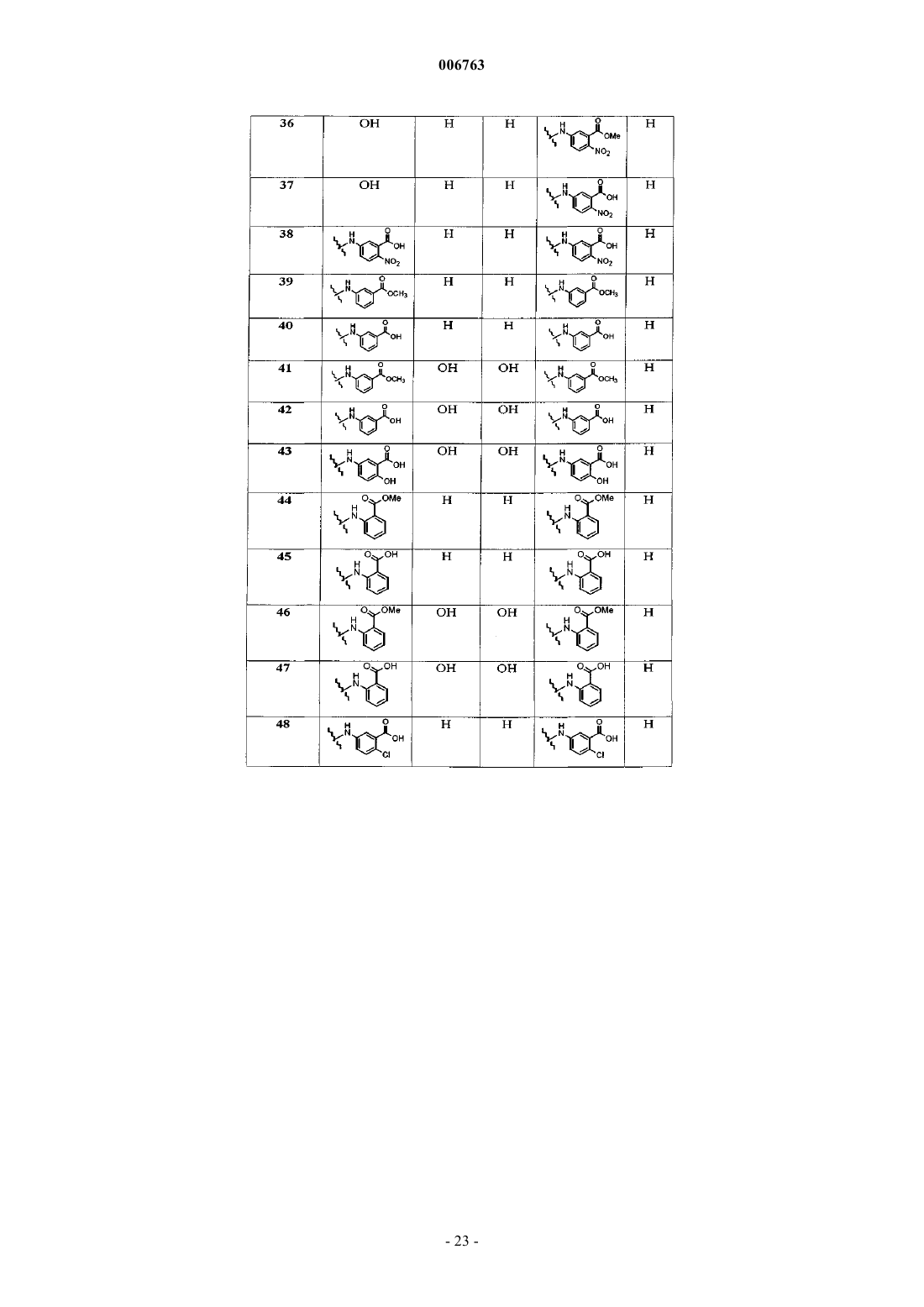
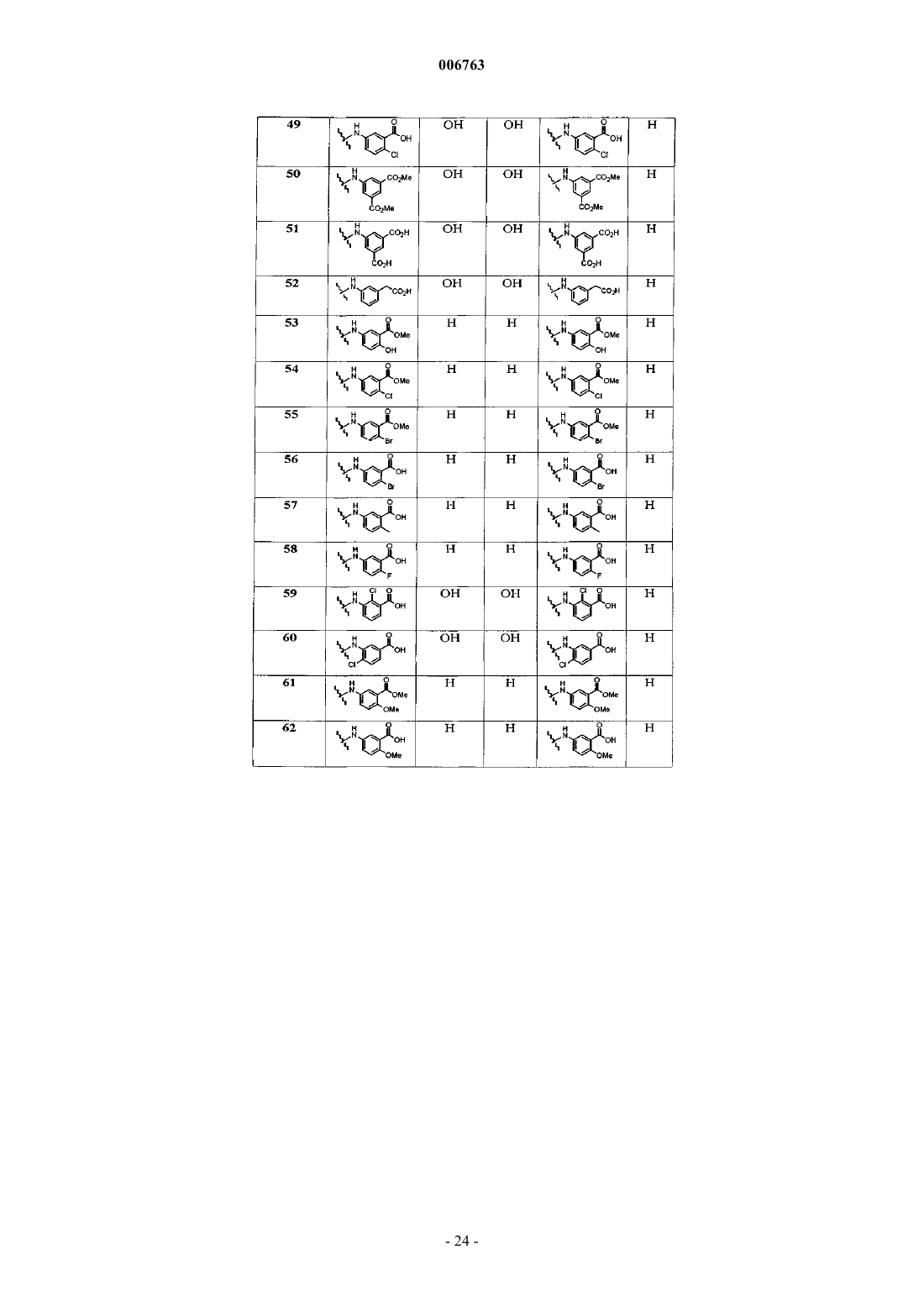
1. Соединение формулы
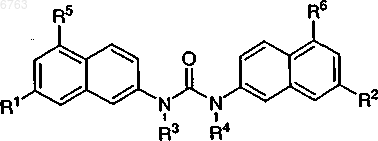
где R1 и R2 независимо друг от друга обозначают -SO2NR10R11, -C(O)NR10R11, -NR11SO2R10, -NR11C(O)R10, -SO2OR10 или C(O)OR10,
R3 и R4 означают независимо друг от друга водород или C1-С6алкил или R3 и R4 вместе означают
-(СН2)2-, -(СН2)3- или -(СН2)4-,
R5 и R6 означают независимо друг от друга водород, гидрокси или C1-С6алкокси, необязательно замещенный одной карбоксильной, (C1-С6алкокси)карбонильной, сульфо или финильной, замещенной сульфогруппой,
каждый R10 независимо означает пиридинил, пиримидинил, пиразинил или фенил, необязательно замещенный 1 или 2 заместителями, выбранными из гидрокси, гало, C1-С6алкил, гало-C1-С6алкил, C1-С6алкокси, -SO2OR11, C(O)OR11, -SO2NHR11, -C(O)NHR11, триазолил, тетразолил, гидроксиизоксазолил и -P(O)(OR11)(ОС1-6алкил), и дополнительно необязательно замещенный 1 или 2 галогенами,
каждый R11 независимо означает водород или C1-6алкил,
и где если R1 и R2 оба обозначают -SO2OH, то R5 и R6 не являются оба выбранными из группы, состоящей из водорода и гидроксила,
или их фармацевтически приемлемые соли в виде отдельных стереоизомеров или смесей стереоизомеров.
2. Соединение по п.1, которое является симметричным.
3. Соединение по п.1, где R1 и R2 независимо друг от друга обозначают -SO2NR10R11, -C(O)NR10R11, -NR11SO2R10 или -NR11C(O)R10.
4. Соединение по п.3, где R1 и R2 независимо друг от друга обозначают -SO2NHR10 или -NHSO2R10.
5. Соединение по п.4, где R1 и R2 оба вместе обозначают -SO2NHR10.
6. Соединение по п.5, где каждый R10 обозначает фенил, необязательно замещенный 1 или 2 заместителями, выбранными из гидрокси, гало, C1-С6алкил, гало-C1-С6алкил, C1-С6алкокси, -SO2OR11, C(O)OR11, -SO2NHR11, -C(O)NHR11, триазолил, тетразолил, гидроксиизоксазолил и -P(O)(OR11)(O-C1-6алкил), и дополнительно необязательно замещенный 1 или 2 галогенами.
7. Соединение по п.6, где каждый R10 обозначает фенил, необязательно замещенный 1 или 2 заместителями, выбранными из гидрокси, гало, -SO2OR11, C(O)OR11, -SO2NHR11, -C(O)NHR11, и дополнительно необязательно замещенный 1 или 2 галогенами.
8. Соединение по п.7, где каждый R10 обозначает фенил, замещенный одним заместителем, выбранным из -SO2OR11, C(O)OR11, -SO2NHR11, -C(O)NHR11, и одним заместителем, выбранным из хлора и гидроксила, в положении, соседнем с первым заместителем фенольного кольца.
9. Соединение по п.8, где каждый R10 обозначает фенил, замещенный одним заместителем, выбранным из -SO2OR11 и C(O)OR11, и одним заместителем, выбранным из хлора и гидроксила, в положении, соседнем с первым заместителем фенильного кольца.
10. Соединение по п.1, где R3 и R4 оба обозначают водород.
11. Соединение по п.1, где R5 и R6 оба обозначают водород или гидроксил.
12. Соединение по п.1, представляющее собой соединение формулы
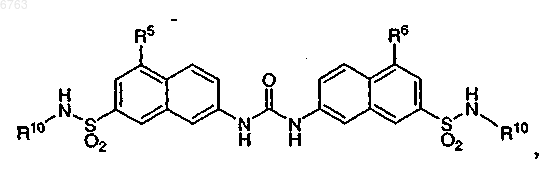
где R5 и R6 оба обозначают водород или оба обозначают гидроксил, а
R10 обозначает фенил, замещенный одним заместителем, выбранным из -SO2OR11 и C(O)OR11, и одним заместителем, выбранным из хлора и гидроксила, в положении, соседнем с первым заместителем фенильного кольца,
или их фармацевтически приемлемые соли.
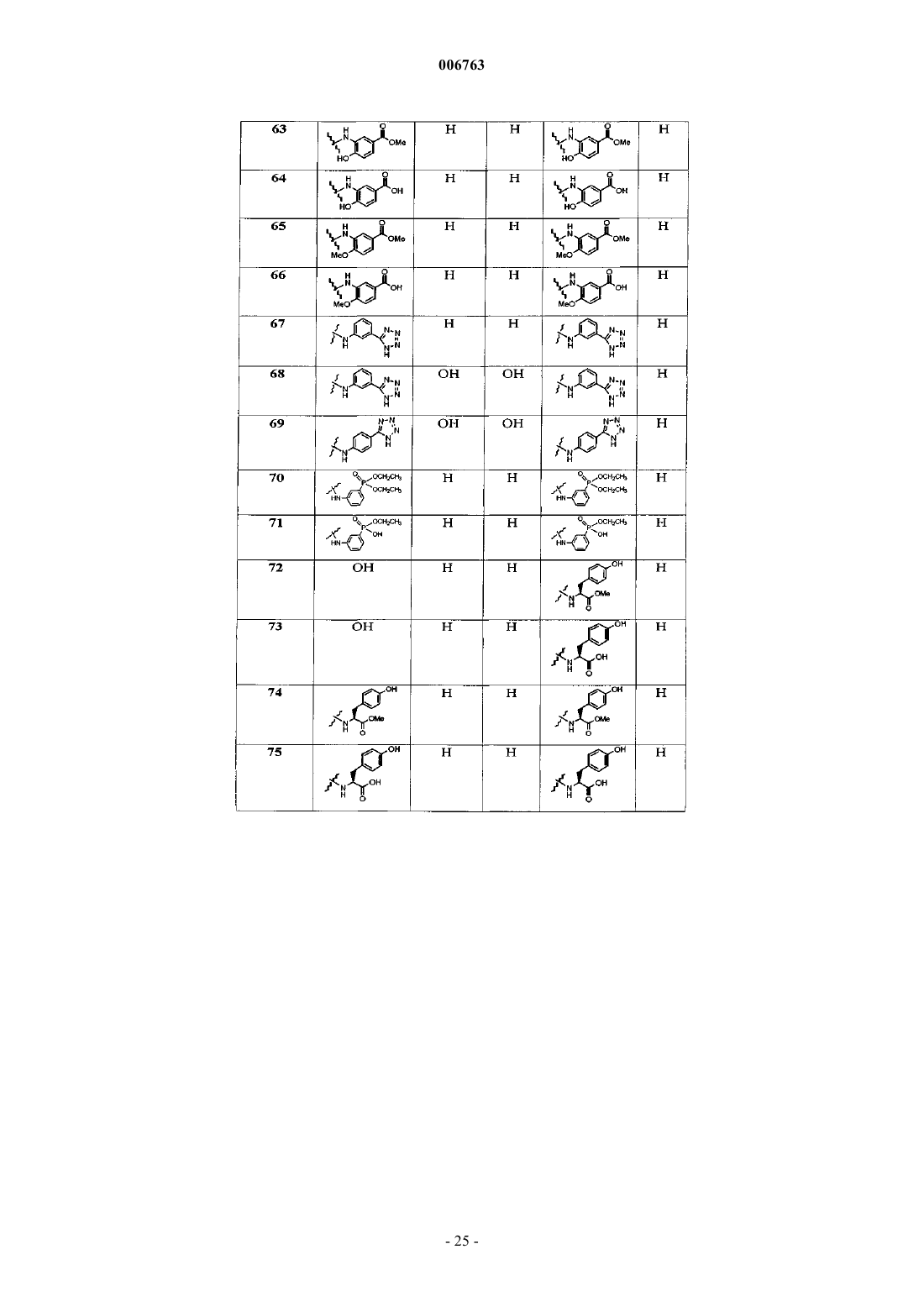
13. Соединение по п.1, выбираемое из группы
3-{[(7-{[N-(7-{[(3-сульфофенил)амино]сульфонил}-2-нафтил)карбамоил]амино}-2-нафтил)сульфонил]амино}бензолсульфокислота,
3-{[(4-гидрокси-7-{[N-(5-гидрокси-7-{[(3-сульфофенил)амино]сульфонил}(2-нафтил))карбамоил]амино}-2-нафтил)сульфонил]амино}бензолсульфоновая кислота,
4-{[(7-{[(7-{[(4-сульфофенил)амино]сульфонил}-2-нафтил)амино]карбониламино}-2-нафтил)сульфонил]амино}бензолсульфоновая кислота,
метиловый эфир 4-({[7-({N-[7-({[4-(метоксикарбонил)фенил]амино}сульфонил)-2-нафтил]карбамоил}амино)-2-нафтил]сульфонил}амино)бензойной кислоты,
4-{[(7-{[(7-{[(4-карбоксифенил)амино]сульфонил}-2-нафтил)амино]карбониламино}-2-нафтил)сульфонил]амино}бензойная кислота,
метиловый эфир 4-({[4-гидрокси-7-({N-[5-гидрокси-7-({[4-(метоксикарбонил)фенил]амино}сульфонил)(2-нафтил)]карбамоил}амино)-2-нафтил]сульфонил}амино)бензойной кислоты,
4-{[(7-{[(7-{[(4-карбоксифенил)амино]сульфонил}-5-гидрокси(2-нафтил))амино]карбониламино}-4-гидрокси-2-нафтил)сульфонил]амино}бензойная кислота,
3-{[(7-{[N-(7-{[(3-карбокси-2-гидроксифенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}-2-гидроксибензойная кислота,
5-{[(7-{[N-(7-{[(3-карбокси-4-гидроксифенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}-2-гидроксибензойная кислота,
метиловый эфир 3-({[7-({[7-({[3-(метоксикарбонил)фенил]амино}сульфонил)-2-нафтил]амино}карбониламино)-2-нафтил]сульфонил}амино)бензойной кислоты,
3-{[(7-{[(7-{[(3-карбоксифенил)амино]сульфонил}-2-нафтил)амино]карбониламино}-2-нафтил)сульфонил]амино}бензойная кислота,
метиловый эфир 3-({[4-гидрокси-7-({5-гидрокси-7-({[3-(метоксикарбонил)фенил]амино}сульфонил)(2-нафтил)амино}карбониламино)-2-нафтил]сульфонил}амино)бензойной кислоты,
3-{[(7-{[(7-{[(3-карбоксифенил)амино]сульфонил}-5-гидрокси(2-нафтил))амино]карбониламино}-4-гидрокси-2-нафтил)сульфонил]амино}бензойная кислота,
5-{[(7-{[N-(7-{[(3-карбокси-4-гидроксифенил)амино]сульфонил}-5-гидрокси(2-нафтил))карбамоил]амино}-4-гидрокси(2-нафтил))сульфонил]амино}-2-гидроксибензойная кислота,
5-{[(7-{[N-(7-{[(3-карбокси-4-хлорфенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}-2-хлорбензойная кислота,
5-{[(7-{[N-(7-{[(3-карбокси-4-хлорфенил)амино]сульфонил}-5-гидрокси(2-нафтил))карбамоил]амино}-4-гидрокси(2-нафтил))сульфонил]амино}-2-хлорбензойная кислота,
метиловый эфир 2-гидрокси-5-({[7-({[7-({[4-гидрокси-3-(метоксикарбонил)фенил]амино}сульфонил)(2-нафтил)]амино}карбониламино)(2-нафтил)]сульфонил}амино)бензойной кислоты,
метиловый эфир 2-хлор-5-({[7-({N-[7-({[4-хлор-3-(метоксикарбонил)фенил]амино}сульфонил)(2-нафтил)]карбамоил}амино)(2-нафтил)]сульфонил}амино)бензойной кислоты,
N-(7-{[(3-(1Н-1,2,3,4-тетразол-5-ил)фенил)амино]сульфонил}(2-нафтил))[(7-{[(3-(1H-1,2,3,4-тетразол-5-ил)фенил)амино]сульфонил}(2-нафтил))амино]карбоксамид,
N-(5-гидрокси)-7-{[(3-(1H-1,2,3,4-тетразол-5-ил)фенил)амино]сульфонил}(2-нафтил)[(5-гидрокси-7-{[(3-(1H-1,2,3,4-тетразол-5-ил)фенил)амино]сульфонил}(2-нафтил))амино]карбоксамид,
N-[7-({[3-(диэтоксифосфорил)фенил]амино}сульфонил)(2-нафтил)]{[7-({[3-(диэтоксифосфорил)фенил]амино}сульфонил)(2-нафтил)]амино}карбоксамид,
N-[7-({[3-(этокси(гидроксифосфорил))фенил]амино}сульфонил)(2-нафтил)]{[7-({[3-(этокси(гидроксифосфорил))фенил]амино}сульфонил)(2-нафтил)]амино}карбоксамид,
2-хлор-5-{[(7-{[(7-{[(4-хлор-3-сульфофенил)амино]сульфонил}(2-нафтил))амино]карбониламино}(2-нафтил))сульфонил]амино}бензолсульфоновая кислота,
2-хлор-5-{[(7-{[(7-{[(4-хлор-3-сульфофенил)амино]сульфонил}-5-гидрокси(2-нафтил))амино]карбониламино}-4-гидрокси(2-нафтил))сульфонил]амино}бензолсульфоновая кислота,
5-[({7-[3-(7-{[(3-карбокси-4-гидроксифенил)амино]сульфонил}(2-нафтил))-2-оксоимидазолидинил](2-нафтил)}сульфонил)амино]-2-гидроксибензойная кислота,
5-[({7-[3-(7-{[(3-карбокси-4-хлорфенил)амино]сульфонил}(2-нафтил))-2-оксоимидазолидинил](2-нафтил)}сульфонил)амино]-2-хлорбензойная кислота,
2-хлор-5-{[(7-{[N-(5-гидрокси-7-{[(3-сульфофенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}бензойная кислота,
5-{[(7-{[N-(7-{[(4-карбоксифенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}-2-хлорбензойная кислота и
5-{[(7-{[N-(7-{[(3-карбоксифенил)амино]сульфонил}(2-нафтил))карбамоил]амино}(2-нафтил))сульфонил]амино}-2-хлорбензойная кислота,
или их фармацевтически приемлемые соли.
14. Соединенеие по п.1, представляющее собой соединение формулы
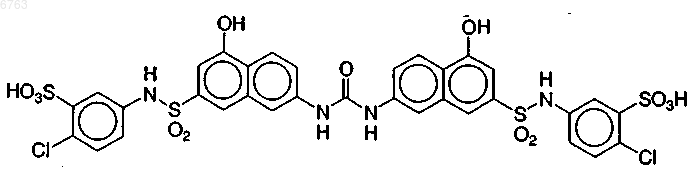
или его фармацевтически приемлемую соль.
15. Соединенеие по п.1, представляющее собой соединение формулы
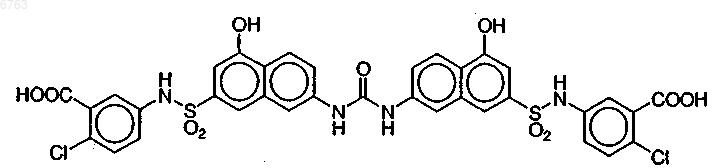
или его фармацевтически приемлемую соль.
16.Фармацевтическая композиция, включающая соединение по любому из пп.1-15.
17. Фармацевтическая композиция по п.16 для лечения или предупреждения болезненных состояний млекопитающих, выбранных из группы, состоящей из гипергликемии, диабета типа I и типа II.
18. Способ лечения или предупреждения болезненных состояний у млекопитающих, выбранных из группы, состоящей из гипергликемии, диабета типа I и типа II, включающий введение млекопитающему соединения по любому из пп.1-15 или фармацевтической композиции по п.16.
19. Применение соединения по любому из пп.1-15 для приготовления лекарственного препарата для лечения или предупреждения болезненного состояния у млекопитающего, выбранного из группы, состоящей из гипергликемии, диабета типа I и типа II.
20. Применение соединения по любому из пп.1-15 в качестве усилителя поглощения глюкозы.
Текст
(а). Область техники. Изобретение относится к способам усиления инсулиннезависимого поглощения глюкозы. Конкретно изобретение относится к соединениям, которые активируют киназу инсулинового рецептора, приводя к повышенному поглощению глюкозы. Изобретение относится также к способам лечения гипергликемии у человека и особенно к способам лечения диабета типа II.(б). Описание известного уровня техники. Среди многочисленных метаболических функций, осуществляемых пептидными и белковыми гормонами, имеется способность взаимодействовать с высокой специфичностью с рецепторами. Инсулиновый рецептор присутствует фактически на всех клетках и в высоких концентрациях на клетках печени,скелетных мышц и жировых тканей. Стимуляция инсулинового рецептора инсулином является существенным элементом метаболизма и накопления углеводов. Больные диабетом или лишены достаточной эндогенной секреции инсулинового гормона (тип I),или имеют опосредованный инсулиновым рецептором сигнальный путь, который устойчив к эндогенному или экзогенному инсулину [тип II или инсулиннезависимый сахарный диабет (NIDDM)]. Диабет типаII является наиболее распространенной формой диабета, поражающей около 5% населения развитых стран. У больных диабетом типа II большинство восприимчивых к инсулину тканей, таких как печень,скелетная мышца и жировая ткань, обладают устойчивостью к инсулину (Haring, Mehnert, Diabetologia,36:176-182 (1993); Haring и др., Diabetologia, 37 Suppl., 2:S149-54 (1994. Устойчивость к инсулину при диабете типа II является сложной и, очевидно, многофакторной, но, по-видимому, вызывается нарушенным сигналом от инсулинового рецептора к транспортной системе глюкозы и гликогенсинтазе. Недостаточность киназы инсулинового рецептора вовлечена в патогенез этого сигнального дефекта. Инсулиновая резистентность найдена также у многих пациентов, не страдающих диабетом, и может быть основным этиологическим фактором в развитии заболевания (Reaven, Diabetes, 37:1595-1607(1988. Известна значительная информация, касающаяся самого рецептора инсулина. Рецептор состоит из четырех отдельных субъединиц, включающих две идентичные - и две идентичные -цепи. Субъединица имеет тирозинкиназную активность и АТФ-связывающие сайты. Инсулиновый рецептор активируется аутофосфорилированием ключевых остатков тирозина в своем цитоплазматическом тирозинкиназном домене. Это аутофосфорилирование необходимо для последующей активности инсулинового рецептора. Аутофосфорилирование стабилизирует киназу активированного рецептора, приводя к каскаду фосфорилирования, включающему внутриклеточные сигнальные белки. В настоящее время подходы к лечению диабета типа II ограничены. Для лечения в настоящее время используют инсулин, но это невыгодно, поскольку инсулин должен быть инъецирован. Несмотря на то,что описаны некоторые пептидные аналоги инсулина, ни один из них с молекулярной массой ниже 5000 Да не сохраняет его активность. Некоторые пептиды, которые взаимодействуют с сайтами на субъединице инсулинового рецептора, проявили усиление активности инсулина на его рецепторе (Kole и др., J. Biol. Chem., 271:31619-31626(1996); Kasuya и др., Biochem. Biophys. Res. Commun., 200:777-83(1994. Kohanski и др. сообщили о разнообразных поликатионных веществах, которые вызывают базальный эффект, но лишь незначительно усиливают действие инсулина (Kohanski, J. Biol. Chem.,264:20984-91 (1989); Xu и др., Biochemistry, 30:11811-19 (1991. Очевидно, эти пептиды действуют на цитоплазматическом киназном домене инсулинового рецептора. Кроме того, было найдено, что некоторые непептидные компоненты усиливают агонистические свойства пептидных гормонов, но ни один из них, по-видимому, не действует на киназу инсулинового рецептора. Например, описана способность тиазолидиндионов, таких как пиоглитазон, усиливать дифференцировку адипоцитов (Kletzien и др., Mol. Pharmacol., 41:393 (1992. Эти тиазолидиндионы представляют класс потенциальных антидиабетических соединений, которые усиливают ответ тканеймишеней на инсулин (Kobayashi, Diabetes, 41:476 (1992. Тиазолидиндионы включают пероксисомный пролиферативно-активированный рецептор(PPAR), ядерный фактор транскрипции, участвующий в дифференцировке адипоцитов (Kliewer и др., J. Biol. Chem., 270:12953 (1995, и не оказывают прямого эффекта на киназу инсулинового рецептора. Применяемые в настоящее время другие антидиабетические агенты включают как средства, усиливающие секрецию инсулина (такие как сульфонилмочевины), так и бигуаниды (такие как метформин), которые ингибируют печеночный выброс глюкозы. До настоящего времени не удалось обнаружить непептидные вещества, которые могут имитировать активирующий эффект инсулина на инсулиновый рецептор. Биснафталинмочевины известны в литературе. О них много написано как о полисульфокислотных производных сурамина и как об азокрасителях. Ряд этих производных полианионных сульфокислот был создан в качестве потенциальных терапевтических средств для разнообразных болезненных симптомов. Сурамин, описанный в 1917 г., представляет собой полисульфокислоту, которая широко исследована(Dressel, J. Chem. Ed., 38:585 (1961); Dressel, J. Chem. Ed., 39:320 (1962. Cyрамин применяется в терапии как антигельминтное и антипротозойное средство. Позднее он был описан как ингибитор обратной транскриптазы некоторых птичьих и мышиных ретровирусов (De Clercq, Cancer Letter, 8:9 (1979);Mitsuya и др., Science, 226:172 (1984); Gagliardi и др., Cancer Chemother. Pharmacol., 41:117 (1988); Doukas и др., Cancer Res., 55:5161 (1995); Mohan и др., Antiviral Chem., 2:215(1991. Существует большое количество соединений, родственных сурамину. Большинство сураминовых аналогов, о которых сообщено,имеют многочисленные функциональные сульфокислотные группы в каждом ароматическом кольце. Недавние исследования указывают на то, что полианионные сураминовые аналоги обладают антиангиогенной, антипролиферативной активностью и противовирусной активностью (Gagliardi и др., CancerChem., 2:215 (1991. Многие биснафтилсульфокислоты описаны в патентной литературе как ингибиторы комплемента (патенты US4132730, 4129591, 4120891, 4102917 б 4051176). Кроме того, имеется множество патентов на азокрасители (патент DE19521589, патент US3716368, патент DE2216592, патент FR1578556), полисульфированные нафталиназопроизводные. О 2-сульфонамид-3 азопроизводных биснафталинмочевины сообщено только как о жидкости для записи (патент JP58191772). Однако ни один из аналогов сурамина или азокрасителей не предложен для применения в лечении гипергликемии или диабета. Сущность изобретения Данное изобретение относится к биснафталинмочевинам, которые усиливают поглощение глюкозы у млекопитающих, к их фармацевтическим композициям и к способам усиления поглощения глюкозы с применением этих соединений. В первом варианте воплощения данное изобретение обеспечивает соединения формулы I Формула I где R1 и R2 являются заместителями в кольцах А и означают независимо друг от друга -SO2NR72,-C(O)NR72, -NR7SO2R7, -NR7C(O)R7, -SO2OR7, -C(O)OR7, -OSO2R7 или -OC(O)R7,R3 и R4 означают независимо друг от друга водород или (низш.)алкил, или R3 и R4 вместе означают-(СН 2)2-, -(СН 2)3- или -(СН 2)4-, или R3 и R4 могут быть электронной парой,R5 и R6 означают независимо друг от друга водород, алкил, замещенный алкил, циано, галоид, нитро, -SR8, -C(O)R8, -SO2OR8, -OSO2R8, -SO2NR82, -NR8SO2R8, -OC(O)R8, -C(O)OR8, -C(O)NR82, -NR8C(O)R8,-OR8 или -NR82,R7 и R8, каждый независимо друг от друга, означают водород, алкил, замещенный алкил, арил, замещенный арил, арил(низш.)алкил, замещенный арил(низш.)алкил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, гетероарил или замещенный гетероарил,Y, каждый независимо друг от друга, означает немешающий заместитель, который не связан с нафталиновым кольцом посредством азо- или амидной связи,х, каждый независимо друг от друга, означает 0, 1 или 2, и линкер соединяет углерод, обозначенный с, с углеродом, обозначенным d, и означает где R означает циано или (низш.)алкил; и где если R1 и R2 оба означают -SO2OH, то (i) Y не означает-SO2OH; (ii) ни R5, ни R6 не означают -SO2OR8 или -OSO2R8 и (iii) R5 и R6 оба не выбирают из группы,состоящей из гидрокси и водорода, если по меньшей мере один (Y)x не означает (Y')х', где х' означает 1 или 2 и Y' означает галоид, и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Эти соединения могут применяться в качестве агонистов поглощения глюкозы и в лечении гипергликемии и диабета. Во втором варианте воплощения данное изобретение обеспечивает фармацевтические композиции,включающие (а) фармацевтически приемлемый носитель и (б) активный ингредиент, соединение по первому варианту воплощения. Эти композиции применимы для стимуляции поглощения глюкозы в клетках млекопитающих или для лечения болезненного состояния млекопитающего, выбранного из группы, состоящей из гипергликемии, диабета типа I и диабета типа II. В третьем варианте воплощения данное изобретение обеспечивает способ стимуляции киназной активности инсулинового рецептора, включающий контакт инсулинового рецептора или его киназной части с соединением по первому варианту воплощения изобретения в количестве, достаточном для стимуляции киназной активности инсулинового рецептора. В четвертом варианте воплощения данное изобретение обеспечивает способ активации инсулинового рецептора, включающий контакт рецептора или его киназной части с соединением по первому варианту воплощения в количестве, достаточном для воздействия на активацию инсулинового рецептора. В пятом варианте воплощения данное изобретение обеспечивает способ стимуляции поглощения глюкозы в клетках с рецептором инсулина, включающий контакт клеток, необязательно в присутствии инсулина, с соединением по первому варианту воплощения в количестве, достаточном для стимуляции поглощения глюкозы в клетках. На поглощение глюкозы в клетках млекопитающего может оказывать влияние введение млекопитающему соединения по изобретению. В других вариантах воплощения изобретение обеспечивает способы лечения гипергликемии, диабета типа I или диабета типа II у млекопитающих, таких как человек, введением терапевтически эффективного количества соединения по первому варианту воплощения или композиции, содержащей упомянутое соединение. Краткое описание чертежей Фиг. 1 показывает фосфорилирование субъединицы IRS-1 и инсулинового рецептора в присутствии соединения 15 с инсулином и без инсулина; фиг. 2 - график, показывающий усиление фосфорилирования инсулинового рецептора при обработке соединениями 13 и 15 в различных концентрациях; фиг. 3 - график, показывающий усиление поглощения глюкозы клетками при обработке соединениями 13 или 15 в присутствии или в отсутствие инсулина; фиг. 4 показывает влияние соединения 13 или 15 на транспорт глюкозы в присутствии или в отсутствие вортманнина; фиг. 5 показывает влияние соединения 15 на транспорт глюкозы в присутствии или в отсутствие вортманнина и цитохалазина Б; фиг. 6 показывает данные иммунофлуоресценции для транспортного белка GLUT4 при обработке клеток соединением 15; фиг. 7 показывает влияние соединения 15 на рецепторы инсулина и эпидермального фактора роста(EGF); фиг. 8 - график, показывающий эффект снижения уровня глюкозы в крови под воздействием соединения 15 в присутствии инсулина у мышей, полученных скрещиванием невосприимчивых к инсулину особей db/db; фиг. 9 - график, показывающий эффект снижения уровня глюкозы в крови у мышей db/db только под воздействием соединения 15; фиг. 10 показывает влияние соединения 15 на некоторые компоненты крови у мышей, полученных-3 006763 скрещиванием особей с ожирением ob/ob; фиг. 11 показывает влияние соединения 15 на уровни глюкозы в крови крысы, получавшей корм с высоким содержанием жира и стрептозотоцин, STZ/HFD; фиг. 12 показывает количество фосфорилированного инсулинового рецептора, обнаруженного в мышечной ткани после перорального введения соединения 15; фиг. 13 показывает эффект соединения 15 у мышей db/db после введения 3 однократных дневных доз; фиг. 14 показывает эффект соединения 15 у крысы STZ/HFD после введения 3 однократных дневных доз. Подробное описание изобретения(а). Определения и общие параметры. Термин алкил, как в алкиле или алкокси, означает одновалентный углеводородный остатокC1-С 20, который может быть линейным, разветвленным или циклическим. Термин (низш.)алкил, как в(низш.)алкиле, галоид(низш.)алкиле, арил(низш.)алкиле или гетероарил(низш.)алкиле, означает алкил C1-С 6. Термин (низш.)алкил включает такие остатки, как метил, этил, изопропил, пропил, бутил,изобутил, втор-бутил, трет-бутил, пентил, гексил, циклопентил, циклопропилметил и циклогексил. Предпочтительными являются (низш.)алкилы C1-С 4. Термин (низш.)алкил, как он использован в контексте, включает остатки с одной двойной связью, такие как аллил. Термин замещенный алкил или замещенный (низш.)алкил означает алкил или (низш.)алкил,соответственно, который обычно моно-, ди- или тризамещен остатком, таким как арил, R'-замещенный арил, гетероарил, нитро, циано, галоид, -OR, -SR, -COR, -OC(O)R, -C(O)OR, -NR2, -SO2OR, -OSO2R,-SO2NR2, -NRSO2R, -CONR2 или -NRCOR, где каждый R означает независимо друг от друга водород,(низш.)алкил, R'-замещенный (низш.)алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил, R'-замещенный арил(низш.)алкил или арил(низш.)алкил, и каждый R' независимо друг от друга означает гидрокси, галоид, (низш.)алкилокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или имино. Замещенные алкилы или замещенные (низш.)алкилы, которые замещены одним-тремя заместителями, выбранными из группы, состоящей из циано, галоида, (низш.)алкилокси, тио,нитро, амино и гидрокси, являются особенно предпочтительными. Термин галоид(низш.)алкил означает (низш.)алкил, замещенный одним-тремя атомами галоида и в дальнейшем в качестве примеров представлен такими радикалами, как -CF3, -CH2CF3 и CH2CCl3. Термин арил, как в ариле, арилокси и арил(низзш.)алкиле, означает радикал, происходящий от ароматического углеводорода, содержащего 6-20 атомов углерода в кольце, имеющий одно кольцо (например, фенил), или два, или несколько колец, предпочтительно 2-3 конденсированных кольца(например, нафтил), или два, или несколько ароматических колец, предпочтительно 2-3 ароматических кольца, которые связаны одинарной связью (например, бифенил). Арил означает предпочтительно С 6-С 16 и даже более предпочтительно С 6-С 14. Термин замещенный арил означает арильный радикал, который моно-, ди- или тризамещен независимо от других такими остатками, как гидрокси, триазолил, тетразолил, гидроксиизоксазолил, фосфоновый или фосфонатный остаток, алкил, R'-замещенный алкил, галоид, трифторметил, циано, нитро, -SR,-OR, -COR, -OCOR, -SO2OR, -OSO2R, -SO2NR2, -NRSO2R, -COOR, -NR2, -CONR2 или -NRCOR, где каждый R независимо друг от друга означает водород, (низш.)алкил, R'-замещенный (низш.)алкил, арил, R'замещенный арил, гетероарил, гетероарил(низш.)алкил, арил(низш.)алкил или R'-замещенный арил(низш.)алкил, и каждый R' означает независимо друг от друга гидрокси, галоид, (низш.)алкилокси,циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил, амино или -COOR, где R имеет приведенные выше значения. Особенно предпочтительными заместителями в замещенном ариле являются (низш.)алкил,галоид(низш.)алкил, галоид, циано, тио, нитро, амино, (низш.)алкилокси или гидрокси. Радикалы-SO2OR, -SO2NR2, -COOR и -CONR2, где R означает водород или (низш.)алкил, являются особенно предпочтительными для замещения в арилах в соединениях по настоящему изобретению. Термин гетероарил, как в гетероариле и гетероарил(низш.)алкиле, означает радикал, происходящий от ароматического углеводорода, содержащего 5-14 атомов в кольце, из которых 1-5 являются гетероатомами, выбираемыми независимо друг от друга из N, О и S, и включает моноциклические, конденсированные гетероциклические и конденсированные карбоциклические и гетероциклические ароматические кольца (например, тиенил, фурил, пирролил, пиримидинил, изоксазолил, оксазолил, триазолил,тетразолил, индолил, изобензофуранил, пуринил, изохинолил, птеридинил, имидазолил, пиридил, пиразолил, пиразинил, хинолил и т.д.). Замещенный гетероарил может иметь от одного до трех заместителей, таких как алкил, R'замещенный алкил, галоид, циано, нитро, -SR, -OR, -COR, -OOCR, -SO2OR, -OSO2R, -SO2NR2, -NRSO2R,-COOR, -NR2, -CONR2 или -NRCOR, где каждый R независимо друг от друга означает водород,(низш.)алкил, R'-замещенный (низш.)алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил, арил(низш.)алкил или R'-замещенный арил(низш.)алкил, и каждый R' независимо друг от друга означает гидрокси, галоид, (низш.)алкокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Кроме того, любые два смежных заместителя в гетероариле необязательно могут образовать-4 006763 вместе (низш.)алкилендиокси. Особо предпочтительные заместители в замещенном гетероариле включают гидрокси, галоид, (низш.)алкокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Термин гетероциклил означает радикал, происходящий от алифатического циклического углеводорода, содержащего 5-14 атомов в кольце, из которых 1-5 являются гетероатомами, выбранными независимо друг от друга из N, О или S. Моноциклические кольца (например, тетрагидрофуранил, тетрагидропиранил, пиперидинил и т.д.) являются предпочтительными. Замещенный гетероциклил может иметь от одного до трех заместителей, как алкил, R'замещенный алкил, галоид, циано, нитро, -SR, -OR, -COR, -OOCR, -SO2OR, -OSO2R, -SO2NR2, -NRSO2R,-COOR, -NR2, -CONR2 или -NRCOR, где каждый R независимо друг от друга означает водород,(низш.)алкил, R'-замещенный алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил,арил(низш.)алкил или R'-замещенный арил(низш.)алкил, и каждый R' независимо друг от друга означает гидрокси, галоид, (низш.)алкокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Предпочтительные заместители в замещенном гетероциклиле включают (низш.)алкил, галоид(низш.)алкильный радикал, содержащий один-три заместителя в гетероарильной части, или в алкильной части радикала, или в обеих частях. Термин (низш.)алкилокси означает радикал -OR, в котором R означает (низш.)алкил. Термин галоид означает бром, фтор или хлор. Термин немешающий заместитель означает заместитель, который, присутствуя в данном соединении, фактически не снижает или иным способом не подавляет его конкретную желаемую биологическую активность, такую как способность соединения стимулировать киназную активность инсулинового рецептора, активировать инсулиновый рецептор или стимулировать поглощение глюкозы в клетках, обладающих рецептором инсулина. Наличие немешающего заместителя не должно оказывать отрицательного воздействия на биологическую активность соединения более чем примерно на 30%. Предпочтительно немешающий заместитель понижает биологическую активность соединения менее чем примерно на 10%. Наиболее предпочтительно немешающий заместитель не понижает биологическую активность соединения до какого-либо определяемого значения. Однако эффект присутствия немешающего заместителя в соединении не должен быть нейтральным. Например, немешающий заместитель может необязательно повышать конкретную биологическую активность соединения. Приемлемые немешающие заместители включают, но без ограничения, алкил, замещенный алкил, циано, галоид, нитро, -SR, -OR и NR2,где каждый R независимо друг от друга означает водород, (низш.)алкил или замещенный (низш.)алкил. Термин азосвязь означает группу -N=N-. Обычная амидная связь означает группу в которой R может быть алкилом, арилом или водородом. Фармацевтически приемлемая соль может быть любой солью, полученной из неорганической или органической кислоты либо неорганического или органического основания. Термин фармацевтически приемлемый анион относится к аниону таких кислотно-аддитивных солей. Термин фармацевтически приемлемый катион относится к катиону, образованному присоединением основания. Выбираемые соль и/или анион либо катион не должны быть биологически или каким-либо другим образом нежелательными. Термин стереоизомеры означает соединения, которые имеют одинаковую последовательность ковалентных связей и отличаются относительным расположением их атомов в пространстве. Внутренние соли или цвиттер-ионы могут быть образованы переносом протона от карбоксильной группы к свободной паре электронов атома азота в аминогруппе. Термин терапевтически эффективное количество означает, что количество, которое при введении млекопитающему для лечения заболевания достаточно, чтобы повлиять на такое лечение заболевания. Термины обработка или лечение заболевания у млекопитающих включают:(1) предупреждение развития заболевания у млекопитающего, которое может быть предрасположенным к нему, но еще не проявляет или не обнаруживает симптомы болезни,(2) подавление заболевания, т.е. остановка его развития или(3) ослабление заболевания, т.е. индукция регрессии заболевания. По отношению к рецептору инсулина термин киназная часть его означает домен цитоплазматической тирозинкиназы инсулинового рецептора.(б). Номенклатура. Соединения формулы I нумеруют и называют, как описано ниже со ссылкой на формулу Iа Формула Iа В соединении формулы Iа заместитель R1 находится в положении 7 нафталинового кольца, заместитель R2 находится в положении 2 нафталинового кольца. Например, если R1 означает -SO2OH, R2 означает -SO2OH, R3 означает Н, R4 означает Н, R5 означает Н, R6 означает Н и K означает О, и аминокарбониламинолинкер присоединен к С 2 нафталинового кольца с заместителем R5 и к С 7 нафталинового кольца с заместителем R6, то соединение имеет следующее название: 7-[(7-сульфо-2-нафтил)амино] карбониламинонафталин-2-сульфоновая кислота.(в). Соединения и их фармацевтические композиции. В одном аспекте соединения по изобретению включают соединения формулы I Формула I где R1 и R2 являются заместителями в кольцах А и означают независимо друг от друга -SO2NR72,-C(O)NR72, -NR7SO2R7, -NR7C(O)R7, -SO2OR7, -C(O)OR7, -OSO2R7 или -OC(O)R7,R3 и R4 означают независимо друг от друга водород или (низш.)алкил, или R3 и R4 вместе означают-(СН 2)2-, -(СН 2)3- или -(СН 2)4-, или R3 и R4 могут быть электронной парой,R5 и R6 означают независимо друг от друга водород, алкил, замещенный алкил, циано, галоид, нитро, -SR8, -C(O)R8, -SO2OR8, -OSO2R8, -SO2NR82, -NR8SO2R8, -OC(O)R8, -C(O)OR8, -C(O)NR82, -NR8C(O)R8,-OR8 или -NR82,R7 и R8, каждый независимо друг от друга, означают водород, алкил, замещенный алкил, арил, замещенный арил, арил(низш.)алкил, замещенный арил(низш.)алкил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, гетероарил или замещенный гетероарил,Y, каждый независимо друг от друга, означает немешающий заместитель, который не связан с нафталиновым кольцом посредством азо- или амидной связи,х, каждый независимо друг от друга, означает 0, 1 или 2, и линкер соединяет углерод, обозначенный с, с углеродом, обозначенным d, и означает где R означает циано или (низш.)алкил; и где если R1 и R2 оба означают -SO2OH, то(iii) R5 и R6 оба не выбирают из группы, состоящей из гидрокси и водорода, если по меньшей мере один (Y)x не означает (Y')х', где х' означает 1 или 2 и Y' означает галоид,и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Предпочтительные соединения формулы I включают соединения формулы II Формула II где линкер соединяет углерод, который обозначен с, с углеродом, который обозначен d, и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Предпочтительно соединения формулы II включают соединения формулы IIа Формула IIа или их фармацевтически приемлемую соль в виде единственного стереоизомера или смеси стереоизомеров, где R1-R6, Y и х имеют значения, описанные ранее для формулы II. Предпочтительно каждый немешающий заместитель Y означает алкил, замещенный алкил, циано,галоид, нитро, -SR9, -OR9 или -NR92, где каждый R9 независимо друг от друга означает водород,(низш.)алкил или замещенный (низш.)алкил. Более предпочтительно каждый Y означает (низш.)алкил,галоид(низш.)алкил, (низш.)алкокси, циано, галоид, тио, нитро, амино или гидрокси. В соединениях формул I, Iа, II и IIа каждый х означает предпочтительно 0 или 1. В особенно предпочтительных вариантах воплощения изобретения каждый х означает 0. В одном предпочтительном варианте осуществления изобретения R1 и R2 означают независимо друг от друга -SO2OR10, -C(O)OR10, -SO2NR11R10, -C(O)NR11R10, -OSO2R10, -OC(O)R10, -NR11SO2R10 или-NR11C(O)R10; каждый R11 независимо друг от друга означает водород или (низш.)алкил; и каждый R10 независимо друг от друга означает алкил, замещенный алкил, арил, замещенный арил, арил(низш.)алкил,замещенный арил(низш.)алкил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, гетероарил или замещенный гетероарил. Предпочтительно R1 и R2 независимо друг от друга означают -SO2NR11R10, -C(O)NR11R10, -NR11SO2R10 или -NR11C(O)R10. В дополнительном предпочтительном варианте воплощения R11 означает водород. Например, в особенно предпочтительных соединениях R1 и R2 независимо друг от друга означают -SO2NHR10 или -NHSO2R10. В альтернативном предпочтительном варианте воплощения R1 означает -SO2OR10, -C(O)OR10,-SO2NR11R10, -C(O)NR11R10, -OSO2R10, -OC(O)R10, -NR11SO2R10 или -NR11C(O)R10, и R2 означает -SO2OR11 или -C(O)OR11, где R10 и R11 имеют значения, приведенные ранее в предыдущем абзаце. Предпочтительно R1 означает -SO2NR11R10, -C(O)NR11R10, -NR11SO2R10 или -NR11C(O)R10. В дополнительном предпочтительном варианте воплощения R11 означает водород. Например, в особенно предпочтительных соединениях R1 означает -SO2NHR10 или -NHSO2R10. В одном предпочтительном варианте воплощения R2 означает -C(O)NR112 или -C(O)OR11. В альтернативном предпочтительном варианте воплощения R2 означает-SO2NR112 или -SO2OR11, такой как -SO2OH. В одном предпочтительном варианте воплощения изобретения каждый R10 независимо друг от друга означает замещенный алкил, замещенный арил, замещенный арил(низш.)алкил, замещенный гетероарил(низш.)алкил, замещенный гетероциклил или замещенный гетероарил; по меньшей мере один из заместителей в R10 означает R12; каждый R12 независимо друг от друга означает -SO2OR13, -C(O)OR13,-7 006763-SO2NR132, -C(O)NR132, гидрокси, триазолил, тетразолил, гидроксиизоксазолил, остаток фосфоновой кислоты или остаток фосфоната; и каждый R13 независимо друг от друга означает водород или(низш.)алкил. В этом варианте воплощения R10 означает предпочтительно замещенный арил или замещенный гетероарил. Особенно предпочтительно, чтобы R10 являлся замещенным фенилом. В предпочтительных соединениях по изобретению каждый R12 независимо друг от друга означает -C(O)OR13,-C(O)NR132, -SO2OR13, гидрокси, триазолил, тетразолил, гидроксиизоксазолил, остаток фосфоновой кислоты или фосфонатный остаток. В частности, предпочтительно, чтобы R12 означал -C(O)OR13, -SO2OR13,гидрокси, триазолил, тетразолил, гидроксиизоксазолил, остаток фосфоновой кислоты или фосфонатый остаток. Например, каждый R12 может быть -С(О)ОН, -SO2OR13 или -С(О)ОСН 3. В альтернативных предпочтительных соединениях каждый R12 независимо друг от друга означает -SO2OR13 или -SO2NR132. Чрезвычайно предпочтительно, чтобы R12 означал -SO2OR13 . В особенно предпочтительных соединениях R12 означает -SO2OH. Предпочтительно, что, когда R12 означает -C(O)OR13 или -SO2OR13, R12 в арильном, гетероарильном или гетероциклильном кольце будет смежным по отношению к такому заместителю, как хлор или гидрокси. В альтернативном предпочтительном варианте воплощения изобретения каждый R10 независимо друг от друга означает арил, гетероарил, арил(низш.)алкил или гетероарил(низш.)алкил. В таком варианте воплощения R10 предпочтительно означает фенил, пиридил, пиразинил или пиримидинил. Еще в других предпочтительных соединениях по изобретению каждый R1 и R2 независимо друг от друга означают -SO2NR72, -C(O)NR72, -SO2OR7 или -C(O)OR7; и каждый R7 независимо друг от друга означает водород или (низш.)алкил. Предпочтительно R1 и R2 независимо друг от друга означают -C(O)OR7 или -C(O)NR72. Однако в других предпочтительных соединениях формулы I R1 и R2 независимо друг от друга означают -SO2OR7 или -SO2NR72. Например, R1 и R2 могут оба означать -SO2OH. Предпочтительно,если R1 и R2 оба означают -SO2OH, тогда R5 и R6 оба не означают ни гидрокси, ни водород. Предпочтительно R3 и R4 соединений по изобретению означают водород. Предпочтительно R5 и R6 независимо друг от друга означают водород, алкил, замещенный алкил,циано, галоид, нитро, -OR8, -NR82 или -SR8 , где каждый R8 независимо друг от друга означает водород,(низш.)алкил, замещенный (низш.)алкил, арил, замещенный арил, арил(низш.)алкил, замещенный арил(низш.)алкил, гетероарил или гете-роарил(низш.)алкил. Наиболее предпочтительно R5 и R6 независимо друг от друга означают водород, гидрокси, галоид, циано, (низш.)алкил, галоид(низш.)алкил,(низш.)алкилокси, нитро, амино или тио. Во многих предпочтительных соединениях по изобретению R5 и R6 оба означают водород или гидрокси. Соединения формулы I и формулы II предпочтительно являются симметричными. Соединения по изобретению, содержащие более одного предпочтительного заместителя, являются предпочтительными. Если одно соединение содержит больше предпочтительных заместителей, чем второе соединение, тогда первое соединение имеет преимущество над вторым. Например, соединения формулы I, которые содержат предпочтительные радикалы для каждого из заместителей R1-R4 и R10-R12,имеют преимущество над теми, которые содержат предпочтительные радикалы только для заместителейR1-R3. Например, предпочтительные соединения по изобретению включают соединения формулы III Формула III где R5 и R6 выбирают из группы, состоящей из водорода и гидрокси; и каждый R10 независимо друг от друга означает замещенный арил или замешенный гетероарил; по меньшей мере один из заместителей вR10 означает R12; каждый R12 независимо друг от друга означает -SO2OR13, -C(O)OR13, -SO2NR132,-C(O)NR132, триазолил, тетразолил, изоксазолил, остаток фосфоновой кислоты или фосфонатный остаток; и каждый R13 независимо друг от друга означает водород или (низш.)алкил, и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Предпочтительно,когда R12 означает -C(O)OR13 или -SO2OR13, то R12 в арильном, гетероарильном или гетероциклильном кольце будет смежным по отношению к такому заместителю, как хлор или гидрокси. Другие примеры соединений по настоящему изобретению включают соединения формулы IV-8 006763 где R5 и R6 выбирают из группы, состоящей из водорода и гидрокси; R10 означает замещенный арил или замещенный гетероарил; по меньшей мере один из заместителей в R10 означает R12; каждый R12 независимо друг от друга означает -SO2OR13, -C(O)OR13, -SO2NR132, -C(O)NR132, триазолил, тетразолил, изоксазолил, остаток фосфоновой кислоты или фосфонатный остаток; и каждый R13 независимо друг от друга означает водород или (низш.)алкил, и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Предпочтительно, когда R12 означает -C(O)OR13 или -SO2OR13,то R12 в арильном, гетероарильном или гетероциклильном кольце будет смежным по отношению к такому заместителю, как хлор или гидрокси. Предпочтительными соединениями по настоящему изобретению, но без ограничения, являются следующие соединения: динатриевая соль 4-гидрокси-7-[(5-гидрокси-7-сульфо(2-нафтиламино]карбониламино-2-нафталин-2-сульфоновой кислоты; 3-[(4-гидрокси-7-[(5-гидрокси-7-[(3-сульфофенил)амино]сульфонил(2-нафтиламино]карбониламино-2-нафтил)сульфонил]аминобензолсульфоновая кислота; 2-[6-([5-(карбоксиметокси)-7-сульфо(2-нафтил)]аминокарбониламино)-3-сульфонафтилокси] уксусная кислота; 3-бром-7-[(6-бром-5-гидрокси-7-сульфо(2-нафтиламино]карбониламино-4-гидроксинафталин-2 сульфоновая кислота; 4-[(2-сульфофенил)метокси]-7-[(7-сульфо-5-[(2-сульфофенил)метокси](2-нафтил)амино)карбониламино]нафталин-2-сульфоновая кислота; 4-гидрокси-7-[(5-метокси-7-сульфо(2-нафтиламино]карбониламинонафталин-2-сульфоновая кислота; 4-метокси-7-[(5-метокси-7-сульфо(2-нафтиламино]карбониламинонафталин-2-сульфоновая кислота; 7-[(5-[(этоксикарбонил)метокси]-7-сульфо(2-нафтил)амино)карбониламино]-4-гидроксинафталин-2-сульфоновая кислота; 4-[(этоксикарбонил)метокси]-7-[(5-[(этоксикарбонил)метокси]-7-сульфо(2-нафтил)амино)карбониламино]нафталин-2-сульфоновая кислота; 4-(3-сульфопропокси)-7-([7-сульфо-5-(3-сульфопропокси)(2-нафтил)]аминокарбониламино) нафталин-2-сульфоновая кислота; 4-гидрокси-7-([7-сульфо-5-(3-сульфопропокси)(2-нафтил)]аминокарбониламино)нафталин-2 сульфоновая кислота;(2S)-2-([7-(N-[7-([(1S)-1-карбокси-2-(4-гидроксифенил)этил]аминосульфонил)(2-нафтил)] карбамоиламино)(2-нафтил)]сульфониламино)-3-(4-гидроксифенил)пропановая кислота; и их фармацевтически приемлемые соли в виде единственных стереоизомеров или смесей стереоизомеров. Синтезы и описания этих соединений приведены ниже в примерах 1-10. Некоторые соединения по изобретению могут иметь один или несколько хиральных центров. В таких случаях все стереоизомеры также попадают в объем данного изобретения. Новые соединения включают выделенные стереоизомеры в индивидуальном состоянии, а также смеси таких стереоизомеров. Соединения по изобретению дополнительно включают фармацевтически приемлемые соли соединений, раскрываемых в описании. Эти фармацевтически приемлемые соли пригодны для применения во всех способах и фармацевтических композициях по настоящему изобретению. Фармацевтически приемлемые соли включают соли, которые могут образоваться, когда присутствующие кислотные протоны способны взаимодействовать с неорганическими или органическими основаниями. Обычно исходное соединение обрабатывают избытком щелочного peaгента, такого как гидроксид, карбонат или алкоксид, содержащего соответствующий катион. Катионы, такие как Na+, K+, Ca 2+ иNH4+, являются примерами катионов, присутствующих в фармацевтически приемлемых солях. Особенно применимы натриевые соли. Следовательно, приемлемые неорганические основания включают гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия. Соли можно также получить, используя органические основания, такие как этаноламин, диэтаноламин, триэтаноламин, Nметилглюкамин и трометамин. Если соединение по изобретению содержит основную группу, может быть получена кислотноаддитивная соль. Кислотно-аддитивные соли соединений получают стандартным способом в подходящем растворителе из исходного соединения и избытка кислоты, такой как хлористо-водородная кислота,бромисто-водородная кислота, серная кислота (образующая сульфатные и бисульфатные соли), азотная кислота, фосфорная кислота и тому подобное, и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота,малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота,этансульфоновая кислота, салициловая кислота, п-толуолсульфокислота, гексановая кислота, гептановая кислота, циклопентанпропионовая кислота, молочная кислота, о-(4-гидроксибензоил)бензойная кислота,1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, пхлорбензолсульфоновая кислота, п-нафталинсульфоновая кислота, камфорсульфоновая кислота, 4 метилбицикло[2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, глюконовая кислота, 4,4'метиленбис(3-гидрокси-2-нафтойная)кислота, 3-фенилпропионовая кислота, триметилуксусная кислота,трет-бутилуксусная кислота, лаурилсерная кислота, глюкуроновая кислота, глутаминовая кислота, 3 гидрокси-2-нафтойная кислота, стеариновая кислота, муконовая кислота и тому подобное. Некоторые из соединений по изобретению образуют внутренние соли или цвиттер-ионы. Изобретение включает фармацевтические композиции всех соединений по настоящему изобретению. Фармацевтические композиции включают (i) соединение по изобретению в качестве активного ингредиента и (ii) фармацевтически приемлемый носитель. Фармацевтические композиции соединений по данному изобретению или их производных могут быть разработаны в виде растворов или лиофилизированных порошков для парентерального введения. Перед применением содержание влаги в порошке может быть восстановлено добавлением соответствующего разбавителя или другого фармацевтически приемлемого носителя. Жидкая лекарственная фор- 10006763 ма обычно представляет собой забуференный изотонический водный раствор. Примерами подходящих разбавителей являются обычный изотонический физиологический раствор, 5% декстроза в воде или забуференный раствор ацетата натрия или аммония. Такие лекарственные формы особенно подходят для парентерального введения, но могут также применяться для перорального применения. Может быть желательным добавление наполнителей, таких как поливинилпирролидон, желатин, гидроксицеллюлоза,гуммиарабик, полиэтиленгликоль, маннит, хлорид натрия или цитрат натрия. В качестве альтернативы эти соединения могут быть инкапсулированы, таблетированы или приготовлены в виде эмульсии или сиропа для перорального введения. Могут быть добавлены фармацевтически приемлемые твердые или жидкие носители, чтобы усилить или стабилизировать композицию или облегчить приготовление композиции. Жидкие носители включают сироп, арахисовое масло, оливковое масло, глицерин, физиологический раствор, спирты и воду. Твердые носители включают крахмал, лактозу, дигидрат сульфата кальция,гипс, стеарат магния или стеариновую кислоту, тальк, пектин, гуммиарабик, агар или желатин. Носитель может также включать материал с замедленным высвобождением, такой, как моностеарат глицерина или дистеарат глицерина, один или с воском. Количество твердого носителя изменяется, но предпочтительно будет между примерно 20 мг и примерно 1 г на дозированную единицу. Фармацевтические препараты получают, следуя общепринятым методикам фармации, включающим измельчение, смешивание, гранулирование и при необходимости прессование в случае таблеточных форм; или измельчение, смешивание и заполнение для форм в виде твердых желатиновых капсул. Если используют жидкий носитель, препарат будет в форме сиропа, эликсира, эмульсии или водной либо неводной суспензии. Такая жидкая лекарственная форма может быть введена непосредственно перорально или заключенной в мягкую желатиновую капсулу. В массовых процентах типичные фармацевтические композиции могут содержать 0,195% активного ингредиента, более предпочтительно 1-80%. Некоторые специфические образцы применимых фармацевтических композиций описаны ниже в примере 25. Как правило, фармацевтическая композиция по настоящему изобретению была бы упакована в емкость с наклейкой, указывающей на применение фармацевтической композиции в лечении гипергликемии, диабета типа I и диабета типа II или сочетания каких-либо проявлений этих заболеваний. Профилактически соединения могут вводиться перед едой, чтобы контролировать избыточный повышенный уровень глюкозы у пациентов с диабетом типа II в течение периода времени, следующего за едой. Альтернативно соединения могут вводиться пациентам с диабетом, чтобы нормализовать избыточно повышенные уровни глюкозы, измеренные с помощью устройства для мониторинга глюкозы. Наконец, известно, что очень маленькое количество остаточного циркулирующего инсулина, найденного у пациентов с диабетом типа I, используются организмом для предотвращения тяжелого липолиза и возникающего в результате кетоацидоза. Данные соединения могут применяться профилактически против кетоацидоза у пациента с диабетом типа I. Введение данных соединений могло бы обеспечить освобождение от кетоацидоза через активацию инсулинового рецептора, не для контроля сахара в крови, а для подавления тяжелого липолиза у пациентов с диабетом типа I, у которых нет быстрого доступа к инсулину.(г). Способы применения соединений по настоящему изобретению. Найдено, что соединения по настоящему изобретению стимулируют аутофосфорилирование инсулинового рецептора (пример 11 и 12 ниже). Кроме того, показано, что эти соединения усиливают способность инсулина воздействовать на транспорт глюкозы в культивированные клетки фибробластов(пример 13 ниже). Показано также, что соединения снижают уровни глюкозы в крови у мышей db/db независимым от инсулина способом (фиг. 8 и 9, пример 11, пример 19). Способность соединений по данному изобретению стимулировать аутофосфоилирование инсулинового рецептора и стимулировать поглощение глюкозы клетками, что продемонстрировано ниже в специальных примерах 11 -24, указывает на их полезность в лечении и ведении пациентов с диабетом. Безотносительно к какой-либо теории считается, что соединения по изобретению действуют непосредственно на киназную функцию инсулинового рецептора и необязательно конкурируют с инсулином за связывание в инсулин-связывающем сайте, также не влияют на активацию рецептора по механизму, подобному тому, который присущ инсулину. Таким образом, они способны непосредственно активировать киназу для аутофосфорилирования, потенцировать эффект инсулина, активировать киназную функцию рецептора при фосфорилировании экзогенных субстратов и влиять на повышенное поглощение глюкозы адипоцитами и вообще клетками, имеющими рецепторы инсулина, и снижать содержание глюкозы в крови у пациентов с диабетом. Соответственно на основании активности соединений по изобретению они могут применяться для стимуляции киназной активности инсулинового рецептора, для усиления активации инсулинового рецептора инсулином, для усиления стимуляции инсулином поглощения глюкозы в клетках и стимуляции поглощения глюкозы у пациентов с диабетом. Таким образом, соединения по данному изобретению применимы в лечении гипергликемии и диабета у млекопитающих. В одном аспекте изобретение относится к способу стимуляции киназной активности инсулинового рецептора. Этот способ включает контакт инсулинового рецептора или его киназной части с соединением по изобретению в количестве, достаточном для того, чтобы стимулировать киназную активность инсулинового рецептора. При стимуляции киназной активности инсулинового рецептора одновременно- 11006763 усиливается аутофосфорилирование, а также фосфорилирование экзогенных субстратов. Стимуляция киназной активности инсулинового рецептора может происходить или in vivo, или in vitro. Способ стимуляции киназной активности инсулинового рецептора необязательно может затем включать также контакт инсулинового рецептора с инсулином. Показано, что соединения по изобретению обладают стимулирующим действием на инсулиновый рецептор с последующим снижением циркулирующих уровней глюкозы в крови для потенциального терапевтического эффекта при заболевании диабетом. Подобным образом другие соединения, проявляющие такие же воздействия на инсулиновый рецептор и, следовательно, на циркуляцию глюкозы, являются потенциальными для применения в лечении диабета. Соединения, заявленные в пределах данного патента, могут использоваться в качестве модели для открытия других новых агентов, которые действуют на инсулиновый рецептор и тем самым снижают циркулирующие уровни глюкозы у пациентов с диабетом. Этапы в способе, по которому эти агенты могут использоваться для открытия новых агонистов/активаторов инсулиновых рецепторов и понижающих уровень глюкозы терапевтических агентов,можно успешно выполнить следующим образом. Соединения могут использоваться для того, чтобы подтвердить достоверность, оптимизировать и стандартизовать анализы, необходимые для открытия других соединений, которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. Эти соединения могут использоваться в качестве эталонного теста для открытия соединений, которые в испытаниях проявляют улучшенную активность, которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. В комбинации с алгоритмами для сравнения структур или химических свойств и/или равноценных структур или химических свойств внутри библиотек исследуемых веществ эти соединения могут использоваться для открытия соединений, которые обладают активностью в биологических испытаниях, соединений, которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. В комбинации с алгоритмами для сравнения структур и/или равноценных структур с целью моделирования молекулярных взаимодействий эти соединения могут использоваться для открытия соединений, которые обладают активностью в биологических исследованиях, соединений, которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. Радиоактивные соединения по данному патенту могут использоваться, чтобы диагностировать диабет, поскольку у пациентов с диабетом типа II и даже у пациентов, имеющих преддиабетические факторы риска, такие как синдром-Х, наблюдается уменьшение числа инсулиновых рецепторов. Простая биопсия ткани, сопровождаемая облучением тканевого образца данными радиоактивными соединениями,может дать измерение счета рецептора в биопсийной ткани. Показатель низкой рецепторной плотности- 12006763 затем может быть использован для диагностики у пациента диабета или преддиабета. Радиоактивные соединения имеют долгую историю применения в открытии новых лекарств. Соединения, заявленные в данном патенте, все обладают потенциалом для легкого введения радиоактивной метки и могут применяться для открытия других новых агентов, которые действуют на инсулиновый рецептор и тем самым снижают циркулирующие в крови уровни глюкозы у пациентов с диабетом. Способ, по которому данные агенты могут быть использованы для открытия новых агонистов/активаторов инсулиновых рецепторов и терапевтических агентов, понижающих уровни глюкозы, состоит в следующем. Радиоактивные соединения по данному патенту могут использоваться, чтобы оценить достоверность, оптимизировать и стандартизовать биологические тесты, применяемые для открытия других соединений, которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. Радиоактивные соединения по данному патенту могут использоваться как эталонный тест для открытия соединений, проявляющих улучшенную активность в биологических испытаниях, соединений,которые 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. В другом варианте воплощения изобретения инсулиновый рецептор активируется путем контакта инсулинового рецептора или его киназной части с соединением по изобретению в количестве, достаточном для активации инсулинового рецептора. Инсулиновый рецептор-мишень необязательно может находиться на поверхности клетки млекопитающего. В таком случае контакт осуществляется ведением млекопитающему соединения или его фармацевтической композиции. Необязательно способ может далее включать контакт инсулинового рецептора с инсулином. В альтернативном варианте воплощения изобретения соединения по изобретению применяют для стимуляции поглощения глюкозы клетками, обладающими рецептором инсулина. Данный способ включает контакт клеток с соединением по изобретению, необязательно в присутствии инсулина, в количестве, достаточном, чтобы стимулировать поглощение глюкозы клетками. Клетки-мишени необязательно могут быть у млекопитающего, и этап контакта рецептора с соединением может быть затем осуществлен введением млекопитающему соединения или его фармацевтической композиции. В одном варианте воплощения способа стимуляции поглощения глюкозы клетками, обладающими инсулиновым рецептором,клетки контактируют также с экзогенным инсулином. Способ лечения гипергликемии у млекопитающих, предпочтительно у человека, также предполагается настоящим изобретением. Способы включают введение млекопитающему терапевтически эффективного количества соединения по данному изобретению или его фармацевтической композиции. Необязательно способ может далее включать лечение млекопитающего с помощью одного или нескольких дополнительных видов терапии или лечение гипергликемии. Например, один способ может включать введение млекопитающему экзогенного инсулина в дополнение к соединению по изобретению. Альтернативно соединения по изобретению могут вводиться млекопитающему в комбинации с неинсулиновым препаратом или в сочетании с другим альтернативным курсом лечения гипергликемии. Общее количество комбинации препаратов, введенных млекопитающему, должно быть терапевтически эффективным,хотя количества каждого индивидуального препарата могут по отдельности быть субоптимальными для терапевтических целей. Очень опасным побочным эффектом введения инсулина является гипогликемия, индуцированная инсулином, с потенциальной комой и, возможно, смертью. Эта проблема может стать довольно острой у пациентов с диабетом, у которых проявляется непредсказуемая реакция на инсулин или сверхизменчивые уровни циркулирующей глюкозы. Для таких пациентов совместное введение данных соединений и субтерапевтических доз инсулина снизит до минимума возможность того, что пациенту с диабетом будет передозирован инсулин, и он пострадает от тяжелых последствий, таких как кома или смерть. Данные соединения, по-видимому, неспособны вызвать гипогликемию в присутствии или в отсутствие инсулина.- 13006763 По-видимому, они повышают эффективность инсулина, но не проявляют миметические эффекты истинного инсулина, подобные гипогликемии. Таким образом, данные соединения являются эффективными детоксикантами инсулина. В одном варианте воплощения изобретения соединения применяют для лечения диабета типа I у млекопитающих. Данный способ включает введение млекопитающему терапевтически эффективного количества соединения по изобретению или его фармацевтической композиции. Способ лечения диабета типа I необязательно может включать далее лечение млекопитающего с помощью одного или нескольких дополнительных видов терапии или курсов лечения диабета типа I. Например, в одном варианте осуществления способа лечения диабета типа I соединение по изобретению и инсулин могут оба вводиться млекопитающему. В качестве альтернативы дополнительным видом лечения диабета типа I, который сочетается с введением соединения по изобретению, может быть применение отличающегося от инсулина антидиабетического агента или другого альтернативного вида лечения диабета типа I. И снова общее количество комбинации антидиабетических агентов, введенных млекопитающему, должно быть терапевтически эффективным, хотя для терапевтических целей количество каждого из индивидуальных препаратов может быть субоптимальным, если эти препараты были даны по отдельности млекопитающему с диабетом типа I. В другом варианте воплощения изобретения соединения по изобретению применяют для лечения диабета типа II у млекопитающих. Данный способ включает введение млекопитающему терапевтически эффективного количества соединения по изобретению или его фармацевтической композиции. Снова предпочтительным субъектом является человек. И снова, как и другие способы лечения по изобретению, данный способ включает далее лечение млекопитающего с помощью одного или нескольких дополнительных видов терапии диабета типа II,таких как введение млекопитающему инсулина. Инсулин дается млекопитающему в количестве, которое терапевтически эффективно при совместном применении с соединением по изобретению. Это терапевтически эффективное количество инсулина при использовании в комбинации с соединением по изобретению может быть меньше того количества инсулина, которое было бы терапевтически эффективно, если бы только оно давалось млекопитающему. Понятно, что инсулин, который вводят при любом способе лечения по настоящему изобретению, может быть, или выделенным из природного источника, или рекомбинантным. Кроме того, аналог инсулина может заменять инсулин при любых способах лечения по настоящему изобретению. Применение соединений по изобретению для лечения диабета типа II с помощью комбинированной терапии может также включать введение млекопитающему соединения по изобретению в сочетании с неинсулиновым антидиабетическим агентом или другим видом терапии диабета типа II. Например, антидиабетический препарат, который вводят млекопитающему в комбинации с соединением по изобретению, необязательно может оыть тиазолидиндионом, таким как троглитазон или сульфонилмочевина. Общее количество препаратов комбинации (соединение по изобретению плюс инсулин и/или другой антидиабетический препарат), вводимое млекопитающему для лечения диабета типа II, должно быть терапевтически эффективным количеством, хотя количество каждого из индивидуальных препаратов, используемых в комбинационной терапии может быть субоптимальным для терапевтических целей, если только этот препарат давали млекопитающему с диабетом типа II. Таким образом, соединения по данному изобретению применяют для усиления поглощения глюкозы у пациентов, которым необходимо такое лечение. Способ лечения включает парентеральное или пероральное введение эффективного количества выбранного соединения по изобретению, предпочтительно диспергированного в фармацевтическом носителе. Стандартные дозировки активного ингредиента обычно выбирают в диапазоне от 0,01 до 1000 мг/кг, предпочтительно 0,01-100 мг/кг и более предпочтительно 0,1-50 мг/кг, но они будут легко определены специалистом в этой области в зависимости от пути введения, возраста и состояния пациента. Соединения по изобретению наиболее предпочтительно вводить в стандартной дозировке 1-10 мг/кг. Эти стандартные дозировки можно вводить один-десять раз ежедневно в случае острого или хронического заболевания. Не ожидаются никакие неприемлемые токсикологические эффекты, если соединения по изобретению вводят в соответствии с настоящим изобретением. Соединения по изобретению могут быть введены любым путем, применимым к пациенту, подвергающемуся лечению, и характеру его симптомов. Пути введения без ограничения охватывают введение с помощью инъекции, включая внутривенную, внутрибрюшинную, внутримышечную и подкожную инъекции, путем трансмукозальной или трансдермальной доставки, посредством местного применения, назального аэрозоля, суппозитория и тому подобного, или могут включать пероральное введение. Лекарственные формы необязательно могут быть липосомальными лекарственными формами, эмульсиями, лекарственными формами, создаваемыми для введения препарата через мембраны слизистой оболочки или транcдермальными лекарственными формами. Применимые лекарственные формы для каждого из этих способов введения можно найти, например, в Remingron's Pharmaceutical Sciences, последнее издание,изд-во Mack Publishing Company, Easton, PA. Способы, применения, активности, введение и фармацевтические композиции, описанные выше для- 14006763 соединений по изобретению, являются предпочтительными для тех соединений, в которых К=О.(д). Примеры. Последующие примеры являются иллюстрацией данного изобретения. Примеры никоим образом не ограничивают объем данного изобретения, а предназначены для того, чтобы показать, как получать и применять соединения по данному изобретению. Соединения формулы I могут быть получены(i) межмолекулярной или внутримолекулярной конденсацией соединения формулы А или присоединением соединения формулы А к соединению формулы Б, где аминогруппы формул А и Б необязательно находятся в защищенной форме, в присутствии активированного бифункционального реагента, который обеспечивает группу K=С-, где K имеет приведенные выше значения; где R1, R2, R3, R4,R5, R6, х и Y имеют значения в соответствии с первым аспектом раздела Сущность изобретения, x может означать R13 или R4, и WZ может означать S=C= или О=С=, или W и Z могут означать R3 или R4; чтобы образовать линкер между соединением формулы А и соединением формулы Б;(ii) химической модификацией одного или нескольких заместителей R1, R2, R5 и R6 или Y, при которой упомянутый заместитель способен превратиться в другой заместитель;(iii) введением заместителя R1, R2, R5 и R6 или Y в одно или несколько нафталиновых колец;(v) модификацией линкера, чтобы превратить упомянутый линкер в другой линкер;(vi) образованием соли или взаимопревращением;(viii) высвобождением свободной кислоты или основания из соединения по п.1 формулы изобретения или(ix) разделением или синтезом стереоизомеров. Подробности очевидны из следующей таблицы, в которой представлены типичные реакции для этапов (i)-(viii). Схема реакции Тип реакции В реакции конденсации при соединении двух или нескольких молекул выделяется простое вещество, такое как вода. Реакция конденсации может происходить при присоединении какого-либо из многочисленных исходных веществ, используемых в органическом синтезе, таких как дибромэтан и дийодпропан, при температуре между 50 и 125 С. Если бы R3 и R4 в формулах А и Б вместе означали -(СН 2)2-,-(СН 2)3- или -(СН 2)4, то конденсация являлась внутримолекулярной (см. реакционную схему VI). Химическая модификация одного или нескольких заместителей R1, R2, R5 и R6 или Y путем превращения одного такого заместителя в другой заместитель может осуществляться гидролизом, солеообразованием, подкислением, алкилированием, этерификацией, окислением или восстановлением. При гидролизе сложноэфирное или амидное производное распадается при взаимодействии с водой. Гидролиз катализируется кислотой или основанием, и гидролиз амида обычно требует более жестких условий (например, более высокой концентрации серной кислоты при 1-100oС в течение 1-5 ч), чем условия, необходимые для гидролиза сложных эфиров. Реакция гидролиза может также проводиться с водной хлористоводородной кислотой при 100-150 С и может потребовать такого длительного времени, как 18 ч. При солеобразовании свободная кислота превращается в соль посредством прибавления основного реагента, такого как водный раствор гидроксида натрия или триэтаноламин, который заменяет часть ионов водорода кислоты или один либо несколько катионов основания. Превращение соединения в его соответствующую кислотно-аддитивную соль осуществляют обработкой стехиометрическим количеством подходящей кислоты, такой как хлористо-водородная кислота. Как правило, свободное основание растворяют в полярном органическом растворителе, таком как метанол или этанол, и кислоту прибавляют в метаноле или этаноле. Поддерживается температура 0-50 С. Соответствующая соль осаждается спонтанно или может быть осаждена из раствора добавлением менее полярного растворителя. При подкислении химическое соединение превращается в кислоту. При алкилировании алкильная группа присоединяется или замещает соединение. Алкилирование проводится в подходящем растворителе, таком как ацетонитрил, ДМФ или ТГФ, при 0-160 С, обычно приблизительно при 25 С кипении и требует 1-18 ч. Наконец, реакция этерификации приводит к образованию по меньшей мере одного сложноэфирного производного. Вкратце, соединения реагирует с 1,0-5,0,предпочтительно 2,0 мол. экв. алканола, тиола или аммиака, моноалкил- или диалкиламина или гетероциклического аминоалканола, необязательно в присутствии 1,0-1,5, предпочтительно 1,25 мол. экв. третичного органического основания, такого как 4-диметиламинопиридин или предпочтительно триэтиламин, в органическом растворителе, таком как диоксан, тетрагидрофуран или предпочтительно дихлорметан. Реакция проходит при -10-50 С, предпочтительно при температуре окружающей среды в течение 124 ч, предпочтительно 4 ч. Некоторые соединения формулы I могут быть получены путем присоединения кислоты. Более того,соединения формулы I могут быть получены путем модификации K (где K имеет приведенные выше значения), например, алкилированием K, сопровождаемым замещением аминогруппой, при котором аминогруппа заменяет, например, уходящую группу, такую как S-метильная группа. В тех случаях, когда защитные группы могут быть введены и в конце удалены, приемлемыми защитами для амино-, гидрокси-, карбоксильных групп являются защиты, описанные в монографии Green и др., Protective Groups in Organic Synthesis, второе издание, изд-во John Wiley and Sons, New York, 1991. Активация карбоновых кислот может быть достигнута с использованием многих различных реагентов,как описано у Larock, Comprehensive Organic Transformations, изд-во VCH Publishers, New York, 1989. Пример 1. Соединения 3, 4, 8-16 и 19-93 получены в соответствии с реакционной схемой I и реакционной схемой II. Динатриевая соль 7-[(7-сульфо-2-нафтил)амино]карбониламинонафталин-2-сульфоновой кислоты (соединение 3). К 5,25 г (0,021 моль) 7-аминонафталин-2-сульфоновой кислоты, суспендированной в 80 мл воды,прибавляли раствор 6,5 мл 10 н. водного раствора NaOH (0,065 моль), разбавленного до 30 мл водой, и порциями раствор 3,20 г (0,011 моль) трифосгена в 30 мл ТГФ, чередуя таким образом, чтобы рН реакционной смеси поддерживать около 8. После окончания реакции по данным ТСХ (этилацетат-изопропанолвода, 6:2:1) значение рН снижали до 1 действием водной НСl, летучие вещества удаляли с помощью роторного испарителя. Твердый продукт собирали вакуумной фильтрацией и промывали водой. Получали 3,41 г соединения 3. Динатриевая соль 4-гидрокси-7-[5-гидрокси-7-сульфо(2-нафтил)амино]карбониламинонафталин 2-сульфоновой кислоты (соединение 4). К 10,77 г (0, 045 моль) 7-амино-4-гидроксинафталин-2-сульфоновой кислоты, растворенной в 45 мл 1 н. водного раствора NaOH, и 50 мл воды прибавляли 3,70 г (0, 045 моль) ацетата натрия. Значение рН раствора было около 9. Реакционную смесь охлаждали примерно до 5 С в бане со смесью льда с водой. Затем 2,23 г (0,045 моль) трифосгена, растворенного в 15 мл ТГФ, прибавляли тремя порциями. Значение рН реакционной смеси снизилось до 4-5 и было снова доведено до 7-8 путем прибавления по каплям 1 н. водного раствора NaOH. TCX (этилацетат-изопропанол-вода, 6:2:1) указывала на то, что реакция не завершена. Прибавляли порциями еще 2,20 г (0,045 моль) трифосгена в 10 мл ТГФ, сохраняя значения рН выше 7 с помощью прибавления 1 н. водного раствора NaOH. Когда по данным ТСХ реакция была признана законченной, значение рН снижали с водной НСl до 1 и летучие вещества удаляли с помощью роторного испарителя. Твердый продукт собирали вакуумной фильтрацией. Получали 10,85 г соединения 4. 4-Метилфениловый эфир 3-аминобензолсульфоновой кислоты (соединение 5). К 50 г (0,463 моль) n-крезола (4-метилфенола) и 37 мл (0,458 моль) пиридина, растворенного в 250 мл хлороформа, прибавляли 50 г (0,226 моль) 3-нитробензолсульфонилхлорида. Реакционную смесь оставляли перемешиваться при температуре окружающей среды. Через 2 ч по данным ТСХ реакция была признана законченной и летучие вещества удаляли с помощью роторного испарителя. Полученный остаток обрабатывали 400 мл 0,5 М раствора бикарбоната натрия. Нерастворимый продукт собирали и промывали раствором бикарбоната натрия (2 раза по 200 мл) и водой (2 раза по 300 мл). Затем твердое вещество обрабатывали метанолом (200 мл), затем водой (200 мл). Твердое вещество собирали вакуумной фильтрацией и промывали водой. Полученное твердое вещество обрабатывали 170 г (0, 897 моль) дихло- 17006763 рида олова, растворенного в 250 мл концентрированной НСl. Реакцию оставляли перемешиваться при температуре окружающей среды в течение 40 ч. Данные ТСХ указывали на то, что реакция не завершена,поэтому реакционную смесь нагревали при 50 С в течение 27 ч. Твердый осадок собирали с помощью вакуумной фильтрации и промывали 6 н. НСl. Твердое вещество экстрагировали этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили над сульфатом магния, фильтровали, летучие вещества удаляли с помощью роторного испарителя, получая 42,5 г соединения 5 в виде масла, которое затвердевало при стоянии.N-[7-(Хлорсульфонил)(2-нафтил)][7-(хлорсульфонил)(2-нафтил)]аминокарбоксамид (соединение 6). К 2,35 г (4,86 ммоль) соединения 3 прибавляли 116 мл сульфолана, 25 мл ацетонитрила, 31 мл хлорокиси фосфора и 1 мл диметилацетамида (ДМА). Реакцию оставляли перемешиваться в течение 72 ч при температуре окружающей среды. Образовывался почти прозрачный раствор. Реакционную смесь выливали на 1,5 л льда и колбу помещали в баню со льдом. После того как весь лед расплавился, твердое вещество собирали вакуумной фильтрацией и промывали водой. Твердое вещество сушили в высоком вакууме в течение 24 ч. Получали 2,56 г соединения 6. 7-[(7-(Хлорсульфонил)-5-гидрокси(2-нафтиламино]карбониламино-4-гидроксинафталин-2 сульфонилхлорид (соединение 7). К 500 мг (0,912 ммоль) соединения 4, суспендированного в 8 мл хлорокиси фосфора, прибавляли 25 мл смеси сульфолан-ацетонитрил (1:1 по объему) и 0,5 мл диметилацетамида. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Реакционная смесь превращалась в прозрачный раствор, который выливали на 500 мл льда. Полученную смесь помещали в баню со льдом и давали нагреться до комнатной температуры. Образующееся твердое вещество собирали вакуумной фильтрацией и промывали водой. Твердое вещество сушили в высоком вакууме в течение 24 ч. Получали 412 мг соединения 7. 7-[(7-[(3-[(4-Метилфенил)оксисульфонил]фениламино)сульфонил]-2-нафтиламино)карбониламино]нафталин-2-сульфоновая кислота (соединение 8) и 4-метилфениловый эфир 3-[(7-[(N-7-[(3-[(4 метилфенил)оксисульфонил]фениламино)сульфонил]-2-нафтилкарбамоил)амино]-2-нафтилсульфонил)амино]бензолсульфоновой кислоты (соединение 9). К 250 мг (0,95 ммоль) 4-метилфенилового эфира 3-аминобензолсульфоновой кислоты (соединение 5), растворенного в 40 мл пиридина, прибавляли раствор 250 мг (0,49 ммоль) соединения 6 в 5 мл ТГФ. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 3 ч. Затем реакционную смесь экстрагировали этилацетатом и 1 н. НСl. Органический слой сушили над сульфатом магния, фильтровали, летучие вещества удаляли с помощью роторного испарителя. Продукты очищали обращенно-фазовой высокоэффективной жидкостной хроматографией (ОФ-ВЭЖХ) (фаза С 18, колонка 30250 мм), используя буферную систему с трифторуксусной кислотой (ТФК) (буфер А: 5% ацетонитрил, 95% вода, 0,05% ТФК; буфер Б: 95% ацетонитрил, 5% вода, 0,05% ТФК; 35 мл/мин, 0-100% Б за 45 мин). Фракции, содержащие соединение, элюированное первым, объединяли и лиофилизовали, получая 9 мг соединения 8. Фракции, содержащие соединение, элюированное позже, объединяли и лиофилизовали,получая 51 мг соединения 9. 4-Гидрокси-7-[(5-гидрокси-7-[(3-[(4-метилфенил)оксисульфонил]фениламино)сульфонил](2 нафтил)амино)карбониламино]нафталин-2-сульфоновая кислота (соединение 10) и 4-метилфениловый эфир 3-[(4-гидрокси-7-[(N-5-гидрокси-7-[(3-[(4-метилфенил)оксисульфонил]фениламино)сульфонил](2-нафтил)сульфонил)амино]бензолсульфоновой кислоты (соединение 11). К 250 мг (0,95 ммоль) 4-метилфенилового эфира 3-аминобензолсульфоновой кислоты (соединение 5), растворенного в 40 мл пиридина, прибавляли раствор 265 мг (0,49 ммоль) соединения 7 в 5 мл ТГФ. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 3 ч. Затем реакционную смесь экстрагировали этилацетатом и 1 н. НСl. Органический слой сушили над сульфатом магния, фильтровали, летучие вещества удаляли с помощью роторного испарителя. Продукты очищали ОФ-ВЭЖХ (фаза С 18, колонка 30250 мм), используя буферную систему с трифторуксусной кислотой(ТФК) (буфер А: 5% ацетонитрил, 95% вода, 0,05% ТФК; буфер Б: 95% ацетонитрил, 5% вода, 0,05% ТФК; 35 мл/мин, 0-100% Б за 60 мин). Фракции, содержащие соединение, элюированное первым, объединяли и лиофилизовали, получая 15 мг соединения 10. Фракции, содержащие соединение, элюированное позже, объединяли и лиофилизовали, получая 65 мг соединения 11. Динатриевая соль 7-[(7-[(3-сульфофенил)амино]сульфонил-2-нафтил)амино]карбониламино нафталин-2-сульфоновой кислоты (соединение 12). К 8 мг (0,011 ммоль) соединения 8 прибавляли 2 мл 5 н. NaOH. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 6 ч. Реакционную смесь подкисляли 6 н. НСl,и раствор наносили на небольшую экстракционную колонку с обращенной (С 18) твердой фазой. Колонку промывали водой, затем смесью ацетонитрил-вода (50:50, по объему), чтобы элюировать продукт. Получали 5 мг соединения 12. Динатриевая соль 3-[(7-[N-(7-[(3-сульфофенил)амино]сульфонил-2-нафтил)карбамоил]амино- 18006763 2-нафтил)сульфонил]аминобензолсульфоновой кислоты (соединение 13). К 35 мг (0,036 ммоль) соединения 9 прибавляли 2 мл 5 н. NaOH. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 6 ч. Реакционную смесь подкисляли 6 н. НСl и раствор наносили на небольшую экстракционную колонку с обращенной фазой (С 18). Колонку промывали водой, затем смесью ацетонитрил-вода (50:50 по объему), чтобы элюировать продукт. Получали 26 мг соединения 13. 4-Гидрокси-7-[(5-гидрокси)-7-[(3-сульфофенил)амино]сульфонил(2-нафтил)амино]карбониламинонафталин-2-сульфоновая кислота (соединение 14). Данное соединение получали из соединения 10 в соответствии с методикой, описанной для синтеза соединения 12. 3-[(4-Гидрокси-7-[N-(5-гидрокси-7-[(3-сульфофенил)амино]сульфонил(2-нафтилкарбамоил] амино-2-нафтил)сульфонил]аминобензолсульфоновая кислота (соединение 15). Данное соединение получали из соединения 11 в соответствии с методикой, описанной для синтеза соединения 12. Динатриевая соль 3-бром-7-[(6-бром-5-гидрокси-7-сульфо(2-нафтиламино]карбониламино-4 гидроксинафталин-2-сульфоновой кислоты (соединение 16). К раствору 123 мг (0,22 ммоль) соединения 4 в 1 мл воды и 2 мл диоксана прибавляли 300 мкл 1 М раствора брома в четыреххлористом углероде. Через 1 ч к реакционной смеси снова прибавляли 200 мкл раствора брома. Еще через 1 ч к реакционной смеси прибавляли дополнительные 150 мкл раствора брома. Через 30 мин реакционную смесь выливали в 100 мл ТГФ, получая коричневый осадок, который собирали вакуумной фильтрацией. Требуемый продукт очищали хроматографией на колонке с силикагелем(этилацетат-изопропанол-вода, 5:2:1), получая 17 мг соединения 16. Пример 2. Альтернативный способ синтеза соединений по изобретению показан на реакционной схеме II. Данный способ применим для синтеза больших количеств требуемых продуктов и иллюстрируется синтезом соединения 15. Реакционная схема II 6-(Ацетиламино)-3-(хлорсульфонил)нафтилацетат (соединение 17). К 50 г (0,209 ммоль) соединения 2 прибавляли 100 мл уксусного ангидрида и 100 мл пиридина. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Твердый осадок собирали вакуумной фильтрацией. Получали 83 г продукта, который сушили в высоком вакууме. К этому твердому веществу прибавляли 260 мл хлорокиси фосфора. Данную суспензию оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Затем темный раствор выливали на 3 л льда. После того, как весь лед растаял (около 3 ч), твердое вещество собирали вакуумной фильтрацией и промывали водой. Твердое вещество сушили в вакууме, получая 50 г соединения 17. Натриевая соль 3-[(7-амино-4-гидрокси-2-нафтил)сульфонил]аминобензолсульфоновой кислоты(соединение 18). К 25 г (0,095 моль) соединения 5, растворенного в 200 мл ТГФ, прибавляли 8,1 мл пиридина. Затем прибавляли 36,3 г (0,106 моль) соединения 17, сопровождаемого дополнительными 200 мл ТГФ. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Затем летучие вещества удаляли и полученный остаток распределяли между этилацетатом и 1 н. НСl. Органический слой промывали насыщенным раствором соли, обрабатывали сульфатом магния, фильтровали, летучие- 19006763 вещества удаляли с помощью роторного испарителя. Полученное твердое вещество растворяли в 220 мл 5 н. NaOH и 30 мл диоксана. Раствор нагревали при 80 С в течение 5 ч. Затем значение рН раствора снижали до 1 действием концентрированной НСl. Твердое вещество собирали вакуумной фильтрацией, затем растворяли в 200 мл воды с 20 мл 5 н. NaON. Раствор нагревали, получая мутный раствор, который фильтровали в горячем виде, чтобы получить прозрачный раствор. Раствор разбавляли водой до объема 1,5 л, затем рН доводили до 1 с помощью 6 н. НСl. Образовывался твердый осадок. Суспензию охлаждали в холодильнике в течение ночи и твердое вещество собирали вакуумной фильтрацией, получая после высушивания 21 г соединения 18. Динатриевая соль 3-[(4-гидрокси-7-[N-(5-гидрокси-7-[(3-сульфофенил)амино]сульфонил(2 нафтилкарбамоил]амино-2-нафтил)сульфонил]аминобензолсульфоновой кислоты (соединение 15). К 17,7 г (0,045 моль) соединения 18 прибавляли 250 мл ацетатного буфера (1 М NaOАс/НОАс, рН 4,6) и 50 мл ТГФ. Образовался темно-коричневый раствор. Раствор 4,4 г (15 ммоль) трифосгена в 40 мл ТГФ прибавляли по каплям к упомянутому выше раствору в течение 3 ч и 10 мин. По данным ВЭЖХ реакция прошла полностью. Реакционную смесь подкисляли концентрированной НСl (15 мл). Все летучие вещества удаляли с помощью роторного испарителя, оставшийся вязкий остаток соупаривали с ацетонитрилом, смесью ацетонитрил/гептан и затем с гептаном. Образующееся твердое вещество растворяли в 140 мл воды при нагревании. Затем прибавляли 250 мл насыщенного раствора соли. Образовалось твердое вещество. Содержимое колбы выдерживали при 4 С в течение 15 ч и затем твердое вещество собирали вакуумной фильтрацией. Твердое вещество промывали небольшим количеством смеси охлажденная льдом вода-насыщенный раствор соли, 3:1. После сушки в высоком вакууме получали 19,2 г соединения 15. Следующие соединения (табл. 1) получены согласно тем же общим методикам, которые приведены на реакционной схеме I или реакционной схеме II и подробно описаны в приведенных выше методиках синтеза соединений 3-18. Разнообразные вещества, которые были использованы вместо соединения 5 для синтеза соединений 19-91, или приобретены у коммерческих поставщиков, или получены стандартными способами, известными специалистам в этой области. Соединения с кислотными группами представлены в табл. 1 в форме свободной кислоты. Пример 3. Соединения 94-102 синтезированы в соответствии с методиками, приведенными на реакционной схеме III. Диаммониевая соль 7-[(5-[(этоксикарбонил)метокси]-7-сульфо(2-нафтил)амино)карбониламино]4-гидроксинафталин-2-сульфоновой кислоты (соединение 94) и диаммониевая соль 4-[(этоксикарбонил)метокси]-7-[(5-[(этоксикарбонил)метокси]-7-сульфо(2-нафтил)амино)карбониламино]нафталин-2 сульфоновой кислоты (соединение 95). К 275 г (0,5 ммоль) соединения 4, суспендированного в 50 мл этанола, прибавляли 2,5 мл 0,2 М раствора этилата натрия в этаноле. Затем прибавляли 56 мкл (0,5 ммоль) этилового эфира бромуксусной кислоты. Смесь перемешивали при кипении в течение 2 ч. Затем твердое вещество отделяли фильтрованием, летучие вещества удаляли из фильтрата, получая 220 мг неочищенного продукта. Продукты очищали обращенно-фазовой ВЭЖХ (фаза С 18, колонка 20250 мм), используя буферную систему с ацетатом аммония (NH4OAc) (буфер А: 5% ацетонитрил, 95% вода, 50 мМ NH4OAc; буфер Б: 70% ацетонитрил, 30% вода, 15 мМ NH4OAc; 15 мл/мин, 0-100% Б за 30 мин). Фракции, содержащие первое элюируемое соединение, объединяли и лиофилизовали, получая 60 мг соединения 94. Фракции, содержащие последнее элюируемое соединение, объединяли и лиофилизовали, получая 32 мг соединения 95. Динатриевая соль 2-(6-[N-(5-гидрокси-7-сульфо(2-нафтилкарбамоил]амино-3-сульфонафтилокси)уксусной кислоты (соединение 96). 25 мг (0,04 ммоль) соединения 94 прибавляли 1 мл 5 н. NaOH. Раствор оставляли при перемешивании в течение 18 ч при температуре окружающей среды. Значение рН уменьшали до 1 с помощью водной НСl, образующееся твердое вещество собирали вакуумной фильтрацией, получая 16 мг соединения 96. Динатриевая соль 2-[6-(N-[5-(карбоксиметокси)-7-сульфо(2-нафтил)]карбамоиламино)-3-сульфонафтилокси]уксусной кислоты (соединение 97). Соединение 95 обрабатывали, как описано выше для соединения 94, получая 11 мг соединения 97. Следующие соединения (табл. 2) получали в соответствии с теми же самыми общими методиками,которые представлены на реакционной схеме III и подробно описаны выше в методиках синтеза соединений 94-97. Разнообразные вещества, которые были использованы вместо этилового эфира бромуксусной кислоты для синтеза соединений 98-102, или приобретены у коммерческих поставщиков, или получены стандартными способами, известными специалистам в данной области. Все соединения приведены в табл. 2 в виде свободных кислот. Таблица 2 Пример 4. Соединения 103-105 синтезированы в соответствии с методикой, представленной на реакционной схеме IV. Реакционная схема IV Дикалиевая соль 3-метил[(7-[метил(3-сульфофенил)амино]сульфонил(2-нафтиламино]карбониламино-(2-нафтил)сульфонил]аминобензолсульфоновой кислоты (соединение 103). К 59 мг (0,071 ммоль) соединения 13 прибавляли 2 мл ДМФ. После этого прибавляли 38 мг карбоната калия. Перемешиваемую суспензию нагревали при 70 С в масляной бане. Затем прибавляли 36 мкл йодметана. Реакционную смесь нагревали в течение 3 ч, после чего летучие вещества удаляли с помощью роторного испарителя. Полученное твердое вещество растворяли в воде и наносили на экстракционную колонку с твердой фазой С 18. Колонку промывали 9 объемами воды. Продукт элюировали 80% ацетонитрилом, получая после упаривания летучих веществ 55 мг соединения 103. Соединения 104 и 105 (табл. 3) получали по той же общей методике, которая приведена выше для синтеза соединения 103, за исключением того, что вместо йодистого метила использовали аллилбромид и вместо соединения 13 использовали соединение 48. Соединения с кислотными группами приведены в табл. 3 в виде свободных кислот. Таблица 3 Пример 5. Соединения 112-114 и 116 синтезировали в соответствии с методиками, представленными на реакционной схеме V. 7-(Флуорен-9-илоксикарбониламино)нафталин-2-карбоновая кислота (соединение 107). К 0,504 г (2,70 ммоль) 7-аминонафталин-2-карбоновой кислоты (106; получена по методике Harrison H.A., Royle F.A., J. Chem. Soc., 1926, 84) прибавляли 10 мл диоксана, 5 мл 10% раствора карбоната натрия и 35 мл воды. К данному прозрачному раствору прибавляли порциями 0,786 г (2,97 ммоль) 9 флуоренилметоксикарбонилхлорида (fmoc-Cl) в течение 15 мин. Через 3 ч реакционную смесь подкисляли 1 н. НСl, полученный белый осадок собирали вакуумной фильтрацией. Данное твердое вещество суспендировали в диэтиловом эфире, получая осадок, который собирали вакуумной фильтрацией. Получали 0,948 г соединения 107. 4-Метилфениловый эфир 3-[7-(флуорен-9-илоксикарбониламино)-2-нафтил]карбониламино бензолсульфоновой кислоты (соединение 108). К 104 мг (0,026 ммоль) соединения 107 прибавляли 6,5 мл хлороформа, 1,3 мл тионилхлорида и 100 мкл пиридина. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 3 ч, затем все летучие вещества удаляли в вакууме. Остаток дважды соупаривали с хлороформом. К полученному твердому веществу, суспендированному 15 мл хлороформа, прибавляли 74 мг(0,033 ммоль) пиридина в виде раствора в 1,5 мл хлороформа. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч, после чего распределяли между этилацетатом и 1 н. НСl (водной). Органический слой сушили (сульфатом магния), фильтровали и летучие вещества удаляли в вакууме. Полученный остаток обрабатывали диэтиловым эфиром, твердый осадок собирали вакуумной фильтрацией. Получали 110 мг соединения 108. 4-Метилфениловый эфир 3-[(7-амино-2-нафтил)сульфонил]аминобензолсульфоновой кислоты(соединение 110). К 104 мг (0,16 ммоль) соединения 108 прибавляли 9 мл ТГФ и 360 мкл пиперидина. Полученный прозрачный раствор оставляли перемешиваться в течение 6 ч. Затем реакционную смесь экстрагировали этилацетатом и 1 н. НСl (водной). Высушенный органический слой (сульфатом магния) фильтровали,летучие вещества удаляли в вакууме. Полученный остаток растворяли в дихлорметане и 3 мл 1 н. НСl в диэтиловом эфире и прибавляли 50 мл диэтилового эфира, чтобы получить осадок, который собирали центрифугированием. После высушивания получали 75 мг соединения 110 в виде гидрохлоридной соли. 4-Метилфениловый эфир 3-[(7-[(N-7-[(3-[(4-метилфенил)оксисульфонил]фениламино)сульфонил]-2-нафтилкарбамоил)амино]-2-нафтилсульфонил)амино]бензолсульфоновой кислоты (соединение 112). К 75 мг (0,17 ммоль) соединения 110, растворенного в 3 мл ТГФ и 1 мл воды, прибавляли чередующимися порциями раствор 280 мкл 5 н. NaOH (водного) в 1 мл воды, затем раствор 54 мг (0,18 ммоль) трифосгена в 1 мл ТГФ. Летучие вещества удаляли до тех пор, пока не образовались твердое вещество и прозрачный раствор. Раствор декантировали, твердое вещество растворяли в дихлорметане и упаривали 3 раза. Полученный таким образом нерастворимый в дихлорметане продукт собирали вакуумной фильтрацией, получая 24 мг соединения 112. Динатриевая соль 3-[(7-[N-(7-[(3-cvльфoфeнил)aминo]cyльфoнил-2-нaфтил)кapбaмoил]aминo- 29006763 2-нафтил)сульфонил]амино)бензолсульфоновой кислоты (соединение 114). К 20 мг (0,02 моль) соединения 112 прибавляли 1,5 мл 1,37 М метилата натрия в метаноле, 1 мл воды и 0,5 мл ТГФ. Полученный раствор оставляли перемешиваться при температуре окружающей среды в течение 2 дней. Реакционную смесь подкисляли 1 н. НСl (водной) и органические летучие вещества удаляли в вакууме. Твердый осадок собирали вакуумной фильтрацией, получая 15 мг соединения 114. Метиловый эфир 3-(7-[(флуорен-9-илметокси)карбониламино]-2-нафтилкарбониламино)бензойной кислоты (соединение 109). К 305 мг (0,75 ммоль) соединения 107 прибавляли 10 мл хлороформа, 3,5 мл тионилхлорида и 180 мкл пиридина. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение трех часов с последующим удалением летучих веществ с помощью роторного испарителя. Полученный остаток соупаривали три раза с хлороформом. Затем прибавляли 50 мл хлороформа, 124 мг(0,82 ммоль) метилового эфира 3-аминобензойной кислоты и 100 мкл пиридина. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Реакционную смесь экстрагировали дважды 1 н. НСl (водной) и один раз водой. Высушенный органический слой (сульфатом магния) фильтровали и летучие вещества удаляли с помощью роторного испарителя. Полученный остаток обрабатывали метанолом, чтобы образовался твердый осадок, который собирали вакуумной фильтрацией. Получали 380 мг соединения 109. Метиловый эфир 3-[(7-амино-2-нафтил)карбониламино]бензойной кислоты (соединение 111). К 380 мг (0,70 ммоль) соединения 109 прибавляли 30 мл дихлорметана, 3 мл ТГФ и 1 мл пиперидина. Полученный прозрачный раствор оставляли перемешиваться в течение 3 ч. Затем реакционную смесь экстрагировали этилацетатом и 1 н. НСl (водной). Высушенный органический слой (сульфатом магния) фильтровали, летучие вещества удаляли в вакууме. Полученный остаток растворяли в дихлорметане и прибавляли 3 мл 1 н. НСl в диэтиловом эфире и 50 мл диэтилового эфира для образования осадка, который собирали вакуумной фильтрацией. После высушивания получали 212 мг соединения 111 в виде гидрохлоридной соли. Метиловый эфир 3-[(7-[N-(7-N-[3-(метоксикарбонил)фенил]карбамоил-2-нафтил)карбамоил] амино-2-нафтил)карбониламино]бензойной кислоты (соединение 113). К 21 мг (0,07 ммоль) соединения 111, растворенного в 2 мл ТГФ и 1 мл воды, прибавляли чередующимися порциями раствор 112 мкл 5 н. NaOH (водного) в 1 мл воды, затем раствор 28 мг (0,10 ммоль) трифосгена в 1 мл ТГФ. Реакционную смесь подкисляли 1 н. НСl и летучие вещества удаляли до тех пор,пока не образовались твердый осадок и прозрачный раствор. Твердое вещество собирали вакуумной фильтрацией, получая 21 мг соединения 113. 3-[(7-Амино-2-нафтил)карбониламино]бензойная кислота (соединение 115). К 51 мг (0,16 ммоль) соединения 111 прибавляли 1 мл метанола, 1 мл воды и 800 мкл 1 н. гидроксида лития (водного). Реакционную смесь оставляли перемешиваться в течение 16 ч при температуре окружающей среды. Значение рН раствора снижали до 3 с 1 н. НСl (водной), летучие вещества удаляли в вакууме. Полученное твердое вещество суспендировали в воде и собирали вакуумной фильтрацией. Получали 16 мг соединения 115. 3-(7-[(N-7-[N-(3-Карбоксифенил)карбамоил]-2-нафтилкарбамоил)амино]-2-нафтилкарбониламино)бензойная кислота (соединение 116). К 10 мг (0,03 ммоль) соединения 115, растворенного в 2 мл ТГФ и 1 мл воды, прибавляли чередующимися порциями раствор 40 мкл 5 н. NaOH (водного) в 0,2 мл воды, затем раствор 4 мг (0,02 ммоль) трифосгена в 0,2 мл ТГФ. Реакционную смесь подкисляли 1 н. НСl, летучие вещества удаляли в вакууме. Твердое вещество собирали вакуумной фильтрацией, получая 9 мг соединения 116. Соединения 112-114 и 116, которые получены с помощью описанных выше методик, приведены в табл. 4. Соединения с кислотными группами приведены в виде свободных кислот. Таблица 4
МПК / Метки
МПК: C07D 211/96, C07D 233/32, C07D 335/18, A61K 31/18, C07C 311/47, C07C 309/51, C07C 335/32, C07D 213/76, C07D 257/04, A61K 31/395
Метки: нафталинмочевины, глюкозы, поглощения, усилители
Код ссылки
<a href="https://eas.patents.su/30-6763-naftalinmocheviny-kak-usiliteli-pogloshheniya-glyukozy.html" rel="bookmark" title="База патентов Евразийского Союза">Нафталинмочевины как усилители поглощения глюкозы</a>
Предыдущий патент: Противовирусный агент
Следующий патент: Частица, содержащая органические вещества, имеющая повышенную температуру самовозгорания
Случайный патент: Лечение стресса и предварительное формирование условных рефлексов против стресса