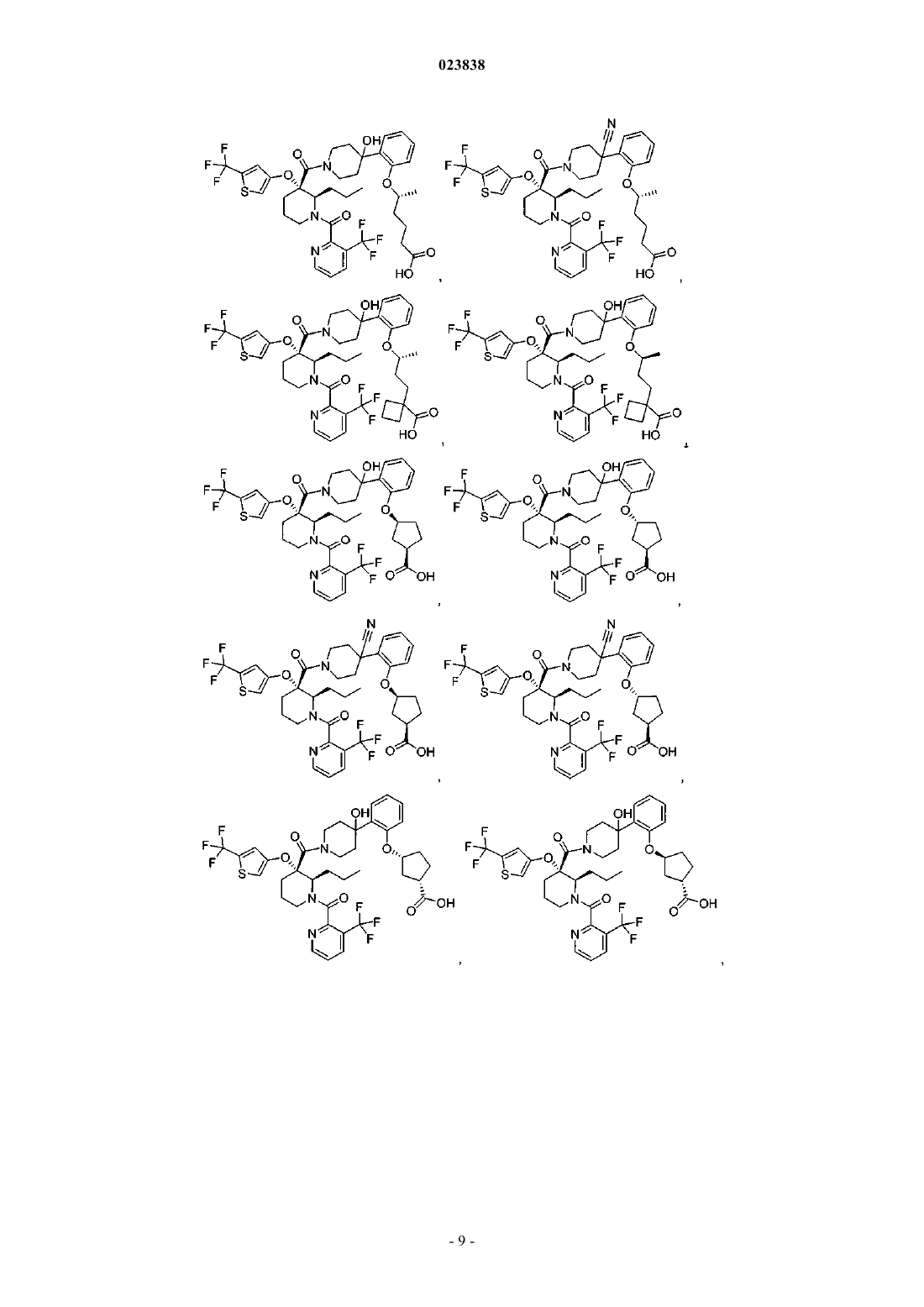
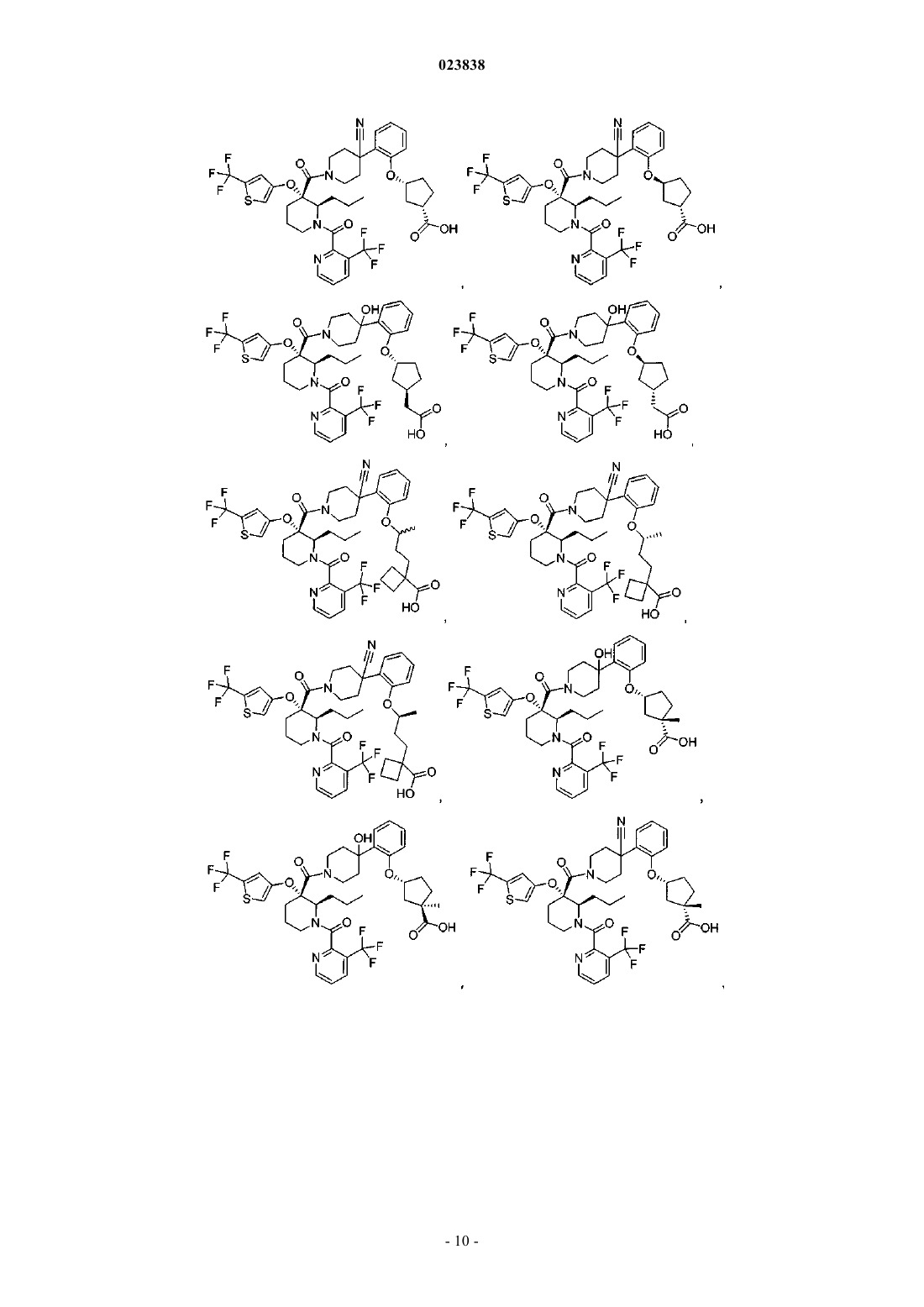
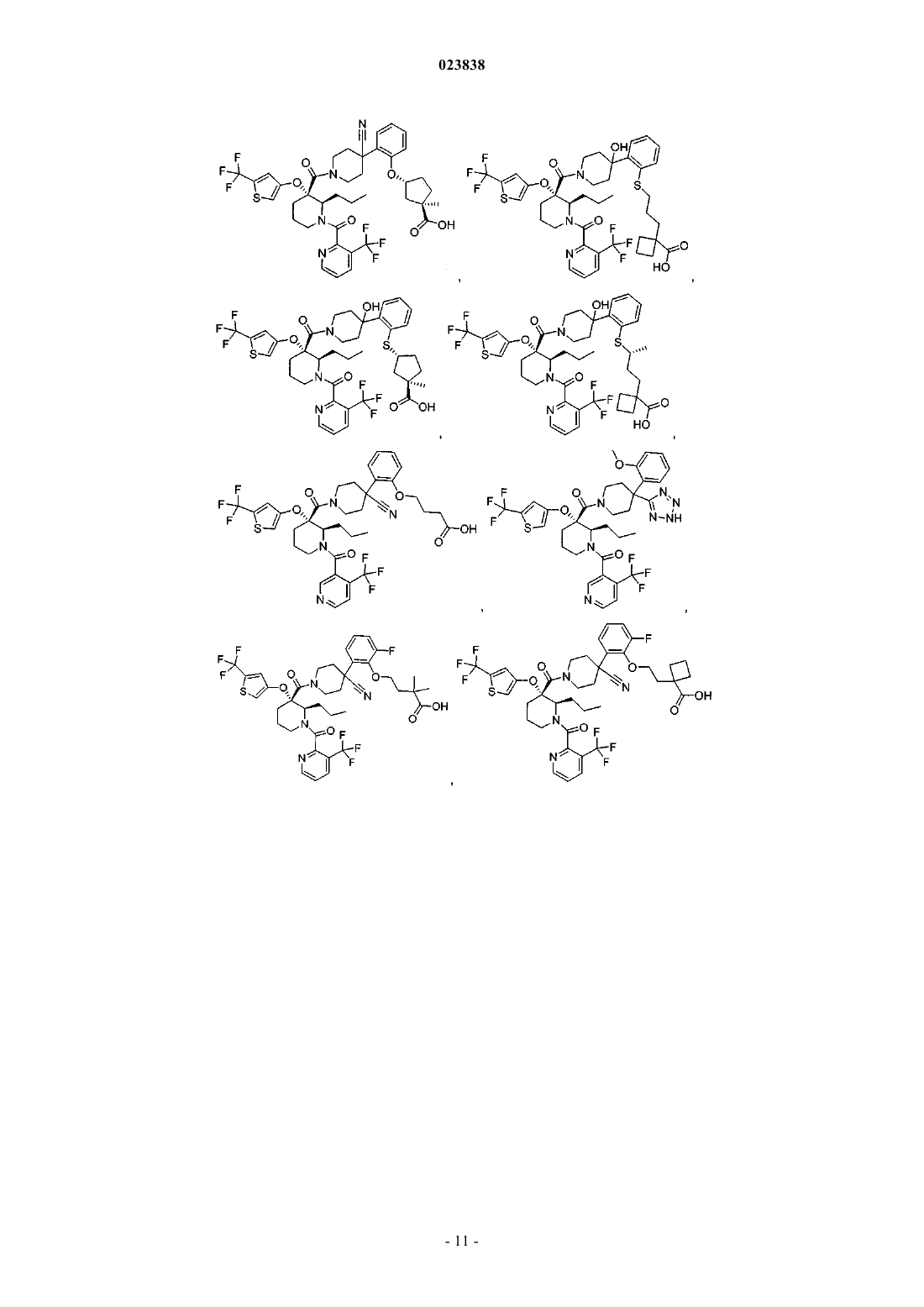
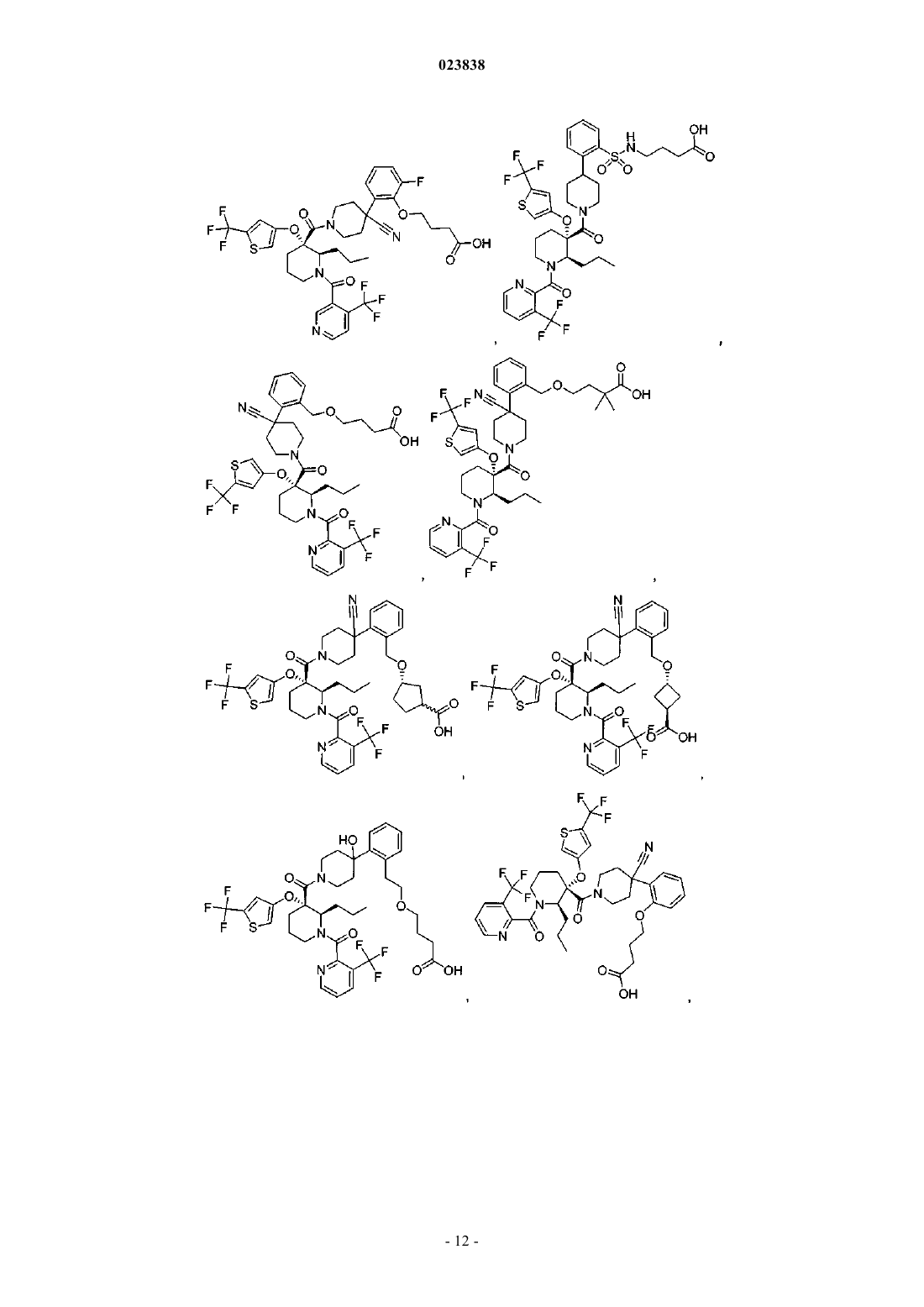
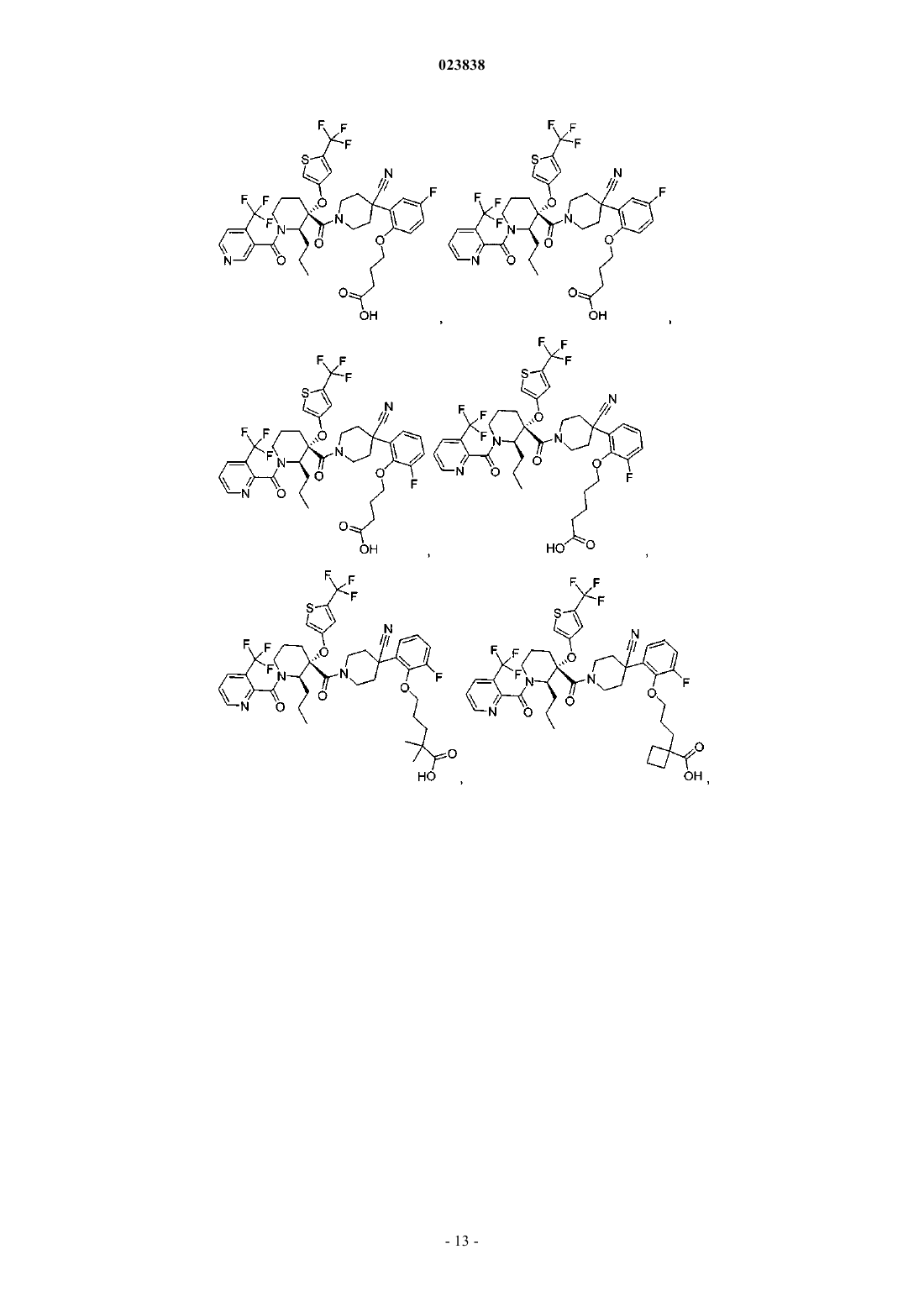
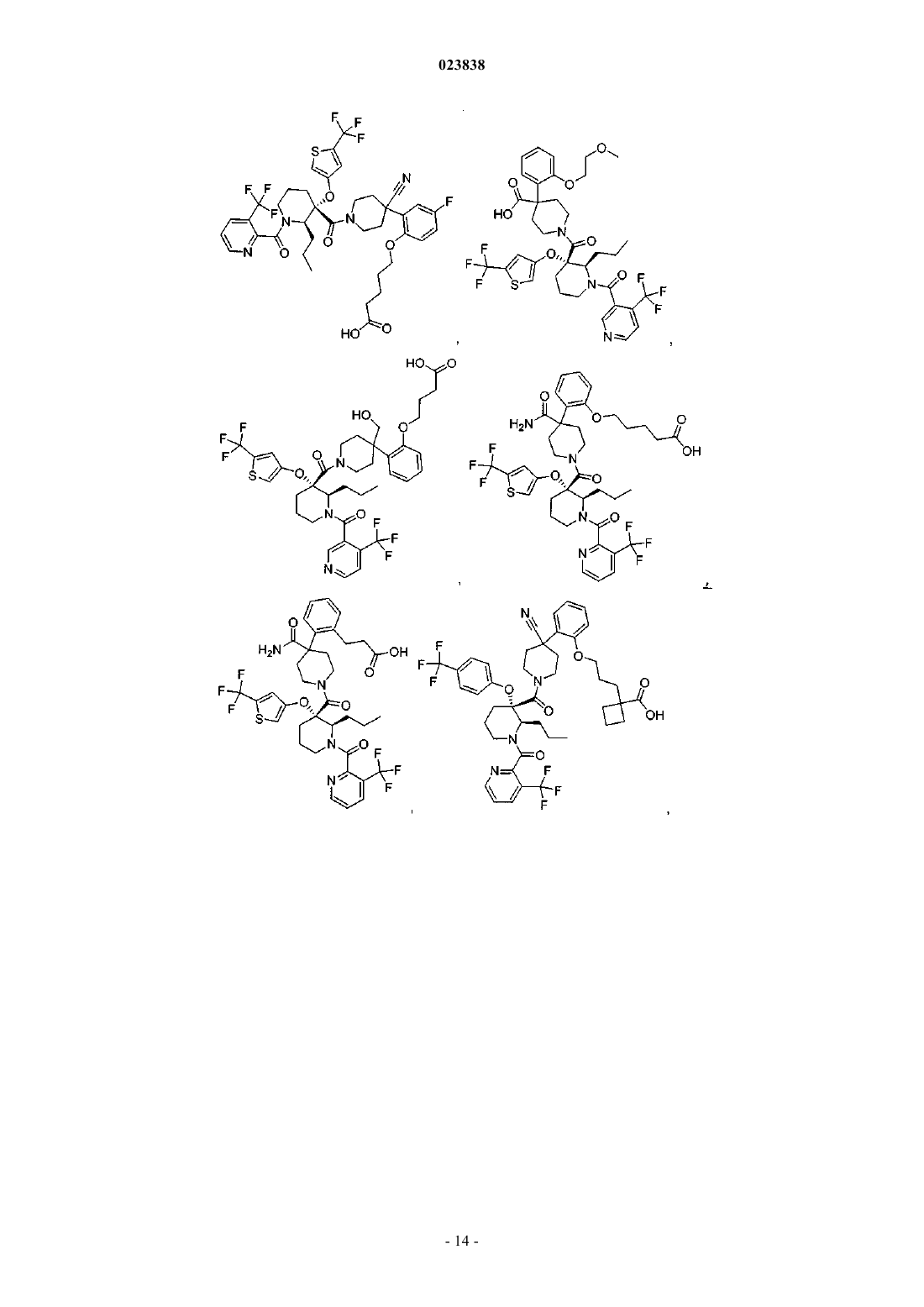
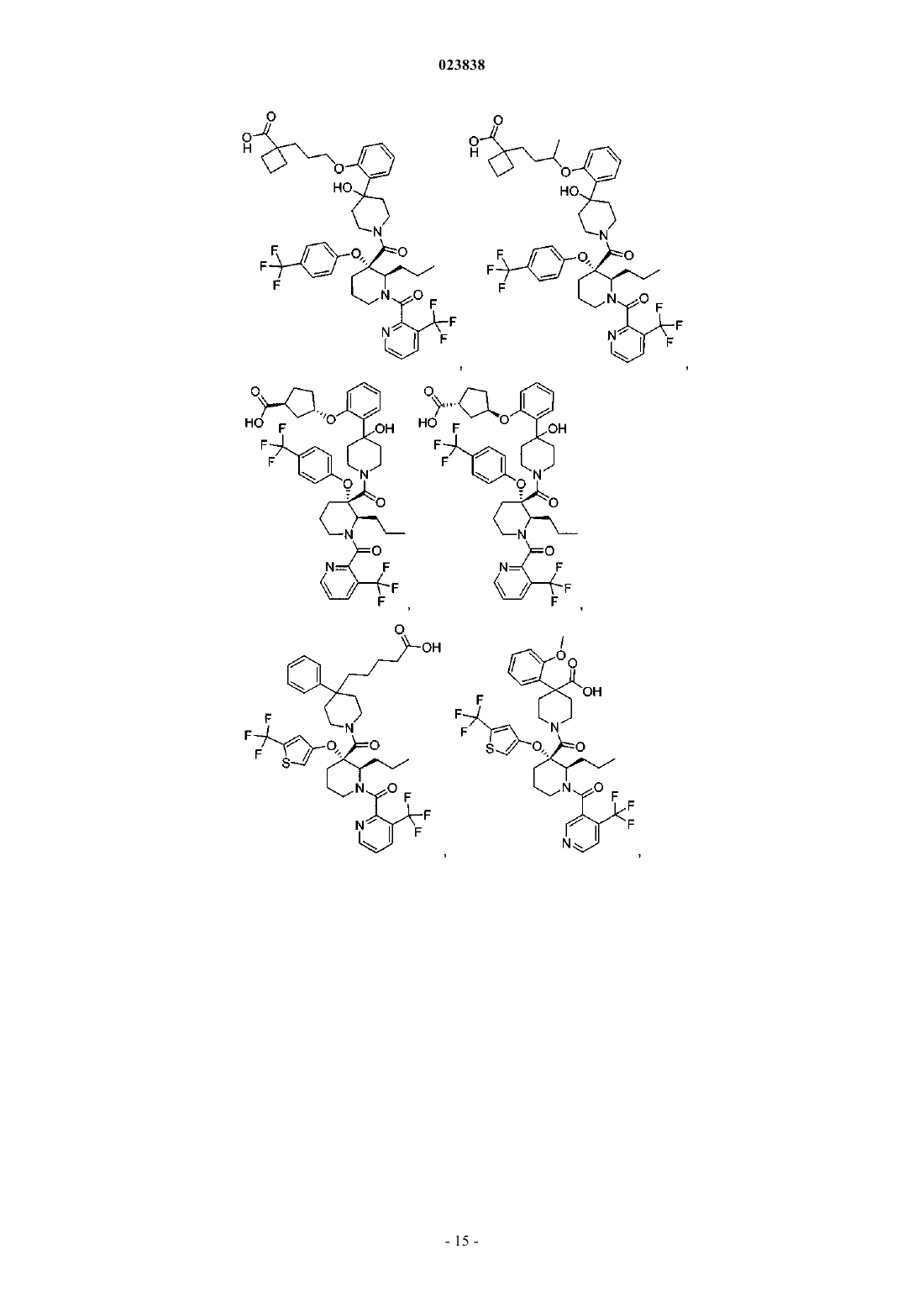
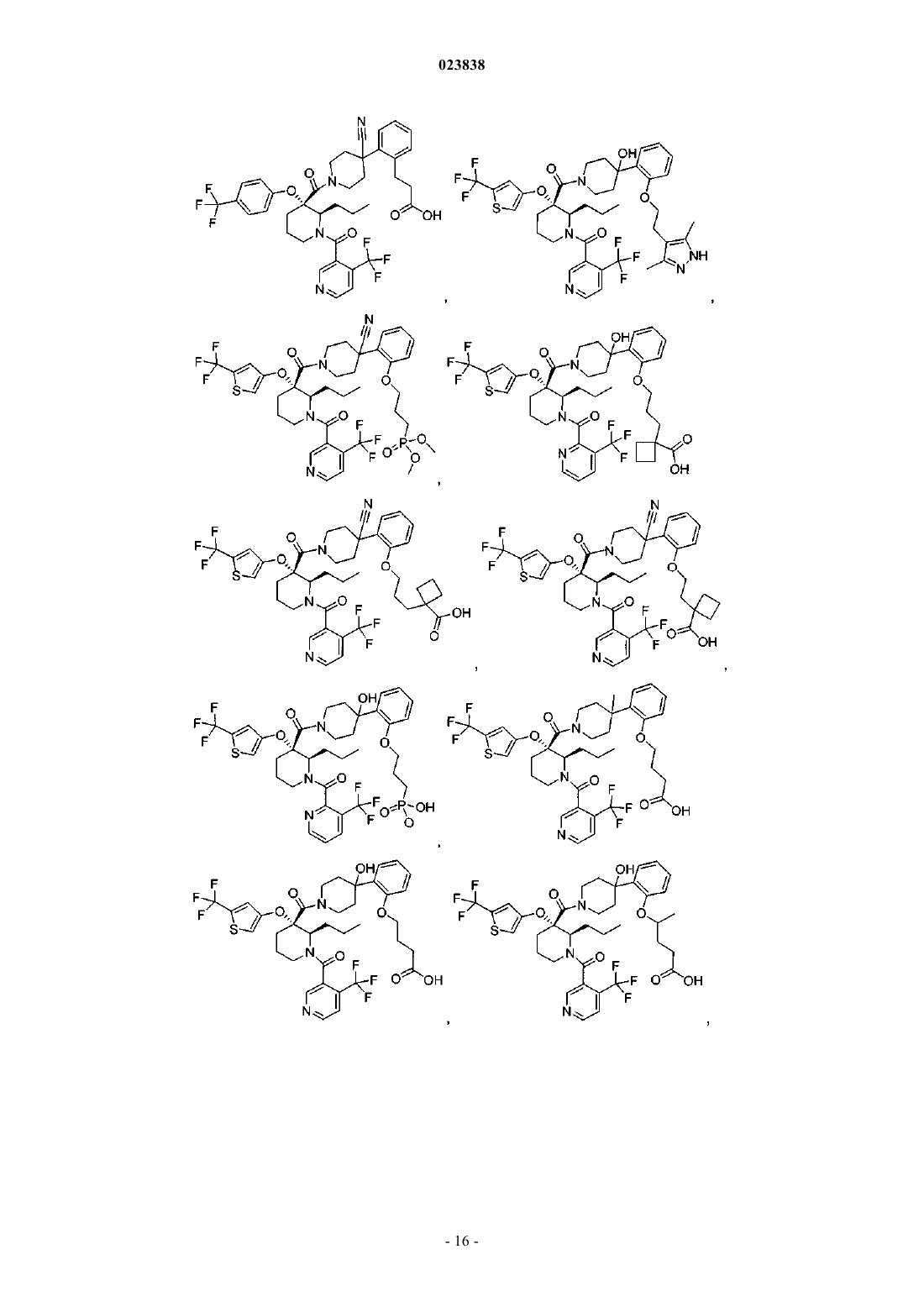
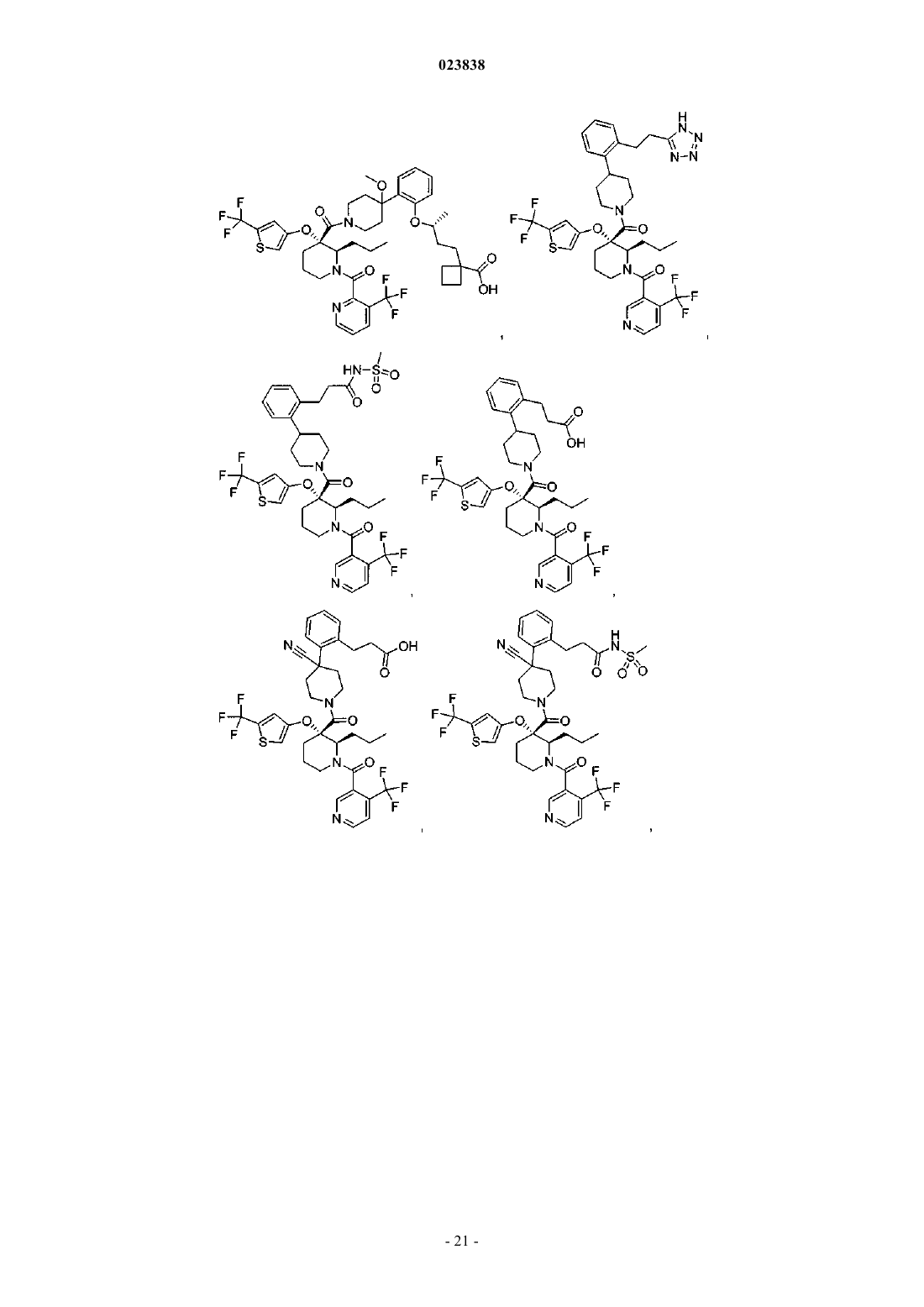
Замещенные пиперидины, которые повышают активность p53, и их применение
Номер патента: 23838
Опубликовано: 29.07.2016
Авторы: Восс Мэттью Эрнст, Маккосс Малкольм, Скапин Джованна, Долл Рональд Дж., Шиппс Джеральд В., Жибо Крейг Р., Тянь Юань, Ринджен Дайан, Ван Яолинь, Зайдель-Дуган Синтия, Божен Стефан Л., Номеир Амин, Кирова-Сноувер Маргарита, Ма Яо, Лю Юань, Сидзука Манами, Кулкарни Бхимашанкар А., Пан Вэйдун, Лахью Брайан Роберт, Гюзи Тимоти Дж., Наир Латха Г., Хиклин Дэнни Дж.
Формула / Реферат
1. Соединение формулы 1
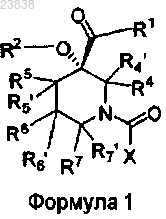
или его фармацевтически приемлемая соль,
где R1 представляет собой
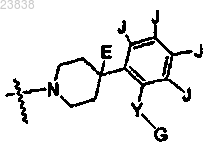 ,
,в которой Е выбран из группы, включающей Н, галоген, ОН, CN, -O(C1-С6)алкил, -(C1-C6)алкил, -С(О)ОН, -C(O)NR8R8', -(C1-C6)алкил-С(О)ОН, -(C1-C6)алкил-ОН, -(C1-C6)алкил-С(О)NR8R8', -(С2-С6)алкенил и -(С2-С6)алкинил;
каждый J независимо выбран из Н и галогена;
Y может присутствовать или отсутствовать, когда Y присутствует, он выбран из О, S, NR8, SO2 и CR8R8';
G выбран из группы, включающей -(CR8R8')n-С(О)ОН, где n=3, 4, 5 или 6, -(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-С(О)ОН, -(CR8R8')n-O-(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-С(О)ОН, -(CR8R8')n-S-(CR8R8')n-C(O)OH и -(CR8R8')n-P(O)OR8OR8'; где
каждый R8 и R8' независимо выбран из Н, D или (C1-C6)алкила или R8 и R8' вместе с атомом углерода, с которым каждый из них связан, образуют (C3-С8)циклоалкил;
если не обозначено иначе, каждый n независимо имеет значение 0-10; при условии, что, когда n имеет значение 0, любой атом кислорода, азота или серы группы Y не связан непосредственно с каким-либо атомом кислорода, серы или фосфора группы G;
R2 представляет собой
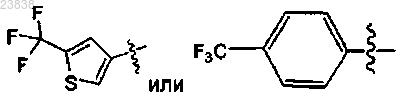 ;
;R4, R4', R5, R5', R6, R6', R7 и R7', каждый независимо, выбраны из водорода и (C1-C6)алкила;
X представляет собой
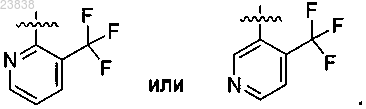
2. Соединение по п.1, в котором Е выбран из группы, включающей Н, галоген, ОН, CN, -О(C1-C6)алкил, (C1-C6)алкил, -С(О)ОН, -C(O)NR8R8', -(C1-C6)алкил-С(О)ОН, -(C1-C6)алкил-ОН и -(C1-C6)алкил-С(О)NR8R8'.
3. Соединение по п.2, в котором указанный -(C1-C6)алкил-ОН представляет собой гидроксиметил; указанный -C(O)NR8R8' представляет собой -C(O)NH2; указанный -(C1-C6)алкил-С(О)ОН представляет собой -(СН2)4С(О)ОН; указанный галоген представляет собой -F; указанный -О(C1-C6)алкил представляет собой метокси; указанный -(C1-C6)алкил представляет собой метил.
4. Соединение по п.1, в котором каждый J независимо представляет собой Н или фтор.
5. Соединение по п.1, в котором Y выбран из группы, включающей О, S, SO2 и CR8R8'.
6. Соединение по п.1, в котором G выбран из группы, включающей -(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-С(О)ОН и -(CR8R8')n-O-(CR8R8')n-(C3-C8)циклоалкил(CR8R8')n-С(О)ОН.
7. Соединение по п.1, в котором указанный -(CR8R8')n-(C3-С8)циклоалкил(CR8R8')n-С(О)ОН выбран из группы, включающей -СН2-циклопентил-С(О)ОН, -циклобутил-С(О)ОН, -циклопентил-С(О)ОН, -циклогексил-С(О)ОН и -циклопентил-СН2-С(О)ОН; указанный -(CR8R8')n-O-(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-C(О)ОН представляет собой -О-циклопентил-С(О)ОН или -О-циклобутил-С(О)ОН; указанный -(CR8R8')n-Р(О)OR8OR8' представляет собой (СН2)3Р(О)(ОН)(ОН) или -(СН2)3Р(О)(ОСН3)(ОСН3).
8. Соединение по п.1, в котором Y представляет собой О и G выбран из группы, включающей -(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-C(O)OH и -(CR8R8')n-P(O)OR8OR8'.
9. Соединение по п.1, в котором Y представляет собой S и G представляет собой -(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-C(O)OH.
10. Соединение по п.1, в котором Y представляет собой О; G представляет собой -(CR8R8')n-С(О)ОН и n=3, 4, 5 или 6.
11. Соединение по п.1, в котором Y представляет собой CR8R8' и G представляет собой -(CR8R8')n-O-(CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-С(О)ОН.
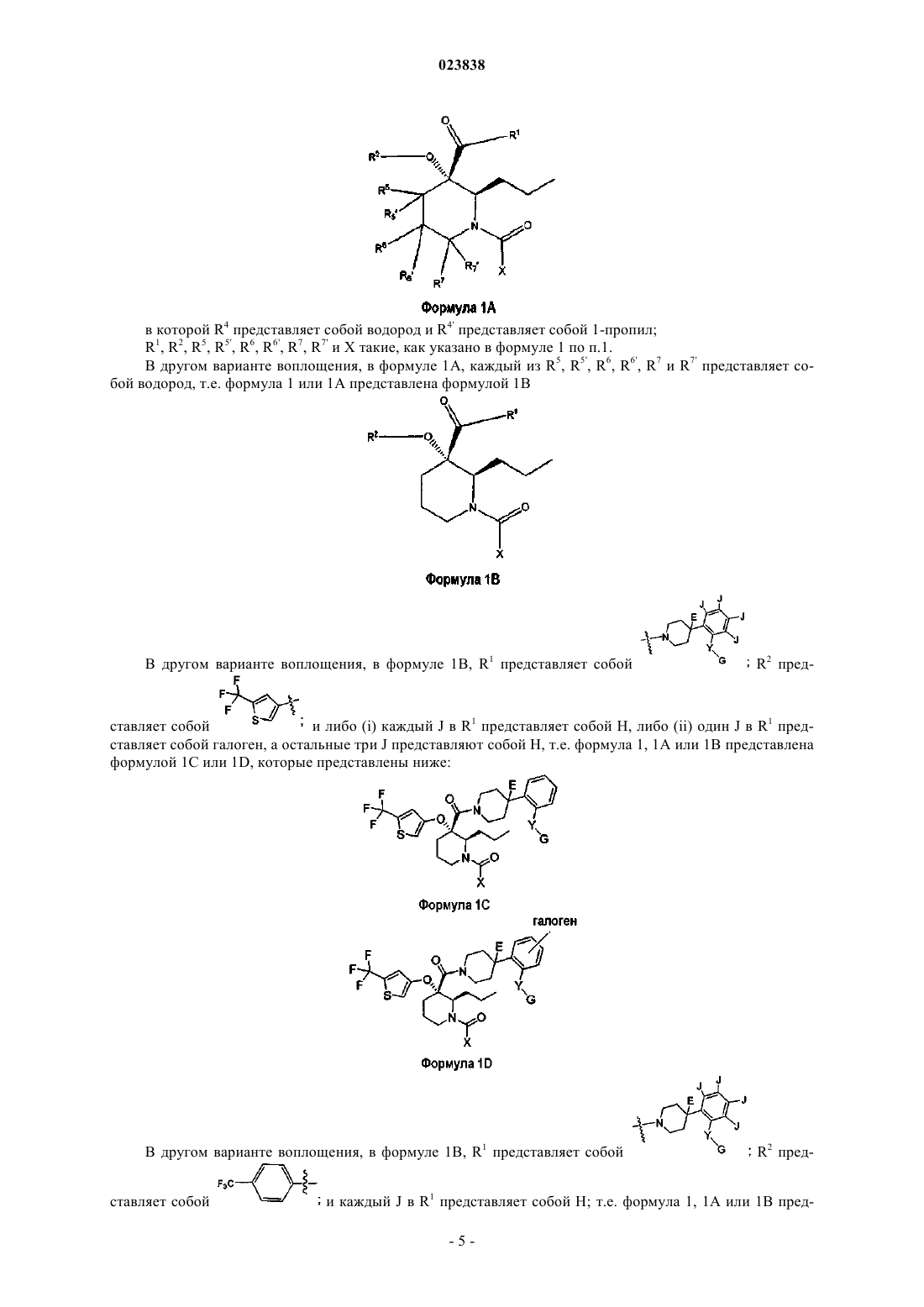
12. Соединение по п.1 формулы 1А
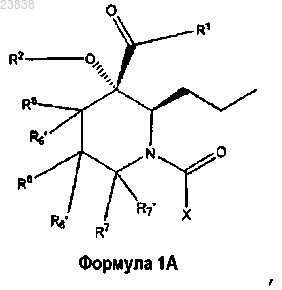
где R4 представляет собой водород;
R4' представляет собой 1-пропил;
R1, R2, R5, R5', R6, R6', R7, R7' и X такие, как указано в формуле 1 по п.1.
13. Соединение по п.12, в котором каждый из R5, R5', R6, R6', R7 и R7' представляет собой водород.
14. Соединение по п.13, в котором
R1 представляет собой
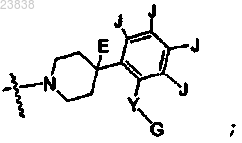
R2 представляет собой
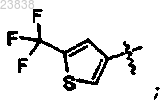
либо (i) каждый J в R1 представляет собой Н, либо (ii) один J в R1 представляет собой галоген, а остальные три J представляют собой Н.
15. Соединение по п.1, в котором
R1 представляет собой

R2 представляет собой
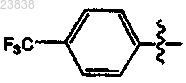
и каждый J в группе R1 представляет собой Н.
16. Соединение по п.14, в котором Е представляет собой CN или ОН, J в R1 представляет собой Н, Y представляет собой О и G представляет собой (CR8R8')n-(С3-С8)циклоалкил(CR8R8')n-С(О)ОН.
17. Соединение по п.14, в котором Е представляет собой CN или ОН, J в R1 представляет собой Н, Y представляет собой О и G выбран из группы, включающей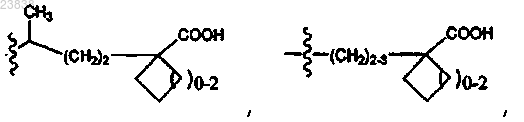 -СН2-циклопентил-С(О)ОН, -циклобутил-С(О)ОН, -циклопентил-С(О)ОН, -циклогексил-С(О)ОН и -циклопентил-СН2-С(О)ОН.
-СН2-циклопентил-С(О)ОН, -циклобутил-С(О)ОН, -циклопентил-С(О)ОН, -циклогексил-С(О)ОН и -циклопентил-СН2-С(О)ОН.
18. Соединение по п.14, в котором Е представляет собой CN или ОН, J в R1 представляет собой Н, Y представляет собой О и G выбран из группы, включающей -СН(СН3)-(СН2)2-3-С(О)ОН, -(СН2)3СН(СН(СН3)2)-С(О)ОН-(CD2)3C(O)OH, -(СН2)1-2-CH (СН3)-(CH2)1-2-С(О)ОН и -СН(CH3)-(СН2)2-3-С(О)ОН.
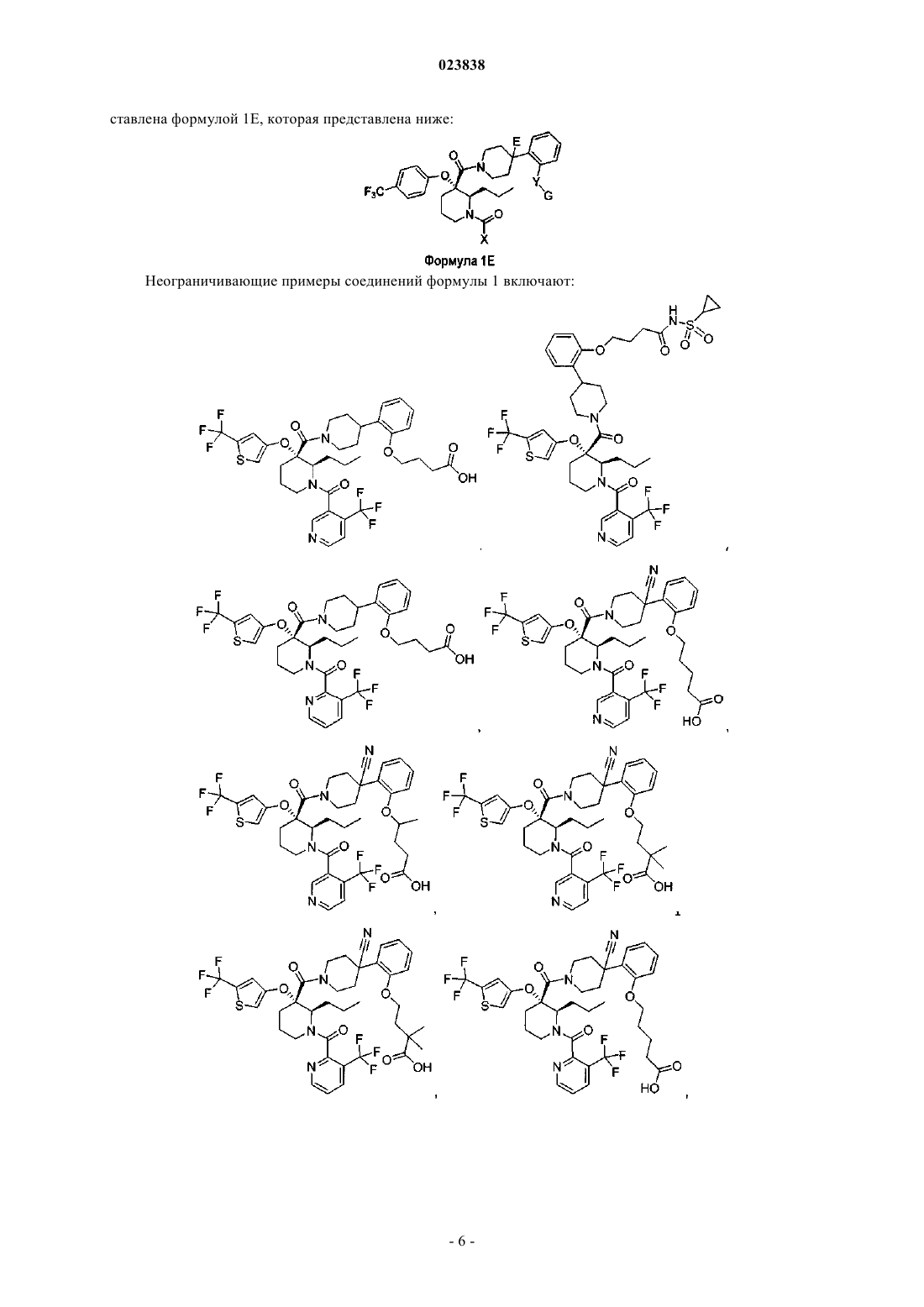
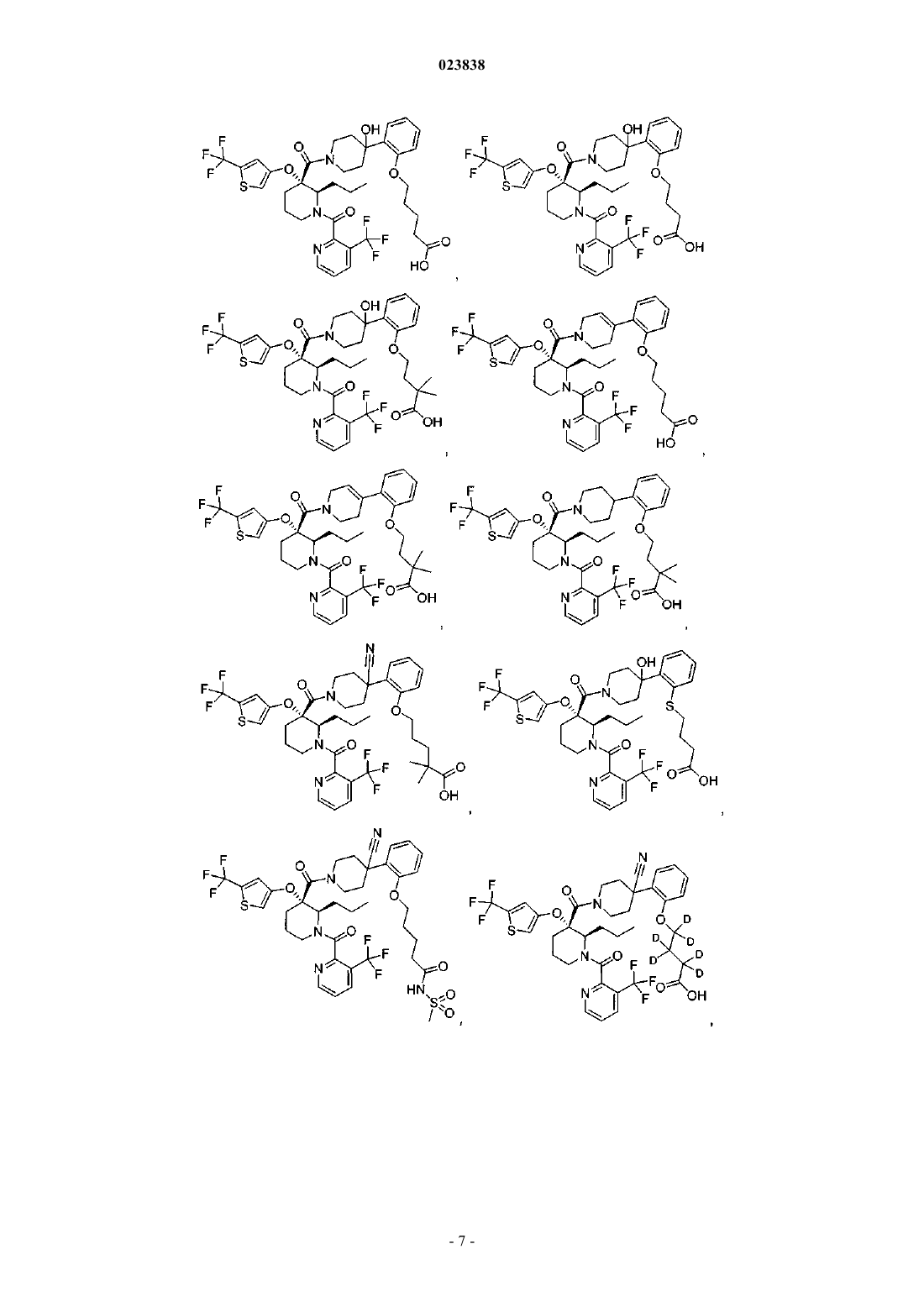
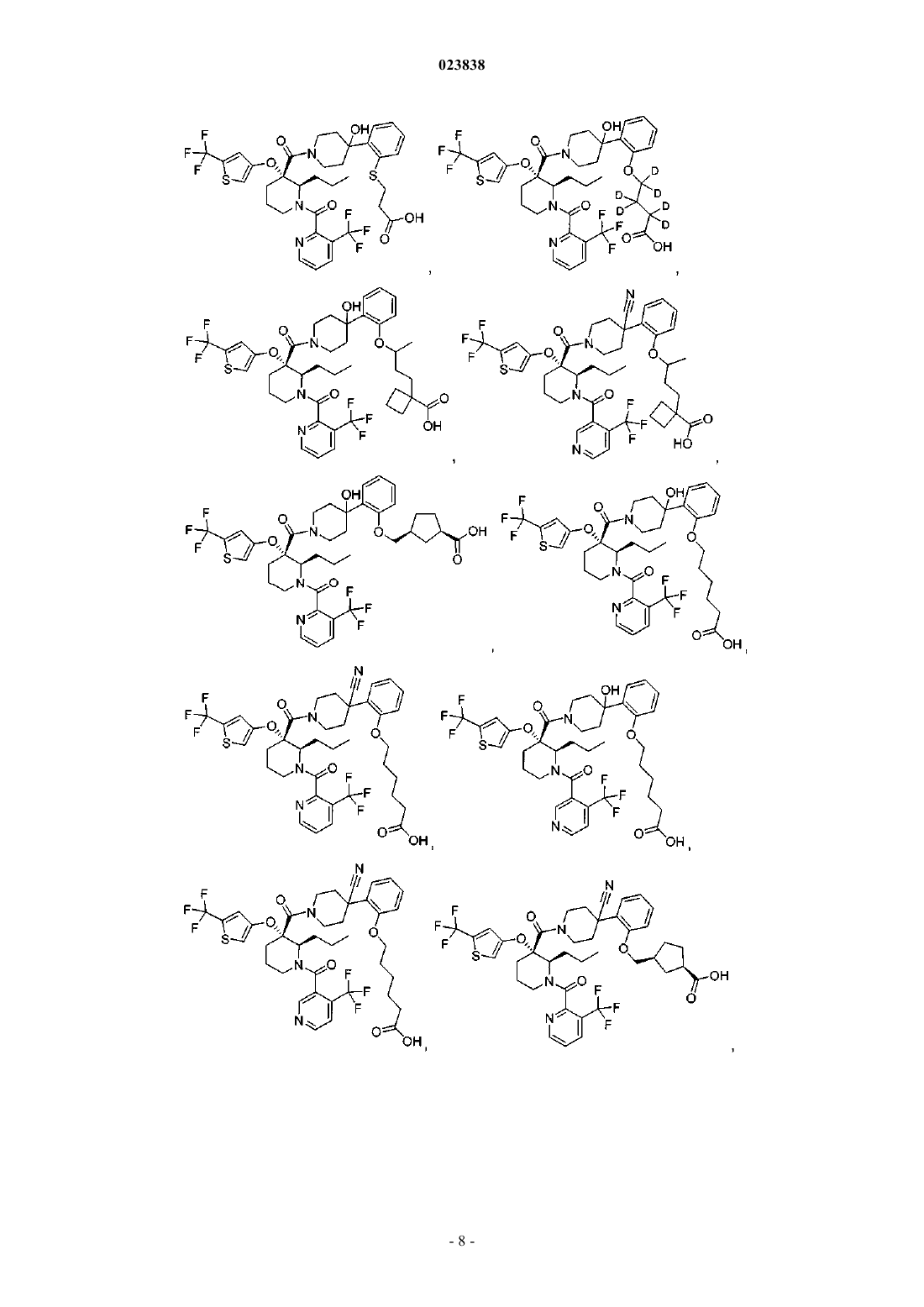
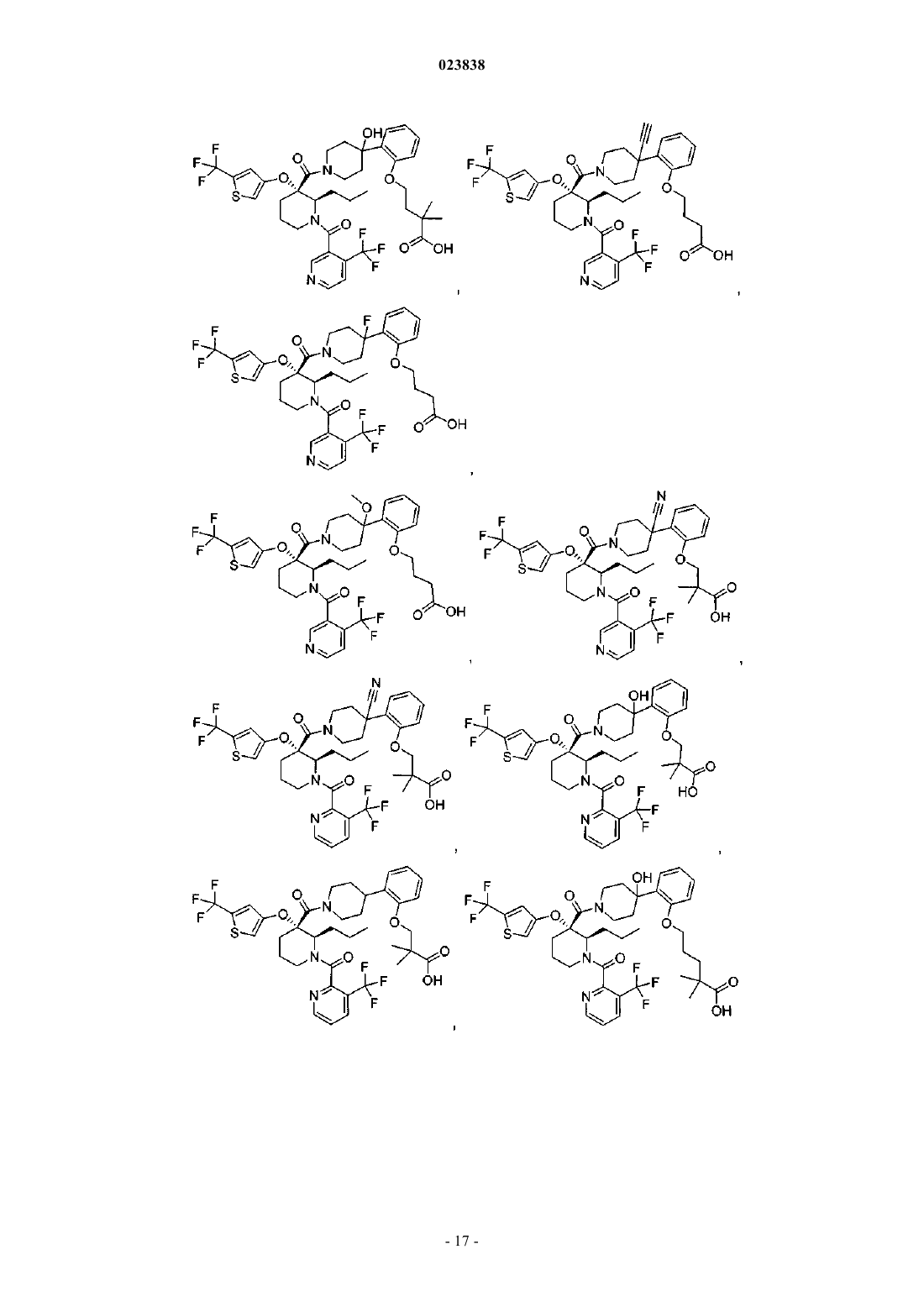
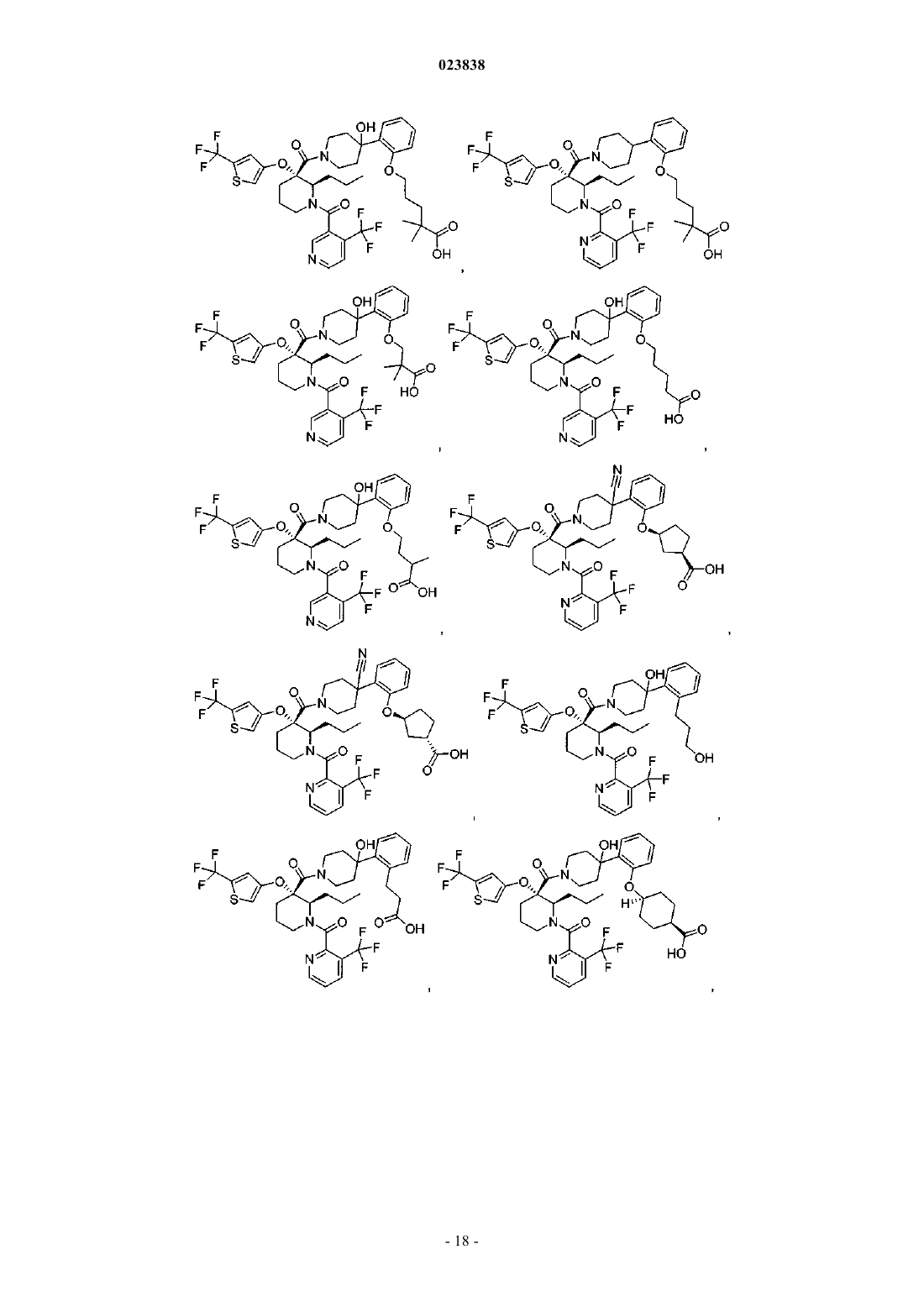
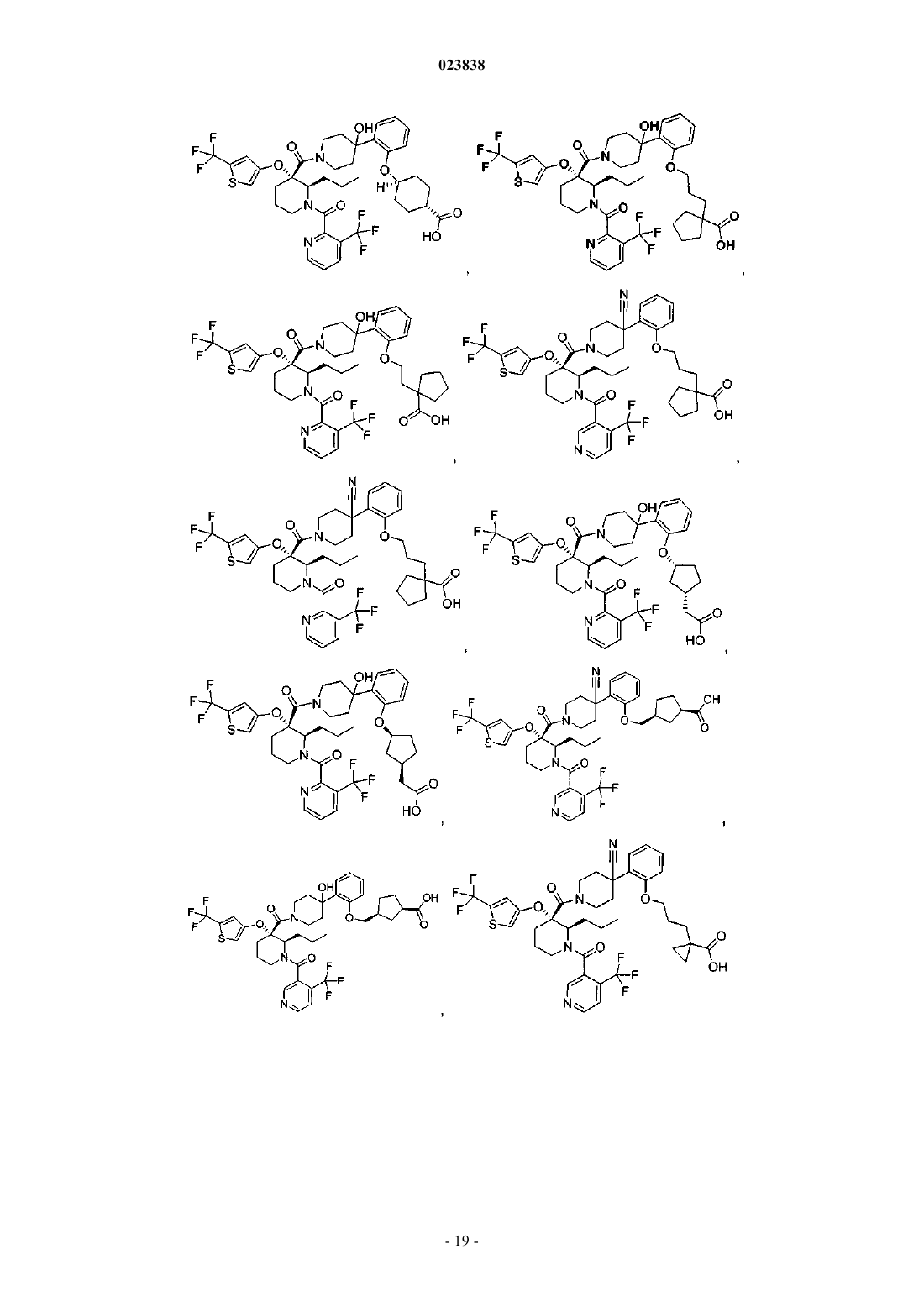
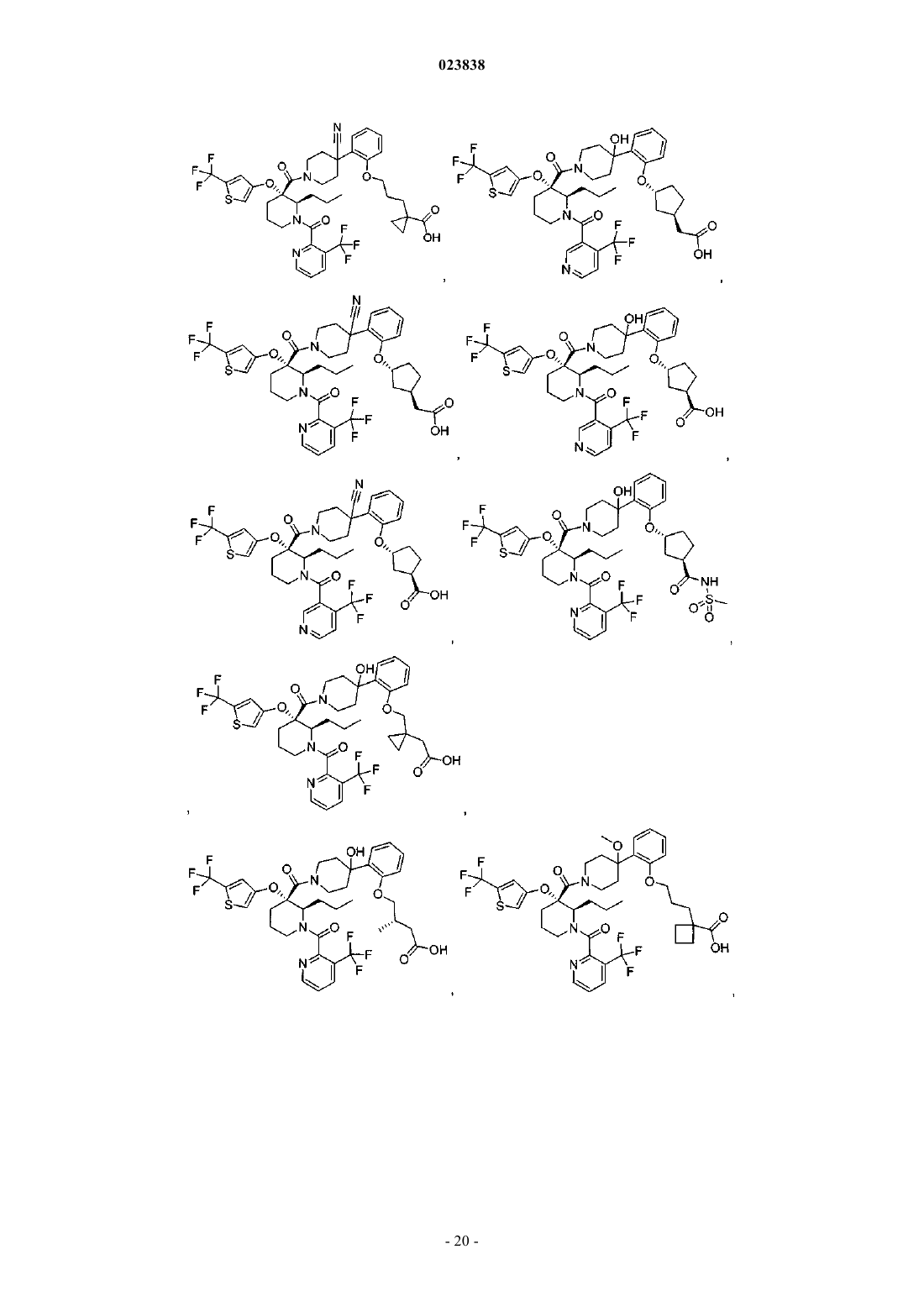
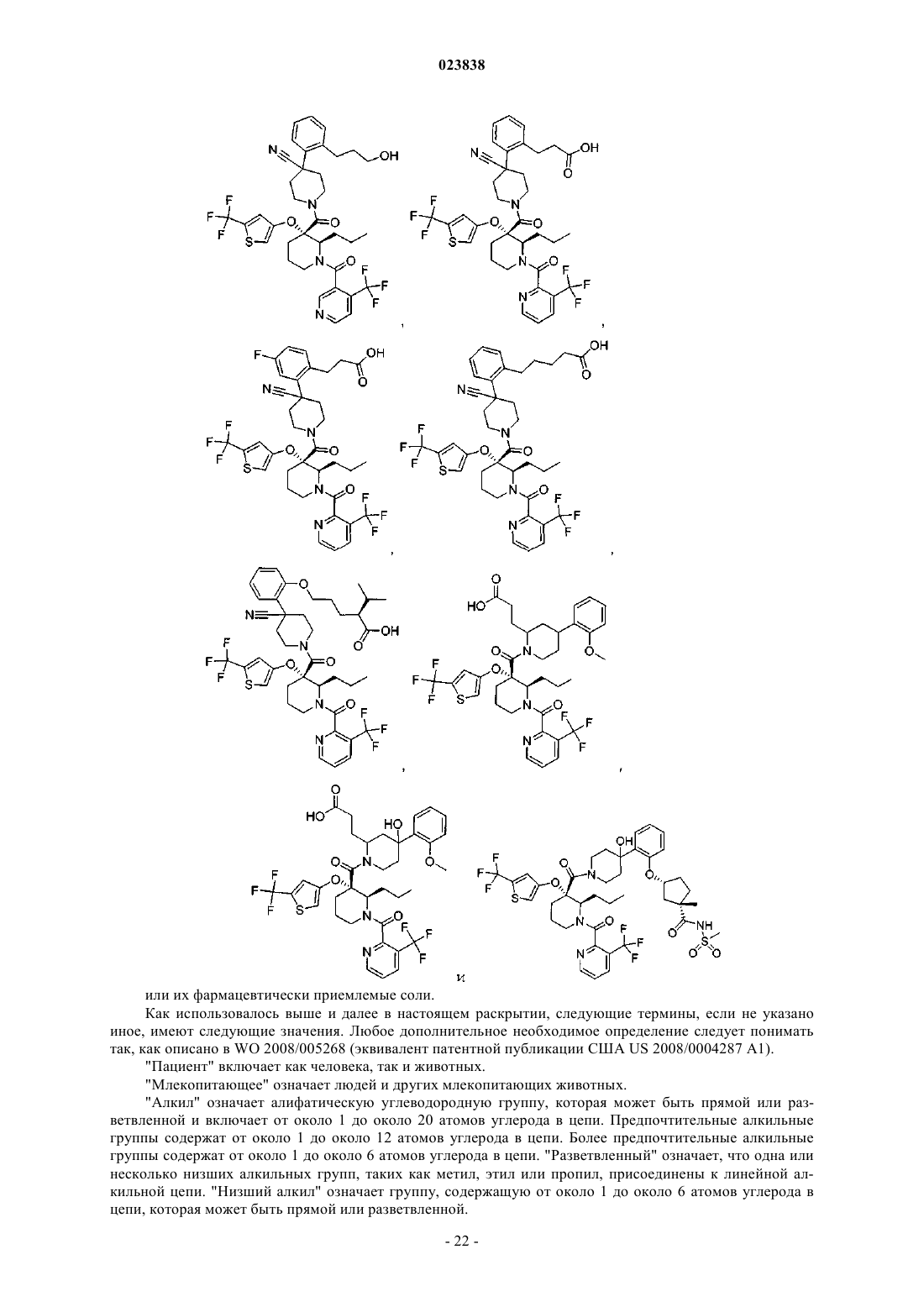
19. Соединение, выбранное из группы, включающей
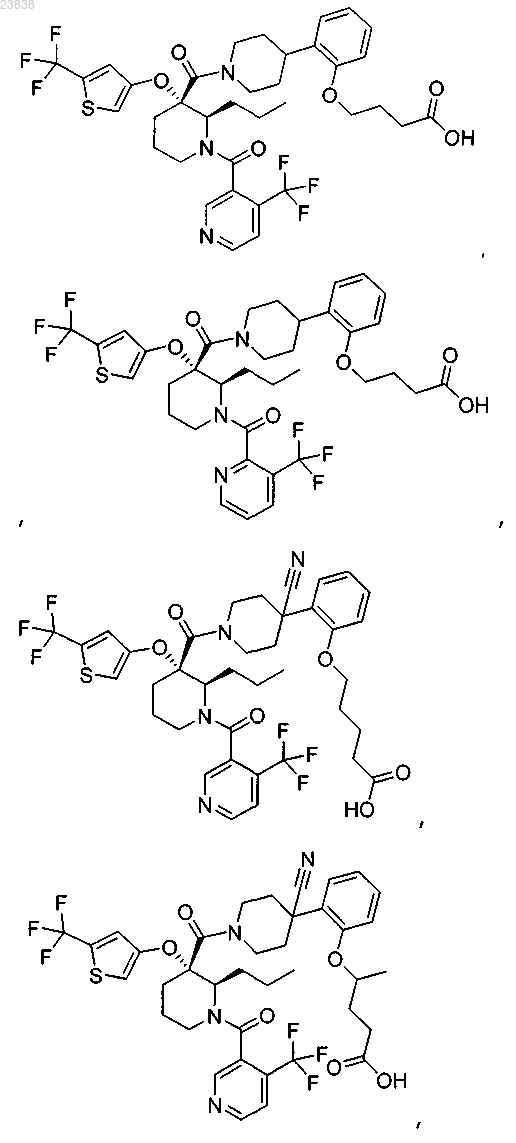
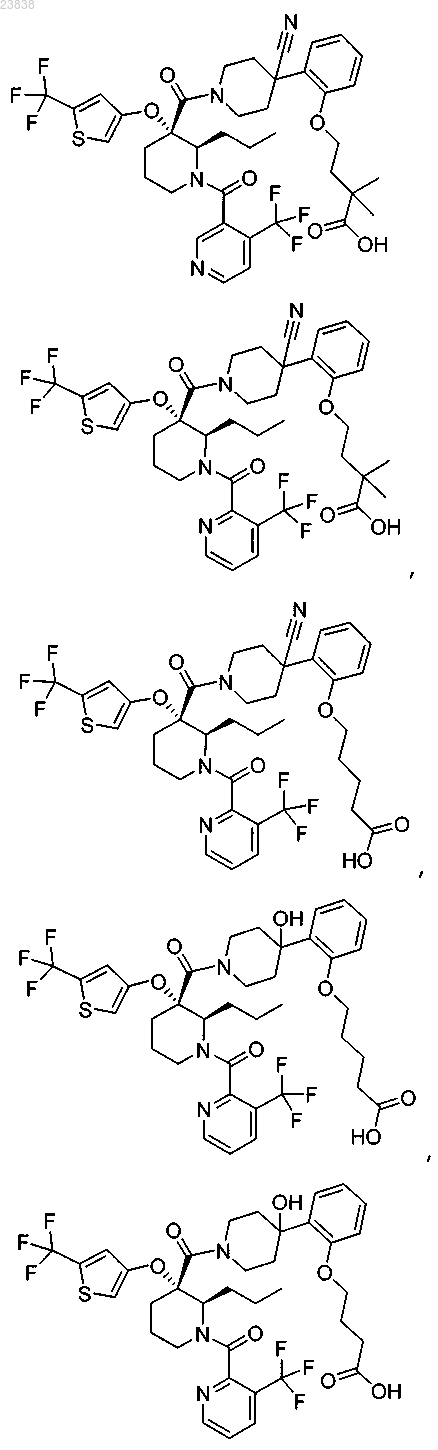
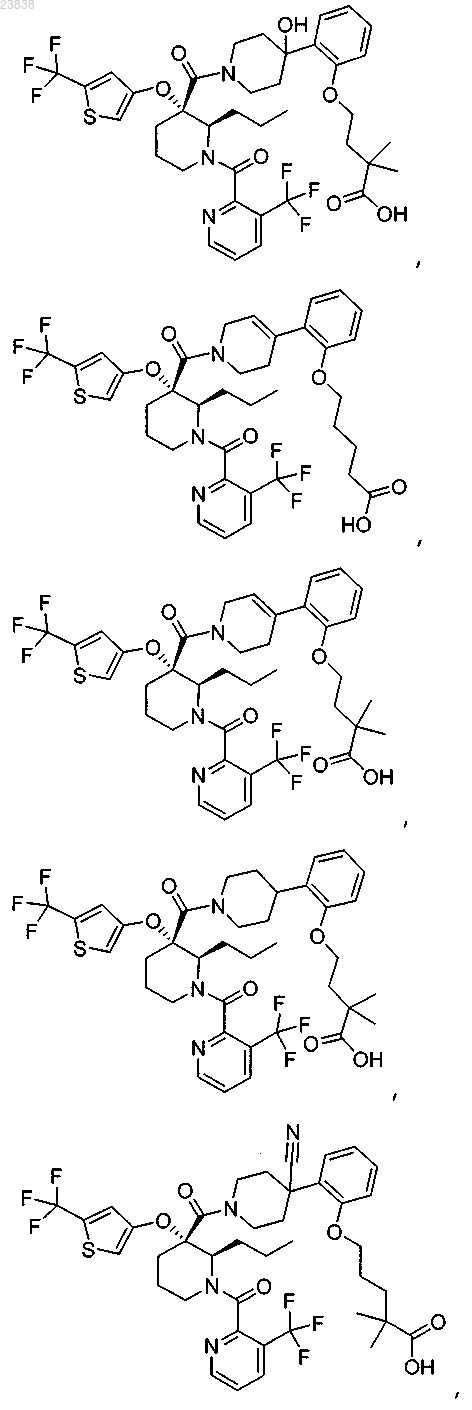
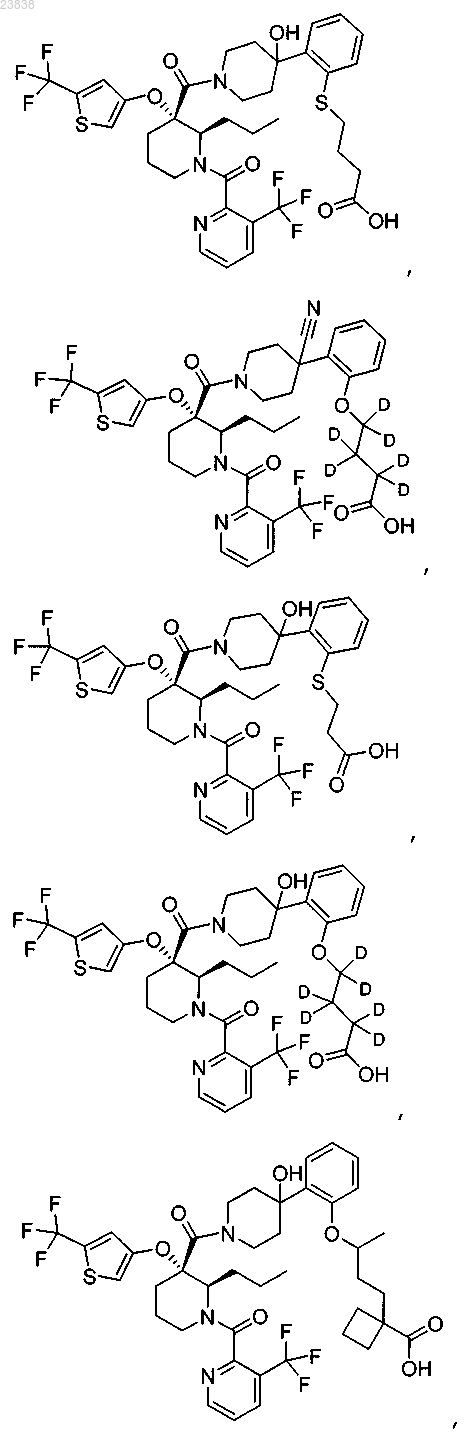
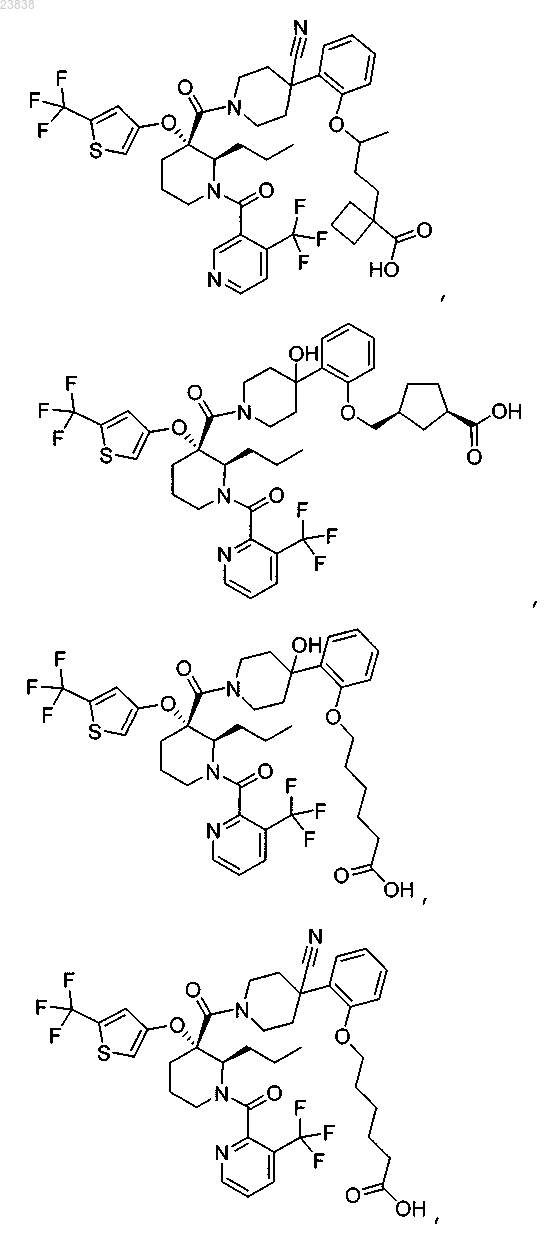


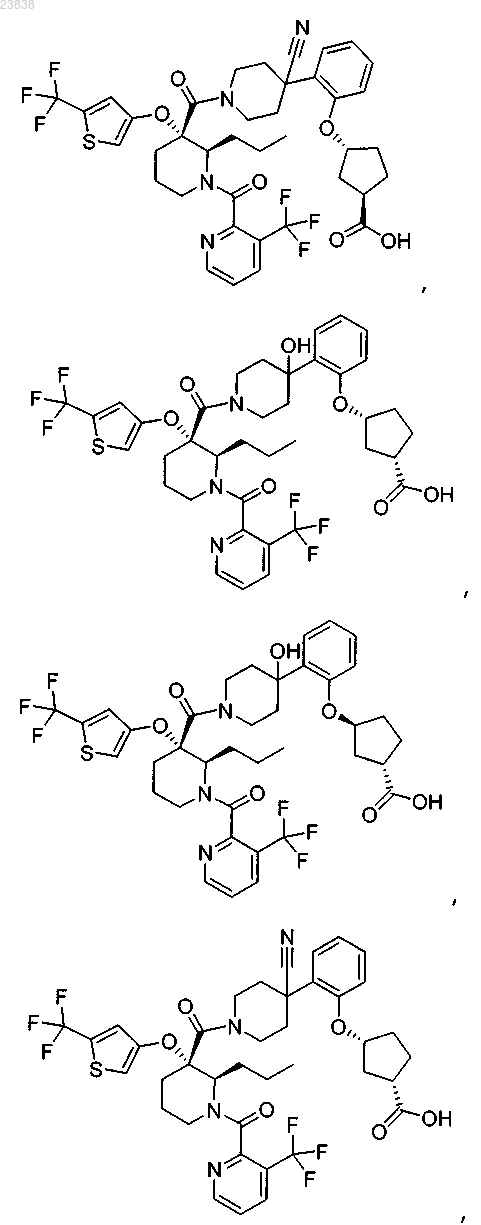
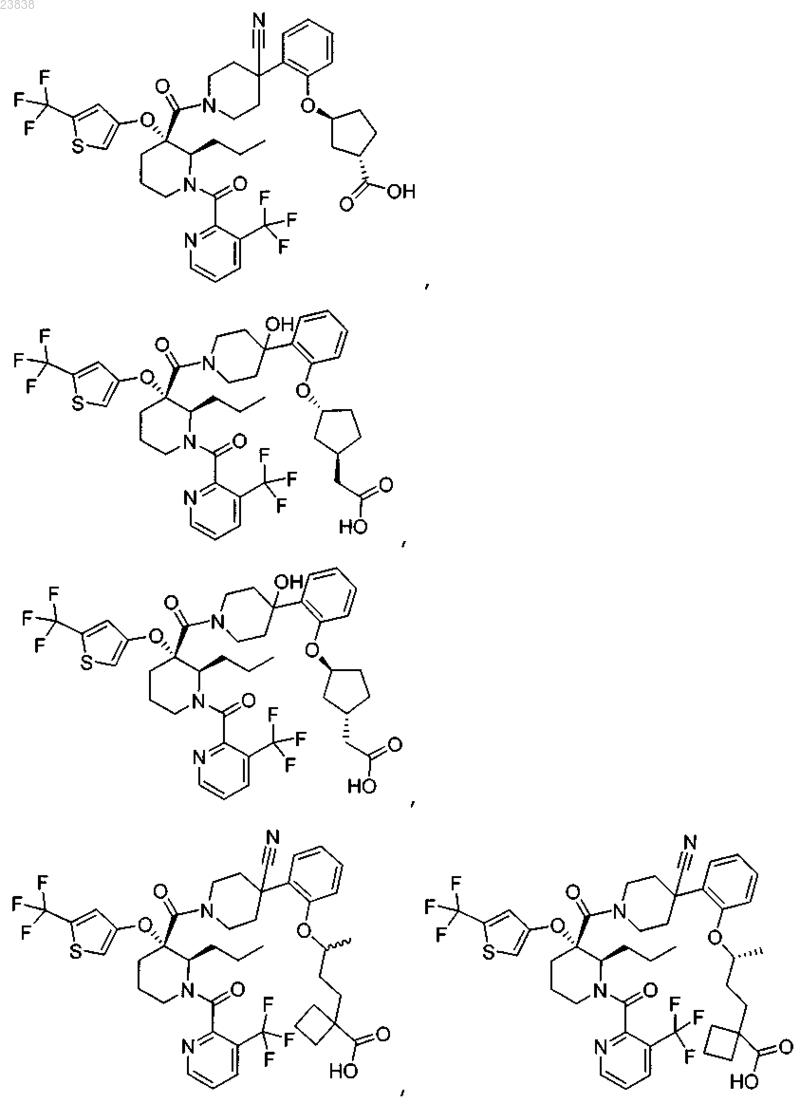
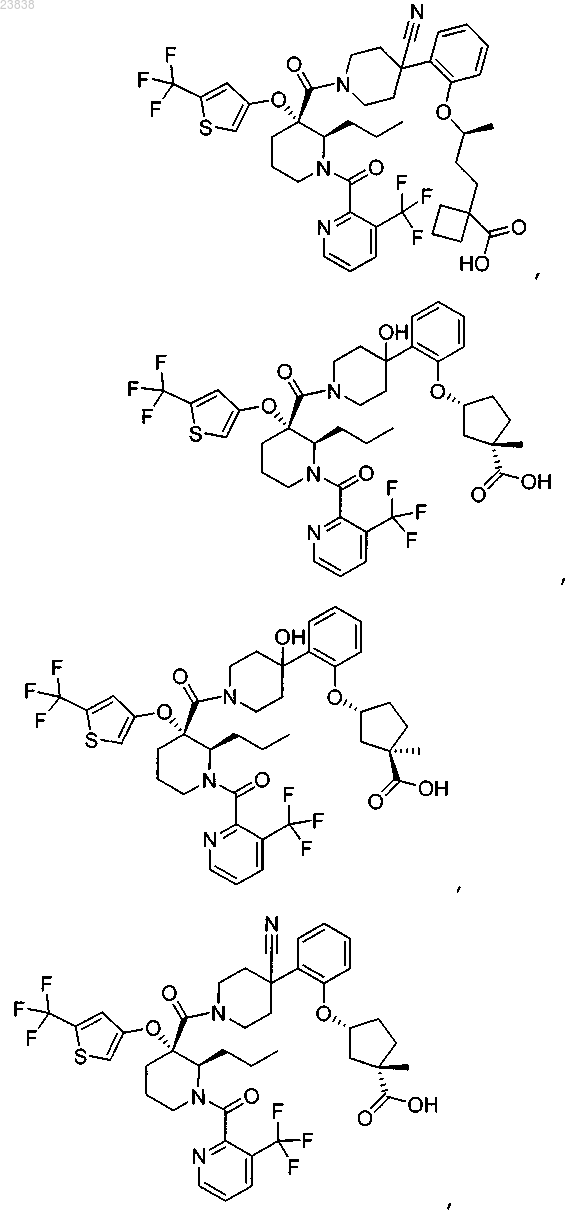
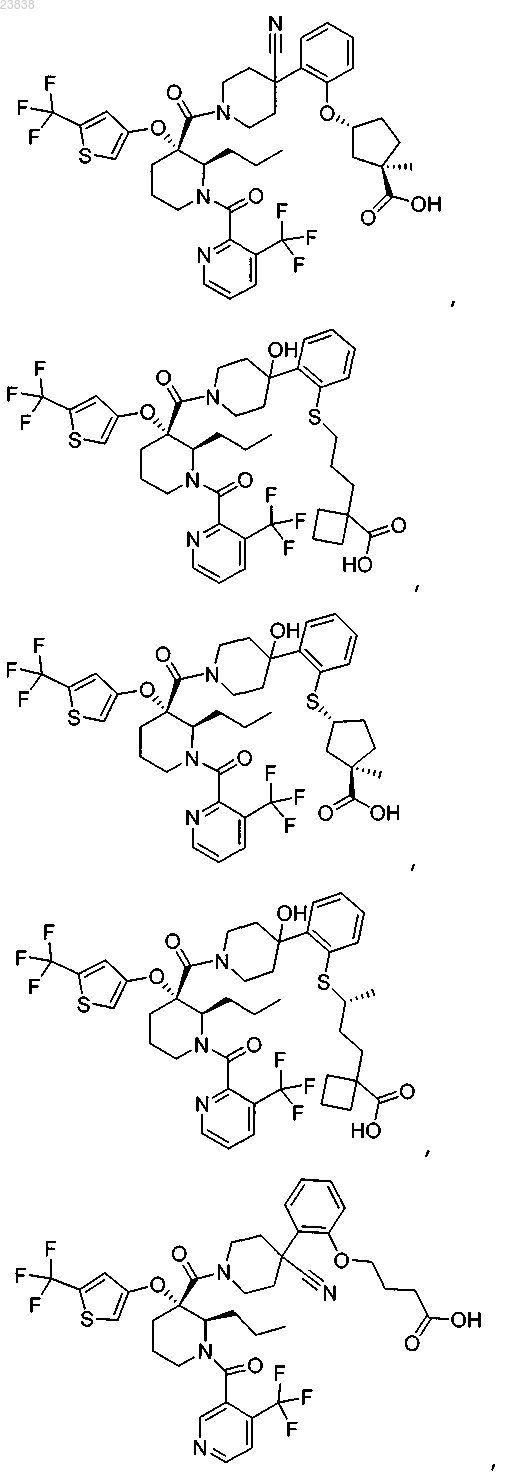

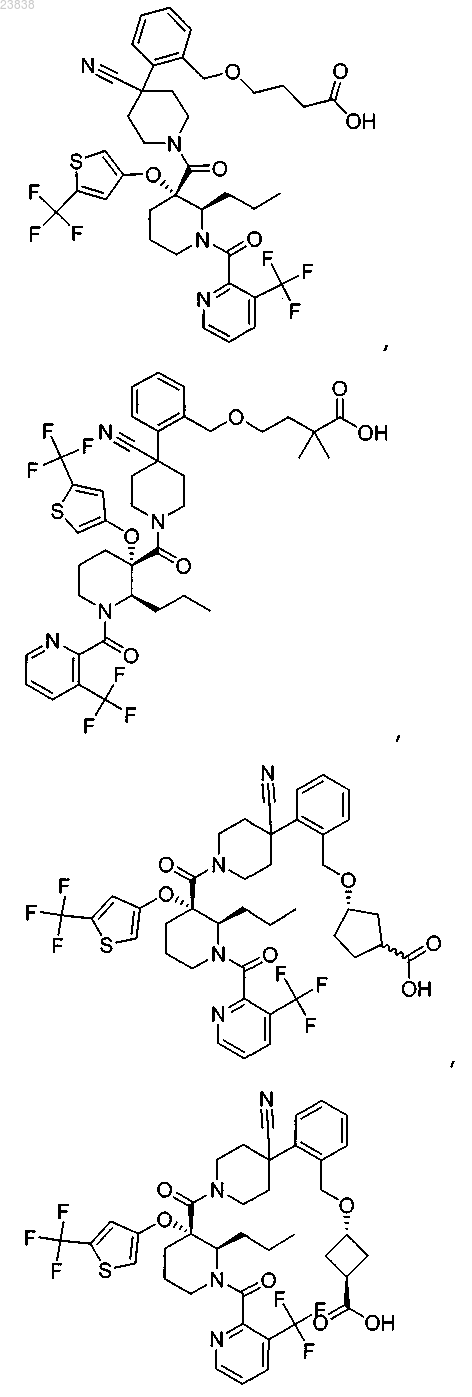
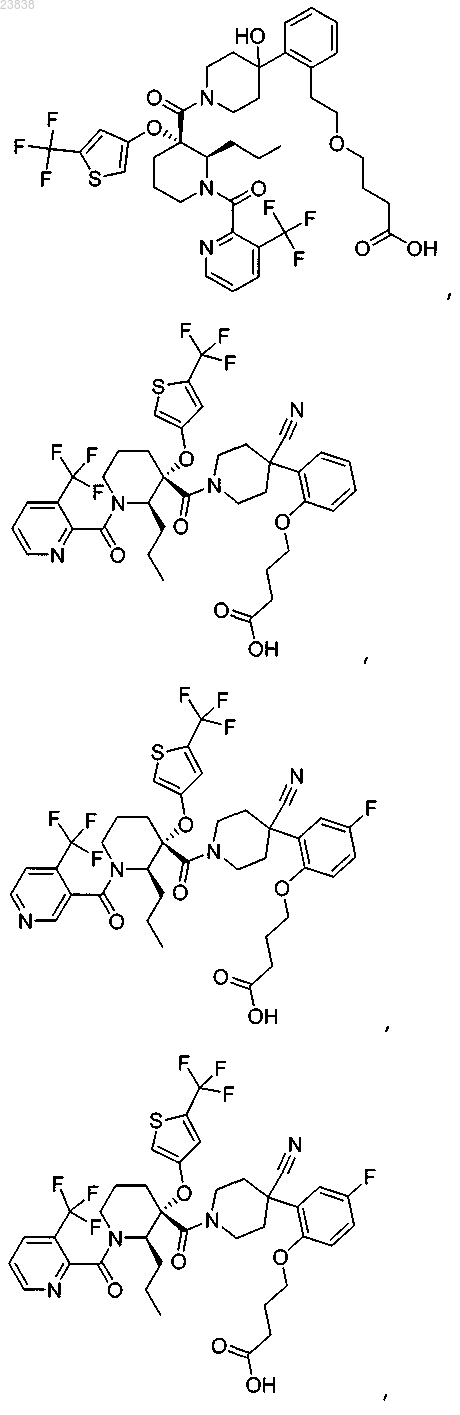
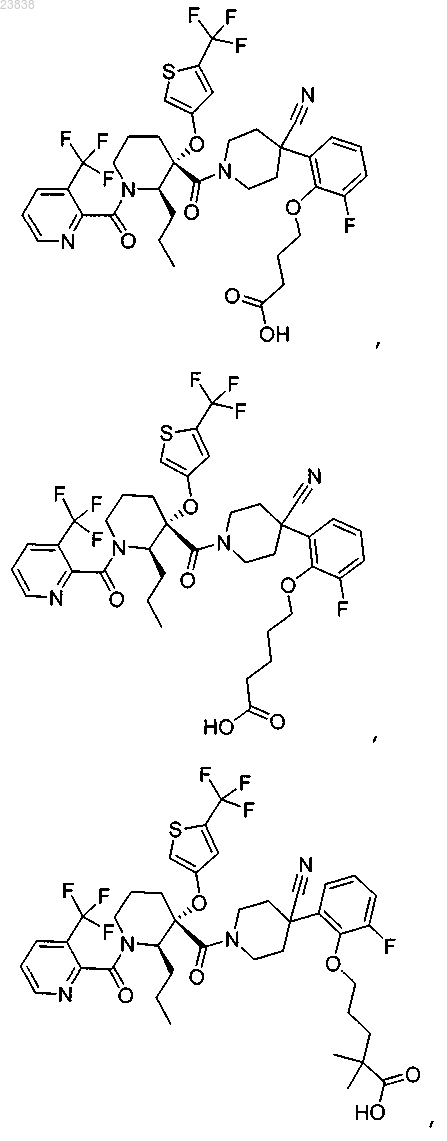
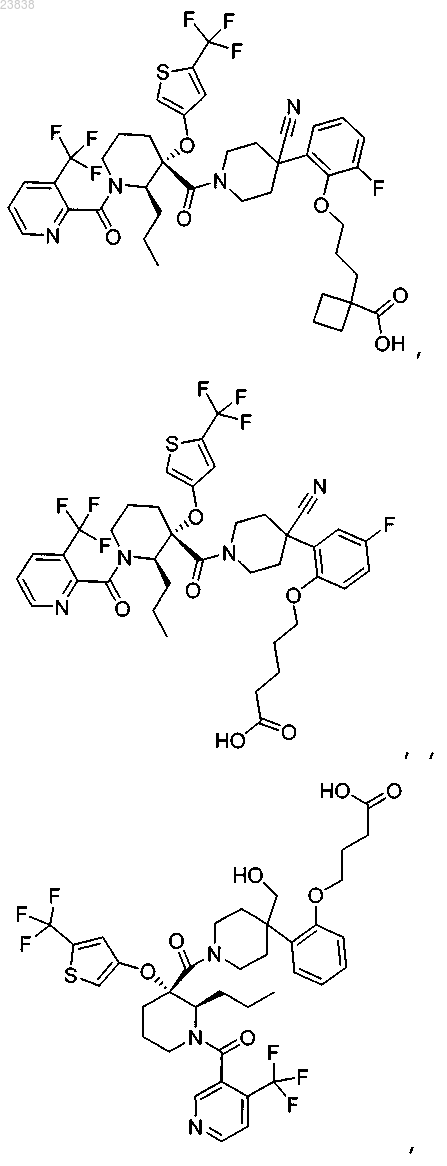
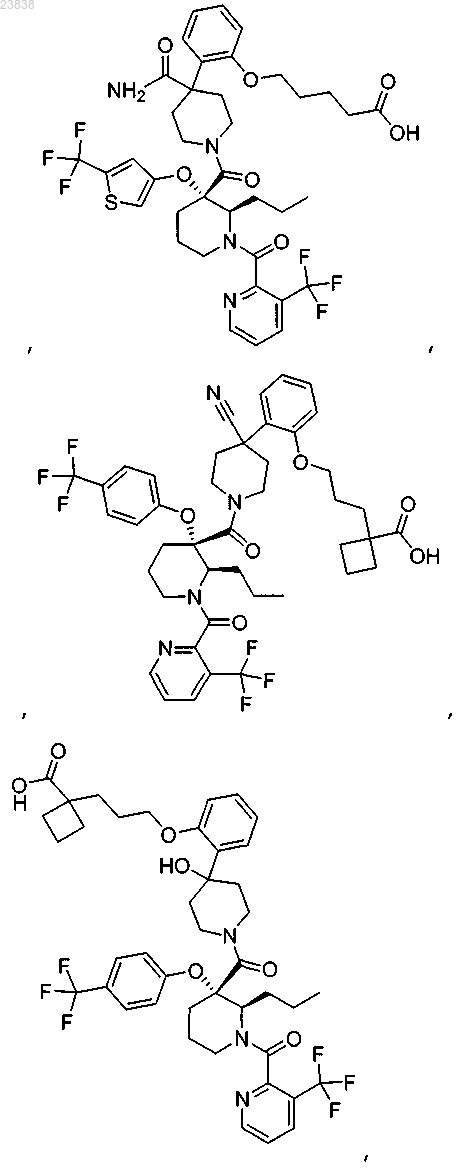

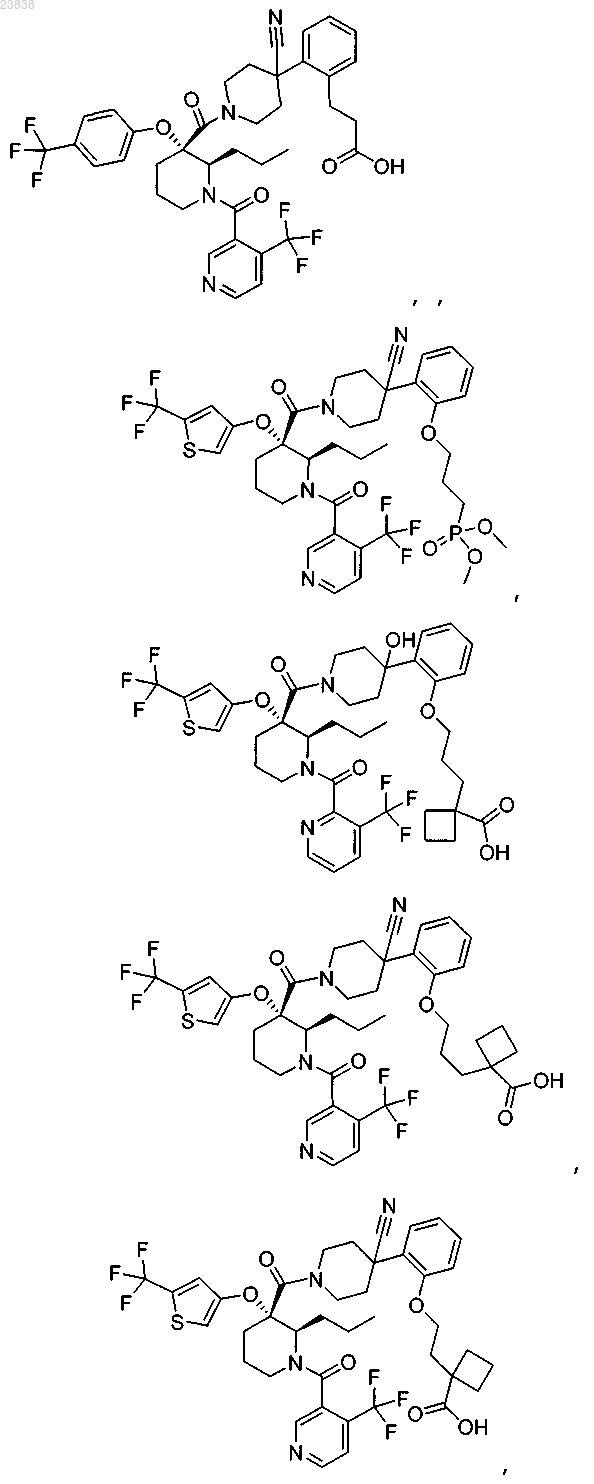
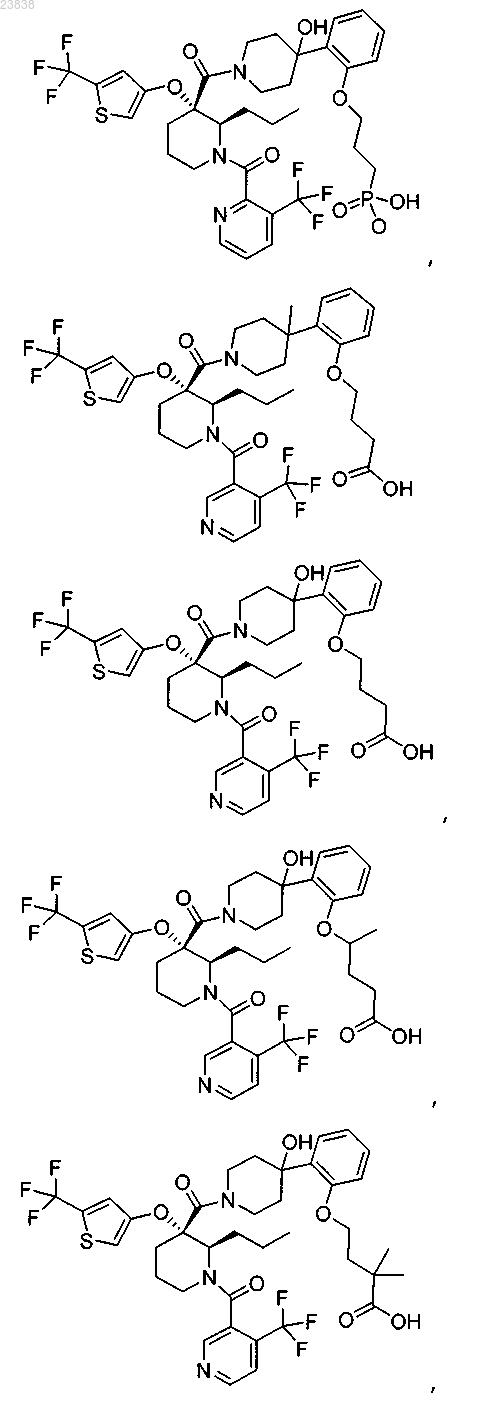
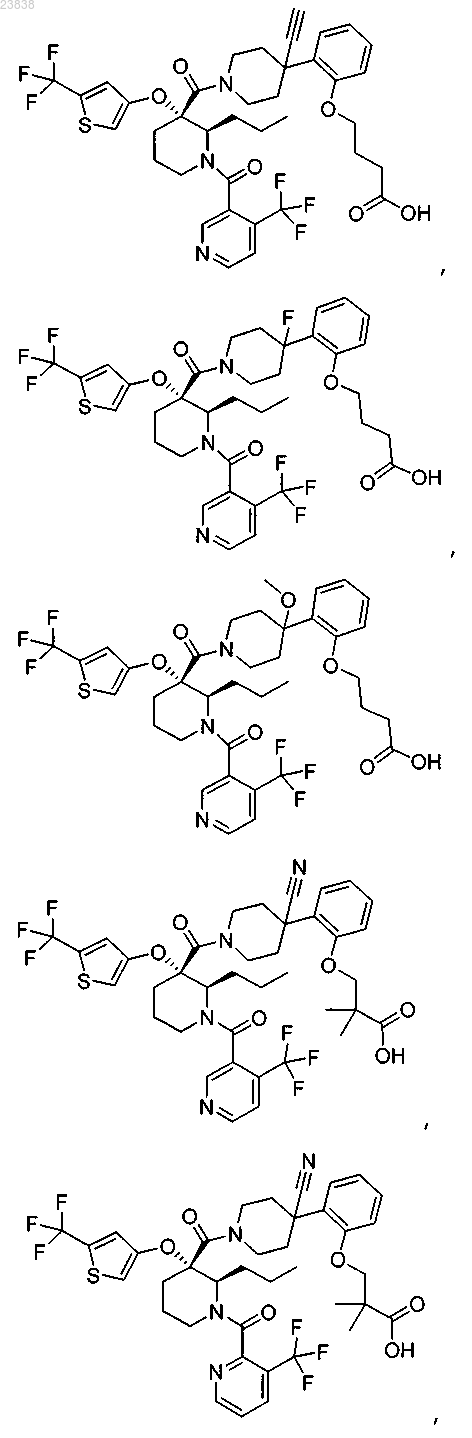
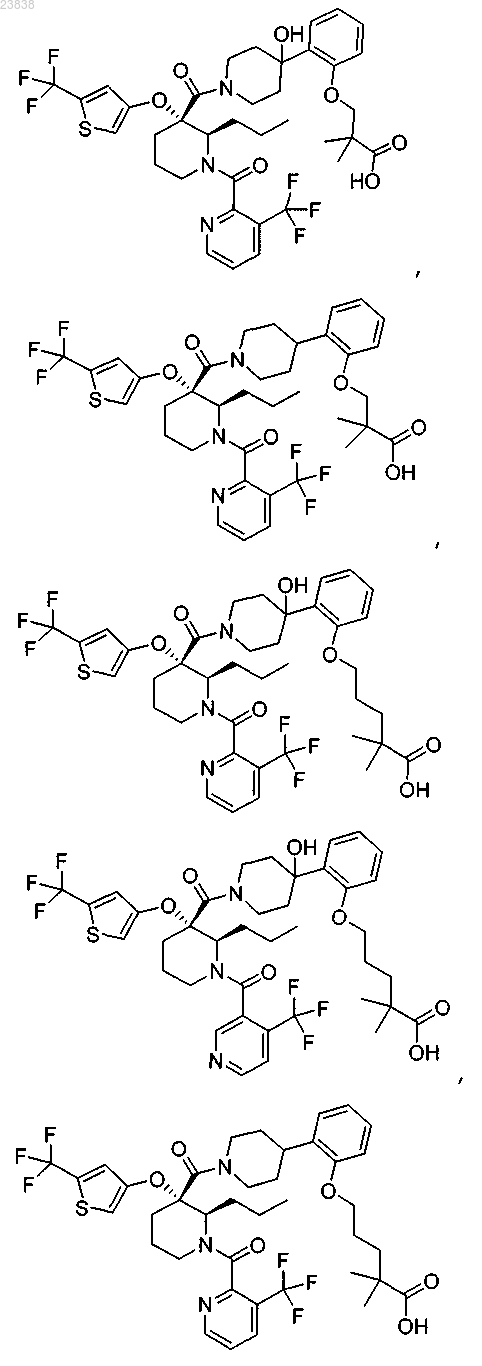
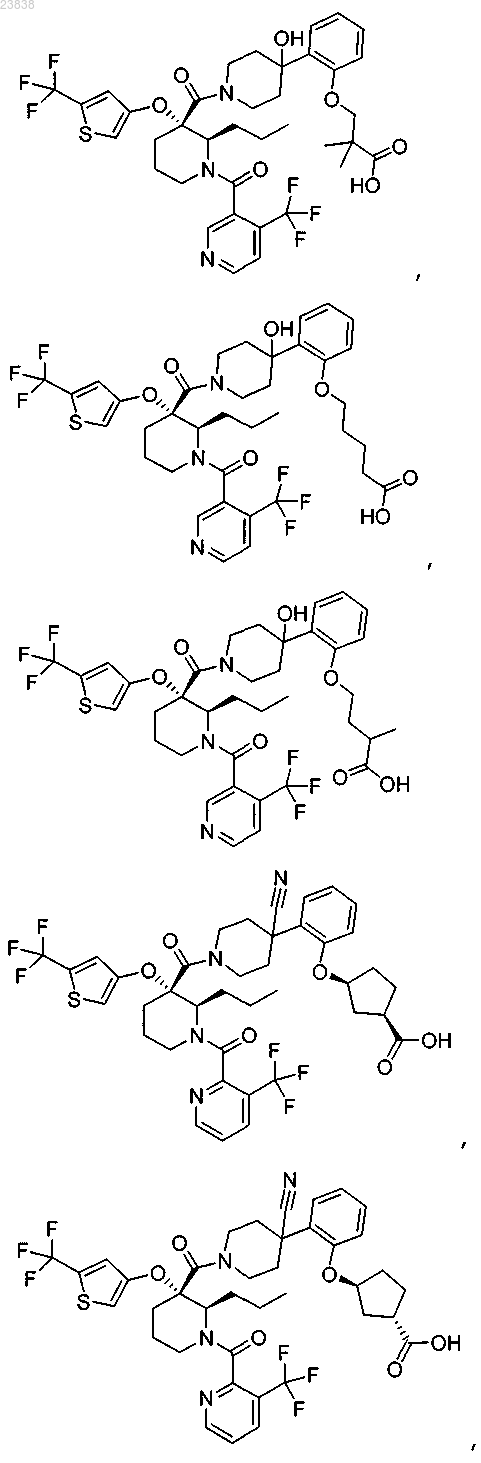
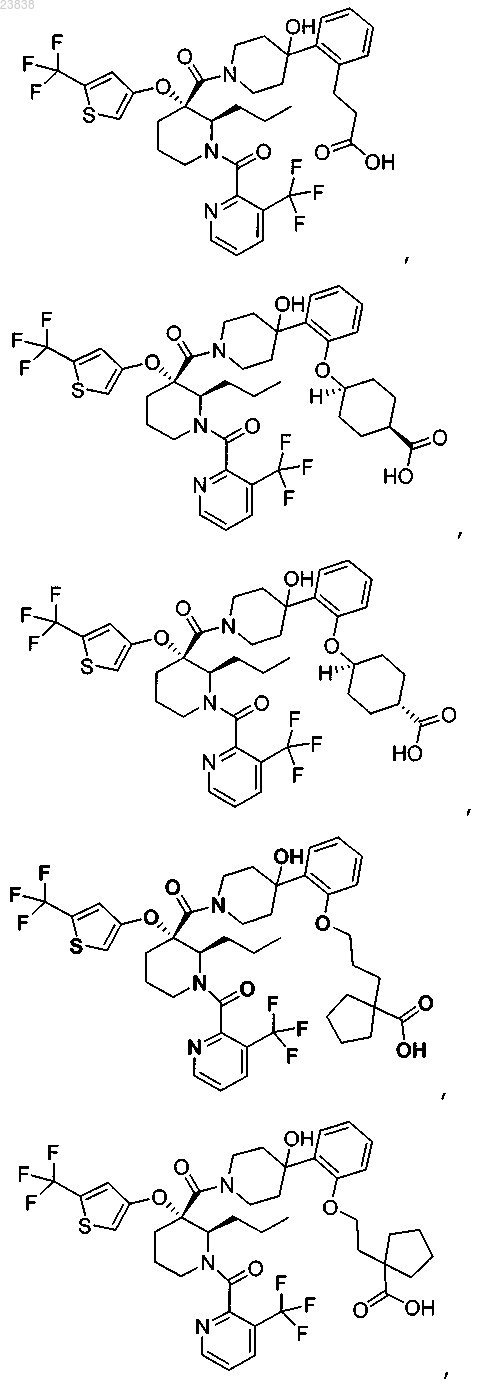
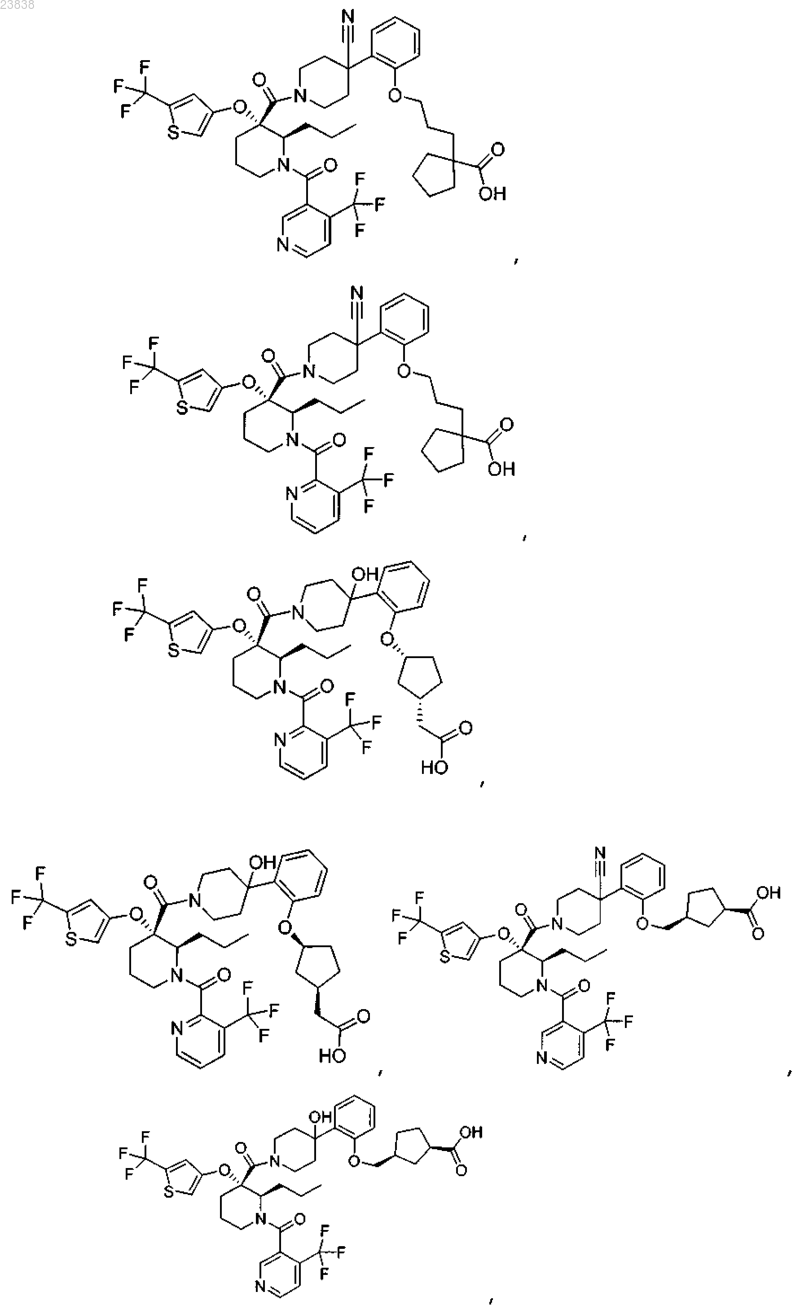
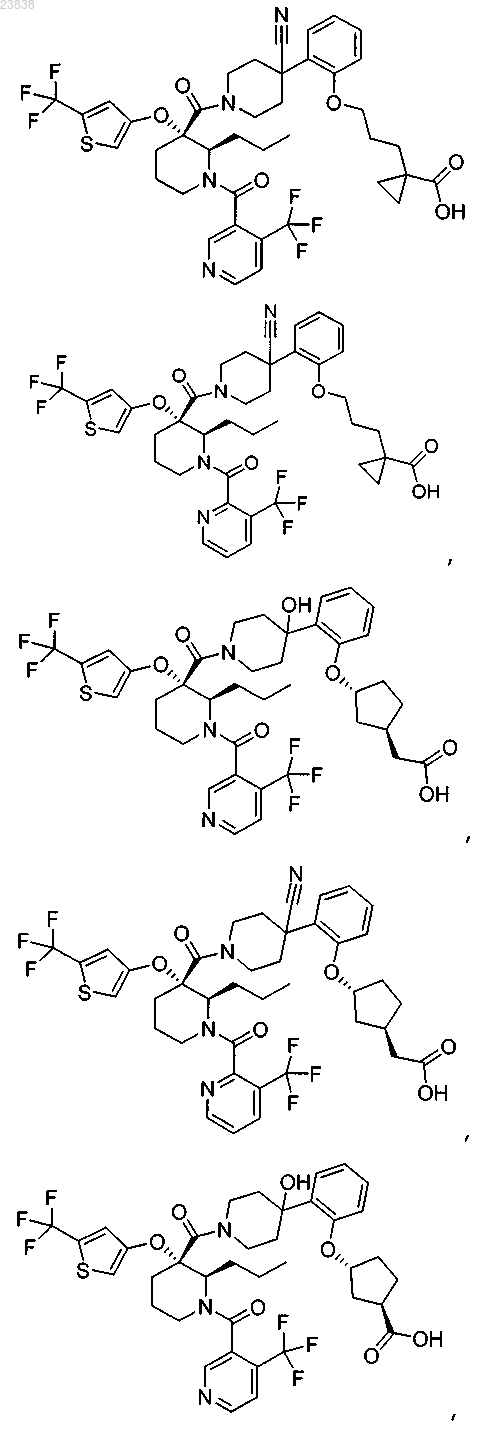
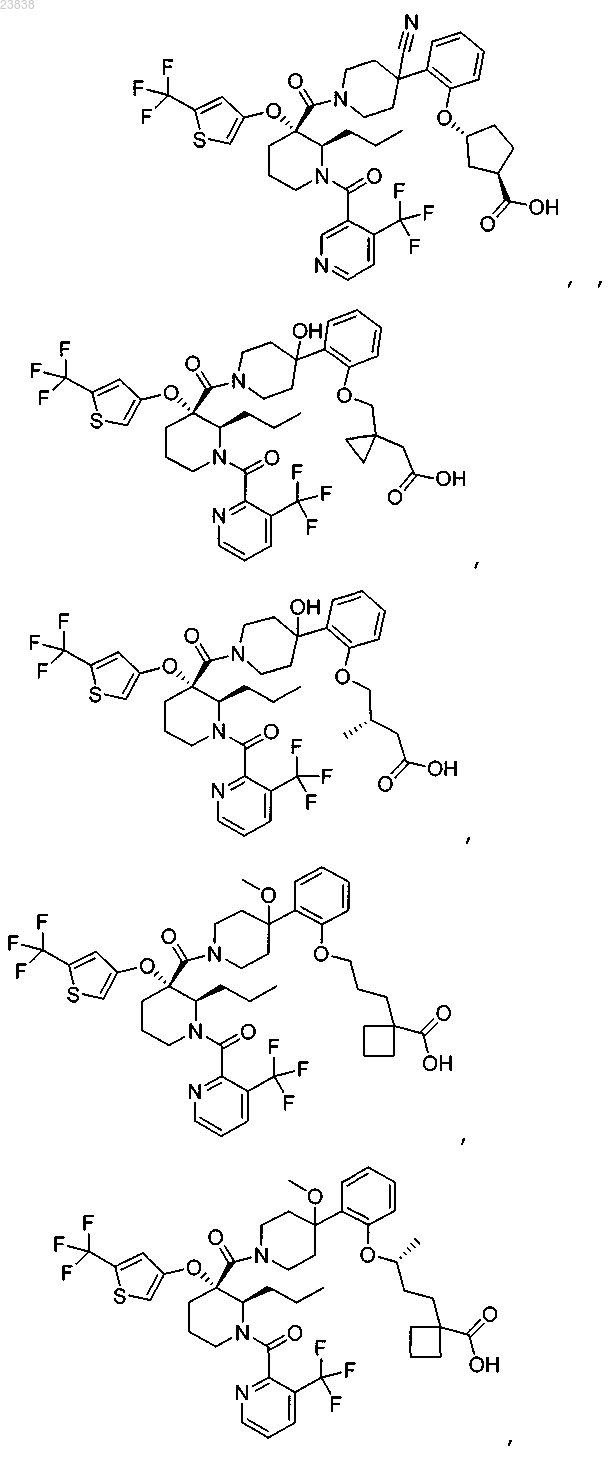
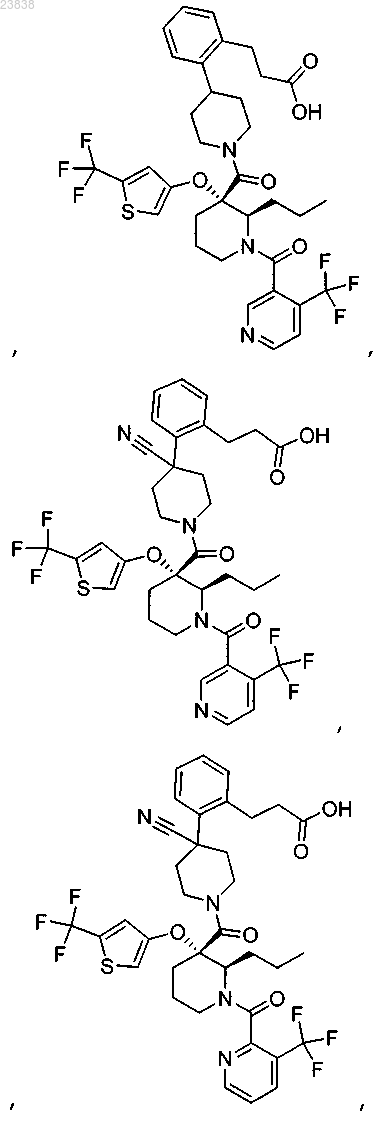
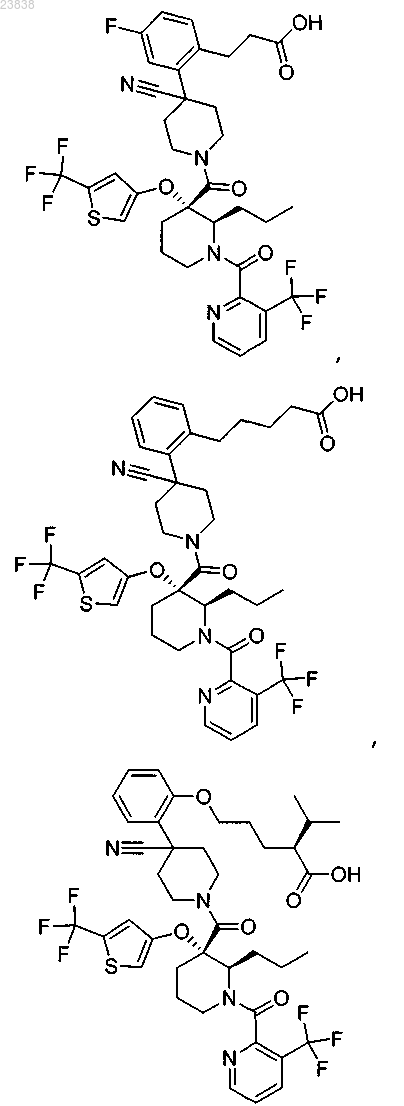
или его фармацевтически приемлемая соль.
20. Соединение, которое представляет собой

или его фармацевтически приемлемая соль.
21. Соединение, которое представляет собой
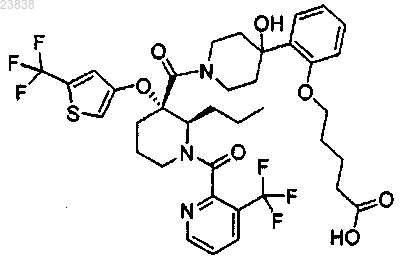
или его фармацевтически приемлемая соль.
22. Соединение, которое представляет собой
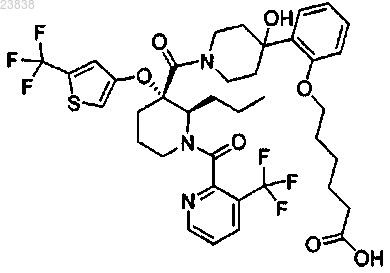
или его фармацевтически приемлемая соль.
23. Соединение, которое представляет собой
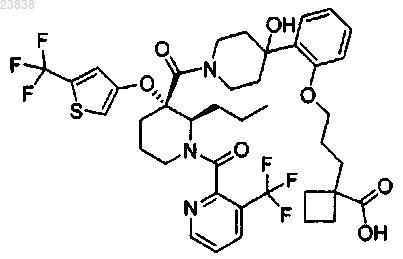
или его фармацевтически приемлемая соль.
24. Соединение, которое представляет собой
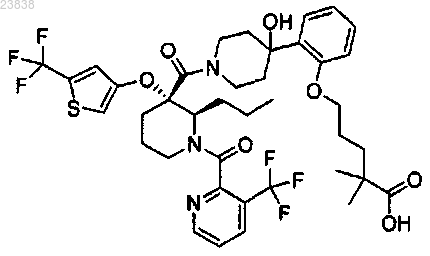
или его фармацевтически приемлемая соль.
25. Фармацевтическая композиция для лечения рака, включающая терапевтически эффективное количество по меньшей мере одного соединения по любому одному из пп.1-24 или его фармацевтически приемлемой соли, в сочетании по меньшей мере с одним фармацевтически приемлемым носителем.
26. Применение соединения по любому одному из пп.1-24 для получения лекарственного средства для лечения рака, выбранного из группы, включающей колоректальный рак, рак почек, мочевого пузыря, молочной железы, толстой кишки, прямой кишки, эндометрия, почек, печени, легких, головы и шеи, пищевода, желчного пузыря, шейки матки, поджелудочной железы, предстательной железы, гортани, яичников, желудка, матки, неходжкинскую лимфому, саркому, остеосаркому, липосаркому, рак щитовидной железы, гематопоэтические опухоли лимфоидной линии, гематопоэтические опухоли миелоидной линии, миелоцитарный лейкоз, миелодиспластический синдром, промиелоцитарный лейкоз, опухоли мезенхимального происхождения, опухоли центральной и периферической нервной системы, меланому, рак кожи, мезотелиому, семиному, тератокарциному, пигментную ксеродерму, роговую кератому, глиобластому, острый миелолейкоз, острый лимфобластный лейкоз, фолликулярный рак щитовидной железы и саркому Капоши.
Текст
ЗАМЕЩЕННЫЕ ПИПЕРИДИНЫ, КОТОРЫЕ ПОВЫШАЮТ АКТИВНОСТЬ p53, И ИХ ПРИМЕНЕНИЕ Изобретение обеспечивает соединение формулы (1), рассмотренное в настоящем патенте, или его фармацевтически приемлемую соль. Соединения являются полезными в качестве ингибиторов белка HDM2. Также раскрыты фармацевтические композиции, включающие описанные выше соединения, и способы лечения рака с использованием этих соединений.(71)(73) Заявитель и патентовладелец: МЕРК ШАРП ЭНД ДОМЭ КОРП. Область, к которой относится изобретение Настоящее изобретение относится к новым соединениям, полезным в качестве ингибиторов, регуляторов или модуляторов человеческого двойного микробелка 2 (Human Double Minute 2 ("HDM2") protein), к фармацевтическим композициям, содержащим такие соединения, и к способам лечения с использованием соединений и композиций для лечения заболеваний, таких как, например, рак, заболевания,включающие аномальную пролиферацию клеток, и заболевания, вызванные нарушением уровня р 53. Настоящее изобретение, в частности, раскрывает замещенные пиперидины в качестве ингибиторовHDM2 белка. Предпосылки создания изобретения Белок-супрессор опухолевого роста р 53 играет центральную роль в поддержании целостности генома в клетке, регулируя экспрессию разнообразных генов, ответственных за репарацию ДНК, подавление клеточного цикла и роста и апоптоз [May et al., Oncogene 18(53) (1999), p. 7621-7636; Oren, Cell DeathDiffer. 10 (4) (2003), p. 431-442, Hall and Peters, Adv. Cancer Res., 68: (1996), p. 67-108; Hainaut et al., Nucleic Acid Res., 25: (1997), p. 151-157; Sherr, Cancer Res., 60: (2000), p. 3689-95]. В ответ на онкогенные стрессовые сигналы клетка включает фактор транскрипции р 53 для активации генов, участвующих в регуляции клеточного цикла, инициируя, таким образом, апоптоз или подавление клеточного цикла. Апоптоз способствует удалению поврежденных клеток из организма, в то время как подавление клеточного цикла позволяет поврежденным клеткам восстановить генетические повреждения [рассмотрено в Ko etal., GenesDevel. 10: (1996), p. 1054-1072; Levine, Cell 88: (1997), p. 323-331]. Потеря защитных функций р 53 провоцирует поврежденные клетки к развитию ракового состояния. Инактивация р 53 у мышей неизменно приводит к необычно высокой скорости роста опухолей [Donehower et al., Nature. 356: (1992),p. 215-221]. Фактор транскрипции р 53 способствует экспрессии ряда регуляторных генов клеточного цикла,включая его собственный отрицательный регулятор, ген, кодирующий мышиный двойной микробелок 2MDM2 (обозначенный HDM2 у человека) проявляет действие, подавляющее р 53 активность саморегулирующим образом [Wu et al., Genes Dev., 7: (1993), p. 1126-1132; Bairak et al., EMBO J, 12: (1993), p. 461468]. В отсутствие онкогенных стрессовых сигналов, т.е. в нормальных клеточных условиях, белокMDM2 служит для поддержания активности р 53 на низких уровнях [Wu et al., Genes Dev., 7: (1993), p. 1126-1132; Barak et al., EMBO J. 12: (1993), p. 461-468]. Однако в ответ на повреждение клеточной ДНК или в условиях клеточного стресса активность р 53 возрастает, помогая предотвратить распространение перманентно поврежденных клонов клеток путем индукции подавления клеточного цикла и роста или апоптоза. Регулирование р 53 функции зависит от надлежащего баланса между двумя компонентами этой p53MDM2 системы авторегулирования. Действительно, этот баланс оказывается существенным для клеточного выживания. Существует по меньшей мере три пути действия MDM2 для подавления активности р 53. Во-первых, MDM2 может связываться с N-концевым доменом активации транскрипции р 53 для блокирования экспрессии р 53-респонсивных генов [Kussie et al., Science, 274: (1996), p. 948-953; Oliner etal., Nature. 362: (1993), p. 857-860; Momand et al., Cell, 69: (1992), p. 1237-1245]. Во-вторых, MDM2 перемещает р 53 из ядра в цитоплазму для облегчения протеолитического разложения р 53 [Roth et al., EMBOAcad. Sci. 96: (1999), p. 3077-3080]. И, наконец, MDM2 обладает собственной Е 3 лигазной активностью для конъюгации убихитина с р 53 для разложения в убихитин-зависимом 26S протеосомном пути [Hondaet al., FEBS Lett. 420: (1997), p. 25-27; Yasuda. Oncogene 19: (2000), p. 1473-1476]. Таким образом, MDM2 препятствует способности р 53 транскрипционного фактора активировать экспрессию его генов-мишеней путем связывания р 53 в ядре. Ослабление авторегулирующей системы р 53-MDM2 может иметь существенное воздействие на клеточный гомеостаз. Неизменно сообщалось о корреляции между гиперэкспрессией MDM2 и образованием опухолей [Chene, Nature 3: (2003), p. 102-109]. Функциональная инактивация р 53 дикого типа обнаружена во многих типах опухолей человека. Восстановление функции р 53 в опухолевых клетках при помощи анти-MDM2 терапии может привести к замедлению пролиферации опухоли и вместо этого стимулировать апоптоз. Поэтому неудивительно, что в настоящее время прилагаются значительные усилия для определения новых противоопухолевых средств, которые препятствуют способности HDM2 взаимодействовать с р 53 [Chene, Nature 3: (2003), p. 102-109]. Было показано, что антитела,пептиды и антисмысловые олигонуклеотиды разрушают взаимодействие p53-MDM2, что позволит освободить р 53 от отрицательного контроля MDM2, приводя к активации р 53 пути, обеспечивая возможность функционирования нормальных сигналов задержки роста и/или апоптоза, что предлагает потенциальный терапевтический подход к лечению рака и других заболеваний, характеризующихся патологической пролиферацией клеток. [См., например, Blaydes et al., Oncogene 14: (1997), p. 1859-1868; Bottger et al., Oncogene 13 (10): (1996), p. 2141-2147]. Публикация США 2005/0037383 A1 описывает модифицированный растворимый HDM2 белок,нуклеиновые кислоты, которые кодируют этот HDM2 белок, кристаллы этого белка, которые являются подходящими для рентгеновского кристаллографического анализа, использование белков и кристаллов для определения, выбора или разработки соединений, которые могут быть использованы в качестве противораковых средств, и некоторых соединений как таковых, которые связываются с модифицированнымHDM2. (Schering-Plough Corp.). Были описаны небольшие молекулы, определенные как антагонизирующие p53-MDM2 взаимодействие. WO 00/15657 (Zeneca Limited) описывает пиперизин-4-фенильные производные в качестве ингибиторов взаимодействия между MDM2 и р 53. Grasberger et al. (J. Med. Chem. 48 (2005), p. 909-912) (JohnsonJohnson Pharmaceutical ResearchDevelopment L.L. С.) описывает открытие и сокристаллическую структуру бензодиазепиндиона в качестве антагониста HDM2, который активирует р 53 в клетках. Galatinet al. (J. Med. Chem. 47 (2004), p. 4163-4165) описывает непептидный сульфонамидный ингибитор взаимодействия p53-MDM2 и активатор р 53-зависимой транскрипции в MDM2-гиперэкспрессирующих клетках.Vassilev (J. Med. Chem. (Perspective), vol. 48, 14 (2005), p. 1-8) (Hoffmann-LaRoche Inc.) описывает некоторые небольшие молекулы-активаторы р 53 для применения в онкологии, включая следующие формулы: Первые четыре соединения, перечисленные выше, были также описаны в Totouhi et al. (Current Topics in Medicinal Chemistry, vol. 3,2 (2005), p. 159-166, at 161) (Hoffmann La Roche Inc.). Последние три соединения, перечисленные выше, были также описаны в Vassilev et al. (Science, vol. 303 (2004): p. 844848) (Hoffmann La Roche Inc.), и их влияние на лейкозную активность лейкемии было исследовано в Kojima et al. (Blood., vol. 1089 (Nov. 2005), p. 3150-3159).Ding et al. (J. Am. Chem. Soc. vol. 127 (2005): 10130-10131) и (J. Med. Chem. vol. 49 (2006): 34323435) описывает некоторые спирооксиндольные соединения в качестве ингибиторов MDM2-p53.Lu, et al. (J. Med. Chem. vol. 49 (2006): 3759-3762) описал 7-[анилино(фенил)метил]-2-метил-8 хинолинол в качестве небольшого молекулярного ингибитора взаимодействия MDM2-p53.Chne (Molecular Cancer Research, vol. 2: (January 2006), p. 20-28) описывает ингибирование взаимодействия p53-MDM2 путем прицельного действия на границу раздела белок-белок. Публикации США 2004/0259867 А 1 и 2004/0259884 А 1 описывают цис-имидазолы (Hoffmann La Roche Inc.),WO 2005/110996A1 и WO 03/051359 описывают цис-имидазолины (Hoffmann La Roche Inc.) в качестве соединений, которые ингибируют взаимодействие MDM2 с р 53-подобными пептидами, приводя к антипролиферации. WO 2004/080460 А 1 описывает замещенные пиперидиновые соединения в качестве ингибиторов MDM2-p53 для лечения рака (Hoffmann La Roche Inc.). ЕР 0947494 A1 описывает производные феноксиуксусной кислоты и феноксиметилтетразол, которые действуют в качестве антагонистов MDM2 и препятствуют взаимодействию белок-белок между MDM2 и р 53, что приводит к противоопухолевым свойствам (Hoffmann La Roche Inc.). Duncan et al., J. Am. Chem. Soc. 123 (4): (2001), p. 554-560 описывает антагонист p-53-MDM2, хлорфузин, из Fusarium Sp. Stoll et al., Biochemistry 40 (2) (2001), p. 336-344 описывает хальконовые производные, которые являются антагонистами взаимодействий между человеческим онкобелком MDM2 и р 53. Существует потребность в эффективных ингибиторах HDM2 или MDM2 белка для лечения или профилактики рака, других болезненных состояний, связанных с клеточной пролиферацией, заболеваний, связанных с HDM2, или заболеваний, вызванных нарушением активности р 53. Настоящее изобретение раскрывает соединения, которые обладают активностью, направленной на ингибирование или антагонизм взаимодействия HDM2-p53 и MDM2-p53 и/или активацию белков р 53 в клетках. В его многочисленных вариантах воплощения настоящее изобретение обеспечивает новые соединения, обладающие активностью антагонистов HDM2 или MDM2, способы получения таких соединений,фармацевтические композиции, включающие одно или несколько из таких соединений, способы получения фармацевтических композиций, включающих одно или несколько из таких соединений, способы лечения и профилактики одного или нескольких заболеваний, связанных с HDM2, MDM2, р 53 или р 53 пептидами, путем введения таких соединений или фармацевтических композиций.WO 2008/005268 (эквивалент патентной публикации США 2008/0004287 А 1) раскрывает замещенные пиперидиновые соединения в качестве ингибиторов HDM2. Краткое изложение изобретения В его многочисленных вариантах воплощения настоящее изобретение обеспечивает новый класс замещенных пиперидиновых соединений, фармацевтические композиции, включающие одно или несколько указанных соединений, и способы применения указанных соединений для лечения или профилактики заболевания, связанного с белком HDM2. Таким образом, в одном аспекте настоящее изобретение обеспечивает соединение формулы 1 или его фармацевтически приемлемую соль, где R1 представляет собой в которой Е выбран из группы, включающей Н, галоген, ОН, CN, -O(C1-С 6)алкил, -(C1-C6)алкил,-С(О)ОН, -C(O)NR8R8', -(C1-C6)алкил-С(О)ОН, -(C1-C6)алкил-ОН, -(C1-C6)алкил-С(О)NR8R8', -(С 2 С 6)алкенил и -(С 2-С 6)алкинил; каждый J независимо выбран из Н и галогена;Y может присутствовать или отсутствовать, когда Y присутствует, он выбран из О, S, NR8, SO2 и 8 8'G выбран из группы, включающей -(CR8R8')n-С(О)ОН, где n=3, 4, 5 или 6, -(CR8R8')n-(С 3 С 8)циклоалкил(CR8R8')n-C(O)OH, (CR8R8')n-O-(CR8R8')n-(С 3-С 8)циклоалкил(CR8R8')n-C(O)ОН, -(CR8R8')n-S(CR8R8')n-C(O)OH и -(CR8R8')n-P(O)OR8OR8'; где каждый R8 и R8' независимо выбран из Н, D или (C1C6)алкила; или где R8 и R8' вместе с атомом углерода, с которым каждый из них связан, образуют (С 3 С 8)циклоалкил; если не обозначено иначе, каждый n независимо имеет значение 0-10; при условии, что, когда n имеет значение 0, любой атом кислорода, азота или серы группы Y не связан непосредственно с какимлибо атомом кислорода, серы или фосфора группы G;R4, R4', R5, R5', R6, R6', R7 и R7', каждый независимо, выбраны из водорода и (C1-C6)алкила;X представляет собой В анализе на активность ингибирования HDM2 (анализ флуоресцентной поляризации) [Zhang et al.,J. Analytical Biochemistry 331: 138-146 (2004)] соединения по настоящему изобретению демонстрируют значения FP IC50 меньше чем 0,5 мкМ. Также исследования ингибирования фермента цитохром Р 4503 А 4 соединениями по настоящему изобретению указывают, что эти соединения имеют значение IC50 CYP3A4(пред- и соинкубация) больше чем 1 мкМ. Соединения по настоящему изобретению, как таковые или в сочетании с одним или несколькими другими подходящими средствами, раскрытыми далее в настоящем изобретении, могут быть полезными в качестве ингибиторов HDM2 или MDM2 и могут быть полезными для лечения и профилактики пролиферативных заболеваний, таких как раковые опухоли. Такое лечение или профилактику можно осуществлять с соединением по настоящему изобретению,а также с фармацевтическими композициями или составами, включающими такое соединение. Подробное описание изобретения В одном варианте воплощения настоящее изобретение обеспечивает соединения, проиллюстрированные как формула 1, описанная выше, или их фармацевтически приемлемые соли, сольваты, сложные эфиры или пролекарства, где различные группы имеют значения, описанные выше. В другом варианте воплощения, в формуле 1, R отсутствует и Е присутствует, т.е. R1 в формуле 1 представляет собой Если не обозначено иначе, каждый n независимо имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, при условии, что, когда n имеет значение 0, любой атом кислорода, азота или серы группы Y не связан непосредственно с каким-либо атомом кислорода, азота, серы или фосфора группы G. В другом варианте воплощения, в формуле 1, Е выбран из группы, включающей Н, галоген, ОН,CN, -О(C1-C6)алкил, (C1-C6)алкил, -С(О)ОН, -C(O)NR8R8', -(C1-C6)алкил-С(О)ОН, -(С 1-С 6)алкил-ОН и-(C1-C6)алкил-С(О)NR8R8'. В другом варианте воплощения, в формуле 1, каждый J, независимо, представляет собой Н или фтор. В другом варианте воплощения, в формуле 1, Y выбран из группы, включающей О, S, SO2 и CR8R8'. В другом варианте воплощения, в формуле 1, Y представляет собой CR8R8', где R8 и R8' оба представляют собой Н, т.е. Y представляет собой СН 2. В другом варианте воплощения, в формуле 1, G выбран из группы, включающей -(CR8R8')n-(С 3 С 8)циклоалкил(CR8R8')n-С(О)ОН и -(CR8R8')n-O-(CR8R8')n-(C3-C8)циклоалкил(CR8R8')n-С(О)ОН. В другом варианте воплощения, в формуле 1, указанный -(CR8R8')n-(С 3-С 8)циклоалкил(CR8R8')nС(О)ОН выбран из группы, включающей -СН 2-циклопентил-С(О)ОН, -циклобутил-С(О)ОН, циклопентил-С(О)ОН, -циклогексил-С(О)ОН и -циклопентил-СН 2-С(О)ОН; указанный -(CR8R8')n-O-(CR8R8')n-(С 3 С 8)циклоалкил(CR8R8')n-С(О)ОН представляет собой -О-циклопентил-С(О)ОН или -О-циклобутилС(О)ОН; указанный -(CR8R8')n-Р(О)OR8OR8' представляет собой (СН 2)3 Р(О)(ОН)(ОН) или-(CR R )n-O-(CR8R8')n-(C3-С 8)циклоалкил(CR8R8')n-C(O)OH. В другом варианте воплощения, в формуле 1, R4 представляет собой водород и R4' представляет собой 1-пропил, таким образом, формула 1 представлена формулой 1 А в которой R4 представляет собой водород и R4' представляет собой 1-пропил;R2 пред ставляет собой и либо (i) каждый J в R1 представляет собой Н, либо (ii) один J в R1 представляет собой галоген, а остальные три J представляют собой Н, т.е. формула 1, 1 А или 1 В представлена формулой 1 С или 1D, которые представлены ниже: В другом варианте воплощения, в формуле 1B, R1 представляет собой ставляет собой Неограничивающие примеры соединений формулы 1 включают: или их фармацевтически приемлемые соли. Как использовалось выше и далее в настоящем раскрытии, следующие термины, если не указано иное, имеют следующие значения. Любое дополнительное необходимое определение следует понимать так, как описано в WO 2008/005268 (эквивалент патентной публикации США US 2008/0004287 А 1)."Алкил" означает алифатическую углеводородную группу, которая может быть прямой или разветвленной и включает от около 1 до около 20 атомов углерода в цепи. Предпочтительные алкильные группы содержат от около 1 до около 12 атомов углерода в цепи. Более предпочтительные алкильные группы содержат от около 1 до около 6 атомов углерода в цепи. "Разветвленный" означает, что одна или несколько низших алкильных групп, таких как метил, этил или пропил, присоединены к линейной алкильной цепи. "Низший алкил" означает группу, содержащую от около 1 до около 6 атомов углерода в цепи, которая может быть прямой или разветвленной."Алкенил" означает алифатическую углеводородную группу, содержащую по меньшей мере одну двойную углерод-углеродную связь, и которая может быть прямой или разветвленной и содержащей от около 2 до около 15 атомов углерода в цепи. Предпочтительные алкенильные группы содержат от около 2 до около 12 атомов углерода в цепи; и, более предпочтительно, от около 2 до около 6 атомов углерода в цепи. "Разветвленный" означает, что одна или несколько низших алкильных групп, таких как метил, этил или пропил, присоединены к линейной алкенильной цепи. "Низший алкенил" означает от около 2 до около 6 атомов углерода в цепи, которая может быть прямой или разветвленной."Алкилен" означает бифункциональную группу, полученную путем удаления атома водорода из алкильной группы, которая определена выше. Неограничивающие примеры алкилена включают метилен,этилен и пропилен."Алкинил" означает алифатическую углеводородную группу, содержащую по меньшей мере одну тройную углерод-углеродную связь, и которая может быть прямой или разветвленной и содержащей от около 2 до около 15 атомов углерода в цепи. Предпочтительные алкинильные группы содержат от около 2 до около 12 атомов углерода в цепи; и, более предпочтительно, от около 2 до около 4 атомов углерода в цепи. "Разветвленный" означает, что одна или несколько низших алкильных групп, таких как метил, этил или пропил, присоединены к линейной алкинильной цепи. "Низший алкинил" означает от около 2 до около 6 атомов углерода в цепи, которая может быть прямой или разветвленной. Неограничивающие примеры подходящих алкинильных групп включают этинил, пропинил, 2-бутинил, 3-метилбутинил."Циклоалкил" означает неароматическую моно- или полициклическую кольцевую систему, содержащую от около 3 до около 10 атомов углерода, предпочтительно от около 5 до около 10 атомов углерода. Предпочтительные циклоалкильные кольца содержат от около 5 до около 7 кольцевых атомов. Циклоалкил может быть необязательно замещенным одним или несколькими "заместителями кольцевой системы", которые могут быть одинаковыми или отличными друг от друга и которые определены выше. Неограничивающие примеры подходящих моноциклических циклоалкилов включают циклопропил,циклопентил, циклогексил, циклогептил и подобные. Неограничивающие примеры подходящих полициклических циклоалкилов включают 1-декалинил, норборнил, адамантил и подобные."Циклоалкилалкил" означает циклоалкильную группу, определенную выше, связанную через алкильную группу (определена выше) с исходным (материнским) ядром. Неограничивающие примеры подходящих циклоалкилалкилов включают циклогексилметил, адамантилметил и подобные."Гидроксиалкил" означает группу НО-алкил-, где алкил определен выше. Предпочтительные гидроксиалкилы содержат низший алкил. Неограничивающие примеры подходящих гидроксиалкильных групп включают гидроксиметил и 2-гидроксиэтил. Термин "замещенный" означает, что один или несколько атомов водорода на указанном атоме замещены членом, выбранным из указанной группы, при условии, что указанная обычная валентность этого атома в существующих условиях не превышена и что такое замещение приводит к стабильному соединению. Сочетания заместителей и/или переменных допустимы только в случае, когда такие сочетания приводят к стабильным соединениям. Под "стабильным соединением" или "стабильной структурой" подразумевается соединение, которое достаточно устойчиво при его выделении до полезной степени чистоты из реакционной смеси и формулировании в эффективное терапевтическое средство. Термин "необязательно замещенный" означает необязательное замещение указанными группами,радикалами или фрагментами. Термин "очищенный", "в очищенной форме" или "в выделенной и очищенной форме" в отношении соединения относится к физическому состоянию указанного соединения после его выделения из процесса синтеза (например, из реакционной смеси) или природного источника или их сочетания. Таким образом, термин "очищенный", "в очищенной форме" или "в выделенной и очищенной форме" в отношении соединения относится к физическому состоянию указанного соединения после его получения способом очистки или способами, описанными в настоящем изобретении или хорошо известными специалистам в данной области (например, хроматография, перекристаллизация и подобные), с достаточной чистотой,чтобы его можно было охарактеризовать стандартными аналитическими методами, описанными в настоящем изобретении или хорошо известными специалистам в данной области. Также следует указать, что предполагается, что любой углерод, а также гетероатом с неудовлетворенными валентностями в тексте, схемах, примерах и таблицах в настоящем изобретении содержит достаточное количество атомов водорода для удовлетворения валентностям. Когда функциональная группа в соединении указана как "защищенная", это означает, что группа находится в модифицированной форме для предотвращения нежелательных побочных реакций на защищенном участке, когда соединение подвергают взаимодействию. Подходящие защитные группы должны быть известны специалистам в данной области, а также из справочной литературы, такой как, например,Т. W. Greene et al., Protective Groups in organic Synthesis (1991), Wiley, New York. Когда какая-либо переменная (например, R2 и т.п.) встречается больше одного раза в какой-либо составляющей или в формуле 1, ее определение в каждом случае ее присутствия независимо от определения в каждом другом случае ее присутствия. Как он используется в настоящем изобретении, термин "композиция" охватывает продукт, включающий указанные ингредиенты в указанных количествах, а также любой продукт, который является результатом, прямым или косвенным, сочетания указанных ингредиентов в указанных количествах. Например, когда соединение формулы 1 или его фармацевтически приемлемая соль содержит карбоново-кислотную функциональную группу, пролекарство может включать сложный эфир, образованный путем замены атома водорода кислотной группы группой, такой как, например, (C1-C8)алкил, (С 2C12)алканоилоксиметил, 1-(алканоилокси)этил, содержащей от 4 до 9 атомов углерода, 1-метил-1(алканоилокси)этил, содержащей от 5 до 10 атомов углерода, алкоксикарбонилоксиметил, содержащей от 3 до 6 атомов углерода, 1-(алкоксикарбонилокси)этил, содержащей от 4 до 7 атомов углерода, 1 метил-1-(алкоксикарбонилокси)этил,содержащей от 5 до 8 атомов углерода,N(алкоксикарбонил)аминометил,содержащей от 3 до 9 атомов углерода,1-(N(алкоксикарбонил)амино)этил, содержащей от 4 до 10 атомов углерода, 3-фталидил, 4-кротонолактонил,гамма-бутиролактон-4-ил, ди-N,N-(С 1-С 2)алкиламино (С 2-С 3)алкил (такой как -диметиламиноэтил),карбамоил(С 1-С 2)алкил, N,N-ди(С 1-С 2)алкилкарбамоил(С 1-С 2)алкил и пиперидино-, пирролидино- или морфолино(С 2-С 3)алкил и подобные. Подобным образом, когда соединение формулы 1 содержит спиртовую функциональную группу,пролекарство может быть образовано путем замены атома водорода спиртовой группы группой, такой 1-С 1-С 6)алканоилокси) этил,1-метил-1-С 1 как,например,(С 1-С 6)алканоилоксиметил,С 6)алканоилокси) этил, (C1-С 6)алкоксикарбонилоксиметил, N-(С 1-С 6)алкоксикарбониламинометил, сукциноил, (С 1-С 6)алканоил, -амино(С 1-С 4)алканил, арилацил и -аминоациламиноацил, где каждая аминоацильная группа независимо выбрана из природных L-аминокислот, P(O)(OH)2, -Р(O)(О(C1C6)алкил)2 или гликозила (радикал, образованный в результате удаления гидроксильной группы гемиацетальной формы углеводорода) и подобные. Когда соединение формулы 1 включает функциональную группу амина, пролекарство может быть образовано путем замены атома водорода в группе амина группой, такой как, например, R-карбонил, ROкарбонил, NRR'-карбонил, где R и R', каждый независимо, представляют собой (C1-C10)алкил, (С 3 С 7)циклоалкил, бензил, или R-карбонил представляет собой природный -аминоацил или природный аминоацил, -С(ОН)С(О)OY1, где Y представляет собой Н, (C1-C6)алкил или бензил, -C(OY2)Y3, где Y2 представляет собой (C1-C4)алкил и Y3 представляет собой (C1-C6)алкил, карбокси (C1-C6)алкил, амино(C1-С 4)алкил или моно-N- или ди-N,N-(C1-C6)алкиламиноалкил, -C(Y4)Y5, где Y4 представляет собой Н или метил и Y5 представляет собой моно-N- или ди-N,N-(С 1-С 6)алкиламино морфолино, пиперидин-1-ил или пирролидин-1-ил и т.п. Одно или несколько соединений по настоящему изобретению могут существовать в несольватированной, а также в сольватированной форме с фармацевтически приемлемыми растворителями, такими как вода, этанол и подобные, и предполагается, что изобретение охватывает как сольватированные, так и несольватированные формы. "Сольват" означает физическую ассоциацию соединения по настоящему изобретению с одной или несколькими молекулами растворителя. Эта физическая ассоциация включает различные степени образования ионных и ковалентных связей, включая водородные связи. В некоторых случаях сольват можно выделить, например, когда одна или несколько молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. "Сольват" охватывает как находящиеся в фазе раствора, так и выделяемые сольваты. Неограничивающие примеры подходящих сольватов включают этаноляты, метаноляты и подобные. "Гидрат" представляет собой сольват, где молекула растворителя представляет собой H2O. Одно или несколько соединений по настоящему изобретению, необязательно, могут быть преобразованы в сольват. Получение сольватов общеизвестно. Таким образом, например, М. Caira et al., J. Pharmaceutical Sci., 93(3), 601-611 (2004) описывают получение сольватов противогрибкового флуконазола в этилацетате, а также из воды. Подобные получения сольватов, гемисольватов, гидратов и т.п. описано Е. С. van Tonder et al., AAPS PharmSciTech., 5(1), article 12 (2004); и A. L. Bingham et al., Chem. Commun.,603-604 (2001). Типичный неограничивающий способ включает растворение соединение по настоящему изобретению в желательных количествах желательного растворителя (органический растворитель или вода, или их смеси) при температуре выше, чем температура окружающей среды, и охлаждение раствора со скоростью, достаточной для образования кристаллов, которые затем выделяют стандартными способами. Аналитические методы, такие как, например, инфракрасная спектроскопия, показывают присутствие растворителя (или воды) в кристаллах в виде сольвата (или гидрата)."Эффективное количество" или "терапевтически эффективное количество" описывает количество соединения или композиции по настоящему изобретению, эффективное для ингибирования указанных выше заболеваний, с получением, таким образом, желательного терапевтического, амелиоративного, ингибиторного или превентативного эффекта. Соединения формулы 1 могут образовывать соли, которые также включены в объем настоящего изобретения. Ссылку на соединение формулы 1 в настоящем изобретении следует рассматривать как включающую ссылку на их соли, если не указано иное. Термин "соль(соли)", как он используется в на- 24023838 стоящем изобретении, означает кислотные соли, образованные с неорганическими и/или органическими кислотами, а также основные соли, образованные с неорганическими и/или органическими основаниями. Кроме того, когда соединение формулы 1 содержит как основную группу, такую как, но не ограничиваясь этим, пиридин или имидазол, так и кислотную группу, такую как, но не ограничиваясь этим, карбоновую кислоту, могут быть образованы цвиттерионы ("внутренние соли"), и они охватываются термином"соль(соли)", как он используется в настоящем изобретении. Фармацевтически приемлемые (т.е. нетоксичные физиологически приемлемые) соли являются предпочтительными, хотя другие соли также являются полезными. Соли соединений формулы 1 могут быть образованы, например, путем взаимодействия соединения формулы 1 с определенным количеством кислоты или основания, таким как эквивалентное количество, в среде, такой как среда, где осаждается соль, или в водной среде, с последующей лиофилизацией. Примеры кислотно-аддитивных солей включают ацетаты, аскорбаты, бензоаты, бензолсульфонаты,бисульфаты, бораты, бутираты, цитраты, камфораты, камфорсульфонаты, фумараты, гидрохлориды, гидробромиды, гидроиодиды, лактаты, малеаты, метансульфонаты, нафталинсульфонаты, нитраты, оксалаты, фосфаты, пропионаты, салицилаты, сукцинаты, сульфаты, тартраты, тиоцианаты, толуолсульфонаты(также известные как тозилаты) и подобные. Кроме того, кислоты, которые, как правило, считаются подходящими для образования фармацевтически полезных солей из основных фармацевтических соединений, обсуждаются, например, в P. Stahl et al., Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties,Selection and Use. (2002) Zurich: Wiley-VCH; S. Berge ef al., Journal of Pharmaceutical Sciences (1977), 66(1) 1-19; P. Gould, International J. of Pharmaceutics (1986), 33, 201-217; Anderson et al., The Practice of MedicinalChemistry (1996), Academic Press, New York; и в The Orange Book (FoodDrug Administration, Washington, D.C. на их web-сайте). Эти раскрытия включены в настоящее изобретение посредством ссылки. Примеры основных солей включают соли аммония, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочно-земельных металлов, такие как соли кальция и магния, соли с органическими основаниями (например, органическими аминами), такими как дициклогексиламины, третбутиламины и соли с аминокислотами, такими как аргинин, лизин и подобные. Основные азотсодержащие группы могут быть кватернизованы при помощи агентов, таких как низшие алкилгалогениды (например, метил-, этил- и бутилхлориды, -бромиды и -иодиды), диалкилсульфаты (например, диметил-, диэтил- и дибутилсульфаты), длинноцепочечные галогениды (например, децил-, таурил- и стеарилхлориды, -бромиды и -иодиды), аралкилгалогениды (например, бензил- и фенэтилбромиды) и др. Все такие кислотные соли и основные соли рассматриваются как фармацевтически приемлемые соли, охватываемые настоящим изобретением, и все кислотные соли и основные соли считаются эквивалентными свободным формам соответствующих соединений для целей настоящего изобретения. Соединения формулы 1 и их соли, могут существовать в их таутомерной форме (например, в форме амида или иминоэфира). Все такие таутомерные формы предусматриваются в настоящем изобретении как часть настоящего изобретения. Соединения формулы 1 могут содержать асимметрические или хиральные центры и поэтому могут существовать в различных стереоизомерных формах. Предполагается, что все стереоизомерные формы соединений формулы 1, а также их смеси, включая рацемические смеси, составляют часть настоящего изобретения. Кроме того, настоящее изобретение охватывает все геометрические изомеры и изомеры положения. Например, когда соединение формулы 1 включает двойную связь или конденсированное кольцо, объемом настоящего изобретения охватываются как цис-, так и трансформы, а также смеси. Диастереомерные смеси можно разделить на их индивидуальные диастереомеры на основании разницы в их физико-химических свойствах с использованием способов, хорошо известных специалистам в данной области, таких как, например, хроматография и/или фракционированная кристаллизация. Энантиомеры можно разделить путем преобразования энантиомерной смеси в диастереомерную смесь путем взаимодействия с подходящим оптически активным соединением (например, хиральным вспомогательным веществом, таким как хиральный спирт или хлорангидрид кислоты Мошера), разделения диастереомеров и преобразования (например, гидролиз) индивидуальных диастереомеров в соответствующие чистые энантиомеры. Также некоторые соединения формулы 1 могут быть в форме атропизомеров (например, замещенные биарилы), и они считаются частью настоящего изобретения. Энантиомеры также можно разделить с использованием хиральной ВЭЖХ колонки. Также соединения формулы 1 могут существовать в различных таутомерных формах, и все такие формы охватываются объемом настоящего изобретения. Также, например, все кето-енольные и иминенаминовые формы соединений включены в изобретение. Все стереоизомеры (например, геометрические изомеры, оптические изомеры и подобные) соединений по настоящему изобретению (включая стереоизомерные формы солей, сольватов, сложных эфиров и пролекарств соединений, а также солей, сольватов и сложных эфиров пролекарств), такие как стереоизомеры, которые могут существовать, благодаря асимметрическим атомам углерода на различных заместителях, включая энантиомерные формы (которые могут существовать даже в отсутствие асимметрических атомов углерода), ротамерные формы, атропизомеры и диастереомерные формы предусматриваются как включенные в объем настоящего изобретения, также как и изомеры положения (такие как, на- 25023838 пример, 4-пиридил и 3-пиридил). (Например, когда соединение формулы 1 включает двойную связь или конденсированное кольцо, как цис-, так и транс-формы, а также смеси охватываются объемом настоящего изобретения. Также, например, все кето-енольные и имин-енаминовые формы соединений включены в настоящее изобретение). Индивидуальные стереоизомеры соединений по настоящему изобретению могут быть, например, по существу свободными от других изомеров или могут присутствовать в виде смесей, например, в виде рацематов или со всеми другими, или другими выбранными, стереоизомерами. Хиральные центры по настоящему изобретению могут иметь S- или R-конфигурацию, определенную в соответствии с рекомендациями IUPAC 1974. Предполагается, что используемые термины "соль", "сольват", "сложный эфир", "пролекарство" и подобные равным образом применимы к соли, сольвату, сложному эфиру и пролекарству энантиомеров, стереоизомеров, ротамеров, таутомеров, изомеров положения,рацематов или пролекарств по настоящему изобретению соединения. Настоящее изобретение также охватывает изотопно меченые соединения по настоящему изобретению, которые идентичны соединениям, представленным в настоящем изобретении, но отличаются тем,что один или несколько атомов заменены атомом, имеющим атомную массу или массовое число, отличные от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению, включают изотопы водорода,углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2 Н, 3 Н, 13 С, 14 С, 15N, 18O, 17O, 31P, 32P, 35S,18F и 36Cl соответственно. Некоторые изотопно меченые соединения формулы 1 (например, соединения, меченые 3 Н и 14 С) являются полезными в анализах распределения соединения и/или ткани субстрата. Меченые тритием (т.е. 3 Н) и углерод-14 (т.е. 14 С) изотопы являются особенно предпочтительными из-за простоты их получения и возможности определения. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий(т.е. 2 Н), может дать некоторые терапевтические преимущества как результат более высокой метаболической стабильности (например, увеличение периода полувыведения in vivo или более низкие необходимые дозы), и, следовательно, могут быть предпочтительными в некоторых условиях. Термин "дейтерированный" в описании соединения по настоящему изобретению означает, что отношение дейтерия к водороду в дейтерированных областях молекулы по существу превышает встречающееся в природе отношение дейтерия к водороду. Википедия (http://en.wikipedia.org/wiki/Deuterium) предполагает, что природная распространенность дейтерия в океанах Земли приблизительно один атом в 6500 водорода (154 ч/млн, ppm). Дейтерий, таким образом, составляет приблизительно 0,015% (в расчете на массу, 0,030%) от всего природного водорода в океанах Земли. Однако другие источники предполагают более высокую распространенность, например, 6-10-4 (6 атомов в 10000, или 0,06% в расчете на атомы). Дейтерирование молекул и получение дейтерированных лекарственных средств известно. См., например, М. Tanabe et al., "The Pharmacologic Effect of Deuterium Substitution on 5-n-Butyl-5-ethyl BarbituricPharma (http://www.concertpharma.com/ConcertAnnouncesPreclinicalResultslCAAC.htm), касающиеся предклинических результатов их дейтерированного антибиотика С-20081,иhttp:/www.concertpharma.com/news/ConcertBeginsCTP347Phasel.htm, касающиеся фазы I клинических испытаний их дейтерий-содержащего модулятора серотонина СТР-347. Изотопно меченые соединения формулы 1, как правило, можно получить с использованием процедур, аналогичных тем, которые раскрыты на схемах и/или в примерах, описанных в настоящем изобретении ниже, путем использования подходящего изотопно меченого реагента вместо немеченого изотопом реагента. Например, дейтерирование специально проиллюстрировано в репрезентативных примерах 63 и 64. Полиморфные формы соединений формулы 1, а также солей, сольватов, сложных эфиров и пролекарств соединений формулы 1 включены в настоящее изобретение.HDM2, Hdm2, hDM2 и hdm2 - все являются репрезентативными эквивалентами человеческого двойного микробелка 2. Подобным образом, MDM2, Mdm2, mDM2 и mdm2 - все являются репрезентативными эквивалентами мышиного двойного микробелка 2. Соединения формулы 1 могут быть ингибиторами или антагонистами взаимодействия человеческого или мышиного двойного микробелка 2 с белком р 53, и это могут быть активаторы р 53 белка в клетках. Кроме того, фармакологические свойства соединений формулы 1 можно использовать для лечения или профилактики рака, лечения или профилактики других болезненных состояний, связанных с аномальной клеточной пролиферацией, и лечения или профилактики заболеваний, являющихся результатом нарушения уровней р 53 белка в клетках. Специалистам в данной области должно быть понятно, что термин "рак" означает заболевания, где клетки организма становятся аномальными и их деление неконтролируемо. Раковые заболевания, которые можно лечить соединениями, композициями и способами по настоящему изобретению, включают, но не ограничиваются этим, сердце: саркому (ангиосаркому, фибросаркому, рабдомиосаркому, липосаркому), миксому, рабдомиому, фиброму, липому и тератому; легкие:(аденокарциному, лимфому, карциноидные опухоли, саркому Капоши, лейомиому, гемангиому, липому,нейрофиброму, фиброму), толстый кишечник (аденокарциному, тубулярную аденому, ворсинчатую аденому, гамартому, лейомиому) колоректальные; мочеполовые пути: почки (аденокарциному, опухоль Вильма [нефробластома], лимфому, лейкоз), мочевой пузырь и уретру (сквамозно-клеточную карциному,переходно-клеточный рак, аденокарциному), предстательную железу (аденокарциному, саркому), мужские половые железы (семиному, тератому, эмбриональную карциному, тератокарциному, хориокарциному, саркому, интерстициально-клеточную карциному, фиброму, фиброаденому, аденоматоидные опухоли, липому); печень: гепатому (гепатоцеллюлярную карциному), холангиокарциному, гепатобластому,ангиосаркому, гепатоцеллюлярную аденому, гемангиому; кость: остеогенную саркому (остеосаркому),фибросаркому, злокачественную фиброзную гистиоцитому, хондросаркому, саркому Эвинга, злокачественную лимфому (ретикулоклеточную саркому), множественную миелому, злокачественную гигантоклеточную опухоль хордому, остеохронфрому (остеохондроцитарные экзостозы), доброкачественную хондрому, хондробластому, хондромиксофиброму, остеоидную остеому и гигантоклеточные опухоли; нервную систему: череп (остеому, гемангиому, гранулему, ксантому, деформирующий остит), мягкие мозговые оболочки (менингиому, менингиосаркому, глиоматоз), головной мозг (астроцитому, медуллобластому, глиому, эпендимому, герминому [пинеалома], мультиформную глиобластому, олигодендроглиому,шванному, ретинобластому, конгенитальные опухоли), нейрофиброму, менингиому, глиому, саркому спинного мозга); гинекологические: матку (эндометриальную карциному), шейку матки (цервикальную карциному, предопухолевую цервикальную дисплазию), яичники (карциному яичника [серозную цистаденокарциному, мукоидную цистаденокарциному, неклассифицированную карциному], гранулезотекально-клеточные опухоли, Сертоли-Лейдиг-клеточные опухоли, дисгерминому, злокачественную тератому), вульву (сквамозно-клеточную карциному, интраэпителиальную карциному, аденокарциному,фибросаркому, меланому), вагину (светлоклеточную карциному, сквамозно-клеточную карциному, ботриоидную саркому (эмбриональную рабдомиосаркому), фаллопиевы трубы (карциному), молочную железу; гематологические: кровь (миелоидный лейкоз [острый и хронический], острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, миелопролиферативные заболевания, множественную миелому, миелодиспластический синдром), болезнь Ходжкина, неходжкинскую лимфому [злокачественная лимфома]; кожу: злокачественную меланому, базально-клеточную карциному, сквамозно-клеточную карциному, саркому Капоши, синдром диспластического невуса, липому, ангиому, дерматофиброму,келоиды, псориаз; и надпочечники: нейробластому. Таким образом, термин "раковая клетка", как это указано в настоящем изобретении, включает клетку, пораженную каким-либо одним из вышеуказанных состояний. В одном варианте воплощения раковые заболевания, которые можно лечить с использованием соединений, композиций и способов по настоящему изобретению, включают, но не ограничиваются этим,легких рак, рак поджелудочной железы, рак толстой кишки, колоректальный рак, миелоидные лейкозы,острый миелогенный лейкоз, хронический миелогенный лейкоз, хронический миеломоноцитарный лейкоз, рак щитовидной железы, миелодиспластический синдром, карциному мочевого пузыря, эпидермальную карциному, меланому, рак молочной железы, рак предстательной железы, рак головы и шеи, рак яичника, рак головного мозга, раковые заболевания мезенхимального происхождения, саркомы, тетракарциномы, нейробластомы, карциномы почек, гепатомы, неходжкинскую лимфому, множественную миелому и анапластическую карциному щитовидной железы. В другом варианте воплощения раковые заболевания, которые можно лечить с использованием соединений, композиций и способов по настоящему изобретению, включают, но не ограничиваются этим,рак молочной железы, предстательной железы, толстой кишки, колоректальный, легких, головного мозга, яичников, желудка, поджелудочной железы, кожи, тонкого кишечника, толстого кишечника, горла,головы и шеи, ротовой полости, кости, печени, мочевого пузыря, почек, щитовидной железы и крови. В другом варианте воплощения раковые заболевания, которые можно лечить с использованием соединений, композиций и способов по настоящему изобретению, включают рак молочной железы, предстательной железы, толстой кишки, яичников, эндометрияи щитовидной железы. В другом варианте воплощения раковые заболевания, которые можно лечить с использованием соединений, композиций и способов по настоящему изобретению, включают рак молочной железы и предстательной железы. Соединения по настоящему изобретению также являются полезными для получения лекарственного средства, которое является полезным для лечения рака. Соединения по настоящему изобретению также являются полезными в сочетании с терапевтическими, химиотерапевтическими и противораковыми средствами. Сочетания соединений, раскрытых в настоящем изобретении, с терапевтическими, химиотерапевтическими и противораковыми средствами включены в объем настоящего изобретения. Примеры таких средств можно найти в Cancer Principles andPractice of Oncology by V.T. Devita and S. Hellman (editors), 6th edition (February 15, 2001), Lippincott WilliamsWilkins Publishers. Специалист в данной области со средней квалификацией сможет определить,какие сочетания средств могут быть полезными, на основании конкретных характеристик лекарственных средств и типа рака. Такие средства включают следующие: модуляторы эстрогенового рецептора, модуляторы урогенового рецептора, модуляторы ретиноидного рецептора, цитотоксические/цитостатические средства, антипролиферативные средства, ингибиторы пренил-протеинтрансферазы, ингибиторы HMGCoA редуктазы и другие ингибиторы ангиогенеза, ингибиторы ВИЧ-протеазы, ингибиторы обратной транскриптазы, ингибиторы клеточной пролиферации и сигнала выживания, бисфосфонаты, ингибиторы ароматазы, siPHK терапевтические средства, ингибиторы -секретазы, средства, которые воздействуют на рецепторные тирозиновые киназы (RTK), и средства, которые воздействуют на контрольные точки клеточного цикла. Соединения по настоящему изобретению являются особенно полезными при совместном применении с лучевой терапией. Термин "модуляторы эстрогенового рецептора" относится к соединениям, которые воздействуют на или ингибируют связывание эстрогена с рецептором, независимо от механизма. Примеры модуляторов эстрогенового рецептора включают, но не ограничиваются этим, тамоксифен, ралоксифен, идоксифен,LY353381, LY117081, торемифен, фулвестрант, 4-[7-(2,2-диметил-1-оксопропокси-4-метил-2-[4-[2-(1 пиперидинил)этокси]фенил]-2 Н-1-бензопиран-3-ил)]фенил-2,2-диметилпропаноат,4,4'дигидроксибензофенон-2,4-динитрофенилгидразон и SH646. Термин "модуляторы урогенового рецептора" относится к соединениям, которые препятствуют или ингибируют связывание урогенов с рецептором, независимо от механизма. Примеры модуляторов урогенового рецептора включают финастерид и другие ингибиторы 5-редуктазы, нитуламид, флутамид, бикалутамид, лиарозол и абиратерон ацетат. Термин "модуляторы ретиноидного рецептора" относится к соединениям, которые препятствуют или ингибируют связывание ретиноидов с рецептором, независимо от механизма. Примеры таких модуляторов ретиноидного рецептора включают бексаротен, третиноин, 13-цисретиноевую кислоту, 9-цис-ретиноевую кислоту, -дифторметилорнитин, ILX23-7553, транс-N-(4'гидроксифенил)ретинамид и N-4-карбоксифенилретинамид."Цитотоксические/цитостатические средства" относятся к соединениям, которые вызывают клеточную гибель или ингибируют клеточную пролиферацию преимущественно посредством вмешательства непосредственно в функционирование клетки, или ингибируют или воздействуют на клеточный миоз,включая алкилирующие средства, факторы некроза опухоли, интеркалирующие средства, гипоксияактивируемые соединения, ингибиторы микротрубочек/стабилизирующие микротрубочки средства, ингибиторы митотических кинезинов, ингибиторы гистон-деацетилазы, ингибиторы киназ, вовлеченных в митотическую прогрессию, ингибиторы киназ, вовлеченных в фактор роста и пути сигнальной трансдукции цитокинов,антиметаболитов,модификаторы биологического ответа,гормональные/антигормональные терапевтические средства, гематопоэтические ростовые факторы, моноклональное антитело-нацеливаемые терапевтические средства, ингибиторы топоизомеразы, ингибиторы протеосомы, ингибиторы убихитин-лигазы и ингибиторы киназы aurora. Примеры цитотоксических/цитостатических средств включают, но не ограничиваются этим, платиновые координирующие соединения, сертенеф, кахектин, ифосфамид, тасонермин, лонидамин, карбоплатин, алтретамин, преднимустин, дибромдулцитол, ранимустин, фотемустин, недаплатин, оксалиплатин, темозоломид, гептаплатин, эстрамустин, импросулфан тозилат, трофосфамид, нимустин, диброспидиум хлорид, пумитепа, лобаплатин, сатраплатин, профиромицин, цисплатин, ирофулвен, дексифосфамид, цис-аминдихлор(2-метилпиридин)платина, бензилгуанин, глуфосфамид, GPX100, (транс, транс,транс)-бис-му-(гексан-1,6-диамин)-му-[диамин-платина (II)]бис[диамин(хлор)платина(II)]тетрахлорид,диаризидинилспермин,триоксид мышьяка,1-(11-додециламино-10-гидроксиундецил)-3,7 диметилксантин, зорубицин, идарубицин, даунорубицин, бисантрен, митоксантрон, пирарубицин, пинафиде,валрубицин,амрубицин,антинеопластон,3'-деамино-3'-морфолино-13-деоксо-10 гидроксикарминомицин, аннамицин, галарубицин, элинафиде, MEN10755, 4-деметокси-3-деамино-3 азиридинил-4-метилсульфонил-даунорубицин (см. WO 00/50032). Примером гипоксия-активируемого соединения является тирапазамин. Примеры ингибиторов протеосомы включают, но не ограничиваются этим, лактацистин и MLN-341(Velcade). Примеры ингибиторов микротрубочек/стабилизирующих микротрубочки средств включают, в основном, таксаны. Конкретные соединения включают паклитаксел (Taxol) (Таксол), виндесин сульфат,3',4'-дидегидро-4'-деокси-8'-норвинкалейкобластин, доцетаксол (Taxotere) (Таксотере), ризоксин, доластатин, мивобулин изетионат, ауристатин, цемадотин, RPR109881, BMS184476, винфлунин, криптофицин, 2,3,4,5,6-пентафтор-N-(3-фтор-4-метоксифенил)бензолсульфонамид, ангидровинбластин, N,Nдиметил-L-валил-L-валил-N-метил-L-валил-L-пролил-L-пролин-трет-бутиламид, TDX258, эпотилоны(см. например, патенты США 6284781 и 6288237) и BMS188797. В одном варианте воплощения эпотилоны не включены в ингибиторы микротрубочек/стабилизирующих микротрубочки средств. Некоторые примеры ингибиторов топоизомеразы включают топотекан, гикаптамин, иринотекан,рубитекан,6-этоксипропионил-3',4'-О-экзо-бензилиден-хартреузин,9-метокси-N,N-диметил-5 нитропиразоло[3,4,5-kI]акридин-2-(6 Н)пропанамин,1-амино-9-этил-5-фтор-2,3-дигидро-9-гидрокси-4 метил-1 Н,12 Н-бензо[de]пирано[3',4':b,7]индолизино[1,2-b]хинолин-10,13(9 Н,15 Н)дион, луртотекан, 7-[2(N-изопропиламино)этил]-(20S)камптотецин, BNP1350, BNPI1100, BN80915, BN80942, этопозид фосфат,тенипозид, собузоксан, 2'-диметиламино-2'-деокси-этопозид, GL331, N-[2-(диметиламино)этил]-9 гидрокси-5,6-диметил-6H-пиридо[4,3-b]карбазол-1-карбоксамид, асулакрин, (5 а,5 аВ,8 аа,9b)-9-[2-[N-[2(диметиламино)этил]-N-метиламино]этил]-5-[4-гидрокси-3,5-диметоксифенил]-5,5 а,6,8,8 а,9 гексогидрофуро(3',4':6,7)нафто(2,3-d)-1,3-диоксол-6-он,2,3-(метилендиокси)-5-метил-7-гидрокси-8 метоксибензо[с]-фенантридиниум, 6,9-бис-[(2-аминоэтил)амино]бензо[g]изогвинолин-5,10-дион, 5-(3 аминопропиламино)-7,10-дигидрокси-2-(2-гидроксиэтиламинометил)-6 Н-пиразоло[4,5,1-de]акридин-6 он,N-[1-[2(диэтиламино)этиламино]-7-метокси-9-оксо-9 Н-тиоксантен-4-илметил]формамид,N-(2(диметиламино)этил)акридин-4-карбоксамид,6-2-(диметиламино)этил]амино]-3-гидрокси-7 Ниндено[2,1-е]хинолин-7-он и димесна. Примеры ингибиторов митотических кинезинов и, в частности, человеческого митотического кинезина KSP, описаны в публикациях WO 03/039460, WO 03/050064, WO 03/050122, WO 03/049527,WO 03/049679, WO 03/049678, WO 04/039774, WO 03/079973, WO 03/099211, WO 03/105855,WO 03/106417, WO 04/037171, WO 04/058148, WO 04/058700, WO 04/126699, WO 05/018638, WO 05/019206, WO 05/019205, WO 05/018547, WO 05/017190, US 2005/0176776. В одном варианте воплощения ингибиторы митотических кинезинов включают, но не ограничиваются этим, ингибиторы KSP, ингибиторы MKLP1, ингибиторы CENP-E, ингибиторы MCAK и ингибиторы Rab6-KIFL. Примеры "ингибиторов гистон-деацетилазы" включают, но не ограничиваются этим, SAHA, TSA,оксамфлатин, PXD101, MG98 и скриптаид. Кроме того, ссылку на другие ингибиторы гистондеацетилазы можно найти в следующем документе: Miller, T.A. et al. J. Med. Chem. 46 (24):5097-5116"Ингибиторы киназ, вовлеченных в митотическую прогрессию" включают, но не ограничиваются этим, ингибиторы киназы aurora, ингибиторы Polo-подобных киназ (PLK; в частности, ингибиторы PLK1), ингибиторы bub-1 и ингибиторы bub-R1. Примером "ингибитора киназы aurora" является VX-680."Антипролиферативные средства" включает антисмысловые РНК и ДНК олигонуклеотиды, такие как G3139, ODN698, RVASKRAS, GEM 231 и INX3001, и антиметаболиты, такие как эноцитабин, кармофур, тегафур, пентостатин, доксифлуридин, триметрексат, флударабин, капецитабин, галоцитабин,цитарабин окфосфат, фостеабин натрий гидрат, ралтитрексед, палтитрексид, эмитефур, тиазофурин, децитабин, нолатрексед, пеметрексед, нелзарабин, 2'-деокси-2'-метилиденцитидин, 2'-фторметилен-2'деоксицитидин, N-[5-(2,3-дигидробензофурил)сульфонил]-N'-(3,4-дихлорфенил)мочевину, N6-[4-деокси 4-[N2-[2(Е),4(Е)-тетрадекадиеноил]глициламино]-L-глицеро-В-L-манно-гептопиранозил]аденин, аплидин,эктеинасцидин,троксацитабин,4-[2-амино-4-оксо-4,6,7,8-тетрагидро-3H-пиримидино[5,4b][1,4]тиазин-6-ил-(S)-этил]-2,5-тиеноил-L-глутаминовую кислоту, аминоптерин, 5-фторурацил, аланозин,эфир 11-ацетил-8-(карбамоилоксиметил)-4-формил-6-метокси-14-окса-1,11 диазатетрацикло(7.4.1.0.0)-тетрадека-2,4,6-триен-9-илуксусной кислоты, сваинсонин, лометрексол, дексразоксан,метиониназу,2'-циано-2'-деокси-N4-пальмитоил-1-В-D-арабинофуранозилцитозин,3 аминопиридин-2-карбоксальдегид тиосемикарбазон и трастузумаб. Примеры моноклональных антитело-нацеливаемых терапевтических средств включают такие терапевтические средства, которые содержат цитотоксические средства или радиоизотопы, присоединенные к раковому клетка-специфическому или мишеневая клетка-специфическому моноклональному антителу. Примеры включают Bexxar."Ингибиторы HMG-CoA редуктазы" относится к ингибиторам 3-гидрокси-3-метилглутарил-СоА редуктазы. Примеры ингибиторов HMG-CoA редуктазы, которые можно использовать, включают, но не ограничиваются этим, ловастатин (MEVACOR; см. патенты США 4231938, 4294926 и 4319039),симвастатин (ZOCOR; см. патенты США 4444784, 4820850 и 4916239), правастатин (PRAVACHOL; см. патенты США 4346227, 4537859, 4410629, 5030447 и 5180589), флувастатин (LESCOL; см. патенты США 5354772, 4911165, 4929437, 5189164, 5118853, 5290946 и 5356896), аторвастатин(LIPITOR; см. патенты США 5273995, 4681893, 5489691 и 5342952) и церивастатин (также известный как ривастатин и BAYCHOL; см. патент США 5177080). Структурные формулы этих и дополнительных ингибиторов HMG-CoA редуктазы, которые можно использовать в способах по настоящему изобретению, описаны на с. 87 М. Yalpani, "Cholesterol Lowering Drugs", ChemistryIndustry, pp.85-89 (5February 1996) и патентах США 4782084 и 4885314. Термин "ингибитор HMG-CoA редуктазы", как он используется в настоящем изобретении, включает все фармацевтически приемлемые формы лактонов и открытые кислотные формы (т.е. где кольцо лактона раскрывается с образованием свободной кислоты), а также солевые и сложноэфирные формы соединений, которые обладают активностью ингибирования
МПК / Метки
МПК: A01N 43/40, A61K 31/445
Метки: замещенные, активность, пиперидины, повышают, применение, которые
Код ссылки
<a href="https://eas.patents.su/30-23838-zameshhennye-piperidiny-kotorye-povyshayut-aktivnost-p53-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные пиперидины, которые повышают активность p53, и их применение</a>