Замещенные пиразол-3-илбензазолы
Номер патента: 2350
Опубликовано: 25.04.2002
Авторы: Вестфален Карл-Отто, Менке Олаф, Шэфер Петер, Хампрехт Герхард, Вальтер Хельмут, Цагар Кирилл, Мислитц Ульф, Менгес Маркус
Формула / Реферат
1. Замещенные пиразол-3-илбензазолы формулы I
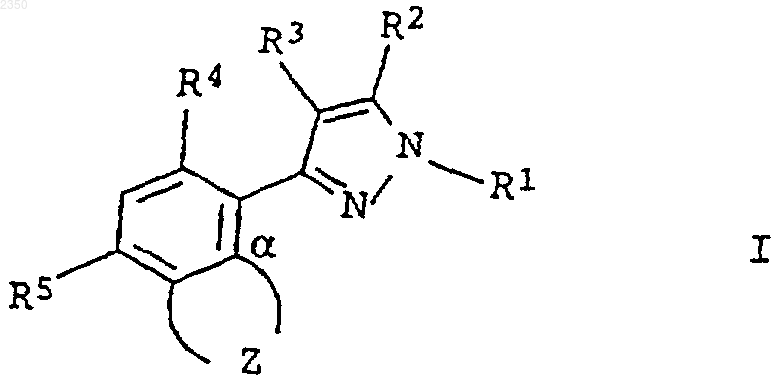
в которой заместители имеют следующие значения:
R1 означает водород, С1-С4алкил или С1-С4галогеналкил;
R2 означает циано, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4галогеналкокси, С1-С4алкилтио, С1-C4галогеналкилтио, С1-С4алкилсульфинил, С1-С4галогеналкилсульфинил, С1-С4алкилсульфонил или С1-С4галогеналкилсульфонил;
R3 означает водород, галоген, циано, нитро, С1-С4алкил или С1-C4галогеналкил;
R4 означает водород или галоген;
R5 означает водород, галоген, циано, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси или С1-С4галогеналкокси;
Z означает группу -N=C(XR6)-O- или -N=C(XR6)-S-, которая может быть связана с a азотом, кислородом или серой;
Х означает химическую связь, кислород, серу, -S(O)-, -SO2-, -NH- или -N(R7)-;
R6, R7 означают независимо друг от друга С1-С6алкил, С1-С6галогеналкил, циано-С1-С4алкил, гидрокси-С1-С4алкил, С3-С6алкенил, циано-С3-С6алкенил, С3-С6галогеналкенил, С3-С6алкинил, циано-С3-С6алкинил, С3-С6галогеналкинил, С1-С4алкокси-С1-С4алкил, С1-С4галогеналкокси-С1-С4алкил, С3-С4алкенилокси-С1-С4алкил, С3-С4алкинилокси-С1-С4алкил, С3-С6циклоалкилокси-С1-С4алкил, амино-С1-С4алкил, С1-С4алкиламино-С1-С4алкил, ди(С1-С4алкил)амино-С1-С4алкил, С1-С4алкилтио-С1-С4алкил, С1-С4галогеналкилтио-С1-С4алкил, С3-С4алкенилтио-С1-С4алкил, С3-С4алкинилтио-С1-С4алкил, С1-С4алкилсульфинил-С1-С4алкил, С1-С4галогеналкилсульфинил-С1-С4алкил, С3-С4алкенилсульфинил-С1-С4алкнил, С3-С4алкинилсульфинил-С1-С4алкил, С1-С4алкилсульфонил-С1-С4алкил, С1-С4галогеналкилсульфонил-С1-С4алкил, С3-С4алкенилсульфонил-С1-С4алкил, С3-С4алкинилсульфонил-С1-С4алкил, гидроксикарбонил-С1-С4алкил, (С1-С4алкокси)карбонил-С1-С4алкил, который может нести циано- или (С1-С4алкокси) карбонильную группу, (С1-С4алкилтио)карбонил-С1-С4алкил, аминокарбонил-С1-С4алкил, С1-С4алкиламинокарбонил-С1-С4алкил, ди(С1-С4алкил)аминокарбонил-С1-С4алкил, ди(С1-С4алкил)фосфонил-С1-С4алкил, (С1-С4алкокси)имино-С1-С4алкил, (С3-С4алкенилокси)имино-С1-С4алкил, С3-С8циклоалкил, С3-С8циклоалкил-С1-С4алкил, фенил, фенил-С1-С4алкил, трех-семизвенный гетероциклил или гетероциклил-С1-С4алкил, причем каждое циклоалкильное и каждое гетероциклильное кольцо может иметь одно карбонильное или тиокарбонильное звено,
и причем каждое циклоалкильное, фенильное и гетероциклильное кольцо может быть замещенным и может нести от 1 до 4 заместителей, выбранных каждый из группы, состоящей из циано, нитро, амино, гидрокси, карбокси, галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси, С1-С4галогеналкокси, С1-С4алкилтио, С1-С4галогеналкилтио, С1-С4алкилсульфонила, С1-С4галогеналкилсульфонила, (С1-С4алкокси)карбонила, (С1-С4алкил)карбонила, (С1-С4галогеналкил)карбонила, (С1-С4алкил)карбонилокси, (С1-С4галогеналкил)карбонилокси и ди(С1-С4алкил)амино;
если Х означает химическую связь, кислород, серу, -NH- или -N(R7)-, то радикал R6 может означать также (С1-С4алкил) карбонил, (С1-С4галогеналкил)карбонил, (С1-С4алкокси) карбонил, С1-С4алкилсульфонил или С1-С4галогеналкилсульфонил;
если Х означает химическую связь, то R6 может означать, кроме того, водород, циано, меркапто, амино, галоген, -СН2-СН (галоген)-R8, -CH=CH-R8 или -СН=С(галоген)-R8, причем
R8 означает гидроксикарбонил, (С1-С4алкокси)карбонил, (С1-С4алкилтио)карбонил, аминокарбонил, С1-С4алкиламинокарбонил, ди(С1-С4алкил)аминокарбонил или ди(С1-С4алкил)фосфонил;
или R6 и R7 вместе означают 1,3-пропиленовую, тетраметиленовую, пентаметиленовую или этиленоксиэтиленовую цепь, которая может быть незамещенной или может нести от 1 до 4 С1-С4алкильных групп и одну или две (С1-С4алкокси) карбонильные группы,
а также применимые в сельском хозяйстве соли этих соединений I.
2. Применение замещенных пиразол-3-илбензазолов и их применимых в сельском хозяйстве солей по п.1 в качестве гербицидов или для десикации/дефолиации растений.
3. Гербицидное средство, содержащее гербицидно эффективное количество, по крайней мере, одного замещенного пиразол-3-илбензазола формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1 и, по крайней мере, один инертный жидкий и/или твердый наполнитель, а также по желанию, по крайней мере, одно поверхностно-активное вещество.
4. Средство для десикации и/или дефолиации растений, содержащее десикантно и/или дефолиантно эффективное количество, по крайней мере, одного замещенного пиразол-3-илбензазола формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1 и, по крайней мере, один инертный жидкий и/или твердый наполнитель, а также по желанию, по крайней мере, одно поверхностно-активное вещество.
5. Способ получения гербицидно активного средства, отличающийся тем, что смешивают гербицидно эффективное количество, по крайней мере, одного замещенного пиразол-3-илбензазола формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1 и, по крайней мере, один инертный жидкий и/или твердый наполнитель, а также по желанию, по крайней мере, одно поверхностно-активное вещество.
6. Способ получения десикантно и/или дефолиантно активных средств, отличающийся тем, что смешивают десикантно- и/или дефолиантно эффективное количество, по крайней мере, одного замещенного пиразол-3-илбензазюыр формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1 и, по крайней мере, один инертный жидкий и/или твердый наполнитель, а также по желанию, по крайней мере, одно поверхностно-активное вещество.
7. Способ борьбы с нежелательным ростом растений, отличающийся тем, что гербицидно эффективным количеством, по крайней мере, одного замещенного пиразол-3-илбензазола формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1, воздействуют на растения, их жизненное пространство или на семена.
8. Способ десикации и/или дефолиации растений, отличающийся тем, что десикантно и/или дефолиантно эффективным количеством, по крайней мере, одного замещенного пиразол-3-илбензазола формулы I или одной применимой в сельском хозяйстве соли соединения согласно п.1, воздействуют на растения.
9. Способ по п.8, отличающийся тем, что обрабатывают хлопок.
10. Способ получения замещенных пиразол-3-илбензазолов формулы I по п.1, у которых Z означает группу -N=C(NH2)-S-, отличающийся тем, что аминофенилпиразол формулы IIIa или IIIb
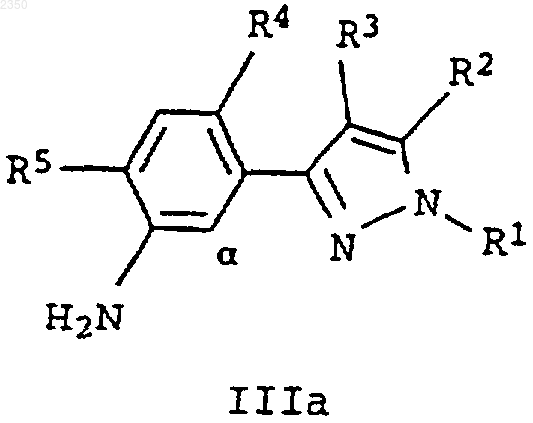
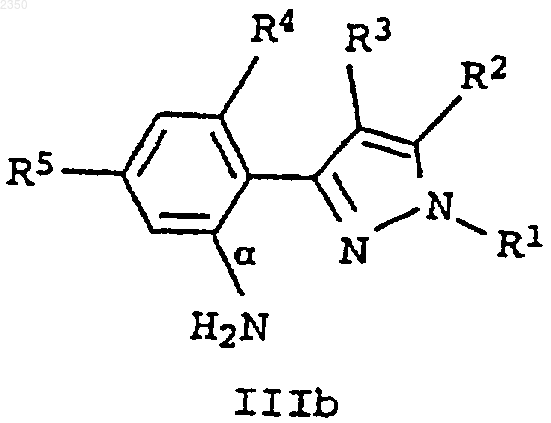
подвергают взаимодействию или с галогеном и тиоцианатом аммония или тиоцианатом щелочного или щелочно-земельного металла, или сначала с тиоцианатом аммония или тиоцианатом щелочного или щелочно-земельного металла и затем с галогеном.
11. Способ получения замещенных пиразол-3-илбензазолов формулы I, в которой XR6 означает галоген или циано, отличающийся тем, что замещенный пиразол-3-илбензазол формулы I, в которой XR6 означает амино, диазотируют и полученную соль диазония подвергают взаимодействию с галогенидом меди(I) или цианидом меди(I).
12. Способ получения замещенных пиразол-3-илбензазолов формулы I, в которой Х означает серу, отличающийся тем, что замещенный пиразол-3-илбензазол формулы I, в которой XR6 означает амино, диазотируют и полученную соль диазония подвергают взаимодействию с диалкилсульфидом формулы R6S-SR6.
13. Способ получения замещенных пиразол-3-илбензазолов формулы I, в которой XR6 означает -СН2-СН(Сl)-R8, -CH2-CH(Br)-R8, -CH=CH-R8, -CH=C(Cl)-R8 или -CH=C(Br)-R8, отличающийся тем, что замещенный пиразол-3-илбензазол, у которого XR6 означает амино, диазотируют и полученную соль диазония подвергают взаимодействию с алкеном формулы H2C=CH-R8 или алкином формулы HC=C-R8 и хлоридом меди(I), бромидом меди(I), хлоридом меди (II) или бромидом меди (II).
14. Способ получения замещенных пиразол-3-илбензазолов формулы I, в которой Х означает кислород, серу, -NH- или -N(R7)-, или в которой -XR6 означает CH(Rb)Rc, причем Rb и Rc независимо друг от друга означают циано или (С1-С4алкокси)карбонил, отличающийся тем, что замещенный пиразол-3-илбензазол, у которого XR6 означает хлор, бром, -SO2-алкил или -SO2-галогеналкил, подвергают взаимодействию с нуклеофилом HOR6, HSR6, H2NR6, HN(R6)R7 или H2C(Rb)Rc в присутствии основания.
15. Способ получения замещенных пиразол-3-илбензазолов формулы I, в которой XR6 означает С1-С6алкил, отличающийся тем, что замещенный пиразол-3-илбензазол, у которого XR6 означает галоген, подвергают взаимодействию с (С1-С6алкил)-соединением Гриньяра по желанию в присутствии катализатора.
16. Способ получения замещенных пиразол-3-илбензазолов формулы I согласно п.1, у которых Z означает -N=C(R6)-O-, отличающийся тем, что аминофенилпиразол формулы IIIa или IIIb
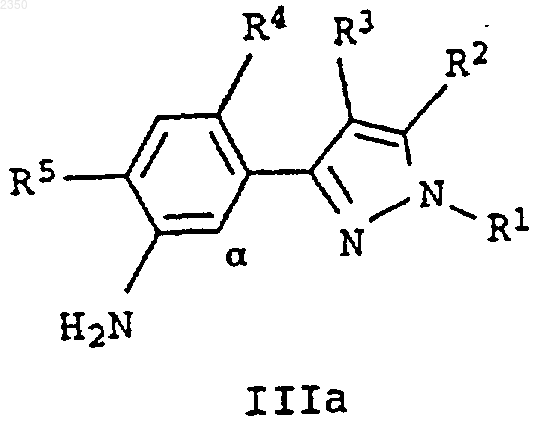
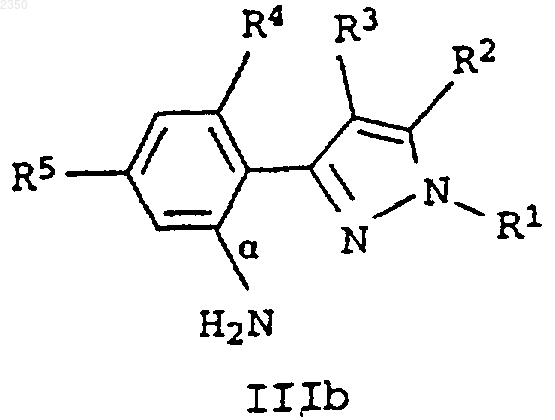
диазотируют, образовавшуюся соль диазония подвергают взаимодействию с азидом щелочного металла с получением азидофенилпиразола формулы Va или Vb
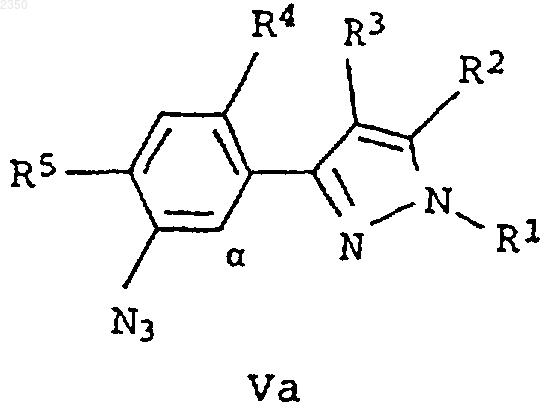
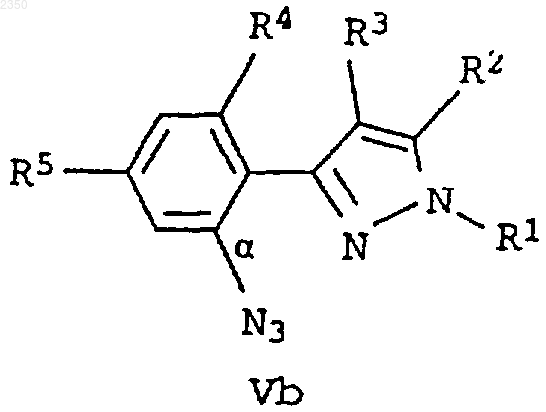
и его подвергают реакции с карбоновой кислотой формулы R6-СООН.
Текст
1 Настоящее изобретение относится к замещенным пиразол-3-илбензазолам формулы I в которой заместители имеют следующие значения:-N=C(XR6)-S-, которая может быть связана сазотом, кислородом или серой; Х означает химическую связь, кислород,серу, -S(O)-, -SO2-, -NH- или -N(R7)-;R6, R7 означают независимо друг от другаC1-С 6-алкил, C1-С 6-галогеналкил, циано-С 1-С 4 алкил, гидрокси-С 1-С 4-алкил, С 3-С 6-алкенил,циано-С 3-С 6-алкенил, С 3-С 6-галогеналкенил, С 3 С 6-алкинил, циано-С 3-С 6-алкинил, С 3-С 6-галогеналкинил, С 1-С 4-алкокси-С 1-С 4-алкил, С 1-С 4 галогеналкокси-С 1-С 4-алкил, С 3-С 4-алкенилокси-С 1-С 4-алкил, С 3-С 4-алкинилокси-С 1-С 4-алкил,С 3-С 8-циклоалкилокси-С 1-С 4-алкил, амино-С 1 С 4-алкил, C1-C4-алкиламино-С 1-С 4-алкил, ди(С 1 С 4-алкил)амино-С 1-С 4-алкил,С 1-С 4-алкилтиоС 1-С 4-алкил, С 1-С 4-галогеналкилтио-С 1-С 4-алкил, С 3-С 4-алкенилтио-С 1-С 4-алкил, С 3-С 4-алкинилтио-С 1-С 4-алкил, С 1-С 4-алкилсульфинил-С 1 С 4-алкил, C1-C4-галогеналкисульфинил-С 1-С 4 алкил,С 3-С 4-алкенилсульфинил-С 1-С 4-алкил,С 3-С 4-алкилсульфинил-С 1-С 4-алкил,С 1-С 4-алкилсульфонил-С 1-С 4-алкил, C1-C4-галогеналкилсульфонил-С 1-С 4-алкил, С 3-С 4-алкенилсульфонил-С 1-С 4-алкил, С 3-С 4-алкилсульфонил-С 1-С 4 алкил, гидроксикарбонил-С 1-С 4-алкил, (C1-C4 алкокси)карбонил-С 1-С 4-алкил, который может нести циано- или (C1-C4-алкокси)карбонильную группу, (С 1-С 4-алкилтио)карбонил-С 1-С 4-алкил,аминокарбонил-С 1-С 4-алкил, С 1-С 4-алкиламинокарбонил-С 1-С 4-алкил, ди(С 1-С 4-алкил)аминокарбонил-С 1-С 4-алкил, ди(С 1-С 4-алкил)фосфонил-С 1-С 4-алкил, (С 1-С 4-алкокси)имино-С 1-С 4 алкил,(С 3-С 4-алкениокси)имино-С 1-С 4-алкил,С 3-С 8-циклоалкил,С 3-С 8-циклоалкил-С 1-С 4 алкил, фенил, фенил-С 1-С 4-алкил, от трех- до семизвенный гетероциклил или гетероциклилС 1-С 4-алкил, причем каждое циклоалкильное и каждое гетероциклильное кольцо может иметь 2 одно карбонильное или тиокарбонильное звено,и причем каждое циклоалкильное, фенильное и гетероциклильное кольцо может быть замещенным и может нести от одного до четырех заместителей, выбранных каждый из группы, состоящей из циано, нитро, амино, гидрокси, карбокси, галогена, С 1-С 4-алкила, С 1-С 4-галогеналкила,С 1-С 4-алкокси, С 1-С 4-галогеналкокси, С 1-С 4 алкилтио,С 1-С 4-галогеналкилтио,С 1-С 4 алкилсульфонила, С 1-С 4-галогеналкилсульфонила, (С 1-С 4-алкокси)карбонила, (С 1-С 4-алкил) карбонила, (C1-C4-галогеналкил)карбонила, (С 1 С 4-алкил)карбонилокси,(С 1-С 4-галогеналкил) карбонилокси и ди(С 1-С 4-алкил)амино; если Х означает химическую связь, кислород, серу , -NH- или -N(R7)- , то радикал R6 может означать также (С 1-С 4-алкил)карбонил, (С 1 С 4-галогеналкил)карбонил, (С 1-С 4-алкокси)карбонил, С 1-С 4-алкилсульфонил или C1-C4-галогеналкилсульфонил; если Х означает химическую связь, то R6 может означать кроме того водород, циано,меркапто, амино, галоген, -СН 2-СН(галоген)-R8,-CH=CH-R8 или -СН=С(галоген)-R8, причемR7 вместе означают 1,3 пропиленовую, тетраметиленовую, пентаметиленовую или этиленоксиэтиленовую цепь, которая может быть незамещенной или может нести от одного до четырех С 1-С 4-алкильных групп и одну или две (С 1-С 4-алкокси)карбонильную группу, а также к применимым в сельском хозяйстве солям этих соединений I. Кроме того, изобретение относится к- применению соединений I в качестве гербицидов и/или для десикации/дефолиации растений,- гербицидным средствам и средствам для десикации и/или дефолиации растений, содержащих соединения I в качестве активных веществ,- способу получения соединений I и гербицидных средств и средств для десикации/дефолиации растений с применением соединений I, а также к- способу борьбы с нежелательным ростом растений и десикации/дефолиации растений соединениями I. Определенные арилпиразолы, при которых в качестве арильного радикала кроме фенила пригодны также различные бензгетероциклильные радикалы, уже были описаны как гербициды в международных патентных заявках WO 92/02509, WO 92/06962, WO 86/01255, WO 96/15115, WO 96/15116 и WO 96/40643. Кроме того, под общую формулу из заявкиWO 96/01254 при подходящем выборе заместителей подпадают также соединения формулы II. которым также приписывается гербицидное действие. Задачей изобретения является создать новые гербицидно действующие пиразолсоединения, с помощью которых можно лучше бороться с нежелательными растениями, чем с известными. Задача распространяется также и на создание новых соединений с десикантным и дефолиантным действием. В соответствии с этим были найдены замещенные пиразол-3-илбезазолы формулы I. Далее были найдены гербицидные средства, которые содержат соединения формулы I и обладают очень хорошим гербицидным действием. Кроме того, были найдены способ получения этих средств и способ борьбы с нежелательным ростом растений с помощью этих соединений. Далее было найдено, что соединения I пригодны для десикации/дефолиации частей растений, при этом они применимы на таких культурных растениях, как хлопок, картофель,рапс, подсолнечник, соя или мелкоплодные бобы, особенно хлопок. В этой связи были найдены средства для десикации и/или дефолиации растений, способ получения этих средств и способ десикации и/или фолиации растений с помощью соединений I. Соединения формулы I в зависимости от вида замещения могут содержать один или несколько центров хиральности и тогда они имеются в форме смесей энантиомеров или диастереомеров. Предметом изобретения являются как чистые энантиомеры или диастереомеры, так и их смеси. Названные при определении заместителейR1 до R3 и R5 до R8 или радикалов циклоалькиных, фенильных или гетероциклических колец органические части молекулы представляют собой, также как и значение галоген, сборные понятия для индивидуального перечисления отдельных частей групп. Все углеродные цепи, а именно алкильные, галогеналкильные,цианоалкильные, оксиалкильные, аминоалкильные, оксикарбонилалкильные, аминокарбонилалкильные, фосфонилалкильные, оксиаминоалкильные, фенилалкильные, гетероциклилалкильные, алкенильные, галогеналкенильные,цианоалкенильные, алкинильные, галогеналкинильные и цианоалкинильные части могут быть разветвленными или неразветвленными. Галогенированные заместители несут предпочительно от одного до пяти одинаковых или различных атомов галогена. Галоген означает при этом фтор, хлор, бром или йод. Далее приводятся примеры значений заместителей:- С 1-С 4-галогеналкил обозначает С 1-С 4 алкил как приведено выше, который замещен частично или полностью фтором, хлором и/или йодом, а именно, например, CH2F, CHF2, СF3,CH2Cl, CH(Cl)2, С(Сl)3, хлорфторметил, дихлорфтор-метил, хлордифторметил, 2-фторэтил,2-хлорэтил, 2-бромэтил, 2-йодэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2-хлор-2-фторэтил, 2 хлор-2,2-дифторэтил,2,2-дихлор-2-фторэтил,2,2,2-трихлорэтил, C2F5, 2-фторпропил, 3-фторпропил, 2,2-дифторпропил, 2,3-дифторпропил,2-хлорпропил, 3-хлорпропил, 2,3-дихлорпропил,2-бромпропил, 3-бромпропил, 3,3,3-трифторпропил, 3,3,3-трихлорпропил, CH2-C2F5, CF2C2F5, 1-(фторметил)-2-фторэтил, 1-(хлорметил)2-хлорэтил, 1-(бромэтил)-2-бромметил, 4-фторбутил, 4-хлорбутил, 4-бромбутил или нонафторбутил;- C1-С 6-галогеналкил обозначает C1-C6 алкил, как приведено выше, который частично или полностью замещен фтором, хлором, бромом и/или йодом, а именно один из названных для С 1-С 4-галогеналкила радикалов или 5-фтор 1-пентил, 5-хлор-1-пентил, 5-бром-1-пентил, 5 йод-1-пентил, 5,5,5-трихлор-1-пентил, ундекафтор-пентил, 6-фтор-1-гексил, 6-хлор-1-гексил,6-бром-1-гексил, 6-йод-1-гексил, 6,6,6-трихлор 1-гексил или додекафторгексил;- фенил-С 1-С 4-алкил обозначает бензил, 1 фенилэтил, 2-фенилэтил, 1-фенилпроп-1-ил, 2 фенилпроп-1-ил,3-фенилпроп-1-ил,1 фенилбут-1-ил, 2-фенилбут-1-ил, 3-фенилбут-1 ил, 4-фенилбут-1-ил, 1-фенилбут-2-ил, 2 фенилбут-2-ил, 3-фенибут-2-ил, 4-фенилбут-2 ил, 1-(бензил)-эт-1-ил, 1-(бензил)-1-(метил)-эт 1-ил или 1-(бензил)-проп-1-ил, предпочтительно бензил или 2-фенилэтил;- С 1-С 4-галогеналкокси обозначает заместитель С 1-С 4-алкокси, как приведено выше, который частично или полностью замещен фтором, хлором, бромом и/или йодом, а именно,например, OCH2F, OCHF2, ОСF3, OCH2Cl,OCH(Cl)2, ОС(Сl)3, хлорфторметокси, дихлорфторметокси, хлордифторметокси, 2-фторэтокси, 2-хлорэтокси, 2-бромэтокси, 2-йодэтокси, 002350- С 1-С 4-галогеналкилтио обозначает заместитель С 1-С 4-алкилтио, как приведено выше,частично или полностью замещенный фтором,хлором, бромом и/или йодом, например,:- С 1-С 4-галогеналкокси-С 1-С 4-алкил обозначает замещенный посредством C1-C4 галогеналкокси - как приведено выше - С 1-С 4 алкил, а именно 2-(ОСНF2)этил, 2-(ОСF3)этил или 2-(ОС 2F5)этил;- С 1-С 4-алкилтио-С 1-С 4-алкил обозначает замещенный посредством С 1-С 4-алкилтио - как приведено выше - С 1-C4-алкил, а именно СН 2SСН 3, CH2-SC2H5, н-пропилтиометил, СН 2SСН(СН 3)2, н-бутилтиометил, (1-метилпропилтио)метил, (2-метилпропилтио)метил, СН 2SС(СН 3)3, 2-(метилтио)этил, 2-(этилтио)этил, 2(н-пропилтио)этил, 2-(1-метилэтилтио)этил, 2(н-бутилтио)этил, 2-(1-метилпропилтио)этил, 2(2-метилпропилтио)этил,2-(1,1-диметилэтилтио)этил, 2-(метилтио)пропил, 2-(этилтио)пропил, 2-(н-пропилтио)пропил, 2-(1-метилэтилтио) пропил, 2-(н-бутилтио)пропил, 2-(1-метилпропилтио)пропил, 2-(2-метилпропилтио)пропил, 2(1,1-диметилэтилтио)пропил, 3-(метилтио)пропил, 3-(этилтио)пропил, 3-(н-пропилтио)пропил, 3-(1-метилэтилтио)пропил, 3-(н-бутилтио) пропил, 3-(1-метилпропилтио)пропил, 3-(2 метилпропилтио)пропил,3-(1,1-диметилэтилтио)пропил, 2-(метилтио)бутил, 2-(этилтио)бутил, 2-(н-пропилтио)бутил, 2-(1-метилэтилтио) бутил, 2-(н-бутилтио)бутил, 2-(1-метилпропилтио)бутил, 2-(2-метилпропилтио)бутил, 2-(1,1 диметилэтилтио)бутил, 3-(метилтио)бутил, 3(этилтио)бутил, 3-(н-пропилтио)бутил, 3-(1 метилэтилтио)бутил, 3-(н-бутилтио)бутил, 3-(1 метипропилтио)бутил,3-(2-метилпропилтио) бутил, 3-(1,1-диметилэтилтио)бутил, 4-(метилтио)бутил, 4-(этилтио)бутил, 4-(н-пропилтио) бутил, 4-(1-метилэтилтио)бутил, 4-(н-бутилтио)бутил, 4-(1-метилпропилтио)бутил, 4-(2-метилпропилтио)бутил или 4-(1,1-диметилэтилтио) бутил, предпочтительно СН 2-SСН 3, CH2-SC2H5,2-(SСН 3)этил или 2-(SС 2 Н 5)этил;- С 1-С 4-галогеналкилтио-С 1-С 4-алкил обозначает замещенный посредством C1-C4 галогенгалкилтио, как приведено выше, С 1-С 4 алкил, а именно 2-(SСНF2)этил, 2-(SСF3)этил или 2-(SС 2F5)этил;(С 1-С 4-алкил)карбонильный радикал, как приведено выше, частично или полностью замещенный фтором, хлором, бромом и/или йодом, а именно, например, CO-CH2F, CO-CHF2, СО-СF3,СО-CH2Cl, СО-СН(Сl)2, СО-С(Сl)3, хлорфторметилкарбонил, дихлорфторметилкарбонил, хлордифторметилкарбонил,2-фторэтилкарбонил, 2-хлорэтилкарбонил, 2-бромэтилкарбонил, 2-йодэтилкарбонил, 2,2-дифторэтилкрабонил, 2,2,2-трифторэтилкарбонил, 2-хлор-2 фторэтилкарбонил, 2-хлор-2,2-дифторэтилкарбонил, 2,2-дихлор-2-фторэтилкарбонил, 2,2,2 трихлорэтилкарбонил, CO-C2F5, 2-фторпропилкарбонил,3-фторпропилкарбонил,2,2 дифторпропилкарбонил, 2,3-дифторпропилкарбонил, 2-хлорпропилкарбонил, 3-хлорпропилкарбонил, 2,3-дихлорпропилкарбонил, 2-бромпропилкарбонил, 3-бромпропилкарбонил, 3,3,3 трифторпропилкарбонил, 3,3,3-трихлорпропилкарбонил, CO-CH2-C2F5, CO-CF2-C2F5, 1-(СН 2F)2-фторэтилкарбонил, 1-(СН 2 Сl)-2-хлорэтилкарбонил, 1-(СН 2 Вr)-2-бромэтилкарбонил, 4-фторбутилкарбонил, 4-хлорбутилкарбонил, 4-бромбутилкарбонил или нонафторбутилкарбонил,предпочтительно СО-СF3 CO-CH2Cl или 2,2,2 трифторэтилкарбонил;- (С 1-С 4-галогеналкил)карбонилокси означает (С 1-С 4-алкил)карбонильный радикал, как приведено выше, частично или полностью замещенный фтором, хлором, бромом и/или йодом, а именно, например, O-CO-CH2F, O-COCHF2, О-СО-СF3, O-СО-СН 2 Сl, O-СО-СН(Сl)2,O-СО-С(Сl)3, хлорфторметилкарбонилокси, дихлорфторметилкарбонилокси,хлордифторметилкарбонилокси, 2-фторэтилкарбонилокси, 2 хлорэтилкарбонилокси,2-бромэтилкарбонилокси, 2-йодэтилкарбонилокси, 2,2-дифторэтилкарбонилокси, 2,2,2-трифторэтилкарбонилокси,2-хлор-2-фторэтилкарбонилокси, 2-хлор-2,2-дифторэтилкарбонилокси, 2,2-дихлор-2-фторэтилкарбонилокси, 2,2,2-трихлорэтилкарбонилокси,O-CO-C2F5, 2-фторпропилкарбонилокси, 3-фторпропилкарбонилокси 2,2-дифторпропилкарбонилокси, 2,3-дифторпропилкарбонилокси, 2 хлорпропилкарбонилокси, 3-хлорпропилкарбонилокси, 2,3-дихлорпропилкарбонилокси, 2 бромпропилкарбонилокси, 3-бромпропилкарбонилокси,3,3,3-трифторпропилкарбонилокси, 9 3,3,3-трихлорпропилкарбонилокси, О-СО-СН 2C2F5, O-CO-CF2-C2F5, 1-(СН 2F)-2-фторэтилкарбонилокси, 1-(СН 2 Сl)-2-хлорэтилкарбонилокси, 1-(СН 2 Вr)-2-бромэтилкарбонилокси, 4 фторбутилкарбонилокси, 4-хлорбутилкарбонилокси, 4-бромбутилкарбонилокси или нонафторбутилкарбонилокси, предпочтительно О-СОСF3, O-CO-CH2Cl или 2,2,2-трифторэтилкарбонилокси;- С 1-С 4-галогеналкилсульфинил обозначает С 1-С 4-алкилфинильный радикал, как приведено выше, частично или полностью замещенный фтором, хлором, бромом и/или йодом, например, SO-CH2F, SO-CHF2, SO-CF3, SO-CH2Cl, SOCH(Cl)2, SO-С(Сl)3, хлорфторметилсульфинил,дихлорфторметилсульфинил,хлордифторметилсульфинил,2-фторэтилсульфинил,2 хлорэтилсульфинил, 2-бромэтилсульфинил, 2 11 йодэтилсульфинил, 2,2-дифторэтилсульфинил,2,2,2-трифторэтилсульфинил,2-хлор-2-фторэтилсульфинил,2-хлор-2,2-дифторэтилсульфинил, 2,2-дихлор-2-фторэтилсульфинил, 2,2,2 трихлорэтилсульфинил,SO-C2F5,2-фторпропилсульфинил,3-фторпропилсульфинил,2,2-дифторпропилсульфинил,2,3-дифторпропилсульфинил, 2-хлорпропилсульфинил, 3 хлорпропилсульфинил, 2,3-дихлорпропилсульфинил, 2-бромпропилсульфинил, 3-бромпропилсульфинил,3,3,3-трифторпропилсульфинил,3,3,3-трихлорпропилсульфинил, SO-CH2-C2F5,SO-CF2-C2F5, 1-(СН 2F)-2-фторэтилсульфинил, 11-(СН 2 Вr)-2(СН 2 Сl)-2-хлорэтилсульфинил,бромэтилсульфинил, 4-фторбутилсульфинил, 4 хлорбутилсульфинил, 4-бромбутилсульфинил или нонафторбутилсульфинил, предпочтительно SO-CF3, SO-CH2Cl или 2,2,2-трифторэтилсульфинил;CH2SOCH3, CH2SOC2H5, н-пропилсульфинилметил, СН 2SOСН(СН 3)2, н-бутилсульфинилметил, (1-метил-пропилсульфинил)метил, (2 метилпропилсульфинил)метил,(1,1-диметилэтилсульфинил)метил, 2-метилсульфинилэтил,2-этилсульфинилэтил, 2-(н-пропилсульфинил) этил,2-(1-метилэтилсульфинил)этил,2-(нбутилсульфинил)этил, 2-(1-метилпропилсульфинил)этил, 2-(2-метилпропилсульфинил)этил,2-(1,1-диметилэтилсульфинил)этил, 2-(SОСН 3) пропил, 3-(SОСН 3)пропил, 2-(SOС 2 Н 5)-пропил,3-(SOС 2 Н 5)пропил,3-(пропилсульфинил)пропил, 3-(бутилсульфинил)пропил, 4-(SОСН 3)бутил, 4-(SOС 2 Н 5)бутил, 4-(н-пропилсульфинил) бутил или 4-(н-бутилсульфинил)бутил, в частности 2-(SOСН 3)этил; С 1-С 4-галогеналкилсульфинил-С 1-С 4 алкил обозначает замещенный C1-C4-галогеналкилсульфинилом, как приведено выше, С 1-С 4 алкил, а именно, например, 2-(2,2,2-трифторэтилсульфинил)этил;- С 1-С 4-галогеналкилсульфонил обозначает С 1-С 4-алкилсульфонильный радикал, как приведено выше, замещенный частично или полностью хлором, фтором, бромом иили йодом, а именно, например, SO2-CH2F, SO2-CHF2, SO2CF3, SO2-СН 2 Сl, SO2-CH(Cl)2, SO2-С(Сl)3, хлорфторметилсульфонил,дихлорфторметилсульфонил, хлордифторметилсульфонил, 2-фторэтилсульфонил,2-хлорэтилсульфонил,2 бромметилсульфонил, 2-йодэтилсульфонил, 2,2 дифторэтилсульфонил, 2,2,2-трифторэтилсульфонил, 2-хлор-2-фторэтилсульфонил, 2-хлор 2,2-дифторэтилсульфонил, 2,2-дихлор-2-фторэтилсульфонил,2,2,2-трихлорэтилсульфонил, 002350- ди(С 1-С 4-алкил)амино-С 1-С 4-алкил обозначает замещенный посредством ди(С 1-С 4 алкил)амино, как приведено выше, С 1-С 4-алкил,а именно, например, CH2N(CH3)2, CH2N(C2H5)2,N,N-дипропиламинометил,N,N-Di[CH(CH3)2]N[С(СН 3)3]-N-(2-метилпропил)аминокарбонил,предпочтительно СО-N(СН 3)2 или CO-N(C2H5)2; ди(С 1-С 4-алкил)аминокарбонил-С 1-С 4 алкил обозначает замещенный ди(С 1-С 4-алкил) аминокарбонилом, как приведено выше, предпочтительно посредством СО-N(СН 3)2 или СОN(С 2 Н 5), радикал С 1-С 4-алкил, а именно СН 2 СО-N(СН 3)2, СН 2-СО-N(C2H5)2, СН(СН 3)-СОN(СН 3)2 или СН(СН 3)-СО-N(С 2 Н 5)2, предпочтительно СН 2-СО-N(СН 3)2 или СН(СН 3)-СОN(СН 3)2;- С 3-С 6-галогеналкенил обозначает С 3-С 6 алкенил, как приведено выше, замещенный частично или полностью фтором, хлором, бромом и или йодом, а именно, например, 2-хлораллил, 3 хлораллил, 2,3-дихлораллил, 3,3-дихлораллил,2,3,3-трихлораллил, 2,3-дихлорбут-2-енил, 2 бромаллил, 3-бромаллил, 2,3-дибромаллил, 3,3 дибромаллил, 2,3,3-трибромаллил или 2,3 дибромбут-2-енил;- С 3-С 6-галогеналкинил обозначает С 3-С 6 алкинил, как приведено выше, замещенный частично или полностью фтором, хлором,бромом и/или йодом, а именно, например, 1,1 дифторпроп-2-ин-1-ил, 4-фторбут-2-ин-1-ил, 4 хлорбут-2-ин-1-ил, 1,1-дифторбут-2-ин-1-ил, 5 фторпент-3-ин-1-ил или 6-фторгекс-4-ин-1-ил;- С 3-С 4-алкенилокси-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4-алкенилокси, таким как аллилокси, бут-1-ен-3-илокси,бут-1-ен-4-илокси, бут-2-ен-1-илокси, 1-метилпроп-2-енилокси или 2-метилпроп-2-енилокси С 1-С 4-алкил, а именно, например, аллилоксиметил,2-аллилоксиметил или бут-1-ен-4 илоксиметил, в частности, 2-аллилоксиэтил;- С 3-С 4-алкинилокси-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4-алкинилокси таким как пропаргилокси, бут-1-ин-3 илокси, бут-1-ин-4-илокси, бут-2-ин-1-илокси, 002350- (С 3-С 4-алкенилокси)имино-С 1-С 4-алкил обозначает замещенный посредством (С 3-С 4 алкенилокси)имино, таким как аллилоксиимино,бут-1-ен-3-илоксиимино, бут-1-ен-4-илоксиимино, бут-2-ен-1-илоксиимино, 1-метилпроп-2 енилоксиимино или 2-метилпроп-2-енилоксиимино С 1-С 4-алкил, а именно, например аллилокси-N=CH-CH2 или бут-1-ен-4-илокси-N=СН, в частности аллилокси-N=СН-СН 2;- С 3-С 4-алкенилтио-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4-алкенилтио,таким как аллилтио, бут-1-ен-3-илтио, бут-1-ен 4-илтио,бут-2-ен-1-илтио,1-метилпроп-2 енилтио или 2-метилпроп-2-енилтио, C1-C4Alkyl, а именно, например, аллилтиометил, 2 аллилтиоэтил или бут-1-ен-4-илтиометил, в частности 2-(аллилтио)этил;- С 3-С 4-алкинилтио-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4-алкинилтио,таким как пропаргилтио, бут-1-ин-3-илтио, бут 1-ин-4-илтио, бут-2-ин-1-илтио, 1-метилпроп-2 инилтио или 2-метилпроп-2-инилтио, предпочтительно пропаргилтио, С 1-С 4-алкил, а именно,например,пропаргилтиометил или 2 пропаргилтиоэтил,в частности 2(пропаргилтио)этил; С 3-С 4-алкенилсульфинил-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4 алкенилсульфинила, такого как аллилсульфинил,бут-1-ен-3-илсульфинил,бут-1-ен-4 илсульфинил,бут-2-ен-1-илсульфинил,1 метилпроп-2-енилсульфинил или 2-метилпроп 2-енилсульфинил С 1-С 4-алкил, а именно, например аллилсульфинилметил, 2-аллилсульфинилэтил или бут-1-ен-4-илсульфинилметил, в частности 2-(аллилсульфинил)этил; С 3-С 4-алкинилсульфинил-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4 алкинилсульфинила, такого как пропаргилсульфинил, бут-1-ин-3-илсульфинил, бут-1-ин-4 илсульфинил,бут-2-ин-1-илсульфинил,1 метилпроп-2-инилсульфинил или 2-метилпроп 2-инилсульфинил, предпочтительно пропаргилсульфинил, C1-C4-алкил, а именно, например пропаргилсульфинилметил или 2-пропаргилсульфинилэтил, в частности 2-(пропаргилсульфинил)этил; С 3-С 4-алкенилсульфонил-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4 алкенилсульфонила, такого как аллилсульфонил,бут-1-ен-3-илсульфонил,бут-1-ен-4 илсульфонил,бут-2-ен-1-илсульфонил,1 метилпроп-2-енилсульфонил или 2-метилпроп 2-енилсульфонил С 1-С 4-алкил, а именно, например, аллилсульфонилметил, 2-аллилсульфонилэтил или бут-1-ен-4-илсульфонилметил, в частности 2-(аллилсульфонил)этил; 19 С 3-С 4-алкинилсульфонил-С 1-С 4-алкил обозначает замещенный посредством С 3-С 4 алкинилсульфонила, такого как пропаргилсульфонил, бут-1-ин-3-илсульфонил, бут-1-ин-4 илсульфонил,бут-2-ин-1-илсульфонил,1 метилпроп-2-инилсульфонил или 2-метилпроп 2-инилсульфонил, предпочтительно пропаргилсульфонил, C1-C4-алкил, а именно, например пропаргилсульфонилметил или 2-пропаргилсульфонилэтил, в частности 2-(пропаргилсульфонил)этил;- С 3-С 8-циклоалкил, содержащий карбонильное или тиокарбонильное звено, обозначает, например циклобутанон-2-ил, циклобутанон 3-ил, циклопентанон-2-ил, циклопентанон-3-ил,циклогексанон-2-ил, циклогексанон-4-ил, циклогептанон-2-ил, циклооктанон-2-ил, циклобутантион-2-ил, циклобутантион-3-ил, циклогептантион-2-ил, циклогептантион-3-ил, циклогексантион-2-ил, циклогексантион-4-ил, циклогептантион-2-ил или циклооктантион-2-ил, предпочтительно циклопентанон-2-ил или циклогексанон-2-ил;- С 3-С 8-циклоалкил-С 1-С 4-алкил, содержащий карбонильное или тиокарбонильное звено,обозначает, например, циклобутанон-2-илметил,циклобутанон-3-илметил, циклопентанон-2-илметил, циклопентанон-3-илметил, циклогексанон-2-илметил, циклогексанон-4-илметил, циклогептанон-2-илметил, циклооктанон-2-илметил, циклобутантион-2-илметил, циклобутантион-3-илметил,циклопентантион-2-илметил,циклопентантион-3-илметил, циклогексантион 2-илметил, циклогексантион-4-илметил, циклогептантион-2-илметил, циклооктантион-2-илметил, 1-(циклобутанон-2-ил)этил, 1-(циклобутанон-3-ил)этил, 1-(циклопентанон-2-ил)этил, 1(циклопентанон-3-ил)этил, 1-(циклогексанон-2 ил)этил, 1-(циклогексанон-4-ил)этил, 1-(циклогептанон-2-ил)этил, 1-(циклооктанон-2-ил)этил, 002350- С 3-С 8-циклоалкокси-С 1-С 4-алкил обозначает циклопропилоксиметил, 1-циклопропилоксиэтил, 2-циклопропилоксиэтил, 1-циклопропилоксипроп-1-ил, 2-цикопропилокси-проп-1 ил, 3-циклопропилокси-проп-1-ил, 1-циклопропилокси-бут-1-ил, 2-циклопропилокси-бут 1-ил, 3-циклопропилокси-бут-1-ил, 4-циклопропилокси-бут-1-ил, 1-циклопропилокси-бут-2-ил,2-циклопропилокси-бут-2-ил, 3-циклопропилокси-бут-2-ил, 3-циклопропилокси-бут-2-ил, 4 циклопропилокси-бут-2-ил, 1-(циклопропиоксиметил)-эт-1-ил,1-(циклопропилоксиметил)-1(СН 3)-эт-1-ил, 1-(циклопропилметилокси)проп 1-ил, циклобутилоксиметил, 1-циклобутилоксиэтил, 2-циклобутилоксиэтил, 1-циклобутилокси-проп-1-ил, 2-циклобутилокси-проп-1 ил, 3-циклобутилокси-проп-1-ил, 1-циклобутилокси-бут-1-ил, 2-циклобутилокси-бут-1-ил, 3 циклобутилокси-бут-1-ил,4-циклобутилоксибут-1-ил, 1-циклобутилокси-бут-2-ил, 2-циклобутилокси-бут-2-ил, 3-циклобутилокси-бут-2 21 ил, 3-циклобутилокси-бут-2-ил, 4-циклобутилокси-бут-2-ил, 1-(циклобутиоксиметил)эт-1-ил,1-(циклобутилоксиметил)-1-(СН 3)-эт-1-ил,1(циклобутилоксиметил)проп-1-ил, циклопентилоксиметил, 1-циклопентилоксиэтил, 2-циклопентилокси-этил, 1-циклопентилокси-проп-1-ил,2-цикопентилокси-проп-1-ил, 3-циклопентилокси-проп-1-ил, 1-циклопентилокси-бут-1-ил, 2 цикопентилокси-бут-1-ил, 3-циклопентилоксибут-1-ил,4-циклопентилокси-бут-1-ил,1 циклопентилокси-бут-2-ил, 2-циклопентилоксибут-2-ил,3-циклопентил-окси-бут-2-ил,3 циклопентилокси-бут-2-ил, 4-циклопентилоксибут-2-ил, 1-(циклопентилоксиметил)эт-1-ил, 1(циклопентилоксиметил)-1-(СН 3)-эт-1-ил,1(циклопентилоксиметил)проп-1-ил, циклогексилоксиметил, 1-циклогексилоксиэтил, 2-циклогексилокси-этил, 1-циклогексилокси-проп-1-ил,2-циклогексилокси-проп-1-ил,3-циклогексилокси-проп-1-ил, 1-циклогексилокси-бут-1-ил,2-циклогексилокси-бут-1-ил, 3-циклогексилокси-бут-1-ил, 4-циклогексилокси-бут-1-ил, 1-циклогексилокси-бут-2-ил, 2-циколгексилокси-бут 2-ил, 3-циклогексилокси-бут-2-ил, 3-циклогексилокси-бут-2-ил, 4-циклогексилокси-бут-2-ил,1-(циклогексилоксиметил)эт-1-ил, 1-(циклогексилоксиметил)-1-(СН 3)-эт-1-ил, 1-(циклогексилоксиметил)-проп-1-ил, циклогептилоксиметил,1-циклогептилоксиэтил,2-циклогептилоксиэтил, 1-циклогептилокси-проп-1-ил, 2-циклогептилокси-проп-1-ил, 3-циклогептилокси-проп 1-ил, 1-циклогептилокси-бут-1-ил, 2-циклогептилокси-бут-1-ил, 3-циклогептилокси-бут-1 ил,4-циклогептилокси-бут-1-ил,1-циклогептилокси-бут-2-ил, 2-циклогептилокси-бут-2 ил,3-циклогептилокси-бут-2-ил,3-циклогептилокси-бут-2-ил, 4-циклогептилокси-бут-2 ил,1-(циклогептилоксиметил)эт-1-ил,1(циклогептиолксиметил)-1-(СН 3)-эт-1-ил,1(циклогептилоксиметил)проп-1-ил, циклооктилоксиметил,1-циклооктилоксиэтил,2 циклооктилокси-этил, 1-циклооктилокси-проп 1-ил,2-циклооктилокси-проп-1-ил,3 циклооктилокси-проп-1-ил, 1-циклооктилоксибут-1-ил,2-циклооктилокси-бут-1-ил,3 циклооктилокси-бут-1-ил,4-циклооктилоксибут-1-ил,1-циклооктилокси-бут-2-ил,2 циклооктилокси-бут-2-ил,3-циклооктилоксибут-2-ил,3-цикооктилокси-бут-2-ил,4 циклооктилокси-бут-2-ил, 1-(циклооктилоксиметил)-эт-1-ил,1-(циклооктилоксиметил)-1(СН 3)-эт-1-ил или 1-(циклооктилоксиметил) проп-1-ил,в частности С 3-С 6-циклоалкоксиметил или 2-(С 3-С 6-циклоалкокси)этил. Под 3- до 7-звенным гетероциклилом следует понимать как насыщенные, частично или полностью ненасыщенные, так и ароматические гетероциклы с одним до трех гетероатомов, выбранных из группы, состоящей из- одного до трех атомов азота,- одного или двух атомов кислорода и- одного или двух атомов серы. Примерами для насыщенных гетероциклов, которые могут содержать одно карбонильное или тиокарбонильное кольцевое звено: оксиранил, тииранил, азиридин-1-ил, азиридин-2 ил, диазиридин-1-ил, диазиридин-3-ил, оксетан 2-ил, оксетан-3-ил, тиетан-2-ил, тиетан-3-ил,азетидин-1-ил, азетидин-2-ил, азетидин-3-ил,тетрагидрофуран-2-ил, тетрагидрофуран-3-ил,тетрагидротиофен-2-ил, тетрагидротиофен-3-ил,пирролидин-1-ил, пирролидин-2-ил, пирролидин-3-ил, 1,3-диоксалан-2-ил, 1,3-диоксалан-4 ил, 1,3-оксатиолан-2-ил, 1,3-оксатиолан-4-ил,1,3-оксатиолан-5-ил, 1,3-оксазолидин-2-ил, 1,3 оксазолидин-3-ил, 1,3-оксазолидин-4-ил, 1,3 оксазолидин-5-ил, 1,2-оксазолидин-2-ил, 1,2 оксазолидин-3-ил, 1,2-оксазолидин-4-ил, 1,2 оксазолидин-5-ил,1,3-дитиолан-2-ил,1,3 дитиолан-4-ил, пирролидин-1-ил, пирролидин 2-ил, пирролидин-5-ил, тетрагидропиразол-1-ил,тетрагидропиразол-3-yl, тетрагидропиразол-4 ил, тетрагидропуран-2-ил, тетрагидропуран-3 ил, тетрагидропуран-4-ил, тетрагидротиопуран 2-ил, тетрагидротилпуран-3-ил, тетрагидропуран-4-ил, пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил, пиперидин-4-ил, 1,3-диоксан-2 ил, 1,3-диоксан-4-ил, 1,3-диоксан-5-ил, 1,4 диоксан-2-ил, 1,3-оксатиан-2-ил, 1,3-оксатиан-4 ил, 1,3-оксатиан-5-ил, 1,3-оксатиан-6-ил, 1,4 оксатиан-2-ил, 1,4-оксатиан-3-ил, морфолин-2 ил, морфолин-3-ил, морфолин-4-ил, гексагидропиридазин-1-ил,гексагидропиридазин-3-ил,гексагидропиридазин-4-ил, гексагидропиримидин-1-ил, гексагидропиримидин-2-ил, гексагидропиримидин-4-ил, гексагидропиримидин-5-ил,пиперазин-1-ил, пиперазин-2-ил, пиперазин-3 ил, гексагидро-1,3,5-триазин-1-ил, гексагидро 1,3,5-триазин-2-ил, оксепан-2-ил, оксепан-3-ил,оксепан-4-ил, тиепан-2-ил, тиепан-3-ил, тиепан 4-ил, 1,3-диоксепан-2-ил, 1,3-диоксепан-4-ил,1,3-диоксепан-5-ил, 1,3-диоксепан-6-ил, 1,3 дитиепан-2-ил, 1,3-дитиепан-2-ил, 1,3-дитиепан 2-ил, 1,3-дитиепан-2-ил, 1,4-диоксепан-2-ил,1,4-диоксепан-7-ил, гексагидроазепин-1-ил, гексагидроазепин-2-ил,гексагидроазепин-3-ил,гексагидроазепин-4-ил,гексагидро-1,3-диазепин-1-ил, гексагидро-1,3-диазепин-2-ил, гексагидро-1,3-диазепин-4-ил, гексагидро-1,4-диазепин-1-ил и гексагидро-1,4-диазепин-2-ил. Примерами для ненасыщенных гетероциклов, которые могут содержать карбонильное или тиокарбонильное звено, могут быть дигидрофуран-2-ил, 1,2-оксазолин-3-ил, 1,2-оксазолин-5-ил, 1,3-оксазолин-2-ил; Среди гетероатомов предпочтительными являются пяти и шестизвенные, а именно фурил, такой как 2-фурил и 3-фурил, тиенил, такой как 2-тиенил и 3-тиенил, пирролил. Такой как 2 пирролил и 3-пирролил, изоксазолил, как 3 изоксазолил, 4-изокасазолил и 5-изоксазолил,изотиазолил. Такой как 3-изотиазолил, 4 изотиазолил и 5-изотиазолил, пиразолил, такой 23 как 3-пиразолил, 4-пиразолил и 5-пиразолил,oксазолил, такой как 2-оксазолил, 4-оксазолил и 5-оксазолил, тиазолил. Такой как 2-тиазолил, 4 тиазолил и 5-тиазолил, 1-имидазолил, такой как 2-имидазолил и 4-имидазолил, оксадиазолил,такой как 1,2,4-оксадиазол-3-ил,1,2,4 оксадиазол-5-ил и 1,3,4-оксадиазол-2-ил, тиадиазолил. Такой как 1,2,4-тиадиазол-3-ил, 1,2,4 тиадтазол-5-ил и 1,3,4-тиадиазол-2-ил, триазолил, такой как 1,2,4-триазол-1-ил, 1,2,4-триазол 3-ил и 1,2,4-триазол-4-ил, пиридинил, такой как 2-пиридинил, 3-пиридинил и 4-пиридинил, пиридазинил, такой как 3-пиридазилин и 4 пиридазилин, пиримидинил, такой как 2 пиримидинил, 4-пиримидинил и 5-пиримидинил, а также 2-пиразинил, 1,3,5-триазин-2-ил и 1,2,4-триазин-3-ил. В частности пиридил, пиримидил, фуранил и тиенил. Все финильные, карбоциклические и гетероциклические кольца являются предпочтительно незамещенными или несут один заместитель. При учете того, замещенные пиразол-3 илбензазолы применяются в качестве гербицидов или десикантов/дефолиантов, предпочтительными являются те соединения формулы I,при которых заместители имеют следующее значение отдельно или в комбинации:R4 водород, фтор или хлор, в частности фтор или хлор;R5 циано, галоген или трифторметил, в частности галоген, особенно хлор; А связанная через кислород или серу сгруппа -N=C(XR6)-O- или -N=C(XR6)-S-, в частности связанная счерез серу группаR6, R7 означают независимо друг от другаC1-C6-алкил, C1-С 6-галогеналкил, циано-С 1-С 4 алкил, гидрокси-С 1-С 4-алкил, С 3-С 6-алкенил, С 3 С 6-алкинил, С 1-С 4-алкокси-С 1-С 4-алкил, С 1-С 4 алкилтио-С 1-С 4-алкил, С 1-С 4-алкилсульфонилС 1-С 4-алкил,(С 1-С 4-алкокси)карбонил-С 1-С 4 алкил,ди(С 1-С 4-алкил)аминокарбонил-С 1-С 4 алкил, С 3-С 8-циклоалкил С 3-С 8-цикоалкил-С 1 С 4-алкил, фенил или фенил-С 1-С 4-алкил; если Х является химической связью, кислородом, серой, -NH- или -N(R7)- , то R6 может также означать (С 1-С 4-алкил)карбонил или С 1 С 4-алкилсульфонил; если X является химической связью, то R6 может, кроме того, означать водород, циано,амино, галоген или -CH=CH-R8;R8 (С 1-С 4-алкокси)карбонил. Особенно предпочтительными являются замещенные пиразол-3-илбензазолы формулы Iа= хлор, R4 = водород, Z = связанная через серу сгруппа -N=C(XR6)-S-), в частности приведенные в таблице 1 соединения. Таблица 1- соединения Id.001 до Id.384, которые отличаются от соответствующих соединений- соединения Ie.001 до Ie.384, которые отличаются от соответствующих соединений- соединения If.001 до If.384, которые отличаются от соответствующих соединений- соединения Ih.001 до Ih.384, которые отличаются от соответствующих соединений Особенно предпочтительными являются замещенные пиразол-3-илбензазолы формулы Ib до It и IA до IT, в частности следующие:- соединения Ib.001 до Ib.384, которые отличаются от соответствующих соединений- соединения If.001 до If.384, которые отличаются от соответствующих соединений- соединения Ic.001 до Ic.384, которые отличаются от соответствующих соединений- соединения Ij.001 до Ij.384, которые отличаются от соответствующих соединений- соединения Ik.001 до Ik.384, которые отличаются от соответствующих соединений- соединения Im.001 до Im.384, которые отличаются от соответствующих соединений- соединения In.001 до In.384, которые отличаются от соответствующих соединений- соединения Io.001 до Io.384, которые отличаются от соответствующих соединений- соединения Iр.001 до Ip.384, которые отличаются от соответствующих соединений- соединения Iq.001 до Iq.384, которые отличаются от соответствующих соединений- соединения Ir.001 до Ir.384, которые отличаются от соответствующих соединений- соединения Is.001 до Is.384, которые отличаются от соответствующих соединений- соединения It.001 до It.384, которые отличаются от соответствующих соединений- соединения IА.001 до IA.384, которые отличаются от соответствующих соединений- соединения IB.001 до IB.384, которые отличаются от соответствующих соединений- соединения IC.001 до IC.384, которые отличаются от соответствующих соединений- соединения ID.001 до ID.384, которые отличаются от соответствующих соединений- соединения IE.001 до IE.384, которые отличаются от соответствующих соединений- соединения IF.001 до IF.384, которые отличаются от соответствующих соединений- соединения IG.001 до IG.384, которые отличаются от соответствующих соединений-соединения IH.001 до IH.384, которые отличаются от соответствующих соединений- соединения IJ.001 до IJ.384, которые отличаются от соответствующих соединений- соединения IК.001 до IK.384, которые отличаются от соответствующих соединений- соединения IM.001 до IM.384, которые отличаются от соответствующих соединений- соединения IN.001 до IN.384, которые отличаются от соответствующих соединений- соединения IO.001 до IO.384, которые отличаются от соответствующих соединений- соединения IP.001 до IP.384, которые отличаются от соответствующих соединений- соединения IS.001 до IS.384, которые отличаются от соответствующих соединений- соединения IT.001 до IT.384, которые отличаются от соответствующих соединений Замещенные пиразол-3-илбензазолы можно получать различным образом, в частности следует привести следующие способы: А) взаимодействие аминофенилпиразола формулы IIIа или IIIb с галогеном или тиоцианатом аммония или тиоцианатом щелочного или щелочно-земельного металла:- соединения IQ.001 до IQ.384, которые отличаются от соответствующих соединений- соединения IR.001 до IR.384, которые отличаются от соответствующих соединенийIa.001 до Ia.384 только тем, что R2 означает ме М= ион щелочного- или 1/2 щелочноземельного металла Предпочтительным галогеном является хлор или бром, предпочительным тиоцианатом щелочного/щелочно-земельного металла является тиоцианат натрия. Как правило, применяют инертный растворитель/разбавитель, например водород, такой как толуол и гексан, галогенированный водород, такой как дихлорметан, эфир, такой как 41 тетрагидрофуран, спирт, такой как этанол, карбоновую кислоту, такую как уксусная кислота,или апротонный растворитель, такой как диметилформамид, ацетоннитрил и диметилсульфоксид. Температура реакции в обычном случае лежит между точкой плавления и точкой кипения реакционной смеси, предпочтительно от 0 до 150 С. Чтобы получить по возможности высокий выход целевого продукта применяют галоген и тиоцианат аммония, соответственно, тиоцианат щелочного-/щелочно-земельного металла в эквимолярном количестве или в избыточном количестве порядка пятикратного молярного количества, по отношению к количеству соединения формулы IIIа или IIIb. Один из вариантов способа состоит в том,что аминофенилпиразол IIIa или IIIb сначала подвергают взаимодействию с тиоцианатом аммония или тиоцианатом щелочного или щелочно-земельного металла с получением тиомочевины IVa или IVb и соединения формулы IVa или IVb путем обработки галогеном превращают в соединение I со значаением Z = -N=C(XR6)-SВ) диазотирование аминофенилпиразола формулы IIIа или IIIb, преобразование соответствующей соли диазония в азидофенилпиразол формулы Va или Vb и его взаимодействие.B.2) сначала с сульфокислотой (в соединения VIa или VIb), гидролиз образовавшегося сульфоната в аминофенол формулы VIIa или Для проведения диазотирования действительны приведенные для способа С) данные. Преобразование в арилазиды Va/Vb осуществляется предпочтительно путем взаимодействия соединений формул IIIа/IIIb с азидом щелочного или щелочноземельного металла, с таким как азид натрия или путем взаимодействия с триметилсилилазидом. При приведенном в способе В.1) взаимодействии с карбоновой кислотой применяют или инертный растворитель, например, эфир,такой как тетрагидрофуран и диоксан, апротон 43 ный растворитель, как например, диметилформамид и ацетонитрил, углеводород, такой как толуол и гексан, галогенированный углеводород, такой дихлорметан, или работают без растворителя в избытке карбоновой кислоты R6COOH. В последнем случае добавка минеральной кислоты, такой как фосфорная кислота, может быть полезной. Взаимодействие осуществляют предпочтительно при повышенной температуре, например при температуре кипения реакционной смеси. Для приведенного в В.2) вначале взаимодействия соединений формулы Va/Vb с сульфоновой кислотой Ra-SО 3 Н (причем Ra означает С 1-С 4-алкил или C1-C4-галогеналкил, предпочтительно метил или трифторметил) действительны приведенные выше для взаимодействия соединений Va/Vb с R6-COOH данные. Заключительный гидролиз сульфонатов VIa/VIb осуществляется предпочтительно водным основанием, таким как натровым и калиевым щелоком,причем по желанию можно добавлять растворитель, например, эфир, такой как диоксан и тетрагидрофуран, или спирт, такой как метанол и этанол. Заключительное преобразование в соединение формулы I является само по себе известным и может осуществляться различным образом. В этой связи следует указать на данные из публикации Хубера-Вейела, Методы органической химии", издание Georg Thieme Verlag Штуттгарт, том Е 8 а 1993, стр.1032 и д. С) диазотирование замещенных пиразол-3 илбензазолов формулы I, в которой XR6 означает амино, и последующее преобразование соли диазония в соединение I при- -XR6 = циано или галоген относительно реакции Зандмейера см. Хубер-Вейл, MethodenVerlag Stuttgart, том. Е 11 1984, стр. 43 и 176,- -XR6 = например, -СН 2-СН(галоген)-R8,-CH=CH-R8, -СН=С(галоген)-R8 в общем здесь речь идет о продукте арилирования, см. например, публикацию C.S. Rondestredt, Org. React. 11, стр. 189 (1960) и Н.Р. Doyle et al., J. Org.Chem. 42, стр. 2431 (1977): В общем соль диазония получают известным образом путем взаимодействия соединения формулы I, где -XR6 = амино, в водном кислотном растворе, например, в соляной кислоте,бромводородной кислоте или серной кислоте, с нитритом, например, с таким, как нитрит натрия и нитрит калия. Имеется также возможность работать в безводной среде, например, в содержащей хлористый водород ледяной уксусной кислоте, в абсолютном спирте, в диоксане или тетрагид 002350 44 рофуране, в ацетонитриле или в ацетоне и при этом обрабатывать исходное соединение (I,. в котором -XR6 = NH2) эфиром азотистой кислоты, таким как тpeт-бутилнитрит и изопентилнитрит. Превращение полученной таким образом соли диазония в соответствующее соединение I,в котором -XR6 означает циано, хлор, бром или йод, осуществляется путем обработки раствором или суспензией соли меди, такой как цианид меди (I), хлорид меди (I), бромид меди (I),йодид меди (I) или раствором соли щелочного металла. Соединения I, в которых -Х- означает серу,получают обычно путем взаимодействия соли диазония с диалкилдисульфидом, таким как диметилдисульфид и диэтилдисульфид или, например, с диаллилдисульфидом или дибензилдисульфидом. При арилировании Мервейна речь идет обычно о взаимодействии соли диазония с алкенами (здесь H2C+CH-R8) или алкинами (здесьHC5C-R8). Алкен или алкин применяют при этом предпочтительно в избытке приблизительно до 3000 мол.%, по отношению к количеству соли дазония. Вышеописанное превращение соли диазония может осуществляться, например, в воде, в водной соляной или бромводородной кислоте, в кетоне, таком как ацетон, диэтилкетон и метилэтилкетон, в нитриле, таком как ацетонитрил, в эфире, таком как диоксан и тетрагидрофуран или в спирту, таком как метанол и этанол. Если при отдельных реакциях не было других указаний, температура реакции лежит обычно при (-30) до +50 С. Все реагенты применяются предпочтительно в стехиометрическом количестве, однако преимущество может давать также и избыточное количество одного или другого компонента,до приблизительно 3000 мол.%.D) окисление замещенного пиразол-3 илбензазола формулы I, в которой Х означает серу, в соединение I, в котором Х = -SO-, осуществляется известным образом (см., например,Хубер-Вейл, Methoden der Organischen Chemie,Georg Thieme Verlag Stuttgart, Bd. E 11/1, 1985,стр. 702 и д. Bd. IX, 4. Auflage. 1955, стр. 211): Подходящим оксилителем является, например, перекись водорода, органические перекиси, такие как перекись уксусной кислоты,перекись трифторуксусной кислоты, м-хлорпербензойная кислота, трет-бутилгидроперекись и трет-бутилгипохлорит, а также неорганические соединения, такие как метаиодат натрия, хромовая кислота и азотная кислота. В зависимости от окислителя, обычно применяют органическую кислоту, такую как уксусная кислота и трихлоруксусная кислота,хлорированный углеводород, например, метиленхлорид, хлороформ и 1,2-дихлорэтан, арома 45 тический углеводород, например, бензол, хлорбензол и толуол или протонный раствор, например метанол и этанол. Могут применяться также и смеси приведенных растворителей. Температура реакции составляет в общем прибл. от (-30)С до точки кипения соответствующей реакционной смеси, причем обычно предпочитают нижний диапазон температур. Исходное соединение и окислитель применяют целесообразно в стехиометрическом соотношении, однако один или другой компонент можно применять в избыточном количестве. Е) окисление замещенного пиразол-3 илбензазола формулы I, в которой Х означает серу или -SO-, в соединение I, в котором Х =-SO2- производится известным методом (см. например, Хубер-Вейл, Methoden der Organischen Chemie, Georg Thieme Verlag Stuttgart, том Е 11/2, 1985, стр. 1132 и д. и том Bd. IX, 4. Auflage, 1955, стр. 222 и д.): В качестве окислителя пригодны, например, перекись водорода, органические перекиси,такие как перекись уксусной кислоты, перекись трифторуксусной кислоты и м-хлорпербензойная кислота, кроме того, неорганические окислители, такие как перманганат калия. Присутствие катализатора, например, вольфрама, может способствовать прохождению реакции. Как правило реакцию взаимодействия осуществляют в инертном растворителе, при этом в зависимости от окислителя применяют,например, органические кислоты, такие как уксусная кислота и пропионовая кислота, хлорированные углеводороды, такие как метиленхлорид, хлороформ и 1,2-дихлорэтан, ароматические углеводороды или галогенуглеводороды,такие как бензол, хлорбензол и толуол, или воду. Также пригодны смеси приведенных растворителей. Обычно реакцию проводят при температуре от (-30)С до температуры кипения соответствующей реакционной смеси, предпочтительно от 10 С до температуры кипения. Исходное соединение I, где Х означает серу или SO, и окислитель применяют целесообразным образом в стехиометрическом соотношении. Для оптимизации реакции взаимодействия рекомендуется избыточное количество окислителя.F) взаимодействие замещенного пиразол-3 илбензазола I, при котором группа -XR6 означает хлор, бром, алкилсульфонил или галогеналкилсульфонил, в присутствии основания со спиртом, меркаптаном, амином или одним СНкислым соединением (VIII):Rb и Rc означают независимо друг от друга циано или (С 1-С 4-алкокси)карбонил. Реакцию взаимодействия проводят целесообразным образом в инертном растворителе,например, в эфире, таком как диэтиловый эфир,метил-трет-бутиловый эфир, диметоксиэтан,диэтиленгликольдиметиловый эфир, тетрагидрофуран и диоксан, в кетоне, таком как ацетон,диэтилкетон, этилметилкетон и циклогексанон,в диполярном, апротонном растворителе, таком как ацетонитрил, диэтилформамид, N-метилпирролидон и диметилсульфоксид, в протонном растворителе, таком как метанол и этанол, в ароматическом, в случае необходимости, галогенированном углеводороде, таким как бензол,хлорбензол и 1,2-дихлорбензол, в гетероароматическом растворителе, таком как пиридин и хинолин или в смеси таких растворителей. Предпочтительными являются тетрагидрофуран, ацетон, диэтилкетон и диметилформамид. В качестве основания могут применяться,например, гидроксиды, гидриды, алкоксиды,карбонаты или гидрокарбонаты щелочных или щелочно-земельных металлов, третичные алифатические амины, такие как триэтиламин, Nметилморфолин и N-этил-N,N-диизопропиламин, би- и трицикличные амины, такие как диазабициклоундекан (ДБУ) и диазабициклооктан (ДБЦО), или ароматические азотные основания, такие как пиридин, 4-диметиламинопиридин и хинолин. Также могут применяться и комбинации различных оснований. Предпочтительными являются гидрид натрия, гидрохлорид натрия, карбонат натрия, карбонат калия, метилат натрия, этилат натрия и трет.-бутилат калия. Амины H2NR6 или HN(R6)R7 могут служить в качестве реагентов и одновременно в качестве основания, причем тогда амин должен быть, по крайней мере, в двойном избыточном количестве по отношению к количеству исходного соединения I. Конечно возможен и больший избыток амина, до 10-кратного молярного количества, по отношению к количеству соединения I, в котором -XR6 означает Cl, Вr, -SO2 алкил или -SO2-галогеналкил. Обычно исходные вещества применяют в стехиометрическом соотношении, однако преимущество может дать избыточное количество одного или другого компонента для по возможности полной конверсии исходного соединенияI -XR6 = Cl, Вr, -SO2-алкил, -SО 2-галогеналкил. Молярное соотношение спирта, меркапто,амина или СН-кислотного соединения (VIII) к основанию составляет в общем 1:1 до 1:3. Концентрация исходных веществ в растворителе составляет обычно от 0,1 до 5,0 моль/л. Реакция взаимодействия проводится при температуре от 0 С до температуры кипения с обратным холодильником соответствующей реакционной смеси.G) взаимодействие замещенного пиразол 3-илбензазола формулы I, при котором -XR6 47 означает галоген, с (С 1-С 6-алкил) - соединением Гриньяра: Гал" означает при этом хлорид или бромид. Как правило, реакцию взаимодействия проводят в инертном растворителе/разбавителе,например, в углеводороде, таком как гексан и толуол, или в эфире, таком как диэтиловый эфир, тетрагидрофуран и диоксан. По желанию может применяться катализатор на основе переходного металла в количестве от 0,0001 до 10 мол.%. Для этого пригодны, например, никелевый и палладиевый катализатор,такие как дихлорид никеля, бис (трифенилфосфин)хлористый никель, дихлорид [бис-(1,2 дифенилфосфино)этан]никеля, дихлорид[бис(1,3-дифенилфосфино)пропан]никеля, дихлорид палладия, тетракис(трифенилфосфин)палладий,дихлорид бис(трифенилфосфин)палладия, дихлорид[бис-(1,2-дифенилфосфино)этан]палладия, дихлорид[бис-(1,3-дифенилфосфино)пропин]палладий и дихлорид [бис(дифенилфосфино)ферроцен]палладия, однако могут применяться также и смеси дихлоридов палладия или никеля и фосфинов, таких как трифенилфосфин,бис-1,2-(дифенилфосфино)этан и бис-1,3(дифенилфосфино)пропан. В зависимости от протекания реакции при этом возникают соединения I, где -XR6 = водород или C1-С 6-алкил или соотвествующие смеси из алкилированных и неалкилированных соединений, которые однако могут быть разделены обычным образом. Как правило, температура реакции составляет от (-100)С до температуры кипения реакционной смеси. Количество реагентов Гриньяра не является критическим, обычно применяют (С 1-С 6 алкил)-МgГал прибл. в зквимолярном количестве или в избыточном количестве до 10-ти кратного молярного количества, по отношению к количеству соединения I, где -XR6 означает галоген. Если по-другому не указано, все вышеописанные способы проводят при атмосферном давлении или при собственном давлении соответствующей реакционной смеси. Подготовку реакционной смеси производят как правило известным образом. Если при вышеописанных способах не указано подругому, целевой продукт получают, например,после разбавления реакционной смеси водой,фильтрацией, кристаллизацией или экстракцией растворителя или удалением растворителя, распределением остатка в смеси из воды и подходящего органического растворителя и разделение органической фазы с получением продукта. Замещенные пиразол-3-илбензазолы могут при изготовлении иметься в форме смесей изомеров, которые могут быть разделены обычными для этого методами, например, кристаллиза 002350 48 цией или хромотографией, также на оптическом адсорбенте, на чистые изомеры. Чистые, оптически активные изомеры можно получать из соотвествующих оптически активных исходных продуктов. Применимые в сельском хозяйстве соли соединений I могут образовываться путем реакции с основанием соответствующего катиона,предпочтительно гидроксилом или гидридом щелочного металла или же реакции c кислотой соотвествующего аниона, предпочтительно хлористо-водородной кислотой, бромисто-водородной кислотой, серной кислотой, фосфорной кислотой или азотной кислотой. Соли соединений I, ион металла которых не является ионом щелочного металла, можно получать обычно путем пересаливания соотвествующей соли щелочного металла, также как и соли аммония, фосфония, сульфония и сульфоксония посредством аммиака, гидроокиси фосфония, сульфония или сульфоксония. Соединения I и их применимые в сельском хозяйстве соли пригодны как смеси изомеров,так и в форме чистых изомеров, в качестве гербицидов. Содержащие соединения I гербицидные средства очень хорошо пригодны для борьбы с нежелательным ростом растений на поверхностях с некультурными растениями, в частности, при высоких дозах внесения. На таких культурах, как пшеница, рис, кукуруза, соя и хлопок они эффективны против сорняков и сорной травы без нанесения вреда культурным растениям. Этот эффект имеет место прежде всего при малых дозах внесения. При учете многосторонности методов применения соединения I, соответственно содержащие их гербицидные средства, могут использоваться на целом ряде других культурных растений для устранения нежелательных растений. Примерами таких культур являютсяdurum, Vicia faba, Vitis vinifera и Zea mays. Кроме того, соединения I могут применяться на культурах, которые вследствие их разведения, включая методы техники генов,терпимы к действию гербицидов. Замещенные пиразол-3-илбезазолы пригодны далее для десикации и/или дефолиации растений. В качестве десикантов они пригодны для высушивания надземных частей культурных растений, таких как картофель, рапс, подсолнечник или соя. Благодаря этому обеспечивается полностью механизированный сбор урожая этих важных культур. Экономический интерес представляет также облегчение сбора урожая, которое обеспечивается путем нацеленного опадания или снижения прилипаемости к деревьям цитрусовых,оливковых или других видов и сортов косточковых и скорлупных плодовых культур. Тот же механизм, т.е. способствование образованию разделительной ткани между плодами, листвой и отростками растений является существенным также и для контролируемого удаления листьев на полезных растениях, в частности на хлопке. Кроме того, снижение интервалов времени, в которые отдельные хлопковые растения созревают, приводит к повышенному качеству волокна после сбора урожая. Соединения формулы I, соответственно содержащие эти соединения гербицидные средства могут применяться, например, в форме непосредственно разбрызгиваемых водных растворов, порошков, суспензий, также и высокопроцентных водных, масляных или прочих суспензий или дисперсий, эмульсий, масляных дисперсий, паст, опыливающих средств, разбрасываемых средств или гранулята, причем они наносятся разбрызгиванием, путем распыления,опыливания, разбрасывания или полива. Формы применения ориентируются на цель применения, они в любом случае должны обеспечивать по возможности тонкое распределение веществ согласно изобретению. В качестве инертных дополнительных веществ пригодны в основном фракции минеральных масел со средней до высокой точками кипения, такие как керосин или дизельное масло,далее масло из каменноугольной смолы, а также масла растительного или животного происхождения, алифатические, циклические или ароматические углеводороды, например, парафин,тетрагидронафталин, алкилированные нафталины или их производные, алкилированные бензолы или их производные, спирты, такие как метанол, этанол, пропанол, бутанол, циклогексанол, кетоны, такие как циклогексанон или сильно полярные растворители, например, амины,такие как N-метилпирролидон или вода. 50 Водные формы применения могут быть приготовлены из концентратов эмульсий, суспензий, паст, смачиваемых порошков или диспергируемого в воде гранулята путем добавки воды. Для изготовления эмульсий, паст или масляных дисперсий субстраты могут гомогенизироваться в воде как сами, так и растворенные в масле или в растворителе, с помощью смачивающих, прилипательных, диспергирующих или эмульгирующих добавок. Также могут изготавливаться состоящие из акивного вещества, из смачивающего, прилипательного или эмульгирующего средства и, при необходимости, растворителя или масла концентраты, которые пригодны для разбавления в воде. В качестве поверхностно-активных веществ могут применяться соли щелочных, щелочно-земельных металлов, аммониевые соли ароматических сульфокислот, например, лигнин-, фенол-, нафталин- и дибутилнафталинсульфокислоты, а также соли жирных кислот,алкил- и алкиларилсульфонаты, алкилсульфаты,лаурилсульфоэфиры, сульфаты жирных спиртов, а также соли сульфатированных гексанолов, гептанолов и октадеканолов, а также гликолевого эфира спирта жирного ряда, продукты конденсации сульфонированного нафталина и его производных с формальдегидом, продукты конденсации нафталина, соответственно, нафталинсульфокислот с фенолом и формальдегидом,эфир полиоксиэтиленоктилфенола, этоксилированный изооктилфенол, октилфенол или нонилфенол, алкилфенилполигликолевый эфир, трибутилфенилполигликолевый эфир, алкиларилполиэфирные спирты, изотридециловый спирт,конденсаты этиленоксидов жирных спиртов,этоксилированное касторовое масло, простой полиоксиэтиленалкиловый эфир или полигликолэфирный ацетат лауриновых спиртов, эфир сорбита, отработанный лигнин-сульфатный щелок или метилцеллюлоза. Порошковые, разбрасываемые и распыливаемые средства могут изготавливаться путем смешения или промеливания активных веществ вместе с твердыми наполнителями. Гранулят, например, пропитанный, оболочковый и гомогенный гранулят может изготавливаться путем связывания активных веществ с твердыми наполнителями. Твердыми наполнителями являются минеральные земли,например, кремниевые кислоты, силикаты,тальк, каолин, известняк, известь, мел, болус,лесс, глина, доломит, диатомовая земля, сульфат кальция и сульфат магния, окись магния,измельченная пластмасса, удобрения, такие как сульфат аммония, фосфат аммония, нитрат аммония, мочевина и растительные продукты, такие как зерновая мука, мука древесной коры,древесная мука и мука ореховой скорлупы, порошок целлюлозы и другие наполнители. Концентрация соединений формулы I в препаративных формах может варьироваться в 51 широких пределах. Препаративные формы содержат в общем 0,001 до 98 вес.%, предпочтительно 0,01 до 95 вес.%, по крайней мере, одного активного вещества. Активные вещества применяются при этом с чистотой от 90% до 100%, предпочтительно от 95% до 100% (по спектру ЯМР). Препаративные формы согласно изобретению можно изготавливать, например, следующим образом:I. 20 вес. долей соединения Nr. Ic.001 растворяют в смеси, состоящей из 80 вес. долей алкилированного бензола, 10 вес. долей продукта присоединения 8 до 10 молей этиленоксида к 1 молю моноэтаноламида N-олеиновой кислоты,5 вес. долей соли кальция додецилбензолсульфокислоты и 5 вес. долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла. Путем выливания и тонкого распределения раствора в 100 000 вес. долей воды получают водную дисперсию, которая содержит 0,02 вес.% активного вещества.II. 20 вес. долей соединения Nr. Ic.321 растворяют в смеси, состоящей из 40 вес. долей циклогексанона, 30 вес. долей изобутанола, 20 вес. долей продукта присоединения 7 молей этиленоксида к 1 молю изооктифенола и 10 весовых долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла. Путем вливания и тонкого распределения в 100 000 вес. долей воды получают водную суспензию,содержащую 0,02 вес.% активного вещества.III. 20 вес. долей активного вещества Nr.Ic.343 растворяют в смеси, состоящей из 25 вес. долей циклогексанона, 65 вес. долей фракции минерального масла с точкой кипения от 210 до 280 С и 10 вес. долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла. Путем вливания и тонкого распределения в 100 000 вес. долей воды получают водную суспензию, содержащую 0,02 вес.% активного вещества.IV. 20 вес. долей активного вещества Nr.If.061 хорошо перемешивают с 3 вес. долями нитриевой соли диизобутилнафталинсульфокислоты, 17 вес. долей натриевой соли лигнинсульфокислоты из отработанного сульфитщелока и 60 вес. долей порошкообразного силикагеля и все промеливают в молотковой мельнице. Благодаря тонкому распределению смеси в 20 000 вес. долях воды получают отвар для опрыскивания, который содержит 0,1 вес.% активного вещества.V. 3 вес. долей активного вещества Nr.Ic.099 смешивают с 97 вес. долями тонкого каолина. Таким образом получают средство распыления, содержащее 3 вес.% активного вещества.VI. 20 вес. долей активного вещества Nr.If.061 хорошо перемешивают с 2 вес. долями соли кальция додецилбензолсульфокислоты, 8 вес. долями полигликолевого эфира жирного спирта, 2 весовыми долями натриевой соли кон 002350 52 денсата фенолмочевинаформальдегид и 68 вес. долями парафинового минерального масла. Получают стабильную масляную дисперсию.VII. 1 вес. долю соединения Ij.043 растворяют в смеси, состоящей из 70 вес. долей циклогексанона, 20 вес. долей этоксилированного изооктилфенола и 10 вес. долей этоксилированного касторового масла. Получают стабильный концентрат эмульсии.Wettol ЕМ 31 (неионный эмульгатор на базе этоксилированного касторового масла). Потом разбавляют водой до желаемой концентрации. Получают стабильный концентрат эмульсии. Применение активных веществ формулы I,соответственно гербицидных средств, может осуществляться довсходовым или послевсходовым методом. Если активные вещества менее переносимы определенными культурными растениями, можно применять технику внесения,при которой гербицидные средства распрыскивают с помощью опрыскивающих приспособлений таким образом, что они по возможности не попадают на листья чуствительных культур, в то время как они попадают на листья растущих внизу нежелательных растений или попадают в незащищенный грунт (методы post-directed, layby). Доза внесения активного вещества I составляет в зависимости от цели применения,времени года, целевых растений и стадии роста от 0,001 до 3,0, предпочтительно от 0,01 до 1,0 кг/га, активного вещества. Для расширения спектра активных веществ и для получения синергитического эффекта соединения замещенные пиразол-3 илбенз(окс/ти/)азолы формулы I могут примешиваться к многочисленным другим гербицидным или регулирующим рост группам активных веществ и вносятся совместно. Например, в качестве партнеров в смеси пригодны: 1,2,4 тиадиазолы, 1,3,4-тиадиазолы, амиды, аминофосфорная кислота и ее производные, аминотриазолы, анилиды, арилалкокси-/гетероарилалкоксиалкенкарбоновые кислоты и их производные, бензойная кислота и ее производные,бензотиадиазиноны,2-(гетароил/ароил)-1,3 циклогександионы, гетариларилкетоны, бензилизоксазолидиноны, производные мета-СF3 фенила, карбаматы, хинолинкарбоновая кислота и ее производные, хлорацетанилиды, производные циклогексан-1,3-диона, диазины, дихлорпропионовая кислота и ее производные, дигидробензофураны, дигидрофуран-3-оны, динитроанилины, динитрофенолы, дифенилэфир, дипиридилы, галогекарбоновые кислоты и их производные, мочевина, 3-фенилурацилы, имидазолы, имидазолиноны, N-фенил-3,4,5,6-тетрагидрофталимиды, оксадиазолы, оксираны, фенолы,сложный эфир арилокси- или гетероарилокси 53 феноксипропионовой кислоты, фенилуксусная кислота и ее производные, фенилпропионовая кислота и ее производные, пиразолы, фенилпиразолы, пиридазины, пиридинкарбоновая кислота и ее производные, пиримидиловый эфир,сульфонамиды, сульфонмочевина, триазины,триазиноны, триазолиноны, триазолкарбоксамиды, урацилы. Кроме того, полезным является смешение соединений формулы I одних или в комбинации с другими гербицидами с другими средствами защиты растений и их совместное внесение,например, со средствами борьбы с вредителями или фитопатогенными грибами или бактериями. Интерес представляет также смешиваемость этих соединений с растворами минеральных солей, которые применяются для устранения дефицитов питательных веществ и микроэлементов. Могут добавляться непитотоксические масла и концентраты. Примеры получения Пример 1. 2-Амино-4-хлор-7-(4-хлор-5 дифторметокси-1-метил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. Ic.080). К раствору из 29,3 г (90 ммоль) 2-хлор-5(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол 3-ил)-4-фторанилина в 500 мл уксусной кислоты подают 9 г (0,36 моль) тиоцианата натрия. После 10 - минутного перемешивания к реакционной смеси прибавляют 28,7 г (0,18 моль) брома. После этого еще 16 ч перемешивают. Потом смесь выливают на 2 л воды. Возникший твердый продукт фильтруют, промывают водой и сушат. Выход продукта: количественный; 1H-ЯМР (270 МГц; CDCl3):[част./млн.] = 3,86 (s, 3H), 5,44 (s, 2H), 6,74 (t, 1H), 7,24 (d, 1H). Пример 2. 4-Хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фтор-2-(метилтио)бензтиазол (Nr. Ic.099). К раствору 0,5 г (1,3 ммоль) 2-амино-4 хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазола в 50 мл дихлорметана подают 0,4 г (3,9 моль) диметилдисульфида и 1,3 г (12,7 ммоль) трет-бутилнитрита. После перемешивания в течение 16 ч реакционную смесь концентрируют. Очистку сырого продукта производят посредством хромотографии на силикагеле (растворитель: гексан/этилацетат = 4:1). Выход продукта: 0,3 г; 1= 2,81 (s, 3H), 3,88 (s, 3H), 6,75 (t, 1H), 7,35 (d,1H). Пример 3. 2-Бром-4-хлор-7-(4-хлор-5 дифторметокси-1-метил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. Ic. 041). К раствору 26,4 г (68 ммоль) 2-амино-4 хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазола в 1 л ацетонитрила подают сначала 35,2 г (0,34 моль) бромида натрия и 19,6 г (0,14 моль) бромида меди(1) и потом по каплям 9,2 г (89 ммоль) трет 002350 54 бутилнитрита. После перемешивания в течение 16 ч к смеси примешивают 0,2 л разбавленной соляной кислоты. После этого твердое вещество фильтруют и промывают посредством 200 мл этилацетата. Оставшийся в водной фазе продукт экстрагируют с помощью еще 200 мл этилацетата. Объединенные органические фазы промывают водой, сушат над сульфатом магния и после этого концентрируют. Очистку сырого продукта производят с помощью хроматографии на силикагеле (растворитель : этилацетат); выход: 17,3 г. Пример 4. 2-Амино-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-4,6-дихлорбензтиазол (Nr. Ib.080). 4,4 г (13 ммоль) 5-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-2,4-дихлоранилина, 4,2 г (52 ммоль) тиоцианата натрия и 4,1 г(26 ммоль) брома подвергают взаимодействию аналогично примеру 1. Выход: количественный. Пример 5. 7-(4-Хлор-5-дифторметокси-1 метил-1 Н-пиразол-3-ил)-4,6-дихлор-2-(этилтио) бензтиазол (Nг. Ib. 100). 0,8 г (2 ммоль) 2-амино-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-4,6 дихлорбензтиазола, 0,7 г (6 ммоль) диэтилсульфида и и 0,3 г (3 ммоль) трет-бутилнитрила подвергают реакции взаимодействия аналогично примеру 2. Выход продукта составляет: 0,2 г. Пример 6. 2-Бром-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-4,6-дихлорбензтиазол (Nr. Ib.041). 3,6 г (9 ммоль) 2-амино-7-(4-хлор-5 дифторметокси-1-метил-1 Н-пиразол-3-ил)-4,6 дихлорбензтиазола, 4,6 г (45 ммоль) бромида натрия, 2,6 г (18 моль) бромида меди(I) и 1,2 г(12 ммоль) трет-бутилнитрита подвергают реакции взаимодействия аналогично примеру 3. Выход продукта составляет 1,8 г. Пример 7. 7-(4-Хлор-5-дифторметокси-1 метил-1 Н-пиразол-3-ил)-4,6-дихлорбензтиазол(Nr. Ib.001). К раствору 0,45 г (1 ммоль) 2-бром-7-(4 хлор-5-дифторметокси-1-метил-1 Н-пиразол-3 ил)-4,6-дихлорбензтиазола в 6 мл диэтилового эфира подают 3 мл двухмолярного раствора пропилхлорида магния в диэтиловом эфире (= 6 ммоль С 3 Н 7 МgСl). Через 5 ч перемешивания в смесь подают 10 мл разбавленной соляной кислоты. После этого отделяют органическую фазу, еще два раза промывают водой и потом сушат над сульфатом магния и концентрируют. Очистку осуществляют с помощью хроматографии на силикагеле (растворитель : гексан/этилацетат = 1:1). Выход: 0,3 г. Пример 8. 2-Амино-4-хлор-7-(4-хлор-1 метил-5-трифторметил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. If. 080). 80 г (0,24 моль) 2-хлор-5-(4-хлор-1-метил 5-трифторметил-1 Н-пиразол-3-ил)-4-фторанилина, 79 г (0,98 моль тиоцианата натрия и 78 г 55 аналогично примеру 1. Выход : количественный. Пример 9. 4-Хлор-7-(4-хлор-1-метил-5 трифторметил-1 Н-пиразол-3-ил)-6-фтор-2(метилтио)бензтиазол (Nr. If.099). 0,7 г (1,8 ммоль) 2-амино-4-хлор-7-(4-хлор 1-метил-5-трифторметил-1 Н-пиразол-3-ил)-6 фторбензтиазола, 0,5 г (5,4 ммоль) диметилдисульфида и 0,33 г (2,7 ммоль) третбутилнитрита подвергают взаимодействию аналогично примеру 2. Выход продукта составляет 0,3 г. Пример 10. 2-Бром-4-хлор-7-(4-хлор-1 метил-5-трифторметил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. If. 041). 73 г (0,12 моль) 2-амино-4-хлор-7-(4-хлор 1-метил-5-трифторметил-1 Н-пиразол-3-ил)-6 фторбензтиазола, 126 г (1,22 ммоль) бромида натрия, 35 г (0,24 моль) бромида меди(I) и 16,3 г(0,16 моль) трет-бутилнитрита Butylnitrit подвергают взаимодействию аналогично примеру 3. Выход: 18,2 g. Пример 11. N-(4-хлор-7-(4-хлор-1-метил-5 трифторметил-1 Н-пиразол-3-ил)-6-фторбензтиазол-2-ил)ацетамид (Nr. If.345). К раствору 0,38 г (6,4 ммоль) ацетамида в 20 мл тетрагидрофурана подают сначала 0,12 г(4,7 ммоль) гидрида натрия и потом 0,7 г (1,6 ммоль) 2-бром-4-хлор-7-(4-хлор-1-метил-5-трифтометил-1 Н-пиразол-3-ил)-6-фторбензтиазола. После этого реакционную смесь перемешивают 16 ч и затем концентрируют. Очистку полученного таким образом сырого продукта производят хроматографией на силикагеле (растворитель : гексан/этилацетат = 4:1 и 1:1). Выход: 0,4 g. Пример 12. Сложный метиловый эфир 3(4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазол-2-ил)акриловой кислоты (Nr. Ic.232). 1 г (3,1 ммоль) 2-амино-4-хлор-7-(4-хлор 5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6 фторбензтиазола, 5,5 г (64 ммоль) сложного метилового эфира акриловой кислоты, 0,45 г (3,4 ммоль) хлорида меди(II) и 0,33 г (3,2 ммоль) трет-бутилнитрита растворяют последовательно в 30 мл ацетонитрила. После этого перемешивают в течение 16 ч, потом реакционную смесь смешивают с 100 мл разбавленной соляной кислоты. Возникший продукт экстрагируют в 200 мл метил-трет-бутиловом эфире. Объединенную органическую фазу промывают два раза водой,сушат над сульфатом магния и потом концентрируют. Очистку полученного таким образом сырого продукта производят хроматографией на силикагеле (растворитель: гексан/этилацетат = 4:1). Выход: 0,13 г. Пример 13. 4-Хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фторбензтиазол (Nr. Ic.001) и 4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фтор-2 метилбензтиазол (Nr. Ic.002). 56 К нагретому на температуру кипения с обратным холодильником раствору 2 г (4,4 ммоль) 2-бром-4-хлор-7-(4-хлор-5-дифторметокси-1 метил-1 Н-пиразол-3-ил)-6-фторбензтиазола и 0,15 г (0,22 ммоль) дихлорида бис(трифенилфосфин)никеля в 20 мл тетрагидрофурана подают по каплям 2,9 мл трехмолярного раствора метилхлорида магния в тетрагидрофуране (= 8,7 ммоль Н 3 СМgСl). После этого реакционную смесь перемешивают 12 ч при температуре кипения с обратным холодильником, после чего к реакционной смеси примешивают 40 мл разбавленной соляной кислоты. Возникший продукт экстрагируют из водной фазы 100 мл этилацитата. Объединенные органичесие фазы промывают два раза водой, сушат над сульфатом магния и потом концентрируют. Очистку сырого продукта производят хроматографией на силикагеле (растворитель : гексан/этилацетат =4:1). В заключении оба целевых продукта отделяют с помощью хромотографии на силикагеле (растворитель : циклогексан/этилацетат = 20:1). Выход 0,11 г (соединение Ic.001) и 0,28 г (соединение Ic.002). Пример 14. 4-Хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фтор-2-пропилбензтиазол (Nr. Ic.004). К раствору 0,4 г (0,9 ммоль) 2-бром-4 хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазола в 30 мл диметилового эфира подают по каплям 0,65 мл двухмолярного раствора пропилхлорида магния в диэтиловом эфире (= 1,3 ммоль С 3 Н 7 МgСl). После этого реакционную смесь перемешивают в течение 16 ч и к ней примешивают 40 мл разбавленной серной кислоты. Возникший продукт экстрагируют из водной фазы посредством 100 мл этилацетата. Объединенные органические фазы сушат над сульфатом магния и потом концентрируют. Очистку сырого продукта производят хроматографией на силикагеле (растворитель : гексан/этилацетат =9:1). Ausbeute: 0,1 g. Пример 15. 4-Хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фтор-2-метоксибензтиазол (Nr. Ic.042). 0,1 г (4,4 ммоль) гидрида натрия растворяют в 20 мл метанола. После окончания выделения газа к раствору примешивают 0,7 г (1,6 ммоль) 2-бром-4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фторбензтиазола. После этого реакционную смесь перемешивают в течение 16 ч. Потом смесь концентрируют. Сырой продукт подвергают очистке хроматографией на силикагеле (растворитель : гексан/этилацетат = 1:1). Выход: 0,5 г. Пример 16. 4-Хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-2-диметиламино-6-фторбензтиазол (Nr. Ic.082). В нагретый на 70-80 С раствор из 0,7 г (1,6 ммоль) 2-бром-4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фторбензтиазола в in 50 мл диметилформамида вводят мед 57 ленным потоком газообразный диметиламин до тех пор, пока не произойдет полная конверсия,(ок. 30 мин). После этого смесь концентрируют,к остатку примешивают 50 мл воды. Из водной фазы экстрагируют возникший продукт посредством 100 мл этилацетата. Собранные органические фазы промывают два раза водой, сушат над сульфатом магния и потом концентрируют. Очистку сырого продукта осуществляют хроматографией на силикагеле (раствор : гексан/ этилацетат =4:1). Выход: 0,46 г. Пример 17. Сложный метиловый эфир Nметил-N-(4-хлор-7-(4-хлор-5-дифторметокси-1 метил-1 Н-пиразол-3-ли)-6-фторбензтиазол-2 ил)аминоуксусной кислоты (Nr. Ic.343). Раствор 0,7 г (1,6 ммоль) 2-бром-4-хлор-7(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол 3-ил)-6-фторбензтиазола, 0,43 г (3,1 ммоль) карбоната калия и 0,43 г (3,1 ммоль) гидрохлорида сложного саркозинметилового эфира в 30 мл диэтилформа-мида нагревают на 100 С в течение 2 ч. После этого реакционную смесь концентрируют, и к остатку примешивают 50 мл воды. Из водной фазы экстрагируют возникший продукт посредством 100 мл этилацетата. Собранные органические фазы промывают еще два раза водой, сушат над сульфатом магния и концентрируют. Очистку сырого продукта осуществляют хроматографией на силикагеле (раствор: гексан/этилацетат = 4:1). Выход: 0,18 г. Пример 18. Сложный метиловый эфир 2(4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазол-2-илокси)пропионовой кислоты (Nr. 1 с. 321). К раствору 0,65 г (6,2 ммоль) сложного метилового эфира 2-гидроксипропионовой кислоты в 20 мл тетрагидрофурана подают 0,11 г (4,7 ммоль) гидрида натрия. После окончания выделения газа к смеси примешивают 0,7 г (1,6 ммоль) 2-бром-4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фторбензтиазола. Потом смесь перемешивают в течение 3 дней и после этого примешивают 50 мл воды. Возникший продукт экстрагируют из водной фазы посредством 100 мл этилацетата. Объединенные органические фазы промывают еще два раза водой, сушат над сульфатом магния и после этого концентрируют. Очистку сырого продукта осуществляют хроматографией на силикагеле (раствор : гексан/этилацетат = 4:1). Выход продукта составляет 0,3 г. Пример 19. 2-Амино-4-хлор-7-(4-хлор-1 метил-5-метилсульфонил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. Ij.080). 7,5 г (21 ммоль) 2-хлор-5-(4-хлор-1-метил 5-метилсульфонил-1 Н-пиразол-3-ил)-4-фторанилина, 6,9 г (85 ммоль) тиоцианата натрия и 6,9 г (43 ммоль) брома подвергают взаимодействию аналогично примеру 1. Выход: количественный. 58 Пример 20. 4-Хлор-7-(4-хлор-1-метил-5 метилсульфонил-1 Н-пиразол-3-ил)-2-этилтио-6 фторбензтиазол (Nr. Ij.100). 1 г (2,5 ммоль) 2-амино-4-хлор-7-(4-хлор 1-метил-5-метилсульфонил-1 Н-пиразол-3-ил)-6 фторбензтиазола, 0,66 г (7,3 ммоль) диэтилдисульфида и 0,37 г (3,7 ммоль) трет-бутилнитрита подвергают взаимодействию аналогично примеру 2. Выход продукта: 0,4 г. Пример 21. 2-Бром-4-хлор-7-(4-хлор-1 метил-5-метилсульфонил-1 Н-пиразол-3-ил)-6 фторбензтиазол (Nr. Ij.041). 6 г (14 ммоль) 2-амино-4-хлор-7-(4-хлор-1 метил-5-метилсульфонил-1 Н-пиразол-3-ил)-6 фторбензтиазола, 7,6 г (70 ммоль) бромида натрия, 4,2 г (30 ммоль) бромида меди(1) и 2,2 г(22 ммоль) трет-бутилнитрита подвергают взаимодействию аналогично примеру 3. Выход: 3,6 г. Пример 22. Сложный моноэтилмоно-третбутиловый эфир 2-(4-хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Н-пиразол-3-ил)-6-фторбензтиазол-2-ил)малоновой кислоты (Nr. Ic.381). К раствору из 0,9 г (5 ммоль) сложного моноэтилмоно-трет-бутилового эфира малоновой кислоты в 10 мл диметилформамида подают 0,1 г (4,7 ммоль) гидрида натрия. После окончания выделения газа к реакционной смеси примешивают 1,5 г (3,3 ммоль) 2-бром-4-хлор-7-(4 хлор-5-дифторметокси-1-метил-1 Н-пиразол-3 ил)-6-фторбензтиазола. Смесь перемешивают один час, потом ее концентрируют. Остаток смешивают с 50 мл воды. Продукт экстрагируют из водной фазы посредством 100 мл этилацетата. Экстракт сушат над сульфатом магния и потом концентрируют. Выход продукта составляет 1 г. Пример 23. Сложный этиловый эфир 2-(4 хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазол-2-ил)уксусной кислоты (Nr. Iс. 021). К раствору из 1 г (1,8 ммоль) сложного моноэтилмоно-трет-бутилового эфира 2-(4 хлор-7-(4-хлор-5-дифторметокси-1-метил-1 Нпиразол-3-ил)-6-фторбензтиазол-2-ил)малоновой кислоты в 10 мл дихлорметана подают 0,30 г (2 ммоль) трифторметансульфокислоты. После этого смесь перемешивают в течение одного часа и потом ее концентрируют. Остаток смешивают с 10 мл уксусной кислоты. Потом нагревают в течение 8 ч на температуру кипения с обратным холодильником. После этого реакционную смесь концентрируют. Остаток смешивают с 50 мл воды. Из водной фазы экстрагируют продукт посредством 100 мл этилацетата. Экстракт промывают разбавленным водным раствором гидрокарбоната натрия и водой, сушат над сульфатом магния и потом концентрируют. Очистку производят с помощью хроматографии на силикагеле (растворитель: гексан/этилацетат =4:1). Выход: 0,4 г. В нижеследующей таблице 2 приведены наряду с вышеописанными активными веществами еще другие пиразол-3-илбензазолы формулы I, которые получены или могут быть получены аналогичным образом. Таблица 2 Пример 24. 4-Хлор-7-(4-хлор-1-метил-5 трифторметил-1 Н-пиразол-3-ил)-2-этил-6 фторбенз-оксазол (Nr. Iq.003). Раствор из 0,5 г (1,4 ммоль) 2-хлор-5-(4 хлор-1-метил-5-трифторметил-1 Н-пиразол-3 ил)-4-фторфенилазида в 100 мл пропионовой кислоты нагревают в течение 20 ч на температуру кипения с обратным холодильником и потом концентрируют. Остаток смешивают с 100 мл этилацетата. Органическую фазу промывают насыщенным водным раствором гидрокарбоната натрия, потом сушат над сульфатом магния и концентрируют. Очистку проводят с помощью хроматографии на силикагеле (растворитель: гексан/этилацетата = 15:1). Выход: 0,3 г; 1= 1,44 (t, 3H), 2,98 (q, 2H), 4,12 (s, 3H), 7,25 (d,1H). Предварительная стадия: 2-хлор-5-(4-хлор 1-метил-5-трифторметил-1 Н-пиразол-3-ил)-4 фторфенилазид. К раствору из 1 г (3 ммоль) 2-хлор-5-(4 хлор-1-метил-5-трифторметил-1 Н-пиразол-3 ил)-4-фторанилина в 20 мл трифторуксусной кислоты подают 0,46 г (4,5 ммоль) третбутилнитрита и 0,3 г (4,5 ммоль) азида натрия. После этого смесь перемешивают в течение 2 ч,после чего к смеси примешивают 50 мл воды. Из водной фазы экстрагируют полученный продукт с помощью 100 мл метил-трет-бутилэфира. Экстракт промывают 10 %-ным натровым щелоком, сушат над сульфатом магния и после этого концентрируют. Очистку сырого продукта осуществляют хроматографией на силикагеле[част./млн] =4,10 (s, 3H), 7,53 (d, 1H), 7,77 (d,1H). Примеры применения (гербицидное действие) Гербицидное действие замещенных пиразол-3-илбензазолов согласно изобретению можно показать с помощью испытаний в теплице. В качестве парниковых емкостей служили пластмассовые горшки с глинистым песком с прибл. 3,0% гумуса в качестве субстрата. Семена испытательных растений высевали с разделением по сорту. При предвсходовой обработке суспендированное в воде активное вещество наносили
МПК / Метки
МПК: C07D 417/04, A01N 43/76
Метки: замещенные, пиразол-3-илбензазолы
Код ссылки
<a href="https://eas.patents.su/30-2350-zameshhennye-pirazol-3-ilbenzazoly.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные пиразол-3-илбензазолы</a>
Предыдущий патент: Очистка нейротрофинов
Следующий патент: Производные сульфонамида, способ их получения и их использование в качестве лекарственных средств.
Случайный патент: Производные бензоимидазола, используемые в качестве антипролиферативного средства












