Цитотоксические агенты, включающие новые производные томаймицина, конъюгаты, способы получения конъюгатов, фармацевтическая композиция, включающая конъюгат, и их терапевтическое применение
Номер патента: 17196
Опубликовано: 30.10.2012
Авторы: Чжао Роберт, Гози Лоранс, Коммерсон Ален, Чари Рави В.Дж., Бушар Эрве, Ли Вэй, Дэн Юнхун
Формула / Реферат
1. Соединения томаймицина формулы (I)
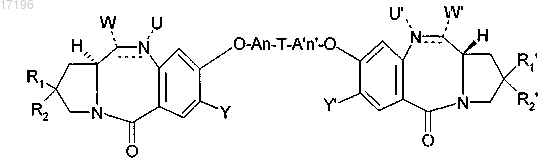 где
гдепредставляет собой необязательную одинарную связь;
представляет собой либо одинарную связь, либо двойную связь;
при условии, что когдапредставляет собой одинарную связь, то U и U', одинаковые или разные, независимо представляют собой Н и W и W', одинаковые или разные, независимо выбраны из группы, состоящей из OH, -OR, -OCOR, -OCOOR, -OCONRR', -NRCONRR', -OCSNHR, -SH, -SR, -SOR, -SOOR,
-SO3-, -NRSOOR, -NRR', -NROR',-NRCOR, -N3, цианогруппы, галогена;
представляет собой двойную связь, то U и U' отсутствуют и W и W' представляют собой H;
R1, R2, R1', R2' являются одинаковыми или разными и независимо выбраны из галогена или C1-12алкила, необязательно замещенного одним или несколькими заместителями из CN, NRR', CF3, OR, фенила, нафтила, S(O)qR, или R1 и R2 и R1' и R2' образуют вместе содержащую двойную связь группу =В и =В' соответственно;
В и В' являются одинаковыми или разными и независимо выбраны из C2-12алкенила, необязательно замещенного одним или несколькими заместителями из CN, R, CF3, OR, фенила, нафтила, S(O)qR;
А, А' являются одинаковыми или разными и независимо выбраны из C1-12алкила или C2-12алкенила, причем каждый необязательно замещен одним или несколькими заместителями из CN, NRR', CF3, OR, S(O)qR, фенила, нафтила, С1-12алкила, С2-12алкенила;
Y, Y' являются одинаковыми или разными и независимо выбраны из Н, OR;
Т представляет собой фенил или пиридил, замещенный одним или несколькими линкерами и необязательно замещен одним или несколькими заместителями из CN, NRR', CF3, OR, S(O)qR;
n, n', одинаковые или разные, равны 0 или 1;
q равно 0, 1 или 2;
R, R' являются одинаковыми или разными и независимо выбраны из Н, C1-12алкила, фенила, нафтила, причем каждый необязательно замещен CN, NRR', CF3, R, OR, S(O)qR, фенилом, нафтилом;
причем указанный линкер включает тиол-, сульфид- или дисульфидсодержащие заместители и представлен формулой
-G -D - (Z)p-S-Z',
где G представляет собой одинарную или двойную связь, -O-, -S- или -NR-;
D представляет собой одинарную связь или -E-, -E-NR-, -E-NR-F-, -E-О-, -E-O-F-, -E-NR-CO-, -E-NR-CO-F-, -E-CO-, -CO-E-, -E-CO-F, -E-S-, -E-S-F-, -E-NR-C-S-, -E-NR-CS-F-;
где Е и F являются одинаковыми или разными и независимо выбраны из неразветвленных или разветвленных следующих остатков:
-(ОСН2СН2)iC1-12алкил(ОСН2СН2)j-,
-C1-12алкил(ОСН2СН2)i-C1-12алкил-,
-(OCH2CH2)i-,
-(ОСН2СН2)iC3-10циклоалкил(ОСН2СН2)j-,
-(ОСН2СН2)iгетероциклил(ОСН2СН2)j-,
-(ОСН2СН2)iарил(ОСН2СН2)j-,
-(ОСН2СН2)iгетероарил(ОСН2СН2)j-,
-C1-12алкил-(ОСН2СН2)iC1-12алкил(ОСН2СН2)j-,
-С1-12алкил-(OCH2CH2)i-,
-С1-12алкил-(OCH2CH2)iC3-10циклоалкил(ОСН2СН2)j-,
-С1-2алкил-(ОСН2СН2)iгетероциклил(ОСН2СН2)j-,
-C1-12алкил-(ОСН2СН2)iарил(ОСН2СН2)j-,
-С1-2алкил-(ОСН2СН2)iгетероарил(ОСН2СН2)j-,
-С3-10циклоалкилС1-12алкил-,
-C1-12алкилС3-10циклоалкил-,
-гетероциклилС1-12алкил-,
-C1-12алкилгетероциклил-,
-C1-12алкиларил-,
-арилС1-12алкил-,
-C1-12алкилгетероарил-,
-гетероарилС1-12алкил-;
где i и j, одинаковые или разные, являются целыми числами и независимо выбраны из 0, 1-2000;
Z представляет собой неразветвленный или разветвленный -C1-12алкил-;
p равно 0 или 1;
Z' представляет собой Н, тиолзащитную группу, такую как COR, R20 или SR20, где R20 представляет собой Н, метил, C1-12алкил, C3-10циклоалкил, арил, гетероарил или гетероциклил, при условии, что когда Z' представляет собой Н, указанное соединение находится в равновесии с соответствующим соединением, образованным внутримолекулярной циклизацией, являющейся результатом присоединения тиольной группы -SH к иминной связи -NH= одного из остатков пирроло[1,4]бензодиазепина (PBD);
где арил представляет собой фенил или нафтил;
гетероцикл представляет собой насыщенный, частично ненасыщенный или ненасыщенный, неароматический стабильный 5-10-членный моно-, би- или полициклический цикл, где по меньшей мере одним членом цикла является гетероатом, выбранный из кислорода, азота, серы;
гетероарил представляет собой пирролил, пиридил, пиразолил, тиенил, пиримидинил, пиразинил, тетразолил, индолил, хинолинил, пуринил, имидазолил, тиенил, тиазолил, бензотиазолил, фуранил, бензофуранил, 1,2,4-тиадиазолил, изотиазолил, триазолил, тетразолил, изохинолил, бензотиенил, изобензофурил, пиразолил, карбазолил, бензимидазолил, изоксазолил, пиридил-N-оксид;
или линкер выбран из следующих групп:
-(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-(CR13R14)t(CR17=CR18)(CR15R16)y(OCH2CH2)ySZ',
-(CR13R14)t(NR19CO)(CR15R16)u(OCH2CH2)ySZ',
-(CR13R14)t(CO)(CR15R16)u(OCH2CH2)ySZ',
-(CR13R14)t(CONR19)(CR15R16)u(OCH2CH2)ySZ',
-(CR13R14)t-фенил-CO(CR15R16)uSZ',
-(CR13R14)t-фурил-CO(CR15R16)uSZ',
-(CR13R14)t-оксазолин-CO(CR15R16)uSZ',
-(CR13R14)t-тиазолил-CO(CR15R16)uSZ',
-(CR13R14)t-тиенил-CO(CR15R16)uSZ',
-(CR13R14)t-имидазолил-CO(CR15R16)uSZ',
-(CR13R14)t-морфолино-CO(CR15R16)uSZ',
-(CR13R14)t-пиперазино-CO(CR15R16)uSZ',
-(CR13R14)t-N-метилпиперазино-CO(CR15R16)uSZ',
-(CR13R14)t-фенил-QSZ',
-(CR13R14)t-фурил-QSZ',
-(CR13R14)t-оксазолил-QSZ',
-(CR13R14)t-тиазолил-QSZ',
-(CR13R14)t-тиенил-QSZ',
-(CR13R14)t-имидазолил-QSZ',
-(CR13R14)t-морфолино-QSZ',
-(CR13R14)t-пиперазино-QSZ',
-(CR13R14)t-N-метилпиперазино-QSZ' или
-O(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-O(CR13R14)t(NR19CO)(CR15R16)u(OCH2CH2)ySZ',
-O(CR13R14)t(CR17=CR18)(CR15R16)t(OCH2CH2)ySZ',
-O-фенил-QSZ',
-О-фурил-QSZ',
-О-оксазолил-QSZ',
-О-тиазолил-QSZ',
-О-тиенил-QSZ',
-О-имидазолил-QSZ',
-О-морфолино-QSZ',
-О-пиперазино-QSZ',
-О-N-метилпиперазино-QSZ',
-OCO-(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)ySZ',
-OCONR12(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-ОСО-фенил-QSZ',
-ОСО-фурил-QSZ',
-ОСО-оксазолил-QSZ',
-ОСО-тиазолил-QSZ',
-ОСО-тиенил-QSZ',
-ОСО-имидазолил-QSZ',
-ОСО-морфолино-QSZ',
-ОСО-пиперазино-QSZ',
-ОСО-N-метилпиперазино-QSZ',
-CO(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-CO-(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)ySZ',
-CONR12(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-CO-фенил-QSZ',
-CO-фурил-QSZ',
-CO-оксазолил-QSZ',
-CO-тиазолил-QSZ',
-CO-тиенил-QSZ',
-CO-имидазолил-QSZ',
-CO-морфолино-QSZ',
-CO-пиперазино-QSZ',
-CO-пиперидино-QSZ',
-CO-N-метилпиперазино-QSZ',
-NR19(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-NR19CO(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-NR19(CR13R14)t(CR17=CR18)(CR15R16)t(OCH2CH2)ySZ',
-NR19CO(CR13R14)t(CR17=CR18)(CR15R16)t(OCH2CH2)ySZ',
-NR19CONR12(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-NR19CONR12(CR13R14)t(CR17=CR18)(CR15R16)t(OCH2CH2)ySZ',
-NR19CO-фенил-QSZ',
-NR19CO-фурил-QSZ',
-NR19CO-оксазолил-QSZ',
-NR19CO-тиазолил-QSZ',
-NR19CO-тиенил-QSZ',
-NR19CO-имидазолил-QSZ',
-NR19CO-морфолино-QSZ',
-NR19CO-пиперазино-QSZ',
-NR19CO-пиперидино-QSZ',
-NR19CO-N-метилпиперазино-QSZ',
-NR19-фенил-QSZ',
-NR19-фурил-QSZ',
-NR19-оксазолил-QSZ',
-NR19-тиазолил-QSZ',
-NR19-тиенил-QSZ',
-NR19-имидазолил-QSZ',
-NR19-морфолино-QSZ',
-NR19-пиперазино-QSZ',
-NR19-пиперидино-QSZ',
-NR19-N-метилпиперазино-QSZ',
-NR19CO-NR12-фенил-QSZ',
-NR19CO-NR12-оксазолил-QSZ',
-NR19CO-NR12-тиазолил-QSZ',
-NR19CO-NR12-тиенил-QSZ',
-NR19CO-NR12-пиперидино-QSZ',
-SCONR12(CR13R14)t(CR15R16)u(OCH2CH2)ySZ',
-SCO-морфолино-QSZ',
-SCO-пиперазино-QSZ',
-SCO-пиперидино-QSZ' и
-SCO-N-метилпиперазино-QSZ',
где Z' представляет собой Н, тиолзащитную группу, R20' или SR20', где R20' представляет собой С1-12алкил, фенил, нафтил;
где Q представляет собой прямую связь или неразветвленный алкил или разветвленный алкил, имеющий 1-10 атомов углерода, или полиэтиленгликолевую связывающую группу с 2-20 повторяющимися этиленоксидными звеньями;
R19 и R12 являются одинаковыми или разными и представляют собой неразветвленный алкил, разветвленный алкил или циклический алкил, имеющий от 1 до 10 атомов углерода, или фенил или нафтил, и R12 помимо этого может быть Н;
R13, R14, R15 и R16 являются одинаковыми или разными и представляют собой Н или неразветвленный или разветвленный алкил, имеющий от 1 до 4 атомов углерода;
R17 и R18 представляют собой H или алкил;
u равно целому числу от 1 до 10 и может быть также равно 0;
t равно целому числу от 1 до 10 и может быть также равно 0;
y равно целому числу от 1 до 20 и также может быть равно 0;
или их фармацевтически приемлемые соли.
2. Соединения по п.1, имеющие следующую формулу (II)
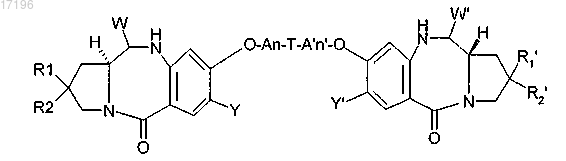
где Y, Y', n, n', R1, R2, R1', R2' A, A', T, W, W' имеют такие же значения, как в п.1.
3. Соединение по п.1 или 2, где В=В' представляет собой =CH2 или =CH-CH3.
4. Соединения по п.1 или 2 формулы
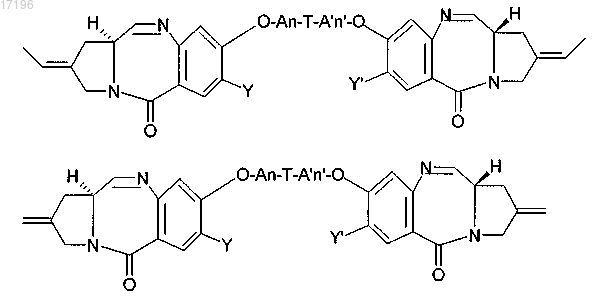
где A, A', Y, Y', T, n, n' имеют такие же значения, как в п.1.
5. Соединения по любому из предыдущих пунктов, где n=n'=1.
6. Соединения по любому из предыдущих пунктов, где A=A'.
7. Соединения по любому из предыдущих пунктов, где A=A'=неразветвленный незамещенный алкил.
8. Соединения по любому из предыдущих пунктов, где Y=Y'.
9. Соединения по любому из предыдущих пунктов, где Y=Y'=OC1-12алкил.
10. Соединения по любому из предыдущих пунктов, где Y=Y'=OMe.
11. Соединения по любому из предыдущих пунктов, где G представляет собой одинарную связь или -O- или -NR-.
12. Соединение по любому из предыдущих пунктов, где G представляет собой -O-.
13. Соединение по любому из предыдущих пунктов, где D представляет собой одинарную связь или -E-, -E-NR-, -E-CO-, -СО-E-, -E-NR-CO-.
14. Соединение по любому из предыдущих пунктов, где D представляет собой -E-NR-CO-.
15. Соединение по любому из предыдущих пунктов, где Е представляет собой неразветвленный или разветвленный -C1-12алкил-, -(ОСН2СН2)- или - C1-12алкилгетероциклил.
16. Соединение по любому из предыдущих пунктов, где Z представляет собой -(СН2)2-С(СН3)2-.
17. Соединение по любому из предыдущих пунктов, где p равно 1.
18. Соединение, выбранное из
8,8'-{5-[3-(4-метил-4-метилдисульфанилпентаноиламино)пропилокси]-1,3-бензолдиилбис(метиленокси)}-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-он];
8,8'-[5-ацетилтиометил-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он];
8,8'-[3-(2-ацетилтиоэтил)-1,5-пентандиилбис(окси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]-бензодиазепин-5-он];
8,8'-[5-(N-4-меркапто-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)]-бис[7-метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он];
8,8'-[5-(N-4-метилдитио-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)]-бис[7-метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[5-(N-метил-N-(2-меркапто-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7-метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[5-(N-метил-N-(2-метилдитио-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7-метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(4-(2-(4-меркапто-4-метил)пентанамидоэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(Е)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(4-(2-(4-метил-4-метилдисульфанил)пентанамидоэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он];
8,8'-[(1-(2-(4-метил-4-метилдисульфанил)пентанамидоэтокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(4-(3-(4-метил-4-метилдисульфанил)пентанамидопропокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(4-(4-(4-метил-4-метилдисульфанил)пентанамидобутокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(4-(3-[4-(4-метил-4-метилдисульфанилпентаноил)пиперазин-1-ил]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(1-(3-[4-(4-метил-4-метилдисульфанилпентаноил)пиперазин-1-ил]пропил)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(4-(2-{2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этокси}этокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(1-(2-{2-[2-(2-{2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этокси}этокси)этокси]этокси}этокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(1-(2-{2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этокси}этокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(4-(2-{2-[2-(2-{2-[2-(4-метил-4-метилдисульфанил-пентаноиламино)этокси]этокси}этокси)этокси]этокси}этокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(1-(2-[метил-(2-метил-2-метилдисульфанилпропил)амино]этокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она];
8,8'-[(4-(3-[метил-(4-метил-4-метилдисульфанилпентаноил)амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(4-(3-[метил-(2-метил-2-метилдисульфанилпропил)амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[(1-(4-метил-4-метилдисульфанил)пентанамидо)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она];
а также их соответствующих меркаптопроизводных или их фармацевтически приемлемых солей.
19. Соединение, выбранное из
8,8'-[4-(3-трет-бутоксикарбониламинопропилокси)]-2,6-пиридиндиилбис(метиленокси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[5-(3-аминопропилокси)-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Н-пирроло[2,1-c][1,4]бензодиазепин-5-она];
8,8'-[5-(N-метил-3-трет-бутоксикарбониламинопропил)-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она].
20. Конъюгат, включающий одно или несколько соединений по любому из пп.1-19, ковалентно связанных со связывающим клетки агентом через линкер, включающий тиол-, сульфид- или дисульфид-связывающую группу в качестве линкерной группы.
21. Конъюгат по п.20, где связывающий клетки агент выбран из антител или фрагмента антитела, который содержит по меньшей мере один сайт связывания, лимфокинов, гормонов, факторов роста, трансферрин.
22. Конъюгат по пп.20, 21, где указанный связывающий клетки агент выбран из моноклональных антител, химерных антител; гуманизированных антител; полностью человеческих антител; одноцепочечных антител; фрагментов антител, таких как Fab, Fab', F(ab')2 и Fv; интерферонов; пептидов; лимфокинов, таких как IL-2, IL-3, IL-4, IL-6; гормонов, таких как инсулин, TRH (тиротропинвысвобождающие гормоны), MSH (меланоцитстимулирующий гормон), стероидных гормонов, таких как андрогены и эстрогены; факторов роста и колониестимулирующих факторов, таких как EGF, TGFα, подобного инсулину фактора роста (IGF-I, IGF-II) G-CSF, M-CSF и GM-CSF; витаминов, таких как фолат и трансферрин.
23. Способ получения конъюгата по любому из пп.20-22, включающий стадию, на которой соединение формулы (I), значение которой указано в п.1, где T представляет собой сульфидную, дисульфидную или тиольную группу, или ее предшественник, подвергают взаимодействию со связывающим клетки агентом, включающим функциональную реакционноспособную в отношении дисульфида или тиола группу, так что соединение и связывающий клетки агент связываются вместе через сульфидную или дисульфидную связь.
24. Способ получения конъюгата, где свободный или защищенный тиолсодержащий связывающий клетки агент взаимодействует с дисульфид- или тиолсодержащим соединением по любому из пп.1-19, причем связывающий клетки агент является пептидом или антителом, модифицированным посредством сшивающего реагента.
25. Способ по п.24, где сшивающим реагентом является N-сукцинимидил-3-(2-пиридилдитио)пропионат, N-сукцинимидил-4-(2-пиридилтио)пентаноат (SPP), 4-сукцинимидилоксикарбонил-α-метил-α-(2-пиридилдитио)толуол (SMPT), N-сукцинимидил-3-(2-пиридилдитио)бутират (SDPB), сукцинимидилпиридилдитиопропионат (SPDP), N-гидроксисукцинимидиловый эфир 4-(2-пиридилдитио)бутановой кислоты (SPDB), сукцинимидил-4-[N-малеимидометил]циклогексан-1-карбоксилат (SMCC), N-сульфосукцинимидил-3-(2-(5-нитропиридилдитио))бутират (SSNPB), 2-иминотиолан или S-ацетилянтарный ангидрид.
26. Способ по п.24, где
моноклональное антитело модифицируют сукцинимидил-пиридилдитиопропионатом и полученную тиопиридильную группу заменяют путем обработки тиолсодержащим соединением по любому из пп.1-19 с получением дисульфидсвязанного конъюгата;
арилтиольную группу соединения по любому из пп.1-19 заменяют сульфгидрильными группами, предварительно введенными в антитело, с получением дисульфидсвязанного конъюгата.
27. Способ по п.24, где тиолсодержащее соединение по любому из пп.1-19 связывается через простую тиоэфирную связь с антителом или связывающим клетки агентом, модифицированным N-сукцинимидил-4-(малеимидометил)циклогексан-карбоксилатом, N-сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбокси-(6-амидокапроатом), N-сукцинимидил-4-(йодацетил)аминобензоатом, N-сукцинимидилйод-ацетатом, N-сукцинимидилбромацетатом или N-сукцинимидил-3-(бромацетамидо)пропионатом.
28. Способ по любому из пп.24-27, где конъюгат очищают стандартными методами хроматографии или диализом, или диафильтрованием.
29. Способ по п.28, где методы хроматографии представляют собой ВЭЖХ, хроматографию с исключением по размеру, адсорбционную хроматографию, ионообменную хроматографию, хроматографию с гидрофобным взаимодействием, аффинную хроматографию, хроматографию на керамическом гидроксиапатите.
30. Фармацевтическая композиция, включающая конъюгат по любому из пп.20-22 или соединение формулы (I) по любому из пп.1-19 вместе с фармацевтически приемлемым носителем.
31. Применение эффективного количества конъюгата по любому из пп.20-22 для изготовления лекарственного средства для лечения рака.
32. Применение эффективного количества соединения формулы (I) по любому из пп.1-19 для изготовления лекарственного средства для лечения рака.
33. Применение конъюгата по любому из пп.20-22 в качестве противоракового агента.
34. Применение соединения по любому из пп.1-19 в качестве противоракового агента.
Текст
ЦИТОТОКСИЧЕСКИЕ АГЕНТЫ, ВКЛЮЧАЮЩИЕ НОВЫЕ ПРОИЗВОДНЫЕ ТОМАЙМИЦИНА, КОНЪЮГАТЫ, СПОСОБЫ ПОЛУЧЕНИЯ КОНЪЮГАТОВ,ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КОНЪЮГАТ, И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ Настоящее изобретение относится к новым производным томаймицина формулы (I),цитотоксическим агентам, включающим их, конъюгатам, способам получения конъюгатов,фармацевтической композиции, включающей конъюгат, и их терапевтическому применению, 017196 где значения радикалов определены в формуле изобретения. 017196 Область техники, к которой относится изобретение Настоящее изобретение относится к новым цитоксическим агентам и их терапевтическому применению. Более конкретно, изобретение относится к новым цитотоксическим агентам, включающим производные томаймицина, и их терапевтическому применению. Эти новые цитотоксические агенты имеют терапевтическое применение в результате доставки производных томаймицина к определенной популяции клеток нацеленным образом химическим связыванием производного томаймицина со связывающим клетки агентом. Уровень техники Появилось много сообщений по предпринятым специфическим нацеливаниям на опухолевые клетки конъюгатами моноклональное антитело-лекарственное средство (Sela et al., in Immunoconjugates,189-216 (C. Vogel, ed. 1987); Ghose et al., in Targeted Drugs 1-22 (E. Goldberg, ed. 1983); Diener et al., insystems, 25-53 (J. Rodwell, ed. 1988); Bumol et al., in Antibody mediated delivery systems, 55-79 (J. Rodwell,ed. 1988); G.A. PieterszK. Krauer, 2, J. Drug Targeting, 183-215 (1994); R.V.J. Chari, 31 Adv. Drug Delivery Revs., 89-104 (1998); W.A. BlattlerR.V.J. Chari, in Anticancer Agents, Frontiers in Cancer Chemotherapy, 317-338, ACS Symposium Series 796; and I. Ojima et al. eds, American Chemical Society 2001. Все цитированные ссылки и патенты включены в описание в качестве ссылки. Цитотоксические лекарственные средства, такие как метотрексат, даунорубицин, доксорубицин,винкристин, винбластин, мелфалан, митомицин С и хлорамбуцил, были конъюгированы с различными мышиными моноклональными антителами. В некоторых случаях молекулы лекарственного средства связывали с молекулами антитела через молекулу промежуточного носителя, такого как сывороточный альбумин (Garnett et al., 46, Cancer Res. 2407-2412 (1986); Ohkawa et al. 23, Cancer Immunol. Immunother. 8186 (1986); Endo et al., 47 Cancer Res. 1076-1080 (1980, дектран (Hurwitz et al., 2 Appl. Biochem. 25-35(1986); Shoval et al., 85, Proc. Natl. Acad. Sci., 8276-8280 (1988, или полиглутаминовая кислота (Tsukadaet al., 73, J. Natl. Canc. Inst., 721-729 (1984); Kato et al. 27 J. Med. Chem., 1602-1607 (1984); Tsukada et al.,52, Br. J. Cancer, 111-116 (1985. Применяли широкий ряд линкерных методик для получения таких иммуноконъюгатов и исследовали как расщепляемые, так и нерасщепляемые линкеры. Однако в большинстве случаев полный цитотоксический потенциал лекарственных средств могли изучить только в тех случаях, если молекулы лекарственного средства могли высвобождаться из конъюгатов в немодифицированной форме у места мишени. Одним из расщепляемых линкеров, которые применяли для получения конъюгатов антителолекарственное средство, является лабильный в кислотной среде линкер на основе цис-аконитовой кислоты, для которого выгодной является кислотная окружающая среда различных внутриклеточных компартментов, таких как цитоплазматические тельца, встречающиеся во время опосредуемого рецептором эндоцитоза, и лизосомы. Shen и Ryser ввели этот способ для получения конъюгатов даунорубицина с макромолекулярными носителями (102 Biochem. Biophys. Res. Commun., 1048-1054 (1981. Yang и Reisfeld применили такую же методику для конъюгации даунорубицина с антителами против меланомы (80 J.Natl. Canc. Inst. 1154-1159 (1988. Dillman et al. также применяли лабильный в кислотной среде линкер аналогичным образом для получения конъюгатов даунорубицина с антителом против T-клеток (48 Cancer Res. 6097-6102 (1988. Альтернативный подход, исследованный Trouet et al., включал связывание даунорубицина с антителом через пептидное промежуточное звено (79 Proc. Natl. Acad. Sci. 626-629 (1982. Это было сделано в соответствии с предпосылкой, что свободное лекарственное средство может высвобождаться из такого конъюгата под воздействием лизосомных пептидаз. Испытания цитотоксичности in vitro, однако, показали, что конъюгаты антитело-лекарственное средство редко достигали такой же цитотоксической активности, как свободные, неконъюгированные лекарственные средства. Это позволило предположить, что механизмы, которыми молекулы лекарственного средства освобождаются от антител, могут быть очень неэффективными. Было обнаружено, что в области иммунотоксинов конъюгаты, образованные посредством дисульфидных мостиков между моноклональными антителами и каталитически активными белковыми токсинами, являются более цитотоксическими, чем конъюгаты, содержащие другие линкеры. См. Lambert et al., 260 J. Biol. Chem. 12035-12041(1985); Lambert et al., in Immunotoxins 175-209 (A. Frankel, ed. 1988); Ghetie et al., 48, Cancer Res. 26102617 (1988). Этот факт приписали высокой внутриклеточной концентрации глутатиона, способствующего эффективному разрыву дисульфидной связи между молекулой антитела и токсином. Несмотря на это имеется только несколько описанных примеров применения дисульфидных мостиков для получения конъюгатов между лекарственными средствами и макромолекулами. Shen et al. (260, J. Biol. Chem. 10905-10908 (1985 описали превращение метотрексата в меркаптоэтиламидное производное с последующим конъюгированием с поли-D-лизином через дисульфидную связь. В другом сообщении описано получение конъюгата, содержащего трисульфид токсичного лекарственного средства калихеамицина с антителом (Hinman et al., 53 Cancer Res. 3336-3342 (1993. Одной причиной недостатка связанных дисульфидом конъюгатов антитело-лекарственное средство-1 017196 является недоступность цитотоксических лекарственных средств, имеющих содержащий атом серы остаток, который можно легко применяют для связывания лекарственного средства с антителом посредством дисульфидного мостика. Кроме того, химическая модификация существующих лекарственных средств является затруднительной без снижения их цитотоксического потенциала. Другим основным недостатком существующих конъюгатов антитело-лекарственное средство является их неспособность доставлять достаточную концентрацию лекарственного средства к месту мишени вследствие ограниченного числа являющихся мишенями антигенов и относительно умеренной цитотоксичности канцеростатических лекарственных средств, подобных метотрексату, даунорубицину и винкристину. Для достижения значительной цитотоксичности связь большого числа молекул лекарственного средства либо непосредственно с антителом, либо через молекулу полимерного носителя становится необходимой. Однако такие сильно модифицированные антитела часто проявляют ослабленное связывание с антигеном-мишенью и быстрое выведение in vivo из кровотока. Несмотря на описанные выше трудности, были описаны полезные цитотоксические агенты, включающие связывающие клетки части и группу цитотоксических лекарственных средств, известных как майтанзиноиды (патент США 5208020, патент США 5416064 и R. V. J. Chari, 31 Advanced Drug DeliveryReviews 89-104 (1998. Аналогично этому, описаны полезные цитотоксические агенты, включающие связывающие клетки части и аналоги и производные сильнодействующего противоопухолевого антибиотика CC-1065 (патент США 5475092, патент США 5585499 и патент США 6756397). Производными томаймицина являются пирроло[1,4]бензодиазепины (PBD), новый класс соединений, обнаруживающие свои биологические свойства при ковалентном связывании с N2 гуанина через малую бороздку спирали ДНК. PBD включают ряд соединений-связывателей через малую бороздку ДНК, такие как антрамицин, неотрамицин и DC-81. Противоопухолевая активность томаймицина, однако, ограничена вследствие его неспецифической токсичности в отношении нормальных клеток. Поэтому существует потребность в повышении терапевтической активности и уменьшении неспецифических токсических действий томаймициновых соединений. Авторы настоящего изобретения обнаружили, что такую проблему можно разрешить направленной доставкой к мишени томаймициновых соединений связыванием их с агентами, связывающими клетки. Кроме того, существует потребность в разработке производных томаймицина, которые являются растворимыми и стабильными в водных растворах. Кроме того,томаймицин не является достаточно сильнодействующим средством, который можно применять в конъюгатах агентов, связывающих клетки. Недавно были описаны некоторые новые производные PBD и их противоопухолевая активность в преклинических моделях (WO 00/12508 и WO 2005/085260). Однако первоначальные клинические испытания на людях показывают, что соединения этого класса являются сильно токсичными в расчете на очень низкую дозу, которую можно ввести людям (I. Puzanov, Proc. AACR-NCI-EORTC International Conference, Philadelphia, USA 2005, Abstract B117). Таким образом, желательно предоставить альтернативные производные, которые являются более сильнодействующими и/или которые можно связать со связывающими клетки агентами. В соответствии с этим, существует огромная потребность в способе лечения заболеваний производными томаймицина, у которых их побочные действия ослаблены без ухудшения их цитотоксичности. Сущность изобретения Как описано в первом варианте осуществления изобретения, одной задачей настоящего изобретения являются создание производных томаймицина, которые являются высокотоксичными, но которые все же можно эффективно применять при лечении многих заболеваний. Другой задачей настоящего изобретения является создание новых производных томаймицина, необязательно способных связываться или связанных со связывающим клетки агентом. Во втором варианте осуществления настоящее изобретение предлагает терапевтическую композицию, включающую:(A) эффективное количество одного или нескольких производных томаймицина, необязательно способных связываться или связанных со связывающим клетки агентом; и(B) фармацевтически приемлемый носитель, разбавитель или эксципиент. В третьем варианте осуществления настоящее изобретение предлагает способ киллинга выбранных популяций клеток, включающий контактирование клеток-мишеней или ткани, содержащей клеткимишени, с цитотоксическим количеством цитотоксического агента, включающего одно или несколько производных томаймицина, необязательно способных связываться или связанных со связывающим клетки агентом. Подробное описание изобретения Данное изобретение основано на синтезе новых производных томаймицина, которые сохраняют высокую токсичность и которые можно эффективно связать с агентами, связывающими клетки. Ранее было обнаружено, что связывание высокотоксичных лекарственных средств с антителами с применением расщепляемой связи, такой как дисульфидная связь, гарантирует высвобождение полностью активных лекарственных средств внутри клетки, и такие конъюгаты являются цитотоксическими в антигенспецифическом способе (патент США 6340701; патент США 6372738; патент США 6436931). Однако-2 017196 данный способ показывает, что очень трудно модифицировать существующие лекарственные средства без уменьшения их цитотоксического потенциала. Данное изобретение преодолевает эту проблему модификацией описанных производных томаймицина химическими остатками. В результате этого описанные новые производные томаймицина сохраняют и в некоторых случаях могут даже повышать цитотоксическую активность производных томаймицина. Комплексы связывающий клетки агент-производное томаймицина позволяют полностью оценить цитотоксическое действие производных томаймицина, которые применяют способом направленного в мишень действия против только нежелательных клеток, тем самым предотвращая побочное действие по повреждению не являющихся мишенями здоровых клеток. Таким образом, изобретение предлагает полезные агенты для ликвидации патологических или аномальных клеток, которые должны убивать или лизировать, например, опухолевые клетки (особенно, клетки солидных опухолей). Цитотоксический агент согласно настоящему изобретению включает одно или несколько производных томаймицина, необязательно способных связываться или связанных со связывающим клетки агентом посредством связывающей группы. Связывающая группа является частью химического остатка, который ковалентно связывают с производным томаймицина при помощи общепринятых методов. В предпочтительном варианте осуществления изобретения химический остаток может быть ковалентно связан с производным томаймицина через дисульфидную связь. Производные томаймицина, пригодные в настоящем изобретении, являются соединениями, имеющими формулу (I), показанную ниже: где представляет собой необязательную одинарную связь; представляет собой либо одинарную связь, либо двойную связь; представляет собой одинарную связь, то U и U', одинаковые или разпри условии, что когда ные, независимо представляют собой Н и W и W', одинаковые или разные, независимо выбраны из группы, состоящей из OH, -OR, -OCOR, -OCOOR, -OCONRR', -NRCONRR', -OCSNHR, -SH, -SR, -SOR, SOOR, -SO3-, -NRSOOR, -NRR', -NROR', -NRCOR, -N3, цианогруппа, галоген; представляет собой двойную связь, то U и U' отсутствуют и W и W' представляют и когда собой H;R1, R2, R1', R2' являются одинаковыми или разными и независимо выбраны из галогена или C1-2 алкила, необязательно замещенного одним или несколькими заместителями из CN, NRR', CF3, OR, фенила, нафтила, S(O)qR, или R1 и R2 и R1' и R2' образуют вместе содержащую двойную связь группу =B и =B',соответственно;B и B' являются одинаковыми или разными и независимо выбраны из C2-12 алкенила, необязательно замещенного одним или несколькими заместителями из CN, R, CF3, OR, фенила, нафтила, S(O)qR;A, A' являются одинаковыми или разными и независимо выбраны из C1-12 алкила или C2-12 алкенила,причем каждый необязательно замещен одним или несколькими заместителями из CN, NRR', CF3, OR,S(O)qR, фенила, нафтила, C1-12 алкила, C2-12 алкенила;Y, Y' являются одинаковыми или разными и независимо выбраны из H, OR; Т представляет собой фенил или пиридил, замещенный одним или несколькими линкерами и необязательно замещен одним или немколькими заместителями из CN, NRR', CF3, OR, S(O)qR;R, R' являются одинаковыми или разными и независимо выбраны из Н, C1-12 алкила, фенила, нафтила, причем каждый необязательно замещен CN, NRR', CF3, R, OR, S(O)qR, фенилом, нафтилом; причем указанный линкер включает тиол-, сульфид- или дисульфидсодержащие заместители и представлен формулойG -D-(Z)p-S-Z' где G представляет собой одинарную или двойную связь, -O-, -S- или -NR-;D представляет собой одинарную связь или -E-, -E-NR-, -E-NR-F-, -E-O-, -E-O-F-, -E-NR-CO-, -ENR-CO-F-, -E-CO-, -CO-E-, -E-CO-F, -E-S-, -E-S-F-, -E-NR-C-S-, -E-NR-CS-F-; где E и F являются одинаковыми или разными и независимо выбраны из неразветвленных или разветвленных-(ОСН 2 СН 2)iC3-10 циклоалкил (ОСН 2 СН 2)j-,-(ОСН 2 СН 2)iгетероциклил (ОСН 2 СН 2)j- ,-(ОСН 2 СН 2)iарил (ОСН 2 СН 2)j-,-(ОСН 2 СН 2)iгетероарил (ОСН 2 СН 2)j-,-C1-12 алкил-(ОСН 2 СН 2)iC1-12 алкил-(ОСН 2 СН 2)j-,-C1-12 алкил-(ОСН 2 СН 2)i-,-C1-12 алкил-(OCH2CH2)iC3-10 циклоалкил(ОСН 2 СН 2)j-,-C1-2 алкил (ОСН 2 СН 2)iгетероциклил (ОСН 2 СН 2)j-,-C1-12 алкил-(ОСН 2 СН 2)iарил (ОСН 2 СН 2)j-, -С 1-2 алкил (ОСН 2 СН 2)iгетероарил (ОСН 2 СН 2)j-,-C3-10 циклоалкилС 1-12 алкил-, -C1-12 алкилС 3-10 циклоалкил-, -гетероциклилС 1-12 алкил-, -C1-12 алкилгетероциклил-, - C1-12 алкиларил-, -арилС 1-12 алкил-, -C1-12 алкилгетероарил-, -гетероарилС 1-12 алкил-; где i и j, одинаковые или разные, являются целыми числами и независимо выбраны из 0, 1-2000;Z представляет собой неразветвленный или разветвленный -C1-12 алкил-;Z представляет собой Н, указанное соединение находится в равновесии с соответствующим соединением, образованным внутримолекулярной циклизацией, являющейся результатом присоединения тиольной группы -SH к иминной связи -NH= одного из остатков PBD; где арил представляет собой фенил или нафтил; гетероцикл представляет собой насыщенный, частично ненасыщенный или ненасыщенный, неароматический стабильный 5-10-членный моно-, би- или полициклический цикл, где по меньшей мере одним членом цикла является гетероатом, выбранный из кислорода, азота, серы; гетероарил представляет собой пирролил, пиридил, пиразолил, тиенил, пиримидинил, пиразинил,тетразолил, индолил, хинолинил, пуринил, имидазолил, тиенил, тиазолил, бензотиазолил, фуранил, бензофуранил, 1,2,4-тиадиазолил, изотиазолил, триазолил, тетразолил, изохинолил, бензотиенил, изобензофурил, пиразолил, карбазолил, бензимидазолил, изоксазолил, пиридил-N-оксид; или линкер выбран из следующих групп:Z' представляет собой Н, тиолзащитную группу, R20' или SR20', где R20' представляет собой C1-12 алкил, фенил, нафтил; где Q представляет собой прямую связь или неразветвленный алкил или разветвленный алкил,имеющий 1-10 атомов углерода, или полиэтиленгликолевая связывающая группа с 2-20 повторяющимися этиленоксизвеньями;R19 и R12 являются одинаковыми или разными и представляют собой неразветвленный алкил, разветвленный алкил или циклический алкил, имеющий от 1 до 10 атомов углерода, или фенил или нафтил,и R12 помимо этого может быть Н,R13, R14, R15 и R16 являются одинаковыми или разными и представляют собой Н или неразветвленный или разветвленный алкил, имеющий от 1 до 4 атомов углерода,R17 и R18 представляют собой H или алкил,u равно целому числу от 1 до 10 и может быть также равно 0,t равно целому числу от 1 до 10 и может быть также равно 0, y равно целому числу от 1 до 20 и также может быть равно 0 или их фармацевтически приемлемые соли. Настоящее изобретение относится к следующим предпочтительным вариантам осуществления или любой комбинации любых из них:G представляет собой одинарную связь или -O- или -NR-;D представляет собой одинарную связь или -E-, -E-NR-CO-, -ЕСО-, -CO-E-;E представляет собой неразветвленный или разветвленный -C1-12 алкил-, -(OCH2CH2)i- или -C1-12 алкилгетероциклил;Z' представляет собой Н или SR20, где R20 представляет собой алкил. Конкретные примеры тиол-, сульфид- или дисульфидсодержащих линкеров включаютZ' представляет собой Н, тиолзащитную группу, R20' или SR20', где R20' представляет собой C1-12 алкил, фенил, нафтил; где Q представляет собой прямую связь или неразветвленный алкил или разветвленный алкил,имеющий 1-10 атомов углерода, или полиэтиленгликолевая спейсерная (связывающая) группа с 2-20 повторяющимися этиленоксизвеньями;R19 и R12 являются одинаковыми или разными и представляют собой неразветвленный алкил, разветвленный алкил или циклический алкил, имеющий от 1 до 10 атомов углерода, или незамещенный или замещенный арил или гетероциклил и R12 помимо этого может быть Н,R13, R14, R15 и R16 являются одинаковыми или разными и представляют собой Н или неразветвленный или разветвленный алкил, имеющий от 1 до 4 атомов углерода,R17 и R18 представляют собой H или алкил,u равно целому числу от 1 до 10 и может быть также равно 0,t равно целому числу от 1 до 10 и может быть также равно 0,y равно целому числу от 1 до 20 и может быть также равно 0. Когда соединение формулы (I) находится в форме иона (например, сульфоната), может присутствовать противоион (например, Na+ или K+). Согласно предпочтительному аспекту соединениями изобретения являются соединения формулы(I), где T представляет собой фенил, замещенный одним или несколькими заместителями из CN, NRR',CF3, OR, S(O)qR, и/или линкером (ами), и A, A', U, U', W, W, m, m', n, n'имеют значения, указанные выше. Согласно другому предпочтительному аспекту, соединения изобретения выбраны из группы, состоящей из 8,8'-[1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-метокси-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11aтетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[1,5-пентандиилбис(окси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-с][1,4]бензодиазепин-5-она]; 8,8'-[1,4-бутандиилбис(окси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-с][1,4]бензодиазепин-5-она]; 8,8'-[3-метил-1,5-пентандиилбис(окси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[2,6-пиридиндиилбис(окси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[4-(3-трет-бутоксисарбониламинопропилокси)-2,6-пиридиндиилбис(метиленокси)]-бис[(S)-2-эт(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(3-аминопропилокси)-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси 1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(N-метил-3-трет-бутоксикарбониламинопропил)-1,3-бензолдиилбис(метиленокси)]-бис[(S)2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-5-[3-(4-метил-4-метилдисульфанилпентаноиламино)пропилокси]-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(Е)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-ацетилтиометил-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11aтетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; трет-бутилового эфира бис-2-[(S)-2-метилен-7-метокси-5-оксо-1,2,3,11a-тетрагидро-5Hпирроло[2,1-c][1,4]бензодиазепин-8-илокси]этилкарбаминовой кислоты; 8,8'-[3-(2-ацетилтиоэтил)-1,5-пентандиилбис(окси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(N-4-меркапто-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)]-бис[7-метокси-2 -метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(N-4-метилдитио-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)]-бис[7 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(N-метил-N-(2-меркапто-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[5-(N-метил-N-(2-метилдитио-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7-8 017196 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(4-(2-(4-меркапто-4-метил)пентанамидоэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(Е)илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(1-(2-(4-метил-4-метилдисульфанил)пентанамидоэтокси)бензол-3,5-диметил)диокси]-бис[(S)2-эт-(Е)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(4-(3-(4-метил-4-метилдисульфанил)пентанамидопропокси)пиридин-2,6-диметил)диокси]бис[(S)-2-эт-(Е)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(4-(4-(4-метил-4-метилдисульфанил)пентанамидобутокси)пиридин-2,6-диметил)диокси]бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(4-(3-[4-(4-метил-4-метилдисульфанилпентаноил)пиперазин-1-ил]пропил)пиридин-2,6 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она]; 8,8'-[(1-(3-[4-(4-метил-4-метилдисульфанилпентаноил)-пиперазин-1-ил]пропил)бензол-3,5 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-с][1,4]бензодиазепин-5-она]; 8,8'-[(4-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)пиридин-2,6 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1 с][1,4]бензодиазепин-5-она]; 8,8'-[(1-(2-2-[2-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)этокси]этоксиэтокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11aтетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(1-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)бензол-3,5 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(4-(2-2-[2-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)этокси]этоксиэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(1-(2-[метил-(2-метил-2-метилдисульфанилпропил)амино]этокси)бензол-3,5-диметил)диокси]бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]-бензодиазепин-5-она]; 8,8'-[(4-(3-[метил-(4-метил-4-метилдисульфанил-пентаноил)амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]-бензодиазепин- 5-она]; 8,8'-[(4-(3-[метил-(2-метил-2-метилдисульфанилпропил)-амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; 8,8'-[(1-(4-метил-4-метилдисульфанил)пентанамидо)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-она]; а также их соответствующих меркаптопроизводных или их фармацевтически приемлемых солей. Предпочтительными соединениями являются соединения формулы где A, A', Y, Y', T, n, n' имеют значения, указанные выше. Применяемые в описании выше или ниже термины имеют следующие значения. Алк представляет собой алкил, алкен или алкин."Алкил" означает алифатическую углеводородную группу, которая может быть неразветвленной или разветвленной и содержит 1-20 атомов углерода в цепи, или циклической и содержит 3-10 атомов углерода. Предпочтительные алкильные группы содержат 1-12 атомов углерода в цепи. "Разветвленная" означает, что одна или несколько низших алкильных групп, таких как метил, этил или пропил, присоединены к неразветвленной алкильной цепи. Примеры алкильных групп включают метил, этил, н-пропил,изопропил, н-бутил, трет-бутил, н-пентил, 3-пентил, октил, нонил, децил, циклопентил и циклогексил."Алкен" означает алифатическую углеводородную группу, которая содержит двойную углеродуглеродную связь и может быть неразветвленной или разветвленной и имеет 2-15 атомов углерода в цепи. Предпочтительные алкенильные группы имеют 2-12 атомов углерода в цепи и, более предпочтительно, приблизительно 2-4 атома углерода в цепи. Примеры алкенильных групп включают этенил, пропенил, н-бутенил, изобутенил, 3-метилбут-2-енил, н-пентенил, гептенил, октенил, ноненил, деценил."Алкин" означает алифатическую углеводородную группу, которая содержит тройную углеродуглеродную связь и может быть неразветвленной или разветвленной и имеет 2-15 атомов углерода в цепи. Предпочтительные алкинильные группы имеют 2-12 атомов углерода в цепи и более предпочтительно 2-4 атома углерода в цепи. Примеры алкинильных групп включают этинил, пропинил, н-бутинил, 2 бутинил, 3-метилбутинил, н-пентинил, гептинил, октинил и децинил."Атом галогена" относится к атомам фтора, хлора, брома или йода; предпочтительно атому фтора и хлора."Арил" означает ароматическую моноциклическую или полициклическую углеводородную систему из 6-14 атомов углерода, предпочтительно 6-10 атомов углерода. Примеры арильных групп включают фенил или нафтил."Het" означает гетероцикл или гетероарил. Применяемые в описании термины "гетероцикл" или "гетероциклический" относятся к насыщенным, частично ненасыщенным или ненасыщенным, неароматическим стабильным 3-14-, предпочтительно 5-10-членным моно-, би- или полициклическим кольцам, где по меньшей мере одним членом кольца является гетероатом. Обычно гетероатомы включают, но не ограничиваются перечисленным, атомы кислорода, азота, серы, селена и фосфора. Предпочтительными гетероатомами являются атомы кислорода,азота или серы. Подходящие гетероциклы описаны также в The Handbook of Chemistry and Physics, 76th Edition, CRCPress, Inc., 1995-1996, pp.2-25 - 2-26, описание которой таким образом включено в качестве ссылки. Предпочтительные неароматические гетероциклы включают, но не ограничиваются перечисленным, пирролицинил, пиразолидинил, имидазолидинил, оксиранил, тетрагидрофуранил, диоксоланил,тетрагидропиранил, диоксанил, диоксоланил, пиперидил, пиперазинил, морфолинил, пиранил, имидазолинил, пирролинил, пиразолинил, тиазолидинил, тетрагидротиспиранил, дитианил, тиоморфолинил, дигидропиранил, тетрагидропиранил, дигидропиранил, тетрагидропиридил, дигидропиридил, тетрагидропиридинил, дигидротиопиранил, азепанил, а также конденсированные системы, являющиеся результатом конденсации с фенильной группой. Применяемый в описании термин гетероарил или ароматические гетероциклы относится к 5-14-,предпочтительно 5-10-членному ароматическому гетероциклическому моно-, би- или полициклическому кольцу. Примеры его включают пирролил, пиридил, пиразолил, тиенил, пиримидинил, пиразинил, тетразолил, индолил, хинолинил, пуринил, имидазолил, тиенил, тиазолил, бензотиазолил, фуранил, бензофуранил, 1,2,4-тиадиазолил, изотиазолил, триазолил, тетразолил, изохинолил, бензотиенил, изобензофурил,пиразолил, карбазолил, бензимидазолил, изоксазолил, пиридил-N-оксид, а также конденсированные системы, являющиеся результатом конденсации с фенильной группой. Термины алкил, циклоалкил, алкенил, алкинил, арил, гетероарил, гетероцикл и тому подобное относятся также к соответствующему алкилену, циклоалкилену, алкенилену, алкинилену, арилену, гетероарилену, гетероциклену и тому подобное, которые образуются удалением двух атомов водорода. Применяемое выражение связываемый с клеткой связывающий агент относится к производным томаймицина, включающим по меньшей мере одну связывающую группу или ее предшественник, подходящий для связывания указанных производных со связывающим клетку агентом; предпочтительными связывающими группами являются тиольные, сульфидные или дисульфидные группы или их предшественники. Применяемое в описании выражение связанный со связывающим клетки агентом относится к молекуле конъюгата, включающей по меньшей мере одно производное томаймицина, связанное со связывающим клетки агентом через подходящую связывающую группу или ее предшественник; предпочтительными связывающими группами являются тиольные или дисульфидные группы или их предшественники. Применяемый в описании термин предшественник данной группы относится к любой группе, которую можно превратить в такую группу любой реакцией снятия защиты, химической модификации или сочетания. Применяемый в описании термин пациент относится к любому животному, такому как ценное животное для целей разведения, компании или охраны или предпочтительно человек или ребенок, который поражен или имеет потенциал быть пораженным одним или несколькими описанными в описании заболеваниями или состояниями. Применяемое в описании выражение терапевтически эффективное количество относится к количеству соединения настоящего изобретения, которое является эффективным при профилактике, ослаблении, устранении, лечении или регуляции симптомов описанных в описании заболеваний или состояний. Предполагается, что термин регулирование относится ко всем способам, при которых может быть замедление, прерывание, задержка, остановка прогресса описанных в описании заболеваний и состояний,но не обязательно означает общее устранение всех симптомов заболевания и состояния и предполагается, что он включает профилактическое лечение.- 10017196 Применяемый в описании термин фармацевтически приемлемый относится к тем соединениям,веществам, эксципиентам, композициям лекарственных форм, которые в пределах тщательной медицинской оценки являются подходящими для контактирования с тканями людей или животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблемных осложнений, соразмерных с приемлемым отношением польза/риск. Приемлемое в описании выражение фармацевтически приемлемые соли относится к производным описанных соединений, где родительское соединение модифицируют образованием солей кислоты или основания. Фармацевтически приемлемые соли включают общепринятые нетоксичные соли или четвертичные аммониевые соли родительского соединения, образованные, например, из нетоксичных неорганических или органических кислот. Такие общепринятые нетоксичные соли включают, например,соли, полученные из неорганических кислот, таких как хлористо-водородная, бромисто-водородная, серная, сульфаминовая, фосфорная, азотная и подобные кислоты; и соли, полученные из органических кислот, таких как уксусная, пропионовая, янтарная, винная, лимонная, метансульфоновая, бензолсульфоновая, глюкуроновая, глутаминовая, бензойная, салициловая, толуолсульфоновая, щавелевая, фумаровая,малеиновая, молочная и подобные кислоты. Дополнительные аддитивные соли включают аммониевые соли, такие как соли трометамина, меглумина, эполамина и т.д., соли металлов, такие как соли натрия,калия, кальция, цинка или магния. Фармацевтически приемлемые соли настоящего изобретения можно синтезировать из исходного соединения, которое содержит основную или кислотную часть, общепринятыми химическими методами. Обычно такие соли можно получить реакцией свободных кислотных или основных форм этих соединений со стехиометрическим количеством подходящего основания или кислоты в воде или в органическом растворителе или в смеси двух из них. Обычно предпочтительными являются неводные среды, подобные простому эфиру, этилацетату, этанолу, изопропанолу или ацетонитрилу. Перечень подходящих солей можно найти в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, PA, 1985,p.1418, описание которой таким образом включено в качестве ссылки. Соединения общей формулы (I), имеющие геометрические изомеры и стереоизомеры, также являются частью изобретения. Известно, что производные томаймицина формулы (I) с N-10, C-11-двойной связью являются легко превращаемыми обратимым образом в соответствующие иминовые аддукты в присутствии воды, спирта,тиола, первичного или вторичного амина, мочевины и других нуклеофилов. Этот процесс является обратимым и соответствующие производные томаймицина можно легко получить в присутствии дегидратирующего агента в непротонном органическом растворителе, в вакууме или при высокой температуре (Z.Tozuka, 36, J. Antibiotics, 276 (1983). Таким образом, данное изобретение предлагает также обратимые производные производных томаймицина общей формулы (II) где A, Y, n, Т, А', Y, n', R1, R2, R1', R2' имеют такие же значения, как в формуле (I), и W, W' являются одинаковыми или разными и выбраны из группы, состоящей из OH, простого эфира, такого как-N3, циано, галогена. Предпочтительно W и W' являются одинаковыми или разными и представляют собой OH, OMe,OEt, NHCONH2, SMe. Соединения формулы (II) можно таким образом рассматривать как сольваты, включая сольваты, когда растворителем является вода; эти сольваты могут быть особенно полезными. Согласно еще одной следующей задаче настоящее изобретение относится также к способу получения соединений формулы (I). Соединения и способы настоящего изобретения можно получить большим числом путей, хорошо известных специалистам в данной области. Соединения можно синтезировать, например, применением или адаптацией способов, описанных ниже, или их вариантов, известных специалисту в данной области. Подходящие модификации и замены должны быть легко очевидны и хорошо известны специалисту в- 11017196 данной области или легко могут быть получены им из научной литературы. В частности, такие способы можно найти в R.C. Larock, Comprehensive Organic Transformations,Wiley-VCH Publishers, 1999. Соединения настоящего изобретения можно получить различными синтетическими путями. Реагенты и исходные вещества являются коммерчески доступными или их легко синтезируют методиками, хорошо известными специалисту в данной области. Все замены, если не оговорено особо, определены предварительно. В реакциях, описанных ниже, может быть необходимо защитить реакционноспособные функциональные группы, например, гидрокси-, амино-, имино-, тио- или карбоксигруппы, которые являются желательными в конечном продукте, чтобы избежать их нежелательного участия в реакциях. Общепринятые защитные группы можно применять согласно стандартной практике, см., например, T.W. Greene andin Protective Groups in Organic Chemistry, Plenum Press, 1973. Некоторые реакции можно проводить в присутствии основания. Нет конкретного ограничения по природе основания, которое применяют в данной реакции, и любое основание, обычно применяемое в реакциях этого типа, можно в равной степени применять здесь, при условии, что не имеется отрицательного влияния на другие части молекулы. Примеры подходящих оснований включают гидроксид натрия,карбонат калия, триэтиламин, гидриды щелочных металлов, такие как гидрид натрия и гидрид калия; алкиллитиевые соединения, такие как метиллитий и бутиллитий, и алкоксиды щелочных металлов, такие как метоксид натрия и этоксид натрия. Реакции обычно проводят в подходящем растворителе. Можно применять различные растворители,при условии, что он не оказывает отрицательное влияние на реакцию или реагенты, участвующие в реакции. Примеры подходящих растворителей включают углеводороды, которыми могут быть ароматическими, алифатическими или циклоалифатическими углеводородами, такими как гексан, циклогексан,бензол, толуол и ксилол; амиды, такие как диметилформамид; спирты, такие как этанол и метанол, и простые эфиры, такие как диэтиловый простой эфир и тетрагидрофуран. Реакции могут протекать на протяжении широкого диапазона температур. В общем, авторами изобретения обнаружено, что реакцию удобно проводить при температуре от -20 до 150C (более предпочтительно от приблизительно комнатной температуры до 100C). Время, требуемое для реакции, может также широко варьировать в зависимости от многие факторов, особенно температуры реакции и природы реагентов. Однако, при условии, что реакцию проводят в предпочтительных условиях, описанных выше, период от 3 до 20 ч обычно бывает достаточным. Соединение, полученное таким образом, можно выделить из реакционной смеси общепринятыми методами. Например, соединения можно выделить отгонкой растворителя из реакционной смеси или,если необходимо, после отгонки растворителя из реакционной смеси выливанием остатка в воду с последующей экстракцией не смешиваемым с водой органическим растворителем и отгонкой растворителя из экстракта. Кроме того, продукт можно, если необходимо, дополнительно очищать различными известными методиками, такими как перекристаллизация, переосаждение или различные хроматографические методики, особенно колоночная хроматография или препаративная тонкослойная хроматография. Способ получения соединений формулы (I) включает стадию снятия защиты у соответствующих соединений формулы (III) где Y, Y', A, A', n, n' , W, W', U, U',R1, R2, R1' , R2',имеют такие же значения, как в формуле (I), X и X' являются кислородом и T' соответствует Т, где функциональная группа(ы) была защищена. Функциональную группу SH предпочтительно защищают и защитной группой предпочтительно является ацетил, бензоил, метансульфонил, метилтио, пиридилтио, нитропиридилтио, триизопропилсилил(TIPS). Стадию удаления защитной группы обычно проводят с применением классических условий, таких как применение основания для удаления ацетильной, бензоильной и метансульфонильной защитных групп, восстанавливающего агента, такого как дитиотреит или трис-(2-карбоксиэтил)фосфин (TCEP) для отщепления метилтиозащитной группы, или, как известно, реакцией соединений с фторидом аммония для удаления TIPS. Соединения формулы (II) можно получить сочетанием соответствующих соединений формул (IV),(IV) и (V) где Y, Y', А, А', n, n' , T', W, W', U, U',R1, R2, R1', R2' имеют значения, указанные для формулы (III), и Lg представляет собой уходящую группу, такую как галоген, OMs, OTs илиOPPh3+ (промежуточное соединение, образованное в реакции Мицунобу). Соединения формул (IV) и (IV) являются обычно известными, как описано, например, в заявках на патенты WO 00/12508, WO 00/12507, WO 2005/040170, WO 2005/085260 или являются коммерчески доступными, и/или являются доступными общим синтезом (M. Mori et al., 42 Tetrahedron, 3793-3806, 1986),или получают с применением Streptomyces species, в частности, по методике патента Франции Fr. 1516743, или их можно получить применением или адаптацией иллюстративных методик, указанных в примерах. Соединения формулы (V) можно получить из соответствующих соединений формулы (VI) где A, A' , n, n', T' имеют значения, указанные для формулы (III). Данную реакцию обычно проводят в присутствии PPh3 и CHal4 или реакцией с хлорсульфонатом в присутствии основания, такого как триэтиламин или гидроксид калия, предпочтительно триэтиламин. Соединения формулы (VI) можно получить из соответствующих соединений формулы (VII) где A, A', n, n' имеют значения, как в формуле (III), и T' представляет собой группу-предшественник для T. Группа-предшественник для T относится к любой группе, которую можно превратить в T любым удалением защитной группы, химической модификацией или сочетанием. T предпочтительно получают сочетанием T' с дополнительной частью, где T' и дополнительная часть включают функциональные группы, которые реагируют друг с другом, например T' включает аминную функциональную группу и дополнительная часть включает кислотную функциональную группу. Репрезентативным примером данной реакции является Данную реакцию обычно проводят в присутствии N-гидроксисукцинимида и HOBT. Соединения формулы (VII) могут быть коммерчески доступными или их можно получить адаптацией или применением известных методов или согласно примерам. Примерная неограничивающая схема для данного варианта осуществления способа изобретения приводится ниже соединение формулы (I) можно получить из соответствующего соединения формулы (III') где Y, Y', A, A', n, n', W, W', U, U',R1, R2, R1', R2' имеют значения, указанные для формулы (I), X и X' являются кислородом и T' представляет собой необязательно защищенную группу-предшественник для Т. Группа-предшественник для T относится к любой группе, которую можно превратить в T химической модификацией или сочетанием. T предпочтительно получают сочетанием T' с соответствующей дополнительной частью, где T' и дополнительная часть включают функциональные группы, которые реагируют друг с другом, например, T' включает аминную функциональную группу и дополнительная часть включает кислотную функциональную группу. Реакцию обычно проводят в присутствии N-гидроксисукцинимида и HOBT. Соединение формулы (III') можно получить сочетанием соответствующих соединений формул (IV),(IV) и (V) где Y, Y', A, A', n, n', W, W', U, U',R1, R2, R1', R2' имеют значения, указанные для формулы (III'), T' представляет собой необязательно защищенную группу-предшественник для T иLg представляет собой уходящую группу, такую как галоген или OMs, OTs или PPh3+ (промежуточное соединение, полученное реакцией Мицунобу). Соединения формул (IV) и (IV) являются обычно известными и доступными общим синтезом (М.Mori et al., 42 Tetrahedron, 3793-3806, 1986) или их получают с применением Streptomyces species, в частности, по методике патента Франции Fr. 1516743. Соединения формулы (V) можно получить из соответствующих соединений формулы (VII) где A, A', n, n' имеют такие же значения, как в формуле (I), T' представляет собой необязательно защищенную группу-предшественник для T'. Данную реакцию обычно проводят в присутствии PPh3 и CHal4. Соединения формулы (VII) могут быть коммерчески доступными или могут быть получены адаптацией или применением известных методов или согласно примерам. Соединения формулы (I) можно также получать путем циклизации соответствующего соединения формулы (VIII) где Y, Y', A, A', n, n', R1, R2, R1', R2', T имеют значения, указанные для формулы (I), X и X' являются кислородом. Данную реакцию обычно проводят в присутствии реагента, такого как гидросульфит натрия (Na2S2O4), в подходящем растворителе, таком как смесь ТГФ и воды, с последующим добавлением метанола и AcCl. Соединение формулы (VIII) можно получить из соответствующего соединения формулы (IX) где Y, Y' A, A', n, n', R1, R2, R1', R2' , T имеют такие же значения, как в формуле (I), X и X' являются кислородом. Данную реакцию обычно проводят в присутствии такого реагента, как DIBAL-H, в подходящем растворителе, таком как толуол. Соединение формулы (IX) можно получить сочетанием соответствующих соединений формул (X) и где Y, Y', A, A', n, n', R1, R2, R1', R2', T имеют такие же значения, как в формуле (I), X и X' являются кислородом. Реакцию обычно проводят добавлением к (X) такого реагента, как оксалилхлорид, в подходящем растворителе, таком как ДМФА с последующим добавлением (XI) в подходящем растворителе, таком как ТГФ. Репрезентативная схема представлена ниже: Указанные выше реакции могут быть проведены специалистом в данной области применением или адаптацией методов, иллюстрированных в указанных ниже примерах. Кроме того, способ получения может также включать дополнительную стадию выделения соединений формул (I) и (II). Это может осуществить специалист в данной области любыми известными общепринятыми методами, такими как методы выделения, описанные выше. Исходные продукты являются коммерчески доступными или их можно получить применением или адаптацией любых известных методов или методами, описанными в примерах. Синтез можно также проводить в одном реакторе как многокомпонентную реакцию. Согласно другой задаче настоящее изобретение относится к молекуле конъюгата, включающей по меньшей мере одно производное томаймицина, ковалентно связанное со связывающим клетки агентом посредством связывающей группы. Указанный конъюгат включает одно или несколько производных томаймицина согласно изобретению, имеющих линкер, включающий связывающую группу, такую как-S- или -S-S-. Указанная связывающая группа ковалентно связывает агент, связывающий клетки, с линкером производного томаймицина. Согласно предпочтительному аспекту указанное производное томаймицина является соединением формулы (I) представляет собой необязательную одинарную связь; представляет собой либо одинарную связь, либо двойную связь; представляет собой одинарную связь, то U и U', одинаковые или разпри условии, что когда ные, независимо представляют собой H и W и W', одинаковые или разные, независимо выбраны из группы, состоящей из OH, -OR, -OCOR, -OCOOR, -OCONRR', -NRCONRR', -OCSNHR, -SH, -SR, -SOR, SOOR, -SO3-, -NRSOOR, -NRR', -NROR', -NRCOR, -N3, цианогруппа, галоген; представляет собой двойную связь, то U и U' отсутствуют и W и W' представляют и когда собой H;R1, R2, R1', R2' являются одинаковыми или разными и независимо выбраны из галогена или C112 алкила, необязательно замещенного одним или несколькими заместителями из CN, NRR', CF3, OR, фенила, нафтила, S(O)qR, или R1 и R2 и R1' и R2' образуют вместе содержащую двойную связь группу =B и=B', соответственно; В и В' являются одинаковыми или разными и независимо выбраны из C2-12 алкенила, необязательно замещенного одним или несколькими заместителями из CN, R, CF3, OR, фенила, нафтила, S(O)qR;A, A' являются одинаковыми или разными и независимо выбраны из C1-12 алкила или C2-12 алкенила,причем каждый необязательно замещен одним или несколькими заместителями из CN, NRR', CF3, OR,S(O)qR, фенила, нафтила, C1-12 алкила, C2-12 алкенила;Y, Y' являются одинаковыми или разными и независимо выбраны из H, OR;T представляет собой фенил или пиридил, замещенный одним или несколькими линкерами и необязательно замещен одним или немколькими заместителями из CN, NRR', CF3, OR, S(O)qR;R, R' являются одинаковыми или разными и независимо выбраны из Н, C1-12 алкила, фенила, нафтила, причем каждый необязательно замещен CN, NRR', CF3, R, OR, S(O)qR, фенилом, нафтилом. Предпочтительно R1 и R2 и R1' и R2' образуют вместе содержащую двойную связь группу =B и =B',соответственно. В и В' являются одинаковыми или разными и независимо выбраны из C2-12 алкенила, необязательно замещенного одним или несколькими заместителями из атома CN, CF3, OR, фенила, нафтила, S(O)qR. Предпочтительно B=B'. Более предпочтительно B=B'==CH2 или =CH-CH3.X, X' являются одинаковыми или разными и независимо выбраны из C1-12 алкила или C2-12 алкенила,причем каждый необязательно замещен одним или несколькими заместителями из CN, NRR', CF3, OR,S(O)qR, фенила, нафтила, C1-12 алкила, C2-12 алкенила. Предпочтительно A=A'. Более предпочтительно A=A'=неразветвленный, незамещенный C1-12 алкил.Y, Y' являются одинаковыми или разными и независимо выбраны из H, OR. Предпочтительно Y=Y'. Более предпочтительно Y=Y' =OC1-12 алкил, более предпочтительно Ометил. Т представляет собой фенил или пиридил, замещенный одним или несколькими заместителями изCN, NRR', CF3, OR, S(O)qR, и замещенный одним или несколькими линкерами. Предпочтительно T представляет собой фенил или пиридил, замещенный одним или несколькими линкерами. Указанный линкер является соединяющей группой. Подходящие связывающие группы хорошо известны в данной области и включают тиольную, сульфидную, дисульфидную группы, простые тиоэфирные группы, лабильные под действием кислот группы, фотолабильные группы, лабильные под действием пептидаз группы и лабильные под действием эстераз группы. Предпочтительными являются дисульфидные группы или простые тиоэфирные группы. Когда связывающей группой является группа, содержащая тиол, сульфид или дисульфид, боковая цепь, содержащая тиольную или дисульфидную группу, может быть неразветвленной или разветвленной, ароматической или гетероциклической. Средний специалист в данной области может легко идентифицировать подходящие боковые цепи. Предпочтительно указанная связывающая группа имеет формулу-G-D-(Z)p-S-Z' где G представляет собой одинарную или двойную связь, -O-, -S- или -NR-;D представляет собой одинарную связь или -E-, -E-NR-, -E-NR-F-, -E-O-, -E-O-F-, -E-NR-CO-, -ENR-CO-F-, -E-CO-, -CO-E-, -E-CO-F, -E-S-, -E-S-F-, -E-NR-C-S-, -E-NR-CS-F-;- 16017196 где Е и F являются одинаковыми или разными и независимо выбраны из неразветвленных или разветвленных -(ОСН 2 СН 2)iалкил(ОСН 2 СН 2)j-, -алкил(ОСН 2 СН 2)iалкил-, -(ОСН 2 СН 2)i-,-(ОСН 2 СН 2)iциклоалкил(ОСН 2 СН 2)j-, -(ОСН 2 СН 2)iгетероциклил(ОСН 2 СН 2)j-, -(ОСН 2 СН 2)iарил(ОСН 2 СН 2)j-,(ОСН 2 СН 2)iгетероарил(ОСН 2 СН 2)j-, -алкил-ОСН 2 СН 2)iалкил (ОСН 2 СН 2)j-, -алкил-(ОСН 2 СН 2)i-, -алкил(ОСН 2 СН 2)iциклоалкил(ОСН 2 СН 2)j-,-алкил(ОСН 2 СН 2)iгетероциклил(ОСН 2 СН 2)j-,-алкил(ОСН 2 СН 2)iарил(ОСН 2 СН 2)j, -алкил(ОСН 2 СН 2)i-гетероарил(ОСН 2 СН 2)j-, -циклоалкилалкил-, -алкилциклоалкил-,-гетероциклилалкил-, -алкилгетероциклил-, -алкиларил-, -арилалкил-, -алкилгетероарил-, -гетероарилалкил-; где i и j, одинаковые или разные, являются целыми числами и независимо выбраны из 0, 1-2000;Z представляет собой неразветвленный или разветвленный -C1-12 алкил-;Z' представляет собой H, указанное соединение находится в равновесии с соответствующим соединением, образованным внутримолекулярной циклизацией, являющейся результатом присоединения тиольной группы -SH к иминной связи -NH= одного из остатков PBD. Арил представляет фенил или нафтил.R, R' являются одинаковыми или разными и независимо выбраны из Н, C1-12 алкила, фенил, причем каждый необязательно замещен атомом CN, NRR', CF3, OR, S(O)qR, фенилом или нафтилом; или его фармацевтически приемлемыми солями, причем указанное производное ковалентно связано со связывающим клетки агентом посредством указанного линкера. Линкер предпочтительно связан со связывающим клетки агентом посредством функциональной группы, реакционноспособной в отношении тиольной, сульфидной или дисульфидной связи. Настоящее изобретение относится к следующим предпочтительным вариантам осуществления или любой комбинации любых из них:G представляет собой одинарную связь или -O- или -NR-;D представляет собой одинарную связь или -E-, -E-NR-, -E-NR-CO-, -E-CO-, -CO-E-;D представляет собой -E-NR-CO-; Е представляет собой неразветвленный или разветвленный -алкил-, -(ОСН 2 СН 2)i- или -C1-12 алкилгетероциклил; Е представляет собой неразветвленный или разветвленный -C1-12 алкил- ;Z' представляет собой Н или SR20, где R20 представляет собой C1-12 алкил. Конкретные примеры тиол-, сульфид- или дисульфидсодержащих линкеров включаютZ' представляет собой Н, тиолзащитную группу, такую как COR, R20' или SR20', где R20' представляет собой C1-12 алкил, фенил, нафтил; где Q представляет собой прямую связь или неразветвленный алкил или разветвленный алкил,имеющий 1-10 атомов углерода, или полиэтиленгликолевая связывающая группа с 2-20 повторяющимися этиленоксизвеньями;R19 и R12 являются одинаковыми или разными и представляют собой неразветвленный алкил, разветвленный алкил или циклический алкил, имеющий от 1 до 10 атомов углерода, или незамещенный или замещенный фенил или нафтил, и R12 помимо этого может быть H,R13, R14, R15 и R16 являются одинаковыми или разными и представляют собой H или неразветвленный или разветвленный алкил, имеющий от 1 до 4 атомов углерода,R17 и R18 представляют собой H или алкил,u равно целому числу от 1 до 10 и может быть также равно 0,t равно целому числу от 1 до 10 и может быть также равно 0,y равно целому числу от 1 до 20 и также может быть равно 0. Согласно данной задаче репрезентативными соединениями формулы (I) являются 8,8'-5-[3-(4-метил-4-метилдисульфанилпентаноиламино)пропилокси]-1,3-бензолдиилбис(метиленокси)-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5 он]; 8,8'-[5-ацетилтиометил-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11aтетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[3-(2-ацетилтиоэтил)-1,5-пентандиилбис(окси)]-бис[(S)-2-метилен-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-он]; 8,8'-[5-(N-4-меркапто-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)бис-[7-метокси 2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[4-(N-4-метилдитио-4,4-диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)бис-[7 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[5-(N-метил-N-(2-меркапто-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[5-(N-метил-N-(2-метилдитио-2,2-диметилэтил)амино-1,3-бензолдиил(метиленокси)]-бис[7 метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(2-(4-меркапто-4-метил)пентанамидоэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]беизодиазепин-5-он]; 8,8'-[(1-(2-(4-метил-4-метилдисульфанил)пентанамидоэтокси)бензол-3,5-диметил)диокси]-бис[(S)2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(3-(4-метил-4-метилдисульфанил)пентанамидопропокси)пиридин-2,6-диметил)диокси]бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(4-(4-метил-4-метилдисульфанил)пентанамидобутокси)пиридин-2,6-диметил)диокси]бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(3-[4-(4-метил-4-метилдисульфанилпентаноил)пиперазин-1-ил]пропил)пиридин-2,6 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(1-(3-[4-(4-метил-4-метилдисульфанилпентаноил)пиперазин-1-ил]пропил)бензол-3,5 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)пиридин-2,6 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(1-(2-2-[2-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэток- 19017196 си)этокси]этоксиэтокси)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11aтетрагидропирроло[2,1-с][1,4]бензодиазепин-5-он]; 8,8'-[(1-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)бензол-3,5 диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(2-2-[2-(2-2-[2-(4-метил-4-метилдисульфанилпентаноиламино)этокси]этоксиэтокси)этокси]этоксиэтокси)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11aтетрагидропирроло[2,1-c][1, 4]бензодиазепин-5-он]; 8,8'-[(1-(2-[метил-(2-метил-2-метилдисульфанилпропил)амино]этокси)бензол-3,5-диметил)диокси]бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3, 11 а-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(3-[метил-(4-метил-4-метилдисульфанилпентаноил)амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(4-(3-[метил-(2-метил-2-метилдисульфанилпропил)амино]пропил)пиридин-2,6-диметил)диокси]-бис[(S)-2-эт-(E)-илиден-7-диметокси-1,2,3,11a-тетрагидропирроло[2,1-c][1,4]бензодиазепин-5-он]; 8,8'-[(1-(4-метил-4-метилдисульфанил)пентанамидо)бензол-3,5-диметил)диокси]-бис[(S)-2-эт-(E)илиден-7-диметокси-1,2,3,11a-тетрагидропирролло[2,1-c][1,4]бензодиазепин-5-он]; а также их соответствующие меркаптопроизводные или их фармацевтически приемлемые соли. Связывающие клетки агенты могут быть любого типа и включают пептиды и не пептиды. Обычно они бывают антителами (особенно, моноклональными антителами) или фрагментом антитела, который содержит, по меньшей мере, один сайт связывания, лимфокинами, гормонами, факторами роста, молекулами переноса питательных веществ (такими как трансферрин) или любой другой связывающей клетки молекулой или веществом. Более конкретные примеры связывающих клетки агентов, которые можно применять, включают моноклональные антитела, химерные антитела; гуманизированные антитела; полностью человеческие антитела; одноцепочечные антитела; фрагменты антител, такие как Fab, Fab', F(ab')2 и Fv Parham, 131 J. Immunol. 2895-2902 (1983); Spring et al., 113 J. Immunol. 470-478 (1974); Nisonoff etal., 89 Arch. Biochem. Biophys. 230-244 (1960); интерфероны; пептиды; лимфокины, такие как IL-2, IL-3,IL-4, IL-6; гормоны, такие как инсулин, TRH (тиротропинвысвобождающие гормоны), MSH (метаноцитстимулирующий гормон), стероидные гормоны, такие как андрогены и эстрогены; факторы роста и колониестимулирующие факторы, такие как EGF, TGFa, подобный инсулину фактор роста (IGF-I, IGF-II)G-CSF, M-CSF и GM-CSF Burgess, 5 Immunology Today 155-158 (1984); витамины, такие как фолат и трансферрин O'Keefe et al., 260 J. Biol. Chem. 932-937 (1985). Выражение связывающий клетки агент, включенное в описании, включает также модифицированные, связывающие клетки агенты, где связывающий клетки агент модифицирован модифицирующим агентом для усиления реакционной способности указанного связывающего клетки агента в отношении связывающей группы линкера производного томаймицина. Указанные модифицирующие агенты включают N-сульфосукцинимидил-4-(5-нитро-2-пиридилдитио)бутаноат (SSNPB), сукцинимидил-4-[Nмалеимидометил]циклогексан-1-карбоксилат (SMCC), N-гидроксисукцинимидиловый эфир 4-(2 пиридилдитио)бутановой кислоты (SPDB) и т.д., как описано ниже. Технология получения моноклонального антитела позволяет получать очень селективные связывающие клетки агенты в форме специфических моноклональных антител. Особенно хорошо известными в данной области являются методики получения моноклональных антител, продуцированных путем иммунизации мышей, крыс, хомячков или любых других млекопитающих представляющим интерес антигеном, таким как интактная клетка-мишень, антигены, выделенные из клетки-мишени, целый вирус, ослабленный целый вирус и вирусные белки, такие как белки вирусной оболочки. Выбор подходящего связывающего клетки агента зависит от конкретной клеточной популяции, которая должна быть мишенью, но обычно предпочтительными являются моноклональные антитела, если подходящее моноклональное антитело является доступным. Например, моноклональным антителом MY9 является мышиное антитело IgG1, которое специфически связывается с антигеном CD33 J.D. Griffin et al. 8 Leukemia Res., 521 (1984) и его можно применять, если клетки-мишени экспрессируют CD33, как при заболевании острым миелобластным лейкозом(AML). Аналогично этому моноклональное антитело анти-B4 является мышиным IgG1, который связывается с антигеном CD19 на В-клетках Nadler et al., 131 J. Immunol. 244-250 (1983), и его можно применять, если клетками-мишенями являются В-клетки или патологические клетки, которые экспрессируют такой антиген, как при неходжкинской лимфоме или хроническом лимфобластном лейкозе. Как указано выше, MY9 и анти-B4-антитела могут быть мышиными, химерными, гуманизированными или полностью человеческими. Кроме того, GM-CSF, который связывается с миелоидными клетками, можно применять в качестве связывающего клетки агента для патологических клеток при остром миелобластном лейкозе. IL-2, который связывается с активированными T-клетками, можно применять для профилактики отторжения трансплантата, для терапии и профилактики гомологичной болезни и для лечения острого T-клеточного лейкоза. MSH, который связывается с меланоцитами, можно применять для лечения меланомы. Молекулы конъюгатов изобретения можно получать любыми методиками. Производные томайми- 20017196 цина изобретения можно связывать с антителом или другим связывающим клетки агентом посредством лабильного под действием кислоты линкера или фотолабильного линкера. Производные можно конденсировать с пептидом, имеющим подходящую последовательность и затем связать со связывающим клетки агентом для получения лабильного под действием пептидазы линкера. Можно получить конъюгаты,которые содержат первичную гидроксильную группу, которую можно сукцинировать и связать со связывающим клетки агентом для получения конъюгата, который можно расщепить внутриклеточными эстеразами для выделения свободного производного. Предпочтительно синтезируют производные, которые содержат свободную или защищенную тиольную группу, и затем одно или несколько дисульфид- или тиолсодержащих производных, каждое, ковалентно связывают со связывающим клетки агентом посредством дисульфидной связи или простой тиоэфирной связи. Многочисленные методы конъюгирования указываются в патенте США 5416064 и патенте США 5475092. Производные томаймицина можно модифицировать для образования свободной аминогруппы и затем связать с антителом или другим связывающим клетки агентом посредством лабильного под действием кислоты линкера или фотолабильного линкера. Производные томаймицина со свободной аминогруппой или карбоксильной группой можно конденсировать с пептидом и затем связать со связывающим клетки агентом для образования лабильного под действием пептидазы линкера. Производные томаймицина со свободной гидроксильной группой на линкере можно сукцинировать и связать со связывающим клетки агентом для получения конъюгата, который можно расщепить внутриклеточными эстеразами для выделения свободного лекарственного средства. Наиболее предпочтительно производные томаймицина обрабатывают для образования свободной или защищенной тиольной группы и затем димеры дисульфид- или тиолсодержащего томаймицина связывают со связывающим клетки агентом посредством дисульфидных связей. Репрезентативными конъюгатами изобретения являются антитело-производное томаймицина,фрагмент антитела-производное томаймицина, производное фактора эпидермального роста(EGF)производное томаймицина, меланоцитстимулирующий гормон(MSH)-производное томаймицина, тироидстимулирующий гормон(TSH)-производное томаймицина, эстроген-производное томаймицина, аналог эстрогена-производное томаймицина, андроген-производное томаймицина, аналог андрогенапроизводное томаймицина и фолат-производное томаймицина. Конъюгаты производного томаймицина и антител, фрагментов антител, белковых или пептидных гормонов, белковых или пептидных факторов роста и других белков получают таким же путем известными методами. Например, пептиды и антитела можно модифицировать сшивающими реагентами, такими как N-сукцинимидил-3-(2-пиридилдитио) пропионат, N-сукцинимидил-4-(2-пиридилтио)пентаноатet al. 1 Anti-Cancer Drug Design 179-184 (1986). Таким образом полученный содержащий свободный или защищенный тиол связывающий клетки агент можно затем подвергнуть реакции с дисульфид- или тиолсодержащим производным томаймицина для получения конъюгатов. Конъюгаты можно очистить ВЭЖХ или гель-фильтрованием. Конъюгатами моноклональное тело- или связывающий клетки агент-производное томаймицина предпочтительно являются конъюгаты, которые соединены через дисульфидную связь, как описано выше, которые способны доставлять производные томаймицина. Такие связывающие клетки конъюгаты получают известными методами например, модификацией моноклональных антител сукцинимидилпиридилдитиопропионатом (SPDP) (Carlsson et al., 173 Biochem. J. 723-737 (1978. Образовавшуюся тиопиридильную группу затем заменяют обработкой тиолсодержащими производными томаймицина для получения связанных дисульфидом конъюгатов. Альтернативно, в случае производных арилдитиотомаймицина получение связывающего клетки конъюгата выполняют прямой заменой арилтиола производного томаймицина сульфгидрильными группами, предварительно введенными в молекулы антитела. Конъюгаты, содержащие 1-10 лекарственных производных томаймицина, связанных через дисульфидный мостик, легко получают любым методом. Более конкретно, раствор дитионитропиридилмодифицированного антитела при концентрации 2,5 мг/мл в буфере 0,05 М фосфата калия с pH 7,5, содержащий 2 мМ EDTA, обрабатывают тиолсодержащим производным томаймицина (1,3 мол. экв./дитиопиридильную группу). Мониторинг высвобождения тионитропиридина из модифицированного антитела проводят спектрофотометрическим методом при 325 нм и завершают приблизительно через 16 ч. Конъюгат антитело-производное томаймицина очищают и освобождают от непрореагировавшего лекарственного средства и другого вещества с низкой молекулярной массой гель-фильтрованием через колонку сефадекс G-25 или сефакрил S300. Число связей остатков- 21017196 производного томаймицина на молекулу антитела можно определить измерением отношения поглощения при 230 и 275 нм. Указанным методом через дисульфидную связь можно связать в среднем 1-10 молекул производного томаймицина на молекулу антитела. Влияние конъюгирования на связывающую аффинность в отношении антиген-экспрессирующих клеток можно определить применением методов, ранее описанных Liu et al., 93 Proc. Natl. Acad. Sci 86188623 (1996). Цитотоксичность производных томаймицина и их конъюгатов с антителом в отношении клеточных линий можно измерить обратной экстраполяцией кривых пролиферации клеток, как описано в Goldmacher et al., 135 J. Immunol. 3648-3651 (1985). Цитотоксичность указанных соединений для прилипающих клеточных линий можно определить клоногенными анализами, как описано в Goldmacher etal., 102 J. Cell Biol. 1312-1319 (1986). Репрезентативными конъюгатами изобретения являются конъюгаты производных томаймицина с антителами, фрагментами антител, фактором эпидермального роста (EGF), меланоцитостимулирующим гормоном (MSH), тироидстимулирующим гормоном (TSH), эстрогеном, аналогами эстрогена, андрогеном и аналогами андрогена. Репрезентативные примеры получения различных конъюгатов производных томаймицина и связывающих клетки агентов описываются ниже. Дисульфидные линкеры. Например, моноклональным антителом MY9 является мышиное антителоIg1, которое специфически связывается с антигеном CD33 J.D. Griffin et al. 8 Leukemia Res., 521 (1984),и его можно применять, если клетки-мишени экспрессируют CD33, как при заболевании острый миелоидный лейкоз (AML). Аналогично этому моноклональным антителом анти-B4 является мышиный IgG1,который связывается с антигеном CD19 на B-клетках Nadler et al., 131 J. Immunol. 244-250 (1983), и его можно применять, если клетками-мишенями являются B-клетки или патологические клетки, которые экспрессируют такой антиген, как при неходжкинской лимфоме или хроническом лимфобластном лейкозе. Кроме того, GM-CSF, который связывается с миелоидными клетками, можно применять в качестве связывающего клетки агента для патологических клеток при остром миелобластном лейкозе. IL-2, который связывается с активированными T-клетками, можно применять для профилактики отторжения трансплантата, для терапии и профилактики гомологичной болезни и для лечения острого T-клеточного лейкоза. MSH, который связывается с меланоцитами, можно применять для лечения меланомы. Антитело или другой связывающий клетки агент модифицируют N-сукцинимидил-3 пиридилдитиопропионатом, как ранее описано (J. Carlsson, H. DrevinR. Axen, Biochem. J., 173:723(1978, для введения в среднем 4-пиридилдитиогрупп на молекулу антитела. Модифицированное антитело подвергают реакции с тиолсодержащим производным для получения дисульфидсвязанного конъюгата. В альтернативном случае конъюгаты можно получить применением и/или адаптацией метода, описанного в WO 2004/103272, содержание которой включено в описании в качестве ссылки. Простые тиоэфирные линкеры. Тиолсодержащие производные настоящего изобретения могут связываться с антителами и другими связывающими клетки агентами через простую тиоэфирную связь, как описано ранее (патент США 5208020). Антитело или другой связывающий клетки агент можно модифицировать коммерчески доступным соединением,таким как(SMCC),N-сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбокси-(6-амидокапроат), который является аналогом с длинной цепью SMCC(LC-SMCC). Эти сшивающие реагенты образуют нерасщепляемые линкеры, образованные из остатков на основе малеимидо. Сшивающие реагенты, содержащие остаток на основе галогенацетила, включают N-сукцинимидил 4-(йодацетил)аминобензоат (SIAB), N-сукцинимидилйодацетат (SIA), N-сукцинимидилбромацетат (SBA) и N-сукцинимидил-3-(бромацетамидо)пропионат (SBAP). Эти сшивающие реагенты образуют нерасщепляемые линкеры, образованные из остатков на основе галогенацетила. Линкеры, лабильные под действием кислоты. Содержащие аминогруппу производные настоящего изобретения можно связать с антителами и другими связывающими клетки агентами через лабильный под действием кислоты линкер, как ранее описано (W. A. Blattler et al., Biochemistry 24, 1517-1524 (1985); патенты США 4542225, 4569789, 4618492, 4764368). Аналогично этому содержащее гидразидогруппу производное настоящего изобретения можно связать с углеводной частью антител и других связывающих клетки агентов через лабильный под действием кислоты гидразоновый линкер (примеры гидразоновых линкеров см. в публикациях В. С. Laguzza et al., J.Med. Chem., 32, 548-555 (1989); R. S. Greenfield et al., Cancer Res., 50, 6600-6607 (1990. Фотолабильные линкеры Содержащие аминогруппу производные настоящего изобретения можно связать с антителами и другими связывающими клетки агентами через фотолабильный линкер, как описано ранее (P. Senter etal., Photochemistry and Photobiology, 42, 231-237 (1985); патент США 4625014). Линкеры, лабильные под действием пептидазы Содержащие аминогруппу производные настоящего изобретения можно также связать со связы- 22017196 вающими клетки агентами через пептидные связывающие группы. Ранее было обнаружено, что короткие пептидные связывающие группы между лекарственными средствами и макромолекулярными белковыми носителями являются стабильными в сыворотке, но легко гидролизуются внутриклеточными пептидазами (A. Trouet et al., Proc. Natl. Acad. Sci., 79, 626-629 (1982. Содержащие аминогруппу производные можно конденсировать с пептидами с применением конденсирующих агентов, таких как 1-этил-3-(3 диметиламинопропил)карбодиимид-HCl (EDC-HCl), чтобы получить производное пептида, которое можно связать со связывающими клетки агентами. Линкеры, лабильные под действием эстеразы Производные настоящего изобретения, имеющие гидроксиалкильную группу, можно сукцинировать янтарным ангидридом и затем связать со связывающим клетки агентом для получения конъюгата,который может расщепляться внутриклеточными эстеразами с выделением свободного лекарственного средства (см., например, Е. Aboud-Pirak et al., Biochem Pharmacol., 38, 641-648 (1989. Конъюгаты, полученные указанными выше методами, можно очищать стандартными методами хроматографии, такими как хроматография с исключением по размеру, адсорбционная хроматография,включающая, но не ограничивающаяся перечисленным, ионообменную хроматографию, хроматографию с гидрофобным взаимодействием, аффинную хроматографию, хроматографию на керамическом гидроксиапатите или на порапаке или ВЭЖХ. Можно также применять очистку диализом или диафильтрованием. Предпочтительными конъюгатами между моноклональными антителами или связывающими клетки агентами и производными настоящего изобретения являются конъюгаты, которые соединены через дисульфидную связь, как обсуждалось ранее. Такие связывающие клетки конъюгаты получают известными методами, такими как модификация моноклональных антител сукцинимидилпиридилдитиопропионатом(SPDP) (Carlsson et al., 173 Biochem. J. 723-737 (1978. Образовавшуюся тиопиридильную группу затем заменяют обработкой тиолсодержащим производным для получения связанных дисульфидом конъюгатов. Данным методом легко получают конъюгаты, содержащие 1-10 производных, связанных через дисульфидный мостик. Конъюгирование данным методом полностью описано в патенте США 5585499,который включен в качестве ссылки. Согласно предпочтительному аспекту, связывающим клетки агентом является антитело, в частности моноклональное антитело. Согласно другому предпочтительному аспекту, связывающим клетки агентом является антигенспецифичный фрагмент антитела, такой как sFV, Fab, Fab' или F(ab')2. Согласно следующей задаче, настоящее изобретение относится также к фармацевтическим композициям, включающим молекулу конъюгата изобретения или соединение формулы (I), указанной выше,вместе с фармацевтически приемлемым носителем. Согласно следующей задаче, настоящее изобретение относится также к способу киллинга или ингибирования роста клеток, предпочтительно выбранных популяций клеток, включающему контактирование клеток-мишеней или ткани, содержащей клетки-мишени с эффективным количеством фармацевтической композиции согласно изобретению. Выбранной популяцией клеток является популяция злокачественных и/или пролиферативных клеток. Согласно следующей задаче, настоящее изобретение относится также к способу лечения, предпочтительно селективного лечения, рака, включающему введение эффективного количества фармацевтической композиции согласно изобретению нуждающемуся в этом пациенту. Согласно настоящему изобретению выражение селективное лечение рака относится к киллингу раковых и/или пролиферативных клеток, по существу, без киллинга нормальных и/или непролиферативных клеток. Согласно следующей задаче, настоящее изобретение относится также к применению молекулы конъюгата изобретения или соединения формулы (I), указанной выше, для изготовления лекарственного средства для лечения рака. Способ ингибирования роста выбранных популяций клеток можно проводить на практике in vitro,in vivo или ex vivo. Примеры применений in vitro включают обработку культур клеток для киллинга всех клеток, за исключением желательных вариантов, которые не экспрессируют антиген-мишень, или киллинг вариантов,которые экспрессируют нежелательный антиген. Условия неклинического применения in vitro легко определяет специалист в данной области. Примеры применений ex vivo включают обработки аутогенного костного мозга перед его трансплантацией тому же самому пациенту для киллинга патологических или злокачественных клеток; обработки костного мозга перед его трансплантацией для киллинга компетентных T-клеток и профилактики гомологичной болезни (GVHD). Клиническую обработку ex vivo для удаления опухолевых клеток или лимфоидных клеток из костного мозга перед аутогенной трансплантацией при лечении рака или при лечении аутоиммунного заболевания, или для удаления T-клеток и других лимфоидных клеток из аллогенного костного мозга или- 23017196 ткани перед трансплантацией, чтобы предотвратить GVHD, можно проводить следующим образом. Костный мозг отбирают у пациента или другого индивидуума и затем инкубируют в среде, содержащей сыворотку, в которую добавляют цитотоксический агент изобретения с диапазоном концентраций от приблизительно 10 мкМ до 1 пМ, в течение от приблизительно 30 мин до приблизительно 48 ч при 37C. Точные условия концентрации и времени инкубации (= доза) легко определяет специалист в данной области. После инкубации клетки костного мозга промывают средой, содержащей сыворотку крови и возвращают пациенту внутривенной инфузией согласно известным методам. В случаях, когда пациент получает другое лечение, такое как курс ампутационной химиотерапии или облучения всего тела между временем отбора костного мозга и реинфузии обработанных клеток, обработанные клетки костного мозга сохраняют замороженными в жидком азоте с применением стандартного медицинского оборудования. Для клинического применения in vivo цитотоксический агент изобретения нужно подавать в виде растворов, которые тестируют на стерильность и уровни эндотоксинов, или в виде лиофилизованного твердого вещества, которое можно снова растворить в стерильной воде для инъекции. Примеры подходящих протоколов введения конъюгата являются следующими. Конъюгаты дают еженедельно в течение 6 недель в виде внутривенного болюса. Дозы болюса дают в 50-400 мл нормального физиологического раствора, в который можно добавить сывороточный альбумин человека (например, 0,5-1 мл концентрированного раствора сывороточного альбумина человека, 100 мг/мл). Дозы будут приблизительно от 50 мкг до 10 мг/кг массы тела в неделю при внутривенном введении (диапазон от 10 мкг до 100 мг/кг на инъекцию). Через шесть недель после лечения пациент может получить второй курс лечения. Конкретные клинические протоколы в отношении пути введения, эксципиентов, разбавителей, доз, времени и т.д. может определить специалист в данной области как предписания для клинических состояний. Примеры медицинских состояний, которые можно лечить согласно способам киллинга выбранных популяций клеток in vivo и ex vivo, включают злокачественность любого типа, в том числе, например,рак легких, молочной железы, толстой кишки, простаты, почек, поджелудочной железы, яичников и лимфатических органов; меланомы; аутоиммунные заболевания, такие как системная красная волчанка,ревматоидный артрит и рассеянный склероз; отторжение трансплантата, такое как отторжение почечного трансплантата, отторжение печеночного трансплантата, отторжение легочного трансплантата, отторжение сердечного трансплантата и отторжение трансплантата костного мозга; гомологичную болезнь; вирусные инфекции, такие как CMV-инфекция, ВИЧ-инфекция, СПИД и т.д.; бактериальную инфекцию и инфекции паразитов, такие как ляблиоз, амебиоз, шистосомоз и другие инфекции, определяемые специалистом в данной области. Возможность идентификации тех субъектов, которые нуждаются в лечении описанными в этом документе заболеваниями и состояниями, находится полностью в пределах умения и знания специалиста в данной области. Ветеринар или врач, являющийся специалистом в данной области, может легко идентифицировать с применением клинических анализов, объективного обследования, истории болезни, семейного анамнеза или биологических и диагностических тестов тех субъектов, которые нуждаются в таком лечении. Терапевтически эффективное количество может легко определить штатный диагност, как диагност в данной области, с применением общепринятых методик и результатов обследования, полученных в аналогичных случаях. При определении терапевтически эффективного количества штатный диагност учитывает ряд факторов, включающих, но не ограничивающихся перечисленным, вид субъекта; его размер, возраст и общее состояние здоровья; конкретное заболевание; степень развития или тяжесть заболевания; реакция отдельного субъекта; конкретное вводимое соединение; способ введения; характеристика биологической доступности вводимого препарата; выбранная схема приема лекарственного средства; применение сопутствующей лекарственной терапии и другие родственные факторы. Количество соединения формулы (I) или конъюгата, которое требуется для достижения требуемого биологического действия, будет варьировать в зависимости от ряда факторов, включающих химические характеристики (например, гидрофобность) применяемых соединений, активность соединений, тип заболевания, вид, к которому принадлежит пациент, патологическое состояние пациента, путь введения, биологическая доступность соединения при выбранном пути, все факторы, которые предписывают требуемые количества доз, доставку и схему, которой нужно вводить лекарственное средство. Термины фармацевтически или фармацевтически приемлемый относятся к молекулярным соединениям и композициям, которые не вызывают отрицательную, аллергическую или другую неблагоприятную реакцию при введении по необходимости животному или человеку. Применяемое в описании выражение фармацевтически приемлемый эксципиент включает любые носители, разбавители, адъюванты или наполнители, такие как консервирующие или антиокислительные агенты, наполнители, дезинтегрирующие агенты, увлажняющие агенты, эмульгирующие агенты, суспендирующие агенты, растворители, диспергирующие среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и замедляющие абсорбцию агенты и тому подобное. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области. Предполагается применение любой общепринятой среды или агента в терапевтических композициях, за исключени- 24017196 ем случаев, когда они являются несовместимыми с активным агентом. В композиции в виде подходящих терапевтических комбинаций можно также включить дополнительные активные ингредиенты. В контексте изобретения термин лечение, применяемый в описании, означает обратное развитие,ослабление, ингибирование прогресса или профилактику нарушения или состояния, для которого такой термин применяют, или одного или нескольких симптомов такого нарушения или состояния. Выражение терапевтически эффективное количество означает количество соединения/лекарственного средства согласно настоящему изобретению, эффективное при предотвращении или лечении указанного в описании патологического состояния. Согласно изобретению термин пациент или пациент, нуждающийся в этом, предназначается для животного или человека, который страдает или, возможно, будет страдать указанным в описании патологическим состоянием. Пациентом предпочтительно является человек. В общих терминах соединения данного изобретения могут быть представлены в водном физиологическом буферном растворе, содержащем 0,1-10% мас./об. соединения и предназначенном для парентерального введения. Типичный диапазон доз составляет от 1 мкг/кг до 0,1 г/кг массы тела в день; предпочтительный диапазон доз составляет от 0,01 мг/кг до 10 мг/кг массы тела в день или эквивалентной дозы для ребенка. Предпочтительная доза вводимого лекарственного средства, вероятно, зависит от таких параметров, как тип и степень прогресса заболевания или нарушения, общее состояние здоровья конкретного пациента, относительная биологическая эффективность выбранного соединения, препарат соединения, путь введения (внутривенный, внутримышечный или другой), фармакокинетические свойства соединения при выбранном пути доставки и скорость (болюс или непрерывная инфузия) и схема введения (число повторений в данный период времени). Соединения настоящего изобретения можно также вводить в стандартных дозах, где термин стандартная доза означает разовую дозу, которая пригодна для введения пациенту, с которой легко работать и которую легко упаковать, которая сохраняется в виде физически и химически стабильной стандартной дозы и включает либо само активное соединение либо его фармацевтически приемлемую композицию,как описано далее. Как таковые, диапазоны типичных общих суточных доз составляют от 0,01 до 100 мг/кг массы тела. В качестве общего руководства, стандартные дозы для людей составляет от 1 до 3000 мг в день. Диапазон стандартных доз предпочтительно бывает 1-500 мг, причем такую дозу вводят одиншесть раз в день, еще более предпочтительна доза от 10 мг до 500 мг, которую вводят один раз в день. Соединения, предложенные в описании, можно изготовить в составе фармацевтических композиций смешиванием с одним или несколькими фармацевтически приемлемыми эксципиентами. Такие композиции в виде стандартных доз можно получить для применения пероральным введением, особенно в форме таблеток, простых капсул или мягких гелевых капсул; или интраназальным введением, особенно в форме порошков, капель для носа или аэрозолей, или дермальным введением, например, местным путем в форме мазей, кремов, лосьонов, гелей или спреев или посредством чрескожных пластырей. Композиции можно подходящим образом вводить в форме стандартной дозы, их можно изготовить любыми методами, хорошо известными в фармацевтической области, например, как описано в Remington: The Science and Practice of Pharmacy, 20th ed.; Gennaro, A. R., Ed.; Lippincott WilliamsWilkins: Philadelphia, PA, 2000. Предпочтительные препараты включают фармацевтические препараты соединений настоящего изобретения, изготовленные для перорального или парентерального введения. Таблетки, пилюли, порошки, капсулы, пастилки и тому подобное для перорального введения могут содержать один или несколько из любых следующих ингредиентов или соединений подобной природы: связывающее вещество, такое как микрокристаллическая целлюлоза или трагакантовая камедь; разбавитель, такой как крахмал или лактоза; дезинтегрирующее вещество, такое как крахмал и производные целлюлозы; смазывающее вещество, такое как стеарат магния; вещество, придающее скольжение, такое как коллоидальный диоксид кремния; подслащивающий агент, такой как сахароза или сахарин; или корригент, такой как перечная мята или метилсалицилат. Капсулы могут быть в форме твердой капсулы или мягкой капсулы, которые обычно изготовляют из смеси желатинов, необязательно смешанных с пластификаторами, а также крахмальной капсулы. Кроме того, дозированные лекарственные формы могут содержать различные другие материалы, которые модифицируют физическую форму стандартной дозы,например покрытия из сахара, шеллака или энтеросолюбильных агентов. Другие пероральные лекарственные формы, сироп или эликсир, могут содержать подслащивающие агенты, консерванты, красители,красящие вещества и корригенты. Кроме того, активные соединения могут быть включены в препараты и композиции с быстрым растворением, модифицированным высвобождением или стойко поддерживаемым высвобождением и такие препараты со стойко поддерживаемым высвобождением предпочтительно являются бимодальными. Предпочтительные таблетки содержат лактозу, кукурузный крахмал, силикат магния, натриевую соль кроскармеллозы, повидон, стеарат магния или тальк в любой комбинации. Жидкие препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Жидкие композиции могут включать также связывающие вещества, буферы, консерванты, хелатирующие агенты, подслащивающие вещества, корригенты и красящие агенты и- 25017196 тому подобное. Неводные растворители включают спирты, пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и органические сложные эфиры, такие как этилолеат. Водные носители включают смеси спиртов и воды, содержащие буферы среды и солевой раствор. Для регулирования высвобождения активных соединений пригодными эксципиентами могут быть, в частности, биосовместимый, биоразрушаемый лактидный полимер, сополимер лактида и гликолида или сополимеры полиоксиэтилен-полиоксипропилен. Наполнители для внутривенного введения могут включать жидкие и питательные наполнители, электролитные наполнители, такие как наполнители на основе декстрозы Рингера и тому подобное. Другие потенциально пригодные системы для парентеральной доставки этих активных соединений включают частицы сополимера этилена и винилацетата, осмотические насосы, имплатируемые системы инфузии и липосомы. Препараты для альтернативных способов введения включают препараты для ингаляции, которые включают такие формы, как сухой порошок, аэрозоль или капли. Они могут быть водными растворами,содержащими, например, полиоксиэтилен-9-лауриловый эфир, гликохолат и деоксихолат, или маслянистыми растворами для введения в форме капель для носа, или в виде геля для внутриносового применения. Препаратами для трансбуккального введения могут быть, например, лепешки или пастилки, такие препараты могут включать также придающую вкус и запах основу, такую как сахароза или аравийская камедь и другие эксципиенты, такие как гликохолат. Препараты, подходящие для ректального введения,предпочтительно выпускают в виде однодозовых суппозиториев с твердой основой, такой как какаомасло, они могут включать салицилат. Препараты для местного нанесения на кожу предпочтительно имеют форму мази, крема, лосьона, пасты, геля, спрея, аэрозоля или масла. Носители, которые можно применять, включают вазелин, ланолин, полиэтиленгликоли, спирты или их комбинации. Препараты,подходящие для трансдермального введения, могут быть представлены в виде отдельных пластырей и могут быть липофильными эмульсиями или содержащими буфер водными растворами, растворенными и/или диспергированными в полимере или клейком веществе. Фигуры На фиг. 1a представлена активность in vitro конъюгата huB4-SPDB-соединение примера 16 в отношении антиген-положительных BJAB-клеток и антиген-отрицательных MOLT-4-клеток. На фиг. 1b - активность in vitro конъюгата huB4-SMCC-соединение примера 16 в отношении антиген-положительных BJAB-клеток и антиген-отрицательных MOLT-4-клеток. На фиг. 1c - активность in vitro свободного соединения примера 16 в отношении клеток BJAB иMOLT-4. На фиг. 2a - активность in vitro конъюгата huB4-SPDB-соединение примера 17 в отношении антиген-положительных BJAB-клеток и антиген-отрицательных MOLT-4-клеток. На фиг. 2b - активность in vitro конъюгата huB4-SMCC-соединение примера 17 в отношении антиген-положительных BJAB-клеток и антиген-отрицательных MOLT-4-клеток. На фиг. 2c - активность in vitro свободного соединения примера 17 в отношении клеток BJAB иMOLT-4. На фиг. 3a - активность in vitro конъюгата huMy-6-SPDB-соединение примера 16 в отношении антиген-положительных HL60/GC-клеток и антиген-отрицательных клеток Рамоса. На фиг. 3b - активность in vitro свободного соединения примера 16 в отношении клеток HL60/GC и клеток Рамоса. Изобретение далее иллюстрируется, но не ограничивается описанием в следующих примерах. Экспериментальная часть Метод A1: высокоэффективная жидкостная хроматография-масс-спектрометрия (ЖХ-МС) Применяют программное обеспечение Micromass MassLynx и анализ проводят на хроматографе ВЭЖХ Agilent 1100 series с колонкой (503 мм) THERMO Hypersil Gold, C18, 3 мкм, применяя градиентное элюирование смесью (A) ацетонитрила и (B) раствора вода/0,1% муравьиная кислота (градиент: от 5% A : 95% B до 95% A : 5% В на протяжении 5 мин, 95% A : 5% В на протяжении 0,5 мин, от 95% A : 5% B до 5% A : 95% В на протяжении 1 мин, 5% A : 95% В в течение 0,5 мин) при скорости потока 0,8 мл/мин; спектрометре Waters-Micromass Platform I, Platform II или ZQ с электрораспылением (положительная и отрицательная ионизация); в ряду двойной матрицы (190-490 нм); вспомогательный детекторSedere (France) Model SEDEX 65 Evaporative Light Scattering (ELS) detector. Метод А 2: высокоэффективная жидкостная хроматография-масс-спектрометрия (ЖХ-МС). Применяют программное обеспечение Micromass MassLynx и анализ проводят на хроматографе WatersAlliance HPLC с колонкой (1003 мм) WATERS XBridge, C18, 3,5 мкм, применяя градиентное элюирование смесью (A) метанола (B) раствора вода/0,1% муравьиная кислота (градиент: от 5% A : 95% B до 95% A : 5% В на протяжении 10 мин, от 95% A : 5% B до 5% A : 95% В на протяжении 1 мин, 5% A : 95% В в течение 2 мин) при скорости потока 1,1 мл/мин; спектрометре Waters-Micromass Platform II с электрораспылением (положительная и отрицательная ионизация); в ряду двойной матрицы (190-500 нм); вспомогательный детектор- 26017196 Метод A3: высокоэффективная жидкостная хроматография-масс-спектрометрия (ЖХ-МС). Применяют программное обеспечение Micromass MassLynx и анализ проводят на хроматографеAgilent 1100 серии HPLC с колонкой (503 мм) XBridge C18, 2,5 мкм, применяя градиентное элюирование смесью (A) ацетонитрила (B) раствора вода/0,1% муравьиная кислота (градиент: от 5% A : 95% B до 100% A на протяжении 5 мин, 100% A в течение 0,5 мин, от 100% A до 5% A : 95% В на протяжении 1 мин, 5% A : 95% В в течение 0,5 мин) при скорости потока 1,1 мл/мин; спектрометре Waters-MicromassZQ с электрораспылением; в ряду двойной матрицы (210-254 нм). Метод В: очистка высокоэффективной жидкостной хроматографией (ВЭЖХ). Очистку ВЭЖХ проводят на колонке (21100 мм, кат.762101) Macherey Nagel Nucleodur, C18Gravity, 5 мкМ, элюируя смесью (A) ацетонитрила и (B) воды (градиент: 5% A : 95% В в течение 5 мин,от 5% A : 95% B до 100% A на протяжении 20 мин, 100% A в течение 8 мин, от 100% A до 5% A : 95% В на протяжении 1 мин, 5% A : 95% В в течение 11 мин) при скорости потока 15 мл/мин (метод В 1) или 20 мл/мин (метод B2). Метод С: масс-спектроскопия с электронной ионизацией (EI). Масс-спектры EI регистрировали с применением масс-спектрометра Finnigan SSQ 7000 (метод EI: 70 эВ, температура источника = 150C, прямой ввод). Метод D: масс-спектроскопия с химической ионизацией (CI) Масс-спектры регистрировали с применением масс-спектрометра Finnigan SSQ 7000 (аммиак). Метод Е: спектроскопия 1H ядерного магнитного резонанса (ЯМР). Спектры 1H ЯМР регистрировали на любом спектрометре из Bruker Avance Drx-500, Bruker AvanceDrx-400 или Bruker Avance Drx-300. Метод F: очистка высокоэффективной жидкостной хроматографией (ВЭЖХ). Очистку ВЭЖХ проводили на колонке Macherey Nagel VP 250/40 мм NUCLEODUR GRAVITY 10010 C18 (кат.762250), элюируя смесью (A) ацетонитрила и (B) раствора вода/HCOONH4 0,01M/NH4OH, pH 9-10 (градиент: 10% A : 90% В в течение 3 мин, от 10% A : 90% B до 95% A : 5% В на протяжении 37 мин, 95% A : 5% В в течение 8 мин, от 95% A : 5% B до 10% A : 90% В на протяжении 1 мин,10% А: 90% В в течение 1 мин) при скорости потока 70 мл/мин. Метод G1: высокоэффективная жидкостная хроматография-масс-спектрометрия (ЖХ-МС). Применяют программное обеспечение Micromass MassLynx и анализ проводят на приборе AcquityUPLC с колонкой (2,1100 мм) Acquity UPLC ВЕН, С 18, 1,7 мкм, применяя градиентное элюирование смесью (A) ацетонитрила и (B) раствора вода/0,1% муравьиная кислота (градиент: от 5% A : 95% B до 95% A : 5% В на протяжении 4,7 мин, от 95% A : 5% B до 5% A : 95% В на протяжении 0,5 мин, 5% A : 95% В в течение 0,8 мин) при скорости потока 1,1 мл/мин; спектрометр Quattro Premier с электрораспылением; в ряду двойной матрицы (210-400 нм). Метод G2: высокоэффективная жидкостная хроматография-масс-спектрометрия (ЖХ-МС). Применяют программное обеспечение Micromass MassLynx и анализ проводят на хроматографе Acquity UPLC с колонкой (2,1100 мм) Acquity UPLC ВЕН С 18, 1,7 мкм, применяя градиентное элюирование смесью (A) ацетонитрила и раствора (B) вода/0,1% муравьиная кислота (градиент: от 5% A : 95% B до 95% A : 5% В на протяжении 10 мин, 95% A : 5% B до 5% A : 95% В на протяжении 1 мин, 5% A : 95% В в течение 2 мин) при скорости потока 0,6 мл/мин; спектрометр Quattro Premier с электрораспылением; в ряду двойной матрицы (210-400 нм). Метод H: метод очистки высокоэффективной жидкостной хроматографией (ВЭЖХ). Очистку ВЭЖХ проводили на Varian HPLC с применением колонки (25021,2 мм, PN А 0490250212, Lot.DT0259, SN 9772196) Kromasil 16 мкм С 18, элюируя смесью (A) воды и (B) ацетонитрила при скорости потока 20 мл/мин. Время сбора было 80 с. Масс-спектры соединений получали на приборе Bruker Esquire 3000. ЯМР-спектры регистрировали на приборе Bruker Avance, действующем при 400 МГц. Градиенты для элюирования соединений из колонки 1. Очистка 8,8'-[5-(N-4-метилдитио-4,4 диметилбутаноил)амино-1,3-бензолдиилбис(метиленокси)]-бис[7-метокси-2-метилен-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-она]. Смесь 55% A : 45% В в течение 8 мин, от 55% A : 45% B до 50% A : 50% В на протяжении 14 мин,от 501 А : 50% B до 10% A : 90% В на протяжении 4 мин, 10% A : 90% В в течение 5 мин, от 10% A : 90% Карбонат калия (22,8 мг), ,'-дибром-м-ксилол (7,3 мг) и иодид калия (9,1 мг) добавляют к перемешиваемому раствору предшественника томаймицина (15 мг) в диметилформамиде (0,5 мл). Реакционную смесь перемешивают в течение 20 ч при 30C. Твердое вещество отделяют фильтрованием, промывают дважды диметилформамидом (0,2 мл), затем выгружают. К объединенному раствору в диметилформамиде добавляют воду (0,4 мл) и образовавшийся раствор вводят для очистки ВЭЖХ согласно методу B1. Подходящие фракции объединяют и концентрируют упариванием на аппарате-центрифугеJouan Model RC10.10, получая при этом 8,8'-[1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(E)-илиден 7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-он] в виде белого порошка (3,33 мг). ЖХ/МС (метод A1, Platform II): ES: m/z=647 MH+ Время удерживания = 3,53 мин 1 8,8'-[5-Метокси-1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11aтетрагидрс-5H-пирроло[2,1-c][1,4]бензодиазепин-5-он] можно получить по методике для получения 8,8'[1,3-бензолдиилбис(метиленокси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5Hпирроло[2,1-c][1,4]бензодиазепин-5-она], исходя из 1,3-бисброметил-5-метоксибензола. ЖХ/МС (метод A1, Platform II):H ЯМР (300 МГц, CDCl3-d1,в м.д.): 1,75 (д, J=7,0 Гц, 6H); 2,96 (м, 4H); 3,81 (с, 3H); 3,89 (м, 2H); 3,96 (с, 6H); 4,26 (ушир.с, 4H); 5,14 (д, J=12,5 Гц, 2H); 5,21 (д, J=12,5 Гц, 2H); 5,60 (м, 2H); 6,82 (с, 2H); 6,95 (ушир.с, 2H); 7,07 (ушир.с, 1H); 7,53 (с, 2H); 7,63 (д, J=4,5 Гц, 2H). 1,3-Бисбромметил-5-метоксибензол можно получить следующим образом: Тетрабромид углерода (663 мг) добавляют к перемешиваемому раствору 1-бромметил-3 гидроксиметил-5-метоксибензола (420 мг) в безводном дихлорметане (10 мл) в атмосфере аргона. После охлаждения образовавшегося раствора при 0C по каплям добавляют раствор трифенилфосфина (500 мл) в безводном дихлорметане (10 мл). Реакционную смесь перемешивают при комнатной температуре в течение 20 ч и затем концентрируют в вакууме до получения остатка. Остаток очищают хроматографией на силикагеле (колонка Merck SuperVarioFlash, 30 г, Si60 15-40 мкм, элюирование смесью дихлорметан/гептан, 40:60), получая при этом 1,3-бисброметил-5-метоксибензол (170 мг).- 28017196 1-Бромметил-3-гидроксиметил-5-метоксибензол можно получить следующим образом. Тетрабромид углерода (3,47 г) добавляют к перемешиваемому раствору 1,3-дигидроксиметил-5 метоксибензола (800 мг) в безводном дихлорметане (16 мл) в атмосфере аргона. После охлаждения образовавшегося раствора при 0C по каплям добавляют раствор трифенилфосфина (2,68 г) в безводном дихлорметане (16 мл). Реакционную смесь перемешивают при комнатной температуре в течение 20 ч и затем концентрируют в вакууме до получения остатка. Остаток очищают хроматографией на силикагеле Карбонат калия (22,8 мг) и 1,5-дийодпентан (8,2 мкл) добавляют к перемешиваемому раствору предшественника томаймицина (15 мг) в диметилформамиде (0,5 мл). Реакционную смесь перемешивают в течение 20 ч при комнатной температуре и добавляют дополнительную порцию карбоната калия (8 мг). Реакционную смесь перемешивают в течение еще 20 ч при комнатной температуре. Твердые вещества отделяют фильтрованием и раствор в диметилформамиде вводят для очистки ВЭЖХ по методу В 2. Подходящие фракции объединяют и концентрируют упариванием при центрифугировании на аппарате Jouan Model RC10.10, получая при этом 8,8'-[1,5-пентандиилбис(окси)]-бис[(S)-2 эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-он] в виде белого порошка (4 мг). ЖХ/МС (метод А 2): 8,8'-[1,4-бутандиилбис(окси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1-с][1,4]бензодиазепин-5-он] можно получить по методике для получения 8,8'-[1,5 пентандиилбис(окси)]-бис[(S)-2-эт-(E)-илиден-7-метокси-1,2,3,11a-тетрагидро-5H-пирроло[2,1 с][1,4]бензодиазепин-5-она] (пример 3), исходя из 1,4-дийодбутана. ЖХ/МС (метод A1, Platform II):
МПК / Метки
МПК: C07D 487/04
Метки: конъюгат, включающие, новые, конъюгаты, способы, терапевтическое, получения, фармацевтическая, конюгатов, применение, цитотоксические, производные, включающая, агенты, композиция, томаймицина
Код ссылки
<a href="https://eas.patents.su/30-17196-citotoksicheskie-agenty-vklyuchayushhie-novye-proizvodnye-tomajjmicina-konyugaty-sposoby-polucheniya-konyugatov-farmacevticheskaya-kompoziciya-vklyuchayushhaya-konyugat-i-ih-terape.html" rel="bookmark" title="База патентов Евразийского Союза">Цитотоксические агенты, включающие новые производные томаймицина, конъюгаты, способы получения конъюгатов, фармацевтическая композиция, включающая конъюгат, и их терапевтическое применение</a>
Предыдущий патент: Концентрат, полученный из молочного продукта, обогащенный природно встречающейся сиалиллактозой, и способ его получения
Следующий патент: Паропроницаемая и водостойкая подошва для предмета обуви, предмет обуви с такой подошвой и способ изготовления такой подошвы и такой обуви
Случайный патент: Комплекс сорбционной очистки загрязненных вод












