Аминоарилсульфонамидные соединения и их применение в качестве 5-нт6 лигандов
Номер патента: 17154
Опубликовано: 30.10.2012
Авторы: Рамакришна Нироджи Венката Сатья, Схинде Анил Карбхари, Джасти Венкатесварлу, Кандикере Нагарадж Вишвоттам, Камбхампати Рама Састри
Формула / Реферат
1. Соединение общей формулы (I)
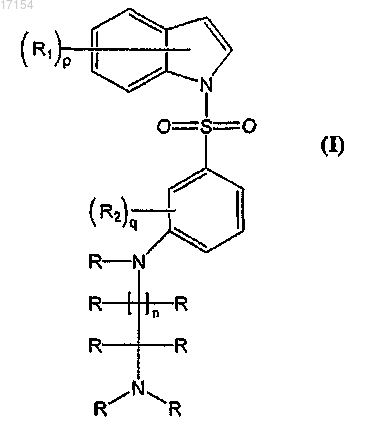
и его фармацевтически приемлемые соли, где
R1 могут быть одинаковыми или отличными друг от друга и каждый независимо представляет собой водород, гидроксил, галоген, (C1-C3)алкил, галоген(C1-C3)алкил, (C1-C3)алкокси, галоген(C1-C3)алкокси, цикло(С3-С6)алкил или цикло(С3-C6)алкокси;
R2 могут быть одинаковыми или отличными друг от друга и каждый независимо представляет собой водород, галоген, (C1-С3)алкил, галоген(С1-С3)алкил, (C1-C3)алкокси или галоген(C1-С3)алкокси, цикло(С3-C6)алкил или цикло(С3-С6)алкокси;
R могут быть одинаковыми или отличными друг от друга, и каждый независимо представляет собой водород или (C1-C3)алкил или (С3-С6)циклоалкил;
n имеет значение от 0 до 4;
p имеет значение от 0 до 6;
q имеет значение от 0 до 4.
2. Соединение по п.1, где R1 представляет собой водород, гидроксил, галоген, (C1-C3)алкил, галоген(C1-C3)алкил, (C1-С3)алкокси или галоген(C1-C3)алкокси.
3. Соединение по п.1, где R представляет собой водород или (C1-C3)алкил.
4. Соединение по п.1, которое выбрано из группы, состоящей из
N'-[2-метокси-5-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
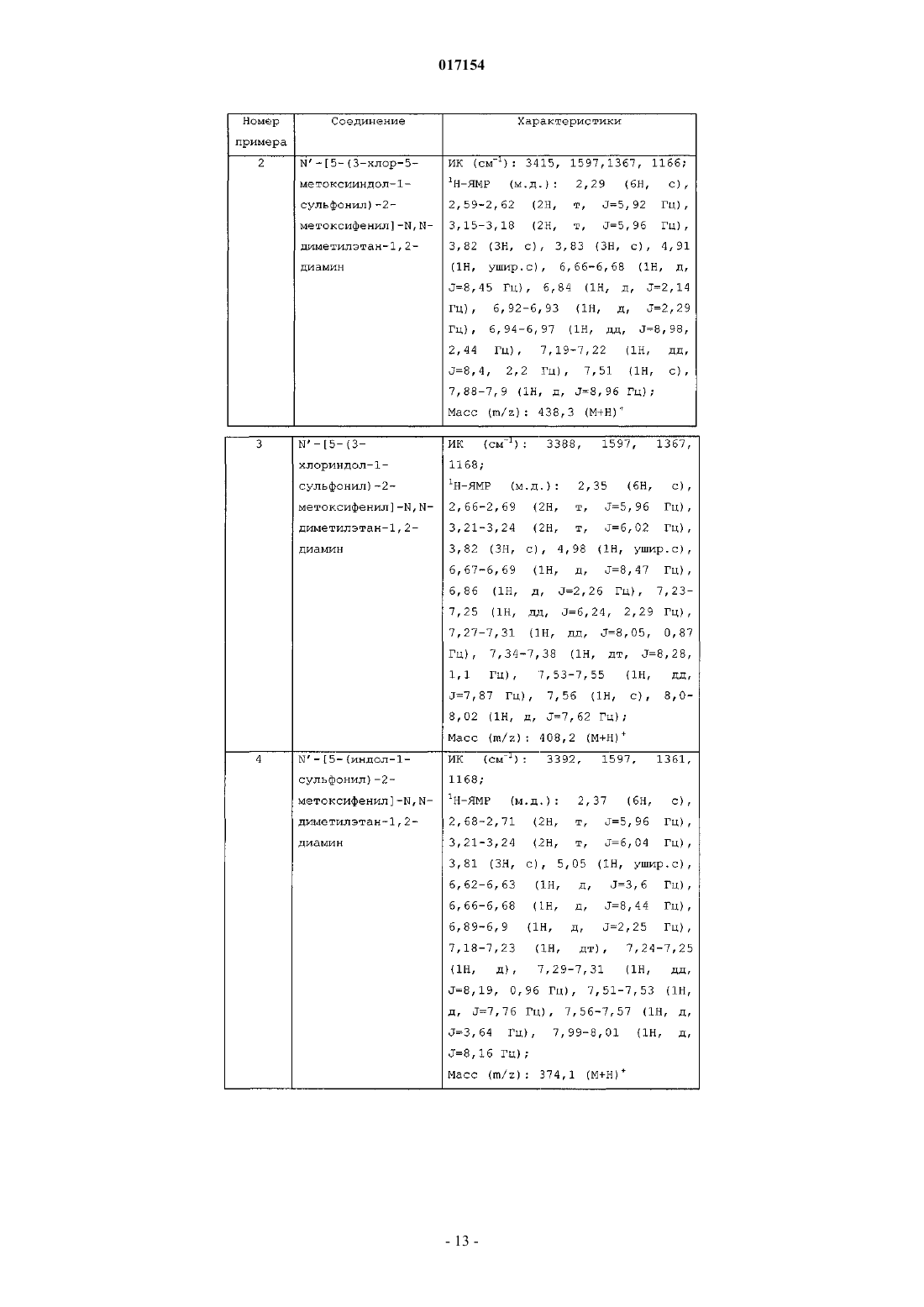
N'-[5-(3-хлор-5-метоксииндол-1-сульфонил)-2-метоксифенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(3-хлориндол-1-сульфонил)-2-метоксифенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(индол-1-сульфонил)-2-метоксифенил]-N,N-диметилэтан-1,2-диамина;
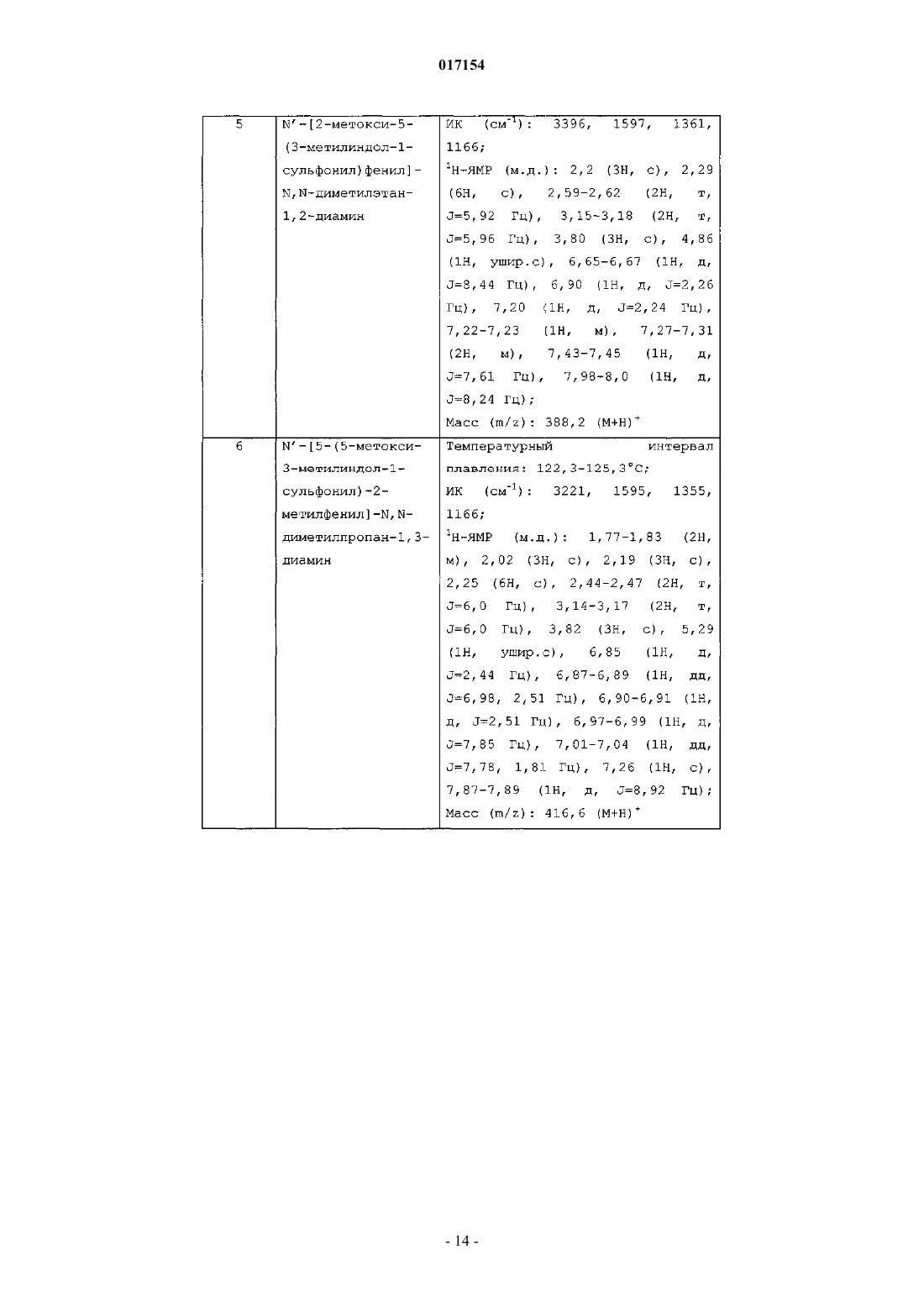
N'-[2-метокси-5-(3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(5-метокси-3-метилиндол-1-сульфонил)-2-метилфенил]-N,N-диметилпропан-1,3-диамина;
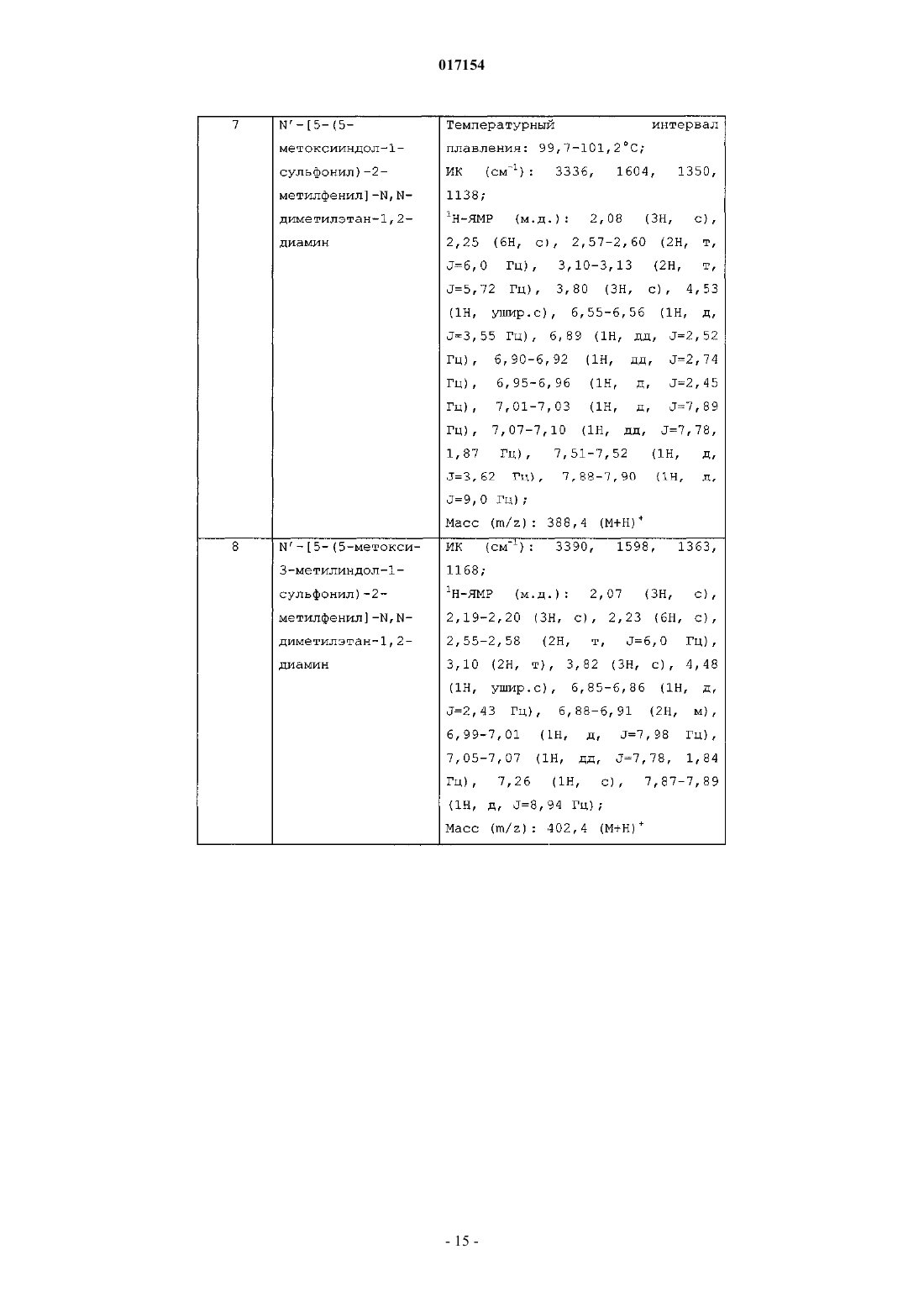
N'-[5-(5-метоксииндол-1-сульфонил)-2-метилфенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(5-метокси-3-метилиндол-1-сульфонил)-2-метилфенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(5-метоксииндол-1-сульфонил)-2-метилфенил]-N,N-диметилпропан-1,3-диамина;
N'-[3-(4-хлор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-хлор-3-метилиндол-1-сульфонил)-2-этилфенил]-N,N-диметилэтан-1,2-диамина;
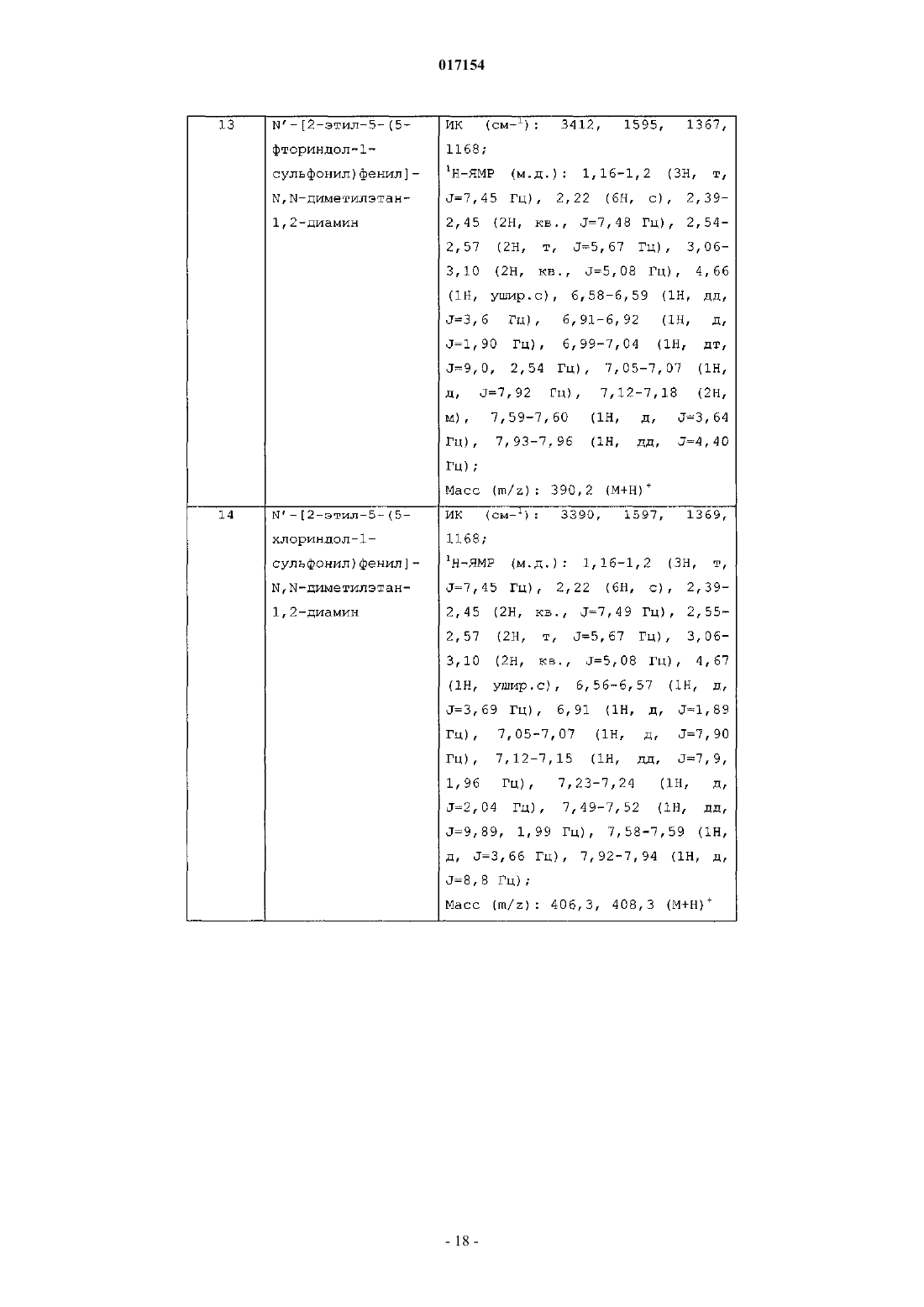
N'-[2-этил-5-(5-фтор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[2-этил-5-(5-фториндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[2-этил-5-(5-хлориндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
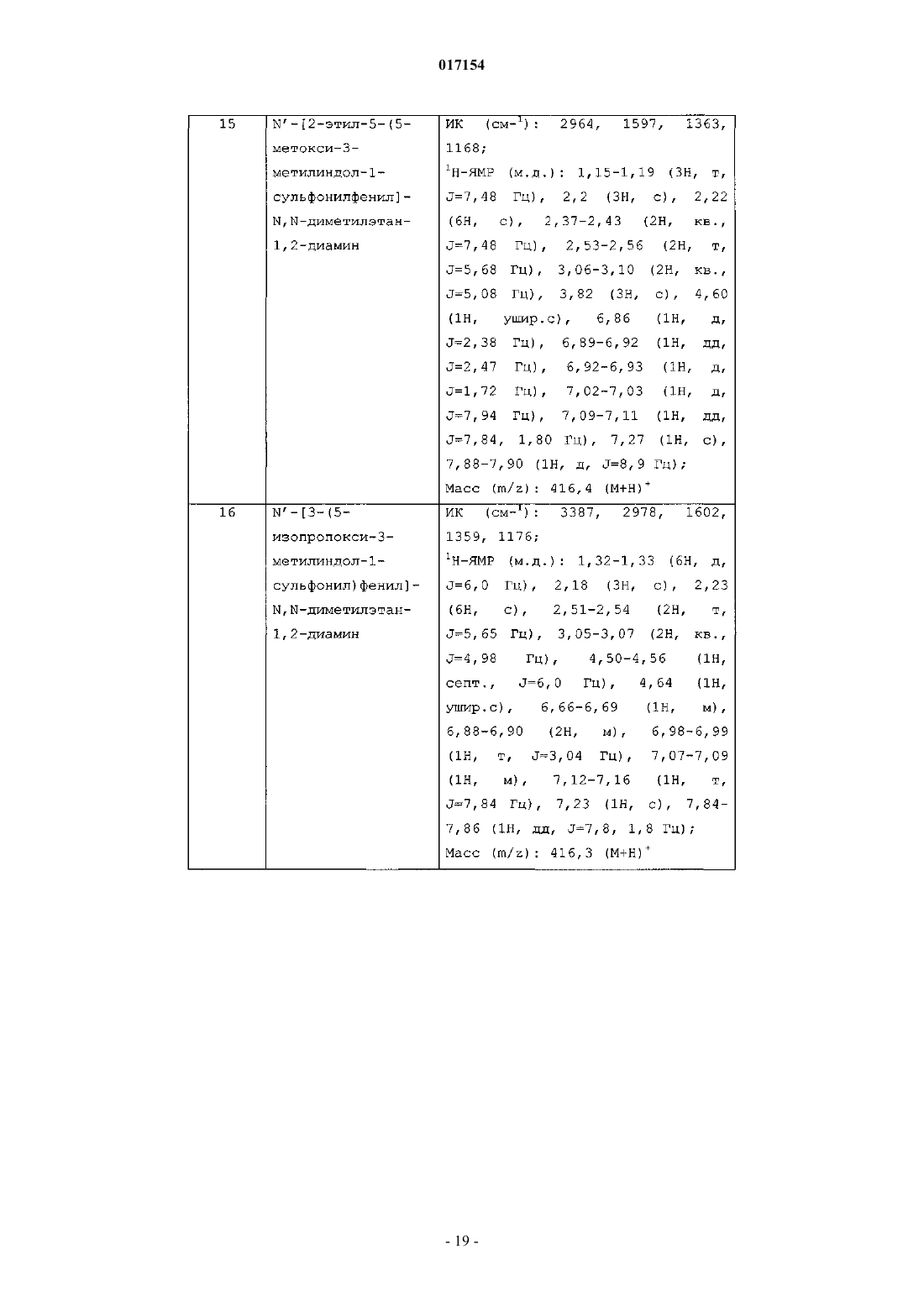
N'-[2-этил-5-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-изопропокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(5-бром-3-метилиндол-1-сульфонил)-2-хлорфенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-этокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
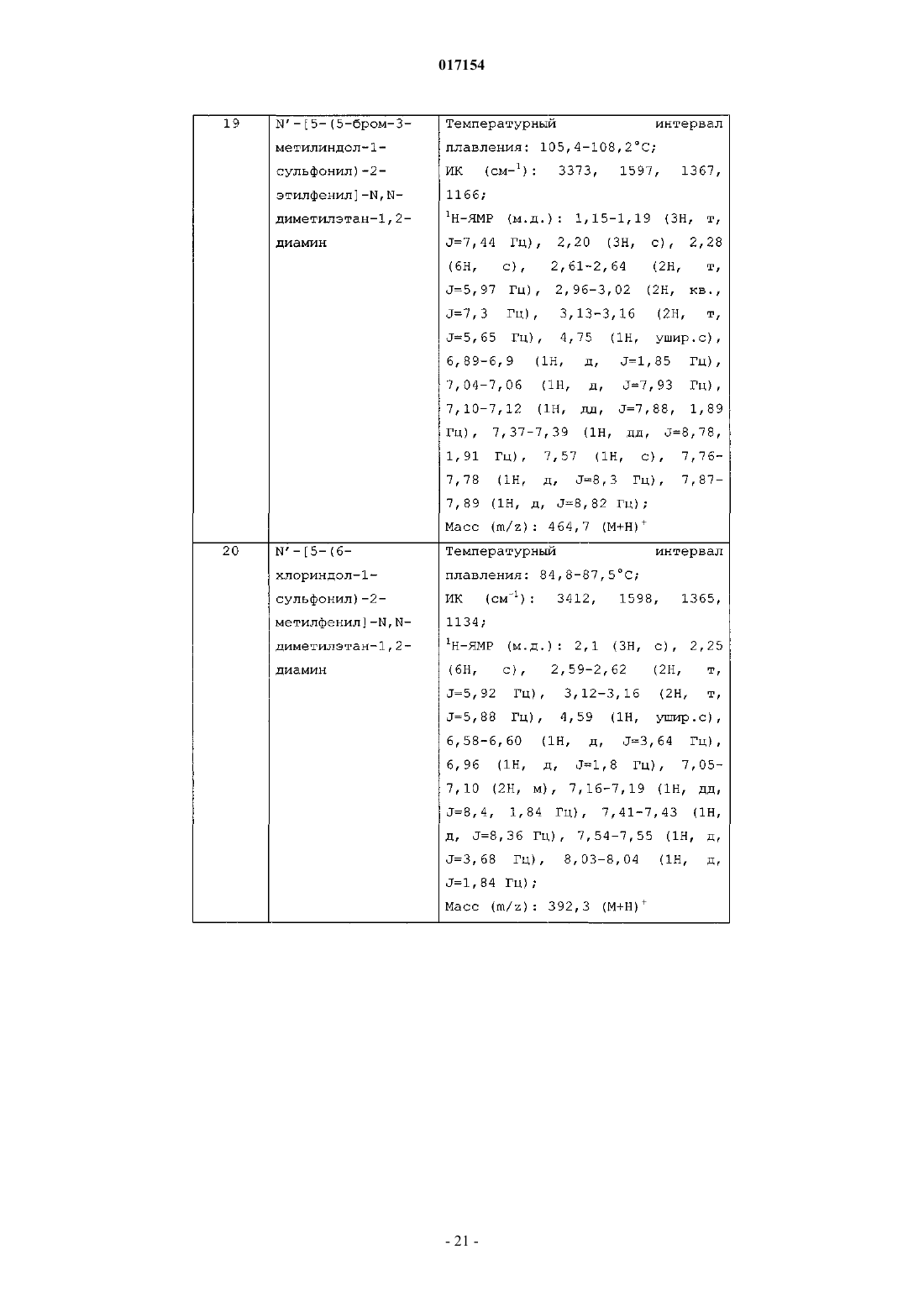
N'-[5-(5-бром-3-метилиндол-1-сульфонил)-2-этилфенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(6-хлориндол-1-сульфонил)-2-метилфенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-броминдол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамин;
N'-[3-(5-изопропоксииндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
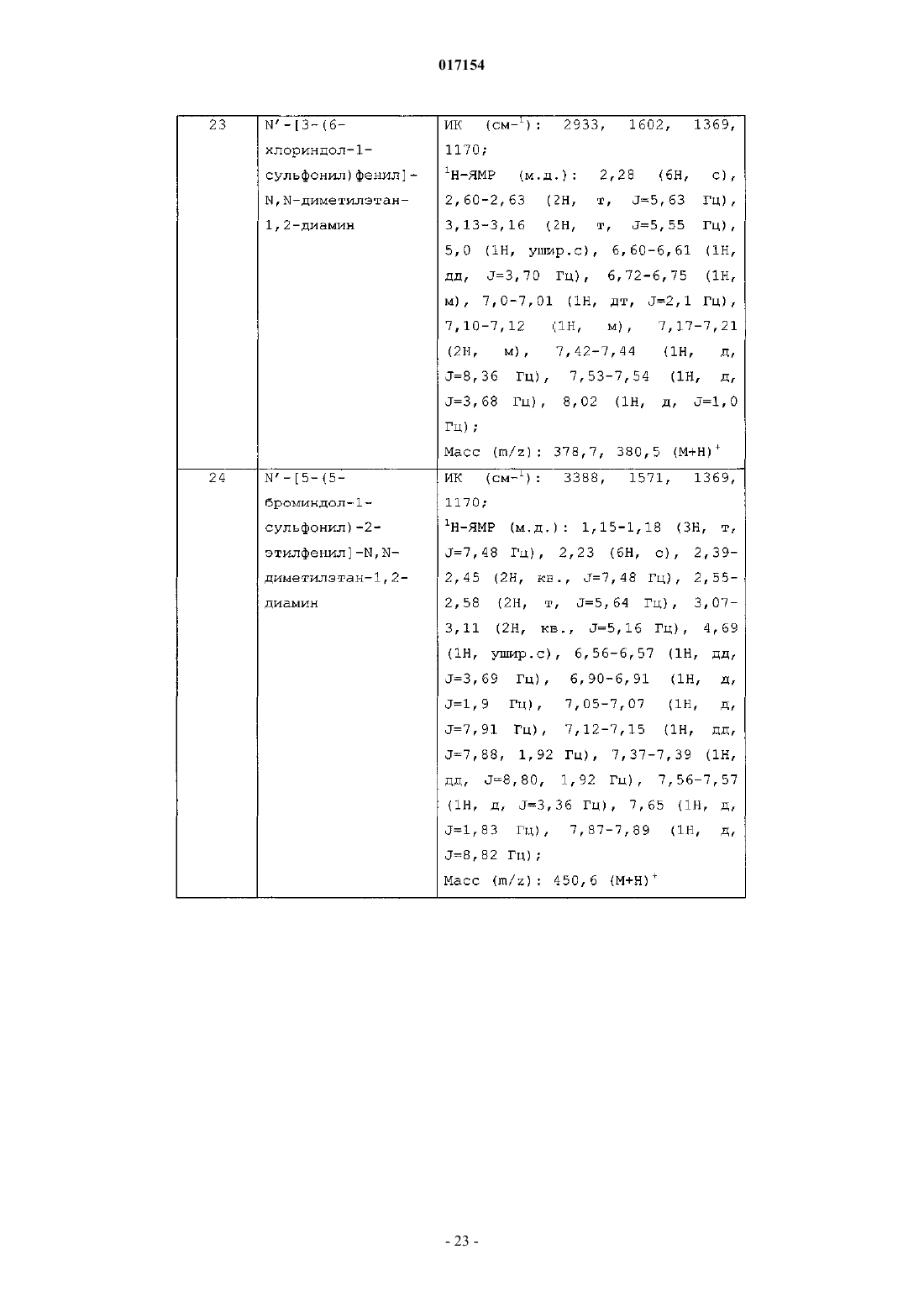
N'-[3-(6-хлориндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[5-(5-броминдол-1-сульфонил)-2-этилфенил]-N,N-диметилэтан-1,2-диамина;
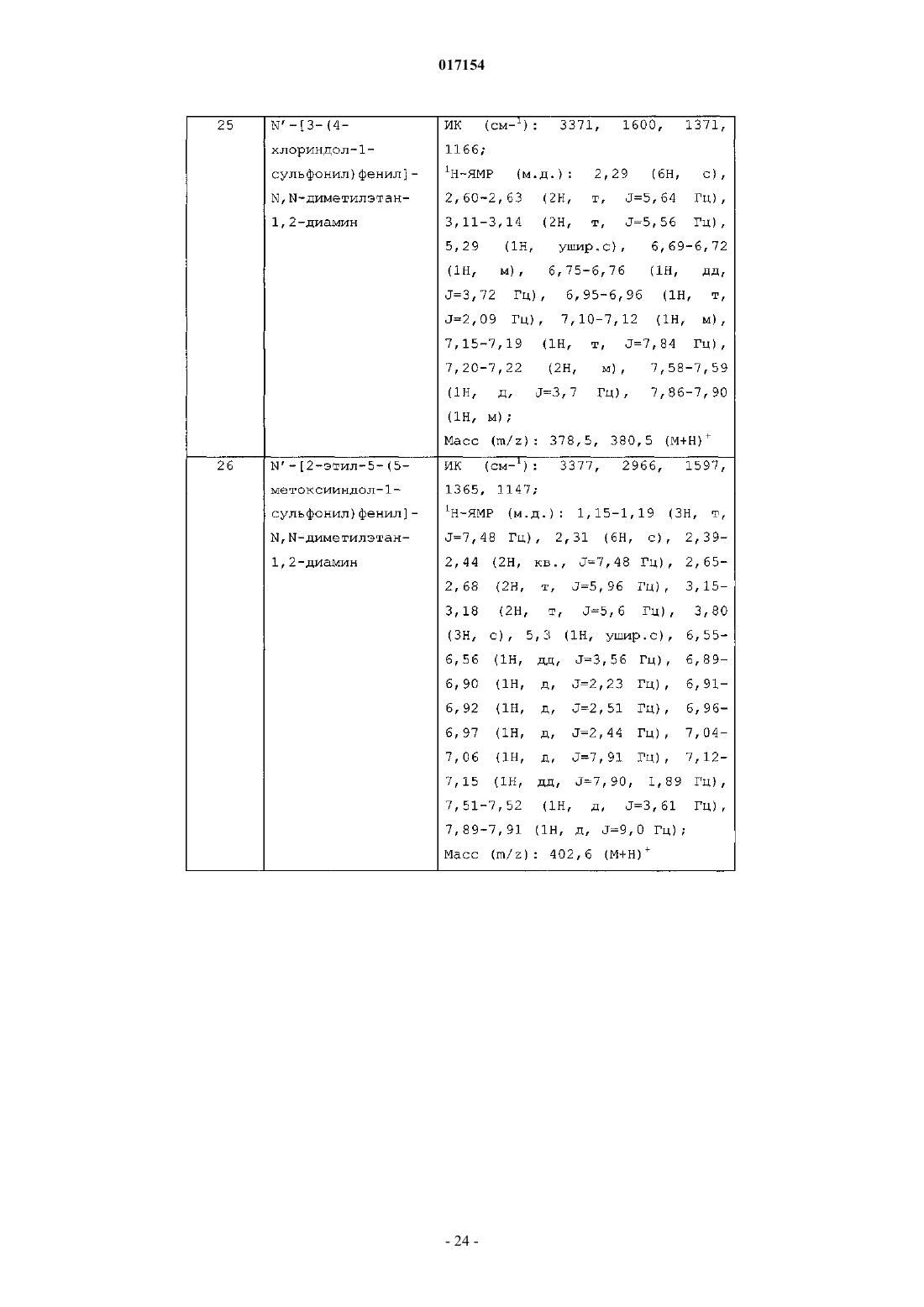
N'-[3-(4-хлориндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[2-этил-5-(5-метоксииндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
N'-[2-метокси-5-(5-хлор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[3-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[2-метокси-5-(5-хлор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
N'-[2-метокси-5-(3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
N'-[2-метокси-5-(5-бром-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
N'-[2-метокси-5-(5-фтор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
N'-[2-метокси-5-(5-фтор-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2-диамина;
N'-[2-метокси-5-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина;
и его фармацевтически приемлемые соли.
5. Способ получения соединения формулы (I) по п.1, который включает взаимодействие соединения формулы (а)

с аминовыми производными
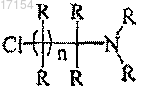
с использованием подходящего основания, в присутствии инертного растворителя, при температуре окружающей среды с получением соединения формулы (I), где все заместители соединения формулы (а), формулы (I) и аминовых производных имеют значения, определенные в п.1.
6. Способ лечения расстройства центральной нервной системы, связанного с 5-HT6 рецептором или на которое влияет 5-HT6 рецептор, у пациента, нуждающегося в этом, включающий обеспечение указанному пациенту терапевтически эффективного количества соединения формулы (I) по любому из пп.1-4.
7. Способ по п.6, где указанное расстройство представляет собой беспокойство, ухудшение познавательной способности, связанное с шизофренией, депрессию, болезнь Альцгеймера, болезнь Паркинсона, ожирение, расстройство познавательной способности, двигательное расстройство и желудочно-кишечное расстройство.
8. Применение соединения по любому из пп.1-4 для получения лекарственного средства для лечения или предотвращения заболеваний, связанных с 5-HT6 рецептором.
9. Применение по п.8 для лечения или предотвращения клинических состояний, выбранных из беспокойства, ухудшения познавательной способности, связанного с шизофренией, депрессии, болезни Альцгеймера, болезни Паркинсона, ожирения, расстройства познавательной способности, двигательного расстройства и желудочно-кишечного расстройства.
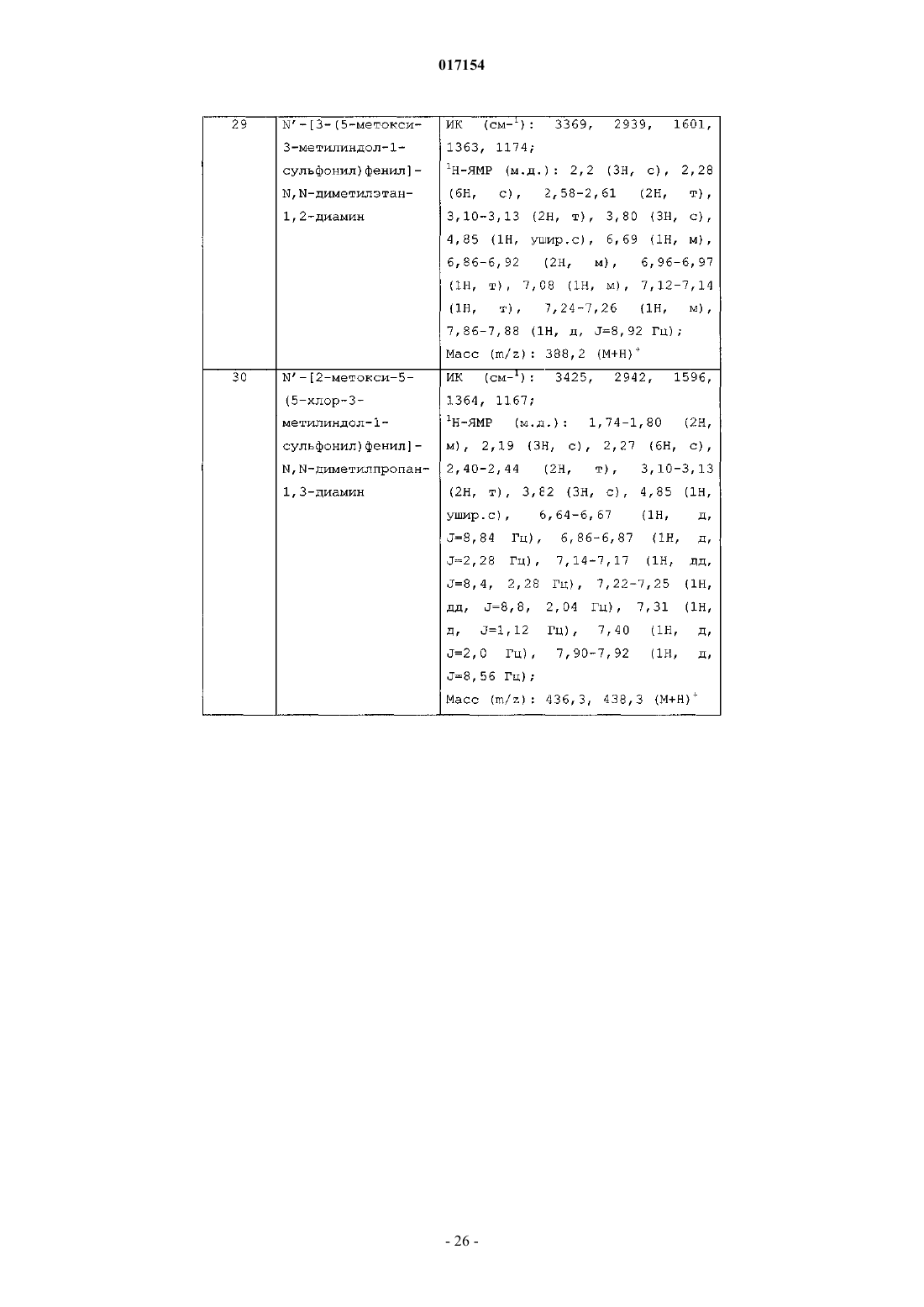
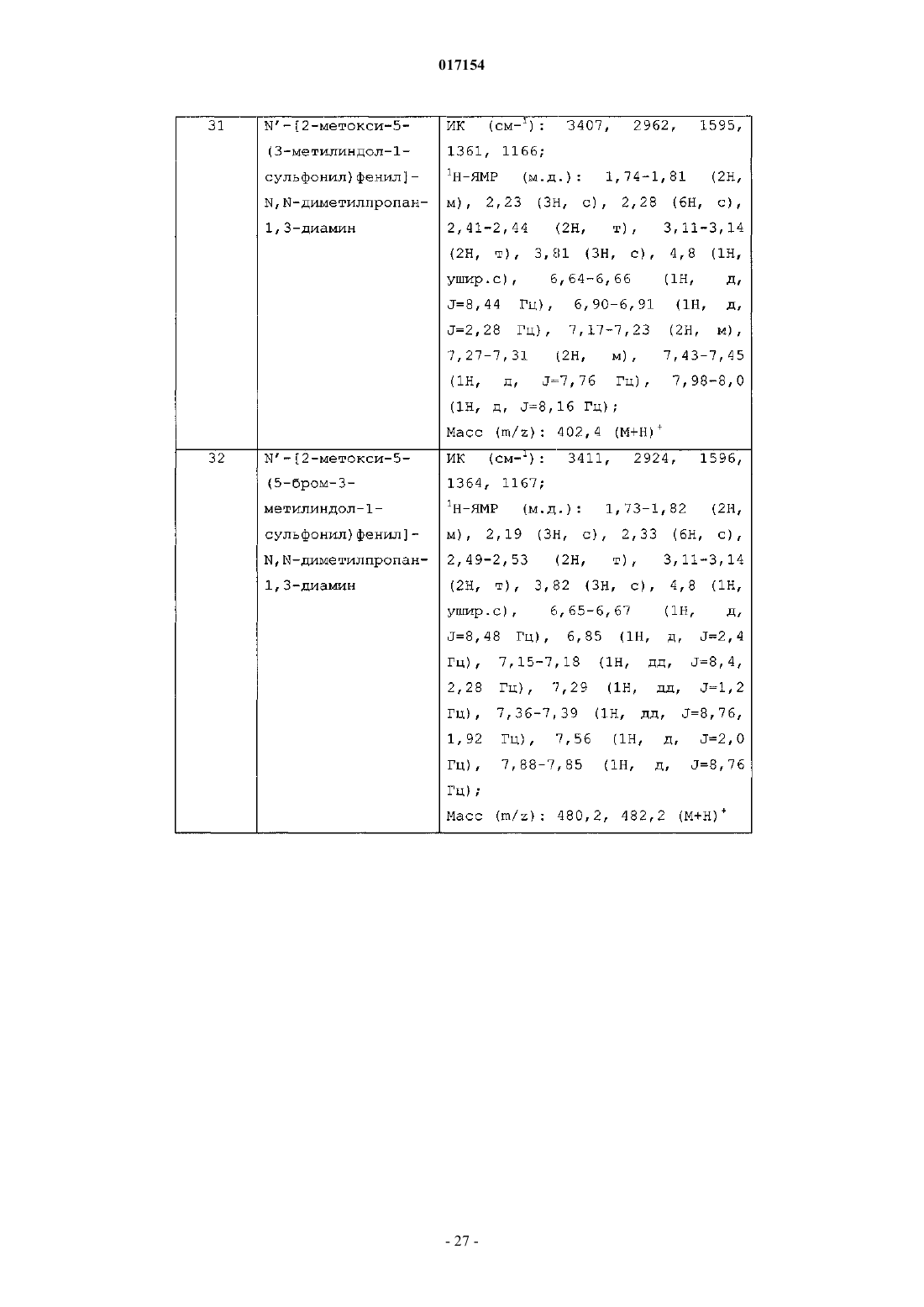
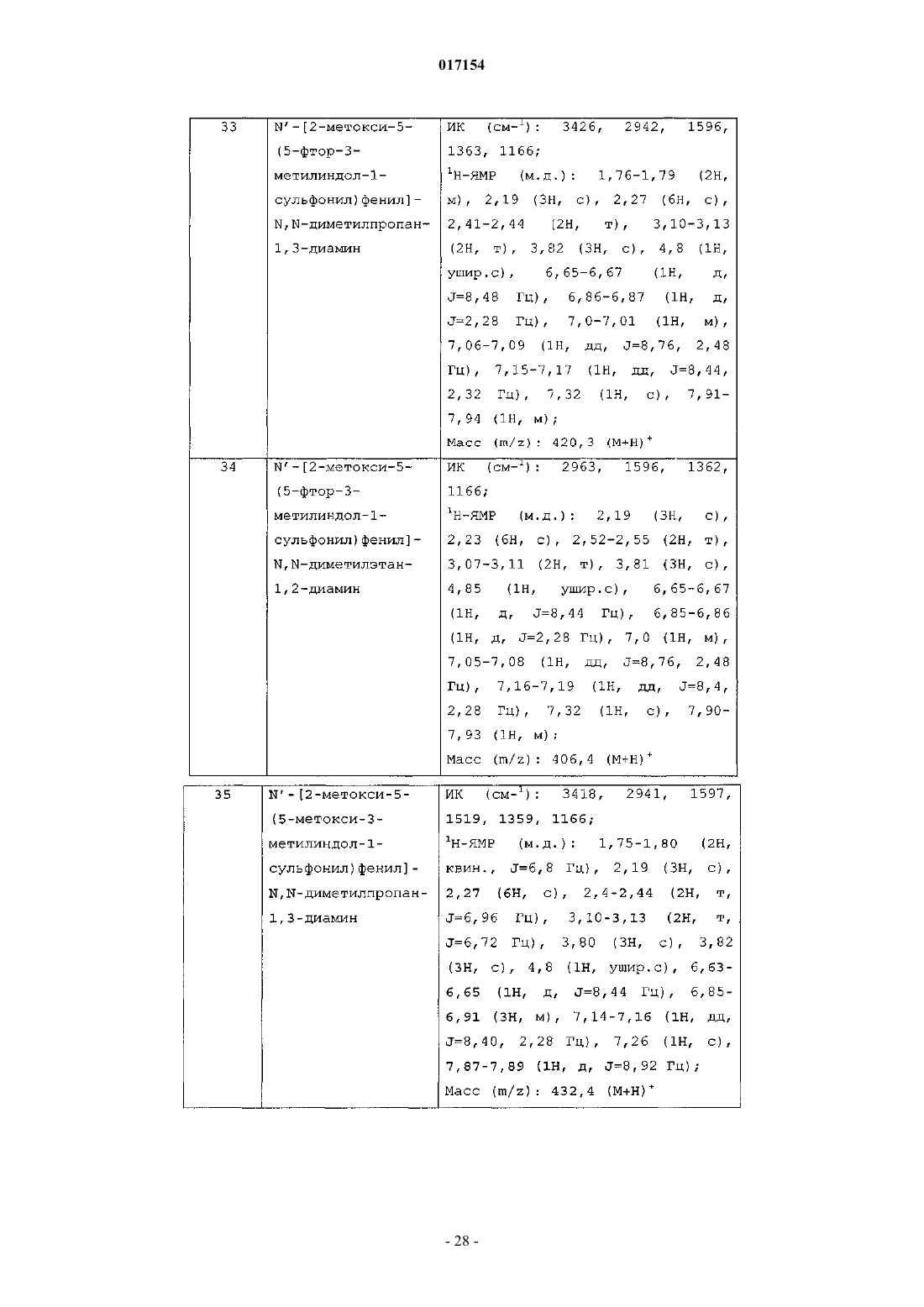
Текст
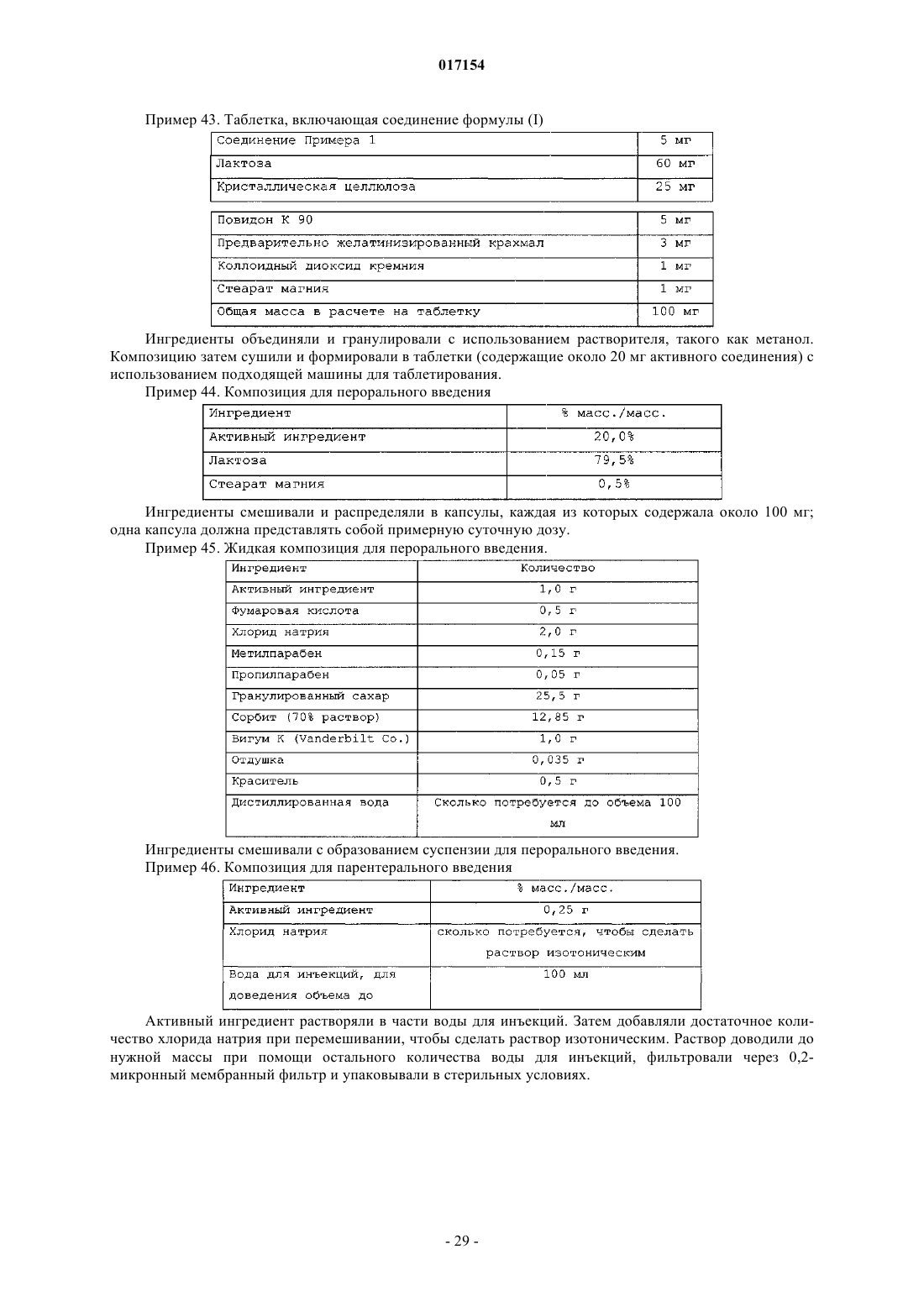
Рамакришна Нироджи Венката Сатья, Камбхампати Рама Састри,Схинде Анил Карбхари, Кандикере Нагарадж Вишвоттам, Джасти Венкатесварлу (IN) Медведев В.Н. (RU) Настоящее изобретение относится к новым аминоарилсульфонамидным соединениям формулы (I),их производным, их стереоизомерам, их фармацевтически приемлемым солям и к содержащим их фармацевтически приемлемым композициям. Настоящее изобретение также относится к способу получения указанных выше новых соединений, их производных, их стереоизомеров,их фармацевтически приемлемых солей и содержащих их фармацевтически приемлемых композиций. Соединения по настоящему изобретению являются полезными для лечения различных расстройств, которые связаны с функциями 5-HT6 рецепторов. В частности, соединения по настоящему изобретению также являются полезными для лечения различных расстройств ЦНС, гематологических расстройств, расстройств пищевого поведения, ожирения, беспокойства,депрессии, заболеваний, связанных с болью, респираторных заболеваний, желудочно-кишечных расстройств, сердечно-сосудистых заболеваний и рака.(71)(73) Заявитель и патентовладелец: СУВЕН ЛАЙФ САЙЕНСИЗ ЛИМИТЕД (IN) 017154 Область изобретения Настоящее изобретение относится к новым аминоарилсульфонамидным соединениям формулы (I),их производным, их стереоизомерам, их фармацевтически приемлемым солям и фармацевтически приемлемым композициям, содержащим такие соединения: Настоящее изобретение также относится к способу получения вышеуказанных новых соединений,их производных, их стереоизомеров, их фармацевтически приемлемых солей и фармацевтически приемлемых композиций, содержащих такие соединения. Эти соединения являются полезными для лечения различных расстройств, которые связаны с функциями 5-НТ 6 рецепторов. В частности, соединения по настоящему изобретению также являются полезными для лечения различных расстройств ЦНС, гематологических расстройств, расстройств пищевого поведения, ожирения, беспокойства, депрессии, заболеваний, связанных с болью, респираторных заболеваний, заболеваний желудочно-кишечного тракта, сердечно-сосудистых заболеваний и рака. Предпосылки изобретения Считается, что различные расстройства центральной нервной системы, такие как беспокойство, депрессия, двигательные расстройства и т.д., включают повреждение нейротрансмиттера 5 гидрокситриптамина (5-HT) или серотонина. Серотонин локализуется в центральной и периферической нервной системе, и известно, что он влияет на многие типы состояний, включая психиатрические расстройства, двигательную активность, пищевое поведение, сексуальную активность и нейроэндокринную регуляцию, среди прочих. Подтипы 5-HT рецептора регулируют различные эффекты серотонина. Известное семейство 5-HT рецепторов включает такие подтипы, как 5-HT1 семейство (например, 5-HT1A),5-HT2 семейство (например, 5-HT2A и 5-HT2C), 5-HT3, 5-HT4, 5-HT5, 5-HT6 и 5-HT7. 5-HT6 подтип рецептора был впервые клонирован из ткани крысы в 1993 г. (Monsma, F. J.; Shen, Y.;Ward, R. P.; Hamblin, M. W., Sibley, D.R., Molecular Pharmacology, 1993, 43, 320-327), а затем из ткани человека (Kohen, R.; Metcalf, M. A.; Khan, N.; Druck, Т.; Huebner, K.; Sibley, D. R., Journal of Neurochemistry, 1996, 66, 47-56). Этот рецептор представляет собрй связанный с G-белком рецептор (GPCR), положительно связанный с аденилатциклазой (Ruat, М.; Traiffort, Е.; Arrang, J-M.; Tardivel-Lacombe, L.; Diaz, L.;Leurs, R.; Schwartz, J-C, Biochemical Biophysical Research Communications, 1993, 193, 268-276). Этот рецептор присутствует почти исключительно в областях центральной нервной системы (ЦНС) как у крыс,так и у человека. Исследования in situ гибридизации 5-HT6 рецептора в головном мозге крысы с использованием мРНК показывают преимущественную локализацию в областях 5-HT проекции, включая полосатое тело,прилежащее ядро, обонятельный бугорок и структуру гиппокампа (Ward, R. P.; Hamblin, M. W.; Lachowicz, J. E.; Hoffman, В. J.; Sibley, D. R.; Dorsa, D. M., Neuroscience, 1995, 64, 1105-1111). Самые высокие уровни мРНК 5-HT6 рецептора наблюдали в обонятельном бугорке, полосатом теле, прилежащем ядре, зубчатой извилине, а также в CA1, CA2 и СА 3 областях гиппокампа. Более низкие уровни мРНК 5HT6 рецептора наблюдали в зернистом слое мозжечка, некоторых диэнцефальных ядрах, миндалевидном теле и в коре головного мозга. Методом нозерн-блоттинга было выявлено, что мРНК 5-HT6 рецептора,как оказалось, исключительно присутствует в головном мозге и мало оснований считать, что она присутствует в периферических тканях. Высокое сродство ряда антипсихотических средств в отношении 5-HT6 рецептора, локализация его мРНК в полосатом теле, обонятельном бугорке и прилежащем ядре говорит о том, что некоторые из клинических действий этих соединений могут быть опосредованы через этот рецептор. Его способность к связыванию с широким рядом терапевтических соединений, используемая в психиатрии, вместе с его интригующей дистрибуцией в головном мозге стимулировали большую заинтересованность в новых соединениях, которые способны взаимодействовать с указанным рецептором (Ref: Sleight, A.J. et al. (1997) 5-HT6 and 5-HT7 receptors: molecular biology, functional correlates and possible therapeutic indications, DrugNews Perspect. 10, 214-224). Предпринимаются существенные попытки к выяснению возможной роли 5HT6 рецептора в психиатрии, нарушении познавательной способности, двигательной функции и контроле, памяти, настроении и т.п. Предпринимаются реальные потытки поиска соединений, которые демонстрируют сродство связывания с 5-HT6 рецептором, как необходимых для исследования 5-HT6 рецептора-1 017154 и как потенциальных терапевтических средств для лечения расстройств центральной нервной системы,например, см. Reavill C. and Rogers D. C., Current Opinion in Investigational Drugs, 2001, 2(1): 104-109,Pharma Press Ltd.Monsma FJ. et al. (1993) и Kohen, R. et al. (2001) показали, что некоторые трициклические соединения, являющиеся антидепрессантами, такие как амитриптилин, и соединения, являющиеся атипичными антидепрессантами, такие как миансерин, обладают высоким сродством к 5-HT6 рецептору. Эти открытия привели к гипотезе, что 5-HT6 рецептор вовлечен в патогенез и/или лечение аффективных расстройств. Модели связанного с беспокойством поведения грызунов дают противоречивые результаты,касающиеся роли 5-HT6 рецептора в состоянии беспокойства. Лечение при помощи антагонистов 5-HT6 рецептора повышает порог судорог в испытании максимального электросудорожного раздражения крысы [Stean, Т. et al. (1999) Anticonvulsant properties of the selective 5-HT6 receptor antagonist SB-271046 in therat maximal electroshock seizure threshold test. Br. J. Pharmacol. 127, 131P; Routledge, C. et al. (2000) Characterization of SB-271046: a potent, selective and orally active 5-HT6) receptor antagonist. Br. J. Pharmacol. 130,1606-1612]. Хотя это говорит о том, что 5-HT6 рецепторы могут регулировать порог судорог, эффект не так сильно выражен, как у известных противосудорожных средств. Выяснение ролей лигандов 5-HT6 рецептора наиболее продвинулось в двух терапевтических показаниях, где этот рецептор, по-видимому, играет основную роль: дефицит запоминания и памяти и аномальное пищевое поведение. Точную роль 5-HT6 рецептора еще нужно установить в других ЦНС показаниях, таких как беспокойство; хотя один 5-HT6 агонист недавно достиг Фазы I клинических испытаний, точная роль рецептора еще не установлена, и на этом сфокусированы серьезные исследования. Существует множество потенциальных терапевтических применений лигандов 5-HT6 рецепторов для человека на основании непосредственных эффектов и показаний, полученных в результате научных исследований, которые являются доступными. Эти исследования включают локализацию рецептора, сродство лигандов с известной in-vivo активностью и различные исследования на животных, проводимые до настоящего времени. Предпочтительно пытаются найти соединения, являющиеся антагонистами 5-HT6 рецепторов, в качестве терапевтических средств. Одно потенциальное терапевтическое применение модуляторов функций 5-HT6 рецепторов имеет целью усиление познавательной способности и памяти при заболеваних человека, таких как болезнь Альцгеймера. Высокие уровни рецептора, обнаруженные в таких структурах, как передний мозг, включая хвостатое ядро/скорлуповое ядро, гиппокамп, прилежащее ядро и кору головного мозга, говорит о роли этого рецептора в памяти и познавательной способности, поскольку известно, что эти области играют ключевую роль в памяти (Gerard, C.; Martres, M.P.; Lefevre, K.; Miquel, M. C; Verge, D.; Lanfumey,R.; Doucet, E.; Hamon, M.; EI Mestikawy, S., Brain Research, 1997, 746, 207-219). Способность известных лигандов 5-HT6 рецепторов усиливать холинергическую трансмиссию также подтверждает потенциальное применение для улучшения познавательной способности (Bentley, J. С; Boursson, A.; Boess, F. G.;Kone, F. C; Marsden, C. A.; Petit, N.; Sleight, A. J., British Journal of Pharmacology, 1999, 126 (7), 15371542). Исследования выявили, что известный селективный антагонист 5-HT6 существенно повышает уровни глутамата и аспартата во фронтальной области коры головного мозга без повышения уровней норадреналина, допамина или 5-HT. Это селективное повышение некоторых нейрохимических веществ,которое отмечается в процессе памяти и распознавания, убедительно говорит о роли 5-НТ 6 лигандов в познавательной способности (Dawson, L.А.; Nguyen, H. Q.; Li, P. British Journal of Pharmacology, 2000,130 (1), 23-26). Проводимые на животных исследования памяти и запоминания с использованием известного селективного антагониста 5-HT6 имеют некоторые положительные эффекты (Rogers, D.C; Hatcher,P. D.; Hagan, J. J. Society of Neuroscience, Abstracts, 2000, 26, 680). Связанное с этим потенциальное терапевтическое применение для лигандов 5-HT6 - это применение для лечения расстройств дефицита внимания (ADD, также известных как расстройство дефицита внимания/гиперактивности, или ADHD) у детей, а также взрослых. Поскольку, как оказалось, антагонисты 5HT6 усиливают активность нигростриарного допаминового пути, и ADHD связывают с аномальностями в хвостатом ядре (Ernst, M.; Zametkin, A. J.; Matochik, J. H.; Jons, P. A.; Cohen, R. M., Journal of Neuroscience, 1998, 18(15), 5901-5907), антагонисты 5-HT6 могут ослаблять расстройства дефицита внимания. В настоящее время существует несколько полностью селективных агонистов. Wyeth агонист WAY181187 в настоящее время находится в Фазе I испытаний его направленного действия на состояние беспокойства [Cole, D.C. et al. (2005) Discovery of a potent, selective and orally active 5-HT6 receptor agonist,WAY-181187. 230th ACS Natl. Meet. (Aug 28-Sept 1, Washington DC), Abstract MEDI 17.] В международной патентной публикации WO 03/066056 A1 сообщается, что антагонизм в отношении 5-HT6 рецептора может способствовать росту нейронов в центральной нервной системе млекопитающего. В другой Международной Патентной Публикации WO 03/065046 А 2 раскрывается новый вариант рецептора 5-HT6 человека и предполагается, что 5-HT6 рецептор связан с различными другими расстройствами. Первоначальные исследования, изучающие сродство различных ЦНС лигандов с известной терапевтической применимостью или высокой структурной схожестью с известными лекарственными сред-2 017154 ствами предполагают роль 5-HT6 лигандов в лечении шизофрении и депрессии. Например, клозапин(эффективное клиническое антипсихотическое средство) обладает высоким сродством в отношении 5HT6 подтипа рецептора. Также некоторые клинические антидепрессанты обладают высоким сродством к рецептору и действуют как антагонисты на этом участке (Branchek, T. A.; Blackburn, T. P., Annual Reviews in Pharmacology and Toxicology, 2000, 40, 319-334). Кроме того, проводимые в последнее время in-vivo исследования на крысах показывают, что модуляторы 5-HT6 могут быть полезными для лечения двигательных расстройств, включая эпилепсию (Stean,T.; Routledge, С.; Upton, N., British Journal of Pharmacology, 1999, 127 Proc. Supplement-13lP; и Routledge,C.; Bromidge, S. M.; Moss, S. F.; Price, G. W.; Hirst, W.; Newman, H.; Riley, G.; Gager, Т.; Stean, Т.; Upton,N.; Clarke, S. E.; Brown, A. M., British Journal of Pharmacology, 2000, 30 (7), 1606-1612). Взятые вместе, указанные выше исследования дают веские основания для предположения, что соединения, которые являются модуляторами 5-HT6 рецепторов, т.е. лигандами, могут быть полезны для терапевтических показаний, включая лечение заболеваний, связанных с дефицитом памяти, познавательной способности и запоминания, таких как болезнь Альцгеймера и расстройство дефицита внимания; лечение расстройств изменения личности, таких как шизофрения; лечение поведенческих расстройств,например беспокойства, депрессии и обсессивно-компульсивных расстройств; лечение нарушения движений или двигательных расстройств, таких как болезнь Паркинсона и эпилепсия; лечение заболеваний,связанных с нейродегенерацией, таких как удар или травма головы, или синдром отмены привыкания к чрезмерному употреблению лекарственных средств, в том числе привыкания к никотину, алкоголю и другим веществам, вызывающим зависимость. Также ожидают, что эти соединения будут полезны для лечения некоторых расстройств желудочнокишечного тракта (GI), таких как функциональное кишечное расстройство. См., например, Roth, B. L.; etal., Journal of Pharmacology and Experimental Therapeutics, 1994, 268, pages 1403-1412; Sibley, D. R.; et al.,Molecular Pharmacology, 1993, 43, 320-327, Sleight, A. J.; et al., Neurotransmission, 1995, 11, 1-5; и Sleight,A. J.; et al., Serotonin ID Research Alert, 1997, 2(3), 115-118. Кроме того, сообщалось об эффективности антагонистов 5-HT6 и 5-HT6 антисмысловых олигонуклеотидов для уменьшения потребления пищи у крыс, таким образом потенциально - для лечения ожирения. См., например, Bentey, J. С.; Boursson, A.; Boess, F. G.; Kone, F. C; Marsden, C. A.; Petit, N.; Sleight,A. J., British Journal of Pharmacology, 1999, 126 (7), 1537-1542); Wooley et al., Neuropharmacology, 2001,41: 210-129 и WO 02/098878. В недавно опубликованном обзоре Holenz, Jo"rg et al., Drug Discovery Today, 11, 7/8, April 2006, Medicinal chemistry strategies to 5-HT6 receptor ligands as potential cognitive enhancers and antiobesity agents,представлено подробное обсуждение эволюции 5-HT6 лигандов. В обзоре представлены фармакологические инструменты и предклинические кандидаты, используемые в оценке рецептора 5-HT6 в таких заболеваниях, как шизофрения, другие связанные с допамином расстройства и депрессия, и для профилирования нейрохимических и электрофизиологических эффектов как блокады, так и активации 5-HT6 рецепторов. Кроме того, их использовали для характеристики 5-HT6 рецептора и исследования его дистрибуции. В настоящее время некоторые клинические кандидаты образуют часть структур индольного типа и структурно тесно связаны с эндогенным лигандом 5-HT, например, соединения, раскрытые в Glennon,R.A. et al., 2-замещенные триптамины: агенты с селективностью в отношении 5-HT6 рецепторов серотонина, J. Med. Chem. 43, 1011-1018, 2000; Tsai, Y. et al., N1-(бензолсульфонил)триптамины в качестве новых антагонистов 5-НТ 6, Bioorg. Med. Chem. Lett. 10, 2295-2299, 2000; Demchyshyn L. et al., ALX-1161: фармакологические свойства сильного и селективного антагониста 5-HT6 рецептора, 31st Annu. Meet.et al., 2-алкил-3-(1,2,3,6-тетрагидропиридин-4-ил)-1 Н-индолы в качестве новых агонистов 5-НТ 6 рецептора, Bioorg. Med. Chem. Lett. 15, 4230-4234, 2005]. Структурно-функциональные взаимосвязи описаны в разделе, относящемся к индолоподобным структурам (и в исследовании с моделированием рецептора, в котором Pullagurla et al. заявляют различные сайты связывания для агонистов и антагонистов [Pullagurla, M.R. et al. (2004) Possible differences inmodes of aginist and antagonist binding at human 5-HT6 receptors. Bioorg. Med. Chem. Lett. 14, 4569-4573]. Большинство антагонистов, о которых были сообщения, образуют часть моноциклических, бициклических и трициклических арилпиперазиновых классов [Bromidge, S.M. et al., (1999) 5-Хлор-N-(4-метокси-3 пиперазин-1-илфенил)-3-метил-2-бензотиофенсульфонамид (SB-271046): Сильный, селективный и перорально биодоступный антагонист 5-HT6 рецептора. J. Med. Chem. 42, 202-205; Bromidge, S.M. et al.(2001). Фенилбензолсульфонамиды являются новыми и селективными антагонистами 5-HT6: Идентификация N-(2,5-дибром-3-фторфенил)-4-метокси-3-пиперазин-1-илбензолсульфонамида (SB-357134). Bioorg. Med. Chem. Lett. 11, 55-58; Hirst, W.D. et al. (2003). Идентификация SB-399885, сильного и селективного антагониста 5-НТ 6 рецептора. 33rd Annu. Meet. Soc. Neurosci. (Nov. 8-12, New Orleans), Abstract-3 017154 576.7; Stadler, H. et al. (1999) антагонисты 5-HT6: Новый подход к симптоматическому лечению болезни Альцгеймера. 37th IUPAC Cong. Berlin, Abstract MM-7; Bonhaus, D. W. et al. (2002) Ro-4368554, высокоаффинный, селективный, проникающий в ЦНС антагонист 5-HT6 рецептора. 32nd Annu. Meet. Soc. Neurosci., Abstract 884.5.; Beard, C.C. et al. (2002). Получение новых индольных производных со сродством к 5HT6 рецептору. WO патент 2002098857].Ro 63-0563: Сильные и селективные антагонисты на 5-HT6 рецепторах человека и крысы. Br. J.Pharmacol. 124, (556-562). Антагонист-кандидат от компании GlaxoSmithKline, SB-742457, находящийся в фазе II испытаний по такому терапевтическому показанию, как нарушение познавательной способности, связанное с болезнью Альцгеймера [Ahmed, M. et al. (2003). Новые соединения. WO патент 2003080580] и соединение LY-483518 от компании Lilly [Filla, S.A. et al. (2002). Получение индол-5 иловых эфиров бензолсульфоновой кислоты в качестве антагонистов 5-HT6 рецептора. WO 2002060871]. Клиническая разработка SB-271046, первого антагониста 5-HT6 рецептора, поступившего в фазу I испытаний, была приостановлена (возможно из-за низкой пенетрации через гематоэнцефалический барьер). Кроме того, SB-271046, селективный антагонист 5-HT6 рецептора оказался неактивным в испытаниях на животных, связанных либо с положительными, либо с отрицательными симптомами шизофрении[Pouzet, В. et al. (2002) Эффекты антагониста 5-HT6 рецептора, SB-271046, в животных моделях шизофрении. Pharmacol. Biochem. Behav. 71, 635-643]. Международные патентные публикации WO 2004/055026 A1, WO 2004/048331 A1, WO 2004/048330A1 и WO 2004/048328 А 2 (все принадлежащие Suven Life Sciences Limited) описывают соответствующий известный уровень техники. Кроме того, WO 98/27081, WO 99/02502, WO 99/37623, WO 99/42465 и WO 01/32646 (все принадлежащие Glaxo SmithKline Beecham PLC) раскрывают ряд арил-сульфонамидных и сульфоксидных соединений в качестве антагонистов 5-HT6 рецепторов, которые заявлены как полезные для лечения различных расстройств ЦНС. Несмотря на то, что к настоящему времени раскрыты некоторые модуляторы 5-HT6, остается потребность в соединениях, которые являются полезными для модуляции 5-HT6. К удивлению, было обнаружено, что аминоарилсульфонамидные соединения формулы (I) демонстрируют очень высокое сродство к 5-HT6 рецептору. Поэтому целью настоящего изобретения является обеспечение соединений, которые являются полезными в качестве терапевтических средств для различных расстройств центральной нервной системы или расстройств, на которые влияет 5-HT6 рецептор. Задача настоящего изобретения Основной задачей настоящего изобретения является создание соединения формулы (I) Другой задачей настоящего изобретения является разработка способа получения соединения формулы (I), включающего контактирование соединения формулы (а) с аминовыми производными, с использованием подходящего основания, в присутствии инертного растворителя, при температуре окружающей среды. Еще одной задачей настоящего изобретения является создание фармацевтической композиции,включающей соединение формулы (I). Следующей задачей настоящего изобретения является создание соединения формулы (I) для использования в получении лекарственного средства для лечения или предотвращения заболеваний или-4 017154 расстройств центральной нервной системы, связанных с 5-HT6 рецептором или на которые влияет 5-HT6 рецептор. Следующей задачей настоящего изобретения является создание средства для предотвращения или лечения заболевания или расстройства центральной нервной системы, связанного с 5-HT6 рецептором или на которое влияет 5-HT6 рецептор, включающего в качестве активного ингредиента соединение формулы (I). Краткое описание изобретения Соответственно, настоящее изобретение относится к соединению формулы (I)R представляет собой водород или (C1-C3)алкил или (C3-C6)циклоалкил; предпочтительно R представляет собой водород или (C1-C3)алкил"n" имеет значение от 0 до 4;"p" имеет значение от 0 до 6;"q" имеет значение от 0 до 4. Настоящее изобретение также относится к способу получения соединения формулы (I)R представляет собой водород или (C1-C3)алкил или (C3-C6)циклоалкил;"n" имеет значение от 0 до 4;"p" имеет значение от 0 до 6;"q" имеет значение от 0 до 4; включающему контактирование соединения формулы (а) где все заместители имеют значение, указанное выше; с аминовыми производными, с использованием подходящего основания, в присутствии инертного растворителя, при температуре окружающей среды; где указанное основание выбрано из карбоната калия и гидроксида натрия; где указанный инертный растворитель выбран из дихлорметана, диметилформамида, диметилсульфоксида и м-ксилола. Настоящее изобретение, кроме того, относится к фармацевтической композиции, включающей соединение формулы (I) и фармацевтически приемлемый носитель, разбавитель, эксципиент или сольват. В одном варианте воплощения фармацевтическая композиция по настоящему изобретению находится в форме таблетки, капсулы, порошка, сиропа, раствора, препарата для инъекций или суспензии,вводимых в виде разовой дозы или нескольких дозируемых единиц. В другом варианте воплощения настоящего изобретения фармацевтическую композицию используют для лечения заболеваний или расстройств центральной нервной системы, связанных с 5-HT6 рецептором или на которые влияет 5-HT6 рецептор, выбранных из группы, включающей двигательное расстройство, беспокойство, расстройство познавательной способности, нейродегенеративное расстройство,болезнь Альцгеймера, хорею Гентингтона, желудочно-кишечное расстройство, ухудшение познавательной способности, связанное с шизофренией, слабовыраженное ухудшение познавательной способности,расстройства пищевого поведения, беспокойство, депрессию, ожирение и/или болезнь Паркинсона. Еще в одном варианте воплощения настоящего изобретения соединение формулы (I) используют для получения лекарственного средства для лечения или предотвращения заболеваний или расстройств центральной нервной системы, связанных с 5-HT6 рецептором или на которые влияет 5-HT6 рецептор,выбранных из группы, включающей двигательное расстройство, беспокойство, расстройство познавательной способности, нейродегенеративное расстройство, болезнь Альцгеймера, хорею Гентингтона,желудочно-кишечное расстройство, ухудшение познавательной способности, связанное с шизофренией,расстройства пищевого поведения, беспокойство, депрессию, ожирение и/или болезнь Паркинсона. В следующем варианте воплощения настоящего изобретения обеспечивается средство для предотвращения или лечения заболевания или расстройства центральной нервной системы, связанного с 5-HT6 рецептором или на которое влияет 5-HT6 рецептор, выбранное из группы, включающей двигательное расстройство, беспокойство, расстройство познавательной способности, нейродегенеративное расстройство, болезнь Альцгеймера, хорею Гентингтона, желудочно-кишечное расстройство, ухудшение познавательной способности, связанное с шизофренией, расстройства пищевого поведения, беспокойство, депрессию, ожирение и/или болезнь Паркинсона; включающее в качестве активного ингредиента соединение формулы (I). В частности, соединения по настоящему изобретению также являются полезными для лечения различных расстройств ЦНС, гематологических расстройств, расстройств пищевого поведения, ожирения,беспокойства, депрессии, заболеваний, связанных с болью, респираторных заболеваний, желудочнокишечных расстройств, сердечно-сосудистых заболеваний и рака. В другом аспекте настоящее изобретение относится к фармацевтическим композициям, содержащим терапевтически эффективное количество по меньшей мере одного соединения формулы (I) или индивидуальных стереоизомеров, рацемической или нерацемической смеси стереоизомеров или их фармацевтически приемлемых солей или сольватов в смеси по меньшей мере с одним подходящим носителем. В другом аспекте настоящее изобретение относится к композициям, включающим соединения формулы (I), и к способам, использующим такие соединения. В следующем аспекте настоящее изобретение относится к использованию терапевтически эффективного количества соединения формулы (I) для получения лекарственного средства, для лечения или предотвращения расстройства с вовлечением селективного сродства в отношении 5-HT6 рецептора. В следующем аспекте настоящее изобретение относится к способу лечения расстройства центральной нервной системы, связанного с 5-HT6 рецептором или на которое влияет 5-HT6 рецептор, у пациента,нуждающегося в этом, включающему обеспечение для указанного пациента терапевтически эффективного количества соединения формулы (I), где указанное расстройство выбрано из группы, включающей двигательное расстройство, беспокойство, расстройство познавательной способности, нейродегенеративное расстройство, болезнь Альцгеймера, хорею Гентингтона, желудочно-кишечное расстройство,ухудшение познавательной способности, связанное с шизофренией, расстройства пищевого поведения,беспокойство, депрессию, ожирение и/или болезнь Паркинсона.-6 017154 Еще в одном аспекте, настоящее изобретение, кроме того, относится к способу получения соединений формулы (I). Далее представлен частичный перечень соединений, относящихся к общей формуле (I). Соединение, заявленное в п.1 формулы изобретения, которое выбрано из группы, состоящей изN'-[2-метокси-5-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилпропан-1,3-диамина; их стереоизомеры; и их фармацевтически приемлемые соли. Подробное описание изобретения Если не указано иное, следующие термины, используемые в описании и формуле изобретения,имеют значения, указанные ниже:"(C1-C3)алкил" означает алкильные радикалы с прямой или разветвленной цепью, содержащие от одного до трех атомов углерода, и включает метил, этил, н-пропил и изопропил;"(C1-C3)алкокси" означает алкильные радикалы, содержащие от одного до трех атомов углерода, и включает метокси, этокси, пропилокси и изопропилокси;"Галоген(C1-C3)алкил" означает линейные или разветвленные алкильные радикалы с прямой или разветвленной цепью, содержащие от одного до трех атомов углерода, и включает фторметил, дифторметил, трифторметил, трифторэтил, фторэтил, дифторэтил и т.п.;"Галоген(C1-C3)алкокси" означает алкильные радикалы с прямой или разветвленной цепью, содержащие от одного до трех атомов углерода, и включает фторметокси, дифторметокси, трифторметокси,трифторэтокси, фторэтокси, дифторэтокси и т.п.;"Цикло(С 3-С 6)алкил" означает циклические или разветвленные циклические алкильные радикалы,содержащие от трех до шести атомов углерода, и включает циклопропил, циклобутил, циклопентил,циклопропилметил, цикло(C3-C6)алкилметил или циклогексил, которые могут быть замещенными или незамещенными, и, необязательно, заместители могут быть выбраны из галогена, (C1-C3)алкила или (C1C3)алкокси;"Цикло(C3-C6)алкокси" означает циклические или разветвленные циклические алкильные радикалы,содержащие от трех до шести атомов углерода, и включает циклопропилокси, циклобутилокси, циклопентилокси, циклопропилметокси или циклогексилокси.-7 017154 Термин "шизофрения" означает шизофрению, шизофрениформное расстройство, шизоаффективное расстройство и психотическое расстройство, где термин "психотический" относится к бреду, заметным галлюцинациям, нарушению речи или дезорганизованному или кататоническому поведению. См. Diagnostic and Statistical Manual of Mental Disorder, fourth edition, American Psychiatric Association, Washington,D.C. Фраза "фармацевтически приемлемый" указывает, что вещество или композиция должны быть совместимы химически и/или токсикологически с другими ингредиентами, составляющими композицию,предназначенную для лечения млекопитающего."Терапевтически эффективное количество" определяется как количество соединения по настоящему изобретению, которое (i) лечит или предотвращает конкретное заболевание, состояние или расстройство, (ii) уменьшает, ослабляет или устраняет один или несколько симптомов конкретного заболевания,состояния или расстройства, (iii) предотвращает или замедляет начало развития одного или нескольких симптомов конкретного заболевания, состояния или расстройства, описанного в настоящем изобретении. Термины "лечащий", "лечить" или "лечение" охватывают все значения, такие как превентивное,профилактическое и паллиативное. Термин "стереоизомеры" является общим термином для всех изомеров индивидуальных молекул,которые отличаются только ориентацией их атомов в пространстве. Он включает зеркальные изомеры(энантиомеры), геометрические (цис-транс) изомеры и изомеры соединений с более чем одним хиральным центром, которые не являются зеркальным отражением друг друга (диастереомеры). Некоторые соединения формулы (I) могут существовать в стереоизомерных формах (например,диастереомеры и энантиомеры), и настоящее изобретение распространяется на каждую из этих стереоизомерных форм и на их смеси, включая рацематы. Разные стереоизомерные формы можно отделить друг от друга обычными способами, или любой определенный изомер можно получить путем стереоспецифического или асимметрического синтеза. Изобретение распространяется также на таутомерные формы и их смеси. Стереоизомеры, как правило, получают в виде рацематов, которые могут быть разделены на оптически активные изомеры способом, известным per se. В случае соединений общей формулы (I), содержащих асимметрический атом углерода, настоящее изобретение относится к D-форме, L-форме и D,Lсмесям, а в случае нескольких асимметрических атомов углерода, диастереомерные формы и изобретение распространяются на каждую из этих стереоизомерных форм и на их смеси, включая рацематы. Те соединения общей формулы (I), которые содержат асимметрический углерод и которые, как правило,получают в виде рацематов, можно отделить друг от друга обычными способами, или любой определенный изомер можно получить путем стереоспецифического или асимметрического синтеза. Однако можно также использовать оптически активное соединение с самого начала, с получением затем соответственно оптически активного энантиомерного или диастереомерного соединения в виде конечного соединения. Стереоизомеры соединений общей формулы (I) можно получить одним или несколькими представленными ниже путями:i) Один или несколько из реагентов можно использовать в их оптически активной форме.ii) Оптически чистый катализатор или хиральные лиганды вместе с металлическим катализатором можно использовать в способе восстановления. Металлический катализатор может представлять собой родий, рутений, иридий и т.п Хиральные лиганды предпочтительно могут представлять собой хиральные фосфины (Principles of Asymmetric synthesis, J. E. Baldwin Ed., Tetrahedron series, 14, 311-316).iii) Смесь стереоизомеров можно разделить традиционными способами, такими как образование диастереомерных солей с хиральными кислотами или хиральными аминами, или хиральными аминоспиртами, хиральными аминокислотами. Полученную смесь диастереомеров затем можно разделить такими способами, как фракционированная кристаллизация, хроматография и т.п., после чего следует дополнительная стадия выделения оптически активного продукта путем гидролиза производного (Jacquesiv) Смесь стереоизомеров можно разделить традиционными способами, такими как микробное разделение, разделение диастереомерных солей, образованных с хиральными кислотами или хиральными основаниями. Хиральные кислоты, которые можно использовать, могут представлять собой винную кислоту,миндальную кислоту, молочную кислоту, камфорсульфоновую кислоту, аминокислоты и т.п. Хиральные основания, которые можно использовать, могут представлять собой алкалоиды хинного дерева, бруцин или основную аминокислоту, такую как лизин, аргинин и т.п. В случае соединений общей формулы (I),содержащих геометрическую изомерию, настоящее изобретение относится ко всем таким геометрическим изомерам. Подходящие фармацевтически приемлемые соли должны быть очевидны для специалистов в данной области и включают соли, описанные в J. Pharm. Sci., 1977, 66, 1-19, такие как кислотно-аддитивные соли, образованные с неорганическими кислотами, например хлористо-водородной, бромистоводородной, серной, азотной или фосфорной кислотой; и органическими кислотами, например янтарной,-8 017154 малеиновой, уксусной, фумаровой, лимонной, винной, бензойной, п-толуолсульфоновой, метансульфоновой или нафталинсульфоновой кислотой. Настоящее изобретение включает как входящие в его объем,все возможные стехиометрические и нестехиометрические формы. Фармацевтически приемлемые соли, образующие часть настоящего изобретения, можно получить путем обработки соединения формулы (I) 1-6 эквивалентами основания, такого как гидрид натрия, метоксид натрия, этоксид натрия, гидроксид натрия, трет-бутоксид калия, гидроксид кальция, ацетат кальция, хлорид кальция, гидроксид магния, хлорид магния и т.п Можно использовать растворители, такие как вода, ацетон, простой эфир, ТГФ, метанол, этанол, трет-бутанол, диоксан, изопропанол, изопропиловый эфир или их смеси. В дополнение к фармацевтически приемлемым солям, другие соли включены в настоящее изобретение. Они могут служить в качестве промежуточных соединений при очистке соединений, для получения других солей или для идентификации и исследования соединений или промежуточных соединений. Соединения формулы (I) можно получить в кристаллической или некристаллической форме и, в случае кристаллической формы, они, необязательно, могут быть сольватированными, например, в виде гидрата. В объем настоящего изобретения включены стехиометрические сольваты (например, гидраты), а также соединения, содержащие различные количества растворителя (например, вода). Настоящее изобретение также обеспечивает способ получения соединения формулы (I) или его фармацевтически приемлемой соли, который включает следующий путь, где ключевое промежуточное соединение синтезируют, как описано в получении 2. Способ по настоящему изобретению включает контактирование соединения представленной ниже формулы (а) с аминовыми производными, в присутствии инертного растворителя, при температуре окружающей среды с получением соединения формулы (I), где все заместители определены выше. Указанную выше реакцию предпочтительно осуществляют в растворителе, таком как тетрагидрофуран (ТГФ), толуол, этилацетат, вода, диметилформамид (DMF), диметилсульфоксид (DMSO), диметиловый эфир (DME), спирты, такие как метанол, этанол, н-пропанол, н-бутанол, трет-бутанол, и ароматические углеводороды, такие как толуол, о-, м-, п-ксилол и т.п., или в смеси таких растворителей и предпочтительно с использованием DMF и м-ксилола. Инертную атмосферу можно поддерживать путем использования инертных газов, таких как N2, Ar или He. Реакцию можно осуществлять в присутствии основания, такого как карбонат калия, бикарбонат натрия, гидрид натрия и гидроксиды щелочных металлов и гидроксиды щелочно-земельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция или смеси таких оснований. Реакцию также можно осуществить в отсутствие основания. Температура реакции может находиться в пределах от 30 до 160C, в зависимости от выбора растворителя, и предпочтительно температура находится в пределах от 30 до 100C. Реакция может продолжаться от 1 до 24 ч, предпочтительно от 8 до 14 ч. Соединения изобретениия, полученные описанным выше способом получения по настоящему изобретению, могут быть преобразованы в другое соединение по настоящему изобретению путем последующих химических модификаций с использованием хорошо известных реакций, таких как окисление,восстановление, защита, удаление защиты, реакция перегруппировки, галогенирование, гидроксилирование, алкилирование, алкилтиолирование, деметилирование, О-алкилирование, О-ацилирование, N-9 017154 алкилирование, N-алкенилирование, N-ацилирование, N-цианирование, N-сульфонилирование, реакция сочетания с использованием переходных металлов и т.п. Если необходимо, можно осуществить любую одну или более из следующих стадий:i) преобразование соединения формулы (I) в другое соединение формулы (I);ii) удаление любых защитных групп илиiii) образование фармацевтически приемлемой соли, сольвата или пролекарства этого соединения. Способ (i) можно осуществить с использованием традиционных процедур взаимопреобразования,таких как эпимеризация, окисление, восстановление, алкилирование, нуклеофильное или электрофильное ароматическое замещение и сложноэфирный гидролиз или образование амидной связи. В способе (ii) примеры защитных групп и способов их удаления можно найти в T. W. Greene 'Protective Groups in Organic Synthesis' (J. Wiley and Sons, 1991). Подходящие аминозащитные группы включают сульфонил (например, тозил), ацил (например, ацетил, 2',2',2'-трихлорэтоксикарбонил, бензилоксикарбонил или трет-бутоксикарбонил) и арилалкил (например, бензил), которые могут быть удалены путем гидролиза (например, с использованием кислоты, такой как хлористо-водородная или трифторуксусная кислота) или восстановительным путем (например, путем гидрогенолиза бензильной группы или восстановительного удаления 2',2',2'-трихлорэтоксикарбонильной группы с использованием цинка в уксусной кислоте), как это является подходящим. Другие подходящие аминозащитные группы включают трифторацетил, который можно удалить путем катализируемого основанием гидролиза или с использованием связанной с твердофазной смолой бензильной группы, такой как связанная со смолой Меррифильда 2,6 диметоксибензильная группа (линкер Эллмана), которую можно удалить путем кислотнокатализируемого гидролиза, например, с использованием трифторуксусной кислоты. В способе (iii) галогенирование, гидроксилирование, алкилирование и/или фармацевтически приемлемые соли можно получить традиционным путем взаимодействия с подходящей кислотой или кислотным производным, как описано подробно выше. Для того чтобы можно было использовать соединения формулы (I) в терапии, они обычно должны быть сформулированы в фармацевтическую композицию в соответствии со стандартной фармацевтической практикой. Фармацевтические композиции по настоящему изобретению могут быть сформулированы традиционным способом с использованием одного или нескольких фармацевтически приемлемых носителей. Таким образом, активные соединения по настоящему изобретению могут быть сформулированы в композицию для перорального, буккального, интраназального, парентерального (например, внутривенного,внутримышечного или подкожного) или ректального введения или в форме, подходящей для введения путем ингаляции или инсуффляции. Для перорального введения фармацевтические композиции могут принимать форму, например,таблеток или капсул, полученных традиционными способами с использованием фармацевтически приемлемых эксципиентов, таких как связующие (например, предварительно желатинизированный кукурузный крахмал, поливинилпирролидон или гидроксилропилметилцеллюлоза); наполнители (например,лактоза, микрокристаллическая целлюлоза или фосфат кальция); смазывающие вещества (например,стеарат магния, тальк или диоксид кремния); разрыхлители (например, картофельный крахмал или натрий-крахмалгликолят) или смачивающие вещества (например, лаурилсульфат натрия). На таблетки может быть нанесено покрытие способами, хорошо известными из уровня техники. Жидкие препараты для перорального введения могут, например, принимать форму растворов, сиропов или суспензий, или они могут быть представлены в виде сухого продукта для реструктурирования водой или другим подходящим носителем перед применением. Такие жидкие препараты можно получить традиционными способами с использованием фармацевтически приемлемых добавок, таких как суспендирующие вещества (например, сироп сорбита, метилцеллюлоза или гидрированные пищевые масла); эмульгаторы (например,лецитин или аравийская камедь); неводные носители (например, миндальное масло, маслянистые сложные эфиры или этиловый спирт) и консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота). Для буккального введения композиция может принимать форму таблеток или лепешек, сформулированных традиционным способом. Активные соединения по настоящему изобретению могут быть сформулированы для парентерального введения путем инъекции, в том числе с использованием традиционных методов катетеризации или инфузии. Композиции для инъекций могут быть представлены в стандартной лекарственной форме, например в ампулах или в многодозовых контейнерах, с добавленным консервантом. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать вещества для формулирования, такие как суспендирующие, стабилизирующие и/или диспергирующие вещества. Альтернативно, активный ингредиент может быть в форме порошка для реструктурирования подходящим носителем, например стерильной апирогенной водой,перед применением. Активные соединения по настоящему изобретению также могут быть сформулированы в композиции для ректального применения, такие как суппозитории или удерживаемые клизмы, например, содер- 10017154 жащие традиционные основы для суппозиторий, такие как масло какао или другие глицериды. Для интраназального введения или введения путем ингаляции активные соединения по настоящему изобретению удобным образом доставляются в форме аэрозольного спрея из контейнера под давлением или распылителя, или из капсулы с использованием ингалятора или инсуффлятора. В случае аэрозоля,находящегося под давлением, можно использовать подходящий пропеллент, например дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ, и единицу дозирования можно определить путем обеспечения клапана для доставки отмеренного количества. Лекарственное средство для контейнера под давлением или распылителя может содержать раствор или суспензию активного соединения, тогда как для капсулы оно предпочтительно должно быть в форме порошка. Капсулы и картриджи (например, из желатина) для использования в ингаляторе или инсуффляторе могут быть сформулированы так, что они содержат порошкообразную смесь соединения по настоящему изобретению и подходящую основу для порошка, такую как лактоза или крахмал. Аэрозольные композиции для лечения состояний, указанных выше (например, мигрени) у среднестатистического взрослого человека, предпочтительно составлены таким образом, чтобы каждая отмеренная доза или "пшик" аэрозоля содержали от 20 до 1000 мкг соединения по настоящему изобретению. Общая суточная доза аэрозольного препарата находится в пределах от 100 мкг до 10 мг. Введение можно осуществлять несколько раз в день, например, 2, 3, 4 или 8 раз, с введением каждый раз, например, по 1,2 или 3 дозы. Эффективное количество соединения общей формулы (I) или его производных, определенных выше, можно использовать для получения лекарственного средства, вместе с традиционными фармацевтическими вспомогательными веществами, носителями и добавками. Такая терапия включает много вариантов выбора: например, введение двух совместимых соединений одновременно в виде одной дозы, или введение каждого соединения индивидуально в виде отдельных доз, или, если это необходимо, с одинаковыми временными интервалами, или отдельно для получения максимально благоприятного эффекта или для уменьшения потенциальных побочных эффектов лекарственных средств, в соответствии с известными принципами фармакологии. Доза активных соединений может варьировать в зависимости от таких факторов, как путь введения,возраст и масса тела пациента, природа и тяжесть заболевания, подлежащего лечению, и подобных факторов. Поэтому любая ссылка в настоящем изобретении на фармакологически эффективное количество соединений общей формулы (I) относится к указанным выше факторам. Предлагаемая доза активных соединений по настоящему изобретению для перорального, парентерального, назального либо буккального введения среднестатистическому взрослому человеку для лечения состояний, указанных выше, составляет от 0,1 до 200 мг активного ингредиента на единицу дозировавния, которую можно вводить, например, от 1 до 4 раз в день. Коммерческие реагенты использовали без дополнительной очистки. Комнатная температура означает 25-30C. Данные ИК-спектра получали с использованием KBr и в твердом состоянии. Если не указано иное, все масс-спектральные анализы осуществляли в условиях ионизации электроспреем (ESI). Спектры 1 Н-ЯМР получали при 400 МГц с использованием устройства Bruker. Дейтерированный хлороформ (99,8% D) использовали в качестве растворителя. TMS использовали в качестве внутреннего стандарта. Значения химического сдвига выражали в миллионных долях . Для ЯМР сигналов использовали следующие аббревиатуры для обозначения мультиплетности: с=синглет, ушир.с=уширенный синглет,д=дублет, т=триплет, кв.=квартет, квинт.=квинтет, гепт.=гептет, дд=двойной дублет, дт=двойной триплет, тт=триплет триплетов, м=мультиплет. Хроматография относится к колоночной хроматографии,осуществляемой с использованием 100-200 меш силикагеля и в условиях давления азота (флэшхроматография). Примеры Новые соединения по настоящему изобретению получали в соответствии со следующими процедурами, с использованием подходящих веществ, и далее они иллюстрируются следующими конкретными примерами. Наиболее предпочтительные соединения по настоящему изобретению представляют собой любые или все, которые конкретно описаны в этих примерах. Эти соединения, однако, не следует рассматривать как образующие один единственный род, который считают изобретением, и любая комбинация соединений или их групп сама может образовывать род. Следующие далее примеры дополнительно иллюстрируют детали получения соединений по настоящему изобретению. Специалистам в данной области должно быть понятно, что для получения этих соединений можно использовать известные варианты условий и способа осуществления следующих препаративных процедур. Получение 1. 1-(3-Ацетамидо-4-метоксибензолсульфонил)-5-метокси-3-метил-1H-индол. Гидрид натрия (2,15 г, 49,3 ммоль) помещали в 250-мл трехгорлую круглодонную колбу, содержащую тетрагидрофуран (50 мл), в атмосфере азота. К полученной смеси добавляли раствор 5-метокси-3 метилиндола (5,3 г, 32,9 ммоль) в тетрагидрофуране (25 мл) при 25C в течение 15 мин. Полученную реакционную массу перемешивали еще в течение 1 ч и массу охлаждали до 0C и добавляли через капельную воронку раствор 3-ацетамидо-4-метоксибензолсульфонилхлорида (13,01 г, 49,3 ммоль) в тетрагид- 11017154 рофуране (65 мл) в течение 20 мин. Этой массе давали охладиться до комнатной температуры и перемешивали в течение ночи (24 ч). Ход реакции отслеживали при помощи тонкослойной хроматографии. После завершения реакции смесь гасили в ледяной воде (100 мл) при перемешивании и продукт экстрагировали этилацетатом (2250 мл). Органическую фазу промывали насыщенным солевым раствором,сушили над безводным сульфатом натрия и концентрировали при пониженном давлении с получением густой сиропообразной массы, которую использовали как таковую на следующей стадии без очистки. Масс (m/z): 389,4 (М+Н)+; Получение 2. 1-(3-Амино-4-метоксибензолсульфонил)-5-метокси-3-метил-1H-индол. 1-(3'-Ацетамидо-4'-метоксибензолсульфонил)-5-метокси-3-метил-1H-индол (10 г, 25,7 ммоль) (получен из получения 1) помещали в 250-мл трехгорлую круглодонную колбу, содержащую этанол (100 мл), и перемешивали массу с получением прозрачного раствора. К этому прозрачному раствору добавляли водный раствор хлористо-водородной кислоты (10 мл, 33%) и нагревали полученную массу при температуре кипения с обратным холодильником в течение 2 ч. Ход реакции отслеживали при помощи тонкослойной хроматографии. После завершения реакции реакционную массу концентрировали в вакууме и остаточную массу гасили в охлажденной воде (100 мл). рН доводили до 9,0-10,0 при помощи разбавленного раствора гидроксида натрия. Продукт экстрагировали дихлорметаном (2100 мл). Органическую фазу промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и концентрировали массу при пониженном давлении с получением неочищенного соединения. Полученный технический продукт очищали колоночной хроматографией с использованием силикагеля (100-200 меш),при этом система элюента представляла собой этилацетат и н-гексан (2:8), с получением 1,0 г указанного в заголовке продукта. ИК (см-1): 3487, 3385, 1616, 1514, 1336, 1226, 1157, 624; 1 Н-ЯМР (м.д.): 2,19 (3H, с), 3,81 (3H, с), 3,82 (3H, с), 3,92 (2 Н, ушир.с), 6,68-6,70 (1 Н, д, J=8,52 Гц),6,85-6,86 (1 Н, д, J=2,44 Гц), 6,88-6,91 (1 Н, дд, J=8,92, 2,52 Гц), 7,05-7,06 (1 Н, д, J=2,32 Гц), 7,23-7,26 (2 Н,м), 7,83-7,85 (1 Н, д, J=8,92 Гц); Масс (m/z): 347,1 (М+Н)+ Пример 1. N'-[2-Метокси-5-(5-метокси-3-метилиндол-1-сульфонил)фенил]-N,N-диметилэтан-1,2 диамин. 1-(3'-Амино-4'-метоксибензолсульфонил)-5-метокси-3-метил-1H-индол (600 мг, 1,7 ммоль) (полученный из получения 2) помещали в 25-мл двухгорлую круглодонную колбу, содержащую DMF (3 мл) и м-ксилол (3 мл). Добавляли гидрохлорид 2-диметиламиноэтилхлорида (490 мг, 3,4 ммоль), нагревали при 135-138C в течение 10 ч и ход реакции отслеживали при помощи тонкослойной хроматографии. После завершения реакции реакционную массу охлаждали до комнатной температуры, гасили в охлажденной воде (25 мл) и pH доводили до 9,0-10,0 при помощи 40% водного раствора гидроксида натрия. Продукт экстрагировали дихлорметаном (250 мл). Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении с получением неочищенного соединения. Полученный технический продукт очищали колоночной хроматографией с использованием в качестве элюента этилацетата и триэтиламина (99:1). ИК (см-1): 3404, 1597, 1359, 1166; 1 Н-ЯМР (м.д.): 2,2 (3H, с), 2,29 (6 Н, с), 2,58-2,61 (2 Н, т, J=5,92 Гц), 3,14-3,16 (2 Н, т, J=5,96 Гц), 3,80(1 Н, д, J=8,93 Гц); Масс (m/z): 418,5 (М+Н)+. Примеры 2-35 Соединения примеров 2-35 получали при помощи следующих процедур, как описано в примере 1, с некоторыми некритическими изменениями.- 28017154 Пример 43. Таблетка, включающая соединение формулы (I) Ингредиенты объединяли и гранулировали с использованием растворителя, такого как метанол. Композицию затем сушили и формировали в таблетки (содержащие около 20 мг активного соединения) с использованием подходящей машины для таблетирования. Пример 44. Композиция для перорального введения Ингредиенты смешивали и распределяли в капсулы, каждая из которых содержала около 100 мг; одна капсула должна представлять собой примерную суточную дозу. Пример 45. Жидкая композиция для перорального введения. Ингредиенты смешивали с образованием суспензии для перорального введения. Пример 46. Композиция для парентерального введения Активный ингредиент растворяли в части воды для инъекций. Затем добавляли достаточное количество хлорида натрия при перемешивании, чтобы сделать раствор изотоническим. Раствор доводили до нужной массы при помощи остального количества воды для инъекций, фильтровали через 0,2 микронный мембранный фильтр и упаковывали в стерильных условиях.
МПК / Метки
МПК: A61P 25/18, A61P 25/28, A61P 25/14, A61K 31/404, C07D 209/08, A61P 25/22
Метки: применение, аминоарилсульфонамидные, 5-нт6, качестве, соединения, лигандов
Код ссылки
<a href="https://eas.patents.su/30-17154-aminoarilsulfonamidnye-soedineniya-i-ih-primenenie-v-kachestve-5-nt6-ligandov.html" rel="bookmark" title="База патентов Евразийского Союза">Аминоарилсульфонамидные соединения и их применение в качестве 5-нт6 лигандов</a>
Предыдущий патент: Непрерывный способ получения алканоламидов жирных кислот
Следующий патент: Резьбовое соединение стальных труб
Случайный патент: 13-членные азалиды и их применение в качестве антибиотических агентов